Inhaltsverzeichnis
Den menstruellen Zyklus hormonell verstehen ist oft nicht einfach, hält er sich nicht immer an die „Regel“ und macht mitunter was er will.
Der weibliche Hormonstoffwechsel ist ein komplexes und hochsensibles System, bei dem mehrere Organe, wie Eierstöcke, Nebennieren, Gebärmutter und Bauchspeicheldrüse, in einem feinen hormonellen Regelkreis zusammenarbeiten. Ein tieferes Verständnis dieser Prozesse ist entscheidend, um Symptome richtig einzuordnen und gezielt Maßnahmen zu ergreifen.
Das Hormonsystem
Die Nebenniere, Eierstöcke, Bauchspeicheldrüse und der Magen-Darm-Trakt bilden zusammen ein Netzwerk hormonproduzierender Organen.
Hormone sind chemische Botenstoffe und stellen ein den komplexen, hormonellen Regelkreis dar. Diese Hormone übermitteln ständig Informationen, sagen Organen, was sie produzieren sollen und regulieren zahlreiche Vorgänge, die für unser Wohlbefinden essentiell sind.
Wenn wir uns ausschließlich auf ein einzelnes Symptom konzentrieren oder ein einzelnes Hormon behandeln, ohne die anderen zu beachten, können wir leicht die eigentliche Ursache übersehen. Ein Beispiel: Wenn die Nebenniere über Jahre hinweg unter großem Stress viel Cortisol ausschütten muss, kann sie nicht genug Progesteron und Testosteron produzieren. Die Folgen dieser Mängel sind erheblich.
Die Haupthormone
Östrogen – Das Hormon der Weiblichkeit
Östrogen ist wahrscheinlich das bekannteste weibliche Hormon. Es ist verantwortlich für die Entwicklung sekundärer Geschlechtsmerkmale, sorgt für Rundungen und spielt eine tiefe Rolle in unserem emotionalen und sozialen Verhalten. Es ist das Hormon des Nestbaus, des Wunsches, sich um Familie zu kümmern und Beziehungen zu pflegen.
Differenzierung
Wenn wir von Östrogen sprechen, sprechen wir eigentlich von einer Familie dreier verschiedener Hormon: Östradiol, Östron und Östreol.
Sie unterscheiden sich fundamental in ihrer chemischen Struktur, biologischen Aktivität, ihren Quellen im Körper und ihren physiologischen Funktionen. Ein Verständnis dieser Unterschiede ist entscheidend für eine effektive Hormonal-Therapie und das Verständnis, warum Frauen in der Perimenopause leiden können, obwohl ihre Östrogenbluttests möglicherweise „normal“ aussehen.
Östradiol – Power-Hormon
Östradiol, chemisch als 17β-Östradiol bekannt, ist das biologisch aktivste Östrogen und wird daher häufig als das „echte“ oder „primäre“ Östrogen bezeichnet. Mit einer relativen biologischen Aktivität von 100 Prozent ist Östradiol etwa zwölfmal stärker als Östron und achtzig Mal stärker als Östreol.
Es wird hauptsächlich in den Granulose-Zellen der Ovarien produziert, besonders während der Follikelphase des Menstruationszyklus, wenn die Östrogen-Konzentration kontinuierlich ansteigt, um den Eisprung auszulösen. Während der Lutealphase bleibt die Östradiol-Konzentration erhöht, aber nicht so dramatisch wie beim präovulatorischen Peak.
Die Funktionen von Östradiol sind vielfältig und lebensnotwendig. Es ist das Hormon, das für den Aufbau und die Proliferation der Gebärmutterschleimhaut verantwortlich ist, ein Prozess, der notwendig ist, um eine befruchtete Eizelle aufzunehmen. Östradiol reguliert auch den Knochenstoffwechsel durch Aktivierung von Osteoblasten (knochenbildende Zellen) und Hemmung von Osteoklasten (knochenabbauende Zellen), wodurch eine stabile Knochendichte erhalten bleibt. Dies ist besonders wichtig für die Prävention von Osteoporose, ein großes Problem für postmenopausale Frauen.
Kardiovaskulär wirkt sich Östradiol schützend aus, indem es Blutgefäße erweitert, die Endothel-Funktion verbessert und dadurch den Blutdruck senkt und den Cholesterinstoffwechsel verbessert. Im Gehirn spielt Östradiol eine entscheidende Rolle für Kognition, Gedächtnis und Neuroplastizität, die Fähigkeit des Gehirns, neue Nervenbahnen zu bilden. Es fördert die Serotonin-Produktion, die für Stimmungsregulation wichtig ist. Auch sexuelle Funktion und Lubrifikation sind stark von Östradiol abhängig.
Im Menstruationszyklus folgt Östradiol einem charakteristischen Muster: niedrig während der Menstruation (10-20 pg/mL), steigt dann während der Follikelphase an, erreicht einen Peak von 200-400 pg/mL kurz vor dem Eisprung, und bleibt dann während der Lutealphase auf mittlerem Niveau (100-150 pg/mL) erhöht.
Mit Beginn der Perimenopause wird dieses Muster chaotisch, denn die Östradiol-Werte können wild schwanken, mal extrem hoch, mal unerwartet niedrig. Nach der Menopause sinken die Östradiol-Spiegel dramatisch auf unter 20 pg/mL und bleiben dort.
Östron – Backup-Hormon
Östron, chemisch sehr ähnlich wie Östradiol, aber mit nur leicht unterschiedlicher Struktur. Es ist etwa zwölfmal schwächer als Östradiol. Trotz dieser geringeren Potenz spielt Östron eine bescheidene Rolle während der reproduktiven Jahre, wird aber in der Menopause zunehmend bedeutsam.
Im Gegensatz zu Östradiol, das hauptsächlich von den Ovarien produziert wird, entsteht Östron primär durch periphere Umwandlung von Androstendion, einer Vorstufe aus den Nebennieren, vor allem in Fettgewebe, Haut und Leber.
Dies ist der Grund, warum übergewichtige Frauen tendenziell höhere Östron-Spiegel haben, besonders nach der Menopause.
Während der reproduktiven Jahre trägt Östron nur etwa fünfzehn bis zwanzig Prozent zur gesamten Östrogenität bei. Seine biologische Wirkung ist viel schwächer. Es ist weniger wirksam bei der Proliferation der Gebärmutterschleimhaut, weniger wirksam für die Knochendichte, kardiovaskuläre und neurologische Schutzeffekte als Östradiol.
Jedoch behält Östron einige grundlegende Östrogeneffekte, und mit zunehmendem Alter wird seine Rolle zunehmend wichtiger.
Nach der Menopause findet eine dramatische Verschiebung statt: Die Eierstöcke produzieren kaum noch Östrogen, aber das Fettgewebe setzt weiterhin Östron frei.
Bei vielen postmenopausalen Frauen wird Östron tatsächlich zur Hauptquelle von Östrogeneffekten im Körper. Dies hat sowohl positive als auch negative Konsequenzen.
Positiv ist, dass Frauen mit erhöhtem Körpergewicht nach der Menopause möglicherweise bessere Knochendichte-Werte aufweisen, ein Phänomen, das „Fett schützt Knochen“ genannt wird.
Negativ ist jedoch, dass Östron kontinuierlich und azyklisch wirkt. Anders als Östradiol, das während der Menstruation abbricht (und den Zellen eine „Ruhe-Phase“ gibt), wird der Körper durch konstantes Östron einer andauernden proliferativen Stimulation ausgesetzt.
Dies ist mit erhöhtem Risiko für Brustkrebs und Endometriumkrebs verbunden, ein Grund, warum übergewichtige postmenopausale Frauen erhöhte Krebsrisiken haben.
Das Zyklus-Muster von Östron ist viel stabiler als das von Östradiol, mit nur leichten Schwankungen über den Menstruationszyklus hinweg. Dies liegt daran, dass es von peripheren Geweben stammt, die nicht zyklisch reguliert sind wie die Ovarien.
Östreol – Schwangerschafts-Hormon
Östreol ist das schwächste der drei Östrogene, etwa achtzig Mal schwächer als Östradiol und sechsmal schwächer als Östron.
Seine chemische Struktur unterscheidet sich durch eine zusätzliche Hydroxyl-Gruppe, die es beim Körper-Metabolismus entstehen lässt.
Der Schlüssel zum Verständnis von Östreol liegt jedoch nicht in seiner schwachen Potenz im nicht-schwangeren Zustand, sondern in seiner massiven Bedeutung während der Schwangerschaft.
Außerhalb einer Schwangerschaft ist Östreol praktisch nicht nachweisbar im Blut einer Frau und hat keine klinische Bedeutung. Ein Bluttest auf Östreol bei einer nicht-schwangeren Frau wäre sinnlos.
Die Situation ändert sich jedoch radikal während der Schwangerschaft. Östreol wird primär von der fetalen Leber und der Plazenta produziert, nicht von der Mutter.
Seine Produktion ist direkt abhängig von der fetalen Aktivität und dem fetalen Wohlbefinden. Dies macht Östreol zu einem wertvollen Überwachungs-Marker während der Schwangerschaft.
Die Funktion von Östreol in der Schwangerschaft ist spezialisiert: Es fördert die Gefäßerweiterung in der Plazenta, verbessert damit die Durchblutung und ermöglicht bessere Nährstoffaufnahme für den Fötus.
Es trägt zur Vorbereitung der Gebärmutter für die Geburt bei, indem es die Elastizität des Myometriums (Gebärmuttermuskel) erhöht.
Interessanterweise ist Östreol weniger stark proliferativ für das Endometrium als Östradiol, die Schwangerschaft ist nicht die Zeit für Endometrium-Wachstum (Gebärmutterschleimhaut), was nahelgt, weshalb schwangere Frauen nicht das gleiche Endometriumkrebsrisiko aufweisen wie Frauen mit chronisch erhöhtem Östron.
Östreol spielt auch eine wichtige Rolle bei der Immuntoleranz des Fötus, es hilft dem mütterlichen Immunsystem, den genetisch „fremden“ Fötus nicht abzustoßen.
Die Östriol-Spiegel steigen kontinuierlich während der Schwangerschaft an: von praktisch Null in der Woche 8, auf etwa 5 ng/mL in Woche 20, auf etwa 20 ng/mL in Woche 30, und schließlich auf 30-50 ng/mL in Woche 40 – ein massiver Anstieg. Nach der Geburt fallen die Östreol-Spiegel schnell wieder auf unmessbar ab, da die Plazenta entfernt wurde.
Klinisch wird Östreol als Teil des Triple-Screenings in der Schwangerschaft zwischen der 16. und 18. Schwangerschaftswoche verwendet. Ein niedriger Östreol-Wert kann auf eine Chromosomenstörung wie das Down-Syndrom hindeuten. Allerdings ist ein niedriger Östreol-Wert nicht definitiv,viele Frauen mit niedrigen Werten gebären völlig gesunde Babys. Es ist ein Screening-Tool, kein diagnostisches Tool und wird nicht von der Krankenkasse kostenseitig übernommen, sondern ist als IGeL-Leistung privat zu tragen.
Folgende Werte werden aus dem pränatalen Blut bestimmt:
- Alpha-Fetoprotein (AFP)
- freies β-HCG (humanes Choriongonadotropin)
- unkonjugiertes Östriol (uE3)
Diese Werte werden zusammen mit dem mütterlichen Alter, dem Schwangerschaftsalter und anderen Faktoren wie Gewicht und medizinischer Vorgeschichte verwendet, um das Risiko für chromosomale Anomalien beim ungeborenen Kind zu berechnen. Dazu gehören vor allem:
- Down-Syndrom (Trisomie 21) – Erkennungsrate ca. 74 %
tritt bei 1 von 600 Lebendgeburten auf; ist keine Krankheit, sondern um eine unveränderliche genetische Abweichung, die die körperliche und geistige Entwicklung beeinflusst und auf einer zufälligen Fehlverteilung der Chromosomen während der Eizellbildung. - Edwards-Syndrom (Trisomie 18) – Erkennungsrate ca. 70 %
tritt bei 1 von 5.500 Lebendgeburten und führt zu schweren Entwicklungsstörungen und zahlreichen Fehlbildungen; Behandlung ist symptomatisch und auf die Linderung von Beschwerden ausgerichtet.
Die Hälfte der Neugeborenen stirbt innerhalb von sechs Tagen, nur 5 bis 10 Prozent überleben ein Jahr, und etwa 15 Prozent erreichen das fünfte Lebensjahr. - Neuralrohrdefekte (NRD, z. B. Spina bifida) – Erkennungsrate ca. 80 %
tritt bei 1 – 1,5 von 1.000 Lebendgeburten auf; angeborene Fehlbildungen des zentralen Nervensystems, die durch einen unvollständigen Verschluss des Neuralrohrs während der frühen embryonalen Entwicklung entstehen, meist zwischen dem 22. und 28. Tag nach Empfängnis.
Das Neuralrohr entwickelt sich aus der Neuralplatte und bildet später Gehirn, Rückenmark, Wirbelsäule und Schädel. Bei einem Neuralrohrdefekt bleibt die Schließung aus, was in offenen oder geschlossenen Fehlbildungen resultieren kann.
Vergleich und klinische Implikationen
Die drei Östrogene können als spezialisierte Werkzeuge betrachtet werden, von denen jede eine andere Aufgabe erfüllt.
Östradiol ist der Hauptakteur während der reproduktiven Jahre, der für Schleimhaut-Aufbau, Knochendichte, kardiovaskulären Schutz und neurologische Funktion verantwortlich ist.
Östron ist das schwache Backup-System, das während der reproduktiven Jahre nur eine kleine Rolle spielt, aber nach der Menopause zur Hauptquelle wird , mit all den damit verbundenen positiven und negativen Konsequenzen.
Östreol ist ein hochspezialisierteres Hormon, das hauptsächlich während der Schwangerschaft relevant ist.
Das Verständnis dieser Unterschiede ist entscheidend, um zu verstehen, weshalb Bluttests manchmal verwirrend sein können.
Eine Frau in der Perimenopause könnte normale oder sogar hohe Gesamtöstrogen-Spiegel haben, aber wenn diese primär aus Östron bestehen (aufgrund von Anovulation und peripher erhöhter Umwandlung), während das biologisch aktivere Östradiol niedrig ist, wird sie dennoch die Symptome eines Östrogen-Mangels erleben. Sie wird über Hitzewallungen, Kopfschmerzen, Knochenschmerzen und Gedächtnisverlust klagen, nicht weil sie kein Östrogen hat, sondern weil sie nicht das richtige Östrogen hat.
In der Perimenopause ist eine häufige Situation, dass Frauen mit anovulatorischen Zyklen einen relativ normalen oder sogar hohen Östron-Spiegel aufweisen, aber einen niedrigen Östradiol-Spiegel, weil es keinen Eisprung gibt und daher keine große ovariell-produzierte Menge an Östradiol. Dies erklärt, warum Frauen in dieser Phase trotz „normaler“ Östrogenspiegel leiden können.
Therapeutisch hat dies Implikationen. Wenn eine Hormonersatztherapie notwendig ist, wird typischerweise Östradiol verwendet, nicht Östron, weil Östradiol das biologisch aktive Hormon ist, das die meisten Schutzeffekte bietet.
Einige traditionelle HRT-Präparate enthalten konjugierte Östrogene, die ein Gemisch aus Östradiol, Östron und Östreol sind, obwohl Östreol bei nicht-schwangeren Frauen nutzlos ist, ist sein Vorhandensein in traditionellen Präparaten ein historischer Zufall, kein therapeutischer Grund.
Diagnostisch bedeutet dies, dass bei Verdacht auf Hormonmangel oder Hormonimbalance, nicht einfach „Östrogen“ gemessen werden sollte, sondern spezifisch Östradiol, Östron und Progesteron in den richtigen Zyklus-Phasen.
Ein einziger Test ist oft nicht ausreichend, mehrere Tests über mehrere Zyklen hinweg können notwendig sein, um das Muster zu verstehen. Die Symptome einer Frau sind oft zuverlässiger als ein einzelner Bluttest, besonders in der Perimenopause, wenn die Hormone chaotisch sind.
Funktionen von Östrogen
- Schleimhautgesundheit
Feuchte Schleimhäute in Mund, Augen und Vagina - Knochenstabilität
Calciumeinlagerung und Knochendichte - Herz-Kreislauf
Gefäßelastizität und Blutdruckregulation - Emotionales Wohlbefinden
Stimmung, Motivation und Sinnlichkeit
Östrogen wird hauptsächlich in der ersten Hälfte des Menstruellen Zyklus produziert. Seine Aufgabe beginnt unmittelbar nach der Menstruation: Es stimuliert die Gebärmutter, ihre Schleimhaut aufzubauen, ähnlich wie das Auslegen einer Watte, die bereit ist, eine befruchtete Eizelle sanft aufzunehmen.
Wenn die Frau älter wird und in die Prämenopause eintritt, beginnt Östrogen zu sinken. Dies führt zu zahlreichen Symptomen, die oft ursächlich übersehen werden:
- Kopfschmerzen
- Schlafstörungen
- Reizbarkeit
- Hitzewallungen
… das allgemeines Gefühl, dass der Körper „auseinanderfällt“.
Wichtige Erkenntnis
Viele Frauen berichten von Bluthochdruck oder Schulterschmerzen (Frozen Shoulder), die mit Östrogenmangel zusammenhängen.
Ein niedrigesr Östrogenspiegel kann zu Bluthochdruck beitragen, da die Gefäße ihre Elastizität verlieren. Schulterschmerzen entstehen, weil an der Schulter viele Östrogen-Rezeptoren vorhanden sind, und ohne ausreichend Östrogen können diese Gelenke und Muskeln leiden.
Progesteron – Das Ruhehormon
Während Östrogen das Hormon der ersten Zyklushälfte ist, ist Progesteron das Hormon der zweiten Hälfte. Nach dem Eisprung (der in der Zyklusmitte stattfindet) wird Progesteron aus dem Gelbkörper freigesetzt, dem Rest des Follikels nach dem Eisprung.
Progesteron sagt der Gebärmutter, dass genug Schleimhaut aufgebaut wurde, und bereitet diese so vor, dass eine befruchtete Eizelle aufgenommen werden kann.
Progesteron ist das Hormon, das beruhigt, hilft zu schlafen und die Nervenerregbarkeit reguliert. Frauen, die unter Progesteronmangel leiden, berichten oft, dass sie sich „ständig angespannt“ fühlen, dass kleine Dinge sie reizen und dass sie in der zweiten Zyklushälfte nicht mehr schlafen können.
Progesteron ist oft das erste Hormon, das weniger produziert wird. Eine Frau kann noch Jahre ihre Menstruation haben aber keinen richtigen Eisprung haben, was bedeutet, dass sie wenig oder kein Progesteron mehr produziert.
In solchen Fällen kann die Gebärmutterschleimhaut unkontrolliert wachsen, was zu extremen Blutungen führt, die die Frau verwirren, weil sie nicht versteht, warum die Menge so massiv ist.
Progesteronmangel-Anzeichen
Wenn eine Frau unter
- extremer Schlaflosigkeit
- starker Reizbarkeit
- heftigen Periodenschmerzen
- unkontrollierten Stimmungsschwankungen
- unerklärlichen Angststörungen
leidet , besonders wenn diese Symptome neu sind oder sich verschlimmert haben, ist oft Progesteronmangel der Auslöser.
Paradoxerweise erkennen Ärzte dies oft nicht, weil sie sich auf den regelmäßigen Menstruationszyklus konzentrieren, nicht auf die fehlende Ovulation.
Testosteron – Energie und Kraft
Obwohl Testosteron oft als das „männliche Hormon“ wahrgenommen wird, produzieren auch Frauen Testosteron. Es gibt Energie, hilft, Muskeln aufzubauen, verbessert den Stoffwechsel und trägt zur Libido bei.
Ausreichendes Testosteron ist mit Vitalität und dem Gefühl verbunden, „durchhalten“ zu können.
Wenn eine Frau einen zu niedrigen Testosteronspiegel hat, fühlt sie sich oft müde und energielos. Das Problem verschärft sich, wenn chronischer Stress die Nebenniere überlastet: Dann kann die Nebenniere nicht genug Testosteron produzieren, um die fehlende Menge aus den Eierstöcken auszugleichen.
Cortisol – Das Überlebenhormon
Cortisol ist das Stresshormon, das von der Nebenniere ausgeschüttet wird. In Momenten großer Belastung ist Cortisol aktiviert es den „Kampf oder Flucht“-Modus, hilft so, Krisen zu überstehen.
Das Problem entsteht, wenn Cortisol chronisch erhöht bleibt:
- dauerhaft erhöhter Blutzucker
- erhöht den Blutdruck
- „stiehlt“ Ressourcen, die der Nebenniere für die Produktion von Progesteron und Testosteron fehlen
Dies schafft einen Teufelskreis:
Chronischer Stress → hohes Cortisol → zu wenig Progesteron und Testosteron → schlechtere Stressresilienz → noch höheres Cortisol.
Die Frau fühlt sich gefangen, erschöpft und kann der Spirale nicht entkommen.
Verursachen Östrogen und Stress Lipödeme?
Die Frage nach den Ursachen des Lipödems ist eine der zentralen Fragen für betroffene Frauen und Ärzte. Jahrzehntelang wurde diese Erkrankung übersehen oder mit mangelhafter Willenskraft erklärt und es hieß: „Sie müssen einfach abnehmen!“
Heute weiß man, dass Lipödem eine biologische Erkrankung ist, bei der genetische Veranlagung und hormonale Faktoren zusammenwirken. Sowohl Östrogen als auch Stress scheinen eine wichtige Rolle beim Ausbruch und bei der Verschlimmerung dieser Erkrankung zu spielen.
Grundlagen Genetik und Hormon-Trigger
Das Lipödem ist ein chronisches Erkrankung des Unterhautfettgewebes, das sich durch abnormale Vermehrung und pathologische Ansammlung von Fettzellen auszeichnet, typischerweise in den Beinen oder auch manchmal in den Armen. Gesäß und die obere Körperhälfte bleiben normalerweise verschont, was zu einem charakteristischen Verhältnis führt: schlanker Oberkörper, aber voluminöse Beine. Die Erkrankung betrifft zu über 95 Prozent Frauen, was stark auf eine hormonale Komponente hindeutet.
Das Verständnis der Lipödem-Ursachen erfordert, zwischen zwei verschiedenen biologischen Ebenen zu unterscheiden, nämlich der genetischen Veranlagung und den hormonalen Auslösefaktoren.
Eine wichtige Erkenntnis aus der modernen Forschung ist, dass genetische Veranlagung allein nicht ausreicht, um ein Lipödem auszulösen, es braucht einen Trigger.
Studien zeigen, dass bis zu 60 Prozent der betroffenen Frauen Verwandte mit denselben Symptomen haben, was auf eine starke erbliche Komponente hindeutet. Allerdings sind nicht alle genetisch veranlagten Frauen erkrankt, manche bleiben ihr Leben lang symptomfrei. Dies zeigt, dass die genetische „Zeitbombe“ erst durch externe Faktoren gezündet werden muss.
Östrogen als primärer Auslösefaktor
Bei über 85 Prozent der betroffenen Frauen zeigt sich der erste Ausbruch des Lipödems während einer Phase hormoneller Umstellung. Dies sind typischerweise drei Lebensereignisse:
- Pubertät
- Schwangerschaft
- Menopause
Die Tatsache, dass das Lipödem so konsistent mit diesen hormonellen Transitionen zusammenfällt, impliziert, dass Östrogen eine zentrale Rolle spielt.
Während der Pubertät steigen die Östrogen-Spiegel dramatisch an. Genau zu dieser Zeit bemerken viele junge Mädchen, dass ihre Beine unnormal anschwellen und an Volumen zunehmen, während ihr Oberkörper schlank bleibt.
Häufig wird dies zu dieser Zeit übersehen oder als normale Gewichtszunahme fehlinterpretiert. Wenn das Mädchen dann auch noch die Antibabypille beginnt, was die Östrogenexposition weiter erhöht, wird die Lipödem-Entwicklung oft beschleunigt.
Ärzte und Patientinnen schreiben die Gewichtszunahme der Pille zu, ohne zu erkennen, dass eine zugrunde liegende Lipödem-Erkrankung zum Leben erwacht ist.
Auch während der Schwangerschaft treten massive hormonelle Veränderungen auf. Der Körper produziert nicht nur mehr Östrogen, sondern auch ein erhöhtes Verhältnis von Östrogen zu Progesteron. Viele Frauen mit bereits bestehendem Lipödem berichten von einer deutlichen Verschlimmerung ihrer Symptome während der Schwangerschaft: mehr Schwellungen, mehr Schmerz, eine schnellere Progression der Erkrankung. In einigen Fällen manifestiert sich das Lipödem zum ersten Mal während einer Schwangerschaft, wenn die genetische Veranlagung vorhanden war, aber noch nicht zum Ausbruch gekommen ist.
In der Menopause ist die Situation paradox: Der Östrogen-Spiegel sinkt dramatisch, und dennoch können viele Frauen mit Lipödem eine Verschlechterung erleben. Dies könnte erklären, dass nicht das absolute Östrogen-Level das Problem ist, sondern die Fluktuation und das Ungleichgewicht zwischen Östrogen und anderen Hormonen wie Progesteron und Testosteron. Wenn der Körper aus dem hormonellen Gleichgewicht gerät, ob durch hohe oder fallende Spiegel, scheinen die Lipödem-Symptome sich zu verschärfen.
Die biologischen Mechanismen, über die Östrogen das Lipödem beeinflusst, sind noch nicht vollständig verstanden, aber mehrere Theorien haben empirische Unterstützung gefunden.
Eine Theorie besagt, dass es um die Dichte und Funktion von Östrogen–Rezeptoren im Unterhautfettgewebe geht. Das Fettgewebe in den Beinen könnte eine höhere Dichte von Östrogen-Rezeptoren aufweisen als Fettgewebe anderswo im Körper, ein „lokales Phänomen“ statt eines systemischen. Wenn Östrogen an diese Rezeptoren bindet, könnte es lokale Signale auslösen, die zu abnormaler Fettzellproliferation und -vergrößerung führen.
Eine andere Theorie betrifft die Kapillar-Funktion: Östrogen könnte die Permeabilität (Durchlässigkeit) der kleinsten Blutgefäße erhöhen, was zum Austreten von Flüssigkeit ins Gewebe führt, was genau dem entspricht, was beim Lipödem beobachtet wird.
Ein besonders interessantes neues Forschungsergebnis bezieht sich auf den Progesteronstoffwechsel. Wissenschaftler haben ein Gen identifiziert, das für das Enzym Aldo-Ketoreduktase kodiert. Dieses Enzym ist verantwortlich für den Progesteronstoffwechsel.
Frauen mit einer Mutation in diesem Gen zeigen abnormale Progesteron-Spiegel, besonders im lokalen Fettgewebe.
Dies könnte ein entscheidender Faktor sein, nicht nur der Östrogen-Level, sondern auch die Balance zwischen Östrogen und Progesteron im lokalen Fettgewebe könnte entscheidend sein. Ein Mangel an Progesteron oder ein Ungleichgewicht zwischen Östrogen und Progesteron könnte die pathologischen Fettprozesse beim Lipödem antreiben.
Hormonale Dysbalance und Lipödem-Schübe
Ein häufiges Muster, das in der klinischen Praxis beobachtet wird, ist das „Schub“-Phänomen bei Lipödem. Patientinnen berichten, dass sich ihre Lipödem-Symptome nicht kontinuierlich verschlimmern, sondern in Episoden, manchmal sind die Symptome stabil, dann plötzlich kommt es zu einer dramatischen Verschlimmerung mit erhöhter Schwellung, Schmerz und möglicherweise auch erhöhter Gewichtszunahme im betroffenen Gebiet.
Diese Schübe fallen oft mit hormonellen Veränderungen zusammen:
- dem Beginn oder Absetzten der Pille
- einer Schwangerschaft oder Fehlgeburt
- Beginn der Menopause.
Die Mechanik dieser Schübe scheint mit hormoneller Dysbalance zusammenzuhängen. Wenn der Körper in einen Zustand versetzt wird, in dem Östrogen hoch und Progesteron niedrig ist, oder in dem die Verhältnisse chaotisch schwanken, scheint dies die Lipödem-Fettzellen zu „triggern“. Sie vermehren sich, sie vergrößern sich, und sie führen zu verstärkten Symptomen.
Dies erklärt, warum manche Frauen unter hormoneller Verhütung, besonders unter östrogendominierten Verhütungsmitteln, eine Verschlimmerung ihres Lipödems erleben und warum die Perimenopause, eine Zeit extremer Hormon-Fluktuation, für viele Lipödem-Patientinnen besonders schwierig ist.
Therapeutisch hat diese Erkenntnis Implikationen. Einige Lipödem-Experten raten Patientinnen, auf hormonelle Verhütung zu verzichten oder zumindest sehr sorgfältig zu experimentieren, um zu sehen, ob ein bestimmtes Verhütungsmittel ihre Symptome verschlimmert.
Bei Patientinnen mit Kinderwunsch wird in einigen Fällen empfohlen, eine Liposuktion (therapeutische Fettabsaugung) vor einer Schwangerschaft durchzuführen, um die Lipödem-Belastung zu reduzieren, bevor die hormonelle Turbulenzen der Schwangerschaft auftreten.
Stress, Cortisol und Entzündung
Während die Hormonforschung bei Lipödem seit Jahrzehnten läuft, ist eine neuere Erkenntnis die Rolle des psychologischen Stresses.
Aktuelle klinische Beobachtungen und erste Forschungsergebnisse deuten darauf hin, dass Stress, neben Hormonen, ein bedeutsamer Triggerfaktor für Lipödem-Schübe sein könnte.
Wenn der Körper unter Stress steht, sei es akuter Stress (wie ein traumatisches Ereignis oder ein bedeutsamer Lebensereignis) oder chronischer Stress (wie berufliche Belastung oder familiäre Konflikte) , setzt er Cortisol frei. Cortisol, das klassische „Stresshormon“, ist ein körpereigenes Corticosteroid, das normalerweise den Körper mobilisiert, um mit Herausforderungen umzugehen. Unter chronischem Stress bleibt der Cortisol-Spiegel jedoch dauerhaft erhöht.
Mehrere klinische Beobachtungen haben gezeigt, dass Lipödem-Patienten, die unter erhöhtem psychischem Stress leiden, häufig unmittelbar danach Lipödem-Schübe erleben.
Einige Patienten berichten, dass nach einem Todesfall in der Familie, einem Jobverlust oder einer Trennung ihre Lipödem-Symptome sich dramatisch verschlechtert haben, teilweise mit einer verzögerten Reaktion von Wochen bis wenigen Monaten. Dies deutet auf einen biologischen Mechanismus hin, durch den psychischer Stress die Lipödem-Pathologie aggraviert.
Cortisol ist bekannt als ein pro-inflammatorisches Hormon, das bei chronischer Erhöhung zu systemischer Entzündung führt.
Lipödem selbst ist mit chronischen Entzündungsprozessen im betroffenen Fettgewebe verbunden, die abnormalen Lipödem-Fettzellen sind ständig von entzündlichen Mediatoren umgeben. Eine Erhöhung des Cortisol-Spiegels durch Stress könnte diese Entzündung amplifiziertieren.
Darüber hinaus supprimiert Cortisol unter chronischer Erhöhung das Immunsystem, was wiederum zu abnormalen Entzündungsmuster führen kann.
Auch die Lymphfunktion, die bei Lipödem oft beeinträchtigt ist, könnte durch chronischen Stress und erhöhtes Cortisol weiter behindert werden.
Stress und Cortisol beeinflussen auch die Hormonachse selbst. Chronischer Stress kann zu Dysregulation des Hypophysen-Hypothalamus-Ovarian-Systems führen, was wiederum zu abnormalen Östrogen- und Progesteron-Mustern führt.
Stress könnte sowohl direkt (durch Cortisol und Entzündung) als auch indirekt (durch Hormonverstärkung) das Lipödem verschlechtern.
Genetik, Hormon, Stress als Gesamtbild
Das aktuelle Verständnis des Lipödems hat sich von einer einfachen „Gewichtsproblem“-Erklärung zu einem komplexen Modell entwickelt, in dem mehrere Faktoren ineinandergreifen.
Die beste aktuelle Formulierung ist: Genetische Veranlagung ist notwendig, aber nicht ausreichend. Es braucht einen Triggerfaktor, meist mehrere Faktoren, um das Lipödem zum Ausbruch zu bringen.
Die primären Triggerfaktoren sind hormoneller Natur:
- Pubertät
- Beginn hormoneller Verhütung
- Schwangerschaft,
- Perimenopause
- Menopause
Diese sind die kritischen Punkte, an denen viele Frauen mit genetischer Veranlagung ihr Lipödem zum ersten Mal bemerken.
Aber auch sekundäre Faktoren spielen eine Rolle. Chronischer psychischer Stress kann das Lipödem triggern oder verschlimmern, wahrscheinlich durch eine Kombination aus Cortisol-Erhöhung, Entzündungsaktivierung und sekundärer Hormonverstärkung. Übergewicht ist kein Ursachenfaktor, kann aber die Symptomatik verschlechtern
Eine übergewichtige Frau ohne genetische Lipödem-Veranlagung wird niemals ein Lipödem entwickeln, aber eine genetisch veranlagte Frau kann durch Übergewicht ihre Symptome verschärfen.
Diese Komplexität erklärt auch, warum das Lipödem so variabel ist. Zwei Frauen mit identischer genetischer Veranlagung können völlig unterschiedliche Verläufe haben, je nachdem, welche Hormon-Trigger sie erleben und welchen Stress sie ausgesetzt sind.
Eine Frau könnte die Pubertät mit minimalen Symptomen überstehen, dann aber eine Schwangerschaft erleben, die zu einem dramatischen Lipödem-Schub führt.
Eine andere Frau könnte das ganze Leben über minimal betroffen sein, bis die Menopause sie mit einem neuen Schub konfrontiert.
Klinische Implikationen
Verstehen, dass Östrogen und Stress relevante Faktoren sind, hat therapeutische Implikationen:
- Lipödem-Patientinnen sollten bei der Wahl von Verhütungsmitteln sehr sorgfältig sein. Ein Wechsel zu einem niedrig-dosierten Östrogenprodukt oder zu nicht-hormonalen Verhütungsmethoden könnte in einigen Fällen Symptome verbessern.
- Stressmanagement ist nicht nur für das psychisches Wohlbefinden wichtig, sondern hat auch eine direkte medizinische Komponente: chronisch erhöhter Stress kann tatsächlich das Lipödem verschlechtern und sollte aktiv adressiert werden.
- Diagnostische Skepsis ist angebracht, wenn ein Bluttest „normale“ Östrogen-Werte zeigt, aber eine Patientin unter Lipödem-Schüben leidet. Das Problem könnte nicht im absoluten Östrogen-Level liegen, sondern in der Balance zwischen Östrogen, Progesteron und Testosteron, oder in den lokalen Hormonkonzentrationen im Fettgewebe selbst, die durch einen Bluttest nicht erfasst werden.
Ein erfahrener Lipödem-Arzt wird mehr tun, als nur den Bluttest zu lesen; er wird die Patientin nach Stress, Lebensveränderungen und Menstruations-Mustern befragen. - Therapeutisch, dass es jenseits von Liposuktion und Kompressiontherapie weitere Ansatzpunkte gibt. Stressabbau, Stressmanagement-Techniken, möglicherweise sogar spezifische Ernährungsanpassungen, die den Hormonhaushalt stabilisieren, könnten theoretisch das Lipödem-Verhalten verbessern. Dies wird derzeit aktiv untersucht.
Studien
Östrogen
- FANG et al. (2026) – Impact of hormones on lipedema development: a systematic literature review„
„Lipödeme scheinen eine multifaktorielle Erkrankung zu sein, die in erster Linie durch eine hormonelle Dysregulation verursacht wird – insbesondere im Zusammenhang mit Östrogen – sowie durch metabolische und mögliche genetische Komponenten. Die Ergebnisse stützen die Neuklassifizierung des Lipödems als hormonell beeinflusste Erkrankung, die sich von Fettleibigkeit unterscheidet, und unterstreichen die Notwendigkeit weiterer Forschung zu diagnostischen Biomarkern, gezielten Therapien und der Rolle der genetischen Anfälligkeit.“ - VIANA et al. (07.2025) – „Menopause as a Critical Turning Point in Lipedema“„
- KATZER et al. (2021) – „Lipedema and the Potential Role of Estrogen in Excessive Adipose Tissue Accumulation„
Zeigt, dass Östrogen die Adipogenese durch ERα-Aktivierung und PPARγ-Expressionsteigerung fördert - VIANA et al. (07.2025) – „Menopause-induced estrogen deficiency amplifies adipose tissue dysfunction by suppressing ERα signaling; enhancing ERβ activity; and disrupting mitochondrial function„
„Der systemische Rückgang des zirkulierenden Östradiols, gepaart mit einer verstärkten intrakrinen Östradiolproduktion im betroffenen Fettgewebe, angetrieben durch Aromatase- und 17β-HSD1-Überexpression und 17β-HSD2-Mangel, zusammen mit einem Ungleichgewicht, das ERβ gegenüber der ERα-Signalgebung begünstigt, schafft ein entzündungsförderndes, profibrotisches und östrogendominantes Mikroumfeld. Dieses hormonelle Milieu fördert die Hypertrophie der Adipozyten, chronische Entzündungen, den Umbau der extrazellulären Matrix und die Resistenz gegen die Lipidmobilisierung.“ - CIFARELLI et al. (2025) – „Lipedema: From Women’s Hormonal Changes to Nutritional Intervention„
Zeigt chronische Entzündung als Kernmechanismus, erwähnt auch Leaky Gut, häufig durch Dysbiose oder andere Darmbarrierestörungen verursacht und geht näher auf entzündungsmindernde Maßnahmen, Nahrungsergänzungsmittel ein.
„Dieser Zustand führt zu einer chronischen, leichten Entzündung, die teilweise auf die Translokation von LPS (Lipopolysacchariden), die Bestandteile der äußeren Membran gramnegativer Bakterien sind, aus dem Darm in den systemischen Kreislauf zurückzuführen ist.
Wenn LPS durch den Blutkreislauf zirkuliert, erreicht es auch Adipozyten, die dann entzündungsfördernde Zytokine wie TNF-α, IL-6 und IL-1β produzieren, die die Funktionen der Adipozyten verändern und eine signifikante lokale Entzündungsreaktion verursachen.“
Stress und Cortisol
- DINNENDAHL et al. (09.05.2024) – „The Expression of Adipogenic Marker Is Significantly Increased in Estrogen-Treated Lipedema Adipocytes Differentiated from Adipose Stem Cells In Vitro„
„Diese Studie weist darauf hin, dass die Expression von ERs und mehreren östrogenmetabolisierenden Enzymen bei Lipödemen unterschiedlich ist, und legt nahe, dass Östrogen eine Rolle bei der Dysregulation des Fettgewebes bei Lipödemen spielen könnte.“
Entzündungs-Biomarker
- Laura Patton e.a. – 27.01.2024 – „Observational Study on a Large Italian Population with Lipedema: Biochemical and Hormonal Profile, Anatomical and Clinical Evaluation, Self-Reported History„
Größte bekannte Kohortenstudie mit 360 Frauen mit Lipödem in Italien
„Normale Bluttests schließen Lipödem nicht aus“ – das Problem liegt nicht im systemischen Hormonspiegel, sondern in der lokalen Hormonverstoffwechselung im Fettgewebe - Fühner R. e. a. – (07.12.2022) – „Lipedema: Insights into Morphology, Pathophysiology, and Challenges„
„Das Lipödem lässt sich anhand seiner einzigartigen morphologischen und molekularen Merkmale von Adipositas und Lymphödem unterscheiden.“
Multidisziplinärer Überblick
Cifarelli V. – (2025) – „Lipedema: Progress, Challenges, and the Road Ahead„
Der Menstruellen Zyklus verstehen
Der Menstruationszyklus ist ein Vier-Wochen-Tanz zwischen zwei Hormonen: Östrogen und Progesteron. Um die Auswirkungen dieser Hormone vollständig zu verstehen, ist es wichtig, den Zyklus in seine Phasen zu unterteilen.
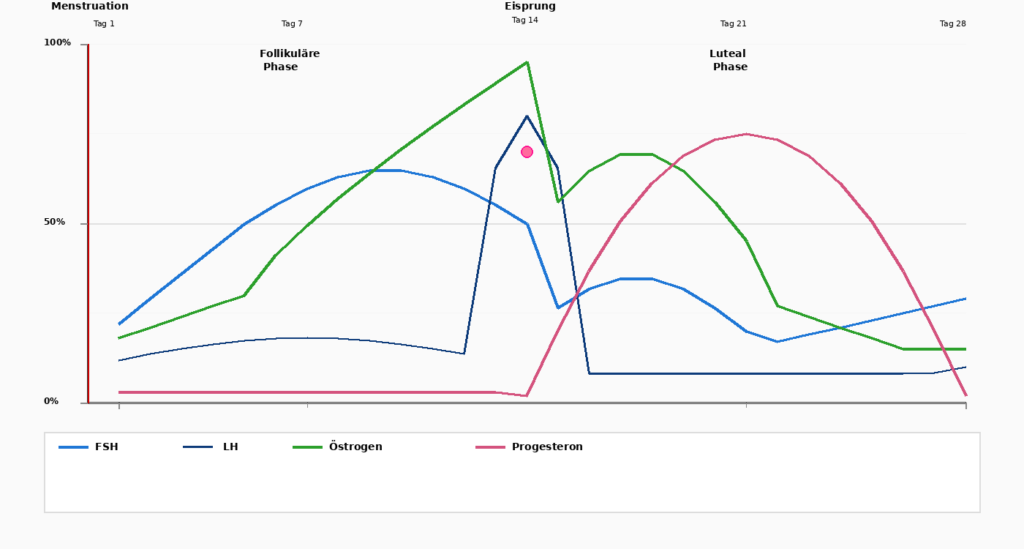
Tage 1–5
Menstruation
Der Zyklus beginnt mit der Menstruation, wenn die aufgebaute Gebärmutterschleimhaut abgestoßen wird. Östrogen und Progesteron sind auf ihren niedrigsten Werten.
Tage 1–14
Follikuläre Phase
Nach der Menstruation beginnt die Hypophyse, FSH (follikelstimulierendes Hormon) auszuschütten, das die Eizellentwicklung in den Eierstöcken stimuliert. Zeitgleich beginnt Östrogen zu steigen. Der Körper wird aktiver, Energie nimmt zu, die Gebärmutterschleimhaut beginnt zu wachsen.
Tag 14
Ovulation (Eisprung)
Ein dramatischer Anstieg von LH (Luteinisierendes Hormon) triggert den Eisprung. Das Ei wird freigesetzt und wandert in die Eileiter. An diesem Punkt erreicht Östrogen seinen Höchstwert, bevor es plötzlich abfällt. Gleichzeitig beginnt Progesteron zu steigen.
Tage 15–28
Lutealphase
Nach dem Eisprung dominiert Progesteron die zweite Hälfte des Zyklus. Progesteron bereitet die Gebärmutterschleimhaut für den Fall vor, dass ein Ei befruchtet wurde.
Gleichzeitig beruhigt Progesteron den Körper: Der Schlaf kann tiefer werden, Nervosität nimmt ab. Wurde das Ei nicht befruchtet, sinken Östrogen und Progesteron am Ende dieser Phase deutlich ab und triggert die nächste Menstruation.
Hormonelle Schwankungen im Menstruellen Zyklus
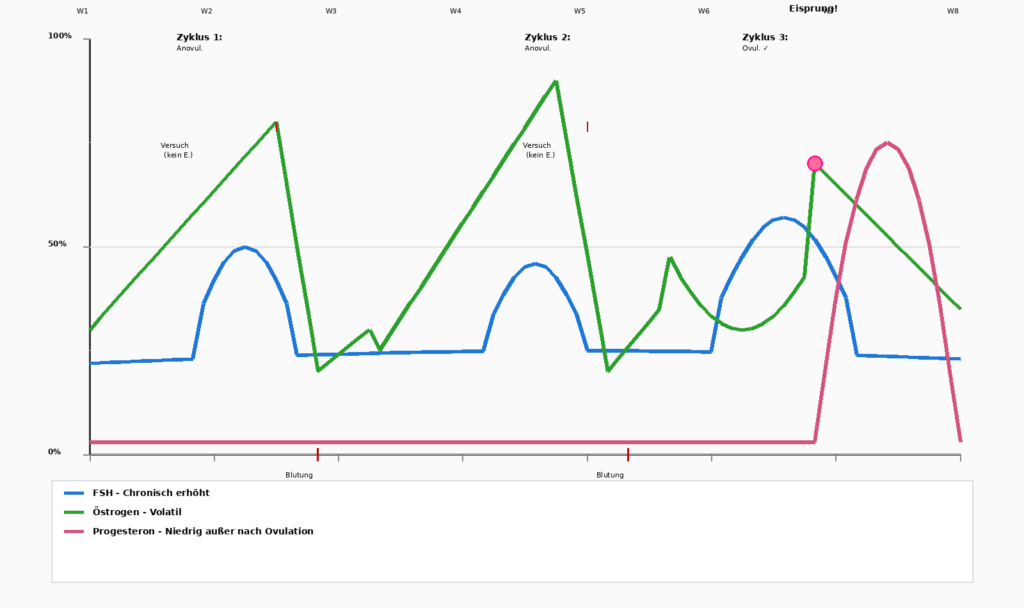
Östrogenberschuss – Das subtile Ungleichgewicht
Es ist wichtig zu beachten, dass nicht immer ein absoluter Mangel das Problem ist, denn manchmal ist es ein Ungleichgewicht. Wenn Progesteron fällt, während Östrogen relativ erhöht bleibt, entsteht eine „Östrogendominanz“ (relative, nicht absolute). Dies führt zu:
- Gewichtszunahme
Erschwerte Gewichtsabnahme trotz Ernährungsumstellung - Kopfschmerzen
Regelmäßige oder verstärkte Kopfschmerzen - Stimmungsschwankungen
Emotionale Labilität - Brustspannung
Persistente Brustschmerzen oder -spannung - Blähungen
Erhöhte Bauchaufblähung - Reizbarkeit
Erhöhte Gereiztheit - Starke Menstruation
Unkontrolliert starke Blutungen
Veränderungen – Prämenopause bis Menopause
Der Hormonstatus einer Frau ist nicht statisch. Er durchläuft verschiedene Phasen, jede mit ihren eigenen Herausforderungen.
- Fruchtbare Jahre (bis ~35 Jahre)
Östrogen und Progesteron befinden sich in einem stabilen Rhythmus. Der Eisprung funktioniert konsistent, und die Menstruation ist vorhersehbar. Die meisten Frauen haben weniger Symptome. - Prämenopause (35–42 Jahre)
Progesteron fällt zuerst. Östrogen bleibt anfangs hoch. Dies führt zu klassischen PMS-Symptomen: Schlaflosigkeit, extreme Reizbarkeit, heftige Blutungen. Das Leben fühlt sich „unmöglich“ an. - Perimenopause/Menopause (42–49 Jahre)
Dies ist die turbulenteste Phase. Progesteron bleibt niedrig, aber Östrogen wird volatil: es schießt hoch und fällt dann plötzlich ab.
Eine Frau weiß nicht, wie sie sich von Tag zu Tag fühlen wird. Manchmal hat sie starke Blutungen, manchmal gar keine. Manchmal hat sie Energie, manchmal fühlt sie sich völlig erschöpft.
Viele Frauen beschreiben diese Phase als „fiese“, schlimmer als sogar die frühen Wechseljahre, weil die Unvorhersehbarkeit ein Gefühl „es“ nicht mehr im Griff zu haben beschert.
Maßnahmen bei Hormonalen Dysbalancen und PMS
Die gute Nachricht ist, dass vieles getan werden kann, um hormonale Symptome zu lindern und die Lebensqualität zu verbessern. Der Ansatz sollte aber mehrschichtig sein.
Diagnostische Grundlagen
Der erste Schritt ist das Verständnis des eigenen Hormonprofils durch Tests.
Bluttests können die Spiegel von Östrogen, Progesteron, FSH, LH und anderen Hormonen messen.
Speicheltests sind weniger invasiv und können auch informativ sein.
Das Wichtigste ist, diese Tests nicht an zufälligen Tagen durchzuführen, das Timing ist entscheidend: Progesteron sollte in der Lutealphase (idealerweise um Tag 21) getestet werden, nicht in der follikulären Phase.
Ernährung
Die moderne Ernährung ist zu oft unzureichend. Studien zeigen, dass Gemüse und Obst heute etwa 80% weniger Vitamine enthalten als vor 50 Jahren. Dies ist kein Versagen der Landwirte, sondern die Folge von z.B. zu intensiver Landwirtschaft, ausgelaugter Böden, geringer Sortenvielfalt, falscher Erntezeitpunkte, längerer Transportwege. Deshalb ist es essentiell, bewusst auf ausreichende Nährstoffzufuhr zu achten.
Blutzuckerstabilität
Ein Schlüssel zur Hormongesundheit ist die Stabilisierung des Blutzuckers. Frauen sollten regelmäßige Mahlzeiten mit ausreichend Protein essen. Besonders in der Lutealphase (zweite Zyklushälfte) benötigt der Körper mehr Kalorien und Nährstoffe.
Stressmanagement und Lebensstil
Chronischer Stress ist einer der Haupttreiber hormonaler Dysbalancen.
Wenn eine Frau unter anhaltendem Stress steht, gibt die Nebenniere ständig Cortisol ab. Dies konkurriert um Ressourcen mit Progesteron und Testosteron.
Die Lösung ist nicht, „Cortisol zu senken“ (was während des Stresses unmöglich und gefährlich wäre), sondern die Stressquellen zu reduzieren. Dies kann bedeuten, von einigen (z.T. vermeintlichen) Verpflichtungen loszulassen, Grenzen zu setzen oder sogar die Karriere zu überdenken.
Schlaf
Sieben bis neun Stunden qualitativ hochwertiger Schlaf sind nicht luxuriös, sie sind essentiell für die Hormonproduktion und -regulation. Ein Mangel an Schlaf verstärkt Progesteronmangel exponentiell.
Nahrungsergänzungsmittel
Während eine gute Ernährung die Grundlage ist, können gezielt eingesetzte Nahrungsergänzungsmittel den Körper unterstützen. Der Schlüssel ist Verständnis: Supplements ersetzen keine Ernährung, aber sie schließen die Lücken, die moderne Landwirtschaft und Lebensstil hinterlassen.
Der Magnesium-Vitamin D3-Vitamin K2 Komplex
Diese drei Substanzen sind untrennbar miteinander verbunden. Oft werden sie fälschlicherweise jedoch von einander isoliert betrachtet.
Der Zusammenhang:
- Magnesium beeinflusst über 400 körperliche Prozesse
- Vitamin D3 (das technisch ein Hormon ist, kein Vitamin) fördert die Calciumabsorption
- Vitamin K2 aktiviert Osteocalcin, das Protein, das Calcium in die Knochenmatrix einleitet
Wenn eines dieser drei fehlt oder auch nur unzureichend vorhanden ist, funktioniert das System nicht richtig.
Andere essentielle Nährstoffe
- Omega-3-Fettsäuren
Hormonregulation, Herz-Kreislauf-Gesundheit, Entzündungshemmung, Sehkraft - B-Vitamine
Unterstützung des Hormonmetabolismus und des Nervensystems - Vitamin C und E
Antioxidantischer Schutz, Kollagenbildung - Zink
Immunfunktion und Hormonproduktion - Eisen
Besonders wichtig bei menstruierenden Frauen wegen der natürlichen Blutverluste - Probiotika
Darmgesundheit, Hormonstoffwechsel, Nährstoffaufnahme
Der Darm ist ein oft übersehenes hormonelles Organ. Ein großer Teil des Hormonstoffwechsels findet im Darm statt. Ein gesundes Mikrobiom fördert nicht nur die Nährstoffaufnahme, sondern auch die Hormonrecirulation. Probiotika (in spezieller Verkapselung, um der Magensäure zu widerstehen) können das Darmgleichgewicht wiederherstellen.
Ätherische Öle
Ätherische Öle sind konzentrierte Pflanzenstoffe, die über Inhalation und topische Anwendung in das Nervensystem eingreifen können. Sie sind kein Ersatz für medizinische Behandlung, aber eine wertvolle Ergänzung.
Lavendel – zur Beruhigung
Wirkeigenschaften
Blutdruckregulation, Herzfrequenz-Stabilisierung, Krampflösung, Sedierung
Indikationen
Schlaflosigkeit, Periodenschmerzen, Bluthochdruck, PMS-assoziierte Symptome
Anwendung
3–4 Tropfen mit Trägeröl (Kokos, Jojoba) auf Bauch, Nacken oder Fußsohlen. Kann auch in einem Diffuser verwendet werden.
Ylang-Ylang – Blutdruck- und Libido-Regulans
Wirkeigenschaften
Blutdruckregulation, Libido-Steigerung, emotionale Balance, Hormonmodulation
Besonderheit
Dieses Öl hat sich als besonders wirksam gegen Bluthochdruck erwiesen, selbst in Fällen, wo Medikamente nicht genug halfen.
Anwendung
2 Tropfen sublingual (auf die Zunge), oder topisch auf Pulspunkte und Nacken
Magnolia – Nebennieren-Adaptogen
Wirkeigenschaften
Nebennieren-Unterstützung, Stressabbau, Angst-Reduktion, Panikattacken-Linderung
Anwendung
Morgens und abends auf die Nierengegend (unterer Rücken) mit Trägeröl auftragen. Regelmäßige Anwendung über einen Monat zeigt deutliche Effekte.
Balance – Harmonisierung und Hitzewallungs
Wirkeigenschaften
Emotionale Stabilisierung, Stimmungsausgleich, Hitzewallungs-Linderung
Anwendung
4 Tropfen mit Trägeröl auf beide Fußsohlen morgens nach dem Aufwaken.
Serenity – (Nacht-)Entspannung
Wirkeigenschaften
Tiefe Entspannung, Schlafförderung, mentale und emotionale Beruhigung
Routine
3–4 Tropfen mit Trägeröl auf die Füße vor dem Schlafengehen führt zu erholsamem Schlaf.
Vetiver und Adaptive
Vetiver bringt Energie und Vitalität. Adaptive ist einzigartig, enthält Rosmarin (für mentale Klarheit) gemischt mit sedierenden Komponenten.
Wichtig
Ätherische Öle sollten immer mit einem Trägeröl verdünnt werden. Die Dosierung ist individuell, manche Frauen reagieren auf 2 Tropfen, andere benötigen 4 oder mehr.
Ein integrativer Ansatz zur Hormongesundheit
Der Schlüssel zu verbesserter Hormongesundheit liegt in einem integrativen Ansatz:
- Tests
Hormonwerte kennen, nicht raten - Ernährung
Echte Nahrung, regelmäßig, mit ausreichend Protein und stabilem Blutzucker - Stress reduzieren
Chronischen Stress identifizieren und systematisch abbauen - Schlaf optimieren
7–9 Stunden konsequent, zur gleichen Zeit - Nahrungsergänzung
Gezielt, basierend auf Tests und Symptomen - Aromatherapie
Ätherische Öle zur emotionalen und körperlichen Unterstützung - Nachverfolgung
Symptome dokumentieren, Hormonwerte regelmäßig überprüfen
Das Ziel ist nicht einfach, Symptome zu lindern, auch wenn das wichtig ist. Das Ziel ist, eine Frau so zu unterstützen, dass sie bis 80, 90 Jahren vital und lebendig bleibt. Ohne diesen integrativen Ansatz können viele Frauen das Gefühl haben, dass ihr Leben mit 50 oder 60 vorbei ist. Mit ihm können sie wieder aufblühen.
Eine Grundlage schaffen ist nicht kompliziert, es erfordert nur Klarheit über, was der Körper braucht, und die Entschlossenheit, es ihm zu geben. Zwei Minuten am Tag, um Gesundheit zu stärken, beeinflussen jede weitere Entscheidung, die man an diesem Tag trifft.