Table des matières
Mise à jour – 18 février 2023
Ce blog ne sera plus continué. Le Blog Corona 2023 traite d'informations de base devenues connues, notamment de la part de l'industrie pharmaceutique et des institutions des autorités sanitaires au niveau international.
Ici, la mise à jour des données est toujours la priorité absolue - des articles sur divers sujets suivent ci-dessous cette rubrique. Le message le plus récent se trouve en haut et comporte un en-tête rouge.
Après que de nombreuses mises à jour aient été manquées en raison de contraintes de temps, vous trouverez ci-dessous des animations vidéo des données pertinentes au fil du temps depuis le premier rapport enregistré d'un effet secondaire à ce jour, dans un ordre chronologique, le plus récent en premier. (Source: Programmation d'analyse de données EMA/EMA).
- Péricardite
- Maladie de Creutzfeldt-Jakob
- Myocardite
- Trouble menstruel
- Syndrome de Guillain-Barré
- paralysie de Bell
- Trouble du sommeil
- Hallucination
- Thrombocytopénie
- Avortement spontané
- Douleur oculaire
- Perte de conscience
- Narcolepsie
- Lymphadénopathie
- La fréquence cardiaque a augmenté
- Maux de tête
- Thrombose cérébrale
- Thrombose du sinus veineux cérébral
- Thrombose veineuse cérébrale
- Thrombose veineuse profonde
- Thrombose de la veine mésentérique
- Thrombose de la veine porte
- Thrombose du sinus sagittal supérieur
- Herpès zoster
- Thrombose
- Thrombose veineuse
- Membre de thrombose veineuse
- Acouphènes
- Mort subite
- Saignements intermenstruels
- Menstruation retardée
- Menstruations irrégulières
- Urticaire
La section ci-dessous ne sera plus mise à jour. Le développement des données EMA sera remplacé par les vidéos ci-dessus !
Mise à jour des données – EMA – VAERS – OMS – Rapports d'effets secondaires
* augmenter du 13 novembre 2021 au 3 décembre 2021 à 368.653 Messages
Total des rapports : EMA 1 254 029 (+ 90 673*) / OMS 2 706 410 (+206 529*) / CDC/FDA 951857 (+71 451*)
Symptôme : Paralysie de Bell (paralysie faciale) – Rapports enregistrés
Augmentation du 30 décembre 2021 au 15 janvier 2022 / du 17 décembre 2021 au 7 janvier 2022 6.620 cas
Sources : adrreports.eu (EMA) / vigiaccess.org (OMS) – Au 10 décembre 2021
Source: vaers.hhs.gov (CDC / FDA) – au 3 décembre 2021
EMA
6.113 (+ 1.350*)
OMS
7.875 (+ 3.650*)
VAERS
5.405 (+ 1.620*)
Symptôme : Troubles menstruels – Rapports enregistrés
Sources : adrreports.eu (EMA) / vigiaccess.org (OMS) – Au 13 novembre 2021
Source: vaers.hhs.gov (CDC / FDA) – Au 5 novembre 2021
EMA
9.849
OMS
15.660
VAERS
4.002
Symptôme : avortement spontané – Rapports enregistrés
Sources : adrreports.eu (EMA) / vigiaccess.org (OMS) – Au 13 novembre 2021
Source: vaers.hhs.gov (CDC / FDA) – Au 5 novembre 2021
EMA
1.823
OMS
3.424
VAERS
2.188
Symptôme : Lymphadénopathie – Rapports enregistrés
* augmenter du 18 décembre 2021 au 24 décembre 2021 / du 10 décembre 2021 au 17 décembre 2021 à 713 cas
Sources : adrreports.eu (EMA) / vigiaccess.org (OMS) – Au 24 décembre 2021
Source: vaers.hhs.gov (CDC/FDA) – Au 17 décembre 2021
EMA
50.222
OMS
94.166
VAERS
31.040
Symptôme : Décès – Rapports enregistrés
Données actuelles sur Surmortalité dans toutes les tranches d’âge peut être trouvé quotidiennement ici.
Les graphiques sont créés à partir des données de 29 pays participants : Belgique, Danemark, Estonie, Finlande, France, Allemagne, Allemagne (Berlin), Allemagne (Hesse), Grèce, Hongrie, Irlande, Israël, Italie, Luxembourg, Malte, Pays-Bas, Norvège. , Portugal, Slovénie, Espagne, Suède, Suisse, Grande-Bretagne (Angleterre), Grande-Bretagne (Irlande du Nord), Grande-Bretagne (Écosse), Grande-Bretagne (Pays de Galles) et Ukraine.
L’Ukraine, l’Allemagne (Berlin) et l’Allemagne (Hesse) n’ont pas été incluses dans les données regroupées.
(Source : Euromomo)
* augmenter du 16 mars 2022 au 26 mars 2022 / du 5 mars 2022 au 18 mars 2022 à 2.595 Décès
(doublement à partir du 15 mars / 4 mars)
Sources : adrreports.eu (EMA) – au 26 mars 2022 / vigiaccess.org (OMS) – Au 26 mars 2022
Source: vaers.hhs.gov (CDC/FDA) – Au 18 mars 2022
EMA
23.157 (+609*)
OMS
19.088 (+736*)
VAERS
25.051 (+1.250*)
Symptôme : Myocardite (inflammation du muscle cardiaque) – Rapports enregistrés
* augmenter du 19 novembre 2021 au 3 décembre 2021 / du 12 novembre 2021 au 29 novembre 2021 à 2.088 Messages
Sources : adrreports.eu (EMA) / vigiaccess.org (OMS) – Au 19 novembre 2021
Source: vaers.hhs.gov (CDC/FDA) – Au 12 novembre 2021
EMA
8.292 (+1.028*)
OMS
13.371 (+1.235*)
VAERS
7.879 (+693*)
Symptôme : Péricardite (inflammation du sac cardiaque) – Rapports enregistrés
* augmenter du 10 décembre 2021 au 24 décembre 2021 à 10.367 Messages
Sources : adrreports.eu (EMA) / vigiaccess.org (OMS) – Au 24 décembre 2021
Source: vaers.hhs.gov (CDC/FDA) – Au 17 décembre 2021
EMA
9.932 (+3.205*)
OMS
16.234 (+5.306*)
VAERS
9.546 (+4.033*)
Symptôme : Herpès Zoster – Rapports enregistrés
Sources : adrreports.eu (EMA) / vigiaccess.org (OMS) – Au 13 novembre 2021
Source: vaers.hhs.gov (CDC / FDA) – Au 5 novembre 2021
EMA
12.876
OMS
23.682
VAERS
9971
Symptôme : Thrombose – Rapports enregistrés
Sources : adrreports.eu (EMA) / vigiaccess.org (OMS) – Au 13 novembre 2021
Source: vaers.hhs.gov (CDC / FDA) – Au 5 novembre 2021
EMA
8.110
OMS
11.254
VAERS
6.284
Symptôme : Mort subite – Rapports enregistrés
Sources : adrreports.eu (EMA) / vigiaccess.org (OMS) – Au 13 novembre 2021
Source: vaers.hhs.gov (CDC / FDA) – Au 5 novembre 2021
EMA
829
OMS
1.463
VAERS
729
Évaluation de l'adéquation de la technique RT‐qPCR pour
Preuve d’une possible infection et
Contagiosité des individus concernant le SRAS-CoV-2
Rapport actuel du Dr. rer. biol. hum. Ulrike Kammerer
Le rapport est ici de la site web le Médecins et scientifiques pour la santé, la liberté et la démocratie, eV ou stocké ici téléchargeable.
Résultats de tests PCR faussement positifs sur banc de test
Les chercheurs Leslie C. Woodcock, P. Stallinga et Igor Khmelinskii de l'Université portugaise de l'Algarve rapportent dans leur article publié dans The Lancet Respiratory Medicine en novembre 2021 Rôle des exosomes dans les tests PCR covid-19 faussement positifs sur leurs résultats de recherche, qui portent sur ceci lien sont disponibles en téléchargement.
Mise à jour des données – EMA – VAERS – OMS – Rapports d'effets secondaires
Les chercheurs Leslie C. Woodcock, P. Stallinga et Igor Khmelinskii de l'Université portugaise de l'Algarve rapportent dans leur article publié dans The Lancet Respiratory Medicine en novembre 2021 Rôle des exosomes dans les tests PCR covid-19 faussement positifs sur leurs résultats de recherche, qui portent sur ceci lien sont disponibles en téléchargement.
Comparaison des effets secondaires signalés des vaccins sur 1 000 cas

Restriction des droits fondamentaux
Dans le Journal officiel de la République fédérale d'Allemagne, partie I 2021, n° 83 du 11 décembre 2021. Loi visant à renforcer
Prévention vaccinale contre le Covid-19 et évolution des autres réglementations en lien avec la pandémie de Covid à compter du 10 décembre 2021 devenir les droits fondamentaux
- intégrité physique
- la liberté de la personne
- liberté de réunion
- de liberté de mouvement
- l'inviolabilité de l'appartement
RESTREINT (Téléchargement PDF):

Les changements suivants entreront en vigueur le 25 novembre 2021 :
Article 16 – Modification du Livre Douzième du Code Social « § 142 Règlement transitoire sur les déjeuners collectifs destinés aux personnes handicapées en raison de la pandémie de Covid-19 ; Autorisation d’édicter des règlements.
Article 17 – Modification de la loi fédérale sur l'approvisionnement
Article 18 – Modification de la loi sur les demandeurs d'asile
Les changements suivants entreront en vigueur le 1er janvier 2022 :
Article 12bis – Modification du Livre Troisième du Code Social
« À l'article 109, paragraphe 5, phrase 3, la mention « 31. décembre 2021 » remplacé par « 31 mars 2022 ».
« L'article 421c est modifié comme suit : « aa) Dans la phrase précédant le numéro 1, les mots « jusqu'au 31 décembre 2021 » sont remplacés par les mots « du 1er janvier 2022 au 31 mars 2022 ». bb) Dans la phrase qui suit le numéro 2, les mots « si le droit aux indemnités de chômage partiel est né au 31 mars 2021 et » sont supprimés.
Les changements suivants entreront en vigueur le 1 janvier 2023 :
Article 2 – Autres modifications de la loi sur la protection contre les infections
« La loi sur la protection contre les infections, modifiée en dernier lieu par l'article 1er de la présente loi, est modifiée comme suit :
- Le §§ 20a et 20b sont abrogées.
- § 73 est modifié comme suit :
a) Le paragraphe 1a, les numéros 7e à 7h sont abrogés
b) Au paragraphe 2, l'information « 7h » est remplacée par l'information « 7d ».
Interview vaccination corona obligatoire : avantages et inconvénients – MDR
Mardi 23 novembre 2021 6h50 - Durée 6h50 min.
Le Interview du MDR est reproduit ci-dessous en tant que transcription et ici en tant que Téléchargement audio disponible. Le modérateur est Tim Deisinger, ses interlocuteurs sont le professeur Peter Dabrock, professeur de théologie à l'université d'Erlangen Nuremberg et le Dr. méd. Steffen Rabe, pédiatre à Munich et membre du conseil d'administration de Médecins pour les décisions individuelles en matière de vaccination e. v. (ÄIIE).
- Modérateur, Tim Deisinger :
Le grand tabou selon lequel la vaccination obligatoire générale n’est plus une réalité, nombreux sont ceux qui s’expriment et la soutiennent. Nous souhaitons l’examiner de plus près ce matin et également connaître votre opinion à ce sujet, nous y reviendrons dans un instant. Tout d’abord, une sorte de base de discussion, pour ainsi dire. Nous voulons entendre deux points de vue.
Le second sera alors pédiatre et médecin de l'adolescence. Le premier est désormais Peter Dabrock, professeur de théologie à l’université d’Erlangen Nuremberg et président du Conseil d’éthique allemand jusqu’en 2020. Monsieur Dabrock, comment voyez-vous cela ? Vaccination générale obligatoire, oui ou non ?
- Professeur Peter Dabrock :
Donc, euh, j'avoue qu'en ce qui concerne la vaccination obligatoire générale, ma position a changé au fil du temps et c'est ce que l'on remarque aussi dans ces questions : il n'y a pas un seul jugement que vous ayez porté une seule fois et que vous vous en tenez ensuite mais il faut l'adapter aux circonstances. J'en fais la promotion depuis des mois et j'espérais également que les gens se rendraient compte qu'il y a un risque minime pour vous-même et de grands avantages pour vous-même et pour les autres.
et que vous vous faites donc vacciner par autoprotection, protection directe des autres et solidarité. Ce n'était pas le cas et lorsque j'ai appris que le système était devenu très rigide, il y a eu une enquête correspondante il y a trois semaines. Ma position a également changé et c'est pourquoi je penche désormais pour dire que nous avons besoin d'exigences générales en matière de vaccination et le plus rapidement possible.
- Modérateur, Tim Deisinger :
Mais compréhensif pour ceux qui ne veulent pas se faire vacciner ou qui ne veulent pas encore se faire vacciner, est-ce que vous avez toujours ça ?
- Professeur Peter Dabrock :
Alors bien sûr, on y pense, surtout quand on ressent une résistance aussi massive à la marche, et puis on entend toujours les deux arguments : c'est effectivement proportionné et ce n'est pas
une atteinte à l’intégrité physique. Les deux sont également liés et je dirais que, premièrement, lorsqu'il s'agit de l'intégrité physique, quiconque s'oppose à la vaccination obligatoire doit être clair sur le fait que les dommages causés au corps si l'on souffre de la maladie ou même si d'autres personnes souffrent de la maladie seront massivement plus grand. Toutes les données scientifiques sérieuses affirment qu’il existe clairement des risques résiduels minimes, mais que les avantages sont nettement plus importants.
L'autre chose, c'est qu'on ne peut jamais rendre l'intégrité physique absolue lorsqu'il s'agit de droits fondamentaux, mais qu'il faut plutôt la mettre en concordance pratique avec d'autres droits fondamentaux et si la liberté de chacun est massivement restreinte parce que, euh, un petit groupe assure que, euh, que si le virus continue à se propager ainsi, alors l'intégrité physique, que je peux comprendre au premier coup d'œil, ne peut pas être rendue absolue.
- Modérateur, Tim Deisinger :
L'avis de Peter Dabok, ancienne présidente du Conseil d'éthique allemand. Et maintenant, nous voulons entendre le docteur Steffen Raabe, pédiatre et médecin pour adolescents, porte-parole du conseil d'administration de l'Association des médecins pour des décisions individuelles en matière de vaccination, M. Rabe, votre ligne de pensée est donc déjà indiquée dans le nom de l'association. Pouvez-vous encore comprendre l'argument de M. Darbrock ?
- Dr. Steffen Rabe
Non, l’argument en faveur de la vaccination obligatoire m’est totalement incompréhensible, surtout avec les vaccins Covid. Et lorsque j’ai entendu M. Darbrock plaider en faveur d’une protection indirecte des tiers, c’est bien sûr là le point crucial. Seul un tel argument peut même justifier l’envisage d’une vaccination obligatoire et c’est justement cet aspect que les vaccins Covid ne couvrent pas. Les vaccins Covid offrent à ceux qui souhaitent se protéger une protection temporaire, mais pas mauvaise, contre une maladie grave. Mais vous ne bénéficiez d’aucune protection tierce pertinente.
Cela signifie que tout argument en faveur de la vaccination obligatoire est écarté. Et s’il parle d’un risque faible et minime lié à la vaccination, c’est tout simplement faux. En tant que pédiatre, je suis confronté à des jeunes hommes de 16, 18 ans à qui je dois dire que s'ils se font désormais vacciner avec Biontech, le seul vaccin recommandé et approuvé pour eux à l'heure actuelle, alors ils seront risque L'incidence de la myocardite résultant directement de cette vaccination est d'au moins 1 : 5 000. M. Deisinger, nous ne connaissons aucun autre médicament. Je n’ai connu aucun autre vaccin depuis 30 ans combinant une maladie aussi grave comme la myocardite avec un risque aussi dramatiquement élevé. Cette vaccination obligatoire n’est en aucun cas intelligente sur le plan juridique, moral ou médical ; elle est plutôt, comme l’a dit à juste titre M. Hans-Jürgen Pape, l’expression d’un sentiment d’impuissance et d’impuissance.
- Modérateur, Tim Deisinger :
Prenons ensuite l'impuissance face à la situation dans les unités de soins intensifs ou dans les hôpitaux en général, qui est présentée comme un argument supplémentaire selon lequel il y a une urgence et qu'il n'y a pas d'autre issue à l'urgence qu'en exigeant la vaccination.
- Dr. Steffen Rabe
Mais Monsieur Deisinger, la vaccination obligatoire n’est pas une mesure immédiate. La préparation juridique, la mise en œuvre politique et l'efficacité médicale, nous nous mentons si nous constatons un effet dans les unités de soins intensifs d'ici deux à trois semaines. Nous devons cesser de réduire les unités de soins intensifs et les lits de soins intensifs. Au lieu de les forcer à quitter la profession avec des vaccinations obligatoires, nous devons enfin montrer aux infirmières la reconnaissance dont elles ont besoin pour rester dans leur profession. Et la politique a complètement échoué pendant deux ans. Cette catastrophe est une catastrophe avec une annonce, M. Deisinger. Nous savions que cet automne serait un autre défi, également pour les hôpitaux et les unités de soins intensifs, et nous avons rapidement démantelé des milliers de lits de soins intensifs. Et cela devrait maintenant servir d'argument pour une intervention dans l'un des droits fondamentaux centraux, et ici je contredis avec véhémence M. Dabrock, le droit à l'intégrité physique, surtout dans un pays comme l'Allemagne, qui a ce passé malheureux, y compris dans le domaine médical avec ces interventions, nous devons être très, très prudents et très, très prudents dans cette réflexion.
Excipients ALC-0315 et ALC-0159 « à des fins de recherche uniquement »
Les excipients contenus dans Pfizer/BioNTech Comirnaty ALC-0315 [(4-Hydroxybutyl)azanediyl]di(hexane-6,1-diyl)bis(2-hexyldécanoate) (CAS 2036272-55-4) et ALC-0159 Le 2-[(polyéthylène glycol)-2000]-N,N-ditétradécylacétamide (CAS 1849616-42-7) est selon le fabricant ABP Biosciences destiné uniquement à un usage de recherche.
Études actuellement disponibles sur ces excipients :
- http://www.eurannallergyimm.com/cont/journals-articles/1043/volume-potential-culprits-immediate-hypersensitivity-reactions-4579allasp1.pdf (PDFTélécharger) 29.04.2021
- https://www.cell.com/molecular-therapy-family/molecular-therapy/fulltext/S1525-0016(21)00064-2?_returnURL=https%3A%2F%2Flinkinghub.elsevier.com%2Fretrieve%2Fpii%2FS1525001621000642%3Fshowall%3Dtrue (PDFTélécharger) 04.02.2021
Site Internet de la Confédération – suppression de la mention « Y aura-t-il une obligation légale de vacciner – NON »
La version datée 17.11.2021 00:39:55 était encore

La version datée 19.11.2021 16:44:31 est maintenant (ici disponible dans l'original) :

Les liens ci-dessus sont via WayBackMachine (https://web.archive.org) pages d'archives sécurisées.
Ce qui est frappant, c’est que « les vaccins continuent d’être surveillés et testés même après avoir été approuvés… ». Les « approbations » ne sont que des approbations – conditionnelles – et doivent être renouvelées chaque année jusqu’à l’approbation finale (voir ci-dessous).
Extension des approbations – conditionnelles – pour les vaccins Covid-19
Les documents respectifs mentionnés ci-dessous et mis à disposition en téléchargement se trouvent dans la rubrique «Procédures de la Commission européenne" via le lien correspondant indiqué ici "Décision d'exécution de la Commission" sous la forme d'un fichier ZIP en cliquant sur le lien correspondant Icône de document peut être téléchargé dans la colonne de droite.
Le premier symbole signifie «Décisions" (Le fichier ZIP commence par "déc", le deuxième pour "Annexes", correspondant à "anx". La fin du nom de fichier des fichiers décompressés représente l'abréviation de la langue (de – allemand)
Dans la (deuxième) colonne «Type de procédure", par exemple, il y a des entrées concernant "Mises à jour mensuelles" (Mises à jour des informations du fabricant sur le produit, les effets secondaires, etc.), "Corrigendum" (corrections de traduction), "Décision rectificative« (décisions en matière de protection de commercialisation, extensions de celle-ci), ainsi que «Renouvellement annuel» (Prolongation de l'approbation conditionnelle).
Comirnaty – BionTech/Pfizer
La Commission européenne à Bruxelles a annoncé le document le 3 novembre 2021 C(2021) 7992 (définitif), ils Décision d'exécution de la Commission du 3 novembre 2021, «portant prolongation annuelle de l’autorisation conditionnelle du médicament à usage humain « Comirnaty – Tozinameran, vaccin à ARNm contre la COVID-19 (nucléoside modifié) » accordée par la décision C(2020) 9598 (finale) et modifiant cette décision", avec: "L'autorisation conditionnelle accordée par la décision C(2020) 9598(finale) du 21 décembre 2020 est prolongée.“
Spikevax – Moderna
La Commission européenne à Bruxelles partagera le document le 4 octobre 2021 C(2021) 7305 (définitif), ils Décision d'exécution de la Commission du 4 octobre 2021, «portant prolongation annuelle de l’autorisation conditionnelle du médicament à usage humain « Spikevax – Vaccin à ARNm contre la COVID-19 (nucléoside modifié) » accordée par la décision C(2020) 94 (finale) et modifiant cette décision", avec: "L'autorisation conditionnelle accordée par la décision C(2021) 94 (finale) du 6 janvier 2021 est prolongée.“
Vaxzévira – AstraZeneca
La Commission européenne à Bruxelles a annoncé le document le 9 novembre 2021 C(2021) 8206 (définitif), ils Décision d'exécution de la Commission du 9 novembre 2021, «portant prolongation annuelle de l’autorisation conditionnelle du médicament à usage humain « Vaxzevira - Vaccin à ARNm contre la COVID-19 (nucléoside modifié) » accordée par la décision C(2020) 698 (finale) et modifiant cette décision", avec: "L'autorisation conditionnelle accordée par la décision C(2021) 698 (finale) du 29 janvier 2021 est prolongée.“
Vaccin Covid-19 – Janssen
Se trouve actuellement avec le document C(2021) 1763 (définitif) seulement ça Décision d'exécution de la Commission pour l’approbation conditionnelle du vaccin à partir du 11 mars 2021.
Dans Article 4 il précise : « La durée de validité de l’agrément est d’un an à compter de la date de publication de la présente décision. »
Définitions de l'Institut Paul Ehrlich (Î.-P.-É.) sur les vaccins contre la COVID-19
Les liens vers la version du 15 août 2021 et du 7 septembre 2021 sont disponibles via WayBackMachine (https://web.archive.org) pages d'archives sécurisées, tandis que la version actuelle du 23 septembre 2021 * via un lien vers le Page originale de l'Î.-P.-É. peut être lu. Les lettres Main Rouge émises par les sociétés pharmaceutiques sont également présentes ici disponible en téléchargement.
Tous les sites Web répertoriés sont disponibles ici en téléchargement PDF.
15/08/2021 – «Les vaccins contre la COVID-19 protègent contre les infections par le virus SARS-CoV-2. » (site Web comme Téléchargement PDF)
09/07/2021 – «Les vaccins contre la COVID-19 protègent contre les infections graves par le virus SARS-CoV-2.“ (Site Web comme Téléchargement PDF)
23 septembre 2021* – «Les vaccins contre la COVID-19 sont indiqués pour l’immunisation active afin de prévenir la maladie COVID-19 causée par le virus SRAS-CoV-2.“ (Site Web comme Téléchargement PDF)
Notre monde en données – Covid-19, vaccinations, décès
Sur le site Notre monde en données L'Université John Hopkins fournit des données officiellement collectées sur divers sujets dans le monde entier, notamment les statistiques suivantes pour l'Allemagne :
Lien vers les statistiques – Proportion de personnes ayant reçu au moins une dose de vaccin contre la COVID-19
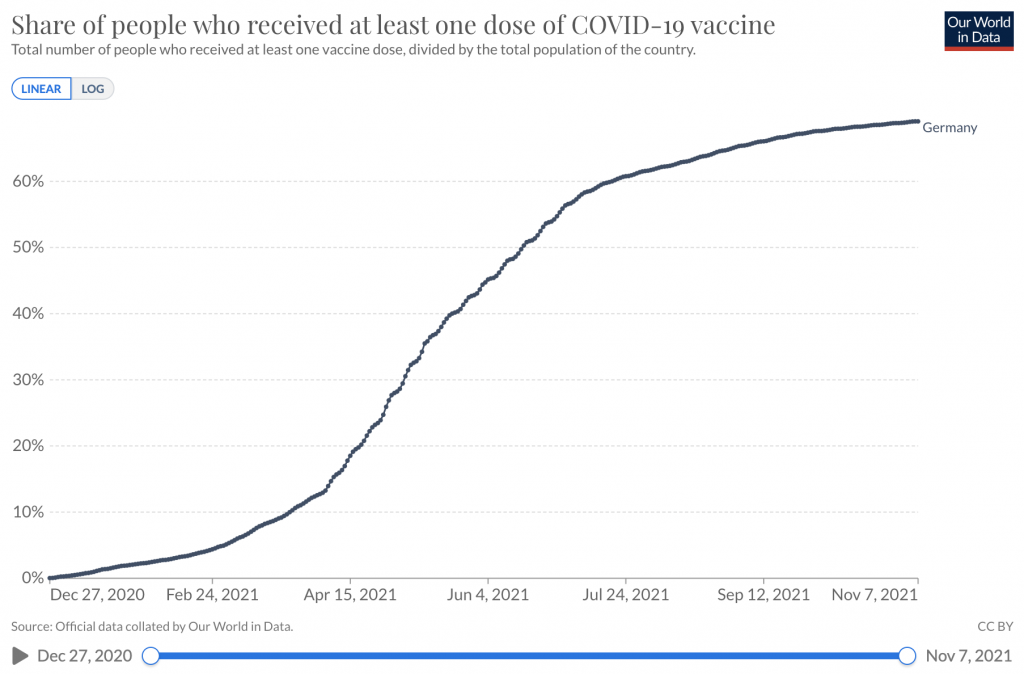
Lien vers les statistiques – Cas cumulés confirmés de COVID-19 par million de personnes
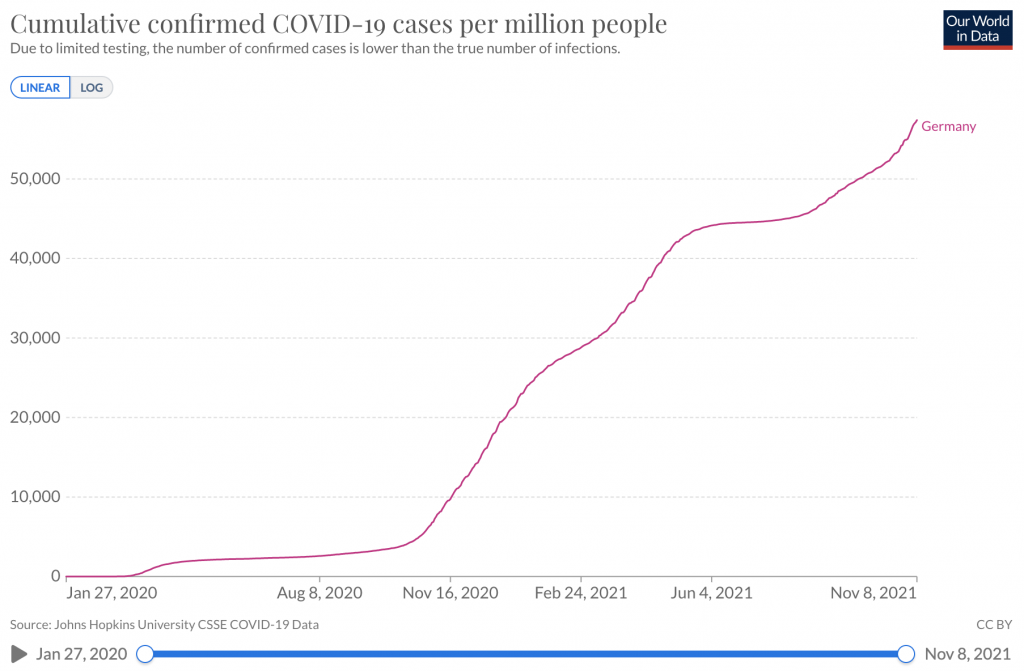
Lien vers les statistiques – Décès cumulés dus au COVID-19 par million de personnes
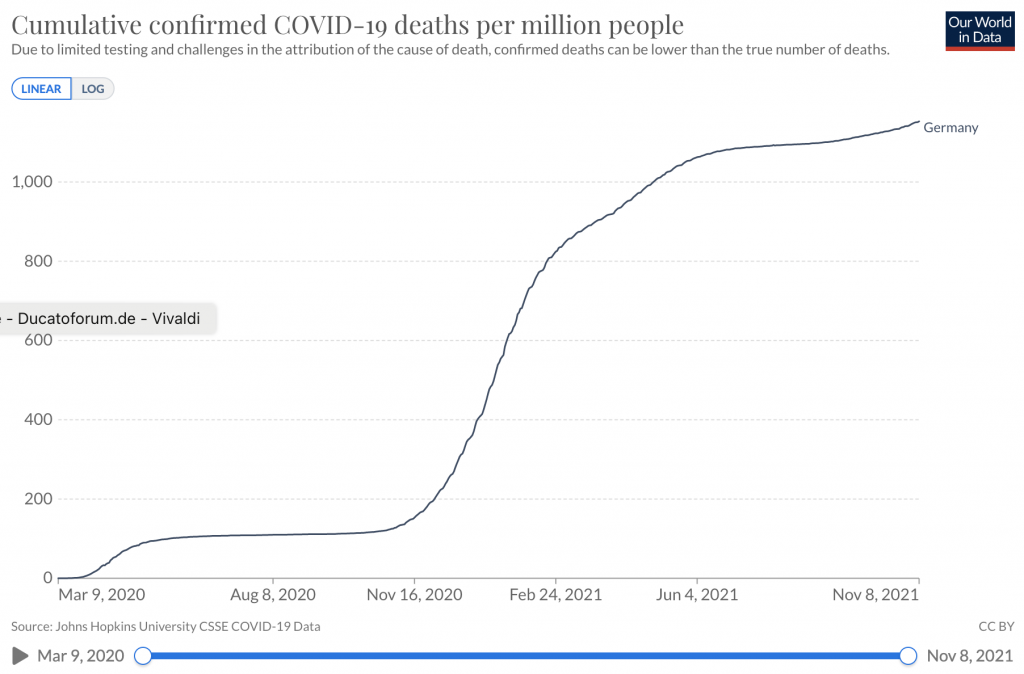
Conseil de l’Europe – Résolution 2361/2021
Le Conseil de l'Europe a, dans sa résolution intitulée Vaccins contre le Covid-19 : considérations éthiques, juridiques et pratiques Des recommandations ont été élaborées qui portent, entre autres, sur la distribution équitable des vaccins, le caractère volontaire de la vaccination et la non-discrimination à l'égard des personnes qui, pour une raison quelconque, choisissent de ne pas se faire vacciner.
« 7.3.1. veiller à ce que les citoyens soient informés que la vaccination n’est pas obligatoire
et que personne ne soit soumis à des pressions politiques, sociales ou autres pour se faire vacciner
s'il ne veut pas le faire lui-même.
"7.3.2 veiller à ce que personne ne soit victime de discrimination parce qu'il n'a pas été vacciné, en raison de risques possibles pour la santé ou parce qu'il ne souhaite pas se faire vacciner."
Le Conseil de l’Europe n’ayant aucun pouvoir législatif, ces recommandations ne sont juridiquement contraignantes pour aucun des États membres.
Ni une interdiction de la vaccination obligatoire ni une discrimination ne peuvent découler de ces recommandations - même si cela serait souhaitable dans l'intérêt des citoyens responsables...
virus de Marbourg
Depuis le début de l’année 2021, les articles sur le virus de Marburg se multiplient. L'un est paru le 25 février 2021 publication d'Elsevier Inc. en Bibliothèque nationale de médecine.
Près de deux mois plus tard, le 22 avril 2021, titrait GAVI L'Alliance du Vaccin „La prochaine pandémie : Marbourg ?“
Déjà en 2018, le Primer Design Ltd. un test PCR”Gènes de la protéine virale 35 (VP35) Kit standard de genèse du virus Marburg„.
Bien que le virus de Marburg, pour la première fois décrit en 1967n était un parent du virus Ebola, les 376 décès à cette époque et seulement 16 depuis 2005 sont très limités.
Dans ce contexte, l’avancée excessive dans le développement d’un vaccin contre le virus de Marburg semble incompréhensible. RiVax® à travers Soligénix Inc.. La précipitation à procéder conformément aux directives de la FDA en matière d'expérimentation animale, en contournant les phases de test habituelles 1, 2 et 3, donne matière à réflexion.
Le 22 septembre 2021, Kieran Morrissey, Dublin, Irlande, résumera ses réflexions sur ce sujet ici ensemble.
Avis juridique sur la vaccination obligatoire indirecte
Dans un document de 111 pages Avis juridique À partir du 4 octobre 2021 Prof. Dr. Dietrich Murswiek, pesant tous les aspects à prendre en compte, est parvenu à la conclusion sommaire : « La discrimination à l'encontre des personnes non vaccinées dans le cadre des réglementations sur l'accès à la vie publique et dans le cadre des règles de quarantaine viole les droits fondamentaux des personnes. personnes concernées et est inconstitutionnelle.
Article_Li
Les hôpitaux devraient embaucher, et non licencier, des infirmières bénéficiant d’une immunité naturelle
PAR MARTIN KULLDORFF 1 OCTOBRE 2021 HISTOIRE, POLITIQUE, SANTÉ PUBLIQUE, SOCIÉTÉ 4 MINUTES
Parmi les nombreux développements surprenants au cours de cette pandémie, le plus étonnant a été la remise en question de l’immunité naturellement acquise après qu’une personne ait contracté la maladie Covid.
Nous comprenons l'immunité naturelle depuis au moins le Peste athénienne en 430 avant JC. Voici Thucydide :
« Pourtant, c'est auprès de ceux qui s'étaient remis de la maladie que les malades et les mourants trouvaient le plus de compassion. Ceux-ci savaient de quoi il s’agissait par expérience et n’avaient aucune crainte pour eux-mêmes ; car le même homme n'a jamais été attaqué deux fois, jamais du moins mortellement. – Thucydide
Nous vivons avec des coronavirus endémiques depuis au moins cent ans, pour lesquels nous bénéficions d’une immunité naturelle de longue durée. Comme prévu, nous bénéficions également d’une immunité naturelle après la maladie Covid-19, car il y a eu extrêmement peu de réinfections entraînant une maladie grave ou un décès, malgré un virus largement circulant.
Pour la plupart des virus, l’immunité naturelle est meilleure que l’immunité induite par le vaccin, et cela est également vrai pour le Covid. Dans le meilleure étude à ce jour, les vaccinés étaient environ 27 fois plus susceptibles de souffrir d’une maladie symptomatique que ceux bénéficiant d’une immunité naturelle, avec une fourchette estimée entre 13 et 57. En l’absence de décès dus au Covid dans l’un ou l’autre groupe, l’immunité naturelle et vaccinale protège bien contre la mort.
Au cours de la dernière décennie, j’ai travaillé en étroite collaboration avec des épidémiologistes hospitaliers. Alors que le rôle des médecins est de traiter les patients et de les rétablir, la tâche de l'épidémiologiste hospitalier est de veiller à ce que les patients ne tombent pas malades pendant leur séjour à l'hôpital, par exemple en attrapant un virus mortel provenant d'un autre patient ou d'un soignant.
À cette fin, les hôpitaux recourent à diverses mesures, allant du lavage fréquent des mains au lavage complet des mains. insignes de contrôle des infections lorsque vous soignez un patient Ebola. Les vaccinations sont un élément clé de ces efforts de contrôle. Par exemple, deux semaines avant une opération de la rate, les patients reçoivent le vaccin antipneumococcique pour minimiser les infections postopératoires, et la plupart du personnel clinique est vacciné contre la grippe chaque année.
Les mesures de contrôle des infections sont particulièrement essentielles pour les patients hospitalisés âgés et fragiles dont le système immunitaire est affaibli. Ils peuvent être infectés et mourir d’un virus auquel la plupart des gens survivraient facilement. L’une des principales raisons justifiant la vaccination des infirmières et des médecins contre la grippe est de garantir qu’ils n’infectent pas ces patients.
Comment les hôpitaux peuvent-ils protéger au mieux leurs patients contre la maladie Covid ? Il s’agit d’une question extrêmement importante, qui concerne également les maisons de retraite. Il existe des solutions standard évidentes, telles que la séparation des patients Covid des autres patients, la minimisation de la rotation du personnel et l’octroi de congés de maladie généreux au personnel présentant des symptômes de type Covid.
Un autre objectif devrait être d’employer du personnel ayant la plus forte immunité possible contre le Covid, car ils sont moins susceptibles de l’attraper et de le transmettre à leurs patients. Cela signifie que les hôpitaux et les maisons de retraite devraient chercher activement à embaucher du personnel naturellement immunisé contre une maladie antérieure à Covid et à utiliser ce personnel pour leurs patients les plus vulnérables.
Nous assistons donc aujourd’hui à une concurrence féroce dans laquelle les hôpitaux et les maisons de retraite tentent désespérément d’embaucher des personnes dotées d’une immunité naturelle. Bien, en fait, pas.
Au lieu de cela, les hôpitaux licencient des infirmières et d’autres membres du personnel dotés d’une immunité naturelle supérieure tout en conservant ceux dont l’immunité induite par le vaccin est plus faible. Ce faisant, ils trahissent leurs patients, augmentant ainsi leur risque d’infections nosocomiales.
En poussant les mandats de vaccination, le conseiller médical en chef de la Maison Blanche, le Dr. Anthony Fauci s'interroge sur l'existence d'une immunité naturelle après la maladie Covid. Ce faisant, il suit l’exemple de la directrice du CDC, Rochelle Walensky, qui a remis en question l’immunité naturelle dans une enquête de 2020. mémorandum publié par Le Lancette. En établissant des obligations vaccinales, les hôpitaux universitaires remettent désormais également en question l’existence d’une immunité naturelle après la maladie Covid.
C'est étonnant.
Je travaille au Brigham and Women's Hospital de Boston, qui a annoncé que toutes les infirmières, médecins et autres prestataires de soins de santé seront licenciés s'ils ne se font pas vacciner contre le Covid. La semaine dernière, j'ai parlé avec une de nos infirmières. Elle a travaillé dur pour soigner les patients du Covid, même si certains de ses collègues sont partis effrayés au début de la pandémie.
Sans surprise, elle a été infectée, mais s’est ensuite rétablie. Elle bénéficie désormais d’une immunité plus forte et plus durable que les administrateurs d’hôpitaux vaccinés travaillant à domicile qui la licencient parce qu’elle n’est pas vaccinée.
Si les hôpitaux universitaires ne parviennent pas à obtenir des preuves médicales exactes sur la science fondamentale de l’immunité, comment pouvons-nous leur faire confiance pour d’autres aspects de notre santé ?
Quelle est la prochaine étape ? Les universités se demandent si la Terre est ronde ou plate ? Au moins, cela ferait moins de mal.

Martin Kulldorff, chercheur principal au Brownstone Institute, est professeur de médecine à la Harvard Medical School
kulldorff@brownstone.org
Plainte pénale et plainte pénale dans le complexe BioNTech
Au procureur général fédéral près la Cour fédérale de justice Dr. Pierre Franck
Le 10 juin 2021, l'avocat Tobias Ulbrich du cabinet d'avocats Robert & Ulbrich, Otto Str. 12, 50859 Cologne ci-dessus a déposé une plainte pénale et une plainte pénale contre « toutes les personnes qui ont développé la substance expérimentale d'ARNm de BioNTech/Pfizer connue sous le nom de ' vaccin' l'a fabriqué, distribué, approuvé pour la vaccination et administré à des gens ignorants. Notamment contre :
1. Alexandra Knauer, Directeur général de la société Knauer Wissenschaftliche Geräte GmbH, Hegauer Weg 38, 14163 Berlin, (fabricant de machines pour la production de nanoparticules lipidiques)
2. Vasant Nasasimhan, PDG de Novartis AG, (titulaire du brevet pour les nanoparticules lipidiques AC – 0135 et AC 0159)
3. James Bradner, MD Président des Novartis Institutes for Bio Medical Research (NIBR), développeur des lipides
4. Thomas D. Madden Ph.D. PDG Acuitas Therapeutics, fabricant de lipides pour Biontech 5. Ying K. Tam, Directeur scientifique Acuitas Therapeutics,
6. Sean Semple, Directeur principal pré-recherche clinique
7. Dr. Dietmar Katinger, PDG Donaustraße 99, 3400 Klosterneuburg, Autriche (fabricant et développeur de production chez Biontech SE)
8. Prof. Dr. Ugur Sahin, PDG de BioNTech SE, Chez Goldgrube 12, 55131 Mayence
9. Sean Marett, CBO et CCO, BioNTech SE, ibid
10. Dr. Sierk Poetting, directeur financier et directeur de l'exploitation, BioNTech SE, ibid
11. PD Dr. Özlem Türeci, directeur marketing, BioNTech SE, ibid
12. Ryan Richardson, CSO, BioNTech SE, ibid
13. Karin Samusch, Dermapharm AG, Lil-Dagover-Ring 7, 82031 Grünwald (Producteur)
14. Hilde Neumeyer, Dermapharm AG, Lil-Dagover-Ring 7, 82031 Grünwald (Producteur) 15. Dr. Hans-Georg Feldmeier, Dermapharm AG, Lil-Dagover-Ring 7, 82031 Grünwald (Producteur)
16. Dr. Jürgen Ott , Dermapharm AG, Lil-Dagover-Ring 7, 82031 Grünwald (producteur) 17. Marc Pfister, Responsable de production pour Biontech chez Novartis AG à Marburg (producteur) 18. Dr. Sabine Marque, Siegfried Hameln, Langes Feld 13, 31789 Hameln, Allemagne (Producteur)
19. Dr. Sven Remmerbach, Baxter Oncology GmbH, Kantstrasse 2, 33790 Halle/Westphalie (Producteur)
20. Dr. Fabrice Guidi, Président; Sanofi-Aventis Deutschland GmbH, parc industriel de Höchst, K703, Brüningstr. 50, 65926 Francfort (producteur)
21. Dr. Matthias Braun, Sanofi-Aventis Allemagne GmbH
22. Olivier Coenenberg, Sanofi-Aventis Deutschland GmbH,
23. Evelyne vendredi, Sanofi-Aventis Deutschland GmbH,
24. Prof. Dr. Jochen Maas, Sanofi-Aventis Deutschland GmbH,
25. Prof. Dr. Cichutek, président de l'Institut Paul Ehrlich, (violation de l'obligation de surveillance et d'avertissement, non-retrait de l'agrément)
26. Professeur Dr. Vieths, vice-président de l'Institut Paul Ehrlich,
27. Dr. Keller-Stanislavski, Département de sécurité des médicaments et des dispositifs médicaux de l'Institut Paul Ehrlich.
28. Professeur Dr. Hildt, Chef du département de virologie à l'Institut Paul Ehrlich
29. Prof. Dr. van Zandbergen, chef du département d'immunologie à l'Institut Paul Ehrlich
30. Dr. Ajouter, chef des départements 3 et 4, vaccins thérapeutiques à l'Institut Paul Ehrlich 31. Matthias Groote, Représentant de l'EMA au Parlement européen, Bergmannstraße 37, 26789 Leer,
32. Karl Broich, Président de l'Institut fédéral des médicaments et des dispositifs médicaux et représentant de l'EMA en Allemagne, Kurt-Georg-Kiesinger-Alle 3, 53175 Bonn,
33. Mme Emer Cooke, Président de l'EMA, Domenico Scarlattilaaan 6, 1083 HS Amsterdam,
34. Le ministre fédéral de la Santé, Jens Spahn, Rochusstraße 1, 53123 Bonn,
35. Prof. Dr. Lothar H. Wieler, à télécharger via l'Institut Robert Koch,
36. Prof. Dr. Christian Drosten, à télécharger via l'Institut Robert Koch,
37. Bill et Melinda Gates,
et autres
De plus, dans les centres de vaccination, il y a tous les vaccinateurs non informatifs qui ont administré le « vaccin » sans référence au statut d'approbation et aux conséquences de la vaccination, qui sont inconnues du signataire.
En raison, entre autres, de génocide, de tentative de génocide, de violation du § 20 KrWKG et de haute trahison contre le gouvernement fédéral„
Le texte intégral très intéressant (194 pages) est ici disponible et cite, entre autres, l'historien Dr. Paul Schreyer, qui a « résumé les événements des 20 dernières années et présenté l'influence des ONG (Organisations Non Gouvernementales) dans la préparation de la pandémie ».
LUBECAVAX – Prof. Winfried Stöcker, Lübeck
Au 31 août 2021
Winfried Stöcker est né en Haute-Lusace en 1947. A étudié la médecine de 1967 à 1973 à Würzburg, a obtenu son doctorat en 1976, professeur à l'Université de médecine Tongji de Wuhan depuis 1999, professeur honoraire à l'Université de Lübeck depuis 2011, a fondé l'entreprise EUROIMMUN Laboratoire Médical Diagnostics AG 1987 avec un accent sur le diagnostic auto-immun et des allergies, ainsi que sur la sérologie des infections et la génétique moléculaire.
Prof. Dr. Stöcker a commencé très tôt à développer un vaccin efficace contre le SRAS CoV2, en le testant d'abord sur lui-même, puis en vaccinant les membres de sa famille et enfin en mettant le vaccin qu'il a fabriqué lui-même à la disposition de ses employés.
Il décrit comment cela fonctionne sur son Blogue comme suit (Citation):
Nous partons du principe qu’une infection corona peut être efficacement évitée grâce à une vaccination. Le Vaccination à Lübeck utilise un petit antigène trivial, fabriqué sur mesure et génétiquement modifié, que le corps n'a pas besoin de synthétiser lui-même, comme c'est le cas avec les processus basés sur le ferry génétique. Il induit la formation d'anticorps dans l'organisme du receveur contre précisément les structures du virus avec lesquelles il se lie aux récepteurs de l'angiotensine-2 des cellules endothéliales chez les personnes non vaccinées. Grâce à ce blocage, les anticorps empêchent les cellules de s’infecter ; le virus ne peut pas s’implanter.
Les vaccinations sont généralement effectuées trois fois : le jour zéro, puis après environ 14 jours et de nouveau après environ quatre semaines supplémentaires. La concentration d'anticorps est mesurée 14 jours plus tard, car nous n'avons pas la certitude officielle que la protection immunitaire aura été constituée d'ici là. Plus de 95% des patients présentent finalement une concentration élevée d'anticorps de la classe des immunoglobulines IgG contre les protéines de pointe du corona, ce qui signifie qu'ils sont probablement immunisés contre le corona. Les personnes immunodéprimées sont vaccinées une ou deux fois avec une double dose - cela ne peut être reconnu qu'en examinant le sérum - et la moitié d'entre elles atteignent alors des titres élevés. En outre, des mesures ont montré que les anticorps étaient capables de neutraliser (inactiver) les virus corona et que l’immunité des lymphocytes T était développée dans les trois quarts des cas.
Il rend également compte du thème de la production de vaccins et de leur application par les médecins en général (Citation):
En Allemagne, chaque médecin est autorisé à mélanger un antigène avec un adjuvant (seulement maintenant, il s'agit d'un vaccin) et à légalement l'injecter ou l'appliquer individuellement à son patient. L'adiuvant détient l'antigène et le présente au système immunitaire. Sans Adiuvans, l’antigène serait distribué dans tout l’organisme et serait donc dilué au point de devenir inefficace. Pour des raisons fonctionnelles, les deux composants doivent être conservés séparément et fraîchement mélangés. Cependant, selon la loi, le médecin n'est pas autorisé à transmettre à des tiers le vaccin qu'il a produit (le mettre sur le marché).
La source est répertoriée sur son blog :
Medidoc GmbH
Jakob-Haringer-Strasse 1
5020 Salzbourg
AUTRICHE
E-mail: info@medidoc.uk
Numéro de téléphone : +43 59333 2000
medidoc.uk
medidoc.us
medidoc.gmbh
UID : ATU33905904
Bureau des impôts de la ville de Salzbourg 114/8583
Registre du commerce : 45971F
Tribunal du registre du commerce : tribunal régional de Salzbourg
Le problème que ce vaccin n’est pas encore reconnu par l’UE (par rapport aux autorisations d’urgence des préparations d’ARNm et de vecteurs) est compensé par le fait qu’il en résulte une immunité aux lymphocytes T, similaire à celle des personnes guéries.
L'immunité des lymphocytes T est déterminée et certifiée par des laboratoires correctement équipés. Ce certificat sert de preuve juridiquement contraignante d’immunité.
Tant que ceux qui se sont rétablis sont et restent sur un pied d'égalité avec ceux qui ont été vaccinés par le gouvernement en ce qui concerne diverses restrictions/assouplissements, ce vaccin est une alternative - désormais bien testée -, sans effets secondaires comparables à l'ARNm. ou des préparations vectorielles.
Vaccin BNT162b2 : possibles erreurs de lecture des codons, erreurs de synthèse protéique et anomalies d'épissage alternatif
Dans un domaine scientifique commentaire daté du 25 mars 2021, publié en prépublication par AUTHOREA, téléchargeable sous PDF en anglais, les effets secondaires possibles du vaccin BioNTec/Pfizer BNT162b2 sont mis en évidence et l'effet général des vaccins à ARNm est présenté. Voici la traduction allemande :
Abstrait
Le vaccin BNT162b2 contre le Covid-19 est constitué d'un ARN de 4284 nucléotides divisés en 6 sections qui fournissent les informations nécessaires pour créer une usine de protéines de pointe S utilisées par le Sars-CoV-2 (Covid-19) pour héberger. Ces protéines sont ensuite dirigées vers l’extérieur de la cellule et déclenchent la réponse immunitaire et la production d’anticorps.
Le problème est la forte altération de l’ARNm : l’uracile est remplacé pour tromper le système immunitaire par de la Ψ (pseudouridine) ; les lettres de tous les triplets de codons sont remplacées par un C ou un G pour augmenter considérablement la vitesse de synthèse des protéines ; Remplacement de certains acides aminés par de la proline ; Ajout d'une séquence (3′-UTR) avec changement inconnu.
Ces déficiences pourraient soulever de forts doutes quant à la présence d’erreurs d’usage des codons. Une éventuelle erreur de traduction a des conséquences sur la physiopathologie de diverses maladies. De plus, l’ARNm injecté est un pré-ARNm, qui peut donner naissance à plusieurs ARNm matures ; Il s’agit d’anomalies d’épissage alternatif qui représentent une source directe de dommages graves à long terme pour la santé humaine.
Essentiellement, ce qui est généré peut ne pas être identique à Protein S Spike : juste une erreur de décodage traductionnel, une mauvaise lecture des codons, la production de différents acides aminés, puis de protéines qui causent de graves dommages à long terme à la santé humaine, bien que l'ADN ne soit pas identique à Protein S Spike. modifié, mais dans le noyau cellulaire et non dans le cytoplasme, où arrive l'ARNm modifié.
Cependant, dans ce cas, la corrélation entre le taux de synthèse et l’expression des protéines avec les erreurs de synthèse ainsi que le mécanisme qui pourrait affecter la traduction de la séquence restent flous, de nombreuses études n’ayant pas encore été réalisées.
introduction
Informations sur le fonctionnement du vaccin
Le vaccin Sars-CoV-2 (Covid-19) de BioNTec/Pfizer appelé BNT162b2, mais également appelé Tozinameran ou Comirnaty, contient environ 30 µg d'ARN qui sont injectés dans une sphère lipidique du corps humain, plus précisément dans le cytoplasme des cellules, mais à l'extérieur du noyau (là où se trouve l'ADN) ; cet ARN a des informations génétiques modifiées (donc modRNA), c'est à dire un ARNm (ARN messager) qui contient des instructions pour construire une usine à protéines, des clones de la protéine S Spike, c'est à dire la protéine (et seulement la protéine, pas le virus entier) du Covid -19 utilisé pour envahir et infecter l'hôte. Une fois produits en série par les ribosomes, ils sont transportés hors de la cellule au-delà de l'enveloppe lipidique ; De cette façon, le système immunitaire identifie ces protéines comme envahisseurs cellulaires et les attaque en produisant des anticorps. Il n’est donc pas concevable que le vaccin induise le Covid-19 ou modifie l’ADN humain.
Notes sur la synthèse des protéines
La traduction est généralement divisée en trois phases : début, extension et fin.
- Le ribosome se lie à l'ARNm au niveau du codon d'initiation ;
- La chaîne polypeptidique s'allonge dans une direction de mouvement des ribosomes par addition successive d'acides aminés ;
- Lorsqu'un codon stop est trouvé, le polypeptide est libéré et le ribosome se dissocie.
Erreurs dans l'assemblage et la traduction des séquences
La conversion de la séquence d'ARNm en polypeptide dépend du transfert d'ARN (ARNt) pour transporter les acides aminés vers le ribosome. Sur les ribosomes, l'ARNt s'apparie à l'ARNm via un appariement de bases complémentaires entre les nucléotides de codon d'ARNm et les nucléotides d'anticodon d'ARNt. Une fois que le bon ARNt est lié par un codon, il transfère son acide aminé à l’extrémité d’une chaîne polypeptidique en croissance.
Le décodage des codons d'ARNm par des ARN de transfert (ARNt) dans le ribosome implique l'appariement de bases Watson-Crick.
Les taux d'erreur généraux de la réplication génomique (environ 10-8) sont estimés à environ 10 000 fois inférieurs à ceux de la synthèse des protéines (environ 10-4), et par conséquent, dans la plupart des cas, la traduction de l'ARNm est le processus clé conduisant à l'inexactitude des données. protéome cellulaire. L'écart entre les taux d'erreur dans la réplication de l'ADN et dans la traduction de l'ARNm peut être dû en partie au fait que la réplication de l'ADN se produit au niveau de nucléotides uniques (avec 41 = 4 permutations possibles), tandis que la machinerie de traduction interprète les codons de l'ARNm en triplets (avec 43 = 64 permutations possibles).(1)
L’efficacité de la machinerie de décodage de l’ARNm est également essentiellement régulée par le biais d’utilisation des codons, caractérisé par des codons synonymes sur ou sous-représentés. En conséquence, l’optimisation de l’oscillation de l’ARNt et de l’utilisation des codons dans l’ARNm peut améliorer considérablement l’efficacité et la précision de la traduction.(1)
La traduction pré ou post-ARNm peut indirectement introduire des erreurs dans la synthèse des protéines lors de la transcription et du traitement post-traductionnel. Cependant, la machinerie de traduction peut directement contribuer à une mauvaise traduction par un mauvais décodage de l'ARNt (conduisant à une mauvaise incorporation ou à l'arrêt de la lecture des codons), une mésacylation de l'ARNt (conduisant à un couplage incorrect de l'ARNt-acide aminé), une réaffectation des codons ou provoquée par des changements de cadre de translocation ribosomique.(1)
Méthode d'examen
Analyse de séquence génétique
Le vaccin est constitué de 4284 nucléotides répartis en 6 sections : cap est le début de la séquence qui commence par les deux nucléotides GA, ce qui indique à tort que l'ARNm provient de la cellule humaine et est donc accepté ; 5′ indique la direction à suivre pour la traduction, tandis que UTR indique la zone où le ribosome doit reposer pour fabriquer des protéines. Dans cette section, l'U de l'uracile a été remplacé par une molécule 1-méthyl-3′-pseudouridine, marquée du signe Ψ, pour contourner le système immunitaire et empêcher la dégradation de l'ARNm qui vient d'être envahi ; Cependant, c’est un facteur qui peut conduire à des erreurs dans la production de protéines. Plusieurs Ψ-synthases sont impliquées dans la modification de positions spécifiques, et des défauts dans plusieurs d'entre elles ont été liés à des maladies humaines (2).
Ensuite, il y a la section sig, appelée séquence de démarrage étendue du peptide signal de la glycoprotéine S, dont les informations sont nécessaires pour diriger la protéine nouvellement formée hors de la cellule via le réticulum endoplasmique ; ici aussi, des modifications sont apportées aux triplets de nucléotides pour que l'ARN soit accepté par le système immunitaire, certaines lettres qui forment l'information, avec d'autres (généralement en troisième place, "se tortiller"), apparemment des "synonymes inoffensifs" (principalement par augmentant le nombre de lettres C et G, qui codent la vitesse de synthèse des protéines). Bien qu’ils spécifient des acides aminés identiques, les deux synonymes ne sont pas exactement les mêmes, du moins en ce qui concerne la traduction. Des études mécanistiques montrent qu'il existe des différences subtiles mais significatives dans la façon dont chacun interagit avec son ARN de transfert (ARNt) correspondant, différences qui affectent à la fois la vitesse et la précision de la traduction.3 S'il est vrai que 3 lettres d'un codon et plus d'un codon codent le même acide aminé, il est également vrai qu’une augmentation disproportionnée du taux de production de protéines pourrait présenter un risque de graves erreurs de traduction.
De plus, les caractères qui composent la séquence liée à la construction de la véritable protéine de pointe S protein_mut ont été modifiés avec plus de C et de G qui pourraient être ajoutés, en respectant les synonymes du tableau standard du code génétique, avec substitution des acides aminés Lysine ( AAA) et valine (GUU) avec proline (CUU) pour empêcher la protéine modifiée de s'effondrer. A la fin de cette séquence il y a 2 codons stop. Il n’est pas entièrement prouvé qu’avec ce remplacement, les mêmes éléments se forment et qu’aucune interprétation erronée ne se produise.
3′-UTR (Untranslated Region 3 First) : Elle était censée indiquer le sens de traduction de la séquence et améliorer la synthèse protéique, cependant nombre de ses fonctions restent inconnues ; Il est donc impossible de vérifier sa sécurité. Ce que l’on sait, c’est ce qu’affirme l’OMS et la phrase suivante : la 3′ UTR du vaccin BioNTech/Pfizer a été extraite de « l’ARNm amino-terminal activateur de division (AES) et de l’ARN ribosomal 12S codé par les mitochondries ».
poly(A) : Nous atteignons alors la fin de la séquence et rencontrons 30 A, puis une liaison GCAUAUGACU de 10 nucléotides, suivie de 70 autres A, car chaque ARNm peut être réutilisé plusieurs fois par l'organisme.
Lorsque le A est épuisé, l’ARNm est dégradé.
Toutes ces modifications sont exclusives pour augmenter l’expression des protéines, dont on ne sait rien de la traduction réelle effectuée par l’organisme.
Anomalies et autres erreurs dans l'épissage alternatif
Un autre problème connexe est qu’un même pré-ARNm peut donner naissance à différents ARNm matures et donc à des protéines légèrement différentes (anomalies d’épissage alternatives). Il a été démontré qu’un changement dans le processus de synthèse des protéines est à l’origine du développement et de la croissance de certains cancers et d’autres maladies, sans aucune modification de l’ADN.
Tous les événements d'épissage identifiés dans les trois gènes de la série PHT impliquent la perte du cadre de lecture de la séquence messagère et l'introduction d'un codon de terminaison prématurée (PTC), qui se trouve toujours à plus de 50-55 nucléotides en amont du dernier exon- exon Connection est la transcription alternative du système de surveillance NMD (nonsense-mediated mRNA decay). Pour le slc15a4/PHT1 humain et de rat, cela a été démontré par des expériences d'inhibition du NMD dans diverses lignées cellulaires, dans lesquelles l'expression de variantes alternatives aux transcrits canoniques était toujours stabilisée après l'inhibition.(4)
Conclusions
Risques possibles à long terme pour la santé humaine
On peut dire que la séquence, en plus d'être non optimisée, soulève de forts doutes sur la présence d'erreurs d'usage des codons. Il est possible de supposer qu’une modification excessive visant à une augmentation extrême de l’expression des protéines pourrait être la source d’erreurs dans l’assemblage des séquences génétiques de l’ARNm.
L'altération de la disponibilité des ARNt peut conduire à des maladies neurodégénératives (Ishimura et al., 2014), et la régulation positive d'ARNt spécifiques favorise les métastases en augmentant la stabilité des transcrits enrichis dans leurs codons apparentés.(5)
Les erreurs de traduction ont des conséquences très graves sur la physiopathologie de diverses maladies, notamment la sclérose en plaques, la neurodégénérescence, la myopathie mitochondriale, l'encéphalopathie, l'acidose lactique, les épisodes de type accident vasculaire cérébral, la maladie de Parkinson et le cancer (genèse, accélération de la croissance et métastases).(6 )
Dans ce cas, la corrélation entre l’augmentation du taux de synthèse protéique de 100 % et les erreurs de traduction de la séquence, ainsi que le mécanisme qui influence la production d’acides aminés, reste obscure car de nombreuses expériences n’ont pas encore été réalisées.
Fondamentalement, on peut dire que le code de la séquence globale est intrinsèquement déséquilibré, trop comparé à son homologue viral naturel, et trop difficile à dire que l'organisme humain reproduit exactement les protéines de pointe S, comme une image exactement identique, ce qui pose un risque de dommages graves à long terme pour la santé humaine, en plus d'une vaccination inadéquate.
Ce qui est produit à partir de cette séquence est loin d'être défini avec précision, mais il est écrit dans les gènes de chaque individu, à travers le profil ribosomal, comment cela se traduit et ce qui est produit, c'est-à-dire le bénéfice ou le préjudice qui en résulte.
Références
1. Ou X, Cao J, Cheng A, Peppelenbosch MP, Pan Q (2019) Erreurs de décodage traductionnel : oscillation de l'ARNt ou mauvaise incorporation ? PLoS Genet 15(3):e1008017. https://doi.org/10.1371/journal.pgen.1008017
2. Biomolécules 2020, 10(5),729 ; https://doi.org/10.3390/biom10050729
3. Robinson R (2014) Quel synonyme de codon est le meilleur ? Cela peut dépendre de ce qu'il y a au menu. PLoS Biol 12(12):e1002014. est ce que je:10.1371/journal.pbio.1002014
4. Andries, O. (2015). Stratégies de modification et de délivrance de l'ARNm pour établir une plate-forme pour une thérapie génique sûre et efficace. Université de Gand. Faculté de Médecine Vétérinaire, Merelbeke, Belgique.
5. eLife 2019 ;8 :e45396 DOI : 10.7554/eLife.45396
6. Mafalda Santos, Patricia M. Pereira, A. Sofia Varanda, Joana Carvalho, Mafalda Azevedo, Denisa D. Mateus, Nuno Mendes, Patricia Oliveira, Fábio Trindade, Marta Teixeira Pinto, Renata Bordeira-Carriço, Fátima Carneiro, Carl Rui Vitira .ino, Olive et Manuel AS Santos (2018) Les ARNt à lecture erronée des codons favorisent la croissance tumorale chez la souris, RNA Biology, 15:6, 773-786, DOI : 10.1080/15476286.2018.1454244.
Des études confirment la reprogrammation du système immunitaire grâce aux vaccins à ARNm et à vecteurs
Stephanie Seneff du Massachusetts Institute of Technology et Greg Nigh de Naturopathic Oncology à Portland, une équipe de recherche du Helmholtz Center for Infection Research, de la Hannover Medical School, de l'Université de Bonn ainsi que des médecins et chercheurs du centre médical Erasmus de Rotterdam parvenir à des résultats cohérents
La teneur des études est la réduction du système immunitaire humain induite par les substances à ARNm par rapport aux récepteurs dits de type outil. Ceux-ci sont responsables de la reconnaissance des structures des agents pathogènes bactériens et viraux.
L'étude par Stéphanie Seneff ea et des Les équipes de recherche de l'Institut Helmholtz sont disponibles en téléchargement ici.
Ça aussi Î.-P.-É. (Institut Paul Ehrlich) signale déjà les anticorps qui augmentent la charge virale dès le 30 juillet 2020 (!) (site internet comme Téléchargement PDF):
« Les anticorps renforçant l’infection ne déclenchent pas l’élimination ou la neutralisation du virus, mais permettent plutôt au virus de se lier aux récepteurs dits Fcγ, qui se trouvent, entre autres, sur des cellules immunitaires spécialisées (appelées phagocytes). Cela permet au virus d’être absorbé dans ces cellules, où les virus peuvent ensuite se multiplier. Ce processus peut entraîner une augmentation de la charge virale.
Le risque accru de thrombose provoqué par l’ARNm et les substances vecteurs ne fait qu’empirer les choses. Le test des D-dimères peut être utilisé pour estimer et détecter au microscope la probabilité d’un risque accru de thrombose.
La valeur de référence pour les adultes est <0,5 mg/l. Les valeurs comprises entre 0,5 et 3,0 mg/l sont définies comme légèrement élevées, les valeurs > 4,0 mg/l comme fortement élevées.
Étudier AVEC
– Résumé (traduction DE)
« L’opération Warp Speed a lancé deux vaccins à ARNm aux États-Unis, ceux de Pfizer et Moderna. Les données préliminaires suggèrent une efficacité élevée pour ces deux vaccins, ce qui a contribué à légitimer l'autorisation d'utilisation d'urgence (EUA) de la FDA.
EUA (Emergency Use Authorization) par la FDA. Cependant, le développement exceptionnellement rapide de ces vaccins grâce à des essais contrôlés et leur utilisation massive soulève de nombreuses inquiétudes en matière de sécurité. Dans cette revue, nous décrivons d’abord en détail la technologie sous-jacente à ces vaccins. Par la suite, tant les composants de ces vaccins que la réponse biologique prévue à ces vaccins, y compris la production de la protéine de pointe elle-même, et leur relation potentielle avec un large éventail de pathologies aiguës et à long terme, telles que les troubles sanguins, les maladies neurodégénératives et maladies auto-immunes. Dans le contexte de ces pathologies potentiellement induites, nous discutons de l’importance des séquences d’acides aminés au sein de la protéine Spike qui sont liées à la protéine prion. Nous fournissons également un bref aperçu de
Des études montrant le potentiel de « excrétion) de protéines de pointe, le transfert de la protéine d'une personne vaccinée à un
personne non vaccinée, ce qui provoque des symptômes chez cette dernière. Enfin, nous aborderons un point fréquemment évoqué, à savoir la question de savoir si ces vaccins pourraient ou non modifier l’ADN des personnes vaccinées. Bien qu’aucune étude ne le prouve définitivement, nous présentons un scénario plausible, étayé par des voies de transformation et de transport du matériel génétique déjà établies, selon lequel l’ARNm injecté pourrait finalement être incorporé dans l’ADN de la cellule germinale, pour être transmis d’une génération à l’autre. Nous concluons par nos recommandations de surveillance visant à clarifier les effets à long terme de ces médicaments expérimentaux et à mieux évaluer le véritable rapport risque-bénéfice de ces nouvelles technologies.„
…
– Conclusion (traduction DE)
„Les vaccins expérimentaux à ARNm présentent de grands avantages, mais ils présentent également un risque de conséquences imprévues tragiques, voire catastrophiques. Les vaccins à ARNm contre le SRAS-CoV-2 ont été introduits en grande pompe, mais de nombreux aspects de leur utilisation généralisée suscitent des inquiétudes. Nous avons abordé ici certaines de ces préoccupations, mais pas toutes, et souhaitons souligner que ces préoccupations sont potentiellement graves et pourraient ne pas se manifester avant des années, voire des générations. Pour éliminer les risques indésirables décrits dans ce document, nous recommandons au moins de respecter les résultats de recherche et les recommandations de surveillance suivantes :
- Une enquête nationale sur les données détaillées sur les événements indésirables associés aux vaccins à ARNm, avec un soutien financier important et bien au-delà des premières semaines après la vaccination.
- Tests répétés d’auto-anticorps dans la population vaccinée. Les autoanticorps testés
pourrait être standardisé et devrait être basé sur des anticorps et des auto-anticorps précédemment documentés qui peuvent être déclenchés par la protéine de pointe. Ceux-ci comprennent des autoanticorps contre les phospholipides, le collagène, l'actine, la thyroperoxydase (TPO), la protéine basique de la myéline, la transglutaminase tissulaire, la transglutaminase et éventuellement d'autres. - Profilage immunologique lié à l'équilibre des cytokines et aux effets biologiques associés. Les tests doivent inclure au moins l'IL-6, l'INF-α, les D-dimères, le fibrinogène et la protéine C-réactive.
- Des études comparant les populations vaccinées avec les vaccins à ARNm et celles non vaccinées pour confirmer le taux d'infection plus faible attendu et les symptômes plus légers du groupe vacciné, tout en comparant les taux de maladies auto-immunes enregistrées.
- Des études visant à évaluer s’il est possible pour une personne non vaccinée d’acquérir des formes spécifiques au vaccin des protéines de pointe auprès d’une personne vaccinée à proximité.
- Études in vitro visant à déterminer si les nanoparticules d'ARNm peuvent être absorbées par les spermatozoïdes et converties en plasmides d'ADNc.„
Étude Institut Helmholtz
– Résumé (traduction DE)
„Le vaccin BNT162b2 à base d'ARNm de Pfizer/BioNTech a été le premier enregistré contre le COVID-19 et s'est révélé efficace pour prévenir les infections par le SRAS-CoV-2 jusqu'à 95 %.
On sait peu de choses sur les effets généraux de la nouvelle classe de vaccins à ARNm, notamment s’ils ont des effets combinés sur les réponses immunitaires innées et adaptatives. Ici, nous avons confirmé que la vaccination BNT162b2 d’individus en bonne santé suscite une immunité humorale et cellulaire efficace contre plusieurs variantes du SRAS-CoV-2. Il est toutefois intéressant de noter que le vaccin BNT162b2 a également modulé la production de cytokines inflammatoires par les cellules immunitaires innées après la production de cytokines inflammatoires par les cellules immunitaires innées, à la fois lorsqu'il est stimulé par des agents spécifiques (SARS-CoV-2) et non spécifiques (viraux, fongiques et bactériens).
La réponse des cellules immunitaires innées aux ligands TLR4 et TLR7/8 était plus faible après la vaccination BNT162b2, tandis que les réponses cytokines induites par les champignons étaient plus fortes. En conclusion, le vaccin à ARNm BNT162b2 entraîne une reprogrammation fonctionnelle complexe des réponses immunitaires innées, qui devrait être prise en compte dans le développement et l’utilisation de cette nouvelle classe de vaccins.
…
En conclusion, nos données montrent que le vaccin BNT162b2 a des effets sur les branches adaptatives et innées de l’immunité et que ces effets sont différents selon les différentes souches du SRAS-CoV-2.
Il est intéressant de noter que le vaccin BNT162b2 provoque également une reprogrammation de la réponse immunitaire innée. Considération : En combinaison avec de fortes réponses immunitaires adaptatives, cela pourrait contribuer à une réponse inflammatoire plus équilibrée lors de l’infection au COVID-19, ou cela pourrait contribuer à une réponse immunitaire innée réduite au virus. Le vaccin BNT162b2 protège clairement contre la COVID-19, mais la durée de cette protection n’est pas encore connue, et il serait concevable que ces connaissances puissent être intégrées aux générations futures du vaccin pour améliorer la portée et la durée de la protection. Nos résultats doivent être confirmés en menant des études de cohorte plus larges auprès de populations d'origines diverses, tandis que d'autres études étudient les interactions potentielles entre le BNT162b2 et d'autres vaccins.„
Lettres de la main rouge
Les sociétés pharmaceutiques émettent des lettres rouges lorsque, entre autres, des risques médicamenteux jusqu'alors inconnus apparaissent ou que des lots de médicaments sont rappelés pour des raisons de sécurité.
Cela s’est également produit pour tous les produits pharmaceutiques (vaccins) contre le COVID-19 :
BionTech/Pfizer
Janssen
- 26.04.2021 – https://csiag.de/wp-content/uploads/2021/09/Rote-Hand-Janssen-26.042021.pdf
- 19.07.2021 – https://csiag.de/wp-content/uploads/2021/09/Rote-Hand-Janssen-19.07.2021.pdf
Astra Zeneca
- 24.03.2021 – https://csiag.de/wp-content/uploads/2021/09/Rote-Hand-AstraZeneca-24.03.2021.pdf
- 02.06.2021 – https://csiag.de/wp-content/uploads/2021/09/Rote-Hand-AstraZeneca-02.06.2021.pdf
- 23.06.2021 – https://csiag.de/wp-content/uploads/2021/09/Rote-Hand-AstraZeneca-23.06.2021.pdf
Informations médicales/dépliants pour les vaccins COVID
Chaque lot d'une boîte de vaccins est accompagné d'une notice d'information et d'informations médicales. Ces informations doivent servir de base à l'information avant de procéder à une vaccination.
Les informations médicales des fabricants sont disponibles ici sous la forme d'un lien EMA et d'un lien de téléchargement PDF. Les brochures d'information ne sont actuellement pas disponibles en ligne ou ne sont plus disponibles.
- Comirnaty – BioNTech
- Dépliant d'information (PDF)
- Informations médicales (Annexe I – EMA) – Informations pour les utilisateurs – (PDF)
- Johnson & Johnson / Janssen
- Dépliant d'information (PDF)
- Informations médicales (Annexe I – EMA) – (PDF)
- Spikevax – Moderna
- Dépliant d'information (PDF)
- Informations médicales (Annexe I – EMA) – (PDF)
- Vaxzevria-AstraZeneca
- Dépliant d'information (PDF)
- Informations médicales (Annexe I – EMA) – Informations médicales (Fabricant) - (PDF)
Dans les informations fournies ci-dessus par le fabricant, l’objectif du vaccin est principalement défini comme « prévenir les maladies liées au COVID ». Une protection complète contre une future infection par le COVID n’est pas garantie.
AstraZeneca pointe également le thème des « croyances religieuses » :
« Chacun doit décider lui-même si son traitement est compatible avec ses propres convictions religieuses. »
Résultats de l'autopsie d'une personne décédée peu de temps après la vaccination BioNTech
Sous le titre Premier cas d’étude post mortem chez un patient vacciné contre le SRAS-CoV-2 le 16 avril 2021, c'est le résultat d'une étude réalisée en coopération avec l'Institut de pathologie, Hôpital universitaire OWL de l'Université de Bielefeld, Campus Lippe, Röntgenstr. 18, D-32756 Detmold et l'Institut de pathologie, KRH Hospital Nordstadt, Hanovre, Allemagne ont publié l'autopsie ici est disponible au format PDF dans l'original.
Le texte intégral suit en traduction allemande :
Résumé
Un homme de 86 ans, auparavant asymptomatique, a reçu la première dose du vaccin à ARNm BNT162b2 contre la COVID-19. Il est décédé 4 semaines plus tard d'une insuffisance rénale et respiratoire aiguë. Bien qu’il ne présentait aucun symptôme spécifique au COVID-19, il a été testé positif au SRAS-CoV-2 avant son décès. La liaison à l’antigène de la protéine Spike (S1) a montré des niveaux significatifs d’immunoglobuline (Ig) G, tandis que les IgG/IgM de la nucléocapside n’ont pas été déclenchées. La bronchopneumonie aiguë et l'insuffisance tubulaire ont été désignées comme causes du décès à l'autopsie ; Cependant, nous n’avons observé aucune caractéristique morphologique distinctive du COVID-19. La cartographie moléculaire post-mortem utilisant la réaction en chaîne par polymérase en temps réel a révélé des seuils pertinents du cycle du SRAS-CoV-2 dans tous les organes examinés (oropharynx, muqueuse olfactive, trachée, poumons, cœur, rein et cerveau), à l'exception du foie et du bulbe olfactif. Ces résultats peuvent suggérer que la première vaccination induit une immunogénicité mais pas une immunité stérile.
Nous rendons compte du cas d'un homme de 86 ans, résident d'une maison de retraite, vacciné contre le SRAS-CoV-2. Les antécédents médicaux comprenaient une hypertension artérielle systémique, une insuffisance veineuse chronique, une démence et un cancer de la prostate. Le 9 janvier 2021, l’homme a reçu le vaccin à ARN modifié par des nucléosides, formulé à partir de nanoparticules lipidiques, BNT162b2, à une dose de 30 μg. Il n'a présenté aucun symptôme clinique ce jour-là et dans les 2 semaines suivantes (Tableau 1). Le 18ème jour, il a été hospitalisé pour une diarrhée qui s'était aggravée. Comme il ne présentait aucun signe clinique de la COVID-19, il n’a pas été isolé dans un cadre précis. Les tests de laboratoire ont révélé une anémie hypochrome et des taux de créatinine sérique élevés. Le test antigénique et la réaction en chaîne par polymérase (PCR) pour le SRAS-CoV-2 se sont révélés négatifs.


Une gastroscopie et une coloscopie ont été réalisées pour étudier plus en détail la cause de la diarrhée. En particulier, la coloscopie a révélé une lésion ulcéreuse de l'angle colique gauche, diagnostiquée histologiquement comme une colite ischémique. L’analyse PCR sur des échantillons de biopsie utilisant une méthode précédemment rapportée (Kaltschmidt et al., 2021) s’est révélée négative pour le SRAS-CoV-2. Le traitement était de soutien avec de la mésalazine et un remplacement du fer par voie intraveineuse. Par la suite, l'état du patient s'est détérioré avec le développement d'une insuffisance rénale. Au jour 24, un patient a été testé positif au SRAS-CoV-2 dans la même chambre d'hôpital que notre cas. Au jour 25, notre patient a été testé positif au SARS-CoV-2 par PCR en temps réel (RT-PCR), avec un seuil de cycle (Ct) bas indiquant une charge virale élevée. Après une analyse plus approfondie de l’échantillon sur écouvillon, il n’y avait aucune preuve des variantes mutées du SRAS-CoV-2 B.1.1.7, B.1.351 ou B.1.1.28.1. Dans l’ensemble, il semble que le patient ait été infecté par le patient dans sa chambre d’hôpital. Notre patient présentait maintenant de la fièvre et des difficultés respiratoires, et l'auscultation pulmonaire montrait des crépitements. Malgré le début d’un supplément d’oxygène (2 L par minute) et d’un traitement antibiotique par ceftriaxone, le patient est décédé le lendemain d’une insuffisance rénale et respiratoire aiguë.
L'évaluation de l'immunogénicité en mesurant la mungglobuline (Ig) G liant l'antigène à la protéine Spike (S1) dans des échantillons de sérum obtenus au jour 25 a montré une réponse en anticorps (8,7 U/ml, valeur de référence 1,0 U/ml ; Roche ECLIA™). Ces résultats indiquent que le patient avait déjà développé une immunogénicité pertinente grâce à la vaccination.
Les études post-mortem ont montré une bronchopneumonie bilatérale aiguë avec des abcès parfois entourés de coques bactériennes (Figure 1). Aucune manifestation fréquemment rapportée de pneumopathie associée au COVID-19 n’a été observée. Au niveau du cœur, nous avons retrouvé une hypertrophie biventriculaire (poids 580 g) et une cardiomyopathie ischémique diagnostiquée histologiquement. Nous avons détecté une amylose de type transthyrétine dans le cœur et, dans une moindre mesure, dans les poumons. Les reins présentaient à la fois des lésions chroniques avec artériolosclérose et fibrose interstitielle et une insuffisance rénale aiguë avec dégénérescence des tubules hydropiques. L'examen cérébral a révélé une nécrose du tissu pseudokystique pariétal gauche, qui a été diagnostiquée comme une zone d'infarctus ancienne.

Le chiffre ci-dessus est ici Disponible en téléchargement en haute résolution au format PDF.
Nous avons effectué une cartographie moléculaire de 9 parties anatomiques différentes de tissus fixés au formol et inclus en paraffine, comme décrit précédemment (Kaltschmidt et al., 2021). L'ARN a été extrait de coupes de paraffine à l'aide du Maxwell RSC (Promega, Madison, WI, USA). L'analyse RT-PCR multiplex a ciblé 2 gènes indépendants du génome du SRAS-CoV-2 (kit fluorotype SARS-CoV-2 plus ; HAIN/Bruker, Nehren, Allemagne) : ARN polymérase dépendante de l'ARN (cible 1) et nucléopeptide (cible 2). La valeur seuil négative était Ct >45. Nous avons examiné 9 échantillons de tissus différents pour rechercher des voies connues et pertinentes de propagation virale dans le corps humain (Figure 1). Pour éviter toute contamination croisée, chaque échantillon a été intégré directement dans des cassettes de tissus distinctes et fixé séparément dans du formol tamponné au phosphate 4%. Nous avons mis en évidence l'ARN viral dans presque tous les organes examinés, à l'exception du foie et du bulbe olfactif (Figure 1).
À la connaissance des auteurs, une étude d’autopsie détaillée comprenant une cartographie virale moléculaire d’un patient vacciné contre le SRAS-CoV-2 avec un test SARS-CoV-2 positif après la vaccination n’a pas été rapportée auparavant. Nous proposons qu’un seul traitement avec le vaccin à ARN BNT162b2b2 ait induit une immunogénicité significative, comme en témoignent les taux sériques d’IgG neutralisants basés sur la protéine de pointe signalés. Depuis les semaines précédant la vaccination, en passant par la vaccination (jour 1), jusqu’à peu avant le décès (jour 24), le patient était exempt de symptômes cliniques généralement attribués au COVID-19. De plus, les analyses de sang n’ont pas montré le titre d’IgM, qui est généralement observé 7 à 14 jours après l’apparition des symptômes (Kim et al., 2020). Cependant, le patient a été testé positif au SRAS-CoV-2. La valeur ct mesurée sur des écouvillons nasopharyngés et celle mesurée sur des échantillons d'autopsie fixés au formol et inclus en paraffine indiquent une charge virale et suggèrent une transmissibilité. Étant donné que notre patient est décédé environ 2 jours après son premier résultat positif au test SARS-CoV-2, nous supposons que les données de cartographie moléculaire reflètent un stade précoce de l’infection virale. Un stade précoce de l’infection pourrait également expliquer pourquoi diverses régions telles que le bulbe olfactif et le foie n’ont pas (encore) été touchées par la propagation systémique du virus.
Nous n’avons pas encore observé de caractéristiques morphologiques distinctives du COVID-19 qui ont été rapportées dans des études d’autopsie morphologique à grande échelle (Schaller et al., 2020, Edler et al., 2020, Ackermann et al., 2020). Nous n'avons pas trouvé de signes typiques de lésions alvéolaires diffuses dans les poumons, mais nous avons identifié une bronchopneumonie aiguë étendue, éventuellement d'origine bactérienne. Nous avons conclu que le patient était décédé des suites d'une bronchopneumonie et d'une insuffisance rénale aiguë.
Nos résultats concordent avec les découvertes précédentes de modèles animaux selon lesquelles l'immunisation contre le SRAS-CoV-2 par vaccination semblait réduire la gravité de la pathogenèse, en particulier en ce qui concerne les maladies pulmonaires graves, tandis que l'ARN viral persistait dans les prélèvements nasaux (Van Doremalen et al., 2020 , Vogel et al., 2021). Récemment, Amit et al. (2021) Résultats d'un essai clinique mené auprès des professionnels de la santé utilisant le vaccin BNT162b2, qui a montré des réductions précoces significatives de l'infection par le SRAS-CoV-2 et des taux de COVID-19 symptomatiques après l'administration de la première dose de vaccin.
Parmi les principaux effets indésirables observés chez les patients vaccinés contre le SRAS-CoV-2, les effets locaux prédominent et les réactions systémiques graves sont rarement décrites (Yuan et al., 2020). Cependant, des rapports récents faisant état d’un risque accru de caillots sanguins, en particulier de thrombose du sinus veineux cérébral dans le cas du vaccin Oxford-AstraZeneca (Mahase 2021), ont soulevé un débat sur la sécurité du vaccin contre la COVID-19 en général. Une analyse complète des données d'autopsie doit être menée pour fournir des informations plus détaillées sur les effets secondaires mortels et les décès associés aux vaccinations.
En conclusion, les résultats de notre étude de cas d’autopsie chez un patient vacciné à ARNm confirment l’idée selon laquelle l’immunogénicité peut déjà être induite par la première vaccination contre le SRAS-CoV-2, alors que l’immunité stérile n’est pas suffisamment développée.
Remerciements
Nous tenons à vous remercier pour le soutien technique expert fourni par Ralf Bode et Nadine Weber (Hôpital universitaire OWL de l'Université de Bielefeld, Lippe Campus, Detmold).
Références
- Ackermann M., Verleden SE, Kuehnel M., Haverich A., Welte T., Laenger F. Endothélialite vasculaire pulmonaire, thrombose et angiogenèse dans Covid-19. N Engl J Med. 2020 ; 383 : 120-128. est ce que je: 10.1056/NEJMoa2015432. [Articles gratuits sur PMC] [PubMed] [RéfCross] [Google Scholar]
- Amit S., Regev-Yochay G., Afek A., Kreiss Y., Leshem E. Réductions précoces des taux d'infection par le SRAS-CoV2 et le COVID-19 chez les receveurs du vaccin BNT162b2. Lancette. 2021;397(10277):875-877. est ce que je: 10.1016/S0140-6736(21)00448-7. [Articles gratuits sur PMC] [PubMed] [RéfCross] [Google Scholar]
- Edler C., Schröder AS, Aepfelbacher M., Fitzek A., Heinemann A., Heinrich F. Dying with SARS-CoV2 infection – une étude d'autopsie des 80 premiers cas consécutifs à Hambourg, en Allemagne. Int J Legal Med. 2020 ; 134 : 1275-1284. est ce que je: 10.1007/s00414-020-02336-7. [Articles gratuits sur PMC] [PubMed] [RéfCross] [Google Scholar]
- Kaltschmidt B., Fitzek ADE, Schaedler J., Förster C., Kaltschmidt C., Hansen T. Vasculopathie hépatique et réponses régénératives du foie dans les cas mortels de COVID-19. Clin Gastroenterol Hépatol. 2021 est ce que je : 10.1016/j.cgh.2021.01.044. Sous presse. [Articles gratuits sur PMC] [PubMed] [RéfCross] [Google Scholar]
- Kim DS, Rowland-Jones S, Gea-Mallorqui E. L’infection par le SRAS-CoV-2 suscitera-t-elle une immunité protectrice ou stérilisante durable ? Implications pour les stratégies vaccinales. Immunol avant. 2020;11:571481. est ce que je: 10.3389/fimmu.2020.571481.eCollection2020. [Articles gratuits sur PMC] [PubMed] [RéfCross] [Google Scholar]
- Mahase E. Covid-19 : Le vaccin AstraZeneca n’est pas lié à un risque accru de caillots sanguins, selon l’Agence européenne des médicaments. BMJ. 2021 ;372 : n774. est ce que je: 10.1136/bmj.n774. [PubMed] [RéfCross] [Google Scholar]
- Schaller T., Hirschbühl K., Burkhardt K., Braun G., Trepel M., Märkl B. Examens post-mortem de patients atteints de COVID19. JAMA. 2020 ; 323 : 2518-2520. est ce que je: 10.1001/jama.2020.8907. [Articles gratuits sur PMC] [PubMed] [RéfCross] [Google Scholar]
- Van Doremalen N, Lambe T, Spencer A, Belij-Rammersdorfer S, Purushotham JN, Port JR Le vaccin ChAdOx1 nCoV-19 prévient la pneumonie par le SRAS-CoV-2 chez les macaques rhésus. Nature. 2020 ; 586 : 578-582. est ce que je: 10.1101/2020.05.13.093195. [PubMed] [RéfCross] [Google Scholar]
- Vogel AB, Kanevsky I, Che Y, Swanson KA, Muik A, Vormehr M. Les vaccins immunogènes BNT162b protègent les macaques rhésus du SRAS-CoV-2. Nature. 2021;592(7853):283-289. est ce que je: 10.1101/2020.12.11.421008. [PubMed] [RéfCross] [Google Scholar]
- Yuan P., Ai P., Liu Y., Ai Z., Wang Y., Cao W. Sécurité, tolérabilité et immunogénicité des vaccins COVID19 : une revue systématique et une méta-analyse. medRxiv. 2020 est ce que je: 10.1101/2020.11.03.20224998. Préimpression. [RéfCross] [Google Scholar]
Résultats de recherche sur l'extrait de pissenlit – inhibe la liaison des protéines de pointe
Extrait/traduction du texte de l’article «RECHERCHE : L'extrait de feuille de pissenlit empêche les protéines de pointe de se lier au récepteur de surface cellulaire ACE2„:
Les protéines de pointe du SRAS-CoV-2 peuvent être neutralisées par une « mauvaise herbe » commune qui est bannie des pelouses chaque année. Un allemand Études universitaires a révélé que le pissenlit (Taraxacum officinale) peut bloquer la liaison des protéines de pointe aux récepteurs de surface cellulaire ACE2 dans les cellules pulmonaires et rénales humaines. L'extrait de pissenlit à base d'eau, dérivé des feuilles séchées de la plante, s'est avéré efficace contre la protéine de pointe D614 et diverses souches mutantes, notamment D614G, N501Y, K417N et E484K.
Voici la traduction allemande de l'étude originale (PDF - Anglais) :
Résumé:
Le 11 mars 2020, la maladie à coronavirus 2019 (COVID-19), causée par le virus SARS-CoV-2, a été déclarée pandémie mondiale par l'Organisation mondiale de la santé (OMS). À ce jour, de nouveaux « variants préoccupants » du SARS-CoV-2, variants britannique (B.1.1.7), sud-africain (B.1.351) ou brésilien (P.1), se propagent rapidement. Tous contiennent de multiples mutations dans le site de reconnaissance du récepteur ACE2 de la protéine Spike, par rapport à la séquence originale de Wuhan, ce qui est d'une grande importance en raison de son potentiel de défense immunitaire. Ici, nous rapportons l’efficacité du pissenlit (Taraxacum officinale) pour bloquer l’interaction protéine-protéine de Spike S1 avec le récepteur de surface cellulaire ACE2 humain. Cela pourrait être démontré pour le pic original D614, mais également pour ses formes mutées (D614G, N501Y et mélange de K417N, E484K, N501Y) dans les cellules pulmonaires HEK293-hACE2-rein et A549-hACE2-TMPRSS2 humaines. Les composés de haut poids moléculaire contenus dans l’extrait à base d’eau sont responsables de cet effet. L’infection des cellules pulmonaires par des particules de lentivirus pseudotypées à pointe SARS-CoV-2 a été efficacement empêchée par l’extrait, tout comme la sécrétion proinflammatoire d’interleukine-6 déclenchée par le virus. Les monographies modernes à base de plantes considèrent que l'utilisation de cette plante médicinale est sûre. Par conséquent, les résultats in vitro rapportés ici devraient stimuler des recherches plus approfondies sur la pertinence clinique et l’applicabilité de l’extrait en tant que stratégie de prévention de l’infection par le SRAS-CoV-2.
Le SRAS-CoV-2 mute constamment lors de la transmission entre personnes. Cela pourrait éventuellement conduire le virus à échapper aux approches thérapeutiques et prophylactiques existantes ciblant la protéine de pointe. Nous avons trouvé une inhibition efficace de l'interaction protéine-protéine entre le récepteur d'entrée des cellules virales humaines ACE2 et la protéine de pointe du SRAS-CoV-2, y compris cinq mutations pertinentes, par des extraits à base d'eau de pissenlit commun (Taraxacum officinale). Cela a été démontré in vitro en utilisant des cellules humaines de rein (HEK293) et de poumon (A549) surexprimant respectivement les protéines ACE2 et ACE2/TMPRSS2. L’extrait a efficacement empêché l’infection des cellules pulmonaires par le lentivirus pseudotypé SARS-CoV-2. Les résultats nécessitent une analyse plus approfondie de l’efficacité du pissenlit dans la prévention du SRAS-CoV-2 et des preuves cliniques de confirmation.
À ce jour, il existe trois nouvelles variantes du SRAS-CoV-2 à propagation rapide, signalées pour la première fois au Royaume-Uni (variante B.1.1.7), en Afrique du Sud (variante B.1.351) et au Brésil (variante P.1), toutes parmi eux partagent la mutation N501Y de la protéine Spike (5). Les variantes du SRAS-CoV-2 présentant des mutations de la protéine Spike D614G prédominent désormais dans le monde entier. En plus du D614G, B.1.351 contient des mutations de pointe supplémentaires, dont trois mutations (K417N, E484K et N501Y) dans le RBD (6). Les données préliminaires suggèrent un lien possible entre l'augmentation du taux de mortalité observée avec la mutation D614G et il est suggéré qu'un changement conformationnel de la protéine de pointe entraîne une infectivité accrue (7). Les calculs de perturbations d'énergie libre pour les interactions des mutations N501Y et K417N, à la fois avec le récepteur ACE2 et avec un anticorps dérivé de patients atteints de COVID-19, soulèvent des questions importantes sur l'éventuelle réponse immunitaire humaine et le succès des vaccins déjà disponibles sur (8) . En outre, une résistance accrue des variantes B.1.351 et B.1.1.7 à la neutralisation par anticorps a été signalée ; pour B.1.351, cela était principalement dû à la mutation E484K de la protéine Spike (9).
L'interférence avec le site d'interaction entre la sous-unité Spike S1 et ACE2 peut être une cible importante pour le traitement ou la prévention (10). Ici, les composés d’origine naturelle peuvent apporter une certaine protection contre l’invasion de cellules virales tout en ayant peu ou pas d’effets secondaires. Nous rapportons ici le potentiel inhibiteur du pissenlit sur la liaison de la protéine Spike S1 RBD au récepteur de surface cellulaire hACE2 et comparons l'effet de la protéine Spike originale D614 avec ses mutations D614G, N501Y et Mix (K417N, E484K, N501Y). .
Le pissenlit commun (Taraxacum officinale) appartient à la famille végétale des Asteraceae, sous-famille des Cichorioideae avec de nombreuses variétés et petites espèces. C'est une plante herbacée vivace originaire des zones tempérées plus chaudes de l'hémisphère nord, habitant les champs, les bords de routes et les sites rudéraux. T. officinale est consommée comme aliment végétal, mais est également utilisée en phytothérapie européenne pour les maladies du foie, de la vésicule biliaire, du tube digestif ou les maladies rhumatismales. Les monographies modernes à base de plantes considèrent que l'utilisation de la plante est sûre et ont évalué l'utilisation empirique de T. officinale avec un résultat positif. Les domaines d'application de T. officinale sont répertoriés dans les monographies de la Commission E allemande, de la Coopérative scientifique européenne pour la phytothérapie (ESCOP) (11, 12) et de la British Herbal Medicine Association (13). La plante contient un large éventail de composés phytochimiques, notamment des terpènes (lactones sesquiterpéniques telles que l'acide taraxique et les triterpènes), des composés phénoliques (acides phénoliques, flavonoïdes et coumarines) et des polysaccharides (14). Le composé phénolique prédominant s’est avéré être l’acide chicorique (acide dicaféoyltartrique). Les autres étaient des acides mono- et dicaféoylquiniques, des dérivés de l'acide tartrique, des flavones et des glycosides de flavonol. En plus de ces classes de composés, les racines contiennent de grandes quantités d’inuline (15). Les formes galéniques comprennent les décoctions et infusions aqueuses, les jus de plantes fraîches pompés, les teintures hydroalcooliques et les dragées à base d'extraits secs, qui sont utilisés comme monopréparations (16), mais aussi comme composants intégrantes des médicaments. Nos recherches ont été menées à l’aide d’extraits aqueux de feuilles de plantes. Nous avons constaté que les extraits de feuilles bloquaient efficacement la protéine Spike ou ses formes mutées du récepteur ACE2 utilisées avant ou après l'incubation et que des composés de haut poids moléculaire étaient responsables de cet effet. Une plante de la même souche (Cichorium intybus) pourrait avoir des effets similaires mais avec une puissance moindre. L’extrait a empêché efficacement l’infection des cellules pulmonaires humaines A549-hACE2-TMPRSS2 par le lentivirus pseudotypé SARS-CoV-2.
Résultats
T. officinale inhibe la liaison Spike S1 – ACE2
Nous avons d’abord examiné l’inhibition de l’interaction entre la protéine de pointe du SRAS-CoV-2, RBD, et ACE2, à l’aide d’extraits de feuilles de T. officinale. La figure 1A montre l'inhibition dépendante de la concentration de la liaison du pic S1-ACE2 lors du traitement avec l'extrait de T. officinale (EC50=12 mg/ml). Les extraits de C. intybus ont également montré une inhibition de liaison dépendante de la concentration, mais avec une puissance inférieure à celle de T. officinale (EC50 = 30 mg/ml) (Fig. 1B). Nous avons ensuite préparé deux fractions de feuilles séchées de T. officinale et de chicorée et séparé les extraits en une fraction de poids moléculaire élevé (> 5 kDa) et une fraction de faible poids moléculaire (<5 kDa). Comme le montre la figure 1C, les composés bioactifs étaient principalement présents dans la fraction HMW. Seule une faible activité a été observée dans la fraction LMW.

.
Effet de T. officinale et de la chicorée sur le pic du Sars-CoV-2 – inhibition de l’ACE 2.
AB) Effet dépendant de la concentration de l'extrait de T. officinale (TO) et de C. intybus (CI). CD) Effet des fractions d'extrait de feuilles TO et CI. Les extraits ont été lyophilisés puis un fractionnement par poids moléculaire a été effectué. Le seuil a été fixé à 5 kDa (HMW > 5 kDa, LMW < 5 kDa). H+L : fractions HMW et LMW ; A titre de référence, 50 mg de feuilles séchées par ml d'eau ont été utilisés. Des quantités de fractions HMW et LMW équivalentes aux feuilles séchées ont été utilisées. L'inhibition de liaison a été évaluée à l'aide de la technique ELISA. Les barres sont moyennes + SD. Contrôle du solvant : eau distillée (ad).
En utilisant des cellules HEK293 surexprimant hACE2, le potentiel des extraits de T. officinale et de C. intybus à bloquer la liaison des pointes aux cellules a été étudié plus en détail. Comme le montre la figure 2, la pré-incubation des cellules avec T. officinale pendant une minute. a efficacement bloqué la liaison cellulaire de Spike de 76,67 % ± 2,9 et sa fraction HMW de 62,5 ± 13,4% par rapport au contrôle de l'eau. Après 3 h, l'inhibition était toujours de 50 ± 13,6 % pour l'extrait et de 35,0 ± 20 % pour la fraction HMW de T. officinale. L'extrait de chicorée était moins efficace dans ce système de test ; Une inhibition de liaison a été observée à 37 ± 20 % après 1 minute. et 5,6 ± 9,9 %.

Inhibition de la liaison de la protéine de pointe S1 aux cellules humaines HEK293-hACE2 par préincubation d'extrait.
Les cellules ont été préincubées pendant les temps indiqués avec l'extrait de 10 mg/ml de T. officinale (TO), sa fraction HMW égale à 10 mg/ml d'extrait (HMW), et 10 mg/ml de C. intybus (CI). ou un témoin de solvant (ad), puis traité avec la protéine de pointe S1 marquée HIS pendant 1 heure sans étape de lavage entre les deux à 4°C. L'inhibition de la liaison a été déterminée par cytométrie en flux. N=3, les barres sont les moyennes + SD. En haut à gauche : Cytogramme de cellules HEK-hACE2 fermées. Milieu : Superposition d’histogrammes représentatifs d’intensité de fluorescence pour l’expression de surface ACE2. En haut à droite : superposition d’histogrammes représentatifs de l’intensité de fluorescence pour l’inhibition de la liaison des pointes par les extraits ou l’annonce ; contrôle positif : 20 µg/ml hACE2 soluble. Les cellules ont été colorées avec un anticorps monoclonal conjugué anti-His-tag Alexa Fluor 647.
Le traitement cellulaire avec des quantités égales de pointe D614 et de ses variantes D614G et N501Y a confirmé une affinité de liaison plus forte de D614G (∼1,5 fois) et de N501Y (∼3 à 4 fois) que la protéine de pointe D614 pour le récepteur de surface ACE2 des cellules HEK293 ( Figure 3A). Un prétraitement rapide avec T. officinale (dans les 30 s) a bloqué la liaison de la pointe au récepteur de surface ACE2 (Fig. 3B-C). Après 30 secondes, il s'agissait de 58,2 ± 28,71 TP3T pour D614, de 88,2 ± 4,61 TP3T pour D614G et de 88 ± 1,31 TP3T pour l'inhibition de la liaison N501Y par l'extrait de T. officinale. Bien que l’inhibition de la liaison des pointes ait été observée pour l’extrait de C. intybus, elle était inférieure d’environ 30 à 701 TP3T à celle de T. officinale, en fonction de la protéine de pointe examinée. Lorsque la liaison a été examinée à 37°C plutôt qu'à 4°C, les résultats étaient comparables pour T. officinale mais encore plus faibles pour l'extrait de chicorée dans cette lignée cellulaire (Figure 3D). Pour les extraits de T. officinale et C. Intybus, l'inhibition de la liaison des pointes était de 47,90 ± 14,72 et 13,12 ± 12,37 (D614), 68,42 ± 14,53 et 8,86 ±, respectivement 15,29 (d614g), 71,66 ± 7,66 et 37,56 ± 16.14 (n501y) , respectivement. Nous avons également demandé si les extraits pouvaient remplacer la liaison des pointes au récepteur de surface ACE2 des cellules humaines. Pour ce faire, nous avons d’abord incubé les cellules avec la protéine Spike D614, D614G ou N501Y puis avec les extraits. Comme le montre la figure 3D, T. officinale a pu éliminer efficacement le pic du récepteur (50% en moyenne) ; La chicorée était alors beaucoup plus faible (en moyenne 25 %). Nous avons étendu nos expériences aux cellules humaines A549-hACE2-TMPRSS2 et avons pu confirmer les résultats observés dans les cellules HEK293-hACE2 pour T. officinale (Figure 3D-G). Cette lignée cellulaire a été transfectée de manière stable avec les gènes humains ACE2 et TMPRSS2 et, fait intéressant, ici l’extrait de C. intybus était plus efficace que les cellules HEK-hACE2. Après prétraitement de l'extrait, l'inhibition de la liaison des pointes aux cellules variait de 73,5% ± 5,2 (D614) à 86,3% ± 3,23 (N501Y) pour l'extrait de T. officinale et de 56,1% ± 5,28 (D614) à 63,07% ± 14,55 (N501Y). ) pour l'extrait de C. intybus. Déjà à 0,6 mg/ml, T. officinale bloquait de manière significative la liaison à la protéine de pointe D614G d'environ 40% (IC50 = 1,73 mg/ml). Lorsque les cellules étaient préincubées avec la protéine Spike avant le traitement de l'extrait, les résultats pour D614 et D614G étaient comparables pour l'extrait de T. officinale mais légèrement inférieurs pour N501Y (Fig. 3C – D). Un mélange des mutants Spike N501Y, K417N et E484K a également été testé dans ce contexte et, ici aussi, l'extrait de T. officinale a bloqué la liaison de 82,97 % ± 6,31 (extrait avant incubation) et 79,7 % ± 9,15 (extrait après incubation).

Inhibition de liaison du Spike D614 et de ses mutants D614G, N501Y ou mélange (N501Y, K417N et E484K) aux cellules humaines HEK293-hACE2 et A549-hACE2-TMPRSS2 par extrait avant ou après incubation.
Superposition de l'histogramme d'intensité de fluorescence pour A) les cellules HEK non colorées, le contrôle de coloration (anti-His tag A647) et les cellules incubées avec le Spike D614, D614G ou N501Y marqué par His pendant 1 heure à 4°C. B) Cellules préincubées avec un contrôle solvant (ad), 10 mg/ml de T. officinale (TO) ou 10 mg/ml de C. intybus (CI) pendant 30 à 60 secondes, puis avec du S1 marqué His. Les protéines Spike D614, D614G ou N501Y ont été traitées pendant 1 h sans lavage entre les deux à 4°C. DG) Effet de l'incubation de l'extrait sur les cellules HEK ou A549 avant ou après l'incubation avec le Spike D614, D614G, N501Y marqué His ou une protéine mixte (N501Y, K417N et E484K) à 37 °C. H) Des extraits de plantes ont été incubés dans la salive de 4 donneurs humains pendant 30 min. à 37°C. Les cellules ont ensuite été prétraitées avec des extraits à 5 mg/ml pendant 60 secondes. à 37°C avant incubation avec la protéine Spike D614 marquée His pendant 0,5 h à 37°C. L'inhibition de la liaison des pointes aux cellules humaines a été évaluée à l'aide d'une analyse cytométrique en flux de cellules colorées avec un anticorps monoclonal conjugué anti-His-tag Alexa Fluor 647. Les barres sont moyennes + SD.
Les extraits incubés dans la salive humaine pendant 30 minutes à 37°C avant le traitement cellulaire ont eu des effets comparables sur l'inhibition du pic D614G (Fig. 3H), indiquant une bonne stabilité des composés bioactifs dans la salive.
Pour voir si l'extrait de T. officinale perturbe l'activité catalytique du récepteur ACE2 ou affecte l'expression de la protéine ACE2, nous avons traité les cellules A549-hACE2-TMPRSS2 avec l'extrait pendant 1 à 24 h avant la lyse cellulaire et la détection. Aucune perte de viabilité cellulaire n'a été observée après 84 h d'exposition des cellules à l'extrait (Fig. 4A). Aucune altération de l'activité enzymatique n'a pu être détectée après 1 ou 24 h (4B). Spike a diminué de manière significative la protéine ACE2 après 6 heures (Figure 4C, barres noires), et cela était également vrai pour l'extrait, soit seul (Figure 4C, barres blanches), soit en combinaison avec Spike (barres noires). Cet effet a été éliminé après 24 heures (4D).

Effet de l'extrait de T. officinale sur l'activité enzymatique ACE2 et l'expression des protéines.
A) La viabilité des cellules A549-hACE2-TMPRSS2 a été déterminée par coloration cellulaire au bleu trypan après 84 h d’exposition à l’extrait. B) Les cellules ont été incubées avec un extrait de TO ou 500 ng/ml de protéine S1 et analysées pour déterminer l'activité enzymatique à l'aide d'un kit de fluorescence. CD) Les cellules ont été exposées pendant 6 h ou 24 h pour extraire 500 ng/ml de protéine S1 sans (barres blanches) ou avec (barres noires) et analysées pour l'expression de la protéine ACE2 à l'aide d'un kit ELISA ACE2 humain ; un. d. : Contrôle des solvants. Les barres sont des moyennes + SD, N ≥ 3 expériences indépendantes.
À l’aide d’un lentivirus pseudotype à pointe SARS-CoV-2, nous avons ensuite examiné si l’extrait pouvait bloquer l’entrée du virus grâce à l’inhibition des pointes. Lorsqu'elle est prétraitée avec l'extrait, la transduction du virus a été réduite d'environ 85% à 20 mg/ml (figure 5A). Dans les différentes conditions de traitement, le signal de luminescence généré par la transduction virale a été inhibé par 70 % ± 16,7 (A), 58 % ± 9,6 (B) et 53 % ± 8,1 (C) à 10 mg/mL d’extrait. Cette inhibition de la transduction du virus par l'extrait s'est accompagnée d'une suppression significative de la réponse inflammatoire déclenchée par le virus, déterminée par la sécrétion réduite de la cytokine pro-inflammatoire IL-6 dans les cellules A549-hACE2-TMPRSS2 (Fig. 5D).

Inhibition de la transduction virale des cellules A549-hACE2-TMPRSS2 par l'extrait de T. officinale.
Les cellules ont été transduites avec 2,5 µl de lentivirus pseudotypé Spike SARS-CoV-2 (reporteur Luc) pendant 24 h A) après prétraitement avec un extrait de T. officinale (TO) pendant 0,5 h, B) 3 h avant l'ajout de TO ou C) sans extrait . Le milieu a ensuite été remplacé par du milieu frais et les cellules ont été incubées avec l'extrait pendant 60 h supplémentaires. La luminescence a été détectée après 1 heure. (-) Contrôle négatif : pseudovirion lentiviral chauve ; (+) contrôle positif : lentivirus luciférase de luciole. D) L'analyse de la sécrétion de cytokines proinflammatoires IL-6 a été réalisée soit après 24h de transduction du virus avec l'extrait (à gauche), après 24h + 60h après l'infection avec l'extrait (au milieu) ou après 60h après l'infection avec l'extrait (à droite) par multiplexage. analyse cytométrique en flux. Contrôle du solvant : eau distillée (ad). N ≥ 3 expériences indépendantes.
discussion
Le développement de stratégies efficaces de prévention et de traitement de l’infection par le SRAS-CoV-2 en est encore à ses débuts. Bien que les premiers vaccins aient désormais reçu une autorisation de mise sur le marché, des défis subsistent concernant les problèmes de distribution ou d'efficacité à long terme, ainsi que le risque de réinfection (17, 18). Cependant, les infections ultérieures peuvent être plus bénignes que la première. En plus de la vaccination contre le COVID-19, le blocage de l'accessibilité du virus à l'ACE2 lié à la membrane en tant que récepteur principal pour l'entrée dans la cellule cible du SRAS-CoV-2 représente une stratégie alternative pour prévenir le COVID-19. Il existe ici différentes approches (19. ), mais bien sûr, chacune de ces stratégies de traitement comporte également ses défis fondamentaux et translationnels qui doivent être surmontés pour obtenir un bénéfice clinique. Les obstacles techniques comprennent le potentiel hors cible, les effets indépendants de l'ACE2, la stabilité ou la toxicité (19). Les composés d’origine naturelle pourraient constituer ici une ressource importante car ils sont décrits à long terme et nombre d’entre eux sont considérés comme sûrs. Bien que les expériences d'amarrage in silico aient impliqué plusieurs produits naturels courants comme inhibiteurs de l'ACE2, il n'a pas encore été démontré que la plupart d'entre eux inhibent la liaison des pointes à l'ACE2, ce qui pourrait s'expliquer par un manque de couverture complète des résidus de liaison de l'ACE2 par les composés (20). . Cependant, pour la glycyrrhizine, la nobilétine et la néohespéridine, la liaison de l'ACE2 se situe partiellement dans la région de contact RBD, et il a donc été proposé que celles-ci bloquent également la liaison des pointes à l'ACE2 (20). Il en va de même pour les inhibiteurs synthétiques de l’ACE2 tels que la N-(2-aminoéthyl)-1 aziridine éthanamine (NAAE) (21). En revanche, l’antibiotique lipoglycopeptide dalbavancine a maintenant été identifié à la fois comme un liant de l’ACE2 et un inhibiteur de l’ACE2 de pointe du SRAS-CoV-2 (22) ; L’infection par le SRAS-CoV-2 a été efficacement inhibée par ce composé dans les modèles de souris et de singe rhésus. Le blocage de l'interaction Spike-ACE2 avec 74 % a également été démontré pour un extrait hydroalcoolique d'écorce de grenade, pour ses principaux composants, la punicalagine avec 64 % et l'acide ellagique avec 36 %. En utilisant une infection par lentivirus pseudotypé par Spike SARS-CoV-2 de cellules rénales humaines 2 (HK-2), l’entrée du virus a ensuite été efficacement bloquée par l’extrait de peau (23). Dans la présente étude, nous avons démontré une puissante inhibition de la protéine ACE2 Spike S1 RBD par des extraits de T. officinale à l'aide d'un test sans cellules et avons confirmé cette découverte en démontrant une inhibition efficace de la liaison à la surface des cellules ACE2 dans deux lignées cellulaires humaines. Nous avons observé une liaison plus forte des variantes D614G et N501Y au récepteur de surface ACE2 des cellules humaines, mais toutes les variantes testées étaient sensibles à l'inhibition de liaison par T. officinale, avant ou après utilisation. À ce jour, plusieurs études indiquent que la lignée du virus D614G est plus infectieuse que le virus D614 (24). La présence de mutations caractéristiques telles que N501Y provenant par ex. G., ce que l’on appelle la variante britannique B.1.1.7, conduit à une infectivité plus élevée que la souche mère, ce qui pourrait être dû à une affinité de liaison plus élevée entre la protéine de pointe et l’ACE2 (25). Par conséquent, nos découvertes sur les extraits de T. officinale peuvent être importantes ici, car de nouvelles variantes virales potentiellement préoccupantes apparaîtront à mesure que la pandémie progresse, ce qui pourrait également réduire l’efficacité de certains vaccins ou entraîner une augmentation des taux de réinfection. Comme mentionné ci-dessus, un problème dans le développement de produits destinés à prévenir l’infection par le SRAS-CoV-2 ou à ralentir la propagation systémique du virus est la sélectivité pour l’entrée de virus à faible toxicité pour l’hôte. Aucun cas de surdosage de T. officinale n'a été signalé pour les indications médicales actuelles (11, 13, 16). La posologie recommandée est de 4 à 10 g (environ 20 à 30 mg par ml d'eau chaude) jusqu'à 3 fois par jour (Commission E et ESCOP). Les contre-indications à l'utilisation de T. officinale, selon les informations de l'Agence européenne des médicaments (EMA), comprennent l'hypersensibilité à la famille des plantes des Astéracées ou à leurs principes actifs, les maladies hépatiques et biliaires, y compris l'obstruction des voies biliaires, les calculs biliaires et la cholangite, ou les maladies actives. estomac -Maladies intestinales, ulcère (16). La plante est une source importante de potassium (26, 27) et met donc en garde contre le risque possible d'hyperkaliémie. L'utilisation chez les enfants de moins de 12 ans, pendant la grossesse et l'allaitement n'a pas été prouvée en raison du manque ou de données suffisantes.
Bien que l'activité enzymatique ACE2 n'ait pas été affectée par l'extrait de T. officinale dans la présente étude, la protéine ACE2 a été temporairement régulée négativement dans la lignée cellulaire pulmonaire surexprimant ACE2, ce qui nécessite plus d'attention dans les études en cours. ACE2 est une mono-carboxypeptidase zinc-dépendante importante dans la voie de signalisation rénine-angiotensine, qui est cruciale pour les effets sur les systèmes cardiovasculaire et immunitaire. Une perturbation de l'équilibre angiotensine II/angiotensine (1-7) par inhibition de l'activité enzymatique ACE2 ou diminution des protéines et une plus grande quantité d'angiotensine II circulant dans le système est par exemple une perturbation de l'équilibre angiotensine II/angiotensine (1-7). G. a reconnu que cela favorise les lésions pulmonaires associées à la maladie COVID-19 (28, 29).
On pense que le poumon est la principale cible d’intérêt, mais l’expression de l’ARNm et des protéines ACE2 a été trouvée dans les cellules épithéliales de tous les tissus buccaux, en particulier dans la muqueuse buccale, la lèvre et la langue (30). Ces données concordent avec l’observation de charges virales très élevées dans la salive chez les patients infectés par le SRAS-CoV-2 (31, 32). La cavité buccale, en tant que partie essentielle des voies aérodigestives supérieures, est donc considérée comme jouant un rôle clé dans la transmission et la pathogénicité du SRAS-CoV-2. Il existe un fort potentiel selon lequel la prévention de la colonisation virale au niveau de la muqueuse buccale et pharyngée pourrait être cruciale pour éviter de nouvelles infections d’autres organes et l’épidémie de COVID-19 (33). Il a donc été suggéré que les bains de bouche virucides commerciaux, principalement à base de povidone iodée, pourraient potentiellement réduire la charge virale du SRAS-CoV-2 chez les personnes infectées (34-36), mais il n'existe à ce jour aucune étude clinique significative (36) . Le blocage de la liaison du virus SARS-CoV-2 aux cellules de la cavité buccale avec des extraits de T. officinale ne peut être tolérable pour un consommateur que pendant des périodes de temps limitées (par exemple, application du produit après un contact avec des personnes infectées ou en cas d'infection). D'autres expériences in vitro physiologiquement pertinentes que nous avons menées ont montré que seuls de courts temps de contact avec l'extrait de T. officinale étaient nécessaires pour bloquer efficacement la liaison des pointes du SRAS-CoV-2 ou pour éliminer les pointes déjà liées de la surface cellulaire. Des preuves supplémentaires de la pertinence ont été fournies par des expériences avec des virus Spike pseudotypés du SRAS-CoV-2. Bien que l’utilisation de ces virus pseudotypés ne permette pas d’évaluer la contribution des caractéristiques du virion telles que les protéines membranaires ou d’enveloppe au tropisme cellulaire (37), ils sont considérés comme un outil utile pour documenter la pertinence de l’ACE2 dans les étapes d’entrée cellulaire mises en œuvre par le Spike. les protéines sont médiées.
Tous les candidats vaccins développés visent à générer des réponses en anticorps (et en lymphocytes T) contre la protéine de pointe, et les séquences de pointe de la première souche de Wuhan ont servi ici de base (38). Cependant, le SRAS-CoV-2 mute constamment lors d’une transmission continue entre les personnes. La dérive antigénique virale est clairement démontrée par l'émergence récente de B.1.1.7, B.1.351 ou B.1.1.28 (P.1). Il évolue pour potentiellement échapper à nos approches thérapeutiques et prophylactiques existantes qui ciblent le pic viral. Par conséquent, des facteurs tels qu'une faible toxicité chez l'homme et une inhibition efficace de la liaison de cinq mutations de pointe pertinentes sur le récepteur ACE2 humain, comme indiqué ici in vitro, encouragent une analyse plus approfondie de l'efficacité de T. officinales dans le SRAS-CoV-2. prévention et nécessite désormais des preuves cliniques de confirmation supplémentaires.
Matériels et méthodologie
matériel végétal
L'étude a été réalisée en utilisant des feuilles séchées de T. officinale (d'Achterhof, Uplengen, Allemagne ; lot n° 37259, B370244 et P351756). Sur trois sites différents dans la région de Fribourg i. Gebr. (Allemagne), le 12 juillet 2020, et a été testé positif dans le test de liaison acellulaire Spike S1-ACE2 (données non présentées). C. intybus a été acheté chez Naturideen (Allemagne).
Lignées et cultures cellulaires
Des cellules de rein embryonnaire humain 293 (HEK293) exprimant de manière stable hACE2 ont été généreusement fournies par le Prof. Stefan Pöhlmann (Göttingen, Allemagne). Les cellules ont été maintenues dans du milieu Eagle modifié par Dulbecco (DMEM) à haute teneur en glucose additionné de 10 sérum de veau fœtal (FCS) %, 100 U / ml de pénicilline / streptomycine et 50 μg / ml de zéocine (Life Technologies, Darmstadt, Allemagne). Des cellules humaines A549-hACE2-TMPRSS2, générées à partir de la lignée cellulaire A549 de poumon humain, ont été achetées auprès d'InvivoGen SAS (Toulouse Cedex 4, France) et maintenues dans du DMEM, riche en glucose supplémenté avec 10 FCS % inactivés par la chaleur, 100 U/ml de pénicilline. /streptomycine, 100 µg/ml de normocine, 0,5 µg/ml de puromycine et 300 µg/ml d'hygromycine. Pour la sous-culture, toutes les cellules ont d'abord été rincées avec une solution saline tamponnée au phosphate (PBS), puis incubées avec de la trypsine 0,251 TP3T-EDTA jusqu'au détachement. Toutes les cellules ont été cultivées à 37 ° C dans un incubateur humidifié avec une atmosphère d'air de 5 % CO2/95 %.
Extraits de plantes
Le matériel végétal séché a été pesé dans un flacon en verre ambré (Carl Roth GmbH, Allemagne) et mélangé avec de l'eau de qualité HPLC (ad) à température ambiante (RT). Les extraits ont ensuite été incubés pendant 1 h et centrifugés à 16 000 g (3 min, TA). Le surnageant a été filtré (0,22 µm) avant utilisation pour les expériences.
Analyse du pic de SARS-COV2 – inhibition de l’interaction ACE2 par ELISA et cytométrie en flux
Pour la détection acellulaire de l’inhibition de l’interaction SARS-CoV-2 Spike – ACE2, un kit de dépistage de l’inhibiteur du SARS-CoV-2 disponible dans le commerce (Kat# : 16605302, Fisher Scientific GmbH, Schwerte, Allemagne) a été utilisé. Ce test ELISA colorimétrique mesure la liaison entre la protéine de pointe du SRAS-CoV-2 RBD immobilisée et la protéine ACE2 humaine biotinylée. La détection colorimétrique est réalisée à l'aide de streptavidine-HRP suivie d'une incubation au TMB. Un inhibiteur du SRAS-CoV-2 (hACE2) a servi de référence méthodologiquement vérifiée.
L'expression de l'ACE2 à la surface cellulaire a été déterminée à l'aide d'un anticorps humain conjugué à l'ACE2 PE (Bio-Techne GmbH, Wiesbaden-Nordenstadt, Allemagne) et d'une analyse cytométrique en flux. Pour analyser la liaison du SARS-CoV-2 S1 Spike RBD -ACE2, 2 x 105 cellules (5 x 106 cellules/ml) ont été prétraitées avec des extraits de plantes à différents moments. Puis 500 ng/ml SARS-CoV-2 Spike S1 (Trenzyme GmbH, Konstanz, Allemagne), Spike S1 D614G, N50Y ou mélange de K417N, E484K et N501Y (Sino Biological Europe GmbH, Eschborn, Allemagne) -Sa protéine recombinante a été ajoutée à chaque échantillon a été ajouté et les échantillons ont ensuite été incubés pendant 30 à 60 minutes. Dans un autre contexte, les cellules ont été prétraitées avec 500 ng/ml de protéine recombinante SARS-CoV-2 Spike-His pendant 30 minutes avant d'être incubées avec l'extrait de plante pendant 30 à 60 secondes à 4°C ou 37°C. Les échantillons ont été incubés dans un tampon PBS contenant du 5% FCS. Les cellules ont ensuite été lavées une fois avec un tampon PBS contenant du FCS 1% à 500 x g pendant 5 min avant d'être colorées avec le mAb His-tag A647 (Bio-Techne GmbH, Wiesbaden-Nordenstadt, Allemagne) pendant 30 min à température ambiante. Les cellules ont ensuite été lavées deux fois comme décrit ci-dessus. Les cellules ont été analysées avec un FACSCalibur (BD Biosciences, Heidelberg, Allemagne), 10 000 événements ont été acquis. L'intensité moyenne de fluorescence (MFI) de chaque échantillon a été déterminée à l'aide du logiciel FlowJo (Ashland, Oregon, USA).
Activité enzymatique ACE2 humaine et quantification des protéines
Les cellules A549-hACE2-TMPRSS2 (2 × 105) ont été ensemencées dans une plaque à 24 puits dans un milieu DMEM à haute teneur en glucose contenant 10 FCS % inactivés par la chaleur à 37 ° C, 5 % CO2. Les cellules ont ensuite été traitées avec un extrait de T. officinale avec/sans 500 ng/ml de protéine SARS-CoV-2 S1 Spike RBD pendant 1 à 24 heures. Les cellules ont ensuite été lavées avec du PBS et lysées. 25 μg de protéine ont été utilisés pour quantifier la protéine ACE2 (kit ACE2 ELISA), 5 μg pour l'activité enzymatique ACE2 (ACE2 Activity Assay Kit, Abcam, Cambridge, Royaume-Uni) conformément aux instructions du fabricant.
Infection des cellules A549-hACE2-TMPRSS2 par le lentivirus pseudotypé SARS-CoV-2
Des particules de lentivirus pseudotypées SARS-CoV-2 Spike préparées avec SARS-CoV-2 Spike (Genbank Accession #QHD43416.1) en tant que glycoprotéines d'enveloppe au lieu du VSV-G couramment utilisé ont été achetées auprès de BPS Bioscience (Catalog# : 7994299). , Biomol, Hambourg). Ces pseudovirions contiennent également le gène de la luciférase de luciole, qui est piloté par un promoteur CMV. Ainsi, l’entrée cellulaire médiée par les pointes peut être quantifiée via l’activité du rapporteur luciférase. Le pseudovirion lentiviral chauve (BPS Bioscience #79943), dans lequel aucune glycoprotéine d'enveloppe n'est exprimée, a été utilisé comme contrôle négatif. Firefly Luciferase Lentivirus (Puromycin) de BPS Bioscience (Catalog# : 79692-P) a été utilisé comme contrôle positif pour la transduction. Ces virus expriment de manière constitutive la luciférase de luciole sous un promoteur CMV. Les cellules pulmonaires ont été cultivées à raison de 0,1 × 106 cellules/cm2 dans des plaques à 96 puits dans du DMEM contenant 10 FCS % inactivés par la chaleur, 100 U/ml de pénicilline/streptomycine, 100 µg/ml de normocine, 0,5 µg/ml de puromycine et 300 µg/ml. . semé de l'hygromycine pendant la nuit. Le milieu a été remplacé par du FCS inactivé par la chaleur DMEM + 10 % et les cellules ont été traitées avec de l'ad ou un extrait de T. officinale soit 30 min avant, soit 3 h après l'ajout de 2,5 µl de particules de lentivirus. Après 24 h d'incubation des particules virales, le milieu a été éliminé par lavage avec du PBS, du milieu frais a été ajouté et les cellules ont été incubées pendant 60 h supplémentaires avec l'ajout d'extrait d'ad ou de T. officinale. La luminescence a été détectée en 1 heure à l'aide du réactif luciférase en une étape de BPS conformément au protocole du fabricant dans un lecteur multiplaque Tecan (Tecan Group Ltd, Crailsheim, Allemagne).
Quantification de la libération de cytokines par technique de billes multiplex
Quantification de la libération de cytokines par technique de billes multiplexAprès 24 h de transduction de lentivirus pseudotypé Spike SARS-CoV-2 et 60 h après l'infection de cellules A549-hACE2-TMPRSS2, les surnageants ont été collectés et stockés à -80 °C jusqu'à l'analyse de la sécrétion de cytokines avec l'humain MACSplex. Kit Cytokine 12 stocké (Miltenyi Biotec GmbH, Bergisch Gladbach, Allemagne) selon le protocole du fabricant.
Fractionnement du poids moléculaire à partir d'extraits de plantes
Des extraits de feuilles de plantes séchées ont été préparés en ajoutant de l'eau bidistillée (5 ml) au matériel végétal (500 mg chacun). Les échantillons ont été incubés dans l'obscurité à température ambiante (TA) pendant 60 min, suivis d'une centrifugation à 16 000 g pendant 3 min. Les surnageants ont été collectés et filtrés sur membrane (0,45 µm), ce qui a donné les extraits. Les aliquotes ont été lyophilisées pendant 48 heures pour déterminer leur rendement en poids. Les extraits ont ensuite été séparés en fractions de poids moléculaire élevé (HMW) et de faible poids moléculaire (LMW) à l'aide d'un tube de centrifugation doté d'un insert doté d'un filtre de coupure de poids moléculaire (5 kDa, Sartorius Stedim Biotech, Göttingen, Allemagne). devenu. . Chaque fraction HMW a été purifiée par rinçage avec 20 ml d'eau, donnant les fractions HMW ainsi que LMW. Les fractions ont été lyophilisées, leur rendement déterminé en poids et conservées à -20°C jusqu'à utilisation.
Détermination de la viabilité cellulaire par coloration au bleu trypan
Détermination de la viabilité cellulaire à l'aide du bleu trypan La viabilité cellulaire a été évaluée à l'aide du test d'exclusion du colorant au bleu trypan comme décrit précédemment (Odongo et al., 2017). En bref, les cellules A549-hACE2-TMPRSS2 ont été cultivées pendant 24 h, puis exposées à des extraits ou à un contrôle par solvant (ad) pendant 84 h.
Analyse statistique
Les résultats ont été analysés à l'aide du logiciel GraphPad Prism 6.0 (La Jolla, Californie, États-Unis). Les données ont été présentées sous forme de moyenne + SD. La signification statistique a été déterminée par un test ANOVA unidirectionnel suivi d'une correction de Bonferroni. Valeurs P < 0,05 () ont été considérés comme statistiquement significatifs et <0,01 (*) considéré comme hautement statistiquement significatif.
Contributions de l'auteur
Conception et conception de l'étude : EL ; Plan expérimental, acquisition de données, analyse de données : HTT, EL, NPKL ; Préparation des fractions d'extrait : CD, MG ; Rédaction de la première ébauche du manuscrit : EL. Tous les auteurs ont commenté les versions précédentes du manuscrit.
Remerciements
Les auteurs remercient le Prof. Dr. Stefan Pöhlmann (Centre allemand des primates, Göttingen, Allemagne) pour avoir fourni des cellules 293 de rein embryonnaire humain (HEK293) qui expriment de manière stable hACE2.
Sources
- 1.↵Lu R, et al. (2020) Caractérisation génomique et épidémiologie du nouveau coronavirus 2019 : implications pour les origines du virus et la liaison aux récepteurs. Lancette 395(10224) :565-574.RéfCrossPubMedGoogle Scholar
- 2.↵Paules CI, Marston HD et Fauci AS (2020) Infections à coronavirus – Plus qu’un simple rhume. JAMA 323(8):707-708.RéfCrossPubMedGoogle Scholar
- 3.↵Berlin DA, Gulick RM et Martinez FJ (2020) Covid-19 sévère. N Engl J Med 383(25):2451-2460.RéfCrossPubMedGoogle Scholar
- 4.↵Huang Y, Yang C, Xu XF, Xu W et Liu SW (2020) Propriétés structurelles et fonctionnelles de la protéine de pointe du SRAS-CoV-2 : développement potentiel de médicaments antiviraux pour le COVID-19. Acta Pharmacol Sin 41(9):1141-1149.RéfCrossPubMedGoogle Scholar
- 5.↵Grubaugh ND, Hodcroft EB, Fauver JR, Phelan AL et Cevik M (2021) Actions de santé publique pour contrôler les nouvelles variantes du SRAS-CoV-2. Cellule.Google Scholar
- 6.↵Zhou D, et al. (2021) Preuve d’évasion du variant B.1.351 du SRAS-CoV-2 à partir de sérums naturels et induits par le vaccin. Cellule.Google Scholar
- 7.↵Becerra-Flores M & Cardozo T (2020) La mutation du pic viral G614 du SRAS-CoV-2 présente un taux de létalité plus élevé. Revue internationale de pratique clinique 74(8):e13525.Google Scholar
- 8.↵Fratev F (2020) Les mutations N501Y et K417N dans la protéine de pointe du SRAS-CoV-2 modifient les interactions avec hACE2 et les anticorps d'origine humaine : une étude sur l'énergie libre de perturbation. bioRxiv :2020.2012.2023.424283.Google Scholar
- 9.↵Ho D, et al. (2021) Résistance accrue des variantes B.1.351 et B.1.1.7 du SRAS-CoV-2 à la neutralisation des anticorps. Place de la Rés.Google Scholar
- 10.↵Perrotta F, Matera MG, Cazzola M et Bianco A (2020) Infection respiratoire sévère par le SRAS-CoV2 : le récepteur ACE2 est-il important ? Respir Med 168:105996.RéfCrossGoogle Scholar
- 11.↵ESCOP (2003) « Taraxaci folium » et « Taraxaci radix ». Monographies sur les utilisations médicinales des plantes médicinales. (Thieme, Stuttgart) deuxième éd., Ed pp 499-504.Google Scholar
- 12.↵Blumenthal M, Busse WR, Goldberg A, Gruenwald J, Hall T, Riggins CW, Rister RS. (eds) « Herbe de pissenlit » et « Racine de pissenlit avec herbe » Dans : Les monographies complètes de la Commission allemande E. Guide thérapeutique des plantes médicinales. Conseil botanique américain, Austin, Texas 1998 ; 118-120.13. Association BHM (1990) « Feuille de pissenlit » et « Racine de pissenlit ». Pharmacopée britannique à base de plantes 1 : 37-39.Google Scholar
- 14.↵Gonzalez-Castejon M, Visioli F et Rodriguez-Casado A (2012) Diverses activités biologiques du pissenlit. Nutr Rév 70(9) :534-547.PubMedGoogle Scholar
- 15.↵Schutz K, Carle R et Schieber A (2006) Taraxacum – une revue de son profil phytochimique et pharmacologique. J Ethnopharmacol 107(3):313-323.RéfCrossPubMedWeb de la scienceGoogle Scholar
- 16.↵Agence européenne des médicaments (EMA) CoHMPH (2009) Rapport d'évaluation sur Taraxacum officinale Weber ex Wigg., folium. HMPC/579634/2008.Google Scholar
- 17.↵Pour KK et al. (2020) Réinfection au COVID-19 par une souche de SRAS-coronavirus-2 phylogénétiquement distincte confirmée par séquençage du génome entier. Clin Infect Dis. 25 août : ciaa1275. est ce que je: 10.1093/cid/ciaa1275.RéfCrossPubMedGoogle Scholar
- 18.↵Edridge AWD, et coll. (2020) L’immunité protectrice contre le coronavirus est de courte durée. medRxiv :2020.2005.2011.20086439.Google Scholar
- 19.↵Jia H, Neptune E et Cui H (2020) Cibler ACE2 pour le traitement COVID-19 : opportunités et défis. Journal américain de biologie cellulaire et moléculaire respiratoire. 9 décembre. est ce que je : 10.1165/rcmb.2020-0322PS.RéfCrossGoogle Scholar
- 20.↵Zhou J & Huang J (2020) Résultats actuels concernant les composants naturels ayant une activité potentielle anti-2019-nCoV. Frontières de la biologie cellulaire et du développement 8:589.Google Scholar
- 21.↵Huentelman MJ, et al. (2004) Découverte basée sur la structure d'un nouvel inhibiteur de l'enzyme de conversion de l'angiotensine 2. Hypertension 44(6):903-906.RéfCrossGoogle Scholar
- 22.↵Wang G, et al. (2021) La dalbavancine se lie à l'ACE2 pour bloquer son interaction avec la protéine de pointe du SRAS-CoV-2 et est efficace pour inhiber l'infection par le SRAS-CoV-2 dans les modèles animaux. Cellule Res 31(1):17-24.Google Scholar
- 23.↵Tito A, et al. (2020) Un extrait d'écorce de grenade comme inhibiteur de la liaison du SARS-CoV-2 Spike à l'ACE2 humain : une source prometteuse de nouveaux médicaments antiviraux. bioRxiv :2020.2012.2001.406116.Google Scholar
- 24.↵Korber B, et al. (2020) Suivi des changements dans le pic du SRAS-CoV-2 : Preuve que le D614G augmente le pouvoir infectieux du virus COVID-19. Cellule 182(4) :812-827 e819.RéfCrossPubMedGoogle Scholar
- 25.↵Santos JC et Passos GA (2021) Le pouvoir infectieux élevé du SRAS-CoV-2 B.1.1.7 est associé à une force d'interaction accrue entre Spike-ACE2 provoquée par la mutation virale N501Y. bioRxiv :2020.2012.2029.424708.Google Scholar
- 26.↵Hook I, McGee A et Henman M (1993) Évaluation du pissenlit pour l'activité diurétique et la variation de la teneur en potassium. Journal international de pharmacognosie 31(1):29-34.Google Scholar
- 27.↵Escudero NL, De Arellano ML, Fernández S, Albarracín G et Mucciarelli S (2003) Taraxacum officinale comme source de nourriture. Aliments végétaux pour la nutrition humaine 58(3):1–10.PubMedWeb de la scienceGoogle Scholar
- 28.↵Imai Y, et al. (2005) L'enzyme de conversion de l'angiotensine 2 protège contre l'insuffisance pulmonaire aiguë sévère. Nature 436(7047):112-116.RéfCrossPubMedWeb de la scienceGoogle Scholar
- 29.↵Kuba K, et al. (2005) Un rôle crucial de l’enzyme de conversion de l’angiotensine 2 (ACE2) dans les lésions pulmonaires induites par le coronavirus du SRAS. Nat Med 11(8) :875-879.RéfCrossPubMedWeb de la scienceGoogle Scholar
- 30.↵Zhong M, et coll. (2020) Les expressions d’ACE2 et de furine dans les cellules épithéliales buccales facilitent peut-être l’infection au COVID-19 par les voies respiratoires et fécales-orales. Front Med (Lausanne) 7:580796.Google Scholar
- 31.↵ Selon KK-W et al. (2020) Détection cohérente du nouveau coronavirus 2019 dans la salive. Maladies infectieuses cliniques : une publication officielle de l'Infectious Diseases Society of America 71(15):841–843.RéfCrossPubMedGoogle Scholar
- 32.↵Yoon JG, et al. (2020) Importance clinique d’une charge virale élevée du SRAS-CoV-2 dans la salive. J coréen Med Sci 35(20) :e195–e195.RéfCrossGoogle Scholar
- 33.↵Wolfel R, et al. (2020) Évaluation virologique des patients hospitalisés atteints de COVID-2019. Nature 581(7809):465-469.RéfCrossPubMedGoogle Scholar
- 34.↵Seneviratne CJ, et al. (2020) Efficacité des bains de bouche commerciaux sur la charge virale du SRAS-CoV-2 dans la salive : essai contrôlé randomisé à Singapour. Infection : 1–7.Google Scholar
- 35.↵ de Toledo Telles-Araujo G, Caminha RDG, Kallas MS, Sipahi AM et da Silva Santos PS (2020) Rince-bouche et sprays nasaux potentiels qui réduisent la charge virale du SRAS-CoV-2 : que savons-nous jusqu'à présent ? Cliniques (Sao Paulo) 75 : e2328.Google Scholar
- 36. Carrouel F, et al. (2021) Activité antivirale des réactifs dans les bains de bouche contre le SRAS-CoV-2. Journal de recherche dentaire 100(2):124-132.Google Scholar
- 37.↵Joglekar AV & Sandoval S (2017) Vecteurs lentiviraux pseudotypés : un vecteur, plusieurs formes. Méthodes Hum Gene Ther 28(6):291-301.RéfCrossGoogle Scholar
- 38.↵Krammer F (2020) Vaccins contre le SRAS-CoV-2 en développement. Nature 586(7830) :516-527.RéfCrossPubMedGoogle Scholar
Conseil de l’Europe – Résolution 2361 (2021) – Pas de vaccination obligatoire
Titre: Vaccins contre le Covid-19 : considérations éthiques, juridiques et pratiques
Dans cette résolution, vous pouvez lire sous 7.1.1 « garantir des procès de haute qualité, solides et menés de manière éthique conformément aux dispositions pertinentes de la Convention pour la protection des droits de l'homme et de la dignité de l'être humain en ce qui concerne la Application de la biologie et de la médecine : Convention sur les Droits de l'Homme et la biomédecine (STE n° 164, Convention d'Oviedo) et son Protocole additionnel concernant la recherche biomédicale (STCE n° 195), et qui incluent progressivement les enfants, les femmes enceintes et les mères allaitantes ;".
L'article 7.1.1 exige que des études de haute qualité et éthiques soient garanties conformément aux dispositions pertinentes de la Convention pour la protection des droits de l'homme et de la dignité des personnes à l'égard des applications de la biologie et de la médecine, conformément à la Convention sur Protection des droits de l'homme et de la biomédecine (SEV n° 164, Convention d'Oviedo (Lien) - PDF) et le protocole additionnel sur la recherche biomédicale (SEV n° 195 (Lien) - PDF), qui inclut à terme les enfants, les femmes enceintes et les mères allaitantes.
L'Accord d'Oviedo STCE 164 (SEV 1164) du 4 avril 1997 prévoit au chapitre IV, article 13, - "Interventions sur le génome humain - Une intervention visant à modifier le génome humain ne peut être entreprise qu'à des fins préventives,
à des fins diagnostiques ou thérapeutiques et seulement si son but est d’introduire une quelconque modification dans le génome d’une quelconque descendance. »
Il est clairement défini ici qu'une intervention visant à modifier le génome humain a uniquement un but préventif,
à des fins diagnostiques ou thérapeutiques et seulement si elle ne vise pas à modifier le génome de la progéniture.
Article 13 – Interventions sur le génome humain
Une intervention visant à modifier le génome humain ne peut être entreprise qu'à des fins préventives,
à des fins diagnostiques ou thérapeutiques et seulement si son objectif n'est pas d'introduire une quelconque modification dans
le génome de tous les descendants.
Le point 7.3.1 dit de « veiller à ce que les citoyens soient informés que la vaccination n’est pas obligatoire et que personne ne subit de pression politique, sociale ou autre pour se faire vacciner s’il ne le souhaite pas ».
En d’autres termes, l’objectif est de garantir que les citoyens soient informés que la vaccination n’est PAS obligatoire et que personne ne sera soumis à des pressions politiques, sociales ou autres pour se faire vacciner s’il ne le souhaite pas.
Le point 7.5.1 souligne que « mettre en place des programmes indépendants d’indemnisation des vaccins pour garantir une indemnisation pour les dommages et préjudices injustifiés résultant de la vaccination ; des programmes d’indemnisation indépendants doivent être mis en place à partir desquels une indemnisation pour les dommages et préjudices inappropriés résultant de la vaccination doit être versée. .
Le point 7.5.2 stipule « d’utiliser les certificats de vaccination uniquement aux fins prévues, à savoir surveiller l’efficacité du vaccin, les effets secondaires potentiels et les événements indésirables ; »
Les certificats de vaccination sont destinés uniquement à contrôler l’efficacité des vaccins, ainsi que leurs effets secondaires et événements indésirables.
En plus de cela, les autres contenus méritent également d’être lus et pris en compte.
Portugal – 0,9 décès % Covid-19 au lieu des 17 000 officiellement
Grâce à une pétition de la population portugaise, le tribunal du Portugal a dû traiter la question du nombre de personnes enregistrées comme mortes du Covid-19 et officiellement estimé à environ 17.000 on estime qu’ils sont effectivement décédés du Covid-19.
Le tribunal a recueilli des preuves et a formulé son Verdict du 19 mai 2021, il est arrivé à la conclusion que seules 152 personnes sont mortes du Covid-19.
Selon la lecture habituelle, toute personne décédée ayant eu un test PCR positif au cours des 28 derniers jours ou ayant été enregistrée comme personne contact doit être comptée comme décès du Covid-19.
Le 11 novembre 2020, la Cour d'appel de Lisbonne avait déjà statué sur le procès contre les mesures de quarantaine ordonnées sur la base des résultats des tests PCR. Il a été mis en évidence dans un document de 34 pages Verdict, sur la base de plusieurs sources scientifiques, l'ordre de quarantaine concernant la validité discutable de la procédure de test PCR.
Point de déclaration pour la clarification des décès après vaccination CORONA
Le syndicat Médecins et scientifiques pour la santé, la liberté et la démocratie eV propose sur son site Internet une large gamme d'informations, de conseils et de suggestions sur l'autopsie des personnes décédées après une vaccination corona. Ceci est également disponible en téléchargement ici PDF publié. Il est notamment précisé explicitement que l'autopsie a été réalisée conformément aux recommandations de
Prof. Dr. Arne Burkhardt
Laboratoire de pathologie de Reutlingen
Eaux supérieures 3-7
72764 Reutlingen
sont à réaliser.
Le conseil d'administration de l'association est composé du Prof. Dr. méd. Sucharit Bhakdi, spécialiste en microbiologie et épidémiologie des infections, professeur émérite. l'Université Johannes Gutenberg de Mayence, de 1991 à 2012, directeur de l'Institut local de microbiologie médicale et d'hygiène, le Dr. méd. Ronald Weikl, gynécologue, Prof. Dr. Stefan Homburg, professeur de finances publiques, Université Leibniz de Hanovre et Daniela Folkinger, consultante psychologique, enseignante, Thurmansbang.
Ostéopathie et vaccination corona
Jens Oskamp*, ostéopathe à Cologne, a rédigé l'information patient suivante, qui fait référence aux risques des vaccins vectoriels et à ARNm en relation avec le traitement ostéopathique et entraîne donc l'exclusion des personnes vaccinées.
„Malheureusement, je dois vous informer que je ne peux pas traiter les personnes qui ont reçu des vaccins dits à ARNm et à vecteur contre le SRAS CoV2. Contrairement aux vaccinations traditionnelles, il s'agit de méthodes de génie génétique qui manipulent les propres cellules de l'organisme pour produire elles-mêmes des parties d'un virus dans le but de déclencher une réponse immunitaire de l'organisme. Ces « vaccins » n’ont qu’une autorisation d’urgence. Il existe peu ou pas de recherches sur les réactions croisées avec d’autres médicaments et thérapies. (Vidéo – Prof. Dr. Hockertz, 2020)
Les problèmes suivants se posent à cet égard pour les traitements ostéopathiques :
On ne sait pas encore clairement quelles zones du corps sont affectées par la formation de thrombose. La thrombose veineuse cérébrale bien connue comme effet secondaire se produit parce que le sang circule relativement lentement dans cette zone du corps (Chen et coll. 2021). Mais le sang circule lentement dans d’autres parties du corps. Des thrombi peuvent également s'y former. (Kadkhoda,2021). Si, par exemple, les vaisseaux sanguins du système veineux des jambes deviennent plus perméables grâce à des techniques ostéopathiques, des thrombus initialement formés peuvent se détacher, ce qui, dans le pire des cas, peut conduire à une embolie pulmonaire. La formation de thrombus se produit souvent sans symptômes.
En outre, il ne peut être exclu que d'autres réactions immunitaires incontrôlées puissent survenir dès que des agents pathogènes sont libérés des tissus lors d'un traitement ostéopathique. Normalement, le système immunitaire peut y faire face facilement. Cependant, un système immunitaire trop réactif peut entraîner de graves complications et détruire les propres tissus de l'organisme (Vojdania et Kharrazianb, 2020), (Talotta,2021).
Un bon traitement ostéopathique élimine les blocages du système lymphatique. À la suite de la manipulation de l'ARNm, une quantité non naturelle d'anticorps spécifiques y est stockée (Chambre 2020). Il ne peut être exclu que des réactions significatives se produisent (Hotez et coll. 2020) dès que ces tissus évoluent dans le cadre d'un traitement ostéopathique. Le système nerveux peut également être touché, comme dans les cas de paralysie fasciale [paralysie faciale] (Shemer et coll. 2021),(Renould et al, 2021) ou des problèmes oculaires dus à un Œdème papillaire (Société allemande d'ophtalmologie, 2021) montrer.
D'autres problèmes proviennent des nanoparticules utilisées dans les vaccins à ARNm (Chen et coll. 2021). Ils conduisent entre autres à une vacuolisation (pratiquement la formation d'œdèmes au niveau cellulaire) de certains types de tissus, notamment le foie. C'est le signe que les cellules correspondantes sont mortes suite à des réactions avec des nanoparticules (Vidéo – Dr. Vanessa Schmidt-Krüger, 2021*). Ici aussi, on ne sait pas exactement ce qui se passe si le liquide provenant de ces « œdèmes » ou des tissus morts pénètre dans la circulation sanguine grâce aux techniques ostéopathiques.
*Liens de téléchargement locaux vers les vidéos du Dr. Vanessa Schmidt-Krüger est ici (Vidéo 1_2) et ici (Vidéo 2_2) disponible.
Si vous avez déjà subi des modifications génétiques grâce aux vaccins ARNm/vecteur, je vous demande de reprendre rendez-vous avec moi au plus tôt 10 mois après ces mesures. Nous discuterons ensuite des tests de laboratoire et des procédures d’imagerie nécessaires pour exclure toute complication. (par exemple Examen pour l'œdème papillaire - Société allemande d'ophtalmologie, 2021)
Les injections multiples augmentent l’intensité et la probabilité des relations décrites ci-dessus. Cela signifie que je me réserve le droit de refuser de manière générale un traitement même après un délai de 10 mois.
Un système immunitaire fort comme alternative à la vaccination nécessite des connaissances !!! Je recommande le matériel vidéo suivant :
- Dr. rer. nat. Markus Stark – Renforcer le système immunitaire et les défenses
- Dr.med.Mathias Rath – Mettre fin à la pandémie actuelle – prévenir de futures pandémies !
- Prof. Dr. Jörg Spitz – Vitamine D – Hype ou espoir„
- Le site de Jens Oskamp (en cours de mise à jour)*
Modification de la loi fondamentale et de la protection contre les infections
Avec celui publié par le Bundestag allemand le 22 juin 2021 Imprimés 19/30938 devient pour le 23.07.2023 la RESTRICTION du droit à l'intégrité physique, qui était encore garanti par la constitution !
' Article 9
Modification de la loi sur la protection contre les infections
§ 36, paragraphe 12, de la loi du 20 juillet 2000 sur la protection contre les infections (BGBl.
I S. 1045), en dernier lieu par l'article 1 de la loi du 28 mai 2021
(BGBl. I p. 1174) a été modifié, est rédigé comme suit :
« (12) Celui basé sur le paragraphe 8 phrase 1 ou le paragraphe 10 phrase 1
La réglementation légale émise entre en vigueur au plus tard un an après l'abrogation de la
Détermination de la situation épidémique de portée nationale par le
Bundestag allemand invalide selon l'article 5, paragraphe 1, phrase 2. Jusqu'au sien
Une réglementation légale édictée sur la base du paragraphe 8, phrase 1 ou du paragraphe 10, phrase 1 peut être modifiée même après la levée de la situation épidémique d'importance nationale.
Article 10
Restriction des droits fondamentaux
Par l'article 9 devenir les droits fondamentaux de l’intégrité physique (article 2, paragraphe 2, phrase 1, de la Loi fondamentale), liberté de la personne
(article 2, paragraphe 2, phrase 2 de la Loi fondamentale), liberté de circulation (article 11
1er alinéa de la Loi fondamentale) et l'inviolabilité du domicile (article 13, alinéa 1 de la Loi fondamentale) limité.
7. L'ancien article 9 devient l'article 11 et le paragraphe 2 est ainsi rédigé :
(2) « Les articles 1, 2, 6, 7, numéros 1, 2 et 4 ainsi que l'article 8 entrent en vigueur en juillet 2023. »
Évaluation de 109 études sur le port du masque
Le 20 avril 2021, une évaluation de 109 études sur les aspects sanitaires du port de masques en période de pandémie a été réalisée. Revue internationale de recherche environnementale et de santé publique publié, le ici au format PDF dans l'original (anglais) et ici La version allemande est disponible en téléchargement.
Les chercheurs arrivent à un résultat qu’ils ne croyaient pas eux-mêmes possible avec un tel niveau de dégâts.
Outre les effets négatifs déjà connus, il convient de souligner le syndrome d'épuisement induit par le masque (MIES).
Les effets du MIES peuvent inclure des problèmes de concentration, de réflexion et d’élocution, une diminution du rythme cardiaque et respiratoire et de la profondeur de la respiration, ce qui peut à son tour causer des dommages au sang et aux artères coronaires et, par conséquent, des maladies neurologiques et cardiaques. Les effets à long terme font toujours l’objet de recherches en cours.
OMS – Modification des recommandations vaccinales pour les enfants
Dans le version Depuis le 3 juin 2021, il est recommandé de ne pas vacciner les enfants pour le moment, car il n’existe toujours aucune preuve fiable permettant de vacciner les enfants contre le Covid-19, d’autant plus que, comme les adolescents, ils ont généralement des cas plus bénins que les adultes. Les vaccinations habituelles recommandées pour les enfants doivent néanmoins être poursuivies.
Dans le version actuelle, publié le 20 juin 2021, le passage ci-dessus a été modifié de sorte que, même si les évolutions plus douces sont signalées et qu'une vaccination ne doit pas nécessairement être effectuée tant que les enfants ne font pas partie d'un groupe à risque, plus des informations sont encore nécessaires pour pouvoir formuler des recommandations générales en matière de vaccination.
Néanmoins, Pfizer BioNTech est défini comme adapté aux enfants de plus de 12 ans. Les enfants âgés de 12 à 15 ans, en tant que membres de groupes à risque, devraient également se voir proposer ce vaccin, ainsi que d'autres groupes prioritaires.
Comme dans l’ancienne version, il est souligné qu’il n’existe pas encore suffisamment de données provenant de séries de tests avec des enfants. Dès que de plus amples informations seront disponibles, des recommandations appropriées seront émises.
Les passages modifiés sont surlignés en jaune dans les documents ci-dessus.
Fort Décision du STIKO pour la 6ème mise à jour de la recommandation vaccinale COVID-19 et la justification scientifique associée en Bulletin épidémiologique 23/2021 Il est conseillé (conformément aux recommandations actuelles de l’OMS) de « vacciner les enfants et les adolescents ayant déjà souffert de maladies avec le vaccin à ARNm Comirnaty (BioNTech/Pfizer) en raison d’un risque accru présumé d’évolution grave de la maladie COVID-19 ». "L'utilisation de Comirnaty chez les enfants et adolescents âgés de 12 à 17 ans sans antécédents de maladie n'est actuellement généralement pas recommandée, mais est possible après avis médical et avec des souhaits individuels et une acceptation du risque."
Î.-P.-É. – Rapport de sécurité
Le PEI (Paul Ehrlich Institute), une agence fédérale du ministère de la Santé liée par des instructions, publie à intervalles de plusieurs semaines des soi-disant rapports de sécurité concernant les vaccins utilisés et leurs effets secondaires.
Le RKI (Institut Robert Koch), une autorité fédérale supérieure indépendante liée par des instructions au sens de Art. 87, paragraphe 3, phrase 1 GG. Elle abrite « plusieurs commissions scientifiques, par exemple la Commission permanente de vaccination, qui élabore des recommandations vaccinales. Il est également responsable du traitement du contenu et de la coordination des rapports fédéraux sur la santé et de l’approbation de l’importation et de l’utilisation de cellules souches embryonnaires humaines.
Résumé des cas :
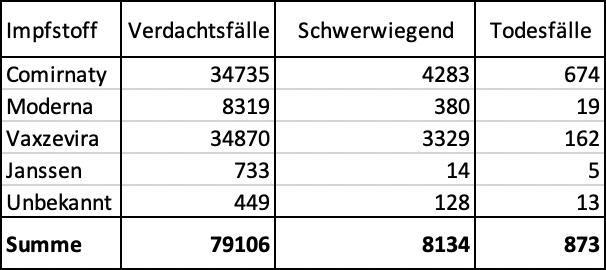
De plus amples informations sur ces autorités sont disponibles sur le site Internet Ministère fédéral de la Santé.
La base de données américaine VAERS donne les chiffres suivants pour les USA :
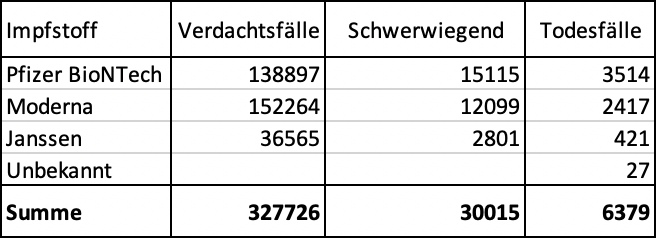
A titre de comparaison : depuis le début des vaccinations contre la diphtérie, la rougeole, les oreillons, la rubéole, la polio et le tétanos, 4 050 personnes sont mortes aux États-Unis. Le premier vaccin contre la diphtérie a été approuvé en Allemagne en 1936, le vaccin contre la rougeole aux États-Unis en 1963, le vaccin contre les oreillons et la rubéole en 1969, le vaccin contre la polio en 1955 et le vaccin contre le tétanos en 1930.
C'est-à-dire de la part du gouvernement comme « sûr » et « très efficace » Les vaccins déclarés contre le Covid-19 ont, sur la base des données disponibles aux États-Unis, généré 150 % de ces décès en six mois (!), ce que toutes les vaccinations mentionnées ci-dessus n'ont pas atteint ensemble depuis six à huit décennies !
Efficacité des vaccins Covid-19
Depuis le 1er juin 2021, le RKI a annoncé dans sa FAQ concernant les vaccins à ARNm : « La durée de la protection vaccinale n’est pas encore connue. La protection ne commence pas immédiatement après la vaccination et certaines personnes vaccinées restent sans protection.
Concernant les vaccins à base de vecteurs, les éléments suivants sont rapportés : « La durée de la protection vaccinale n’est pas encore connue. La protection ne commence pas immédiatement après la vaccination et certaines personnes vaccinées restent sans protection.
Cela soulève la question de savoir dans quelle mesure les « effets secondaires indésirables » et les « décès » enregistrés dans les rapports de sécurité de l’Île-du-Prince-Édouard ou dans d’autres bases de données peuvent être justifiés s’il est ouvertement admis que ni une protection immédiate ni une protection après plusieurs vaccinations ne sont accordées. informations disponibles sur la durée d’une éventuelle protection.
Messages archivés :
FAQ – Tests Corona
Post du 31 mars 2021 08:43
Les « tests » sont un compagnon presque quotidien de nos jours. Et la question se pose souvent de savoir quoi, quels tests testent, comment et avec quelle signification. Vous trouverez ci-dessous une liste des procédures et propriétés de test disponibles :
Test PCR
... est utilisé pour détecter l'ARN du SRAS-CoV-2, c'est-à-dire des parties du matériel génétique du virus Covid-19, mais pas pour détecter le virus actif, c'est-à-dire reproductible.
Pour une détection à l’aide d’une ligne de fluorescence spécifique, le matériel génétique contenu dans l’échantillon doit être dupliqué. La fréquence des cycles de reproduction est reflétée par ce que l'on appelle la valeur Ct (valeur de seuil de cycle).
Idéalement, cette valeur Ct est documentée sur le rapport de laboratoire.
Un test PCR positif avec une valeur Ct de 30...35 indique une faible charge virale, et une valeur Ct >35 indique une charge virale très faible.
Une valeur Ct de 25, par exemple, représente une charge virale importante. (Source: Test PCR – Pertinence de la valeur Ct)
Cependant, comme en pratique les valeurs de Ct ne sont ni documentées ni traitées de manière standardisée par les différents laboratoires, et que certains travaillent avec des valeurs de Ct de 40 ou plus (jusqu'à 50), les résultats des tests PCR ne sont ni comparables ni significatifs. . Le risque de résultats de test faussement positifs augmente à mesure que la valeur Ct augmente, avec toutes les conséquences négatives La Lancette rapporté dans le cadre d’une enquête au Royaume-Uni.
Ce n’est pas pour rien que les recommandations sont : OMS Le résultat d’un test PCR doit toujours être évalué en relation avec les symptômes de la maladie existants et les diagnostics cliniques.
Test d'antigène
... est destiné à détecter une infection aiguë (structures protéiques du virus corona), mais nécessite une charge virale élevée. Une confirmation par un test PCR ultérieur (avec une faible valeur Ct) est donc requise.
Une liste de ceux en Allemagne avec une autorisation spéciale (Expire mi-mai 2021) Les tests antigéniques mis sur le marché sont disponibles sur le site Internet de l'Institut fédéral des médicaments et des dispositifs médicaux (BfArM). BfArM – Tests antigéniques avec agrément spécial.
Le test peut conduire à des résultats faussement positifs si l'équipement de test a été stocké en dessous de la température de stockage recommandée et est ensuite utilisé.
Test d'anticorps (échantillon de sang – test Elisa / test rapide)
... détecter les anticorps spécifiques produits par l'organisme en réponse au virus corona.
Peu importe que la réponse immunitaire (formation des anticorps détectés) soit due à une infection antérieure par le Covid-19 ou à une vaccination contre le Covid-19.
Entretien avec le Dr. Greiner, laboratoire de diagnostic, Vienne
Covid-19 – Ce que disent les anticorps.
Éradiquer le Covid-19 ?
Post du 31 mars 2021 09:06
Est-il possible d'éradiquer un virus ?
– Combien de temps a-t-il fallu pour que le virus de la rougeole soit (à moitié) « vaincu » ?
Le premier vaccin antirougeoleux comportant un vaccin fragmenté inactivé a été approuvé aux États-Unis en 1963 et a été continuellement développé. Cependant, après près de 60 ans, la rougeole n’est toujours pas éradiquée (source : Virus de la rougeole).
– Combien de temps a-t-il fallu pour éradiquer le virus de la polio ?
La première vaccination contre la polio avec un virus inactivé a été administrée pour la première fois en 1955 (source : Vaccination contre la polio), une seconde suivit en 1960. L’OMS déclara l’éradication de la polio en 2015, 60 ans plus tard(!).
Et aujourd'hui, on pense que les vaccins développés en quelques mois, qui utilisent des technologies vectorielles ou ARNm, n'ont pas été testés avec succès sur des animaux, ni sur des humains avec des études de phase I .. III conçues de manière conventionnelle, sur leurs effets secondaires et à long terme. effets Il n'y a aucune déclaration, et les produits n'ont été mis sur le marché qu'avec une autorisation d'urgence, ce qui n'est pas indiqué dans les formulaires de consentement, selon laquelle ils sont capables de vaincre ou même d'éradiquer un virus - et cela en quelques mois ?!
À l’instar des virus de la poliomyélite et de la rougeole, on peut supposer qu’il faudra au moins deux générations au Covid-19 avant d’être éradiqué, ou du moins maîtrisé.
Voulez-vous continuer à imposer le confinement, la vaccination obligatoire (encore seulement indirectement), la quarantaine, l'isolement, l'obligation de porter un masque, etc. jusqu'au certificat de vaccination numérique ?!
Le seul moyen efficace et garanti d’éradiquer le virus reste soit un confinement de près de 60 ans, soit l’élimination de l’hôte du virus, c’est-à-dire l’extermination de chaque personne. La survie du virus est alors éliminée.
Au fait : cela explique aussi qu'un virus s'efforce toujours de ne pas tuer son hôte pour pouvoir continuer à se multiplier. Les mutations poursuivront donc toujours l’objectif de se reproduire de manière optimisée, mais sans devenir plus dangereuses pour son hôte. Il ne fait aucun doute que les virus peuvent encore être mortels pour les personnes précédemment malades.
Comment comprendre les allers-retours du gouvernement ?
Poste du 03. avril 2021 22h11
Avant de tenter d’aborder cette question afin d’élaborer l’une des réponses possibles, il est utile de s’imaginer en 2012.
Le Bundestag allemand a commandé en 2012 une « analyse des risques dans la protection civile », dont le rapport a été publié le 3 janvier 2013 sous la forme d'un imprimé 17/12051, disponible à l'adresse suivante : Rapport d'analyse des risques – imprimé 17/12051 v. 01/03/2013 peut être consulté et téléchargé au format PDF.
Au chapitre 2.3, page 5, vous trouverez le thème « Analyse des risques « Pandémie causée par le virus Modi-SARS ».
Cela a été suivi par un document de 17 pages intitulé « Comment maîtriser le COVID-19 », classé comme « information classifiée à usage officiel uniquement », qui était toujours disponible sur le site Internet du ministère fédéral de l'Intérieur le 20 mai 2020. Comment maîtriser le COVID-19 était disponible et téléchargeable. Aujourd'hui il n'y est plus accessible, mais via ce lien de sauvegarde Document de situation classifié sur la COVID-19 du ministère fédéral de l'Intérieur.
Toutes les actions passées, actuelles et futures du gouvernement fédéral en lien avec le COVID-a9 en découlent.
Les efforts actuels du gouvernement visant à limiter progressivement l'influence de toutes les institutions en amont sur les décisions du Chancelier, à les exclure, à priver le pouvoir législatif de sa fonction constitutionnellement consacrée, ainsi que les changements structurels du personnel des tribunaux de la République fédérale d'Allemagne, visent tous à la direction qui a déjà commencé en 1933. Mais cette fois, aucun allié n’est disponible pour permettre l’instauration d’une nouvelle loi fondamentale qui mettrait précisément un terme à cette entreprise !
EMA – arrière-plans
Message du 20 avril 2021 02:43
Les liens entre la fonction de l'EMA (Agence européenne des médicaments) et la carrière, ainsi que les conflits d'intérêts qui en résultent, de la présidente de l'EMA, Emer Cooke, sont présentés ici, comme l'a rapporté epochtimes.de le 7 avril 2021 : La présidente de l'EMA, Emer Cooke, a été lobbyiste pour la plus grande organisation pharmaceutique européenne pendant des années.
surmortalité
Post du 20 avril 2021 08:09
Toujours heureux d’aborder le sujet de la surmortalité. Outre le manque de capacité en lits de soins intensifs, l’argument de la surmortalité est un compagnon constant pour justifier les mesures du gouvernement.
On pourrait penser que les chiffres de l'Office fédéral de la statistique devraient également être connus lors des conférences de presse fédérales (voir : Nombre de décès en mars 2021 : 11 % en dessous de la moyenne des années précédentes).
Néanmoins, M. Hanno Kautz, porte-parole du ministre de la Santé Jens Spahn, sait Conférence de presse fédérale du 19 avril 2021 rien sur ces chiffres. Interrogé par M. Reitschuster : « Monsieur Kautz, selon l'Office fédéral de la statistique, nous avons eu un faible taux de mortalité le mois dernier. En mars, il y a eu 11 pour cent de décès de moins que la moyenne des années 2017 à 2020. Comment expliquez-vous cela ? » il répond simplement : « Je ne commente pas les chiffres que je n'ai jamais vus auparavant. » et « Vous citez un numéro très précis, que je ne connais pas, dont je ne connais pas le contexte. Je ne peux pas commenter cela à ce stade.
La question se pose : si ces chiffres sont si inintéressants et que les gens ne les ont même pas remarqués ou ne les connaissent pas, pourquoi sont-ils constamment cités pour justifier des mesures de plus en plus strictes ?