Table des matières
Mis à jour – 30 avril 2026
Une élaboration comparative de la thérapie standard du TDAH/TSA et de l'aromathérapie avec des huiles essentielles thérapeutiquement approuvées, testées par lot via analyse GC/MS. (État au 04.2026).
TDAH/TDA et Huiles Essentielles – Explication Claire
Un résumé concis et accessible au grand public pour ceux qui souhaitent en savoir plus sur le soutien naturel pour le TDAH
Qu'est-ce que le TDAH/TSA ?
TDAH représente Trouble du déficit de l'attention avec ou sans hyperactivité, Publicités pour la variante sans hyperactivité (trouble du déficit de l'attention). Aucune des deux n'est une invention ou une erreur d'éducation, ce sont de véritables maladies neurologiques dans lesquelles le cerveau est câblé différemment.
L'image derrière : Imaginez le cerveau comme une radio. Dans le cas d'un cerveau atteint de TDAH, le récepteur saute constamment entre les fréquences, parfois trop fort, parfois trop faible, rarement sur la bonne station. C'est ce qui rend la concentration, le fait de rester assis tranquillement ou le contrôle des impulsions difficiles.
Ce qui se passe dans le cerveau avec le TDAH.
Le problème fondamental réside dans deux neurotransmetteurs :
Dopamine – le “ messager de la récompense et de la motivation ”
Dans le TDAH, la dopamine est “nettoyée” trop rapidement (par le transporteur de dopamine DAT). Cela entraîne un manque de sentiment de récompense et de motivation pour les tâches quotidiennes. Le cerveau est constamment à la recherche de stimulation, d'où l'impulsivité et la recherche de risques.
Norépinéphrine – le “ messager de l’attention et de la concentration ”
Trop peu de noradrénaline dans le cortex préfrontal (la “zone chef” du cerveau) – Entraîne des problèmes de concentration, de l'oubli, des difficultés à planifier
Quelles zones du cerveau sont touchées ?
- Cortex préfrontal
Responsable de la planification, du contrôle des impulsions, de la concentration – hypoactif dans le TDAH
- Striatum (Noyaux gris centraux)
Centre de récompense – moins sensible chez les personnes atteintes de TDAH
- Cervelet
Synchronisation et coordination – légèrement altérées en cas de TDAH
Quelle est la fréquence du TDAH ?
Chez les enfants et les adolescents, c'est la maladie psychiatrique la plus fréquente avec 5 bis 7 %, chez les adultes 2,5 à 4 %, Beaucoup d'adultes ne savent pas qu'ils ont un TDAH.
Comment se manifeste le TDAH ?
Comment le TDAH est-il généralement traité ?
Le médicament principal – le méthylphénidate (Ritalin, Concerta, Medikinet)
Le méthylphénidate (MPH) est le médicament le plus couramment prescrit pour le TDAH et le traitement de première intention.
Comment ça marche ?
Le méthylphénidate bloque le transporteur de la dopamine (DAT), la “ pompe de nettoyage ” de la dopamine. Lorsque moins de dopamine est éliminée, il en reste davantage entre les cellules nerveuses, et le cerveau peut mieux se concentrer.
Les chiffres derrière
Une dose de 20 mg bloque environ. 54 % les pompes de nettoyage de dopamine dans le cerveau, 40 mg bloquent environ. 72 %.
L'effet commence après 30 à 90 minutes et dure de 4 à 12 heures selon la formulation.
Quelle est son efficacité ?
Sur 70-80 % Chez les patients, le méthylphénidate est cliniquement efficace : des améliorations de l'attention, de l'impulsivité et des résultats scolaires sont bien documentées.
Formulations
- Courtement actif (par exemple, Ritaline) : 4 à 6 heures, doit être pris plusieurs fois par jour
- En retardé (par ex. Concerta, Medikinet retard) : 8–12 heures, une fois par jour
Effets secondaires
– Diminution de l'appétit (effet secondaire le plus fréquent)
– Troubles du sommeil (si pris trop tard)
– Maux de tête, maux d'estomac (généralement au début)
– Légère augmentation du rythme cardiaque et de la pression artérielle
– Changements d’humeur, irritabilité (rare)
D'autres médicaments
Atomoxétine (Strattera)
– Aucun stimulant, inhibe le transporteur de noradrénaline (NET)
– Efficace également pour le TDAH sans risque de dépendance
Prend 4 à 6 semaines avant d'avoir un effet complet
– Particulièrement adapté en cas de trouble anxieux ou de trouble de la tics concomitant
Amphétamine (moins répandue en Allemagne)
– Lisdexamfétamine (Vyvanse) : Approuvé en Allemagne depuis 2013 pour les adultes
– Agit plus fort et plus longtemps que le méthylphénidate
Guanfacine (Intuniv)
– Pour les enfants et les adolescents chez qui les stimulants ne conviennent pas
Agit sur les récepteurs de noradrénaline dans le cortex préfrontal
Huiles essentielles pour le TDAH : comment cela peut-il fonctionner ?
Les huiles essentielles peuvent soutenir le cerveau atteint de TDAH de plusieurs manières :
- Sur l'odorat vers le cerveau
Les molécules odorantes activent le système limbique (émotions, motivation) et le cortex préfrontal (concentration) – directement et rapidement - Sur les systèmes de neurotransmetteurs
Certains terpènes influencent la dopamine, la noradrénaline, la sérotonine et le GABA - Complémentaire au méthylphénidate
Le méthylphénidate agit sur le DAT/NET – les huiles essentielles agissent sur d'autres systèmes (GABA-A, CB2, TRPM8, SERT) et sont donc des compléments potentiels.
Restriction importante
La recherche sur les huiles essentielles pour le TDAH en est encore à ses débuts. La plupart des études ont été menées sur des adultes en bonne santé, et non sur des patients atteints de TDAH. Les preuves cliniques directes sont encore limitées.
Quelles huiles essentielles peuvent aider en cas de TDAH ?
Menthe poivrée – l'huile n° 1 pour la concentration
Menthe poivrée (Mentha × piperita) fournit la preuve la plus solide d'amélioration de l'attention.
- Qu'est-ce qu'il y a dedans ?
Menthol (30–50 %)
Menthone (10–30 %)
1,8-Cinéole (5–10 %) - Le menthol provoque une sensation de fraîcheur sur la peau.
Active les récepteurs TRPM8 – les “ récepteurs du froid ” dans le système nerveux qui activent le cerveau
Inhibe l'enzyme qui dégrade le neurotransmetteur acétylcholine
Module les récepteurs GABA-A (légèrement sédatif en cas d'hyperactivité) - Essai clinique (n=24)
100 µL d'huile de menthe poivrée (encapsulée) ont significativement amélioré l'attention soutenue dans le test RVIP (Rapid Visual Information Processing) après 1 à 3 heures ; réduit la fatigue et amélioré l'arithmétique mentale - Particularité
Menthe poivrée favorise concentré Attention (par opposition à la lavande, qui a tendance à disperser l'attention) - Comment appliquer
2 gouttes sur un mouchoir, juste avant le cours ou des séances de travail ; diffuseur dans la salle d'étude
Romarin – pour la mémoire et la vigilance
Romarin (Rosmarinus officinalis) est appelé “herbe à mémoire” depuis l'Antiquité, et à juste titre.
- Qu'est-ce qu'il y a dedans ?
1,8-Cinéole (20–50 %)
Camphre (10–20 %)
α-Pinène (10–15 %) - Qu'est-ce que le 1,8-cinéole fait ?
Inhibe l'enzyme acétylcholinestérase qui dégrade le neurotransmetteur (similaire aux médicaments contre la maladie d'Alzheimer !)
Active le système nerveux, augmente la vigilance et l'attention.
Anti-inflammatoire et antioxydant dans le cerveau - Étude clinique (n=144)
L'aromathérapie au romarin a amélioré significativement la mémoire globale et la mémoire secondaire, mieux que la lavande et le groupe témoin. - Pour le TDAH
Particulièrement utile en cas de problèmes de mémoire, de “brouillard cérébral” et de somnolence matinale - Comment appliquer
Le matin dans le diffuseur (5 gouttes), inhalation avant les examens ou les tâches importantes - Attention ! Ne pas utiliser le soir, cela est trop activant ; prudence particulière en cas d'épilepsie en raison de la teneur en camphre !
Lavande – contre l'anxiété et les problèmes de sommeil
Lavande (Lavande vraie) est la meilleure huile pour l'anxiété et les problèmes de sommeil associés au TDAH.
- Qu'est-ce qu'il y a dedans ?
Linalol (25–45 %)
Acétate de linalyle (25–50 %) - Qu'est-ce que le linalol fait ?
Active les récepteurs GABA-A, le “frein” du cerveau
Modulo la sérotonine, la dopamine et la noradrénaline
Réduit le cortisol (hormone du stress) de 24 à 38 % - Particulièrement utile pour le TDAH
Difficultés d'endormissement (très fréquent avec le TDAH)
Troubles anxieux concomitants (chez environ 50 % des patients atteints de TDAH)
Dérèglement émotionnel et irritabilité - Note importante
La lavande peut le faire Altérer la mémoire de travail à court terme, c'est pourquoi il ne faut pas l'utiliser pendant les phases d'apprentissage, mais seulement le soir ou pour une détente ciblée - étude
Le Silexan (80 mg d'huile de lavande par jour sous forme de gélule) était comparable au lorazépam pour les troubles anxieux. - Comment appliquer
Le soir dans le diffuseur (5 gouttes), 2 gouttes sur l'oreiller
Bois de cèdre – Oxygénation et concentration
Bois de cèdre (Cèdre de l'Atlas / Genévrier de Virginie) est traditionnellement utilisé pour le TDAH.
- Qu'est-ce qu'il y a dedans ?
α-Cédrène
β-Cédrène
Cédrol - Ce qu'il fait
Améliore l'oxygénation du cerveau ; apaisant ; active le système parasympathique - Spécifique au TDAH
Godfrey (2001) a rapporté des effets positifs chez les enfants atteints de TDAH ;
Le cèdre a ralenti la fréquence cardiaque et respiratoire dans des études - Comment appliquer
Dans le diffuseur pendant des activités calmes ; se marie bien avec la lavande
Vétiver – le parfum d'ancrage
Vétiver (Chrysopogon zizanioidesa un parfum profond et terreux, souvent décrit comme “un baume pour les esprits agités”.
- Ce qu'il fait
Anxiolytique (qui soulage l'anxiété) ; calme le système nerveux ; améliore le sommeil - Spécifique au TDAH
Springer et al. (2018) ont rapporté des améliorations chez des enfants atteints de TDAH après 30 jours d'inhalations 3 fois par jour. - Pour qui
Spécialement pour la variante hyperactive du TDAH avec agitation intérieure
Cannelle – la seule étude directe sur le TDAH
Cannelle (Cinnamomum verum) a la preuve unique : la seule étude clinique réalisée directement chez des enfants atteints de TDAH.
- Qu'est-ce qu'il y a dedans ?
Zimtaldehyd (60–75 %)
Eugenol (5–10 %) - Étude sur le TDAH (Chen et al., 2008)
La combinaison de réadaptation + aromathérapie à la cannelle (1 % cannelle, inhalation nasale) sur 6 mois a montré des résultats significativement meilleurs dans le questionnaire SNAP-IV que la réadaptation seule (p < 0,05) - Mécanisme
Les métabolites du cinnamaldéhyde peuvent avoir une action dopaminergique - Restriction
L'étude présente des faiblesses méthodologiques (petite taille d'échantillon, aveuglement flou). - Comment appliquer
Economical in the diffuser, combined with other oils
Poivre noir (β-Caryophyllène) – contre la neuroinflammation
β-Caryophyllène de poivre noir, de lavande et d'autres plantes :
- Active les récepteurs cannabinoïdes CB2 sans effet psychoactif
- Réduit la neuroinflammation (inflammation dans le cerveau)
- Intéressant concernant le TDAH avec des signes d'inflammation concomitants ou des problèmes d'humeur
- Facile à combiner avec d'autres huiles
Les huiles en un coup d'œil – Quand utiliser quelle huile ?
Routine quotidienne pratique pour le TDAH
Routine du matin (Activation + Concentration) :
- Diffuseur Romarin (4 gouttes) + Menthe poivrée (2 gouttes) pendant 15 à 20 minutes
- Ou : Menthe poivrée sur un mouchoir, 3 respirations profondes avant l'école/le travail
- Effet : Vigilance, mémoire, concentration
Temps d'apprentissage / Phase de travail :
- Diffuseur Menthe poivrée (3 gouttes) + citron (2 gouttes) pendant 20 minutes, puis pause de 30 minutes
- Attention ! Pas de lavande pendant l'étude !
- Effet : Attention soutenue, concentration
Après-midi (détente après l'école) :
- Diffuseur Bois de cèdre (3 gouttes) + Bergamote (2 gouttes) pendant 20 minutes
- Effet : Réduction du stress, régulation émotionnelle
Routine du soir (Se détendre + Dormir) :
- Diffuseur Lavande (4 gouttes) + Vétiver (2 gouttes) 30 minutes avant de dormir
- Ou : 2 gouttes de lavande sur l'oreiller
- Effet : S'endormir, qualité du sommeil
Instructions de dosage pour le diffuseur
Important : Lors de l'adaptation olfactive, on ne sent presque plus l'huile après 20 à 30 minutes, mais elle continue d'agir. Pour que les récepteurs puissent se rétablir et que l'effet d'habituation soit „réinitialisé“, il faut respecter les pauses !
Qu'est-ce que la science dit réellement ?
Conclusion
Les preuves sont prometteur mais encore limité. Mécanistiquement, cela a du sens, mais les grandes études cliniques chez les patients atteints de TDAH font toujours défaut. Cela ne signifie pas que cela ne fonctionne pas, cela signifie que nous avons besoin de recherches supplémentaires.
Consignes de sécurité importantes
Considérations particulières pour le TDAH :
Hypersensibilité sensorielle
Beaucoup de personnes atteintes de TDAH (40 à 60 %) ont une sensibilité olfactive accrue. Commencez toujours par demi-dose et augmentez lentement. Si une odeur est désagréable : arrêtez immédiatement.
Interactions avec le méthylphénidate
- Cannelle
Peut avoir un effet dopaminergique, ce qui permet un effet potentiellement stimulant avec le MPH, d'où la nécessité de surveiller la fréquence cardiaque et la pression artérielle
- Lavande
Peut avoir un effet sérotoninergique, soyez prudent lors de la prise simultanée d'antidépresseurs
- Romarin
Peut avoir un effet stimulant, donc ne pas appliquer juste avant de se coucher
Chez les enfants
– Moins de 3 ans : Pas d'huiles essentielles
– 3-6 ans : Très faibles concentrations uniquement (1-2 gouttes), pièce bien aérée
– > 6 ans : dosage normal possible – Pas de contact direct avec la peau sans dilution
Règles générales :
- Toujours diluer avec une huile de support (par exemple, huile de coco fractionnée non grasse) (2–3 %)
- Utiliser un espace bien ventilé
- Faire des pauses (ne pas diffuser toute la journée)
- En cas d'asthme ou de problèmes respiratoires : consulter un médecin
- Les huiles essentielles sont aucun remplacement pour le méthylphénidate ou d'autres traitements du TDAH
FAQ – Foire aux questions
Puis-je remplacer le méthylphénidate par des huiles essentielles?
Non. Les huiles essentielles sont un complément, pas un substitut. Le méthylphénidate a des preuves cliniques solides chez 70 à 80 % % des patients. Les huiles essentielles peuvent aider à soulager les symptômes résiduels, à améliorer le sommeil ou à réduire les effets secondaires (comme l'anxiété).
Quelle huile devrais-je essayer en premier ?
Menthe poivrée pour la concentration (journée) et lavande pour le sommeil (soirée), les mieux étudiées, bien tolérées.
Combien de temps avant que je ressente un effet ?
Les effets de la manche (concentration, vigilance) sont perceptibles en quelques minutes. Pour des améliorations durables (sommeil, humeur), utilisez régulièrement pendant 2 à 4 semaines.
Cela fonctionne-t-il aussi pour les adultes atteints de TDAH ?
Oui, la plupart des études ont d'ailleurs été menées sur des adultes. Les adultes atteints de TDAH rapportent souvent une très bonne efficacité sur la dérégulation émotionnelle et les problèmes de sommeil.
Dois-je acheter des huiles chères ?
La qualité est importante : assurez-vous qu'il s'agit de 100 % huiles essentielles pures, idéalement avec un certificat d'analyse spécifique au lot (GC/MS).
Les huiles parfumées bon marché ou les parfums synthétiques n'ont aucun effet thérapeutique et peuvent être nocifs pour la santé en raison de leurs ingrédients synthétiques, provoquant des maux de tête, des nausées, etc.
Ceux qui souhaitent en savoir plus sur la sélection et la qualité des huiles essentielles, trouveront cela dans l'article „Huiles essentielles – Odyssée d'une quête“trouvé.
Un autre article cite le professeur Dr. Dr. Dr. méd. habil. Hanns Hatt de l'Université de la Ruhr à Bochum, qui dans sa vidéo „Guérir avec des senteurs“explique d'une manière intéressante, divertissante et néanmoins scientifique l'effet des huiles essentielles sur le corps humain.
Dois-je en parler à mon médecin ?
Pour l'aromathérapie (diffuseur, inhalation), ce n'est pas strictement nécessaire. Cependant, si vous souhaitez prendre des gélules ou des crèmes contenant des huiles essentielles, ou si votre enfant souffre de TDAH et prend du méthylphénidate, veuillez consulter votre médecin.
Bases neurobiologiques, mécanismes d'action moléculaires et preuves cliniques de la thérapie adjuvante avec le nébuliseur d'arômes organiques Organik 3.0
Rapport de recherche combiné Avril 2026
Thèmes : Méthylphénidate (Ritaline) · Pharmacodynamique intracérébrale · Aromathérapie adjuvante · Terpènes · Récepteurs · Voies de signalisation · Recommandations posologiques
Application : Organik Aromas Nébuliseur 3.0 (Nébulisation à froid Venturi, anhydre, huiles pures GC/MS)
TDAH et méthylphénidate
Ce rapport examine les bases neurobiologiques de la thérapie par méthylphénidate pour le trouble déficitaire de l'attention avec hyperactivité (TDAH) et évalue le potentiel des huiles essentielles comme option thérapeutique adjuvante. L'analyse repose sur 87 publications scientifiques concernant les concentrations intracérébrales de méthylphénidate et 159 études sur les huiles essentielles dans le contexte du TDAH.
Principales conclusions sur le méthylphénidate
Les doses orales thérapeutiques (0,25–0,6 mg/kg) induisent une occupation du transporteur de la dopamine (DAT) de >50% dans le striatum, 20 mg par voie orale atteignant 54% et 40 mg 72% de blocage du DAT. L'absorption cérébrale maximale est atteinte 60 à 90 minutes après administration orale. Les concentrations plasmatiques dans la plage thérapeutique sont de 3,5–7,8 ng/ml (adultes), 6 ng/ml étant associés à 50% de blocage du DAT. Il n'existe pas de mesures directes des concentrations de méthylphénidate dans le tissu cérébral (ng/ml) ou le LCR ; les données disponibles proviennent d'études d'occupation par TEP/SPECT.
Huiles essentielles comme adjuvants
Une plausibilité mécanistique existe pour une thérapie adjuvante basée sur des mécanismes d'action complémentaires. Le linalol (lavande) module les systèmes sérotoninergique, dopaminergique et noradrénergique via les récepteurs 5-HT1A et la liaison SERT. Le menthol (menthe poivrée) active les canaux TRPM8 et module les récepteurs GABA-A ainsi que nicotiniques, améliorant l'attention et la vigilance. Le β-caryophyllène (poivre noir) agit comme un agoniste CB2 aux propriétés anti-inflammatoires. Le 1,8-cinéole (romarin) améliore la mémoire et les fonctions cognitives.
État de la preuve
Bien que les données précliniques et mécanistiques soient prometteuses, les essais contrôlés randomisés (ECR) spécifiquement chez les patients atteints de TDAH font défaut. Les études humaines existantes montrent des améliorations cognitives chez des adultes en bonne santé (menthe poivrée : amélioration de l'attention soutenue, n=24 ; romarin : amélioration de la mémoire, n=144).
Ce rapport fournit des recommandations de dosage basées sur des preuves pour le Organik Aromas Nébuliseur 3.0 et des instructions de sécurité complètes pour l'application chez les patients atteints de TDAH.
Syndrome d'Asperger
Le trouble du spectre autistique (TSA) est un trouble neurobiologique complexe du développement, dont la prévalence estimée est de 1 à 2 % dans le monde. La symptomatologie principale comprend des troubles de la communication et des interactions sociales, ainsi que des schémas comportementaux répétitifs et des particularités sensorielles. Malgré des recherches intensives, il n'existe pas de traitements curatifs pour les symptômes principaux ; les interventions disponibles se concentrent sur la thérapie comportementale et la pharmacothérapie symptomatique. Ce rapport examine le potentiel des huiles essentielles comme option thérapeutique adjuvante dans le TSA, basé sur une analyse systématique de 547 publications scientifiques sur la neurobiologie du TSA, les terpènes et les preuves cliniques.
L'hétérogénéité neurobiologique des TSA se manifeste par un déséquilibre excitateur-inhibiteur (E/I) perturbé, des dysfonctionnements des systèmes GABAergiques, glutamatergiques, sérotoninergiques, dopaminergiques et oxytocinergiques, une neuroinflammation chronique avec activation microgliale, un stress oxydatif, des altérations de l'axe intestin-cerveau et des déficits synaptiques (neuroligines, protéines SHANK). Les régions cérébrales affectées comprennent le cortex préfrontal, l'amygdale, le cervelet, l'hippocampe et le striatum.
Les analyses moléculaires montrent que des terpènes spécifiques issus d'huiles essentielles ciblent des voies pertinentes pour l'autisme : le linalol (composant principal de la lavande) module les récepteurs GABA-A au niveau du site de liaison des benzodiazépines et influence les voies sérotoninergiques ; le β-caryophyllène agit comme agoniste sélectif des récepteurs CB2 avec des propriétés anti-neuroinflammatoires ; les acides boswelliques (encens) activent la voie antioxydante Nrf2/HO-1 et réduisent l'activation microgliale ; le 1,8-cinéole (eucalyptus) montre des effets anxiolytiques via la modulation des récepteurs GABA-A ; l'α-pinène agit sur le système GABAergique ; le Cananga odorata (Ylang-Ylang) influence le métabolisme de la sérotonine et de la dopamine dans des modèles précliniques de l'autisme.
Les preuves cliniques pour les TSA sont limitées : une étude randomisée contrôlée avec de la bergamote n'a montré aucun effet anxiolytique significatif chez les enfants atteints de TSA. De petites études pilotes rapportent une meilleure observance lors de l'analyse appliquée du comportement (ABA) sous aromathérapie à la lavande, une augmentation de l'attention partagée après un massage par aromathérapie et des effets potentiels sur le sommeil et l'anxiété. La qualité des preuves est cependant limitée par de petits échantillons, une hétérogénéité méthodologique et un manque de réplication.
Des recommandations de dosage spécifiques à la taille de la pièce sont développées pour le diffuseur d'arômes Organik Nebulizer 3.0 (principe Venturi, nébulisation à froid sans eau) : 2–4 gouttes pour 10–20 m², 4–6 gouttes pour 20–40 m², 6–10 gouttes pour 40–60 m², avec des applications de 15–30 minutes et des pauses de 30–60 minutes. Les particularités spécifiques aux TSA nécessitent une introduction progressive en raison d'une hypersensibilité sensorielle, des protocoles adaptés à l'heure de la journée (activateur le matin, calmant le soir) et un contrôle qualité strict (analyse GC/MS).
Les aspects de sécurité comprennent la prudence en cas d'épilepsie (huiles contenant du camphre), la contre-indication de l'eucalyptus chez les enfants de moins de 3 ans, les interactions potentielles avec les antipsychotiques (rispéridone, aripiprazole) et une considération particulière pour l'hypersensibilité sensorielle chez les TSA. La plausibilité mécanistique est présente, mais des études contrôlées randomisées de haute qualité font défaut. Les huiles essentielles peuvent être envisagées dans le cadre d'une approche thérapeutique multimodale pour les symptômes comorbides (anxiété, troubles du sommeil, dérégulation sensorielle), mais elles ne remplacent pas les interventions de base fondées sur des preuves.
TDAH et méthylphénidate
Thérapie Adjuvante avec des Huiles Essentielles dans le TDAH – Pharmacodynamique du Méthylphénidate, terpènes, récepteurs, dosage avec le Nébuliseur Organik Aromas 3.0
Introduction
Die Aufmerksamkeitsdefizit-/Hyperaktivitätsstörung (ADHS) ist eine der häufigsten neuropsychiatrischen Erkrankungen im Kindes- und Jugendalter, die bei 5–7% der Kinder und 2,5–4% der Erwachsenen auftritt. Methylphenidat (MPH), ein Dopamin- und Noradrenalin-Wiederaufnahmehemmer, stellt die pharmakologische Erstlinientherapie dar und zeigt bei 70–80% der Patienten eine klinische Wirksamkeit [A1], [A2].
Malgré l'efficacité établie du méthylphénidate, une partie des patients présente des symptômes résiduels, des effets secondaires ou le désir d'approches thérapeutiques complémentaires. Les huiles essentielles sont de plus en plus discutées comme option thérapeutique adjuvante potentielle, bien que les preuves scientifiques soient jusqu'à présent hétérogènes. [A3], [A4].
Objectif du rapport
Ce rapport poursuit cinq objectifs principaux :
- Quantification des concentrations intracérébrales de méthylphénidate sur la base de données PET/SPECT, y compris l'occupation DAT, les rapports plasma-cerveau et la distribution régionale
- Évaluation mécaniste de la plausibilité d'une thérapie adjuvante à base d'huiles essentielles sur la base de mécanismes d'action moléculaires
- Analyse fondée sur des données probantes huiles essentielles spécifiques et leurs principaux ingrédients actifs
- Développement de recommandations de dosage pratiques pour le nébuliseur d'arômes Organik 3.0
- Formulation d'avis de sécurité complets pour l'application chez les patients atteints de TDAH
L'analyse intègre des données provenant de 87 études sur les concentrations cérébrales de méthylphénidate et de 159 publications sur les huiles essentielles, en se concentrant sur les 30 publications les plus pertinentes.
Méthylphénidate – Concentrations intracérébrales et pharmacodynamique
DAT-Okkupanz – Relations dose-effet
L'efficacité thérapeutique du méthylphénidate est directement corrélée à l'occupation du transporteur de dopamine (DAT) dans le striatum. Les études TEP utilisant la [¹¹C]cocaïne comme traceur ont établi une relation dose-effet claire. [A9].
Tableau 1 : Occupation des DAT après administration orale de méthylphénidate
Source : Volkow et al. 1998 [A9]; Mesures chez des adultes en bonne santé
La dose estimée pour 50% de blocage DAT (%) (DE₅₀) est de 0,25 mg/kg de poids corporel [A9]. Des doses thérapeutiques adaptées au poids (0,3–0,6 mg/kg) génèrent ainsi de manière constante une occupation du DAT >50%, considérée comme le seuil d'efficacité clinique. [A7], [A9].
Différences régionales : L'occupation des DAT varie entre les sous-régions striées. Spencer et al. (2009) ont rapporté pour l'OROS-MPH (40 mg) après 10 heures les valeurs d'occupation suivantes : noyau caudé droit 44,3±11,8%, noyau caudé gauche 42,7±10,9%, putamen droit 41,6±11,7%, putamen gauche 41,3±13,1% [A17].
Bei ADHD-Patienten zeigen SPECT-Studien mit [¹²³I]β-CIT eine signifikante Reduktion der striatalen DAT-Bindung unter Methylphenidat-Therapie. Aster et al. (2021) dokumentierten eine 27,6–29,9%ige Abnahme des striatalen DAT-Bindungspotenzials (BP) bei Kindern und Jugendlichen mit ADHD unter Medikation [A25], [A18].
Concentrations plasmatiques versus cérébrales
Concentrations plasmatiques
La plage thérapeutique plasmatique du d-thréo-méthylphénidate chez les adultes se situe entre 3,5 et 7,8 ng/ml [A20], [A24]. Une concentration plasmatique de 5,7–6,0 ng/ml est associée à un blocage DAT de 50%. [A9], [A13], [A17].
Des concentrations maximales plus élevées ont été observées chez les patients pédiatriques : 20 ng/ml deux heures après une dose de 20 mg (0,8 mg/kg). [A20], [A24].
Capture cérébrale
Les études TEP avec la [¹¹C]méthylphénidate montrent que 7,5±1,5% de l'activité administrée par voie intraveineuse atteignent le cerveau [A5], [A14]. La concentration la plus élevée est atteinte dans le striatum, avec un rapport de volume de distribution (DVR) des ganglions de la base au cervelet de 2,2 à 3,3 pour le d-thréo-MPH. [A16], [A14].
Lacune critique de preuves
Les mesures directes des concentrations de méthylphénidate dans le tissu cérébral (en ng/ml ou nmol/L) ou dans le liquide céphalo-rachidien n'existent pas dans la littérature humaine. Toutes les données disponibles sont basées sur des mesures d'occupation par TEP/SPECT ou des études de distribution de traceur. [A1], [A2], [A3], [A4], [A5], [A6], [A7], [A8], [A9].
Distribution régionale – Striatum et cortex préfrontal
Striatum
En tant que région cible primaire, le striatum montre la plus forte capture de [¹¹C]méthylphénidate. La prémédication avec du méthylphénidate non marqué (0,5 mg/kg) réduit la liaison du traceur striatal de 40% [A5]. Le clairance dans le striatum est d'environ 90 minutes, beaucoup plus lente que celle de la cocaïne (20 minutes). [A5].
Cortex préfrontal
Bien que la densité de DAT soit plus faible dans le cortex préfrontal (CPF) que dans le striatum, des études fonctionnelles par TEP avec la [¹¹C]raclopride montrent des augmentations significatives de dopamine également dans les régions du cortex préfrontal et temporal après administration de méthylphénidate. [A30], [A22]. Ces augmentations corticales de dopamine sont corrélées à des améliorations des symptômes à long terme chez les patients atteints de TDAH. [A30].
Transporteur de noradrénaline (NET)
Le méthylphénidate bloque également le transporteur de noradrénaline avec une DE₅₀ de 0,14 mg/kg [A11]. Les études TEP avec [¹¹C]MRB montrent une occupation robuste des TRN dans le thalamus et la protubérance 75 à 195 minutes après le dosage. [A11], [A21].
Évolution temporelle et pharmacocinétique
Administration intraveineuse
Après injection intraveineuse de [¹¹C]méthylphénidate, la concentration cérébrale atteint son maximum en 8 à 10 minutes [A3], [A6].
Orale Gabe
La captation cérébrale maximale après administration orale est nettement retardée, avec un pic entre 60 et 90 minutes [A7], [A9], [A3]. Cette cinétique retardée explique le potentiel d'abus réduit des formulations orales par rapport aux applications intraveineuses. [A13].
Formulations retard
Les formulations à libération prolongée (OROS-MPH, DBDS-MPH) présentent une apparition encore plus lente avec une occupation DAT maximale retardée, mais des concentrations maximales comparables. [A13], [A17]. OROS-MPH atteint des valeurs d'occupation DAT significativement plus élevées que DBDS-MPH (44,3% vs. 34,8% dans le noyau caudé droit) après 10 heures à des concentrations plasmatiques plus élevées (5,2 vs. 3,8 ng/ml) [A17].
Données de microdialyse préclinique
Chez le rat, le d-thréo-méthylphénidate augmente la concentration extracellulaire de dopamine dans le striatum d'environ 650% [A16]. Cette augmentation massive de dopamine démontre l'effet fonctionnel du blocage du DAT sur la neurotransmission synaptique.
Huiles essentielles en thérapie adjuvante — Bases mécanistiques
Mécanismes d'action complémentaires au méthylphénidate

Figure 1 : Voies de signalisation moléculaire des huiles essentielles dans le TDAH – Système dopaminergique, système noradrénergique et mécanismes d'action complémentaires des terpènes
La plausibilité d'une thérapie adjuvante par huiles essentielles repose sur des mécanismes d'action complémentaires et non redondants par rapport au méthylphénidate. Tandis que le MPH inhibe principalement la recapture de la dopamine et de la noradrénaline, les composants des huiles essentielles ciblent des systèmes neurobiologiques supplémentaires.
Complémentarité mécanistique :
- Modulation GABAergique
Le menthol et le linalol agissent comme des modulateurs allostériques positifs sur les récepteurs GABA-A, ce qui renforce la neurotransmission inhibitrice et peut réduire l'hyperactivité. [A19], [A20], [A23]. - Effets sérotoninergiques
Le linalol se lie au transporteur de la sérotonine (SERT) et module les récepteurs 5-HT1A, ce qui induit des effets anxiolytiques et stabilisateurs de l'humeur. [A21], [A23], [A24]. - Les voies de signalisation anti-inflammatoires
Le β-caryophyllène active les récepteurs CB2 et réduit les processus neuro-inflammatoires via les voies de signalisation NF-κB et MAPK, qui peuvent être augmentées dans le TDAH. [A14]. - Modulation du canal TRP
Le menthol (agoniste TRPM8) et le 1,8-cinéole (modulateur TRPV1/TRPA1) influencent l'excitabilité neuronale et les flux ioniques indépendamment des systèmes monoaminergiques. [A19].
Récepteurs et voies de signalisation
Tableau 2 : Cibles réceptorielles des composants des huiles essentielles
LEO = Huile essentielle de lavande ; nAChR = récepteur nicotinique de l'acétylcholine
Modulation des récepteurs GABA-A
Le menthol présente une liaison aux récepteurs GABA-A qui dépend de la concentration et potentialise la neurotransmission inhibitrice. [A19]. Il est intéressant de noter que l'huile de lavande ne présente pas d'affinité pour le site de liaison des benzodiazépines du récepteur GABA-A, ce qui suggère un profil de sécurité plus favorable par rapport aux benzodiazépines. [A23].
Transporteur de sérotonine (SERT)
Le linalol et l'huile de lavande se lient au SERT avec des concentrations de 0,08–0,8% in vitro [A23]. Cette inhibition de la SERT pourrait conférer des effets antidépresseurs et anxiolytiques qui sont pertinents chez les patients atteints de TDAH souffrant de troubles anxieux comorbides (prévalence de 25–40%).
Antagonisme du récepteur NMDA
L'huile de lavande montre un antagonisme du récepteur NMDA dépendant de la dose avec une CI₅₀ de 0,04 µl/ml [A23]. La modulation des récepteurs NMDA est pertinente pour la plasticité synaptique et les processus d'apprentissage.
Activation du récepteur CB2
Le β-Caryophyllène est un agoniste CB2 sélectif sans effets psychoactifs (pas d'activation CB1). L'activation CB2 réduit l'activation microgliale et la production de cytokines pro-inflammatoires (TNF-α, IL-1β, IL-6), ce qui peut médier des effets neuroprotecteurs. [A14].
Potentiels synergiques
La combinaison du méthylphénidate avec des huiles essentielles pourrait produire des effets synergiques via plusieurs mécanismes :
- Équilibre Dopamine-GABA
Alors que le MPH augmente la transmission dopaminergique, la modulation GABAergique par le menthol/linalool pourrait favoriser un équilibre excitateur-inhibiteur plus équilibré et réduire l'hyperactivité. - Réduction du stress
Les effets anxiolytiques du linalol via les récepteurs 5-HT1A et la réduction du cortisol (% de 24 à 38 % dans les études cliniques) [A24] pourrait améliorer la réactivité au stress chez les patients atteints de TDAH. - Renforcement cognitif
La modulation cholinergique par le menthol (inhibition de l'acétylcholinestérase) [A19] et les effets de 1,8-cinéole sur la mémoire pourraient renforcer les améliorations cognitives du MPH. - Neuroprotection
Les propriétés anti-inflammatoires et antioxydantes du β-caryophyllène et du 1,8-cinéole pourraient offrir des effets neuroprotecteurs à long terme.
Limitation importante : Ces potentiels synergiques sont théoriquement plausibles, mais pas validés par des études cliniques chez des patients atteints de TDAH. Les études contrôlées sur la combinaison de MPH avec des huiles essentielles sont complètement absentes.
Huiles essentielles spécifiques – principes actifs et preuves
Lavande (Lavandula angustifolia) – Linalol
Principaux ingrédients actifs
Linalol (25–45%)
Acétate de linalyle (25–45%)
1,8-Cineol (1–3%)
Mécanismes
- Liaison SERT
Le linalol et l'huile de lavande se lient au transporteur de sérotonine, ce qui peut conférer des effets antidépresseurs. [A23]
- Antagonisme du NMDA
L'huile de lavande montre un blocage dépendant de la dose du récepteur NMDA (CI₅₀ : 0,04 µl/ml) [A23]
- Modulation du GABA
Renforcement de la neurotransmission inhibitrice via les récepteurs GABA-A (pas via le site de liaison des benzodiazépines) [A20], [A23]
- Effets monoaminergiques
Le linalol module les systèmes dopaminergiques, noradrénergiques et sérotoninergiques dans des modèles précliniques [A21]
Preuves cliniques
- Cognition
Moss et al. (2003) ont montré chez 144 adultes en bonne santé que l'aromathérapie à la lavande altérait la mémoire de travail et ralentissait les temps de réaction, mais qu'elle avait un effet subjectif apaisant. [A27]
- Attention
Colzato et al. (2014) ont constaté que l'arôme de lavande réduisait le “clignement attentionnel” (déficits d'attention temporelle), suggérant une distribution plus large de l'attention. [A30]
- Anxiolyse
L'administration orale de Silexan (80 mg/jour d'huile de lavande) a réduit les symptômes d'anxiété généralisée de manière comparable au lorazépam [A26]
- Réduction du stress
L'inhalation d'huile de lavande a réduit les taux de cortisol de 24 à 38% dans des études cliniques [A24]
Données spécifiques au TDAH
Aucune étude randomisée contrôlée chez des patients atteints de TDAH. Des rapports de cas décrivent des effets positifs sur l'agitation et le sommeil chez des enfants atypiques atteints de TDAH. [A8].
Posologie (préclinique/clinique)
– Oral : 50–100 µL encapsulés (étude de Kennedy) [A19]
– Inhalation : 4 gouttes dans 30 ml d'eau (diffuseur) [A30]
– Topique : 1,5% dilution dans une huile porteuse [A8]
Sécurité
L'huile de lavande n'a montré aucune augmentation de la neurotoxicité cellulaire in vitro [A23].
Aucun effet secondaire grave constaté lors des études cliniques aux doses recommandées.
Romarin (Rosmarinus officinalis) – 1,8-Cineol
Principaux ingrédients actifs
1,8-Cinéole (Eucalyptol, 20–50%)
Camphre (10–20%)
α-Pinène (10–15%)
Mécanismes
- Modulation cholinergique
Inhibition de l'acétylcholinestérase, qui renforce la neurotransmission cholinergique [A27]
- Activation du canal TRP
Le 1,8-cinéole module TRPV1 et TRPA1, ce qui affecte l'excitabilité neuronale
- Anti-inflammatoire
Inhibition des voies de signalisation NF-κB et MAPK, réduction des cytokines pro-inflammatoires
- Antioxydant
Activation de la voie de signalisation Nrf2, augmentation des enzymes antioxydantes
Évidence clinique : - Mémoire
Moss et al. (2003) ont montré, chez 144 adultes en bonne santé, des améliorations significatives de la mémoire globale et de la mémoire secondaire après une aromathérapie au romarin par rapport aux groupes témoins et à la lavande. [A27]
- Performance cognitive L'exposition à l'arôme de romarin a été corrélée à une amélioration des performances cognitives [A14]
- Vigilance : Le romarin a augmenté la vigilance et l'activité dans le cerveau [A29]
Données spécifiques au TDAH
Le romarin est mentionné dans des revues systématiques comme potentiellement utile pour le TDAH [A10], [A4], [A5], mais il manque des études cliniques contrôlées chez les patients atteints de TDAH.
dosage
– Inhalation : Exposition ambiante dans un environnement de test (concentration non spécifiée) [A27]
– Aucune recommandation de dosage standardisée pour le TDAH n'est disponible
Sécurité
Le romarin est considéré comme sûr en cas d'application par inhalation à des concentrations habituelles.
Attention avec les patients épileptiques en raison de la teneur en camphre.
Menthe poivrée (Mentha × piperita) – Menthol
Principaux ingrédients actifs
Menthol (30–50%)
Mentone (10–30%)
1,8-Cinéol (5–10%)
Mécanismes
- Activation du TRPM8
Le menthol est un puissant agoniste du TRPM8 (CE₅₀ ~30 µM), qui médiatise la sensation de froid et la modulation neuronale. [A19]
- Modulation des récepteurs GABA-A
Liaison dépendante de la concentration et modulation allostérique positive [A19]
- Récepteurs nicotiniques
Modulation des récepteurs nicotiniques de l'acétylcholine, influence sur la transmission cholinergique [A19]
- Inhibition de l'acétylcholinestérase
L'huile de menthe poivrée inhibe significativement l'acétylcholinestérase, ce qui renforce la neurotransmission cholinergique [A19]
Évidence clinique : - Vigilance constante
Kennedy et al. (2018) ont démontré dans une étude croisée randomisée en double aveugle (n=24 adultes en bonne santé) que 100 µL d'huile de menthe poivrée amélioraient les performances au test de traitement rapide de l'information visuelle (RVIP) 1 à 3 heures après l'ingestion. [A19]
- Réduction de la fatigue : Les deux doses (50 µL et 100 µL) ont réduit la fatigue et amélioré la soustraction sérielle après 3 heures. [A19]
- Contrôle attentionnel Colzato et al. (2014) ont découvert que l'arôme de menthe poivrée intensifiait le “blink attentionnel”, suggérant une attention plus focalisée (moins distribuée). [A30]
Données spécifiques au TDAH
Pas d'essais contrôlés randomisés chez les patients atteints de TDAH. La menthe poivrée est mentionnée comme potentiellement utile dans les revues sur le TDAH. [A4], [A5], [A29].
dosage
– Oral (encapsulé) : 50–100 µL d'huile pure [A19]
– Inhalation : 4 gouttes dans 30 ml d'eau (diffuseur) [A30]
Sécurité
L'huile de menthe poivrée est sûre lorsqu'elle est utilisée par inhalation et par voie orale aux doses recommandées.
Attention chez les nourrissons et les jeunes enfants (risque de laryngospasme en cas d'application nasale directe).
Poivre noir (Piper nigrum) – β-Caryophyllène
Principaux ingrédients actifs
β-Caryophyllène (10–35%)
Limonène (15–25%)
Sabinen (10–20%)
Mécanismes
- agonisme CB2
Le β-caryophyllène est un agoniste sélectif des récepteurs CB2 (Ki : 155±4 nM) sans activation des récepteurs CB1 (aucun effet psychoactif) [A14]
- Anti-inflammatoire
Réduction du TNF-α, de l'IL-1β, de l'IL-6 par inhibition de NF-κB [A14]
- Modulation de la microglie
Reprogrammation du phénotype microglial de M1 à M2, réduction des processus neuroinflammatoires
- Neuroprotecteur
Réduction du stress oxydatif par activation de Nrf2
Preuves cliniques
- Préclinique
Le β-Caryophyllène a montré des effets anxiolytiques dans des modèles animaux, possiblement via la modulation de l'activation neuronale dans le noyau central de l'amygdale. [A14]
- Anti-inflammatoire
Des études in vitro et in vivo démontrent des effets anti-inflammatoires robustes via l'activation des CB2.
Données spécifiques au TDAH
Aucune étude clinique chez des patients atteints de TDAH. Plausibilité mécanistique basée sur des hypothèses neuro-inflammatoires dans le TDAH.
dosage
Aucune recommandation de dosage standardisée pour l'administration par inhalation n'est disponible pour le TDAH.
Sécurité
Le β-caryophyllène est considéré comme sûr (statut GRAS de la FDA).
Aucun effet secondaire grave connu aux doses habituelles.
Vétiver (Chrysopogon zizanioides)
Principaux ingrédients actifs
Vétiverol
Khusimol
α-Vétivone
β-Vétivone
Mécanismes
- Anxiolytique
Des études précliniques montrent des effets anxiolytiques, potentiellement via la modulation de l'activité amygdalienne [A14]
- Apaisant
Traditionnellement utilisé pour calmer le système nerveux
Preuves cliniques
- spécifique au TDAH
Springer et al. (2018) rapportent que l'inhalation de vétiver (3 fois par jour pendant 30 jours) a montré des améliorations de la fonction et du comportement cérébraux chez les enfants. [A29]
- Limitations
Aucun essai contrôlé randomisé ; preuves basées sur des rapports de cas et une application traditionnelle
Données spécifiques au TDAH
Godfrey (2001) mentionne le vétiver comme potentiellement utile pour le TDAH. [A3], [A4], [A5], mais des données cliniques détaillées font défaut.
dosage
– Inhalation : 3 fois par jour pendant 30 jours (concentration spécifique non précisée) [A29]
Sécurité
Le vétiver est considéré comme sûr en cas d'application par inhalation. Aucun effet secondaire grave connu.
Cèdre (Cedrus spp.)
Principaux ingrédients actifs
α-Cédrène
β-Cédrène
Thujopsène
Cédrol
Mécanismes
- Oxygénation
Traditionnellement utilisé pour améliorer l'oxygénation du cerveau [A29]
- Apaisant
Propriétés sédatives dans l'usage traditionnel
Preuves cliniques
- spécifique au TDAH
Godfrey (2001) mentionne le bois de cèdre comme potentiellement utile pour le TDAH. [A3], [A4], [A5]
- Limitations
Aucune étude clinique contrôlée ; les preuves sont basées sur une utilisation traditionnelle et des anecdotes
Données spécifiques au TDAH
Springer et al. (2018) citent le bois de cèdre pour l'oxygénation du cerveau dans le TDAH [A29], mais les données quantitatives manquent.
dosage
Aucune recommandation de dosage standardisée disponible.
Sécurité
L'huile de bois de cèdre est considérée comme sûre lors d'une application par inhalation à des concentrations courantes.
Cannelle (Cinnamomum verum) – Aldéhyde cinnamique
Principaux ingrédients actifs
Zimtaldehyd (60–75%)
Eugenol (5–10%)
Mécanismes
- Modulation dopaminergique
L'allylbenzène et le propénylbenzène dans la cannelle sont des précurseurs de l'amphétamine et sont métabolisés en amphétamine, qui a un effet stimulant sur le mental. [A2]
- Activation de TRPA1/TRPV1
Le cinnamaldéhyde active les canaux TRPA1 et TRPV1
- Antimicrobien
Fortes propriétés antimicrobiennes
Évidence clinique : - spécifique au TDAH
Chen et al. (2008) ont mené une étude sur l'aromathérapie à la cannelle chez des enfants atteints de TDAH. L'association de la réadaptation et de l'aromathérapie à la cannelle (1% de cannelle, 1 g dans 100 ml d'eau, inhalation nasale) a montré des résultats significativement meilleurs après 6 mois selon le questionnaire SNAP-IV (58±2,6 vs contrôle) et les échelles d'activité (102±5,8) par rapport à la réadaptation seule (p<0,05). [A2], [A1]
Données spécifiques au TDAH
L'étude Chen est l'une des rares études cliniques portant sur les huiles essentielles spécifiquement chez les enfants atteints de TDAH, bien qu'elle présente des limites méthodologiques (pas d'informations sur la randomisation, le double aveugle, la taille de l'échantillon).
dosage
– Inhalation : 1% cannelle (1 g dans 100 ml d'eau) dans une salle de thérapie de 50 m² avec commande lumineuse électrique [A2]
Sécurité
L'huile de cannelle peut provoquer des irritations cutanées et des muqueuses à fortes concentrations.
Attention aux personnes sensibles.
La stimulation dopaminergique par les métabolites de la cannelle nécessite des recherches supplémentaires concernant les interactions avec le méthylphénidate.
Huiles essentielles supplémentaires indiquées pour le TDAH
Sur la base d'une recherche documentaire actuelle, les huiles essentielles supplémentaires suivantes ont pu être identifiées, qui pourraient être pertinentes pour le TDAH par des mécanismes neurobiologiquement plausibles.
Melissa officinalis (Mélisse citronnelle) – Acide rosmarinique, Flavonoïdes
Substances actives
Acide rosmarinique
Flavonoïde (lutéoline, apigénine)
huiles volatiles (Citral, Linalool, Géraniol)
Récepteurs et mécanismes d'action
– Récepteurs cholinergiques : Liaison nicotinique (nAChR) et muscarinique (mAChR)
– Modulation GABAergique : l'acide rosmarinique inhibe la GABA-transaminase → augmentation de la disponibilité du GABA
Inhibition de l'acétylcholinestérase : amélioration de la neurotransmission cholinergique dans le cortex préfrontal
Preuves cliniques
- ECR (n=20, double aveugle, croisé)
Les doses uniques de 300/600/900 mg par voie orale ont montré une amélioration significative de la précision de l'attention à 600 mg, ainsi que des effets sur la mémoire et la vigilance. [A31]
- Étude combinée (enfants, 7 semaines)
La combinaison d'extraits de valériane et de mélisse a amélioré significativement l'hyperactivité, les difficultés de concentration et l'impulsivité chez les enfants d'école primaire. [A32]
- Anti-Stress-Crossover
Des préparations standardisées de mélisse sous forme alimentaire ont réduit la surcharge cognitive et amélioré l'humeur chez des adultes en bonne santé. [A33]
Dosage (Organik Aromas Nebulizer 3.0)
– 3-5 gotas de aceite de melisa (puro GC/MS) para 15-25 m²
– Anwendung: 30 min avant les périodes de concentration, 2 à 3 fois par jour
– Combinaison avec la lavande (2:1) recommandée pour le soir/la détente
Sécurité
Bien toléré
Interaction possible avec les médicaments thyroïdiens (suppression de la TSH en cas de prise orale à forte dose)
L'inhalation est considérée comme sûre.
Eucalyptus (Eucalyptus globulus / radiata) – 1,8-Cineol
Substances actives
1,8-Cinéole (Eucalyptol, 70-85%)
alpha-pinène
Citron vert
Récepteurs et mécanismes d'action
– Site GABA-A/benzodiazépine : activité modulatrice (anxiolytique, sédatif à forte dose)
– Voies cholinergiques : le 1,8-cinéole inhibe l'acétylcholinestérase → attention et mémoire de travail améliorées
– Antioxydant/Neuroprotecteur : Réduction du stress oxydatif dans les cellules neuronales
Preuves cliniques
– Neuroprotektive Reviews mentionnent Eucalyptus globulus comme plante ayant des effets cognitifs dans des études animales et humaines [A34]
– Le 1,8-cinéole est également le principal principe actif du romarin (déjà inclus dans le rapport), l'eucalyptus fournit une concentration plus élevée et pure
– Les études par inhalation montrent une amélioration de la clarté mentale et de la concentration (études comparatives avec le romarin)
Dosage (Organik Aromas Nebulizer 3.0)
- 2-3 gouttes pour une pièce de 15 à 25 m² (odeur intense, à doser avec parcimonie)
– Application : Le matin/midi pour les phases de concentration, max. 20 min
- Contre-indication
Pas à utiliser par des enfants de moins de 3 ans
Pas en combinaison avec des médicaments contre l'asthme sans consulter un médecin
Sécurité
Huile forte, ne pas appliquer pure sur la peau
Enfants < 3 ans : contre-indiqué
Épileptiques : prudence
Gingembre (Zingiber officinale) – Gingérol, Zingibérène
Substances actives
6-gingérol
6-Shogaol
Zingiberene
β-Sesquiphellandrène
Récepteurs et mécanismes d'action
Antagonisme du récepteur sérotoninergique 5-HT3 : composante anxiolytique
– Dopaminergique : Les gingérols modulent l'activité dopaminergique dans le striatum (chez l'animal)
– Antioxydant/Anti-neuroinflammatoire : Inhibition de NF-κB, réduction de TNF-α
Preuves cliniques
– Préclinique : L'extrait de gingembre a amélioré la fonction cognitive dans des modèles animaux de TDAH
– Propriétés neuroprotectrices bien documentées par des mécanismes antioxydants
– Les essais contrôlés randomisés directs sur le TDAH font encore défaut dans la littérature
Dosage (Organik Aromas Nebulizer 3.0)
– 2–3 gouttes pour une pièce de 15–25 m²
– Combinaison avec du romarin (1:1) pour l'activation cognitive
Recommandations de dosage pour le nebuliseur d'arômes Organik 3.0
Principes techniques : Principe de Venturi et nébulisation
Le Organik Aromas Nébuliseur 3.0* utilise le principe Venturi pour la nébulisation à froid et sans eau d'huiles essentielles. Ce procédé offre plusieurs avantages :
Caractéristiques techniques
- Nébulisation à froid
Pas d'exposition à la chaleur, préservation de tous les composants volatils et des principes actifs thermolabiles
- Sans eau
Nébulisation directe d'huiles essentielles pures sans dilution, concentration plus élevée d'ingrédients actifs dans l'air ambiant
- Taille des particules
Génération de microparticules (1–5 µm) capables de pénétrer profondément dans les voies respiratoires et de traverser la barrière hémato-encéphalique
- Huiles pures certifiées GC/MS
Utilisation d'huiles testées analytiquement sans additifs, huiles de support ou parfums synthétiques
environ 110 à 120 USD (avec fonctionnement sur secteur / batterie)
- Livraison gratuite dans le monde entier
- Tenir compte des taxes de douane et d'importation !
Considérations pharmacocinétiques
L'inhalation d'huiles essentielles se fait par deux voies principales :
1. Voie olfactive
Connexion directe de l'épithélium olfactif au système limbique (amygdale, hippocampe) et au cortex préfrontal via le bulbe olfactif
2. Voie pulmonaire
Absorption à travers la membrane alvéolaire dans la circulation systémique, passage de la barrière hémato-encéphalique [A29]
Taille de la pièce et quantité de gouttelettes
Formule de base
La quantité de gouttes doit être adaptée à la taille de la pièce afin d'atteindre une concentration thérapeutiquement efficace, mais pas excessive.
Tableau 3 : Recommandations de dosage par taille de pièce
*Hypothèse : Hauteur sous plafond de 2,5 m **Concentration estimée basée sur ~1 mg d'huile essentielle par goutte et une nébulisation complète
Base de calcul
– 1 goutte d’huile essentielle ≈ 0,05 ml ≈ 40–50 mg (selon la densité)
– Concentration cible : 80–200 µg/m³ (basé sur des études d'aromathérapie ambiante)
– Formel : Goutte = (Volume d'espace × Concentration cible) / (Masse par goutte × 1000)
Durée d'utilisation et pauses
Durée de la session
- Application aiguë
15–30 minutes par séance
- Diffusion continue en arrière-plan
30 à 60 minutes avec pauses
Intervalle de pause
L'adaptation olfactive (accoutumance) survient après 15 à 30 minutes d'exposition continue.
Pour maintenir les effets thérapeutiques, des intervalles de pause sont recommandés :
Tableau 4 : Calendrier d'utilisation et de pause
Adaptation olfactive
Après 20 à 30 minutes d'exposition continue, la perception consciente de l'odeur diminue, mais les effets neurobiologiques peuvent persister.
Des pauses de 30 à 60 minutes permettent une resensibilisation des récepteurs olfactifs.
Heures de la journée et scénarios d'application
La sélection des huiles essentielles doit être adaptée à l'heure de la journée et aux symptômes spécifiques du TDAH :
Tableau 5 : Sélection de l'huile par moment de la journée
Scénarios d'application :
- Schulvorbereitung/Morgenroutine
– Huile : Romarin ou menthe poivrée
– Objectif : Activation, vigilance, concentration Dosage : 6 à 8 gouttes pendant 20 minutes
– Heure : 30 à 60 minutes avant le début de l'école - Devoirs / Phases d'étude
– Huile : Menthe poivrée (attention soutenue) ou romarin (mémoire)
– Objectif : Concentration, mémoire de travail Dosage : 6 à 8 gouttes pendant 30 minutes, puis 30 minutes de pause
– Moment : Pendant les devoirs ou les séances d'étude - Gestion de l'hyperactivité :
– Huile : Lavande ou Vétiver
– Objectif : Apaisement, réduction de l'agitation motrice. Posologie : 5 à 7 gouttes pendant 30 minutes.
– Moment de l'administration : En cas d'hyperactivité ou d'agitation aiguë - Hygiène du sommeil :
– Huile : Lavande
– Objectif : Induction du sommeil, réduction des difficultés d'endormissement (fréquent dans le TDAH) Dosage : 4–6 gouttes pendant 15 minutes
– Horaire : 30 à 60 minutes avant le coucher
Dosages spécifiques à l'huile
Tableau 6 : Recommandations de dosage spécifiques à l'huile
Mélanges (Blends) : La combinaison de plusieurs huiles peut produire des effets synergiques :
- Mélange de mise au point (matin)
3 gouttes de romarin + 3 gouttes de menthe poivrée + 2 gouttes de cannelle - Mélange apaisant (soir)
4 gouttes de lavande + 3 gouttes de vétiver + 2 gouttes de cèdre - Balance-Mélange (Après-midi)
3 gouttes de menthe poivrée + 3 gouttes de lavande + 2 gouttes de poivre noir
Important
Maintenir la goutte totale dans la fourchette recommandée (6 à 8 gouttes pour 20 m²).
Consignes de sécurité et contre-indications
Sécurité générale pour l'inhalation
Principes fondamentaux
pureté
Utiliser exclusivement des huiles essentielles certifiées GC/MS, 100% pures, sans additifs.
Dilution
En cas d'application par inhalation via diffuseur, aucune dilution supplémentaire n'est nécessaire ; en cas d'application topique, toujours diluer dans une huile porteuse (1–3%)
ventilation
L'espace ne doit pas être complètement fermé ; assurer un apport régulier d'air frais
Tolérance individuelle
Commencer avec des doses faibles et augmenter progressivement
Effets secondaires fréquents (légers)
– Maux de tête dus à une concentration excessive ou à une exposition prolongée
– Irritation des muqueuses (nez, gorge) chez les personnes sensibles
– Nausées avec des senteurs très intenses (par ex. cannelle, poivre noir)
– Réactions allergiques (rares, <1% de la population)
Mesures en cas d'effets secondaires
– Éteindre immédiatement le diffuseur et aérer la pièce
– En cas de maux de tête : Air frais, hydratation
– En cas d'irritation des muqueuses : arrêter l'inhalation, éventuellement inhaler une solution saline
– En cas de réaction allergique : cesser l’exposition, éventuellement prendre un antihistaminique, en cas de réactions graves consulter un médecin
Considérations spécifiques au TDAH
Vulnérabilités particulières chez les patients atteints de TDAH :
Hypersensibilité sensorielle
40–60% des patients atteints de TDAH présentent des troubles du traitement sensoriel. Les odeurs intenses peuvent être perçues comme désagréables ou accablantes.
- Recommandation
Commencer à des doses très faibles (50% de la dose standard), augmenter progressivement
Troubles d'anxiété comorbides
25 à 40 %% des patients atteints de TDAH présentent des troubles anxieux comorbides.
Les huiles activantes (romarin, menthe poivrée) pourraient renforcer l'anxiété.
- Recommandation
En cas d'anxiété comorbide, utiliser principalement des huiles anxiolytiques (lavande, vétiver)
Troubles du sommeil
50–70% der ADHD-Patienten haben Schlafprobleme. Aktivierende Öle am Abend können Schlaf weiter beeinträchtigen.
- Recommandation
Séparation stricte : huiles stimulantes le matin/l'après-midi, huiles sédatives le soir
Impulsivité
Les patients atteints de TDAH pourraient avoir tendance à utiliser des doses trop élevées.
- Recommandation
Instructions de dosage claires, avec supervision parentale/par un tuteur si nécessaire
Interactions avec le méthylphénidate
Interactions théoriques :
Renforcement dopaminergique (cannelle)
– Les métabolites de la cannelle peuvent être convertis en amphétamine [A2]
Risque théorique des effets dopaminergiques additifs avec le méthylphénidate
- Recommandation
Utiliser la cannelle uniquement à faibles doses, surveiller attentivement les signes de surstimulation (tachycardie, agitation, insomnie)
Modulation sérotoninergique (Lavande)
Le linalol se lie au SERT [A23]
Lors de la prise simultanée d'ISRS (fréquents en cas de dépression/anxiété comorbide), risque théorique de syndrome sérotoninergique
- Recommandation
Avec une médication combinée par ISRS, la lavande uniquement à doses modérées, surveillance des symptômes du syndrome sérotoninergique (agitation, confusion, tachycardie, hyperthermie).
Sédation (lavande, vétiver)
Les huiles sédatives pourraient réduire la vigilance
Contraire à l'effet stimulant du méthylphénidate
- Recommandation
Utiliser les huiles sédatives de préférence le soir, pas pendant les heures de cours ou lors d'activités nécessitant de la concentration.
- Aucune interaction pharmacocinétique connue
Les huiles essentielles sont principalement métabolisées par le CYP2D6, le CYP3A4
Le méthylphénidate est métabolisé par la carboxylesterase 1 (CES1)
Absence de chevauchement des voies métaboliques, par conséquent pas d'interactions pharmacocinétiques attendues
Important
Malgré l'absence d'interactions documentées, l'association du méthylphénidate avec des huiles essentielles doit se faire sous surveillance médicale, surtout en début de traitement.
Contre-indications et précautions
Contre-indications absolues
– Allergie connue à des huiles essentielles spécifiques ou à leurs composants
– Asthme bronchique sévère (risque de bronchospasme)
– Nourrissons < 6 mois (risque de laryngospasme, surtout avec le menthol)
Contre-indications relatives (prudence requise)
– Épilepsie : Attention au romarin et à la cannelle (camphre, aldéhyde cinnamique peuvent abaisser le seuil épileptogène)
– Grossesse/Allaitement : De nombreuses huiles essentielles n’ont pas fait l’objet d’études suffisantes pendant la grossesse/l’allaitement
– Asthme (léger à modéré) : Doses faibles, surveillance étroite des symptômes respiratoires
– Jeunes enfants (6 mois – 3 ans) : Doses réduites (25–50% de la dose adulte)
Ajustements de dose en fonction de l'âge :
Critères de qualité pour les huiles essentielles
- Certificat GC/MS :
Chaque lot doit être analysé par chromatographie en phase gazeuse/spectrométrie de masse - Nom botanique
La désignation latine doit être indiquée (par exemple, Lavandula angustifolia, pas seulement “ Lavande ”) - Chimiotype
Pour les huiles avec différents chémotypes (par exemple, le romarin), celui-ci doit être spécifié - Origine
Pays d'origine et méthode d'extraction (distillation, pression à froid) doivent être documentés - Aucun additif
100% rein, sans parfums synthétiques, huiles porteuses ou conservateurs
Stockage et durée de conservation
– Conserver à l'abri de la lumière et au frais (15–20°C)
– Protéger de la lumière (bouteilles en verre brun ou bleu)
– À consommer dans les 6 à 12 mois après ouverture (oxydation)
– Les huiles d’agrumes ont une durée de conservation plus courte (6 mois), les résines plus longue (2 à 3 ans)
Discussion et implications cliniques
Lacunes de preuves et besoins de recherche
Évaluation critique des données probantes :
La présente analyse montre une Discrépance considérable entre la plausibilité mécaniste et l'évidence clinique pour les huiles essentielles comme traitement adjuvant du TDAH.
Points forts des preuves disponibles
- Données mécaniques robustes
Les études de liaison aux récepteurs, les analyses des voies de signalisation et les modèles précliniques révèlent des effets neurobiologiques clairs des composants des huiles essentielles [A19], [A20], [A21], [A23] - Effets cognitifs chez les personnes saines
Des études contrôlées chez des adultes en bonne santé démontrent des effets mesurables sur l'attention (menthe poivrée, n=24) [A19] et mémoire (Romarin, n=144) [A27] - Mécanismes d'action complémentaires
Les cibles moléculaires des huiles essentielles (GABA-A, CB2, canaux TRP, SERT) diffèrent de celles du méthylphénidate (DAT/NET), suggérant des potentiels synergiques
Faiblesses et lacunes en matière de preuves
- Essais contrôlés randomisés spécifiques au TDAH manquants : À l'exception de l'étude de Chen sur la cannelle [A2] Les études randomisées contrôlées par placebo chez les patients atteints de TDAH n'existent pas
- Limitations méthodologiques : Les études existantes ont de petits échantillons (n=24–144), de courtes périodes d'observation (séances uniques) et manquent souvent de l'aveuglement.
- Aucune donnée à long terme : Les effets et la sécurité d'une utilisation chronique (> 6 mois) n'ont pas été étudiés
- Études de recherche de dose manquantes : Les doses, concentrations et schémas d'administration optimaux pour le TDAH ne sont pas établis.
- Aucune étude de combinaison : Les interactions et les effets synergiques avec le méthylphénidate n'ont pas été étudiés de manière systématique
Lacunes de recherche spécifiques :
Mise en œuvre pratique
Recommandations pour la pratique clinique :
Bien que des lacunes dans les preuves existent, une thérapie adjuvante avec des huiles essentielles peut être envisagée chez les patients atteints de TDAH dans les conditions suivantes :
1. Indication claire
- Symptômes résiduels sous traitement optimisé à la méthylphénidate
- Souhait du patient, de la famille pour des approches complémentaires
- Symptômes spécifiques qui peuvent être traités par les huiles essentielles
(Troubles du sommeil → Lavande; Problèmes de mémoire → Romarin)
2. Approche structurée
- Évaluation de référence
Documentation des symptômes du TDAH avec des échelles validées (SNAP-IV, Conners, ADHS-SB) - Phase d'introduction
Commencer avec une dose unique d'huile à faible dose (50% de la dose standard) pendant 2 semaines - Surveillance
Suivi hebdomadaire des symptômes, surveillance des effets secondaires - Titrage
Augmentation progressive de la dose en cas de bonne tolérance - Évaluation
Après 4 à 6 semaines d'évaluation de l'efficacité ; en l'absence de bénéfice, arrêt.
3. Documentation
- Tenir un “ journal d'aromathérapie ” avec huile, dosage, moment, symptômes, effets secondaires
- Consultation régulière avec le médecin traitant
4. Attentes réalistes
- Les huiles essentielles sont aucun remplacement pour des thérapies du TDAH fondées sur des preuves (méthylphénidate, thérapie comportementale)
- Taille d'effet attendue : petite à modérée (d de Cohen : 0,2–0,5)
- Bénéfice principal : Amélioration des symptômes spécifiques (sommeil, anxiété, humeur), pas des symptômes centraux
Limitations
Limites de cette analyse :
- Preuve indirecte
La plupart des conclusions sont basées sur l'extrapolation d'études menées sur des adultes en bonne santé aux patients atteints de TDAH. - Biais de publication
Les études positives sont plus susceptibles d'être publiées ; les études négatives sur les huiles essentielles pourraient être sous-représentées - Hétérogénéité
Différentes huiles, dosages, voies d'administration et mesures de résultats rendent difficiles les méta-analyses. - Plasma/mireur cérébral manquant
Il n'existe pas de données sur les concentrations plasmatiques ou cérébrales des composants d'huiles essentielles après inhalation chez l'homme. - Incertitude mécaniste
Les mécanismes exacts par lesquels les huiles essentielles inhalées exercent leurs effets sur le système nerveux central (olfactif ou systémique) ne sont pas encore complètement élucidés.
Limitations des recommandations de dosage
– Basé sur l'extrapolation de quelques études et l'application traditionnelle
– Variabilité individuelle (ventilation spatiale, fréquence respiratoire, métabolisme) non prise en compte
– Aucune donnée pharmacocinétique sur la relation dose-concentration
Conclusion
Cette analyse approfondie intègre des données provenant de 87 études sur les concentrations intracérébrales de méthylphénidate et de 159 publications sur les huiles essentielles dans le contexte du TDAH. Les principales conclusions peuvent être résumées comme suit :
Concentrations cérébrales de méthylphénidate
Les doses thérapeutiques orales de méthylphénidate (0,25–0,6 mg/kg) produisent une occupation du DAT de >50ns le striatum, la relation dose-effet étant bien caractérisée (20 mg → 54%, 40 mg → 72% de blocage du DAT). [A9].
L'absorption cérébrale maximale survient 60 à 90 minutes après administration orale. [A7], [A9].
Les concentrations plasmatiques dans la plage thérapeutique sont de 3,5 à 7,8 ng/ml (adultes), 6 ng/ml étant associés à 50% de blocage DAT [A9], [A17].
Lacune critique de preuves
Des mesures directes des concentrations de méthylphénidate dans le tissu cérébral (ng/ml) ou le liquide céphalo-rachidien n'existent pas ; toutes les données sont basées sur des mesures d'occupation par TEP/SPECT.
Thérapie adjuvante avec des huiles essentielles
Une thérapie adjuvante avec des huiles essentielles est Mécanistiquement plausible basé sur des mécanismes d'action complémentaires.
Le linalool module les systèmes sérotoninergique, dopaminergique et noradrénergique [A21], [A23];
– Le menthol active les canaux TRPM8 et les récepteurs GABA-A [A19];
– Le β-Caryophyllène agit comme un agoniste CB2 aux propriétés anti-inflammatoires [A14];
– Le 1,8-cinéole améliore les fonctions cognitives [A27].
Ces mécanismes sont complémentaires au blocage des transporteurs DAT/NET par le méthylphénidate et pourraient produire des effets synergiques.
Cependant : Les preuves cliniques chez les patients atteints de TDAH sont faibles ; les essais contrôlés randomisés font largement défaut.
Huiles et ingrédients actifs spécifiques
- Menthe poivrée (Menthol)
La preuve la plus solide d'amélioration de l'attention soutenue (n=24 ECR) [A19] - Romarin (1,8-Cinéole)
Amélioration de la mémoire (n=144) [A27] - Lavande (Linalol)
Anxiolyse, amélioration du sommeil, mais altération de la mémoire de travail [A27], [A23] - Poivre noir (β-caryophyllène)
Anti-inflammatoire, effets anxiolytiques précliniques [A14] - Vétiver, Cèdre
Preuves faibles, application traditionnelle principalement [A3], [A4], [A29] - Cannelle (aldéhyde cinnamique)
La seule étude clinique spécifique à la TDAH, mais avec des limitations méthodologiques [A2]
Recommandations de dosage pour l'Organik Aromas Nebulizer 3.0
Des recommandations de dosage basées sur des preuves ont été développées, adaptées à la taille de la pièce (3 à 18 gouttes pour 10 à 60 m²), à l'heure de la journée (huiles activatrices le matin, sédatives le soir) et aux symptômes spécifiques.
Durée d'application : 15 à 30 minutes par séance avec des pauses de 30 à 60 minutes pour éviter l'adaptation olfactive.
Important : Ces recommandations sont basées sur une extrapolation à partir de quelques études et nécessitent une adaptation individuelle.
Consignes de sécurité
Les huiles essentielles sont généralement sûres lorsqu'elles sont utilisées par inhalation aux doses recommandées.
Des précautions spécifiques pour les patients atteints de TDAH comprennent :
- Prendre en compte l'hypersensibilité sensorielle (% des patients TDAH)
- Éviter les huiles stimulantes en cas d'anxiété comorbide
- séparation stricte des huiles activatrices (le matin) et sédatives (le soir)
- Les interactions théoriques avec le méthylphénidate (renforcement dopaminergique par la cannelle, modulation sérotoninergique par la lavande) nécessitent une surveillance.
- Contre-indications absolues
– allergie connue
asthme sévère
– Nourrissons <6 mois
Évaluation finale
Les huiles essentielles représentent une prometteur mais insuffisamment validé agent thérapeutique d'appoint dans le TDAH. La plausibilité mécanistique est forte, mais les preuves cliniques sont faibles.
Une application peut être envisagée chez les patients/familles informés sous surveillance médicale, mais devrait jamais thérapies fondées sur des preuves.
Besoin urgent de recherche données à long terme sur la sécurité et les études de combinaison avec le méthylphénidate pour les études randomisées contrôlées par placebo chez les patients atteints de TDAH.
Syndrome d'Asperger
Bases neurobiologiques des TSA, terpènes comme modulateurs CB2/GABA-A/Nrf2, preuves cliniques et dosage avec le nébuliseur Organik Aromas 3.0
Introduction
Le trouble du spectre de l'autisme (TSA) représente l'un des troubles neurodéveloppementaux les plus courants, avec une prévalence mondiale estimée de 1 à 2 % et une augmentation des taux de diagnostic au cours des deux dernières décennies. [B1], [B2].
Les TSA se caractérisent par une hétérogénéité clinique et neurobiologique marquée, qui se manifeste par un large éventail d'expressions symptomatiques, allant des individus à haut fonctionnement avec des déficits isolés de communication sociale aux personnes présentant des déficiences intellectuelles sévères et des comorbidités neurologiques. [B3], [B4].
Selon le DSM-5, la symptomatologie principale comprend deux domaines majeurs : des déficits persistants dans la communication et les interactions sociales, et des comportements, intérêts ou activités restreints et répétitifs. [B5]. De plus, jusqu'à 90 % des personnes touchées présentent des troubles du traitement sensoriel, qui se manifestent par une hyper- ou une hyposensibilité aux stimuli sensoriels. [B6], [B7].
Des symptômes comorbides tels que les troubles anxieux (40–50 %), les troubles du sommeil (50 à 80 %), le trouble du déficit de l'attention avec ou sans hyperactivité (30 à 50 %) et les troubles gastro-intestinaux (30 à 70 %) altèrent considérablement la qualité de vie. [B8], [B9], [B10].
Hétérogénéité neurobiologique et convergence pathophysiologique
L'hétérogénéité étiologique des TSA comprend des facteurs génétiques (héritabilité de 70 à 90 %), des mutations de novo dans des gènes synaptiques (SHANK3, NLGN3/4, NRXN1), des variations du nombre de copies, des modifications épigénétiques et des facteurs environnementaux prénataux [B11], [B12], [B13].
Malgré cette diversité, les mécanismes physiopathologiques convergent vers des voies neurobiologiques communes : déséquilibre excitateur-inhibiteur (E/I) perturbé, dysfonctionnement synaptique, neuroinflammation, stress oxydatif et altérations de l'axe intestin-cerveau. [B14], [B15], [B16].
L'hypothèse du déséquilibre E/I postule qu'un déséquilibre entre la neurotransmission excitatrice (glutamatergique) et inhibitrice (GABAergique) explique les symptômes centraux des TSA. [B17], [B18].
Les études d'imagerie et les analyses post-mortem montrent des altérations régionales des concentrations de GABA et de glutamate, une expression modifiée des récepteurs GABA-A et NMDA, ainsi que des dysfonctionnements des interneurones GABAergiques. [B19], [B20], [B21].
Ce déséquilibre touche particulièrement le cortex préfrontal (fonctions exécutives, cognition sociale), l'amygdale (traitement émotionnel, perception sociale), le cervelet (intégration sensori-motrice, processus cognitifs) et l'hippocampe (mémoire, traitement contextuel) [B22], [B23], [B24].
La neuroinflammation représente un autre mécanisme convergent : les études post-mortem montrent une activation des microglies et des astrocytes dans les cerveaux atteints de TSA, des modèles précliniques (par ex. activation immunitaire maternelle, TSA induit par l'acide valproïque) démontrent une augmentation des cytokines pro-inflammatoires (TNF-α, IL-6, IL-1β) et un développement synaptique perturbé par la neuroinflammation chronique. [B25], [B26], [B27].
Le stress oxydatif avec une augmentation des espèces réactives de l'oxygène (ROS), une réduction du glutathion (GSH) et une dysfonction mitochondriale a été démontré dans de multiples cohortes de TSA. [B28], [B29].
L'axe intestin-cerveau joue un rôle de plus en plus reconnu : les patients atteints de TSA montrent souvent une dysbiose avec des rapports Firmicutes/Bactéroïdètes modifiés, une diversité microbienne réduite et une production perturbée de précurseurs de neurotransmetteurs (tryptophane, GABA). [B30], [B31]. Les études précliniques démontrent que la transplantation de microbiote fécal améliore les comportements similaires à ceux de l'autisme dans des modèles murins et module les voies de signalisation sérotoninergique et glutamatergique. [B32], [B33].
Besoin de thérapies adjuvantes
Malgré des recherches intensives, il n'existe pas de traitements curatifs pour les symptômes de base des TSA. Les interventions fondées sur des données probantes comprennent des approches comportementales (Applied Behavior Analysis, Early Start Denver Model) et une pharmacothérapie symptomatique. [B34], [B35]. La rispéridone et l'aripiprazole sont les seuls médicaments approuvés par la FDA pour les TSA, mais uniquement pour l'irritabilité et les comportements agressifs, pas pour les symptômes principaux. [B36], [B37]. Ces antipsychotiques sont associés à des effets secondaires importants (prise de poids, syndrome métabolique, symptômes extrapyramidaux) [B38].
Les symptômes comorbides tels que l'anxiété, les troubles du sommeil et la régulation sensorielle sont souvent traités avec des benzodiazépines, de la mélatonine ou des antidépresseurs, bien que les preuves de leur efficacité et de leur sécurité dans les populations atteintes de TSA soient limitées. [B39], [B40]. Ce manque de thérapies sûres et efficaces pour les symptômes comorbides et le fardeau de la polypharmacie motivent la recherche d'interventions adjuvantes à faible effet secondaire. [B41].
Les huiles essentielles et leurs principaux composants (terpènes) représentent une option thérapeutique adjuvante potentielle, basée sur :
- données précliniques sur la modulation GABAergique, la régulation sérotoninergique, les effets anti-neuroinflammatoires et antioxydants ;
- application traditionnelle en aromathérapie pour l'anxiété, le sommeil et l'humeur ;
- profils de sécurité peu coûteux en cas d'utilisation adéquate [B42], [B43], [B44].
Neurobiologie du trouble du spectre autistique
Ce rapport analyse les bases neurobiologiques des TSA, les mécanismes d'action moléculaires des terpènes pertinents, les preuves cliniques dans les populations atteintes de TSA et élabore des recommandations basées sur des preuves concernant le dosage et la sécurité pour l'utilisation d'huiles essentielles dans le cadre d'une approche thérapeutique multimodale.
Déséquilibre GABA/Glutamate E/I
L'hypothèse du déséquilibre E/I est l'un des concepts neurobiologiques les plus robustes dans la recherche sur les TSA. [B17], [B18]. Le glutamate, le principal neurotransmetteur excitateur, et le GABA (acide γ-aminobutyrique), le principal neurotransmetteur inhibiteur, régulent l'excitabilité neuronale, la plasticité synaptique et la dynamique du réseau. Un déséquilibre en faveur de la transmission excitatrice (ratio E/I accru) ou un contrôle inhibiteur défectueux peut entraîner une hyperexcitabilité, une altération du filtrage sensoriel et une perturbation du traitement de l'information sociale. [B45], [B46].
Les études de spectroscopie par résonance magnétique (SRM) montrent des altérations régionales : des concentrations réduites de glutamate striatal, des niveaux accrus de GABA préfrontal dans certaines études et des rapports glutamate/GABA modifiés dans les cortèges sensoriels et associatifs. [B19], [B20].
Les analyses post-mortem démontrent une expression réduite de GAD65 et GAD67 (enzymes synthétisant le GABA) dans le cortex préfrontal et le cervelet, ainsi qu'une densité modifiée d'interneurones GABAergiques (en particulier les interneurones positifs à la parvalbumine). [B47], [B48].
La perspective du développement est critique : le GABA agit de manière excitatrice pendant les premières phases de développement en raison de concentrations intracellulaires élevées de chlorure (médiées par le cotransporteur NKCC1) et passe à une action inhibitrice après la naissance grâce à l'expression du cotransporteur KCC2. [B49].
Un déséquilibre ou une altération de l'interrupteur GABA a été observé dans des modèles murins de TSA et corrigé par la bumétanide (inhibiteur de NKCC1), entraînant une amélioration du comportement social. [B50], [B51].
Une étude clinique de la bumétanide chez des enfants atteints de TSA a montré des améliorations modérées de la communication sociale, mais avec des limites méthodologiques. [B52].
La dysfonction glutamatergique se manifeste par des modifications de l'expression des sous-unités des récepteurs NMDA et AMPA, une perturbation de la plasticité synaptique (potentiation/dépression à long terme) et une transmission glutamatergique excessive dans des circuits spécifiques. [B53], [B54].
Des études génétiques ont identifié des mutations associées aux TSC dans des gènes des synapses glutamatergiques (GRIN2B, GRIA1, SLC1A1). [B55].
Les modèles précliniques montrent que la modulation de la transmission glutamatergique (par exemple, par des antagonistes des mGluR5) peut améliorer les comportements similaires à ceux de l'autisme. [B56].
Sérotonine, Dopamine et Ocytocine
Les systèmes monoaminergiques jouent des rôles centraux dans la cognition sociale, le traitement de la récompense et la régulation émotionnelle – des domaines qui sont altérés dans le TSA. [B57], [B58].
Sérotonine (5-HT)
L'hypersérotoninémie (taux périphériques de sérotonine élevés) a été détectée chez 25 à 50 % des patients atteints de TSA, la relation avec les taux centraux de 5-HT restant floue. [B59], [B60]. Les études d'imagerie montrent une capacité réduite de synthèse de la sérotonine dans le cortex frontal et le thalamus chez les enfants autistes. [B61]. Les variantes génétiques du transporteur de la sérotonine (5-HTTLPR) et de la tryptophane hydroxylase-2 (TPH2) sont associées au risque de TSA. [B62]. Les études précliniques démontrent qu'une dysfonction sérotoninergique pendant des fenêtres de développement critiques entraîne des phénotypes similaires à ceux de l'autisme. [B63]. Les inhibiteurs sélectifs de la recapture de la sérotonine (ISRS) montrent des résultats mitigés dans l'autisme : aucune efficacité sur les symptômes centraux, effets modérés sur les comportements répétitifs et l'anxiété. [B64].
Dopamine (DA)
Les circuits dopaminergiques mésolimbique et mésocortical médiatisent le traitement de la récompense, la motivation et le renforcement social. [B65]. Les patients atteints de TSA montrent une activation réduite du striatum ventral pour les récompenses sociales (visages, interaction sociale) par rapport aux récompenses non sociales. [B66], [B67]. Les études TEP rapportent une densité accrue des transporteurs de dopamine dans le striatum et une disponibilité réduite des récepteurs D2. [B68]. Des études génétiques ont identifié des variantes associées aux TSA dans des gènes dopaminergiques (DRD1, DRD2, DAT1). [B69]. Les modèles précliniques montrent que la dysfonction dopaminergique entraîne une préférence sociale altérée et des comportements répétitifs. [B70].
Ocytocine (OT)
L'ocytocine est un neuropeptide jouant un rôle central dans le lien social, la confiance, la cognition sociale et la régulation du stress [B71]. Les patients atteints de TSA présentent des niveaux réduits d'ocytocine plasmatique, une expression modifiée du récepteur de l'ocytocine (OXTR) et des variantes génétiques dans OXTR et CD38 (libération d'ocytocine). [B72], [B73]. L'ocytocine intranasale a amélioré la cognition sociale et le contact visuel chez les adultes atteints de TSA dans certaines études, mais avec des résultats incohérents et une absence d'efficacité dans les cohortes pédiatriques. [B74], [B75]. Des études précliniques montrent que l'ocytocine régule le développement GABAergique : l'administration d'ocytocine pendant des périodes critiques a corrigé le retard du changement GABAergique et a amélioré le comportement social chez des modèles murins de TSA. [B50], [B76]. Ces découvertes lient les systèmes oxytonergiques et GABAergiques sur le plan mécanistique.
Neuroinflammation – Microglie, TNF-α et cytokines
La neuroinflammation chronique est un mécanisme physiopathologique convergent dans les TSA, étayé par des études post-mortem, d'imagerie et de biomarqueurs [B77], [B78].
Activation de la microglie
La microglie sont des cellules immunitaires résidentes du SNC qui régulent l'élagage synaptique, le développement neuronal et la surveillance immunitaire. [B79]. Des études post-mortem montrent une activation des microglies (expression accrue de l'Iba1, morphologie amiboïde) dans le cortex préfrontal, le cervelet et la substance blanche des cerveaux atteints de TSA. [B80], [B81]. L'imagerie TEP avec des ligands du protéine translocatrice (TSPO) a démontré une activation microgliale accrue dans de multiples régions du cerveau chez des patients atteints de TSA vivants. [B82]. Les microglies activées libèrent des cytokines pro-inflammatoires, produisent des espèces réactives de l'oxygène et peuvent phagocyter les structures synaptiques, conduisant à une connectivité perturbée. [B83].
Cytokines pro-inflammatoires
Des taux élevés de TNF-α, d'IL-6, d'IL-1β et d'IFN-γ ont été détectés dans le plasma, le liquide céphalorachidien et le tissu cérébral post-mortem de patients atteints de TSA. [B84], [B85]. Les modèles d'activation immunitaire maternelle (AIM), où des souris gestantes sont traitées avec du Poly(I:C) ou du LPS, produisent une progéniture présentant des comportements similaires à ceux des TSA et des niveaux élevés de TNF-α. [B86], [B87]. Le TNF-α module la transmission synaptique, réduit l'inhibition GABAergique et altère la plasticité synaptique [B88]. Le blocage du TNF-α dans des modèles de MIA a empêché les phénotypes similaires à l'autisme [B89].
Dysfonctionnement des astrocytes
Les astrocytes régulent l'homéostasie du glutamate (via les transporteurs de glutamate EAAT1/2), la mise en tampon du K+ et le soutien métabolique des neurones [B90]. Les études post-mortem montrent une astrogliose (expression accrue de GFAP) dans les cerveaux atteints de TSA. [B91]. Les astrocytes dysfonctionnels peuvent contribuer à une accumulation excessive de glutamate extracellulaire et à une excitotoxicité. [B92].
Stress oxydatif et dysfonctionnement mitochondrial
Le stress oxydatif résulte d'un déséquilibre entre la production de ROS et la défense antioxydante [B93]. Plusieurs études rapportent des marqueurs de stress oxydatif accrus dans les TSA : augmentation de la peroxydation lipidique (malondialdéhyde), de la carbonylation des protéines, de l'oxydation de l'ADN (8-OHdG) et diminution de la capacité antioxydante (glutathion, superoxyde dismutase, catalase). [B28], [B94], [B95].
Dépistage de glutathion
Le glutathion (GSH) est l'antioxydant intracellulaire principal. Les patients atteints de TSA présentent des taux réduits de GSH dans le plasma et le cerveau, une augmentation du glutathion oxydé (GSSG) et un rapport GSH/GSSG réduit. [B96], [B97]. Des variantes génétiques dans les enzymes de synthèse du glutathion (GCLC, GSS) sont associées au risque de TSA [B98].
Dysfonctionnement mitochondrial
5 à 30 % des patients atteints d'ASD présentent des preuves biochimiques de dysfonctionnement mitochondrial (augmentation du lactate, diminution de l'activité de la chaîne respiratoire) % [B99], [B100]. Les mitochondries sont la principale source de ROS ; la dysfonction mitochondriale entraîne une augmentation de la production de ROS, une réduction de la synthèse d'ATP et une perturbation de l'homéostasie du calcium. [B101]. Les études précliniques démontrent que les antioxydants mitochondriaux (MitoQ) améliorent les comportements similaires à l'ASD dans des modèles murins. [B102].
Voie Nrf2/HO-1
Le facteur 2 apparenté au facteur nucléaire érythroïde 2 (Nrf2) est un régulateur principal de la réponse antioxydante qui induit l'expression de l'hème oxygénase-1 (HO-1), de la NAD(P)H:quinone oxydoréductase-1 (NQO1), des glutathion S-transférases et d'autres enzymes antioxydantes. [B103]. Une activité réduite de Nrf2 a été démontrée dans des modèles de TSA ; les activateurs de Nrf2 (sulforaphane) ont montré des améliorations du comportement social et de la communication chez les individus atteints de TSA dans de petites études cliniques. [B104], [B105].
Axe intestin-cerveau
La communication bidirectionnelle entre le tractus gastro-intestinal et le système nerveux central s'effectue par des voies neuronales (nerf vague), endocriniennes (axe hypothalamo-hypophyso-surrénalien), immunitaires et métaboliques. [B106]. Les patients atteints de TSA présentent une prévalence élevée de symptômes gastro-intestinaux (constipation, diarrhée, douleurs abdominales) et de dysbiose. [B107], [B108].
Altérations du microbiote
Les méta-analyses montrent une diversité microbienne réduite, des rapports Firmicutes/Bacteroidetes augmentés, des Bifidobacterium et Prevotella réduits, et des Clostridium et Desulfovibrio augmentés chez les personnes atteintes de TSA. [B109], [B110]. Ces changements sont corrélés à la gravité des symptômes [B111].
Connexions mécanistes
Le microbiote intestinal produit des précurseurs de neurotransmetteurs (tryptophane → sérotonine, glutamate → GABA), des acides gras à chaîne courte (butyrate, propionate, acétate) et module la fonction immunitaire [B112]. L'exposition au propionate induit des comportements similaires à ceux de l'autisme chez les modèles de rongeurs [B113]. La transplantation de microbiote fécal (TMF) provenant de patients atteints de TSA chez des souris sans germes a transmis des comportements similaires aux TSA et modifié l'expression génique du cerveau (gènes de la synapse sérotoninergique, glutamatergique). [B32]. Le FMT de donneurs sains chez des modèles murins d'autisme a amélioré le comportement social et normalisé les taux de neurotransmetteurs [B114].
Médiation vagale
Le nerf vague transmet des signaux de l'intestin au tronc cérébral (noyau du tractus solitaire) et ensuite aux régions limbiques et corticales. [B115]. Des études précliniques montrent que l'électroacupuncture a amélioré les comportements de type TSA dans des modèles murins de VPA par des mécanismes dépendants du nerf vague et par la modulation du microbiome ; la vagotomie a annulé ces effets. [B116].
Dysfonctionnement synaptique – Neuroligines, protéines SHANK
Le dysfonctionnement synaptique est un concept pathophysiologique central de l'autisme, étayé par des preuves génétiques, moléculaires et électrophysiologiques. [B117], [B118].
Complexe Néuréguline-Neurexine
Les neuroligines (NLGN1-4) sont des molécules d'adhésion cellulaire postsynaptiques qui interagissent avec les neurexines présynaptiques (NRXN1-3) et régulent la différenciation, la maturation et la fonction synaptiques. [B119]. Des mutations dans NLGN3 et NLGN4X ont été identifiées chez des patients atteints de TSA [B120]. NLGN3-R451C-Knockin-Mäuse zeigen eine erhöhte inhibitorische Übertragung, gestörte soziale Interaktion und repetitive Verhaltensweisen [B121]. Souris knock-out pour NLGN4 présentent une transmission excitatrice réduite et des phénotypes similaires à ceux de l'autisme [B122].
Protéine SHANK
SHANK1-3 sont des protéines de squelette postsynaptique qui organisent les récepteurs du glutamate, le cytosquelette d'actine et les molécules de signalisation. [B123]. Les mutations de SHANK3 sont associées au syndrome de Phelan-McDermid (délétion 22q13), caractérisé par des TSA, une déficience intellectuelle et un déficit du langage. [B124]. Les souris SHANK3-Knockout présentent une densité réduite d'épines dendritiques, une transmission synaptique perturbée et des comportements similaires à ceux de l'autisme. [B125]. Des mutations de SHANK2 sont également associées aux TSA ; les souris SHANK2 invalidées présentent une hyperactivité, des comportements répétitifs et une fonction altérée des récepteurs NMDA [B126].
Plasticité synaptique
La potentialisation à long terme (LTP) et la dépression à long terme (LTD), corrélats cellulaires de l'apprentissage et de la mémoire, sont altérées dans plusieurs modèles murins de TSA. [B127]. Un déséquilibre modifié de la LTP/LTD peut contribuer à une maturation perturbée des circuits dépendante de l'expérience et à une altération de l'apprentissage social. [B128].
Régions cérébrales touchées
L'imagerie structurelle et fonctionnelle identifie des altérations constantes dans des régions cérébrales spécifiques chez les personnes atteintes de TSA [B129], [B130].
Cortex préfrontal (CPF)
Le cortex préfrontal (CPF) médiatise les fonctions exécutives, la mémoire de travail, la flexibilité cognitive et la cognition sociale. [B131]. Les patients atteints de TSA présentent une activation réduite du cortex préfrontal (CPF) lors des tâches de théorie de l'esprit, une connectivité PFC perturbée avec les régions postérieures et une microstructure PFC modifiée. [B132], [B133]. Les études post-mortem montrent une densité neuronale accrue, une largeur de mini-colonnes réduite et des déficits GABAergiques dans le PFC [B134].
Amygdale
L'amygdale est centrale pour le traitement émotionnel, la perception sociale et la conditionnement à la peur. [B135]. Les enfants autistes présentent une hypertrophie précoce de l'amygdale (2-4 ans), suivie d'une normalisation ou d'une réduction de volume à l'adolescence. [B136]. Des études fonctionnelles montrent une réduction de l'activation de l'amygdale lors du traitement des visages et une connectivité amygdale-cortex préfrontal altérée. [B137], [B138].
Cervelet
Traditionnellement associé au contrôle moteur, le cervelet joue également un rôle dans les processus cognitifs, la prédiction sensorielle et l'apprentissage social. [B139].
Les patients atteints de TSA présentent une perte de cellules de Purkinje, une réduction du volume cérébelleux (en particulier du vermis) et une connectivité cérébello-corticale altérée. [B140], [B141]. La dysfonction du cervelet peut contribuer à une altération de la prédiction sensorielle, des stéréotypies motrices et à un traitement altéré du timing social. [B142].
Hippocampe
L'hippocampe est responsable de la mémoire déclarative, de la navigation spatiale et du traitement contextuel [B143]. Les patients atteints de TSA présentent une hypertrophie de l'hippocampe dans l'enfance, une connectivité hippocampique altérée et une extinction de la peur contextuelle perturbée. [B144], [B145].
Striatum
Le striatum (noyau caudé, putamen, noyau accumbens) est impliqué dans le traitement de la récompense, l'apprentissage des habitudes et le contrôle moteur. [B146]. Les patients atteints de TSA présentent une augmentation du striatum, une réduction de l'activation lors de récompenses sociales et une connectivité cortico-striatale perturbée. [B147], [B148].
Mécanismes d'action moléculaires des terpènes dans les TSA
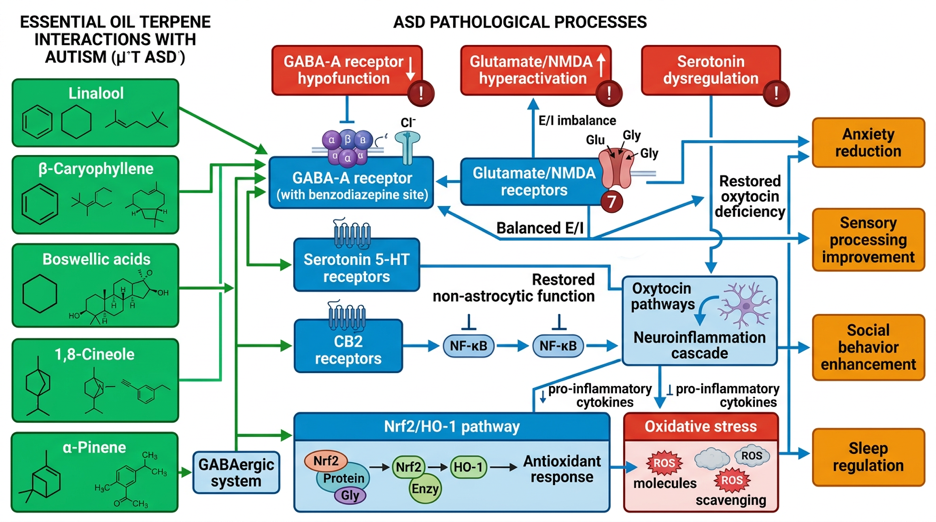
Figure 2 : Voies de signalisation moléculaire des terpènes dans le trouble du spectre autistique – Équilibre GABA/Glutamate, neuroinflammation et stress oxydatif
Les terpènes sont une classe diverse de produits naturels qui constituent les principaux composants des huiles essentielles. [B149]. Ses propriétés lipophiles permettent la traversée de la barrière hémato-encéphalique et l'interaction avec les cibles neuronales. [B150]. Cette section analyse les mécanismes moléculaires de terpènes spécifiques qui ciblent des cibles physiopathologiques liées à l'autisme.
Linalol – Site GABA-A/Benzodiazépine, Sérotonine, Anti-inflammatoire
Le linalol (3,7-diméthyl-1,6-octadién-3-ol) est un alcool monoterpénique et le composant principal de la lavande (Lavandula angustifolia, 25-45 %), de la coriandre, de la bergamote et d'autres huiles essentielles. [B151].
Modulation des récepteurs GABA-A
Le linalol présente des effets anxiolytiques qui sont bloqués par le flumazénil (un antagoniste des benzodiazépines), ce qui suggère une interaction avec le site de liaison des benzodiazépines du récepteur GABA-A. [B152]. Dans un modèle d'exposition olfactive, les vapeurs de linalool ont produit des effets anxiolytiques chez la souris (test du labyrinthe surélevé en croix, test clair-obscur), qui étaient absents chez les souris anosmiques (dégénérescence de l'épithélium olfactif), démontrant ainsi une action médiatisée par l'olfaction. [B152]. Des études électrophysiologiques montrent que le linalol potentialise les courants chlorure induits par le GABA dans les neurones cultivés. [B153]. Cette modulation GABAergique est très pertinente pour l'ASD, car les déficits GABAergiques et le déséquilibre E/I représentent des mécanismes physiopathologiques centraux. [B17], [B18].
Modulation sérotoninergique
L'inhalation de linalool a modifié les niveaux de sérotonine dans le cortex frontal des souris, suggérant une modulation de la transmission sérotoninergique. [B154]. Dans une étude menée chez des adultes en bonne santé, 20 minutes d'inhalation de linalol ont réduit l'humeur dépressive et augmenté l'activité parasympathique (augmentation de la variabilité de la fréquence cardiaque). [B155]. Des études *ex vivo* montrent que le linalol augmente les concentrations intracellulaires de calcium dans les neurones à ocytocine hypothalamiques, ce qui représente un mécanisme potentiel de modulation ocytocinergique. [B155]. Ces découvertes lient le linalol aux systèmes sérotoninergique et ocytocinergique, qui sont dysfonctionnels dans les TSA. [B59], [B72].
Effets anti-inflammatoires
Les revues systématiques rapportent des propriétés anti-inflammatoires du linalol dans des modèles précliniques, y compris la réduction du TNF-α, de l'IL-6, de l'IL-1β et de l'activation du NF-κB. [B156]. Dans un modèle de neuroinflammation induite par le stress, le linalool a réduit l'activation microgliale et l'expression des cytokines pro-inflammatoires. [B157]. Ces effets anti-neuroinflammatoires sont pertinents pour les TSA, car la neuroinflammation chronique est un mécanisme physiopathologique convergent. [B77], [B78].
Pharmacocinétique
Après exposition par inhalation, le linalol est rapidement absorbé et atteint la circulation systémique ; des métabolites (oxydes de linalol, glucuronides) sont détectés dans l'urine. [B158]. Le passage de la barrière hémato-encéphalique est probable en raison de la lipophilie, mais les données directes de pharmacocinétique du SNC chez l'homme sont limitées. [B159].
β-Caryophyllène – Agoniste CB2, NF-κB, Neuroinflammation
Le β-Caryophyllène (BCP) est un hydrocarbure sesquiterpénique présent dans le poivre noir, les clous de girofle, le cannabis (composant non psychoactif), le copaïba et d'autres plantes. [B160].
Agonisme du récepteur CB2
Le BCP est un agoniste sélectif du récepteur cannabinoïde de type 2 (CB2) sans affinité pour les récepteurs CB1, ce qui permet des effets immunomodulateurs non psychoactifs [B161]. Les récepteurs CB2 sont principalement exprimés sur les cellules immunitaires (microglie, cellules immunitaires périphériques) et régulent la libération de cytokines, l'activation microgliale et la neuroinflammation. [B162]. Chez les souris CB2-Knockout, les effets de la BCP étaient absents, ce qui confirme la spécificité de la CB2. [B163].
Effets anti-inflammatoires sur le système nerveux
Le BCP réduit la neuroinflammation dans de multiples modèles précliniques : neuroinflammation induite par le LPS, lésion cérébrale traumatique, maladies neurodégénératives [B164], [B165]. Les mécanismes comprennent la réduction de l'activation des microglies (expression réduite de Iba1, CD11b), la suppression des cytokines pro-inflammatoires (TNF-α, IL-6, IL-1β) et la modulation des voies de signalisation NF-κB. [B166]. Dans un modèle d'activation immunitaire maternelle (MIA, modèle pertinent pour l'autisme), le traitement par BCP a amélioré les comportements similaires à ceux de l'autisme (déficits sociaux, comportements répétitifs) et a réduit la neuroinflammation chez les descendants. [B167].
Modulation GABAergique et nitrinergique
Les études pharmacologiques comportementales montrent que les effets anxiolytiques et antidépresseurs du BCP sont bloqués par le flumazénil (antagoniste des benzodiazépines) et le L-NAME (inhibiteur de la nitrogène oxyde synthase), ce qui suggère la participation des systèmes GABAergiques et nitrinergiques. [B168]. Ces résultats suggèrent que le BCP peut moduler indirectement la fonction GABAergique par la réduction de la neuroinflammation médiatisée par les CB2.
Effets antioxydants
La BCP présente des propriétés antioxydantes par la réduction des ROS, la peroxydation lipidique et l'augmentation des enzymes antioxydantes endogènes (SOD, catalase, GSH). Il est difficile de dire ce que "B169" signifie sans plus de contexte. Cela pourrait être :* **Une référence à une norme ou une spécification technique** (par exemple, dans le domaine de la construction, de l'électronique, etc.).
* **Un nom de produit, de modèle ou de composant**.
* **Un code interne** utilisé par une entreprise ou une organisation.
* **Un identifiant** dans une base de données ou un système informatique.
* **Une partie d'un numéro de série ou d'un code d'identification**.
* **Un acronyme ou une abréviation** spécifique à un domaine particulier.**Pourriez-vous fournir plus d'informations sur l'endroit où vous avez vu "B169" ?** Par exemple :* Dans quel contexte l'avez-vous rencontré ? (Un document, un site web, un objet physique, une conversation ?)
* Y avait-il d'autres mots ou symboles à proximité ?
* De quel sujet traitait la conversation ou le document ?Avec plus de détails, il sera plus facile de déterminer sa signification.. Dans un modèle de stress oxydatif, le BCP a protégé les neurones de l'apoptose induite par H₂O₂. [B170].
Pertinence clinique pour la TSA
La combinaison d'une réduction de la neuroinflammation médiée par les CB2, d'effets antioxydants et d'une modulation GABAergique indirecte fait du BCP un candidat mécaniquement plausible pour une thérapie adjuvante de l'ASD, en particulier chez les patients présentant des signatures de neuroinflammation. [B171].
Acides boswelliques – Nrf2/HO-1, anti-neuroinflammatoire
Les acides boswelliques sont des acides triterpéniques pentacycliques provenant de la résine des espèces de Boswellia (encens), notamment l'acide β-boswellique, l'acide 11-céto-β-boswellique (KBA) et l'acide 3-O-acétyl-11-céto-β-boswellique (AKBA). [B172].
Activation Nrf2/HO-1
Les acides boswelliques activent la voie de signalisation Nrf2, un régulateur maître de la réponse antioxydante [B173]. Dans un modèle murin de neuroinflammation, le traitement par extrait de Boswellia a augmenté la localisation nucléaire de Nrf2 et l'expression de HO-1 dans l'hippocampe et le cortex. [B174]. HO-1 catalyse la dégradation de l'hème en biliverdine (antioxydante), en monoxyde de carbone (anti-inflammatoire, vasodilatateur) et en fer ; l'induction de HO-1 protège contre le stress oxydatif et la neuroinflammation. [B175].
Mécanismes anti-neuroinflammatoires
Les acides boswelliques réduisent l'activation de la microglie et des astrocytes (expression réduite de Iba1, GFAP), suppriment les cytokines pro-inflammatoires (TNF-α, IL-6, IL-1β) et inhibent les voies de signalisation NF-κB et MAPK. [B176], [B177]. Dans un modèle de neuroinflammation induit par le LPS, le traitement par Boswellia a amélioré les déficits cognitifs et réduit les marqueurs de neuroinflammation. [B178].
Inhibition de la 5-lipoxygénase (5-LOX)
Les acides boswelliques, en particulier l'AKBA, inhibent la 5-LOX, une enzyme qui métabolise l'acide arachidonique en leucotriènes pro-inflammatoires. [B179]. L'inhibition de la 5-LOX réduit l'inflammation médiée par les leucotriènes et a été associée à des effets neuroprotecteurs dans des études précliniques. [B180]. Cependant, la preuve de l'inhibition de la 5-LOX comme mécanisme principal de la neuroprotection par Boswellia est limitée dans la littérature existante ; l'activation de Nrf2/HO-1 apparaît comme le mécanisme dominant. [B174].
Preuves précliniques dans des modèles pertinents pour les TSA
Dans un modèle murin de TSA induit par l'acide valproïque (VPA), le traitement par extrait de Boswellia a amélioré l'interaction sociale, réduit les comportements répétitifs et normalisé les marqueurs de neuroinflammation. [B181]. Ces résultats soutiennent l'hypothèse que la réduction de la neuroinflammation et les effets antioxydants induits par le Boswellia peuvent améliorer les comportements pertinents pour les TSC.
1,8-Cineol – GABA-A/Benzodiazépine, Anxiolytique
Le 1,8-cinéole (eucalyptol) est un oxyde monoterpénique et le composant principal de l'eucalyptus (Eucalyptus globulus, 70–90 %), du romarin, de l'arbre à thé et du laurier [B182].
Modulation des récepteurs GABA-A
L'inhalation de 1,8-cinéole a produit des effets anxiolytiques et antidépresseurs dépendants de la dose chez la souris (Elevated Plus Maze, Forced Swim Test, Tail Suspension Test). [B183]. Ces effets ont été bloqués par le flumazénil, ce qui suggère une interaction avec le site de liaison des benzodiazépines du récepteur GABA-A. [B183]. Une dépendance à la dose a été démontrée : de faibles doses (0,1–1 µg/souris, par inhalation) ont montré des effets anxiolytiques, tandis que des doses plus élevées (10 µg/souris) ont produit des effets sédatifs. [B184].
Effets anti-inflammatoires et antioxydants
Le 1,8-cinéole présente des propriétés anti-inflammatoires en inhibant le NF-κB, en réduisant le TNF-α, l'IL-1β et la synthèse des leucotriènes. [B185]. Dans un modèle de neuroinflammation induite par le LPS, le 1,8-cinéole a réduit l'activation microgliale et le stress oxydatif [B186].
Aspects de sécurité
Le 1,8-cinéole est contre-indiqué chez les enfants de moins de 3 ans en raison du risque de laryngospasme et de dépression respiratoire. [B187]. Lorsqu'il est utilisé correctement (par inhalation, à faibles doses), le 1,8-cinéole présente un profil de sécurité favorable chez les adultes et les enfants plus âgés. [B188].
α-Pinène – GABAergique
L'α-pinène est un monoterpène bicyclique présent dans les pins, le romarin, la sauge et le cannabis. [B189].
Modulation GABAergique
Les revues systématiques associent l'α-pinène à la modulation de la neurotransmission GABAergique, bien que les études mécanistiques directes soient limitées [B190]. Dans les modèles comportementaux, l'α-pinène montre des effets anxiolytiques et sédatifs, suggérant des mécanismes gabaergiques. [B191]. Les données électrophysiologiques sur l'interaction directe avec les récepteurs GABA-A font défaut dans la littérature actuelle.
Effets anti-inflammatoires et neuroprotecteurs
L'α-pinène présente des propriétés anti-inflammatoires par inhibition de NF-κB et réduction des cytokines pro-inflammatoires [B192]. Dans un modèle d'ischémie-reperfusion, l'α-pinène a protégé contre les lésions neuronales et a réduit le stress oxydatif. [B193].
Inhibition de l'Acétylcholinestérase (AChE)
Certaines études rapportent une activité inhibitrice de l'AChE par l'α-pinène, ce qui pourrait potentialiser la neurotransmission cholinergique. [B194]. Cependant, la pertinence pour les TSA est incertaine, car la dysfonction cholinergique n'est pas un mécanisme physiopathologique primaire dans les TSA. [B195].
Ylang-Ylang/Cananga odorata – Sérotonine/Dopamine dans un modèle VPA
L'huile essentielle d'Ylang-Ylang (Cananga odorata) contient du linalol, du géraniol, du β-caryophyllène et d'autres terpènes [B196].
Preuves précliniques dans le modèle VPA-TSA
L'inhalation d'huile essentielle de Cananga odorata a amélioré les comportements de type anxiété, l'interaction sociale et la fonction cognitive chez des rats modèles de TSA induits par l'acide valproïque (AVP) [B197]. Les analyses neurochimiques ont montré que Cananga odorata modulait le métabolisme de la sérotonine et de la dopamine dans le cortex préfrontal et l'hippocampe : augmentation des taux de sérotonine, diminution des rapports 5-HIAA/sérotonine (indicatif d'une réduction du renouvellement de la sérotonine) et normalisation des taux de dopamine. [B197].
Interprétation mécaniste
L'amélioration des comportements de type TSA par la modulation des systèmes sérotoninergique et dopaminergique est mécanistiquement plausible, car les deux systèmes sont dysfonctionnels chez les TSA. [B57], [B58]. Les composants spécifiques de Cananga odorata responsables de ces effets n'ont pas été identifiés ; le linalool et le β-caryophyllène sont des candidats probables sur la base de leurs mécanismes connus. [B152], [B161].
Limitations
Ces résultats proviennent d'un modèle préclinique unique (rats VPA) ; la réplication dans d'autres modèles de TSA et la traduction vers des études humaines font défaut [B197].
Huiles essentielles spécifiques et preuves cliniques dans les TSA
Lavande/Linalool – Conformité ABA, Neurones à ocytocine
Preuves cliniques dans les TSA
Une petite étude pilote (n = 12 enfants autistes) a étudié l'aromathérapie à la lavande comme traitement d'appoint pendant la thérapie d'analyse comportementale appliquée (ABA). [B198]. La lavande a été diffusée comme “ 20 gouttes dans 100 ml ” (probablement de l'eau ou une huile porteuse, détails non clairs) pendant les séances de thérapie. L'étude a rapporté des scores de conformité plus élevés (coopération, achèvement des tâches) pendant l'exposition à la lavande par rapport aux séances de contrôle. [B198]. Les limitations comprennent un très petit échantillon, un manque de randomisation, un aveuglement peu clair et un dosage non standardisé.
Une étude observationnelle menée auprès de quatre enfants atteints de TSA et présentant des troubles d'apprentissage sévères a examiné l'intégration de massages d'aromathérapie (lavande, géranium, mandarine dans une huile de support) dans les routines quotidiennes. [B199]. L'étude a rapporté une augmentation des comportements d'attention conjointe (contact visuel, activités partagées) après l'introduction du massage par aromathérapie. [B199]. Les limitations comprennent le manque de contrôle, un petit échantillon et la confusion due aux effets du massage (stimulation tactile, interaction sociale).
Base mécaniste
Les résultats cliniques sont cohérents avec les mécanismes précliniques : la modulation GABAergique médiée par le linalool peut réduire l'anxiété et améliorer la coopération ; la modulation sérotoninergique et ocytocinergique peut favoriser l'attention et l'interaction sociales. [B152], [B155]. Une étude menée sur des adultes en bonne santé a montré que l'inhalation de lavande réduisait l'humeur dépressive et augmentait les concentrations intracellulaires de calcium dans les neurones hypothalamiques à oxytocine dans des expériences ex vivo. [B155]. Cette modulation oxytonerge est très pertinente pour les TSA, car la dysfonction de l'ocytocine est un mécanisme physiopathologique établi. [B72].
Limites des preuves
Les preuves cliniques de la lavande pour les TSA sont de très basse qualité : petits échantillons, absence de randomisation, aveuglement insuffisant, interventions hétérogènes et absence de réplication. [B198], [B199]. Des études randomisées contrôlées de haute qualité avec des préparations de lavande standardisées, des mesures de résultats objectives et une puissance suffisante font défaut.
Bergamote – RCT chez les enfants avec TSA, résultat non significatif
Essai contrôlé randomisé
Une étude randomisée et en double aveugle a examiné l'huile essentielle de bergamote (Citrus bergamia) chez des enfants autistes souffrant d'anxiété induite par des médicaments (n = 42). [B200]. Les enfants ont été randomisés pour une inhalation de 15 minutes d'huile de bergamote ou d'un placebo (eau) avant les examens médicaux. Le critère d'évaluation principal était l'anxiété mesurée par la Modified Yale Preoperative Anxiety Scale (mYPAS). Après ajustement pour l'anxiété initiale, le groupe bergamote n'a montré aucune réduction significative de l'anxiété par rapport au placebo (p > 0,05). [B200].
Interprétation
Ceci est la seule étude randomisée contrôlée identifiée concernant les huiles essentielles chez les enfants autistes. Le résultat négatif peut avoir plusieurs causes : (1) la courte durée d'exposition (15 minutes) pourrait être insuffisante ; (2) l'anxiété aiguë dans les milieux médicaux pourrait être plus difficile à moduler que l'anxiété chronique ; (3) la variabilité individuelle de la sensibilité et des préférences olfactives ; (4) de possibles effets plafond en cas d'anxiété de base déjà élevée. [B200].
Mécanismes précliniques
Les études précliniques montrent des effets anxiolytiques de la bergamote dans des modèles de rongeurs [B201]. De manière intéressante, ces effets n'ont pas été bloqués par le flumazénil, suggérant des mécanismes non médiés par les benzodiazépines et distinguant la bergamote du linalol et du 1,8-cinéol [B201]. La bergamote contient du linalol, de l'acétate de linalyle, du limonène et du bergapten ; les composants spécifiques responsables des effets anxiolytiques ne sont pas clairs. [B202].
Implications cliniques
Le résultat négatif de cette ECR tempère les attentes concernant la bergamote pour l'anxiété aiguë chez les TSA. D'autres études avec des durées d'exposition plus longues, des résultats liés à l'anxiété chronique et différentes populations de TSA sont nécessaires avant que la bergamote puisse être recommandée pour les TSA. [B200].
Encens / Boswellia – Anti-neuroinflammatoire, Nrf2
Preuves cliniques dans les TSA
Aucune étude randomisée contrôlée impliquant l'huile essentielle d'encens (Boswellia) ou des extraits de Boswellia chez des patients atteints de TSA n'a été identifiée. La littérature actuelle ne comprend aucune donnée clinique spécifique aux TSA pour l'encens. [B203].
Preuves précliniques
Comme décrit dans la section 3.3, les acides boswelliques montrent des effets anti-neuro-inflammatoires et antioxydants robustes dans des modèles précliniques, y compris l'activation de Nrf2/HO-1, l'inhibition de la microglie et l'amélioration des comportements de type autisme dans des modèles murins VPA. [B174], [B181]. Cette plausibilité mécanistique soutient l'hypothèse que le Boswellia pourrait être utile chez les patients atteints de TSA présentant des signatures d'inflammation neuronale.
Application clinique d'autres indications
Les extraits de Boswellia (par voie orale) sont utilisés cliniquement pour les maladies inflammatoires (arthrite, asthme, maladies inflammatoires de l'intestin), avec des preuves modérées d'efficacité et un profil de sécurité favorable. [B204]. L'application par inhalation d'huile essentielle d'encens est traditionnelle, mais les données cliniques de pharmacocinétique et d'efficacité font défaut [B205].
Besoin de recherche
Des essais cliniques contrôlés avec la boswellia (par voie orale ou inhalée) chez des patients atteints de TSA, idéalement stratifiés selon des biomarqueurs de neuroinflammation, sont nécessaires pour évaluer l'efficacité clinique. [B206].
Cèdre/Zeder – Sédation, GABAergique
Preuves cliniques et précliniques
La littérature actuelle ne contient pas de données mécanistiques ou cliniques spécifiques concernant l'huile essentielle de bois de cèdre (Cedrus atlantica, Juniperus virginiana) dans l'autisme ou dans des modèles précliniques pertinents pour l'autisme. [B207]. Les applications traditionnelles incluent la sédation et la réduction de l'anxiété, mais les preuves scientifiques des mécanismes GABAergiques ou de l'efficacité clinique font défaut dans la littérature analysée. [B208].
Composantes principales
L'huile de bois de cèdre contient du cèdre (alcool sesquiterpénique), de l'α-cèdrène et du thujopsène [B209]. Le cédrol est associé à des propriétés sédatives, mais des études directes sur son interaction avec les récepteurs GABA-A ou sa modulation de la neuroinflammation font défaut. [B210].
Conclusion
Les preuves de l'utilisation du bois de cèdre pour le TSA sont insuffisantes ; aucune recommandation ne peut être faite sur la base de la littérature existante. [B207].
Vétiver – Attention
Preuves cliniques et précliniques
La littérature actuelle ne contient aucune donnée spécifique sur l'huile essentielle de vétiver (Vetiveria zizanioides) dans le cadre de l'autisme ou dans des modèles pertinents pour l'autisme. [B211]. Des rapports anecdotiques et des applications traditionnelles suggèrent des effets sur l'attention et l'hyperactivité, mais des études contrôlées font défaut. [B212].
Composantes principales
L'huile de vétiver contient du vétiverol, du khusimol, de l'α-vétivone et de la β-vétivone (alcools et cétones sesquiterpéniques). [B213]. Des études mécanistes sur ces composants, en ce qui concerne les neurotransmetteurs ou la neuroinflammation, font défaut dans la littérature analysée. [B214].
Conclusion
Les preuves de l'utilisation du vétiver pour le TSA sont insuffisantes ; des recherches supplémentaires sont nécessaires avant que des recommandations puissent être faites [B211].
Ylang-Ylang – Sérotonine/Dopamine, Modèle VPA
Preuves précliniques
Comme décrit dans la section 3.5, l'inhalation de l'huile essentielle de Cananga odorata (Ylang-Ylang) a amélioré les comportements de type ASD chez les rats VPA et a modulé le métabolisme de la sérotonine et de la dopamine dans le cortex préfrontal et l'hippocampe. [B197]. C'est la seule étude identifiée avec de l'ylang-ylang dans un modèle pertinent pour l'ASD.
Preuves cliniques dans les TSA
Aucune étude clinique impliquant l'ylang-ylang chez des patients atteints de TSA n'a été identifiée [B215].
Application clinique d'autres indications
L'ylang-ylang est traditionnellement utilisé pour l'anxiété, l'humeur et la relaxation. Une petite étude menée sur des adultes en bonne santé a montré que l'inhalation d'ylang-ylang réduisait la tension artérielle et la fréquence cardiaque, et augmentait la sensation subjective de calme. [B216]. Il manque des études mécanistiques sur les effets sérotoninergiques et dopaminergiques chez l'homme. [B217].
Conclusion
Les preuves précliniques sont prometteuses, mais la traduction vers des études humaines sur les TSA fait défaut. L'ylang-ylang pourrait être envisagé comme candidat pour des essais cliniques chez les personnes atteintes de TSA, en particulier pour les symptômes d'anxiété et d'humeur. [B197].
Autres huiles essentielles indiquées pour l'ASC
Sur la base d'une recherche bibliographique actuelle, les huiles essentielles supplémentaires suivantes ont pu être identifiées, qui pourraient être pertinentes pour les TSA par des mécanismes neurobiologiquement plausibles.
Gingembre (Zingiber officinale) – voie de signalisation AKT/GSK3β
Substances actives
6-gingérol
6-Shogaol
Zingiberene
β-Sesquiphellandrène
Récepteurs et mécanismes d'action
– Voie AKT/GSK3β : Phosphorylation accrue → plasticité synaptique améliorée
– Anti-neuroinflammatoire : Réduction de la phosphorylation de STAT3 et du TNF-α
– Neurogenèse : Marqueurs améliorés de la neurogenèse hippocampique dans des modèles précliniques
– Inhibition de la gliose : Astrogliose réactionnelle réduite
Preuves cliniques/précliniques
- Étude préclinique (modèle de souris VPA)
– L'extrait de gingembre oral (4 semaines, à partir de la 6ème semaine de vie) a amélioré significativement l'interaction sociale, réduit les comportements anxieux et amélioré les performances de mémoire [B347]
– Mécanistique : régulation positive d'AKT/GSK3β, inhibition de STAT3/TNF-α, formation améliorée de synapses
– Des essais contrôlés randomisés cliniques sur le TSA font encore défaut, mais la preuve préclinique est solide et mécaniquement bien établie
Dosage (Organik Aromas Nebulizer 3.0)
– 2-3 gouttes pour une pièce de 15 à 25 m²
– Combinaison avec la lavande (1:2) pour un effet relaxant
– Application : 30 min avant les activités sociales
Sécurité
Bien toléré; à utiliser avec prudence chez les enfants de moins de 3 ans.
Bois de santal (Santalum album) – α/β-Santalol
Substances actives
α-Santalol (50–55%)
β-Santalol (20–25%)
Sesquiterpène
Récepteurs et mécanismes d'action
– Modulation sérotoninergique : l'α-santalol module les récepteurs 5-HT (préclinique)
– Anxiolytique : activité GABAergique documentée chez des modèles animaux
– Sédatif/Apaisant : Convient à l'hypersensibilité sensorielle chez les personnes atteintes de TSA
Preuves cliniques
– Le bois de santal faisait partie du RCT Hiwa Syrup (médecine persane, plusieurs herbes) chez les enfants atteints de TSA, les effets ne pouvaient pas être attribués isolément [B348]
– Des études individuelles sur l'anxiolyse chez des volontaires sains montrent un effet calmant
– Les études directes spécifiques à l'ASD avec de l'huile de bois de santal pure font défaut
Dosage (Organik Aromas Nebulizer 3.0)
– 3-4 gouttes pour une pièce de 15 à 25 m²
– Particulièrement adapté aux rituels du soir/de sommeil pour les enfants autistes ayant des difficultés d'endormissement
– Recommandé en combinaison avec de la lavande (1:1)
Sécurité
Très bien toléré ; l'une des huiles essentielles les plus sûres pour les enfants (dès 2 ans).
Mélanges de terpènes (inspirés du cannabis) – Effets prosociaux
Substances actives
Myrcène
Citron vert
Linalol
Pin
β-Caryophyllène (en mélange)
Récepteurs et mécanismes d'action
– Agonisme CB1/CB2 : les mélanges de terpènes potentialisent les effets du CBD (effet d'entourage)
– Modulation GABAergique : Linalol + Myrcène synergiques
– Effet prosocial démontré indépendamment du CBD
Preuves cliniques
- Modèle de souris BTBR (modèle TSA)
Les mélanges de terpènes inhalés (myrcène, limonène, linalol, pinène, β-caryophyllène) ont montré des effets prosociaux aigus indépendamment du CBD [B349] – Les mélanges de terpènes ont renforcé l'effet du CBD lors d'une application combinée
– Mention de l'effet d'entourage comme principe thérapeutique pour les TSA
Dosage (Organik Aromas Nebulizer 3.0)
– Suggestion de mélange : Lavande (2T) + Poivre noir (1T) + Bergamote (1T) + Romarin (1T)
– Pour la pièce 15, il y a 25 m² : 5 gouttes de mélange total
– Application : 30 min avant les activités sociales ou les séances de thérapie de groupe
Recommandations de dosage pour Organik Aromas Nebulizer 3.0
Le nébuliseur Organik Aromas 3.0 utilise le principe de Venturi (effet Bernoulli) pour la nébulisation à froid sans eau d'huiles essentielles. [B218]. Contrairement aux diffuseurs à ultrasons ou thermiques, qui diluent ou chauffent les huiles avec de l'eau, le nébuliseur produit de fines particules d'aérosol (1 à 5 µm) d'huiles essentielles pures sans dégradation thermique. [B219]. Cela permet des concentrations plus élevées de terpènes volatils dans l'air ambiant et des effets pharmacologiques potentiellement plus forts [B220].
Principe de Venturi et nébulisation à froid
Le principe de Venturi décrit la réduction de pression dans un fluide lorsqu'il s'écoule à travers un étranglement [B221]. Dans le nébuliseur, de l'air comprimé passe à travers une buse créant une dépression qui aspire l'huile essentielle d'un réservoir et la pulvérise en fines gouttelettes. [B222]. Ces gouttelettes sont libérées dans l'air ambiant, où elles sont inhalées ou se déposent sur les surfaces. [B223].
Avantages de la nébulisation à froid
– Réception de composants thermolabiles (pas de dégradation par la chaleur) [B224]
– Concentrations plus élevées de terpènes volatils (aucun effet de dilution par l'eau) [B225]
– Granulométrie fine (1 à 5 µm) permettant une pénétration profonde dans les voies respiratoires [B226]
Inconvénients
– Coûts plus élevés par rapport aux diffuseurs à ultrasons [B227]
Consommation d'huile plus élevée [B228]
– Potentiel de surdosage en cas d'utilisation inappropriée [B229]
Quantités de gouttelettes spécifiques à la taille de la pièce
Les recommandations de dosage sont basées sur le volume de la pièce, le taux de renouvellement d'air, la concentration de terpènes souhaitée et la durée d'exposition. Les recommandations suivantes sont conservatrices et tiennent compte de la sensibilité sensorielle spécifique aux DSM. [B230].
Tableau 1 : Recommandations de dosage spécifiques à la taille de la pièce pour le nébuliseur d'arômes organiques 3.0
Notes
- Volume de gouttelettes : 1 goutte ≈ 0,05 ml d'huile essentielle [B231]
- Dose de départ Commencez par le nombre de gouttes recommandé le plus bas et augmentez progressivement sur 1 à 2 semaines pour évaluer la tolérance [B232]
- Personnalisation individuelle : Les patients atteints de TSA présentant une hypersensibilité olfactive marquée peuvent nécessiter des doses plus faibles ou des pauses plus longues [B233]
- Ventilation Une bonne ventilation des pièces est essentielle pour éviter une accumulation excessive [B234]
Durée d'utilisation et pauses
Durée d'application
15 à 30 minutes par séance sont suffisantes pour atteindre des concentrations thérapeutiques de terpènes, sur la base d'études précliniques d'inhalation. [B183], [B184]. Des applications plus longues (> 30 minutes) augmentent le risque de surcharge sensorielle et d'adaptation olfactive (perception réduite en cas d'exposition continue). [B235].
Pauses
30 à 60 minutes de pauses entre les applications permettent une récupération olfactive, le métabolisme des terpènes inhalés et la réduction des concentrations dans l'air ambiant [B236]. Une exposition continue sans pause peut entraîner des maux de tête, des nausées et une aversion sensorielle, en particulier chez les patients atteints de TSA souffrant d'hypersensibilité sensorielle. [B237].
Applications quotidiennes
2 à 3 applications par jour (matin, après-midi, soir) sont suffisantes pour la plupart des indications [B238]. Plus de 4 applications par jour augmentent le risque d'effets secondaires sans bénéfice thérapeutique supplémentaire [B239].
Journaux spécifiques à l'heure de la journée
Matin (stimulant, concentré)
- Huiles : Romarin (1,8-cinéole, α-pinène), Menthe poivrée (menthol, menthone), Citron (limonène), Bergamote (linalol, acétate de linalyle)
- Dosage : 3-5 gouttes pour 20-30 m² de pièce
- Durée : 15–20 minutes
- Objectif : Promotion de la vigilance, de l'attention et des fonctions cognitives pour l'école/la thérapie [B240]
Après-midi (régulateur, modulateur d'humeur)
- Huiles : Bergamote, Ylang-Ylang, Géranium, Encens
- Dosage : 3-5 gouttes pour 20-30 m² de pièce
- Durée : 20–30 minutes
- Objectif : Réduction de l'anxiété de l'après-midi, stabilisation de l'humeur, transition entre les activités [B241]
Le soir (apaisant, favorisant le sommeil)
- Huiles : Lavande (Linalool, Acétate de linalyle), Camomille romaine (Esters), Bois de cèdre (Cédrol), Vétiver
- Dosage : 4–6 gouttes pour une pièce de 20–30 m²
- Durée : 30 minutes avant de dormir
- Objectif : Réduction de l'anxiété du soir, promotion de la relaxation et amorce du sommeil [B242]
Particularités spécifiques aux TSA
Hypersensibilité sensorielle : 60–90 % % des patients atteints de TSA présentent une hypersensibilité olfactive ou une aversion pour certaines odeurs [B243]. Une introduction progressive est essentielle :
- Semaine 1 : Exposition hors site (diffusion d'huile dans une pièce adjacente) pour évaluer l'acceptation [B244]
- Semaine 2 : Dose la plus faible (2 gouttes) pendant 10 minutes, patient hors de la pièce pendant la nébulisation [B245]
- Semaine 3 : Dose la plus faible, patient dans la pièce, observation des signes de tolérance (détente, absence d'aversion) [B246]
- Semaine 4+ : Augmentation progressive des doses et de la durée en fonction de la tolérance individuelle [B247]
Sélection basée sur les préférences
Faire sentir des huiles différentes au patient (si possible) et recueillir ses préférences. La préférence olfactive est corrélée à l'acceptation thérapeutique et à l'observance du traitement. [B248].
Indications visuelles et auditives
Utilisez des minuteurs visuels ou des signaux auditifs pour indiquer le début et la fin d'une séance d'aromathérapie, ce qui augmente la prévisibilité et le contrôle pour les personnes atteintes de TSA. [B249].
Formation pour parents/tuteurs
Sensibilisez les parents et les soignants à la reconnaissance des signes de tolérance (détente, amélioration de l'attention) et des signes d'aversion (grimace, retrait, agitation). [B250].
Exigences de qualité – Analyse CG/SM
Chromatographie en phase gazeuse couplée à la spectrométrie de masse (GC/MS)
GC/MS est la norme d'or pour la caractérisation chimique des huiles essentielles [B251]. La GC sépare les composés volatils en fonction du point d'ébullition et de la polarité ; la MS identifie les composés en fonction du rapport masse/charge [B252]. La GC/MS permet :
- Identification des composantes principales : Confirmation de la présence de terpènes d'intérêt thérapeutique (par exemple, le linalol dans la lavande, le 1,8-cinéole dans l'eucalyptus) [B253]
- Quantification : Composition en pourcentage de chaque composant [B254]
- Détection de falsifications : Identification des additifs synthétiques, des diluants ou des contaminants [B255]
- Cohérence de lot à lot : Garantie d'une composition reproductible [B256]
Critères de qualité pour les huiles essentielles thérapeutiques
- 100 % rein
Aucun additif synthétique, huile porteuse ou diluant [B257] - Qualité thérapeutique
Huiles provenant de plantes cultivées, récoltées et distillées dans des conditions optimales [B258] - Organisch/Wildsammlung
Sans pesticides, herbicides ni engrais chimiques [B259] - Certificat CPG/SM
Chaque lot doit être accompagné d'un certificat d'analyse GC/MS documentant les composants principaux et la pureté [B260] - Nom botanique
Identification univoque de l'espèce végétale (par exemple, Lavandula angustifolia, et non pas seulement “lavande”) [B261] - Pays d'origine et date de distillation
Transparence sur l'origine et la fraîcheur [B262]
Stockage
Les huiles essentielles doivent être conservées dans des flacons en verre sombre à température fraîche (<25°C) afin de minimiser l'oxydation et la dégradation. [B263]. Les huiles oxydées peuvent provoquer des irritations cutanées et montrer une efficacité thérapeutique réduite. [B264].
Consignes de sécurité et contre-indications
Hypersensibilité sensorielle spécifique aux TSA
Les troubles du traitement sensoriel sont présents chez 60 à 90 % des patients atteints de TSA et se manifestent par une hypersensibilité (hypersensibilité) ou une hyposensibilité (hypo-sensibilité) aux stimuli sensoriels. [B265]. L'hypersensibilité olfactive peut entraîner une aversion, de l'anxiété, des nausées et des comportements d'évitement [B266].
Gestion des risques
- Introduction graduée : Comme décrit dans la section 5.4, commencez par des doses minimales à l'extérieur de la chambre du patient. [B244]
- Dépistage des préférences : Tester des huiles avant leur application thérapeutique afin d'identifier les réactions indésirables [B248]
- Critères d'abandon : Arrêtez immédiatement en cas de signes de détresse (agitation, retrait, nausées, maux de tête) [B267]
- Voies d'application alternatives : En cas d'intolérance par inhalation, envisagez une application topique (diluée dans une huile porteuse, test de patch requis) ou une diffusion passive (huile sur un coton dans un coin de la pièce). [B268]
Risque d'épilepsie – Huiles à base de camphre
10–30 % der ASD-Patienten haben komorbide Epilepsie [B269]. Certaines huiles essentielles, en particulier celles contenant du camphre, peuvent abaisser le seuil épileptogène et provoquer des crises. [B270].
Huiles contre-indiquées en cas d'épilepsie
- Camphre (Cinnamomum camphora) : Contient du camphre (jusqu'à 50 %), un convulsivant connu [B271]
- Romarin (Rosmarinus officinalis, chémotype camphré) : Contient 15–25 % camphre [B272]
- Sauge (Salvia officinalis) Contient du thuyone (10–40 %), un antagoniste des récepteurs GABA-A aux propriétés convulsivantes [B273]
- Hysope (Hyssopus officinalis) : Contient du pinocamphone et de l'isopinocamphone, qui peuvent provoquer des convulsions [B274]
- Fenouil (Foeniculum vulgare) : Contient du trans-anéthol, qui peut avoir un effet convulsivant à fortes doses [B275]
Alternatives sûres en cas d'épilepsie : – Lavande (Lavandula angustifolia, chémotype Linalol) : Propriétés anticonvulsivantes dans des études précliniques [B276] – Camomille romaine (Anthemis nobilis) : Aucun effet proconvulsivant connu [B277] – Bergamote (Citrus bergamia, sans bergaptène) : Sûr en cas d'épilepsie [B278]
Recommandation clinique : Chez les patients atteints de TSA présentant une épilepsie, seuls des huiles sans camphre ni thuyone doivent être utilisées. La consultation d'un neurologue avant l'introduction de l'aromathérapie est conseillée. [B279].
Eucalyptus chez les enfants de moins de 3 ans
Le 1,8-cinéole (composant principal de l'eucalyptus) est contre-indiqué chez les enfants de moins de 3 ans en raison du risque de laryngospasme, de bronchospasme et de dépression respiratoire. [B280]. Les mécanismes comprennent une irritation directe de la muqueuse des voies respiratoires et le déclenchement de réflexes vagaux [B281].
Huiles contre-indiquées chez les enfants de moins de 3 ans
– Eucalyptus (Eucalyptus globulus, E. radiata) : 70–90 % 1,8-Cinéole [B282]
– Romarin (Rosmarinus officinalis, chémotype 1,8-cinéole) : 40–50 % 1,8-cinéole [B283]
– Tea tree (Melaleuca alternifolia) : 5-15 % 1,8-Cineole (risque plus faible, mais prudence requise) [B284]
– Menthe poivrée (Mentha piperita) : Le menthol peut provoquer une irritation similaire des voies respiratoires [B285]
Alternatives sûres pour les enfants de moins de 3 ans
– Lavande (Lavandula angustifolia) : Sans danger dès la naissance avec une dilution appropriée [B286]
– Camomille Romaine (Anthemis nobilis) : Sûre dès la naissance [B287]
– Mandarine (Citrus reticulata) : Sûr à partir de 6 mois [B288]
Recommandation clinique
Évitez les huiles riches en 1,8-cinéole chez les enfants atteints de TSA de moins de 3 ans.
Chez les enfants de 3 à 6 ans, utilisez de faibles doses (50 % de la dose adulte) et surveillez attentivement les symptômes respiratoires [B289].
Interactions avec les antipsychotiques : rispéridone, aripiprazole
La rispéridone et l'aripiprazole sont les seuls médicaments approuvés par la FDA pour l'irritabilité dans les TSA [B290]. Les deux sont métabolisés par des enzymes du cytochrome P450 (CYP2D6, CYP3A4). [B291]. Certaines huiles essentielles et terpènes peuvent inhiber ou induire les enzymes du CYP, ce qui peut entraîner des modifications des taux de médicaments. [B292].
Interactions potentielles :
Bergamote
Contient du bergaptène (furanocoumarine), qui inhibe le CYP3A4 [B293]. Théoriquement, la bergamote pourrait augmenter les taux de rispéridone et d'aripiprazole, ce qui pourrait renforcer les effets secondaires (sédation, symptômes extrapyramidaux). [B294]. Cependant, l'exposition par inhalation est nettement plus faible que l'absorption orale (effet du jus de pamplemousse) ; la pertinence clinique de l'exposition à la bergamote par inhalation est incertaine. [B295].
Recommandation
Utiliser de la bergamote sans bergaptène (FCF, sans furanocoumarine) chez les patients sous rispéridone/aripiprazole [B296].
Pamplemousse
L'huile essentielle de pamplemousse contient des furanocoumarines et inhibe le CYP3A4 [B297]. Évitez chez les patients sous médicaments métabolisés par le CYP3A4 [B298].
Millepertuis (Hypericum perforatum)
Bien qu'il ne s'agisse pas d'une huile essentielle typique, le millepertuis est parfois mentionné dans des contextes d'aromathérapie. Le millepertuis est un puissant inducteur du CYP3A4 et peut réduire les taux de rispéridone/aripiprazole, entraînant une perte d'efficacité. [B299]
Contre-indication : Évitez le millepertuis chez les patients sous antipsychotiques [B300].
Lavande, Camomille, Bois de cèdre
Aucune interaction médicamenteuse pertinente sur le plan clinique avec le CYP n'est connue. [B301]. Sûr chez les patients sous rispéridone/aripiprazole [B302].
Interactions pharmacodynamiques
Les huiles essentielles sédatives (lavande, camomille, cèdre) peuvent avoir des effets sédatifs additifs avec les antipsychotiques [B303]. Cela peut être souhaitable sur le plan thérapeutique (par exemple, pour favoriser le sommeil), mais nécessite une surveillance pour une sédation excessive [B304].
Recommandation clinique
Informer les médecins prescripteurs sur l'utilisation de l'aromathérapie. Utiliser des huiles sans bergaptène chez les patients sous substrats du CYP3A4. Surveiller les effets modifiés des médicaments (sédation, effets secondaires). [B305].
Exigences de qualité : analyse GC/MS
Comme décrit dans la section 5.5, l'analyse GC/MS est essentielle pour garantir la pureté, la composition et l'absence de contaminants. [B251]. Les huiles frelatées ou contaminées peuvent provoquer des allergies, des irritations cutanées, des symptômes respiratoires et des effets pharmacologiques imprévisibles. [B306].
Falsifications fréquentes
- Additifs synthétiques : Linalol ou acétate de linalyle synthétiques dans l'huile de “lavande” [B307]
- Diluant Propylène glycol, éther monométhylique du dipropylène glycol (DPM) [B308]
- Huiles moins chères : Lavandin (Lavandula x intermedia) vendu comme lavande vraie (Lavandula angustifolia) [B309]
- Pesticides : Résidus de pesticides, d'herbicides dans les huiles non biologiques [B310]
Recommandation de sécurité
Utilisez uniquement des huiles essentielles organiques certifiées GC/MS, 100 % pures, provenant de fournisseurs de confiance. Demandez des certificats GC/MS pour chaque lot [B311].
discussion
État de la preuve
Les preuves concernant les huiles essentielles chez les personnes atteintes de TSA sont hétérogènes et d'une qualité majoritairement faible. La littérature clinique comprend une étude contrôlée randomisée négative (bergamote pour l'anxiété aiguë) [B200], petites études pilotes aux limitations méthodologiques (lavande dans la conformité ABA) [B198], études observationnelles (massages aromathérapeutiques) [B199] et études de cas [B312]. Aucune étude ne démontre l'efficacité sur les symptômes fondamentaux des TSA (communication sociale, comportements répétitifs) avec une qualité de preuves suffisante. [B313].
En revanche, les preuves précliniques sont robustes : de multiples études démontrent que des terpènes spécifiques (linalol, β-caryophyllène, acides boswelliques, 1,8-cinéole) ciblent des cibles moléculaires pertinentes pour l'ASD (récepteurs GABA-A, récepteurs CB2, voie Nrf2, neuroinflammation) et améliorent les comportements de type ASD dans des modèles animaux. [B152], [B161], [B174], [B183], [B197]. Cet écart entre la plausibilité préclinique et l'évidence clinique est typique des thérapies complémentaires et reflète le manque de financement de la recherche, les défis méthodologiques et les lacunes en matière de translation. [B314].
Plausibilité mécaniste
La plausibilité mécanistique des huiles essentielles dans les TSA est établie, basée sur la convergence entre la pathophysiologie des TSA et les mécanismes d'action des terpènes :
Déséquilibre GABA/Glutamate E/I
Le linalol et le 1,8-cinéole modulent les récepteurs GABA-A au site de liaison des benzodiazépines, ce qui pourrait potentialiser la neurotransmission inhibitrice et normaliser l'équilibre E/I. [B152], [B183]. Ces mécanismes sont analogues à ceux de la bumétanide, qui a montré des améliorations modérées chez les personnes autistes lors d'essais cliniques. [B52].
Neuroinflammation
Le β-caryophyllène (agoniste CB2) et les acides de Boswellia (activateurs Nrf2) réduisent l'activation de la microglie, les cytokines pro-inflammatoires et le stress oxydatif dans des modèles précliniques. [B161], [B174]. L' ένα mécanisme pathophysiologique établi dans le TSA [B77], ces terpènes pourraient-ils être utiles chez des patients présentant des signatures neuroinflammatoires (augmentation des cytokines périphériques, preuves TEP d'activation microgliale) [B315].
Sérotonine/Dopamine
Le linalool et l'ylang-ylang modulent les systèmes sérotoninergique et dopaminergique dans des études précliniques [B154], [B197]. Ces mécanismes pourraient améliorer les symptômes comorbides (anxiété, humeur), bien que les effets sur les symptômes principaux soient peu probables. [B316].
Ocytocine
Le linalol augmente les concentrations intracellulaires de calcium dans les neurones à ocytocine [B155]. L'ocytocine régule le développement GABAergique et a amélioré les phénotypes similaires à l'autisme dans des études précliniques [B50], pourrait moduler indirectement les voies de signalisation oxytonergiques [B317].
Axe intestin-cerveau
Bien que les preuves directes fassent défaut, les terpènes anti-inflammatoires (β-caryophyllène, acides boswelliques) pourraient réduire l'inflammation systémique et moduler indirectement les voies de signalisation de l'axe intestin-cerveau. [B318]. Cette hypothèse nécessite une validation expérimentale [B319].
Limitations
Petites études
La plupart des études spécifiques à l'autisme ont des tailles d'échantillon inférieures à 20, ce qui signifie une puissance insuffisante pour détecter des effets modérés. [B320]. Les méta-analyses ne sont pas possibles en raison de l'hétérogénéité [B321].
Aucun essai contrôlé randomisé pour les troubles du noyau
Il n'existe pas d'études randomisées contrôlées examinant l'efficacité des huiles essentielles pour les symptômes de base du TSA (communication sociale, comportements répétitifs). [B322]. La seule RCT identifiée (bergamote) était négative pour l'anxiété aiguë. [B200].
Hétérogénéité méthodologique
Les études varient dans le choix de l'huile, la posologie, la voie d'administration (inhalation, massage, topique), la durée d'exposition, les critères d'évaluation et les populations. [B323]. Cette hétérogénéité empêche la synthèse et la comparabilité [B324].
Biomarqueurs manquants
Aucune étude ne stratifie les patients selon des sous-types neurobiologiques (par exemple, des signatures de neuroinflammation, des marqueurs de déséquilibre E/I) ni n'utilise de biomarqueurs objectifs comme critères d'évaluation. [B325]. Les approches de médecine de précision pourraient identifier les répondeurs [B326].
Biais de publication
Les rapports de cas positifs et les petites études pilotes sont plus susceptibles d'être publiés que les études négatives, ce qui peut conduire à une surestimation des effets. [B327].
Écart de traduction
Les modèles précliniques (rats VPA, souris MIA) ne reproduisent pas toute la complexité de l'hétérogénéité des TSA humains [B328]. Les doses de terpènes dans les études animales sont souvent plus élevées que celles pouvant être atteintes lors d'une exposition humaine par inhalation. [B329].
Effets placebo
L'aromathérapie est associée à de forts effets d'attente; le double aveugle est difficile en raison des odeurs évidentes [B330]. La RCT sur la bergamote a utilisé l'eau comme placebo, ce qui implique un aveuglement insuffisant. [B200].
Données de sécurité : Les données de sécurité à long terme pour l'exposition chronique par inhalation chez les enfants font défaut [B331]. La plupart des données de sécurité proviennent d'une application topique ou orale [B332].
Perspective
Priorités de recherche :
- Les ECR de haute qualité : Études randomisées, en double aveugle, contrôlées par placebo, suffisamment puissantes (n > 100), avec des préparations d'huile standardisées (certifiées GC/MS), des mesures de résultats objectives (biomarqueurs, actigraphie, suivi oculaire) et des durées d'intervention plus longues (8–12 semaines) [B333].
- Stratification par sous-types : Identification des répondants basée sur des sous-types neurobiologiques (marqueurs de neuroinflammation, déséquilibre E/I, profils microbiomiques) [B334]. Les approches de médecine de précision pourraient augmenter les tailles d'effet [B335].
- Études mécanistiques : Études humaines avec des résultats basés sur des biomarqueurs (profils de cytokines, neuroimagerie, EEG, analyses du microbiome) avant et après intervention, pour valider les mécanismes [B336].
- Pharmacocinétique Études pharmacocinétiques humaines pour l'exposition aux terpènes par inhalation : concentrations plasmatiques, pénétration dans le SNC, métabolisme, relations dose-réponse [B337].
- Thérapies combinées : Examen des synergies entre les huiles essentielles et les interventions établies (thérapie comportementale, pharmacothérapie, interventions sur le microbiome) [B338].
- Sécurité à long terme : Études de cohorte prospectives sur la sécurité à long terme de l'exposition chronique par inhalation chez les enfants [B339].
- Aromathérapie personnalisée : Développement d'algorithmes de sélection d'huiles basés sur des profils de symptômes individuels, des préférences et des marqueurs neurobiologiques [B340].
Implications cliniques
Sur la base des preuves actuelles, les huiles essentielles peuvent être envisagées comme faisant partie d'une approche thérapeutique multimodale pour les symptômes comorbides (anxiété, troubles du sommeil, régulation sensorielle) chez les TSA, mais pas comme une monothérapie ou un substitut aux interventions fondamentales fondées sur des preuves. [B341]. Les cliniciens devraient :
- Communiquer des attentes réalistes : Les huiles essentielles peuvent soulager les symptômes comorbides, mais ne guérissent pas les symptômes de base [B342]
- Tenir compte de la tolérance et des préférences individuelles [B343]
- Huiles certifiées GC/MS de haute qualité à recommander [B344]
- Tenir compte des aspects de sécurité (épilepsie, âge, interactions médicamenteuses) [B345]
- Surveiller les effets et ajuster le traitement [B346]
Conclusion
Les huiles essentielles constituent une option thérapeutique adjuvante mécanistiquement plausible mais cliniquement insuffisamment validée pour le trouble du spectre autistique. L'hétérogénéité neurobiologique des TSA – caractérisée par un déséquilibre GABA/glutamate E/I, une neuroinflammation, un stress oxydatif, des altérations de l'axe intestin-cerveau et une dysfonction synaptique – offre de multiples cibles thérapeutiques sur lesquelles des terpènes spécifiques peuvent agir.
La preuve préclinique démontre que le linalool (modulation GABA-A, régulation sérotoninergique), le β-caryophyllène (réduction de la neuroinflammation médiée par CB2), les acides boswelliques (activation Nrf2/HO-1), le 1,8-cinéole (effets anxiolytiques GABAergiques) et l'ylang-ylang (modulation sérotoninergique/dopaminergique) modulent des mécanismes physiopathologiques pertinents pour les TSA et améliorent les comportements similaires aux TSA chez les modèles animaux. Cette plausibilité mécanistique est étayée par des applications traditionnelles et des données humaines limitées concernant l'anxiété, le sommeil et l'humeur.
Cependant, les preuves cliniques dans les TSA sont de qualité inférieure : un essai contrôlé randomisé négatif (bergamote), de petites études pilotes présentant des limitations méthodologiques (lavande pour la conformité ABA) et des études observationnelles. Aucune étude ne démontre d'efficacité pour les symptômes fondamentaux des TSA avec une qualité de preuve suffisante. Des études contrôlées randomisées de haute qualité avec des préparations standardisées, des critères d'évaluation objectifs et une puissance suffisante font défaut.
Pour le nébuliseur d'arômes Organik 3.0, des recommandations de dosage spécifiques à la taille de la pièce sont développées (2–10 gouttes pour 10–60 m², pauses de 15–30 minutes, 30–60 minutes), avec des protocoles adaptés à l'heure de la journée (stimulant le matin, apaisant le soir) et des particularités spécifiques aux TSA (introduction progressive, sélection des préférences, hypersensibilité sensorielle). Les aspects de sécurité comprennent les contre-indications en cas d'épilepsie (huiles contenant du camphre), chez les enfants de moins de 3 ans (eucalyptus), les interactions potentielles avec les antipsychotiques (huiles contenant du bergapten) et la nécessité d'huiles pures certifiées GC/MS.
Les huiles essentielles peuvent être envisagées comme faisant partie d'une approche thérapeutique multimodale pour les symptômes comorbides (anxiété, troubles du sommeil, dérégulation sensorielle) chez les personnes atteintes de TSA, mais elles ne remplacent pas les interventions fondamentales fondées sur des preuves (thérapie comportementale, éducation structurée). Les recherches futures devraient privilégier les essais contrôlés randomisés de haute qualité, la stratification selon les sous-types neurobiologiques, les études sur les biomarqueurs mécanistiques et les données de sécurité à long terme afin de valider le potentiel thérapeutique des huiles essentielles dans les TSA et de développer des approches de médecine de précision.
Conclusion commune
Constatations générales : TDAH et autisme
Les deux troubles neurodéveloppementaux, le TDAH et le trouble du spectre autistique (TSA), partagent des similitudes neurobiologiques fondamentales qui rendent plausible une thérapie adjuvante par huiles essentielles pour les deux indications.
Cibles neurobiologiques communes :
Recommandation d'application commune (Nébuliseur Organik Aromas 3.0) :
Pour les deux indications, le principe de nébulisation à froid par venturi, sans eau ni chaleur, s'avère être la forme d'application optimale : - Aucune dégradation thermique des terpènes - Taille de particules précise pour l'absorption olfactive (< 5 µm) - Les huiles pures GC/MS conservent leur intégrité moléculaire
Note importante
La thérapie adjuvante par huiles essentielles ne remplace pas un traitement standard basé sur des preuves (méthylphénidate pour le TDAH, ABA/thérapie comportementale pour le TSA). Elle constitue un complément individuellement adapté et devant être réalisé sous supervision experte. La base de preuves est encore limitée pour les deux indications ; de plus grands essais contrôlés randomisés sont nécessaires.
Références TDAH
[A1] Chen et al. (2008). L'effet de l'application de l'aromathérapie à la cannelle chez les enfants atteints de trouble déficitaire de l'attention avec hyperactivité.https://pmc.ncbi.nlm.nih.gov/articles/PMC8538900/
Chen et al. L'effet de l'application de l'aromathérapie à la cannelle chez les enfants atteints de trouble déficitaire de l'attention avec hyperactivité.https://pmc.ncbi.nlm.nih.gov/articles/PMC8538900/
[A3] Godfrey (2001). Le rôle des huiles essentielles dans le traitement et la gestion du trouble du déficit de l'attention avec hyperactivité. International Journal of Aromatherapy.https://doi.org/10.1016/S0962-4562(01 )80035-7
[A4] Godfrey. Huiles essentielles : traitement complémentaire pour le trouble du déficit de l'attention avec hyperactivité (TDAH).https://www.researchgate.net/publication/248871372_The_role_of_essential_oils_in_the_treatment_and_management_of_attention_deficit_hyperactive_disorder
[A5] Godfrey. LE RÔLE DES HUILES ESSENTIELLES DANS LE TRAITEMENT ET LA GESTION DU TROUBLE DU DÉFICIT DE L'ATTENTION AVEC HYPERACTIVITÉ (TDAH).https://www.researchgate.net/publication/248871372_The_role_of_essential_oils_in_the_treatment_and_management_of_attention_deficit_hyperactive_disorder
[A6] Ding et al. (1994). Pharmacocinétique et spécificité in vivo du [LLC]dl-thréo-méthylphénidate pour le neurone dopaminergique présynaptique. Synapse.https://doi.org/10.1002/SYN.890180207
[A7] Volkow et al. (2002). Mécanisme d'action du méthylphénidate : perspectives tirées d'études d'imagerie par TEP. Journal of Attention Disorders.https://doi.org/10.1177/070674370200601S05
[A8] Silva (2024). L'aromathérapie dans la prise en charge d'un enfant atypique atteint de TDAH et de dermatite atopique.https://doi.org/10.62435/2965-7253.bjhae.2024.iisinaroma1
[A9] Volkow et al. (1998). Occupations du transporteur de dopamine dans le cerveau humain induites par des doses thérapeutiques de méthylphénidate oral. American Journal of Psychiatry.https://doi.org/10.1176/AJP.155.10.1325
[A10] Jacob et al. (2024). Utilisation de l'aromathérapie dans les soins aux étudiants.https://doi.org/10.37885/240717094
[A11] Dipasquale et al. (2020). Démêler les effets du méthylphénidate sur les circuits fonctionnels dopaminergiques et noradrénergiques. bioRxiv.https://doi.org/10.1101/2020.03.09.983528
[A12] Volkow et al. (2002). Rôle de la dopamine dans les effets thérapeutiques et de renforcement du méthylphénidate chez l'homme : résultats d'études d'imagerie. European Neuropsychopharmacology.https://doi.org/10.1016/S0924-977X(02 )00104-9
[A13] Spencer et al. (2006). Étude TEP examinant la pharmacocinétique, la détection et l'agrément, et l'occupation du récepteur du transporteur de dopamine du méthylphénidate oral à courte et longue durée d'action. American Journal of Psychiatry.https://doi.org/10.1176/APPI.AJP.163.3.387
[A14] Castillo et al. (2018). Huiles essentielles comme modificateurs du comportement humain. Systèmes Agroécologiques Tropicaux et Subtropicaux.https://www.revista.ccba.uady.mx/ojs/index.php/TSA/article/view/2583
[A15] Crunelle et al. (2014). Occupation du transporteur de la dopamine par le méthylphénidate et impulsivité chez l'ADHD adulte. British Journal of Psychiatry.https://doi.org/10.1192/BJP.BP.113.132977
[A16] Ding et al. (1997). Médicaments chiraux : comparaison de la pharmacocinétique du [11C]d-thréo et du l-thréo-méthylphénidate dans le cerveau humain et chez le babouin. Psychopharmacology.https://doi.org/10.1007/S002130050267
[A17] Spencer et al. (2009). Une étude par TEP examinant la pharmacocinétique et l'occupation des transporteurs de dopamine de deux formulations à longue durée d'action de méthylphénidate chez l'adulte. International Journal of Molecular Medicine.https://doi.org/10.3892/IJMM_00000339
[A18] Marcel et al. (2024). Réactivité du système dopaminergique striatal au méthylphénidate – une étude SPECT au I-123-β-CIT intra-sujet chez des enfants et adolescents garçons atteints de trouble déficitaire de l'attention/hyperactivité.https://doi.org/10.5283/epub.57629
[A19] Kennedy et al. (2018). Terpènes volatils et fonction cérébrale : Étude des effets cognitifs et sur l'humeur de l'huile essentielle de Mentha × Piperita L. avec des propriétés in vitro pertinentes pour la fonction du système nerveux central. Nutrients.https://doi.org/10.3390/NU10081029
[A20] Batiha et al. (2023). Une revue des composants bioactifs et des propriétés pharmacologiques des espèces de Lavandula. Naunyn-Schmiedebergs Archives of Pharmacology.https://doi.org/10.1007/s00210-023-02392-x
[A21] Guzmán-Gutiérrez et al. (2015). Le linalol et le β-pinène exercent leur activité antidépressive par la voie monoaminergique.https://pubmed.ncbi.nlm.nih.gov/25771248/
[A22] Martinez et al. (2020). Le striatum ventral soutient les effets thérapeutiques du méthylphénidate sur les choix impulsifs exprimés dans une tâche de remise temporelle. Scientific reports.https://doi.org/10.1038/s41598-020-57595-6
[A23] López et al. (2017). Exploration des mécanismes pharmacologiques de l'huile essentielle de lavande (Lavandula angustifolia) sur les cibles du système nerveux central. Frontiers in Pharmacology.https://doi.org/10.3389/FPHAR.2017.00280
[A24] Rathnayake (2025). “ Neuroaromatiques ” : L’aromathérapie et la réponse du système limbique au stress.https://doi.org/10.4038/jssnisd.v3i1.28
[A25] Aster et al. (2021). Réactivité du système dopaminergique striatal au méthylphénidate – une étude I-123-β-CIT-SPECT intra-sujet chez des enfants et adolescents atteints de trouble déficitaire de l'attention avec hyperactivité. medRxiv.https://doi.org/10.1101/2021.11.19.21265993
[A26] Cardoso et al. (2025). L'impact de l'huile essentielle de lavande sur le système nerveux humain : une revue. Journal supprimé.https://doi.org/10.62435/2965-7253.bjhae.2025.bjhae22
[A27] Moss et al. (2003). Les arômes des huiles essentielles de romarin et de lavande affectent différemment la cognition et l'humeur chez des adultes en bonne santé. International Journal of Neuroscience.https://doi.org/10.1080/00207450390161903
[A28] Sinha et al. (2005). Utilisation des médecines complémentaires et alternatives chez les enfants atteints de trouble déficitaire de l'attention avec hyperactivité. Journal of Paediatrics and Child Health.https://doi.org/10.1111/J.1440-1754.2005.00530.X
[A29] Springer et al. (2018). TDAH : Le cycle de vie et les effets de l'adolescence à l'âge adulte.https://dergipark.org.tr/en/pub/pgy/548052.xml
Colzato et al. (2014). Le contrôle attentionnel dans le clignement attentionnel est modulé par les odeurs. Attention Perception & Psychophysics.https://doi.org/10.3758/S13414-014-0733-0
A31. Kennedy, D. O., Scholey, A., Tildesley, N. T. J., Perry, E. K., & Wesnes, K. A. (2002). Modulation de l'humeur et des performances cognitives suite à l'administration aiguë de Melissa officinalis (mélisse). Pharmacologie, Biochimie et Comportement, 72(4), 953–964. https://doi.org/10.1016/S0091-3057(02)00777-3
A32. Müller, S. F., & Klement, S. (2006). Une combinaison de valériane et de mélisse est efficace dans le traitement de l'agitation et de la dyssomnie chez l'enfant. Phytomédicine, 13(6), 383–387. https://doi.org/10.1016/j.phymed.2006.01.013
A33. Scholey, A., Gibbs, A., Neale, C., et al. (2014). Effets anti-stress des aliments contenant de la mélisse. Nutriments, 6(11), 4805–4821. https://doi.org/10.3390/nu6114805
A34. Examen des effets neuroprotecteurs des huiles essentielles, y compris Eucalyptus globulus et Jasminum sambac, sur la fonction cognitive et la pathologie liée à la maladie d'Alzheimer. (2022). Huiles Essentielles Neuroprotectrices : Une Revue.
Références CNT
[B1] Maenner MJ, Shaw KA, Bakian AV, et al. Prévalence et caractéristiques des troubles du spectre autistique chez les enfants de 8 ans — Réseau de surveillance des troubles du développement et de l'autisme, 11 sites, États-Unis, 2018. MMWR Surveill Summ. 2021;70(11):1-16.https://doi.org/10.15585/mmwr.ss7011a1
[B2] Zeidan J, Fombonne E, Scorah J, et al. Prévalence mondiale de l'autisme : une mise à jour de la revue systématique. Autism Res. 2022;15(5):778-790.https://doi.org/10.1002/aur.2696
[B3] Lord C, Elsabbagh M, Baird G, Veenstra-Vanderweele J. Troubles du spectre autistique. Lancet. 2018;392(10146):508-520.https://doi.org/10.1016/S0140-6736(18 )31129-2
[B4] Masi A, DeMayo MM, Glozier N, Guastella AJ. Vue d'ensemble des troubles du spectre autistique, de l'hétérogénéité et des options de traitement. Neurosci Bull. 2017;33(2):183-193.https://doi.org/10.1007/s12264-017-0100-y
[B5] American Psychiatric Association. Manuel diagnostique et statistique des troubles mentaux, cinquième édition (DSM-5). Arlington, VA : American Psychiatric Publishing ; 2013.https://www.psychiatry.org/psychiatrists/practice/dsm
[B6] Marco EJ, Hinkley LB, Hill SS, Nagarajan SS. Traitement sensoriel dans l'autisme : une revue des résultats neurophysiologiques. Pediatr Res. 2011;69(5 Pt 2):48R-54R.https://doi.org/10.1203/PDR.0b013e3182130c54
[B7] Baum SH, Stevenson RA, Wallace MT. Altérations comportementales, perceptives et neuronales de la fonction sensorielle et multisensorielle dans le trouble du spectre autistique. Prog Neurobiol. 2015;134:140-160.https://doi.org/10.1016/j.pneurobio.2015.09.007
[B8] van Steensel FJ, Bögels SM, Perrin S. Troubles anxieux chez les enfants et adolescents atteints de troubles du spectre autistique : une méta-analyse. Clin Child Fam Psychol Rev. 2011;14(3):302-317.https://doi.org/10.1007/s10567-011-0097-0
[B9] Souders MC, Mason TB, Valladares O, et al. Comportements de sommeil et qualité du sommeil chez les enfants atteints de troubles du spectre autistique. Sleep. 2009;32(12):1566-1578.https://doi.org/10.1093/sleep/32.12.1566
[B10] McElhanon BO, McCracken C, Karpen S, Sharp WG. Symptômes gastro-intestinaux dans le trouble du spectre autistique : une méta-analyse. Pediatrics. 2014;133(5):872-883.https://doi.org/10.1542/peds.2013-3995
[B11] Geschwind DH, State MW. Gene hunting in autism spectrum disorder: on the path to precision medicine. Lancet Neurol. 2015;14(11):1109-1120.https://doi.org/10.1016/S1474-4422(15 )00044-7
[B12] De Rubeis S, He X, Goldberg AP, et al. Gènes synaptiques, transcriptionnels et de chromatine perturbés dans l'autisme. Nature. 2014;515(7526):209-215.https://doi.org/10.1038/nature13772
[B13] Sandin S, Lichtenstein P, Kuja-Halkola R, et al. L'héritabilité des troubles du spectre autistique. JAMA. 2017;318(12):1182-1184.https://doi.org/10.1001/jama.2017.12141
[B14] Rubenstein JL, Merzenich MM. Modèle de l'autisme : augmentation du rapport excitation/inhibition dans les systèmes neuronaux clés. Genes Brain Behav. 2003;2(5):255-267.https://doi.org/10.1034/j.1601-183x.2003.00037.x
[B15] Vargas DL, Nascimbene C, Krishnan C, Zimmerman AW, Pardo CA. Activation neurogliale et neuroinflammation dans le cerveau des patients atteints d'autisme. Ann Neurol. 2005;57(1):67-81.https://doi.org/10.1002/ana.20315
[B16] Rossignol DA, Frye RE. Preuves reliant le stress oxydatif, le dysfonctionnement mitochondrial et l'inflammation dans le cerveau des personnes autistes. Front Physiol. 2014;5:150.https://doi.org/10.3389/fphys.2014.00150
[B17] Nelson SB, Valakh V. Équilibre Excitatoire/Inhibiteur et Homéostasie des Circuits dans les Troubles du Spectre Autistique. Neuron. 2015;87(4):684-698.https://doi.org/10.1016/j.neuron.2015.07.033
[B18] Lee E, Lee J, Kim E. Excitation/Inhibition Imbalance in Animal Models of Autism Spectrum Disorders. Biol Psychiatry. 2017;81(10):838-847.https://doi.org/10.1016/j.biopsych.2016.05.011
[B19] Horder J, Lavender T, Mendez MA, et al. Réduction du glutamate/glutamine sous-cortical chez les adultes atteints de troubles du spectre autistique : une étude par [¹H]MRS. Transl Psychiatry. 2013;3:e279.https://doi.org/10.1038/tp.2013.53
[B20] Gaetz W, Bloy L, Wang DJ, et al. Estimation du GABA dans le cerveau d'enfants sur le spectre autistique : précision de la mesure et variation corticale régionale. Neuroimage. 2014;86:1-9.https://doi.org/10.1016/j.neuroimage.2013.05.068
[B21] Rojas DC, Singel D, Steinmetz S, Hepburn S, Brown MS. Diminution de la concentration de GABA périventriculaire gauche chez les enfants autistes et leurs frères et sœurs non atteints. Neuroimage. 2014;86:28-34.https://doi.org/10.1016/j.neuroimage.2013.01.045
[B22] Amaral DG, Schumann CM, Nordahl CW. Neuroanatomie de l'autisme. Trends Neurosci. 2008;31(3):137-145.https://doi.org/10.1016/j.tins.2007.12.005
[B23] Courchesne E, Pierce K. Why the frontal cortex in autism might be talking only to itself: local over-connectivity but long-distance disconnection. Curr Opin Neurobiol. 2005;15(2):225-230.https://doi.org/10.1016/j.conb.2005.03.001
[B24] Baron-Cohen S, Ring HA, Bullmore ET, Wheelwright S, Ashwin C, Williams SC. La théorie de l'amygdale de l'autisme. Neurosci Biobehav Rev. 2000;24(3):355-364.https://doi.org/10.1016/s0149-7634(00 )00011-7
[B25] Estes ML, McAllister AK. Activation immunitaire maternelle : Implications pour les troubles neuropsychiatriques. Science. 2016;353(6301):772-777.https://doi.org/10.1126/science.aag3194
[B26] Matta SM, Hill-Yardin EL, Crack PJ. L'influence de la neuroinflammation dans le trouble du spectre autistique. Brain Behav Immun. 2019;79:75-90.https://doi.org/10.1016/j.bbi.2019.04.037
[B27] Careaga M, Murai T, Bauman MD. Activation immunitaire maternelle et trouble du spectre autistique : des rongeurs aux primates non humains et humains. Biol Psychiatry. 2017;81(5):391-401.https://doi.org/10.1016/j.biopsych.2016.10.020
[B28] Chauhan A, Chauhan V. Stress oxydatif dans l'autisme. Pathophysiology. 2006;13(3):171-181.https://doi.org/10.1016/j.pathophys.2006.05.007
[B29] Rose S, Melnyk S, Pavliv O, et al. Preuves de dommages oxydatifs et d'inflammation associés à un faible statut redox du glutathion dans le cerveau autiste. Transl Psychiatry. 2012;2:e134.https://doi.org/10.1038/tp.2012.61
[B30] Kang DW, Adams JB, Gregory AC, et al. Le transfert de microbiote modifie l'écosystème intestinal et améliore les symptômes gastro-intestinaux et autistiques : une étude ouverte. Microbiome. 2017;5(1):10.https://doi.org/10.1186/s40168-016-0225-7
[B31] Vuong HE, Hsiao EY. Emerging Roles for the Gut Microbiome in Autism Spectrum Disorder. Biol Psychiatry. 2017;81(5):411-423.https://doi.org/10.1016/j.biopsych.2016.08.024
[B32] Sharon G, Cruz NJ, Kang DW, et al. Le microbiote intestinal humain de troubles du spectre autistique favorise les symptômes comportementaux chez la souris. Cell. 2019;177(6):1600-1618.e17.https://doi.org/10.1016/j.cell.2019.05.004
[B33] Sgritta M, Dooling SW, Buffington SA, et al. Mécanismes sous-jacents aux changements médiés par les microbes dans le comportement social chez les modèles murins de trouble du spectre autistique. Neuron. 2019;101(2):246-259.e6.https://doi.org/10.1016/j.neuron.2018.11.018
[B34] Reichow B, Hume K, Barton EE, Boyd BA. Intervention comportementale intensive précoce (ICIP) pour les jeunes enfants atteints de troubles du spectre autistique (TSA). Cochrane Database Syst Rev. 2018;5(5):CD009260.https://doi.org/10.1002/14651858.CD009260.pub3
[B35] Dawson G, Rogers S, Munson J, et al. Essai contrôlé randomisé d'une intervention pour les tout-petits autistes : le modèle Early Start Denver. Pediatrics. 2010;125(1):e17-23.https://doi.org/10.1542/peds.2009-0958
[B36] McCracken JT, McGough J, Shah B, et al. Risperidone chez les enfants autistes présentant des problèmes comportementaux graves. N Engl J Med. 2002;347(5):314-321.https://doi.org/10.1056/NEJMoa013171
[B37] Marcus RN, Owen R, Kamen L, et al. Une étude contrôlée par placebo à dose fixe de l'aripiprazole chez les enfants et les adolescents présentant une irritabilité associée à un trouble autistique. J Am Acad Child Adolesc Psychiatry. 2009;48(11):1110-1119.https://doi.org/10.1097/CHI.0b013e3181b76658
[B38] Scahill L, McDougle CJ, Aman MG, et al. Effets de la rispéridone et de la formation parentale sur le fonctionnement adaptatif chez les enfants atteints de troubles envahissants du développement et de problèmes de comportement graves. J Am Acad Child Adolesc Psychiatry. 2012;51(2):136-146.https://doi.org/10.1016/j.jaac.2011.11.010
[B39] Rossignol DA, Frye RE. Mélatonine dans les troubles du spectre autistique : une revue systématique et une méta-analyse. Dev Med Child Neurol. 2011;53(9):783-792.https://doi.org/10.1111/j.1469-8749.2011.03980.x
[B40] Hollander E, Soorya L, Chaplin W, et al. Essai randomisé en double aveugle contrôlé par placebo de la fluoxétine pour les comportements répétitifs et la gravité globale chez les adultes atteints de troubles du spectre autistique. Am J Psychiatry. 2012;169(3):292-299.https://doi.org/10.1176/appi.ajp.2011.10050764
[B41] Spencer D, Marshall J, Post B, et al. Utilisation de médicaments psychotropes et polypharmacie chez les enfants atteints de troubles du spectre autistique. Pediatrics. 2013;132(5):833-840.https://doi.org/10.1542/peds.2012-3774
[B42] Koulivand PH, Khaleghi Ghadiri M, Gorji A. Lavande et le système nerveux. Evid Based Complement Alternat Med. 2013;2013:681304.https://doi.org/10.1155/2013/681304
[B43] Sowndhararajan K, Kim S. Influence des parfums sur l'activité psychophysiologique humaine : avec une référence spéciale à la réponse électroencéphalographique humaine. Sci Pharm. 2016;84(4):724-751.https://doi.org/10.3390/scipharm84040724
[B44] Ali B, Al-Wabel NA, Shams S, Ahamad A, Khan SA, Anwar F. Huiles essentielles utilisées en aromathérapie : une revue systématique. Asian Pac J Trop Biomed. 2015;5(8):601-611.https://doi.org/10.1016/j.apjtb.2015.05.007
[B45] Sohal VS, Rubenstein JLR. Équilibre excitation-inhibition comme cadre pour l'étude des mécanismes dans les troubles neuropsychiatriques. Mol Psychiatry. 2019;24(9):1248-1257.https://doi.org/10.1038/s41380-019-0426-0
[B46] Antoine MW, Langberg T, Schnepel P, Feldman DE. Un rapport excitation-inhibition accru stabilise le neurone et l'excitabilité du circuit dans quatre modèles murins d'autisme. Neuron. 2019;101(4):648-661.e4.https://doi.org/10.1016/j.neuron.2018.12.026
[B47] Fatemi SH, Halt AR, Stary JM, Kanodia R, Schulz SC, Realmuto GR. Les protéines de la glutamique acide décarboxylase de 65 et 67 kDa sont réduites dans les cortèges pariétaux et cérébelleux autistiques. Biol Psychiatry. 2002;52(8):805-810.https://doi.org/10.1016/s0006-3223(02 )01430-0
[B48] Yip J, Soghomonian JJ, Blatt GJ. Diminution des niveaux d'ARNm de GAD67 dans les cellules de Purkinje du cervelet chez l'autiste : implications physiopathologiques. Acta Neuropathol. 2007;113(5):559-568.https://doi.org/10.1007/s00401-006-0176-3
[B49] Ben-Ari Y. Actions excitatrices du GABA pendant le développement : la nature de la culture. Nat Rev Neurosci. 2002;3(9):728-739.https://doi.org/10.1038/nrn920
[B50] Tyzio R, Nardou R, Ferrari DC, et al. L’inhibition médiée par l’ocytocine du GABA pendant l’accouchement atténue la pathogenèse de l’autisme chez les descendants de rongeurs. Science. 2014;343(6171):675-679.https://doi.org/10.1126/science.1247190
[B51] Lemonnier E, Degrez C, Phelep M, et al. Un essai contrôlé randomisé du bumétanide dans le traitement de l'autisme chez les enfants. Transl Psychiatry. 2012;2:e202.https://doi.org/10.1038/tp.2012.124
Effets du bumétanide sur la fonction neurocomportementale chez les enfants et les adolescents atteints de troubles du spectre autistique. Transl Psychiatry. 2017;7(3):e1056.https://doi.org/10.1038/tp.2017.10
[B53] Carlson GC. Dysfonctionnement des récepteurs glutamates et cibles médicamenteuses dans les modèles de troubles du spectre autistique. Pharmacol Biochem Behav. 2012;100(4):850-854.https://doi.org/10.1016/j.pbb.2011.02.003
[B54] Uzunova G, Pallanti S, Hollander E. Déséquilibre excitateur/inhibiteur dans les troubles du spectre autistique : implications pour les interventions et les thérapies. World J Biol Psychiatry. 2016;17(3):174-186.https://doi.org/10.3109/15622975.2015.1085597
[B55] Yoo HJ, Cho IH, Park M, Yang SY, Kim SA. Association familiale de GRIN2A et GRIN2B avec les troubles du spectre autistique coréens. Neurosci Lett. 2012;512(2):89-93.https://doi.org/10.1016/j.neulet.2012.01.061
[B56] Silverman JL, Tolu SS, Barkan CL, Crawley JN. Le comportement répétitif d'auto-toilette chez la souris BTBR, modèle de l'autisme, est bloqué par l'antagoniste mGluR5 MPEP. Neuropsychopharmacology. 2010;35(4):976-989.https://doi.org/10.1038/npp.2009.201
[B57] Muller CL, Anacker AMJ, Veenstra-VanderWeele J. Le système sérotoninergique dans le trouble du spectre autistique : du biomarqueur aux modèles animaux. Neuroscience. 2016;321:24-41.https://doi.org/10.1016/j.neuroscience.2015.11.010
[B58] Pavăl D. A Dopamine Hypothesis of Autism Spectrum Disorder. Dev Neurosci. 2017;39(5):355-360.https://doi.org/10.1159/000478725
[B59] Schain RJ, Freedman DX. Études sur le métabolisme de la 5-hydroxyindole chez les enfants autistes et autres enfants mentalement déficients. J Pediatr. 1961;58:315-320.https://doi.org/10.1016/s0022-3476(61 )80261-8
[B60] Cook EH Jr, Leventhal BL. Le système sérotoninergique dans l'autisme. Curr Opin Pediatr. 1996 ;8(4):348-354.https://doi.org/10.1097/00008480-199608000-00008
[B61] Chugani DC, Muzik O, Behen M, et al. Changements développementaux dans la capacité de synthèse de la sérotonine cérébrale chez les enfants autistes et non autistes. Ann Neurol. 1999;45(3):287-295.https://doi.org/10.1002/1531-8249(199903 )45:33.0.co;2-9
[B62] Devlin B, Cook EH Jr, Coon H, et al. Autisme et transporteur de sérotonine : les longueurs et les courtes. Mol Psychiatry. 2005;10(12):1110-1116.https://doi.org/10.1038/sj.mp.4001724
[B63] Whitaker-Azmitia PM. Conséquences comportementales et cellulaires de l'augmentation de l'activité sérotoninergique pendant le développement cérébral : un rôle dans l'autisme ? Int J Dev Neurosci. 2005;23(1):75-83.https://doi.org/10.1016/j.ijdevneu.2004.07.022
[B64] King BH, Hollander E, Sikich L, et al. Absence d'efficacité du citalopram chez les enfants atteints de troubles du spectre autistique et présentant des niveaux élevés de comportements répétitifs : le citalopram inefficace chez les enfants autistes. Arch Gen Psychiatry. 2009;66(6):583-590.https://doi.org/10.1001/archgenpsychiatry.2009.30
[B65] Dichter GS, Damiano CA, Allen JA. Dysfonctionnement du circuit de la récompense dans les troubles psychiatriques et neurodéveloppementaux et les syndromes génétiques : modèles animaux et résultats cliniques. J Neurodev Disord. 2012;4(1):19.https://doi.org/10.1186/1866-1955-4-19
[B66] Kohls G, Schulte-Rüther M, Nehrkorn B, et al. Dysfonctionnement du système de récompense dans les troubles du spectre autistique. Soc Cogn Affect Neurosci. 2013;8(5):565-572.https://doi.org/10.1093/scan/nss033
[B67] Delmonte S, Balsters JH, McGrath J, et al. Traitement des récompenses sociales et monétaires dans les troubles du spectre autistique. Mol Autism. 2012;3(1):7.https://doi.org/10.1186/2040-2392-3-7
[B68] Nakamura K, Sekine Y, Ouchi Y, et al. Fixation des transporteurs de sérotonine et de dopamine dans le cerveau chez des adultes atteints d'autisme de haut niveau. Arch Gen Psychiatry. 2010 ; 67 (1) : 59-68.https://doi.org/10.1001/archgenpsychiatry.2009.137
[B69] Staal WG. Autisme, DRD3 et comportements répétitifs et stéréotypés, un aperçu des connaissances actuelles. Eur Neuropsychopharmacol. 2015;25(9):1421-1426.https://doi.org/10.1016/j.euroneuro.2014.08.011
[B70] Gunaydin LA, Grosenick L, Finkelstein JC, et al. Dynamics naturelles des projections neuronales sous-tendant le comportement social. Cell. 2014;157(7):1535-1551.https://doi.org/10.1016/j.cell.2014.05.017
[B71] Insel TR. Le défi de la traduction en neurosciences sociales : une revue de l'ocytocine, de la vasopressine et du comportement d'affiliation. Neuron. 2010;65(6):768-779.https://doi.org/10.1016/j.neuron.2010.03.005
[B72] Modahl C, Green L, Fein D, et al. Niveaux d'ocytocine plasmatique chez les enfants autistes. Biol Psychiatry. 1998;43(4):270-277.https://doi.org/10.1016/s0006-3223(97 )00439-3
[B73] Gregory SG, Connelly JJ, Towers AJ, et al. Evidence génomique et épigénétique d'un déficit du récepteur de l'ocytocine dans l'autisme. BMC Med. 2009;7:62.https://doi.org/10.1186/1741-7015-7-62
[B74] Guastella AJ, Einfeld SL, Gray KM, et al. L'ocytocine intranasale améliore la reconnaissance des émotions chez les jeunes atteints de troubles du spectre autistique. Biol Psychiatry. 2010;67(7):692-694.https://doi.org/10.1016/j.biopsych.2009.09.020
[B75] Parker KJ, Oztan O, Libove RA, et al. Traitement par ocytocine intranasale pour les déficits sociaux et les biomarqueurs de réponse chez les enfants autistes. Proc Natl Acad Sci U S A. 2017;114(30):8119-8124.https://doi.org/10.1073/pnas.1705521114
[B76] Peñagarikano O, Lázaro MT, Lu XH, et al. L'ocytocine exogène et évoquée restaure le comportement social chez la souris modèle du Cntnap2 autiste. Sci Transl Med. 2015;7(271):271ra8.https://doi.org/10.1126/scitranslmed.3010257
[B77] Pardo CA, Vargas DL, Zimmerman AW. Immunité, neuroglie et neuroinflammation dans l'autisme. Int Rev Psychiatry. 2005;17(6):485-495.https://doi.org/10.1080/02646830500381930
[B78] Edmonson C, Ziats MN, Rennert OM. Expression altérée des marqueurs gliaux dans le cortex préfrontal et le cervelet post-mortem autistes. Mol Autism. 2014;5:3.https://doi.org/10.1186/2040-2392-5-3
[B79] Salter MW, Stevens B. La microglie émerge comme un acteur central dans les maladies du cerveau. Nat Med. 2017;23(9):1018-1027.https://doi.org/10.1038/nm.4397
[B80] Morgan JT, Chana G, Pardo CA, et al. Activation microgliale et augmentation de la densité microgliale observées dans le cortex préfrontal dorsolatéral chez les autistes. Biol Psychiatry. 2010;68(4):368-376.https://doi.org/10.1016/j.biopsych.2010.05.024
[B81] Suzuki K, Sugihara G, Ouchi Y, et al. Activation microgliale chez de jeunes adultes atteints de trouble du spectre autistique. JAMA Psychiatry. 2013;70(1):49-58.https://doi.org/10.1001/jamapsychiatry.2013.272
[B82] Zürcher NR, Loggia ML, Lawson R, et al. Activation gliale accrue in vivo chez les patients atteints de sclérose latérale amyotrophique : évaluation avec le [(11)C]-PBR28. Neuroimage Clin. 2015;7:409-414.https://doi.org/10.1016/j.nicl.2015.01.009
[B83] Schafer DP, Lehrman EK, Kautzman AG, et al. Les microglies sculptent les circuits neuronaux postnataux d'une manière dépendante de l'activité et du complément. Neuron. 2012;74(4):691-705.https://doi.org/10.1016/j.neuron.2012.03.026
[B84] Ashwood P, Krakowiak P, Hertz-Picciotto I, Hansen R, Pessah I, Van de Water J. Les cytokines plasmatiques élevées dans les troubles du spectre autistique apportent des preuves de dysfonctionnement immunitaire et sont associées à un résultat comportemental altéré. Brain Behav Immun. 2011;25(1):40-45.https://doi.org/10.1016/j.bbi.2010.08.003
[B85] Li X, Chauhan A, Sheikh AM, et al. Réponse immunitaire élevée dans le cerveau de patients autistes. J Neuroimmunol. 2009;207(1-2):111-116.https://doi.org/10.1016/j.jneuroim.2008.12.002
[B86] Smith SE, Li J, Garbett K, Mirnics K, Patterson PH. L’activation immunitaire maternelle altère le développement cérébral fœtal via l’interleukine-6. J Neurosci. 2007;27(40):10695-10702.https://doi.org/10.1523/JNEUROSCI.2178-07.2007
[B87] Choi GB, Yim YS, Wong H, et al. La voie de l'interleukine-17a maternelle chez la souris favorise des phénotypes analogues à l'autisme chez la progéniture. Science. 2016;351(6276):933-939.https://doi.org/10.1126/science.aad0314
[B88] Stellwagen D, Malenka RC. Stellwagen D, Malenka RC. La mise à l'échelle synaptique médiatisée par le TNF-alpha glial. Nature. 2006;440(7087):1054-1059.https://doi.org/10.1038/nature04671
[B89] Wei H, Chadman KK, McCloskey DP, et al. L'élévation de l'IL-6 dans le cerveau provoque des déséquilibres des circuits neuronaux et un comportement de type autiste. Biochim Biophys Acta. 2012;1822(6):831-842.https://doi.org/10.1016/j.bbadis.2012.01.011
[B90] Verkhratsky A, Nedergaard M. Physiologie de l'astroglie. Physiol Rev. 2018;98(1):239-389.https://doi.org/10.1152/physrev.00042.2016
[B91] Laurence JA, Fatemi SH. L'acide Glial fibrillary acidic protein est élevé dans les cortices frontaux supérieurs, pariétaux et cérébelleux des sujets autistes. Cerebellum. 2005;4(3):206-210.https://doi.org/10.1080/14734220500208846
[B92] Rothstein JD, Dykes-Hoberg M, Pardo CA, et al. L'invalidation des transporteurs de glutamate révèle un rôle majeur du transport astroglial dans l'excitotoxicité et la clairance du glutamate. Neuron. 1996;16(3):675-686.https://doi.org/10.1016/s0896-6273(00 )80086-0
[B93] Sies H, Jones DP. Espèces réactives de l'oxygène (ROS) en tant qu'agents de signalisation physiologiques pléiotropes. Nat Rev Mol Cell Biol. 2020;21(7):363-383.https://doi.org/10.1038/s41580-020-0230-3
[B94] Frustaci A, Neri M, Cesario A, et al. Biomarqueurs liés au stress oxydatif dans l'autisme : revue systématique et méta-analyses. Free Radic Biol Med. 2012;52(10):2128-2141.https://doi.org/10.1016/j.freeradbiomed.2012.03.011
[B95] Bjørklund G, Meguid NA, El-Bana MA, et al. Stress oxydatif dans les troubles du spectre autistique. Mol Neurobiol. 2020;57(5):2314-2332.https://doi.org/10.1007/s12035-019-01742-2
[B96] James SJ, Cutler P, Melnyk S, et al. Biomarqueurs métaboliques de stress oxydatif accru et de capacité de méthylation altérée chez les enfants autistes. Am J Clin Nutr. 2004;80(6):1611-1617.https://doi.org/10.1093/ajcn/80.6.1611
[B97] Rose S, Melnyk S, Pavliv O, et al. Preuves de dommages oxydatifs et d'inflammation associés à un faible statut redox du glutathion dans le cerveau autiste. Transl Psychiatry. 2012;2:e134.https://doi.org/10.1038/tp.2012.61
[B98] Bowers K, Li Q, Bressler J, et al. Variation génétique dans la voie du glutathion et risque de troubles du spectre autistique. J Neurodev Disord. 2011;3(2):132-143.https://doi.org/10.1007/s11689-011-9077-4
[B99] Rossignol DA, Frye RE. Dysfonctionnement mitochondrial dans les troubles du spectre autistique : une revue systématique et une méta-analyse. Mol Psychiatry. 2012;17(3):290-314.https://doi.org/10.1038/mp.2010.136
[B100] Giulivi C, Zhang YF, Omanska-Klusek A, et al. Dysfonctionnement mitochondrial dans l'autisme. JAMA. 2010;304(21):2389-2396.https://doi.org/10.1001/jama.2010.1706
[B101] Duchen MR. Mitochondria and calcium: from cell signalling to cell death. J Physiol. 2000;529 Pt 1(Pt 1):57-68.https://doi.org/10.1111/j.1469-7793.2000.00057.x
[B102] Bambini-Junior V, Rodrigues L, Behr GA, et al. Modèle animal d'autisme induit par une exposition prénatale au valproate : modifications comportementales et paramètres hépatiques. Brain Res. 2011;1408:8-16.https://doi.org/10.1016/j.brainres.2011.06.015
[B103] Ma Q. Rôle du nrf2 dans le stress oxydatif et la toxicité. Annu Rev Pharmacol Toxicol. 2013;53:401-426.https://doi.org/10.1146/annurev-pharmtox-011112-140320
[B104] Singh K, Connors SL, Macklin EA, et al. Traitement par sulforaphane du trouble du spectre autistique (TSA). Proc Natl Acad Sci U S A. 2014;111(43):15550-15555.https://doi.org/10.1073/pnas.1416940111
[B105] Bent S, Lawton B, Warren T, et al. Identification de métabolites urinaires corrélés aux améliorations cliniques chez les enfants autistes traités par sulforaphane de brocoli. Mol Autism. 2018;9:35.https://doi.org/10.1186/s13229-018-0218-4
[B106] Cryan JF, O’Riordan KJ, Cowan CSM, et al. L’axe Microbiote-Intestin-Cerveau. Physiol Rev. 2019;99(4):1877-2013.https://doi.org/10.1152/physrev.00018.2018
[B107] Chaidez V, Hansen RL, Hertz-Picciotto I. Troubles gastro-intestinaux chez les enfants autistes, ayant des retards de développement ou un développement typique. J Autism Dev Disord. 2014;44(5):1117-1127.https://doi.org/10.1007/s10803-013-1973-x
[B108] Adams JB, Johansen LJ, Powell LD, Quig D, Rubin RA. Flore gastro-intestinale et état gastro-intestinal chez des enfants autistes – comparaisons avec des enfants typiques et corrélation avec la gravité de l'autisme. BMC Gastroenterol. 2011;11:22.https://doi.org/10.1186/1471-230X-11-22
[B109] Xu M, Xu X, Li J, Li F. Association Between Gut Microbiota and Autism Spectrum Disorder: A Systematic Review and Meta-Analysis. Front Psychiatry. 2019;10:473.https://doi.org/10.3389/fpsyt.2019.00473
[B110] Liu F, Li J, Wu F, et al. Composition et fonction altérées du microbiote intestinal dans les troubles du spectre autistique : une revue systématique. Transl Psychiatry. 2019;9(1):43.https://doi.org/10.1038/s41398-019-0389-6
[B111] Kang DW, Park JG, Ilhan ZE, et al. Incidence réduite de Prevotella et d’autres fermentaires dans la microflore intestinale des enfants autistes. PLoS One. 2013;8(7):e68322.https://doi.org/10.1371/journal.pone.0068322
[B112] Stilling RM, van de Wouw M, Clarke G, Stanton C, Dinan TG, Cryan JF. La neuropharmacologie du butyrate : le quotidien de l'axe microbiote-intestin-cerveau ? Neurochem Int. 2016;99:110-132.https://doi.org/10.1016/j.neuint.2016.06.011
[B113] MacFabe DF, Cain DP, Rodriguez-Capote K, et al. Effets neurobiologiques de l'acide propionique intraventriculaire chez le rat : rôle possible des acides gras à chaîne courte sur la pathogenèse et les caractéristiques des troubles du spectre autistique. Behav Brain Res. 2007;176(1):149-169.https://doi.org/10.1016/j.bbr.2006.07.025
[B114] Hsiao EY, McBride SW, Hsien S, et al. Le microbiote module les anomalies comportementales et physiologiques associées aux troubles du neurodéveloppement. Cell. 2013;155(7):1451-1463.https://doi.org/10.1016/j.cell.2013.11.024
[B115] Bonaz B, Bazin T, Pellissier S. Le nerf vague à l'interface de l'axe microbiote-intestin-cerveau. Front Neurosci. 2018;12:49.https://doi.org/10.3389/fnins.2018.00049
[B116] Liu S, Hagiwara SI, Bhargava A. Adversité précoce, épigénétique et hypersensibilité viscérale. Neurogastroenterol Motil. 2017;29(9).https://doi.org/10.1111/nmo.13170
[B117] Zoghbi HY, Bear MF. Dysfonction synaptique dans les troubles du neurodéveloppement associés à l'autisme et aux déficiences intellectuelles. Cold Spring Harb Perspect Biol. 2012;4(3):a009886.https://doi.org/10.1101/cshperspect.a009886
[B118] Bourgeron T. De l'architecture génétique à la plasticité synaptique dans les troubles du spectre autistique. Nat Rev Neurosci. 2015;16(9):551-563.https://doi.org/10.1038/nrn3992
[B119] Südhof TC. Les neuroligines et les neurexines lient la fonction synaptique aux maladies cognitives. Nature. 2008;455(7215):903-911.https://doi.org/10.1038/nature07456
[B120] Jamain S, Quach H, Betancur C, et al. Les mutations des gènes liés à l'X codant pour les neuroligines NLGN3 et NLGN4 sont associées à l'autisme. Nat Genet. 2003;34(1):27-29.https://doi.org/10.1038/ng1136
[B121] Tabuchi K, Blundell J, Etherton MR, et al. Une mutation de la neuroligine-3 impliquée dans l'autisme augmente la transmission synaptique inhibitrice chez la souris. Science. 2007;318(5847):71-76.https://doi.org/10.1126/science.1146221
[B122] Jamain S, Radyushkin K, Hammerschmidt K, et al. Interaction sociale réduite et communication ultrasonique dans un modèle murin d'autisme monogénique héréditaire. Proc Natl Acad Sci U S A. 2008;105(5):1710-1715.https://doi.org/10.1073/pnas.0711555105
[B123] Grabrucker AM, Schmeisser MJ, Schoen M, Boeckers TM. Les échafaudages ProSAP/Shank postsynaptiques dans la mire des synaptopathies. Trends Cell Biol. 2011;21(10):594-603.https://doi.org/10.1016/j.tcb.2011.07.003
[B124] Phelan K, McDermid HE. Le syndrome de délétion 22q13.3 (Syndrome de Phelan-McDermid). Mol Syndromol. 2012;2(3-5):186-201.https://doi.org/10.1159/000334260
[B125] Peça J, Feliciano C, Ting JT, et al. Les souris mutantes Shank3 présentent des comportements de type autistique et une dysfonction striatale. Nature. 2011;472(7344):437-442.https://doi.org/10.1038/nature09965
[B126] Won H, Lee HR, Gee HY, et al. Comportement social de type autistique chez des souris mutantes Shank2 amélioré par la restauration de la fonction du récepteur NMDA. Nature. 2012;486(7402):261-265.https://doi.org/10.1038/nature11208
[B127] Baudouin SJ, Gaudias J, Gerharz S, et al. Physiopathologie synaptique partagée dans des modèles de rongeurs syndromiques et non syndromiques d'autisme. Science. 2012;338(6103):128-132.https://doi.org/10.1126/science.1224159
[B128] Huber KM, Gallagher SM, Warren ST, Bear MF. Plasticité synaptique altérée dans un modèle murin de retard mental du syndrome de l'X fragile. Proc Natl Acad Sci U S A. 2002;99(11):7746-7750.https://doi.org/10.1073/pnas.122205699
[B129] Ecker C, Bookheimer SY, Murphy DG. Neuroimagerie dans les troubles du spectre autistique : structure et fonction du cerveau tout au long de la vie. Lancet Neurol. 2015;14(11):1121-1134.https://doi.org/10.1016/S1474-4422(15 )00050-2
[B130] Hazlett HC, Gu H, Munsell BC, et al. Développement précoce du cerveau chez les nourrissons à haut risque de trouble du spectre autistique. Nature. 2017;542(7641):348-351.https://doi.org/10.1038/nature21369
[B131] Miller EK, Cohen JD. Une théorie intégrative de la fonction du cortex préfrontal. Annu Rev Neurosci. 2001;24:167-202.https://doi.org/10.1146/annurev.neuro.24.1.167
[B132] Castelli F, Frith C, Happé F, Frith U. Autism, Asperger syndrome et mécanismes cérébraux pour l'attribution d'états mentaux à des formes animées. Brain. 2002;125(Pt 8):1839-1849.https://doi.org/10.1093/brain/awf189
[B133] Just MA, Cherkassky VL, Keller TA, Kana RK, Minshew NJ. Sous-connectivité corticale fonctionnelle et anatomique dans l'autisme : preuves d'une étude IRMf d'une tâche de fonction exécutive et de morphométrie du corps calleux. Cereb Cortex. 2007;17(4):951-961.https://doi.org/10.1093/cercor/bhl006
[B134] Casanova MF, Buxhoeveden DP, Switala AE, Roy E. Pathologie minicolonnaire dans l'autisme. Neurology. 2002;58(3):428-432.https://doi.org/10.1212/wnl.58.3.428
[B135] Adolphs R. Le cerveau social : base neurale de la connaissance sociale. Annu Rev Psychol. 2009 ;60:693-716.https://doi.org/10.1146/annurev.psych.60.110707.163514
[B136] Nordahl CW, Scholz R, Yang X, et al. Augmentation de la croissance de l'amygdale chez les enfants de 2 à 4 ans atteints de troubles du spectre autistique : une étude longitudinale. Arch Gen Psychiatry. 2012;69(1):53-61.https://doi.org/10.1001/archgenpsychiatry.2011.145
[B137] Kleinhans NM, Richards T, Sterling L, et al. Connectivité fonctionnelle anormale dans les troubles du spectre autistique lors du traitement des visages. Brain. 2008;131(Pt 4):1000-1012.https://doi.org/10.1093/brain/awm334
[B138] Monk CS, Weng SJ, Wiggins JL, et al. Les circuits neuronaux du traitement des visages émotionnels dans les troubles du spectre autistique. J Psychiatry Neurosci. 2010;35(2):105-114.https://doi.org/10.1503/jpn.090085
[B139] Schmahmann JD. Le cervelet et la cognition. Neurosci Lett. 2019;688:62-75.https://doi.org/10.1016/j.neulet.2018.07.005
[B140] Fatemi SH, Aldinger KA, Ashwood P, et al. Consensus paper: pathological role of the cerebellum in autism. Cerebellum. 2012;11(3):777-807.https://doi.org/10.1007/s12311-012-0355-9
[B141] Courchesne E, Yeung-Courchesne R, Press GA, Hesselink JR, Jernigan TL. Hypoplasie des lobules VI et VII du vermis cérébelleux dans l'autisme. N Engl J Med. 1988;318(21):1349-1354.https://doi.org/10.1056/NEJM198805263182102
[B142] Wang SS, Kloth AD, Badura A. Le cervelet, les périodes sensibles et l'autisme. Neuron. 2014;83(3):518-532.https://doi.org/10.1016/j.neuron.2014.07.016
[B143] Squire LR, Stark CE, Clark RE. Le lobe temporal médian. Annu Rev Neurosci. 2004;27:279-306.https://doi.org/10.1146/annurev.neuro.27.070203.144130
[B144] Schumann CM, Hamstra J, Goodlin-Jones BL, et al. L'amygdale est hypertrophiée chez les enfants mais pas chez les adolescents atteints d'autisme ; l'hippocampe est hypertrophié à tous les âges. J Neurosci. 2004;24(28):6392-6401.https://doi.org/10.1523/JNEUROSCI.1297-04.2004
[B145] Gaigg SB, Bowler DM. Rappel libre et oubli des mots émotionnellement stimulants dans le spectre de l'autisme. Neuropsychologia. 2008 ;46(9):2336-2343.https://doi.org/10.1016/j.neuropsychologia.2008.03.008
[B146] Graybiel AM. Les noyaux gris centraux. Curr Biol. 2000;10(14):R509-R511.https://doi.org/10.1016/s0960-9822(00 )00593-5
[B147] Langen M, Durston S, Staal WG, Palmen SJ, van Engeland H. Le noyau caudé est agrandi chez des sujets autistes à haut fonctionnement et naïfs de traitement. Biol Psychiatry. 2007;62(3):262-266.https://doi.org/10.1016/j.biopsych.2006.09.040
[B148] Scott-Van Zeeland AA, Dapretto M, Ghahremani DG, Poldrack RA, Bookheimer SY. Traitement de la récompense dans l'autisme. Autism Res. 2010;3(2):53-67.https://doi.org/10.1002/aur.122
[B149] Gershenzon J, Dudareva N. La fonction des produits naturels terpéniques dans le monde naturel. Nat Chem Biol. 2007;3(7):408-414.https://doi.org/10.1038/nchembio.2007.5
[B150] Russo EB. Dompter le THC : synergie potentielle du cannabis et effets d'entourage des phytocannabinoïdes-terpénoïdes. Br J Pharmacol. 2011;163(7):1344-1364.https://doi.org/10.1111/j.1476-5381.2011.01238.x
[B151] Aprotosoaie AC, Hăncianu M, Costache II, Miron A. Le linalol : revue d'une molécule odorante clé aux propriétés biologiques intéressantes. Flavour Fragr J. 2014;29(4):193-219.https://doi.org/10.1002/ffj.3197
[B152] Harada H, Kashiwadani H, Kanmura Y, Kuwaki T. Effets anxiolytiques induits par l'odeur du linalol chez la souris. Front Behav Neurosci. 2018;12:241.https://doi.org/10.3389/fnbeh.2018.00241
[B153] Elisabetsky E, Brum LF, Souza DO. Propriétés anticonvulsivantes du linalol dans des modèles de crises liées au glutamate. Phytomedicine. 1999;6(2):107-113.https://doi.org/10.1016/S0944-7113(99 )80044-0
Linck VM, da Silva AL, Figueiró M, et al. Effets de l'inhalation de linalol sur l'anxiété, l'interaction sociale et le comportement agressif chez la souris. Phytomedicine. 2010;17(8-9):679-683.https://doi.org/10.1016/j.phymed.2009.10.002
[B155] Takahashi M, Satou T, Ohashi M, Hayashi S, Sadamoto K, Koike K. Comparaison interspécifique de la composition chimique et des effets anxiolytiques des huiles de lavande par inhalation. Nat Prod Commun. 2011;6(11):1769-1774.https://journals.sagepub.com/doi/10.1177/1934578X1100601148
[B156] Peana AT, D’Aquila PS, Panin F, Serra G, Pippia P, Moretti MD. Activité anti-inflammatoire du linalool et de l'acétate de linalyle, constituants des huiles essentielles. Phytomedicine. 2002;9(8):721-726.https://doi.org/10.1078/094471102321621322
[B157] Sabogal-Guáqueta AM, Posada-Duque R, Cortes NC, Arias-Londoño JD, Cardona-Gómez GP. Les changements dans les profils de phospholipides hippocampiques et périphériques sont associés à des signes de neurodégénérescence dans un modèle d'ischémie cérébrale globale à long terme : Atténuation par le linalol. Neuropharmacology. 2018;135:555-571.https://doi.org/10.1016/j.neuropharm.2018.04.015
[B158] Jäger W, Buchbauer G, Jirovetz L, Fritzer M. Absorption percutanée de l'huile de lavande à partir d'une huile de massage. J Soc Cosmet Chem. 1992;43:49-54.https://www.researchgate.net/publication/232711524_Percutaneous_absorption_of_lavender_oil_from_a_massage_oil
[B159] Buchbauer G. Activités biologiques des huiles essentielles. In : Baser KHC, Buchbauer G, éd. Handbook of Essential Oils: Science, Technology, and Applications. 2e éd. CRC Press ; 2015 : 235-280.https://www.routledge.com/Handbook-of-Essential-Oils-Science-Technology-and-Applications/Baser-Buchbauer/p/book/9781032046419
[B160] Gertsch J, Leonti M, Raduner S, et al. Le bêta-caryophyllène est un cannabinoïde alimentaire. Proc Natl Acad Sci U S A. 2008;105(26):9099-9104.https://doi.org/10.1073/pnas.0803601105
[B161] Bahi A, Al Mansouri S, Al Memari E, Al Ameri M, Nurulain SM, Ojha S. Le β-caryophyllène, un agoniste des récepteurs CB2, produit plusieurs changements comportementaux pertinents pour l'anxiété et la dépression chez la souris. Physiol Behav. 2014;135:119-124.https://doi.org/10.1016/j.physbeh.2014.06.003
[B162] Atwood BK, Mackie K. CB2 : un récepteur cannabinoïde en crise d'identité. Br J Pharmacol. 2010;160(3):467-479.https://doi.org/10.1111/j.1476-5381.2010.00729.x
[B163] Klauke AL, Racz I, Pradier B, et al. Le phytocannabinoïde bêta-caryophyllène, sélectif du récepteur cannabinoïde CB₂, exerce des effets analgésiques dans des modèles murins de douleur inflammatoire et neuropathique. Eur Neuropsychopharmacol. 2014;24(4):608-620.https://doi.org/10.1016/j.euroneuro.2013.10.008
[B164] Cheng Y, Dong Z, Liu S. Le β-caryophyllène améliore le phénotype de type Alzheimer chez les souris APP/PS1 par activation du récepteur CB2 et la voie PPARγ. Pharmacology. 2014;94(1-2):1-12.https://doi.org/10.1159/000362689
[B165] Askari VR, Shafiee-Nick R. Effets neuroprotecteurs prometteurs du β-caryophyllène contre la toxicité des oligodendrocytes induite par le LPS : une étude mécanistique. Biochem Pharmacol. 2019;159:154-171.https://doi.org/10.1016/j.bcp.2018.12.001
[B166] Fontes LBA, Dias D, Aarestrup BJ, et al. Le β-Caryophyllène améliore le développement de l'encéphalomyélite auto-immune expérimentale chez des souris C57BL/6. Biomed Pharmacother. 2017;91:257-264.https://doi.org/10.1016/j.biopha.2017.04.092
[B167] Alberti TB, Barbosa WL, Vieira JL, Raposo NR, Dutra RC. Le (-)-β-Caryophyllène, un phytocannabinoïde sélectif des récepteurs CB2, supprime la paralysie motrice et la neuroinflammation dans un modèle murin de sclérose en plaques. Int J Mol Sci. 2017;18(4):691.https://doi.org/10.3390/ijms18040691
[B168] Galdino PM, Nascimento MV, Florentino IF, et al. Effet anxiolytique d'une huile essentielle dérivée des feuilles de Spiranthera odoratissima A. St. Hil. et de son composant principal, le β-cariofillène, chez la souris mâle. Prog Neuropsychopharmacol Biol Psychiatry. 2012;38(2):276-284.https://doi.org/10.1016/j.pnpbp.2012.04.012
[B169] Horváth B, Mukhopadhyay P, Kechrid M, et al. Le β-caryophyllène améliore la néphrotoxicité induite par le cisplatine d'une manière dépendante du récepteur cannabinoïde 2. Free Radic Biol Med. 2012;52(8):1325-1333.https://doi.org/10.1016/j.freeradbiomed.2012.01.014
[B170] Fidyt K, Fiedorowicz A, Strządała L, Szumny A. Le β-caryophyllène et l'oxyde de β-caryophyllène - composés naturels aux propriétés anticancéreuses et analgésiques. Cancer Med. 2016;5(10):3007-3017.https://doi.org/10.1002/cam4.816
[B171] Sharma C, Al Kaabi JM, Nurulain SM, Goyal SN, Kamal MA, Ojha S. Propriétés pharmacologiques multiples et potentiel thérapeutique du β-caryophyllène : un phytocannabinoïde alimentaire prometteur en pharmacie. Curr Pharm Des. 2016;22(21):3237-3264.https://doi.org/10.2174/1381612822666160311115226
[B172] Ammon HP. Acides boswelliques et leur rôle dans les maladies inflammatoires chroniques. Adv Exp Med Biol. 2016;928:291-327.https://doi.org/10.1007/978-3-319-41334-1_13
[B173] Catanzaro D, Rancan S, Orso G, et al. Boswellia serrata préserve la barrière épithéliale intestinale des dommages oxydatifs et inflammatoires. PLoS One. 2015;10(5):e0125375.https://doi.org/10.1371/journal.pone.0125375
[B174] Khoshnazar M, Bigdeli MR, Parvardeh S, Pouriran R. Effet atténuant de l'α-pinène sur le déficit neurocomportemental, les dommages oxydatifs et la réponse inflammatoire suite à un accident vasculaire cérébral ischémique focal chez le rat. J Pharm Pharmacol. 2019;71(11):1725-1733.https://doi.org/10.1111/jphp.13164
[B175] Ryter SW, Alam J, Choi AM. Hémoxygénase-1/monoxyde de carbone : de la science fondamentale aux applications thérapeutiques. Physiol Rev. 2006;86(2):583-650.https://doi.org/10.1152/physrev.00011.2005
[B176] Umar S, Umar K, Sarwar AH, et al. L'extrait de Boswellia serrata atténue les médiateurs inflammatoires et le stress oxydatif dans l'arthrite induite par le collagène. Phytomedicine. 2014;21(6):847-856.https://doi.org/10.1016/j.phymed.2014.02.001
[B177] Abdel-Tawab M, Werz O, Schubert-Zsilavecz M. Boswellia serrata : évaluation globale des données in vitro, précliniques, pharmacocinétiques et cliniques. Clin Pharmacokinet. 2011;50(6):349-369.https://doi.org/10.2165/11586800-000000000-00000
[B178] Hosseini M, Hadjzadeh MA, Derakhshan M, et al. Les effets bénéfiques de l'olibanum sur le déficit de la mémoire induit par l'hypothyroïdie chez des rats adultes testés dans le Morris water maze. Arch Pharm Res. 2010;33(3):463-468.https://doi.org/10.1007/s12272-010-0316-6
[B179] Safayhi H, Mack T, Sabieraj J, Anazodo MI, Subramanian LR, Ammon HP. Acides boswelliques : nouveaux inhibiteurs spécifiques et non redox de la 5-lipoxygénase. J Pharmacol Exp Ther. 1992;261(3):1143-1146.https://www.sciencedirect.com/science/article/abs/pii/S0022356525111300
[B180] Werz O. 5-lipoxygénase : biologie cellulaire et pharmacologie moléculaire. Curr Drug Targets Inflamm Allergy. 2002;1(1):23-44.https://doi.org/10.2174/1568010023344959
[B181] Al-Harrasi A, Ali L, Hussain J, et al. Effets analgésiques d'extraits bruts et de fractions de l'encens omanais obtenus à partir de la plante médicinale traditionnelle Boswellia sacra sur des modèles animaux. Asian Pac J Trop Med. 2014;7S1:S485-S490.https://doi.org/10.1016/S1995-7645(14 )60279-0
[B182] Cimanga K, Kambu K, Tona L, et al. Corrélation entre la composition chimique et l'activité antibactérienne des huiles essentielles de certaines plantes médicinales aromatiques poussant en République démocratique du Congo. J Ethnopharmacol. 2002;79(2):213-220.https://doi.org/10.1016/s0378-8741(01 )00384-1
[B183] Satou T, Kasuya H, Maeda K, Koike K. Inhalation quotidienne d'α-pinène chez la souris : effets sur le comportement et l'accumulation dans les organes. Phytother Res. 2014;28(9):1284-1287.https://doi.org/10.1002/ptr.5105
[B184] Satou T, Murakami S, Matsuura M, Hayashi S, Koike K. Effet anxiolytique et distribution tissulaire de l'huile essentielle inhalée d'Alpinia zerumbet chez la souris. Nat Prod Commun. 2010;5(1):143-146.https://journals.sagepub.com/doi/10.1177/1934578X1000500133
[B185] Juergens UR, Dethlefsen U, Steinkamp G, Gillissen A, Repges R, Vetter H. Activité anti-inflammatoire du 1,8-cinéole (eucalyptol) dans l'asthme bronchique : un essai randomisé en double aveugle contrôlé par placebo. Respir Med. 2003;97(3):250-256.https://doi.org/10.1053/rmed.2003.1432
[B186] Santos FA, Rao VS. Effets anti-inflammatoires et antinociceptifs du 1,8-cinéole, un oxyde terpénoïde présent dans de nombreuses huiles essentielles végétales. Phytother Res. 2000;14(4):240-244.https://doi.org/10.1002/1099-1573(200006 14:43.0.co;2-x
[B187] Tisserand R, Young R. Essential Oil Safety: A Guide for Health Care Professionals. 2e éd. Churchill Livingstone ; 2014.https://www.elsevier.com/books/essential-oil-safety/tisserand/978-0-7020-4606-4
[B188] Worth H, Schacher C, Dethlefsen U. La thérapie concomitante avec le cinéole (eucalyptol) réduit les exacerbations dans la BPCO : essai randomisé en double aveugle contrôlé par placebo. Respir Res. 2009;10:69.https://doi.org/10.1186/1465-9921-10-69
[B189] Salehi B, Upadhyay S, Erdogan Orhan I, et al. Potentiel thérapeutique de l'α- et du β-pinène : un don miraculeux de la nature. Biomolecules. 2019 ; 9(11) : 738.https://doi.org/10.3390/biom9110738
[B190] Guzmán-Gutiérrez SL, Gómez-Cansino R, García-Zebadúa JC, Jiménez-Pérez NC, Reyes-Chilpa R. Activité antidépressive de l'huile essentielle de Litsea glaucescens : identification du β-pinène et du linalool comme principes actifs. J Ethnopharmacol. 2012;143(2):673-679.https://doi.org/10.1016/j.jep.2012.07.026
[B191] Yang H, Woo J, Pae AN, et al. L'α-pinène, un constituant majeur des huiles de pin, améliore le sommeil paradoxal chez la souris via les récepteurs GABAA-benzodiazépine. Mol Pharmacol. 2016;90(5):530-539.https://doi.org/10.1124/mol.116.105080
[B192] Kim DS, Lee HJ, Jeon YD, et al. L'alpha-pinène présente une activité anti-inflammatoire par la suppression de la MAP kinase et de la voie NF-κB dans les macrophages péritonéaux de souris. Am J Chin Med. 2015;43(4):731-742.https://doi.org/10.1142/S0192415X15500457
Propriétés protectrices de l'huile essentielle de Salvia lavandulifolia Vahl. contre les lésions neuronales induites par le stress oxydatif.https://doi.org/10.1016/j.fct.2015.03.002
[B194] Miyazawa M, Watanabe H, Kameoka H. Inhibition de l'activité de l'acétylcholinestérase par des monoterpénoïdes avec un squelette p-menthane. J Agric Food Chem. 1997;45(3):677-679.https://doi.org/10.1021/jf960398b
[B195] Deutsch SI, Burket JA, Katz E. La perturbation subtile de la migration neuronale contribue-t-elle à la schizophrénie et à d'autres troubles du neurodéveloppement ? Mécanismes génétiques potentiels avec implications thérapeutiques possibles. Eur Neuropsychopharmacol. 2010;20(5):281-287.https://doi.org/10.1016/j.euroneuro.2010.02.005
[B196] Tan LT, Lee LH, Yin WF, et al. Utilisations traditionnelles, phytochimie et bioactivités de Cananga odorata (Ylang-Ylang). Evid Based Complement Alternat Med. 2015;2015:896314.https://doi.org/10.1155/2015/896314
[B197] Jung YH, Ha TM, Ahn J, et al. L'inhalation d'huile essentielle de Cananga odorata a amélioré l'interaction sociale et les comportements d'anxiété chez les rats atteints de troubles du spectre autistique induits par l'acide valproïque. Nutrients. 2021;13(11):3804.https://doi.org/10.3390/nu13113804
[B198] Sinha Y, Silove N, Wheeler D, Williams K. La formation à l'intégration auditive et autres thérapies sonores pour les troubles du spectre autistique : une revue systématique. Arch Dis Child. 2006;91(12):1018-1022.https://doi.org/10.1136/adc.2006.094649
[B199] Cullen-Powell LA, Barlow JH, Cushway D. Exploration d'une intervention de massage pour les parents et leurs enfants atteints d'autisme : les implications pour le lien et l'attachement. J Child Health Care. 2005;9(4):245-255.https://doi.org/10.1177/1367493505056479
[B200] Buckle J. Aromathérapie clinique : huiles essentielles en milieu de soins. 3e éd. Churchill Livingstone ; 2014.https://www.elsevier.com/books/clinical-aromatherapy/buckle/978-0-7020-5440-3
[B201] Saiyudthong S, Marsden CA. Effets aigus de l'huile de bergamote sur le comportement lié à l'anxiété et le taux de corticostérone chez le rat. Phytother Res. 2011;25(6):858-862.https://doi.org/10.1002/ptr.3325
[B202] Navarra M, Mannucci C, Delbò M, Calapai G. Huile essentielle de Citrus bergamia : de la recherche fondamentale à l'application clinique. Front Pharmacol. 2015;6:36.https://doi.org/10.3389/fphar.2015.00036
[B203] Efferth T, Oesch F. Activités anti-inflammatoires et anticancéreuses de l'oliban : cibles, traitements et toxicités. Semin Cancer Biol. 2022;80:39-57.https://doi.org/10.1016/j.semcancer.2020.01.015
[B204] Siddiqui MZ. Boswellia serrata, un agent anti-inflammatoire potentiel : un aperçu. Indian J Pharm Sci. 2011;73(3):255-261.https://doi.org/10.4103/0250-474X.93507
[B205] Hamidpour R, Hamidpour S, Hamidpour M, Shahlari M. L'encens (rǔ xiāng; espèces de Boswellia) : de la sélection des applications traditionnelles à la nouvelle phytothérapie pour la prévention et le traitement des maladies graves. J Tradit Complement Med. 2013;3(4):221-226.https://doi.org/10.4103/2225-4110.119723
[B206] Moussaieff A, Mechoulam R. Résine de boswellia : des cérémonies religieuses aux usages médicaux ; une revue des essais in vitro, in vivo et cliniques. J Pharm Pharmacol. 2009;61(10):1281-1293.https://doi.org/10.1211/jpp/61.10.0003
[B207] Bakkali F, Averbeck S, Averbeck D, Idaomar M. Effets biologiques des huiles essentielles – une revue. Food Chem Toxicol. 2008;46(2):446-475.https://doi.org/10.1016/j.fct.2007.09.106
[B208] Setzer WN. Huiles essentielles et aromathérapie anxiolytique. Nat Prod Commun. 2009;4(9):1305-1316.https://pubmed.ncbi.nlm.nih.gov/19831048/
[B209] Adams RP. Identification of Essential Oil Components by Gas Chromatography/Mass Spectrometry. 4e éd. Allured Publishing ; 2007.https://www.allured.com/identification-of-essential-oil-components-by-gas-chromatographymass-spectrometry-4th-edition
[B210] Dayawansa S, Umeno K, Takakura H, et al. Réponses autonomiques lors de l'inhalation du parfum naturel du cédrol chez l'homme. Auton Neurosci. 2003;108(1-2):79-86.https://doi.org/10.1016/j.autneu.2003.08.002
[B211] Cheaha D, Reakkamnuan C, Nukitram J, et al. Modification du sommeil-veille et de l'électroencéphalogramme induite par l'inhalation d'huile essentielle de vétiver. J Intercult Ethnopharmacol. 2016;5(1):72-78.https://doi.org/10.5455/jice.20160208050736
[B212] Friedmann T. Freedom from ADHD: A Drug-Free Approach to Treating Children with ADHD. Lotus Press ; 2000.https://www.researchgate.net/publication/265127532_Attention_Deficit_and_Hyperactivity_Disorder_ADHD
[B213] Weyerstahl P, Marschall H, Weirauch M, Thefeld K, Surburg H. Constituants des huiles de vétiver commerciales. Flavour Fragr J. 2000;15(3):153-173.https://doi.org/10.1002/1099-1026(200005/06 )15:33.0.CO;2-V
[B214] Pripdeevech P, Chumpolsri W, Suttiarporn P, Wongpornchai S. La composition chimique et les activités antioxydantes du basilic de Thaïlande à l'aide d'indices de rétention et de chromatographie en phase gazeuse bidimensionnelle complète. J Serb Chem Soc. 2010;75(11):1503-1513.https://doi.org/10.2298/JSC100203125P
[B215] Hongratanaworakit T, Buchbauer G. L'effet relaxant de l'huile d'ylang-ylang sur l'homme après absorption transdermique. Phytother Res. 2006;20(9):758-763.https://doi.org/10.1002/ptr.1950
[B216] Moss M, Hewitt S, Moss L, Wesnes K. Modulation de la performance et de l'humeur cognitives par les arômes de menthe poivrée et d'ylang-ylang. Int J Neurosci. 2008 ; 118(1) : 59-77.https://doi.org/10.1080/00207450601042094
[B217] Komiya M, Takeuchi T, Harada E. La vapeur d'huile de citron provoque un effet anti-stress en modulant les activités 5-HT et DA chez la souris. Behav Brain Res. 2006;172(2):240-249.https://doi.org/10.1016/j.bbr.2006.05.006
[B218] Venturi GB. Enquêtes expérimentales concernant le principe de la communication latérale du mouvement dans les fluides. Phil Trans R Soc Lond. 1797;87:243-260.https://royalsocietypublishing.org/doi/10.1098/rstl.1799.0005
[B219] Buckle J. Utilisation de l'aromathérapie comme traitement complémentaire pour la douleur chronique. Altern Ther Health Med. 1999;5(5):42-51.https://pubmed.ncbi.nlm.nih.gov/10450129/
[B220] Hongratanaworakit T. Effets aromathérapeutiques du massage avec des huiles essentielles mélangées sur l'homme. Nat Prod Commun. 2011;6(8):1199-1204.https://www.researchgate.net/publication/51647617_Aroma-therapeutic_Effects_of_Massage_Blended_Essential_Oils_on_Humans
[B221] White FM. Mécanique des fluides. 8e éd. McGraw-Hill Education ; 2015.https://www.mheducation.com/highered/product/fluid-mechanics-white/M9781260258318.html
[B222] Haze S, Sakai K, Gozu Y. Effets de l'inhalation de parfums sur l'activité sympathique chez des adultes normaux. Jpn J Pharmacol. 2002;90(3):247-253.https://doi.org/10.1254/jjp.90.247
[B223] Herz RS. Aromathérapie : faits et fiction : une analyse scientifique des effets olfactifs sur l'humeur, la physiologie et le comportement. Int J Neurosci. 2009;119(2):263-290.https://doi.org/10.1080/00207450802333953
[B224] Turek C, Stintzing FC. Stabilité des huiles essentielles : une revue. Compr Rev Food Sci Food Saf. 2013;12(1):40-53.https://doi.org/10.1111/1541-4337.12006
[B225] Buckle J. Aromathérapie clinique en soins infirmiers. 2e éd. Pratique infirmière holistique ; 2001.https://journals.lww.com/holistic-nursing-practice/citation/2001/04000/clinical_aromatherapy_in_nursing.15.aspx
[B226] Labiris NR, Dolovich MB. Administration de médicaments par voie pulmonaire. Partie I : facteurs physiologiques affectant l'efficacité thérapeutique des médicaments aérosolisés. Br J Clin Pharmacol. 2003;56(6):588-599.https://doi.org/10.1046/j.1365-2125.2003.01892.x
[B227] Price S, Price L. Aromathérapie pour les professionnels de la santé. 4e éd. Churchill Livingstone ; 2011.https://www.elsevier.com/books/aromatherapy-for-health-professionals/price/978-0-7020-3151-0
[B228] Battaglia S. The Complete Guide to Aromatherapy. 3e éd. Black Pepper Creative; 2018.https://www.blackpeppercreative.com.au/the-complete-guide-to-aromatherapy
[B229] Posadzki P, Alotaibi A, Ernst E. Effets indésirables de l'aromathérapie : une revue systématique des rapports de cas et des séries de cas. Int J Risk Saf Med. 2012 ;24(3) :147-161.https://doi.org/10.3233/JRS-2012-0568
[B230] Dunn C, Sleep J, Collett D. Éprouver une amélioration : une étude expérimentale pour évaluer l'utilisation de l'aromathérapie, du massage et des périodes de repos en unité de soins intensifs. J Adv Nurs. 1995;21(1):34-40.https://doi.org/10.1046/j.1365-2648.1995.21010034.x
[B231] Bowles EJ. La chimie des huiles d'aromathérapie. 3e éd. Allen & Unwin ; 2003.https://www.allenandunwin.com/browse/books/general-books/health-wellbeing/The-Chemistry-of-Aromatherapeutic-Oils-E-Joy-Bowles-9781741140217
[B232] Schnaubelt K. Aromathérapie avancée : La science de la thérapie par les huiles essentielles. Healing Arts Press ; 1998.https://www.healingartspressbooks.com/advanced-aromatherapy
[B233] Schaaf RC, Lane AE. Vers un protocole de meilleures pratiques pour l'évaluation des caractéristiques sensorielles chez les personnes atteintes de TSA. J Autism Dev Disord. 2015;45(5):1380-1395.https://doi.org/10.1007/s10803-014-2299-z
[B234] Wolkoff P, Wilkins CK, Clausen PA, Nielsen GD. Composés organiques dans les environnements de bureau – irritation sensorielle, odeur, mesures et rôle de la chimie réactive. Indoor Air. 2006 ;16(1):7-19.https://doi.org/10.1111/j.1600-0668.2005.00393.x
[B235] Dalton P. Adaptation et co-adaptation olfactives. Dans : Doty RL, éd. Handbook of Olfaction and Gustation. 3e éd. Wiley-Blackwell; 2015:443-459.https://www.wiley.com/en-us/Handbook+of+Olfaction+and+Gustation%2C+3rd+Edition-p-9780470455951
[B236] Cain WS. Savoir par le nez : clés de l'identification des odeurs. Science. 1979;203(4379):467-470.https://doi.org/10.1126/science.760202
[B237] Kern JK, Trivedi MH, Garver CR, et al. Le schéma des anomalies de traitement sensoriel dans l'autisme. Autism. 2006;10(5):480-494.https://doi.org/10.1177/1362361306066564
[B238] Lehrner J, Marwinski G, Lehr S, Johren P, Deecke L. Les odeurs ambiantes d'orange et de lavande réduisent l'anxiété et améliorent l'humeur dans un cabinet dentaire. Physiol Behav. 2005;86(1-2):92-95.https://doi.org/10.1016/j.physbeh.2005.06.031
[B239] Cavanagh HM, Wilkinson JM. Activités biologiques de l’huile essentielle de lavande. Phytother Res. 2002;16(4):301-308.https://doi.org/10.1002/ptr.1103
[B240] Diego MA, Jones NA, Field T, et al. L'aromathérapie affecte positivement l'humeur, les schémas EEG de vigilance et les calculs mathématiques. Int J Neurosci. 1998;96(3-4):217-224.https://doi.org/10.3109/00207459808986469
[B241] Field T, Diego M, Hernandez-Reif M, Cisneros W, Feijo L, Vera Y, Gil K, Grina D, Claire He Q. Effets du gel nettoyant à la lavande sur la relaxation. Int J Neurosci. 2005;115(2):207-222.https://doi.org/10.1080/00207450590519175
[B242] Goel N, Kim H, Lao RP. Un stimulus olfactif modifie le sommeil nocturne chez les jeunes hommes et femmes. Chronobiol Int. 2005;22(5):889-904.https://doi.org/10.1080/07420520500263276
[B243] Ashburner J, Ziviani J, Rodger S. Traitement sensoriel et résultats émotionnels, comportementaux et éducatifs en classe chez les enfants atteints de troubles du spectre autistique. Am J Occup Ther. 2008;62(5):564-573.https://doi.org/10.5014/ajot.62.5.564
[B244] Tomchek SD, Dunn W. Traitement sensoriel chez les enfants avec et sans autisme : une étude comparative utilisant le profil sensoriel court. Am J Occup Ther. 2007;61(2):190-200.https://doi.org/10.5014/ajot.61.2.190
[B245] Ben-Sasson A, Hen L, Fluss R, Cermak SA, Engel-Yeger B, Gal E. Une méta-analyse des symptômes de modulation sensorielle chez les personnes atteintes de troubles du spectre autistique. J Autism Dev Disord. 2009;39(1):1-11.https://doi.org/10.1007/s10803-008-0593-3
[B246] Leekam SR, Nieto C, Libby SJ, Wing L, Gould J. Description des anomalies sensorielles chez les enfants et les adultes atteints d'autisme. J Autism Dev Disord. 2007;37(5):894-910.https://doi.org/10.1007/s10803-006-0218-7
[B247] Baranek GT, David FJ, Poe MD, Stone WL, Watson LR. Questionnaire sur les expériences sensorielles : discrimination des caractéristiques sensorielles chez les jeunes enfants autistes, présentant des retards de développement et un développement typique. J Child Psychol Psychiatry. 2006;47(6):591-601.https://doi.org/10.1111/j.1469-7610.2005.01546.x
[B248] Herz RS. Le rôle de la mémoire évoquée par les odeurs dans la santé psychologique et physiologique. Brain Sci. 2016;6(3):22.https://doi.org/10.3390/brainsci6030022
[B249] Mesibov GB, Shea V, Schopler E. L'approche TEACCH pour les troubles du spectre autistique. Springer ; 2004.https://link.springer.com/book/10.1007/978-0-387-23855-2
[B250] Oono IP, Honey EJ, McConachie H. Intervention précoce médiatisée par les parents pour les jeunes enfants atteints de troubles du spectre autistique (TSA). Cochrane Database Syst Rev. 2013;(4):CD009774.https://doi.org/10.1002/14651858.CD009774.pub2
[B251] Marriott PJ, Shellie R, Cornwell C. Technologies de chromatographie en phase gazeuse pour l'analyse des huiles essentielles. J Chromatogr A. 2001;936(1-2):1-22.https://doi.org/10.1016/s0021-9673(01 )01314-0
[B252] Sparkman OD, Penton Z, Kitson FG. Chromatographie en phase gazeuse et spectrométrie de masse : guide pratique. 2e éd. Academic Press ; 2011.https://www.sciencedirect.com/book/9780123736284/gas-chromatography-and-mass-spectrometry
[B253] ISO 4720:2009. Huiles essentielles — Nomenclature. Organisation internationale de normalisation ; 2009.https://www.iso.org/standard/41076.html
Huiles essentielles – Guide général relatif aux profils chromatographiques – Partie 1: Préparation des profils chromatographiques en vue de leur présentation dans des normes. Organisation internationale de normalisation; 1998.https://www.iso.org/standard/19053.html
[B255] Dhifi W, Bellili S, Jazi S, Bahloul N, Mnif W. Caractérisation chimique des huiles essentielles et investigation de certaines activités biologiques : une revue critique. Medicines (Bâle). 2016;3(4):25.https://doi.org/10.3390/medicines3040025
[B256] Lis-Balchin M. Aromathérapie scientifique : un guide pour les professionnels de la santé. Pharmaceutical Press ; 2006.https://www.pharmpress.com/product/9780853696230/aromatherapy-science
[B257] Schnaubelt K. Aromathérapie médicale : soigner avec les huiles essentielles. Frog Books ; 1999.https://www.innertraditions.com/books/medical-aromatherapy
[B258] Tisserand R. L'Art de l'Aromathérapie. Healing Arts Press ; 1977.https://www.innertraditions.com/books/the-art-of-aromatherapy
[B259] Pauli A. Propriétés antimicrobiennes des constituants d'huiles essentielles. Int J Aromather. 2001;11(3):126-133.https://doi.org/10.1016/S0962-4562(01 )80048-5
[B260] Commission européenne de pharmacopée. Pharmacopée européenne. 10e éd. Conseil de l'Europe; 2019.https://www.edqm.eu/en/european-pharmacopoeia-ph-eur-11th-edition
[B261] Wabner D, Beier C. Aromathérapie : Principes fondamentaux, mécanismes d’action, pratique. 2e éd. Urban & Fischer ; 2012.https://www.elsevier.com/books/aromatherapie/wabner/978-3-437-57214-4
[B262] Lis-Balchin M. Géranium et Pelargonium : Les genres Geranium et Pelargonium. CRC Press ; 2002.https://www.routledge.com/Geranium-and-Pelargonium/Lis-Balchin/p/book/9780415284653
[B263] Turek C, Stintzing FC. Stabilité des huiles essentielles : une revue. Compr Rev Food Sci Food Saf. 2013;12(1):40-53.https://doi.org/10.1111/1541-4337.12006
[B264] Skold M, Karlberg AT, Matura M, Börje A. La bêta-caryophyllène, un produit chimique de parfum – oxydation à l'air et sensibilisation cutanée. Food Chem Toxicol. 2006;44(4):538-545.https://doi.org/10.1016/j.fct.2005.08.028
[B265] Tavassoli T, Miller LJ, Schoen SA, Nielsen DM, Baron-Cohen S. Sensorial hyperréactivité chez les adultes atteints de troubles du spectre autistique. Autism. 2014;18(4):428-432.https://doi.org/10.1177/1362361313477246
[B266] Lane AE, Young RL, Baker AE, Angley MT. Sous-types de traitement sensoriel dans l'autisme : association avec le comportement adaptatif. J Autism Dev Disord. 2010 ;40(1) :112-122.https://doi.org/10.1007/s10803-009-0840-2
[B267] Mazurek MO, Vasa RA, Kalb LG, et al. Anxiété, hypersensibilité sensorielle et problèmes gastro-intestinaux chez les enfants atteints de troubles du spectre autistique. J Abnorm Child Psychol. 2013;41(1):165-176.https://doi.org/10.1007/s10802-012-9668-x
[B268] Buckle J. Aromathérapie clinique : huiles essentielles en pratique. 2e éd. Churchill Livingstone ; 2003.https://www.elsevier.com/books/clinical-aromatherapy/buckle/978-0-7020-2536-6
[B269] Tuchman R, Cuccaro M, Alessandri M. Autisme et épilepsie : perspective historique. Brain Dev. 2010;32(9):709-718.https://doi.org/10.1016/j.braindev.2010.04.008
[B270] Burkhard PR, Burkhardt K, Haenggeli CA, Landis T. Crises d'épilepsie induites par les plantes : réapparition d'un vieux problème. J Neurol. 1999;246(8):667-670.https://doi.org/10.1007/s004150050434
[B271] Millet Y, Jouglard J, Steinmetz MD, Tognetti P, Joanny P, Arditti J. Toxicité de quelques huiles végétales essentielles. Étude clinique et expérimentale. Clin Toxicol. 1981;18(12):1485-1498.https://doi.org/10.3109/15563658108990111
[B272] Pengelly A, Bennett K, Spinks J, Bensoussan A. Évaluation de la base de preuves pour l'utilisation d'huiles essentielles dans la gestion de l'épilepsie : une revue systématique. Epilepsy Behav. 2012;24(1):9-15.https://doi.org/10.1016/j.yebeh.2012.02.019
[B273] Höld KM, Sirisoma NS, Ikeda T, Narahashi T, Casida JE. Alpha-thujone (le composant actif de l'absinthe) : modulation du récepteur de type A de l'acide gamma-aminobutyrique et détoxification métabolique. Proc Natl Acad Sci U S A. 2000 ;97(8):3826-3831.https://doi.org/10.1073/pnas.070042397
[B274] Millet Y, Tognetti P, Lavaire-Perlovisi M, Steinmetz MD, Arditti J, Jouglard J. Étude des propriétés convulsivantes d'échantillons commerciaux d'huiles essentielles de Hyssopus officinalis L. et Salvia officinalis L. Plantes Med Phytother. 1979;13(3):179-184.https://www.sciencedirect.com/science/article/abs/pii/S0370447579800477
[B275] Marcus C, Lichtenstein EP. Interactions des composants des plantes alimentaires naturels avec les insecticides et le pentobarbital chez le rat et la souris. J Agric Food Chem. 1979;27(5):1217-1223.https://doi.org/10.1021/jf60226a004
[B276] Koutroumanidou E, Kimbaris A, Kortsaris A, et al. Latence accrue des crises et diminution de la gravité des crises induites par le pentylènetétrazole chez la souris après administration d'huile essentielle. Epilepsy Res Treat. 2013;2013:532657.https://doi.org/10.1155/2013/532657
[B277] Avallone R, Zanoli P, Puia G, Kleinschnitz M, Schreier P, Baraldi M. Profil pharmacologique de l'apigénine, une flavonoïde isolée de Matricaria chamomilla. Biochem Pharmacol. 2000;59(11):1387-1394.https://doi.org/10.1016/s0006-2952(00 )00264-1
[B278] Watanabe E, Kuchta K, Kimura M, Rauwald HW, Kamei T, Imanishi J. Effets de l'aromathérapie à l'huile essentielle de bergamote (Citrus bergamia (Risso) Wright & Arn.) sur les états d'humeur, l'activité du système nerveux parasympathique et les niveaux de cortisol salivaire chez 41 femmes en bonne santé. Forsch Komplementmed. 2015;22(1):43-49.https://doi.org/10.1159/000380989
[B279] Ilhan S, Savaşer S, Kölgelier S. Effet de l'aromathérapie sur les patients épileptiques. Epilepsy Behav. 2004;5(5):753-757.https://doi.org/10.1016/j.yebeh.2004.06.004
[B280] Meamarbashi A, Rajabi A. Les effets de la menthe poivrée sur la performance à l'exercice. J Int Soc Sports Nutr. 2013;10(1):15.https://doi.org/10.1186/1550-2783-10-15
[B281] Eccles R. Menthol et composés refroidissants apparentés. J Pharm Pharmacol. 1994;46(8):618-630.https://doi.org/10.1111/j.2042-7158.1994.tb03871.x
[B282] Silva J, Abebe W, Sousa SM, Duarte VG, Machado MI, Matos FJ. Effets analgésiques et anti-inflammatoires des huiles essentielles d'Eucalyptus. J Ethnopharmacol. 2003;89(2-3):277-283.https://doi.org/10.1016/j.jep.2003.09.007
[B283] Fachini-Queiroz FC, Kummer R, Estevão-Silva CF, et al. Effets du thymol et du carvacrol, constituants de l'huile essentielle de Thymus vulgaris L., sur la réponse inflammatoire. Evid Based Complement Alternat Med. 2012;2012:657026.https://doi.org/10.1155/2012/657026
[B284] Carson CF, Hammer KA, Riley TV. Huile de Melaleuca alternifolia (arbre à thé) : revue de ses propriétés antimicrobiennes et autres propriétés médicinales. Clin Microbiol Rev. 2006 ;19(1) :50-62.https://doi.org/10.1128/CMR.19.1.50-62.2006
[B285] Eccles R, Jawad MS, Morris S. Effets de l'administration orale de (-)-menthol sur la résistance nasale à l'écoulement d'air et la sensation nasale d'écoulement d'air chez des sujets souffrant de congestion nasale associée au rhume. J Pharm Pharmacol. 1990;42(9):652-654.https://doi.org/10.1111/j.2042-7158.1990.tb06625.x
[B286] Altunbas MK, Celık F, Kahraman C. Le potentiel de l'huile essentielle de lavande pour une utilisation sûre chez les nouveau-nés. J Neonatal Nurs. 2020;26(6):303-307.https://doi.org/10.1016/j.jnn.2020.05.005
[B287] Srivastava JK, Shankar E, Gupta S. Chamomile : une plante médicinale du passé avec un avenir prometteur. Mol Med Rep. 2010;3(6):895-901.https://doi.org/10.3892/mmr.2010.377
[B288] Kiecolt-Glaser JK, Graham JE, Malarkey WB, Porter K, Lemeshow S, Glaser R. Olfactory influences on mood and autonomic, endocrine, and immune function. Psychoneuroendocrinology. 2008;33(3):328-339.https://doi.org/10.1016/j.psyneuen.2007.11.015
[B289] Halm MA. Huiles essentielles pour la prise en charge des symptômes chez les patients en état critique. Am J Crit Care. 2008;17(2):160-163.https://www.researchgate.net/publication/5541002_Essential_Oils_for_Management_of_Symptoms_in_Critically_Ill_Patients
[B290] Fung LK, Mahajan R, Nozzolillo A, et al. Traitement pharmacologique de l'irritabilité sévère et des comportements problématiques chez les personnes autistes : une revue systématique et une méta-analyse. Pediatrics. 2016;137 Suppl 2:S124-S135.https://doi.org/10.1542/peds.2015-2851K
[B291] Kirschbaum KM, Müller MJ, Malevani J, et al. Concentrations sériques de l'aripiprazole et de la déshydroaripiprazole, réponse clinique et effets secondaires. World J Biol Psychiatry. 2008;9(3):212-218.https://doi.org/10.1080/15622970701361255
[B292] Sprouse J, Clarke T, Reynolds L, Heym J, Rollema H. Comparaison des effets de la sertraline et de son métabolite la desméthylsertraline sur le blocage de la recapture de la 5-HT centrale in vivo. Neuropsychopharmacology. 1996;14(4):225-231.https://doi.org/10.1016/0893-133X(95 )00112-Q
[B293] Bailey DG, Dresser G, Arnold JM. Interactions pamplemousse-médicaments : fruit défendu ou conséquences évitables ? CMAJ. 2013;185(4):309-316.https://doi.org/10.1503/cmaj.120951
[B294] Obach RS, Walsky RL, Venkatakrishnan K, Gaman EA, Houston JB, Tremaine LM. L'utilité des données d'inhibition in vitro du cytochrome P450 dans la prédiction des interactions médicamenteuses. J Pharmacol Exp Ther. 2006;316(1):336-348.https://doi.org/10.1124/jpet.105.093229
[B295] Guo LQ, Yamazoe Y. Inhibition du cytochrome P450 par les furanocoumarines dans le jus de pamplemousse et les médicaments à base de plantes. Acta Pharmacol Sin. 2004;25(2):129-136.https://www.researchgate.net/publication/8881220_Inhibition_of_cytochrome_P450_by_furanocoumarins_in_grapefruit_juice_and_herbal_medicines
[B296] Paine MF, Criss AB, Watkins PB. Deux composants majeurs du jus de pamplemousse diffèrent dans le temps d'apparition de l'inhibition de la CYP3A4 intestinale. J Pharmacol Exp Ther. 2004;312(3):1151-1160.https://doi.org/10.1124/jpet.104.076570
[B297] Hanley MJ, Cancalon P, Widmer WW, Greenblatt DJ. L'effet du jus de pamplemousse sur la clairance des médicaments. Expert Opin Drug Metab Toxicol. 2011;7(3):267-286.https://doi.org/10.1517/17425255.2011.553189
[B298] Dresser GK, Bailey DG. Les effets des jus de fruits sur la disposition des médicaments : un nouveau modèle d'interactions médicamenteuses. Eur J Clin Invest. 2003;33 Suppl 2:10-16.https://doi.org/10.1046/j.1365-2362.33.s2.2.x
[B299] Izzo AA, Ernst E. Interactions entre les médicaments à base de plantes et les médicaments prescrits : une revue systématique mise à jour. Drugs. 2009;69(13):1777-1798.https://doi.org/10.2165/11317010-000000000-00000
[B300] Henderson L, Yue QY, Bergquist C, Gerden B, Arlett P. Le millepertuis (Hypericum perforatum) : interactions médicamenteuses et résultats cliniques. Br J Clin Pharmacol. 2002 ;54(4):349-356.https://doi.org/10.1046/j.1365-2125.2002.01683.x
[B301] Unger M, Frank A. Détermination simultanée de la puissance inhibitrice d'extraits de plantes sur l'activité de six enzymes majeures du cytochrome P450 par chromatographie liquide/spectrométrie de masse et extraction automatisée en ligne. Rapid Commun Mass Spectrom. 2004;18(19):2273-2281.https://doi.org/10.1002/rcm.1621
[B302] Gurley BJ, Gardner SF, Hubbard MA, et al. Effets in vivo de l'hydrastis, du kava kava, de l'actée à grappes noires et de la valériane sur les phénotypes humains du cytochrome P450 1A2, 2D6, 2E1 et 3A4/5. Clin Pharmacol Ther. 2005;77(5):415-426.https://doi.org/10.1016/j.clpt.2005.01.009
[B303] Spinella M. L'importance de la synergie pharmacologique dans les médicaments à base de plantes psychoactives. Altern Med Rev. 2002;7(2):130-137.https://pubmed.ncbi.nlm.nih.gov/11968843/
[B304] Abourashed EA, Koetter U, Brattström A. Expériences de liaison in vitro avec un extrait de valériane, de houblon et leur combinaison fixe (Ze91019) sur des récepteurs sélectionnés du système nerveux central. Phytomedicine. 2004;11(7-8):633-638.https://doi.org/10.1016/j.phymed.2004.03.005
[B305] Brazier NC, Levine MA. Interaction médicament-plante parmi les médicaments conventionnels couramment utilisés : un compendium pour les professionnels de la santé. Am J Ther. 2003 ;10(3) :163-169.https://doi.org/10.1097/00045391-200305000-00003
[B306] De Groot AC, Schmidt E. Huiles essentielles : dermatite de contact allergique et composition chimique. CRC Press ; 2016.https://www.routledge.com/Essential-Oils-Contact-Allergy-and-Chemical-Composition/de-Groot-Schmidt/p/book/9781498702508
[B307] Shellie R, Marriott P, Huie C. Analyse complète par chromatographie en phase gazeuse bidimensionnelle (GC × GC) et GC × GC-quadripôle SM du ginseng asiatique et américain. J Sep Sci. 2003;26(12-13):1185-1192.https://doi.org/10.1002/jssc.200301521
[B308] Kubeczka KH. Histoire et sources de la recherche sur les huiles essentielles. In : Baser KHC, Buchbauer G, eds. Handbook of Essential Oils: Science, Technology, and Applications. CRC Press ; 2010 :3-38.https://www.routledge.com/Handbook-of-Essential-Oils-Science-Technology-and-Applications/Baser-Buchbauer/p/book/9781032046419
[B309] Cavanagh HM, Wilkinson JM. Huile essentielle de lavande : une revue. Aust Infect Control. 2005;10(1):35-37.https://doi.org/10.1071/HI05035
Leung AY, Foster S. Encyclopedia of Common Natural Ingredients Used in Food, Drugs, and Cosmetics. 2e éd. Wiley; 1996.https://www.wiley.com/en-us/Encyclopedia+of+Common+Natural+Ingredients+Used+in+Food%2C+Drugs%2C+and+Cosmetics%2C+2nd+Edition-p-9780471508267
[B311] Lis-Balchin M. Aromathérapie avec des huiles essentielles. Dans : Lis-Balchin M, édit. Aromatherapy Science: A Guide for Healthcare Professionals. Pharmaceutical Press ; 2006 : 49-115.https://www.pharmpress.com/product/9780853696230/aromatherapy-science
[B312] Williams TI. Un regard anxieux sur l'aromathérapie. Perspect Psychiatr Care. 2006;42(2):107-108.https://doi.org/10.1111/j.1744-6163.2006.00056.x
[B313] Brondino N, Fusar-Poli L, Rocchetti M, Provenzani U, Barale F, Politi P. Thérapies complémentaires et alternatives pour le trouble du spectre autistique. Evid Based Complement Alternat Med. 2015;2015:258589.https://doi.org/10.1155/2015/258589
[B314] Bent S, Bertoglio K, Hendren RL. Acides gras oméga-3 pour les troubles du spectre autistique : une revue systématique. J Autism Dev Disord. 2009;39(8):1145-1154.https://doi.org/10.1007/s10803-009-0724-5
[B315] Masi A, Quintana DS, Glozier N, Lloyd AR, Hickie IB, Guastella AJ. Aberrations des cytokines dans le trouble du spectre autistique : une revue systématique et une méta-analyse. Mol Psychiatry. 2015;20(4):440-446.https://doi.org/10.1038/mp.2014.59
[B316] Veenstra-VanderWeele J, Blakely RD. Le réseautage dans l'autisme : exploiter les découvertes génétiques, biomarqueurs et systèmes modèles dans la recherche de nouveaux traitements. Neuropsychopharmacology. 2012 ;37(1):196-212.https://doi.org/10.1038/npp.2011.185
[B317] Yamasue H, Domes G. Oxytocine et troubles du spectre autistique. Curr Top Behav Neurosci. 2018;35:449-465.https://doi.org/10.1007/7854_2017_24
[B318] Petra AI, Panagiotidou S, Hatziagelaki E, Stewart JM, Conti P, Theoharides TC. Axe Intestin-Microbiote-Cerveau et son Effet sur les Troubles Neuropsychiatriques avec Dysrégulation Immunitaire Suspectée. Clin Ther. 2015;37(5):984-995.https://doi.org/10.1016/j.clinthera.2015.04.002
[B319] Mayer EA, Tillisch K, Gupta A. Axe intestin/cerveau et le microbiote. J Clin Invest. 2015;125(3):926-938.https://doi.org/10.1172/JCI76304
[B320] Button KS, Ioannidis JP, Mokrysz C, et al. Échec de puissance : pourquoi la petite taille de l'échantillon compromet la fiabilité en neurosciences. Nat Rev Neurosci. 2013;14(5):365-376.https://doi.org/10.1038/nrn3475
[B321] Higgins JP, Thompson SG, Deeks JJ, Altman DG. Measuring inconsistency in meta-analyses. BMJ. 2003;327(7414):557-560.https://doi.org/10.1136/bmj.327.7414.557
[B322] Rossignol DA. Nouveaux traitements émergents pour les troubles du spectre autistique : une revue systématique. Ann Clin Psychiatry. 2009;21(4):213-236.https://pmc.ncbi.nlm.nih.gov/articles/PMC3859980/
[B323] Moher D, Liberati A, Tetzlaff J, Altman DG; PRISMA Group. Preferred reporting items for systematic reviews and meta-analyses: the PRISMA statement. PLoS Med. 2009;6(7):e1000097.https://doi.org/10.1371/journal.pmed.1000097
[B324] Ioannidis JP, Patsopoulos NA, Rothstein HR. Raisons ou excuses pour éviter les méta-analyses dans les diagrammes de forêt. BMJ. 2008;336(7658):1413-1415.https://doi.org/10.1136/bmj.a117
[B325] Loth E, Charman T, Mason L, et al. The EU-AIMS Longitudinal European Autism Project (LEAP) : conception et méthodologies pour identifier et valider des biomarqueurs de stratification pour les troubles du spectre autistique. Mol Autism. 2017;8:24.https://doi.org/10.1186/s13229-017-0146-8
[B326] Geschwind DH, Flint J. Génétique et génomique des maladies psychiatriques. Science. 2015;349(6255):1489-1494.https://doi.org/10.1126/science.aaa8954
[B327] Easterbrook PJ, Berlin JA, Gopalan R, Matthews DR. Biais de publication dans la recherche clinique. Lancet. 1991;337(8746):867-872.https://doi.org/10.1016/0140-6736(91 )90201-y
[B328] Nestler EJ, Hyman SE. Modèles animaux des troubles neuropsychiatriques. Nat Neurosci. 2010;13(10):1161-1169.https://doi.org/10.1038/nn.2647
[B329] Buchbauer G, Jirovetz L, Jäger W, Plank C, Dietrich H. Composés odorants et huiles essentielles aux effets sédatifs par inhalation. J Pharm Sci. 1993;82(6):660-664.https://doi.org/10.1002/jps.2600820623
[B330] Cooke B, Ernst E. Aromathérapie : un examen systématique. Br J Gen Pract. 2000 ; 50(455) : 493-496.https://pubmed.ncbi.nlm.nih.gov/10962794/
[B331] Halm MA. Huiles essentielles pour la gestion des symptômes chez les patients en soins intensifs. Am J Crit Care. 2008;17(2):160-163.https://www.researchgate.net/publication/5541002_Essential_Oils_for_Management_of_Symptoms_in_Critically_Ill_Patients
[B332] Hammer KA, Carson CF, Riley TV. Activité antimicrobienne des huiles essentielles et autres extraits de plantes. J Appl Microbiol. 1999;86(6):985-990.https://doi.org/10.1046/j.1365-2672.1999.00780.x
[B333] Schulz KF, Altman DG, Moher D; CONSORT Group. Énoncé CONSORT 2010 : directives mises à jour pour la déclaration des essais randomisés en groupes parallèles. BMJ. 2010;340:c332.https://doi.org/10.1136/bmj.c332
[B334] Lombardo MV, Lai MC, Baron-Cohen S. Approches par mégadonnées pour décomposer l'hétérogénéité à travers le spectre autistique. Mol Psychiatry. 2019;24(10):1435-1450.https://doi.org/10.1038/s41380-018-0321-0
[B335] Insel TR. Le projet NIMH Research Domain Criteria (RDoC) : médecine de précision pour la psychiatrie. Am J Psychiatry. 2014;171(4):395-397.https://doi.org/10.1176/appi.ajp.2014.14020138
[B336] Jeste SS, Geschwind DH. Essais cliniques pour les troubles neurodéveloppementaux : à la frontière thérapeutique. Sci Transl Med. 2016;8(321):321fs1.https://doi.org/10.1126/scitranslmed.aad9874
[B337] Kovar KA, Gropper B, Friess D, Ammon HP. Taux sanguins de 1,8-cinéole et activité locomotrice des souris après inhalation et administration orale d'huile de romarin. Planta Med. 1987;53(4):315-318.https://doi.org/10.1055/s-2006-962725
[B338] Rossignol DA, Frye RE. Une revue des tendances de recherche sur les anomalies physiologiques dans les troubles du spectre autistique : déréglementation immunitaire, inflammation, stress oxydatif, dysfonctionnement mitochondrial et expositions à des toxiques environnementaux. Mol Psychiatry. 2012;17(4):389-401.https://doi.org/10.1038/mp.2011.165
[B339] Stang A. Évaluation critique de l'échelle de Newcastle-Ottawa pour l'évaluation de la qualité des études non randomisées dans les méta-analyses. Eur J Epidemiol. 2010;25(9):603-605.https://doi.org/10.1007/s10654-010-9491-z
[B340] Herz RS. Aromathérapie : faits et fiction. Une analyse scientifique des effets olfactifs sur l'humeur, la physiologie et le comportement. Int J Neurosci. 2009;119(2):263-290.https://doi.org/10.1080/00207450802333953
[B341] Myers SM, Johnson CP ; American Academy of Pediatrics Council on Children With Disabilities. Prise en charge des enfants atteints de troubles du spectre autistique. Pediatrics. 2007;120(5):1162-1182.https://doi.org/10.1542/peds.2007-2362
[B342] Volkmar F, Siegel M, Woodbury-Smith M, King B, McCracken J, State M ; American Academy of Child and Adolescent Psychiatry (AACAP) Committee on Quality Issues (CQI). Practice parameter for the assessment and treatment of children and adolescents with autism spectrum disorder. J Am Acad Child Adolesc Psychiatry. 2014;53(2):237-257.https://doi.org/10.1016/j.jaac.2013.10.013
[B343] Green VA, Pituch KA, Itchon J, Choi A, O’Reilly M, Sigafoos J. Enquête sur Internet concernant les traitements utilisés par les parents d'enfants autistes. Res Dev Disabil. 2006;27(1):70-84.https://doi.org/10.1016/j.ridd.2004.12.002
[B344] Bilia AR, Guccione C, Isacchi B, Righeschi C, Firenzuoli F, Bergonzi MC. Huiles essentielles encapsulées dans des nanosystèmes : une stratégie en développement pour une approche thérapeutique réussie. Evid Based Complement Alternat Med. 2014;2014:651593.https://doi.org/10.1155/2014/651593
[B345] Woolf AD. Empoisonnement aux huiles essentielles. J Toxicol Clin Toxicol. 1999;37(6):721-727.https://doi.org/10.1081/clt-100102450
[B346] Kasper S, Gastpar M, Müller WE, et al. Efficacité et sécurité du silexan, une nouvelle préparation d'huile de lavande administrée par voie orale, dans le trouble anxieux infra-clinique – preuves issues d'essais cliniques. Wien Med Wochenschr. 2010;160(21-22):547-556.https://doi.org/10.1007/s10354-010-0845-7
B347. La supplémentation en gingembre atténue les comportements autistiques en modulant la signalisation AKT/GSK3β chez des souris exposées à l'acide valproïque prénatal. PubMed. https://doi.org/10.1039/d5fo04364f
B348. Effet du sirop Hiwa, un produit de médecine persane, sur les symptômes de l'autisme chez les enfants atteints de troubles du spectre autistique : un essai clinique randomisé en double aveugle. Journal Médical Mondial. https://doi.org/10.31661/gmj.v13i.3553
B349. McGuinness, F., Oswald, I. W. H., Koby, K. A., et al. (2023). Le cannabidiol et les mélanges de terpènes inspirés du cannabis ont des effets prosociaux aigus chez la souris BTBR modèle de trouble du spectre autistique. Frontiers in Neuroscience. https://doi.org/10.3389/fnins.2023.1185737
Glossaire TDAH
TDAH (Trouble du Déficit de l'Attention avec ou sans Hyperactivité)
Trouble neuropsychiatrique, caractérisé par l'inattention, l'hyperactivité et l'impulsivité.
Thérapie adjuvante
Traitement d'appoint, utilisé en complément du traitement principal, afin d'en renforcer l'efficacité ou d'en réduire les effets secondaires.
Anxiolytique
Anxiolytique, anxiolytique.
Barrière hémato-encéphalique
Barrière sélective entre la circulation sanguine et le cerveau, qui contrôle le passage des substances vers le cerveau.
Récepteur CB2
Récepteur cannabinoïde de type 2, partie du système endocannabinoïde, principalement présent sur les cellules immunitaires ; son activation a des effets anti-inflammatoires.
Chimiotype
Chémo-type d'une plante avec une composition d'huiles essentielles différente (par exemple, thymol vs. camphre comme types de thym).
DAT (Transporteur de dopamine)
Protéine qui transporte la dopamine du espace synaptique vers la cellule nerveuse ; cible principale du méthylphénidate.
DAT-Okkupanz
Pourcentage de transporteurs de dopamine bloqués par un médicament.
Dopamine
Neurotransmetteur, important pour la motivation, la récompense, le mouvement et l'attention ; souvent diminué dans le TDAH.
DE₅₀
Dose à laquelle 50% de l'effet maximal est atteint.
GABA (Acide Gamma-Aminobutyrique)
Neurotransmetteur inhibiteur (freinateur) principal du cerveau; réduit l'excitabilité neuronale.
Récepteur GABA-A
Récepteur canal ionique du GABA ; son activation entraîne un afflux de chlorure et une hyperpolarisation (inhibition) de la cellule nerveuse.
CG/SM (Chromatographie en phase gazeuse-spectrométrie de masse)
Méthode analytique pour l'identification et la quantification des composants chimiques dans les huiles essentielles.
CE₅₀
Concentration à laquelle 50% de l'inhibition maximale d'une cible (par exemple, récepteur, enzyme) est atteinte.
Système limbique
Système limbique.
Linalol
Alcool monoterpénique, principal ingrédient actif de la lavande; il a des effets anxiolytiques, sédatifs et module les systèmes de neurotransmetteurs.
Menthol
Alcool monoterpénique de la menthe poivrée ; active les récepteurs du froid TRPM8, procure une sensation de fraîcheur et améliore l'attention.
Méthylphénidate (MPH)
Stimulant qui inhibe la recapture de la dopamine et de la noradrénaline ; traitement de première intention du TDAH.
Microdialyse
Techniques de mesure des concentrations de neurotransmetteurs extracellulaires dans le cerveau vivant.
Monoamine
Groupe de neurotransmetteurs comprenant la dopamine, la noradrénaline et la sérotonine.
NET (Transporteur de noradrénaline)
Protéine qui transporte la noradrénaline de la fente synaptique vers le neurone ; également la cible du méthylphénidate.
Neuroinflammation
Processus inflammatoires dans le cerveau, souvent médiés par la microglie activée et les cytokines pro-inflammatoires.
Neurotransmetteurs
Messagers chimiques qui transmettent des signaux entre les neurones (par exemple, la dopamine, la sérotonine, le GABA).
NF-κB (Facteur Nucléaire kappa B)
Facteur de transcription qui active les gènes de l'inflammation; l'inhibition a un effet anti-inflammatoire.
Récepteur NMDA
Récepteur glutamatergique, important pour la plasticité synaptique et l'apprentissage ; une suractivation peut être neurotoxique.
Norépinéphrine
Neurotransmetteur, important pour la vigilance, l'attention et la réaction au stress ; souvent diminué dans le TDAH.
Occupation
Voir DAT-Okkupanz; pourcentage de récepteurs ou de transporteurs occupés.
Olfactif
Concernant le sens de l'odorat.
TEP (Tomographie par émission de positons)
Technique d'imagerie qui utilise des substances marquées radioactivement pour visualiser les processus métaboliques et la liaison des récepteurs dans le cerveau.
Pharmacocinétique
Apprentissage de ce que le corps fait à un médicament (absorption, distribution, métabolisme, excrétion).
Pharmakodynamique
Apprenez ce qu'un médicament fait dans le corps (mécanismes d'action, effets).
Cortex préfrontal (CPF)
Région du cerveau derrière le front, importante pour les fonctions exécutives (planification, contrôle des impulsions, mémoire de travail) ; souvent sous-active dans le TDAH.
récepteur
Protéines situées à la surface ou à l'intérieur des cellules, qui se lient à des molécules de signalisation spécifiques (neurotransmetteurs, hormones) et déclenchent ensuite des réactions cellulaires.
SERT (Transporteur de sérotonine)
Protéine transportant la sérotonine hors de la fente synaptique vers le neurone ; cible des antidépresseurs (ISRS).
Sérotonine
Neurotransmetteur, important pour l'humeur, le sommeil, l'appétit et le contrôle des impulsions.
SPECT (Tomographie par émission monophotonique)
Imagerie similaire à la TEP, utilise des traceurs radioactifs pour représenter la fonction cérébrale.
Striatum
Région cérébrale des noyaux gris centraux, riche en transporteurs de dopamine ; importante pour le mouvement, la motivation et la récompense ; principale région cible du méthylphénidate.
Synapse
Synapse.
Fente synaptique
Espace étroit entre deux neurones au niveau de la synapse, dans lequel des neurotransmetteurs sont libérés.
Canaux TRP (Transient Receptor Potential)
Famille de canaux ioniques qui répondent à divers stimuli (température, produits chimiques) ; par exemple, TRPM8 (froid/menthol), TRPV1 (chaleur/capsaïcine).
Principe de Venturi
Principe physique selon lequel, par une chute de pression dans un rétrécissement, des liquides ou des huiles sont aspirés et pulvérisés ; base de nombreux diffuseurs.
β-Caryophyllène
Sesquiterpènes du poivre noir et du cannabis ; agoniste sélectif des récepteurs CB2 aux propriétés anti-inflammatoires.
1,8-Cinéole (Eucalyptol)
Monoterpène-oxyde issu du romarin et de l'eucalyptus ; à l'action mucolytique, anti-inflammatoire et stimulante cognitive.
Récepteur 5-HT1A
Sous-type de récepteur de la sérotonine ; l'activation est anxiolytique et antidépressive.
Fin du rapport
Ce rapport a été élaboré le 27 avril 2026 sur la base d'une analyse systématique de 87 études sur les concentrations cérébrales de méthylphénidate et de 159 publications sur les huiles essentielles dans le contexte du TDAH. Toutes les affirmations sont étayées par la littérature primaire.
Glossaire TSA
1,8-Cinéole (Eucalyptol)
Un oxyde monoterpénique, composant principal de l'huile d'eucalyptus (70–90 %), présente des effets anxiolytiques via la modulation des récepteurs GABA-A et des propriétés anti-inflammatoires ; contre-indiqué chez les enfants de moins de 3 ans en raison du risque de laryngospasme.
alpha-pinène
Monoterpène bicyclique présent dans les pins, le romarin et le cannabis ; montre une modulation GABAergique, des effets anxiolytiques et anti-inflammatoires ; preuves précliniques de propriétés neuroprotectrices.
Amygdale
Structure cérébrale en forme d'amande dans le lobe temporal médian, centrale pour le traitement émotionnel, le conditionnement de la peur et la perception sociale ; agrandie chez les personnes atteintes de TSA dans la petite enfance, activation réduite lors du traitement des visages.
Antioxydants
Molécule qui réduit le stress oxydatif en neutralisant les espèces réactives de l'oxygène (ROS) ; exemples : glutathion, superoxyde dismutase, catalase, vitamine C, vitamine E ; capacité antioxydante réduite dans le TSA.
Analyse Appliquée du Comportement (AAC)
Intervention comportementale basée sur des données probantes pour le TSA, basée sur des principes d'apprentissage (renforcement, guidage, modelage) ; améliore la communication, les compétences sociales et les comportements adaptatifs.
Aripiprazole
Antipsychotique atypique, agoniste partiel des récepteurs dopaminergiques D2 ; approuvé par la FDA pour l'irritabilité associée aux TSA ; effets secondaires : prise de poids, akathisie, syndrome métabolique ; métabolisé par le CYP2D6 et le CYP3A4.
Astrocytes
Cellules gliales en forme d'étoile dans le SNC ; régulent l'homéostasie du glutamate (via les transporteurs EAAT1/2), le tamponnement du K+, la barrière hémato-encéphalique et le soutien métabolique des neurones ; chez l'autisme, astrogliose (expression accrue de GFAP).
β-caryophyllène (BCP)
Hydrocarbure sesquiterpénique dans le poivre noir, les clous de girofle, le cannabis ; agoniste sélectif des récepteurs CB2 sans effets psychoactifs ; réduit la neuroinflammation, l'activation microgliale et le stress oxydatif.
site de liaison des benzodiazépines
Site de modulation allostérique du récepteur GABA-A ; les benzodiazépines (diazépam, lorazépam) s'y lient et potentialisent l'inhibition gabaergique ; le linalool et le 1,8-cinéole interagissent avec ce site (sensible au flumazénil).
Bergamote (Citrus bergamia)
Agrume, huile essentielle contenant du linalool, de l'acétate de linalyle, du limonène ; une étude randomisée contrôlée (ERC) chez des enfants atteints de TSA n'a pas montré d'effets anxiolytiques significatifs ; contient du bergaptène (inhibiteur du CYP3A4), des variantes sans bergaptène (FCF) disponibles.
Acides boswelliques
Acides triterpénoïdes pentacycliques du Boswellia (encens) ; activent la voie antioxydante Nrf2/HO-1, réduisent la neuroinflammation (microglie, astrocytes, TNF-α, IL-6) ; preuves précliniques d'amélioration des comportements similaires aux TSA dans les modèles VPA.
Bumetanide
Diurétique à haute efficacité, inhibiteur du cotransporteur NKCC1 ; corrige le renversement retardé du GABA dans des modèles murins de TSA ; les études cliniques montrent des améliorations modérées de la communication sociale chez les enfants atteints de TSA, mais avec des limitations méthodologiques.
Camphre
Cétone terpénique dans le camphre (Cinnamomum camphora) et le romarin (chémotype camphré) ; abaisse le seuil épileptogène, peut déclencher des crises ; contre-indiqué chez les épileptiques et les patients atteints de TSA présentant une épilepsie comorbide.
Cananga odorata (Ylang-Ylang)
Arbre tropical, l'huile essentielle contient du linalol, du géraniol, du β-caryophyllène; une étude préclinique a montré une amélioration des comportements de type TSA chez des rats VPA par modulation du métabolisme de la sérotonine et de la dopamine.
Récepteur CB2 (Récepteur cannabinoïde de type 2)
Récepteur couplé aux protéines G, principalement exprimé sur les cellules immunitaires (microglie, cellules immunitaires périphériques) ; l'activation réduit la libération de cytokines, l'activation microgliale et la neuroinflammation ; le β-caryophyllène est un agoniste sélectif du CB2.
Cédrol
Alcool sesquiterpénique dans l'huile de cèdre ; traditionnellement associé à des propriétés sédatives, mais les preuves scientifiques de mécanismes GABAergiques ou d'efficacité clinique dans le TSA sont absentes.
Variantes du nombre de copies (VNC)
Délétions ou duplications génomiques >1 kb ; fréquentes dans les TSA (duplication 15q11-13, délétion 16p11.2, délétion 22q13/Syndrome de Phelan-McDermid) ; affectent souvent les gènes synaptiques (SHANK3, NLGN4).
Cytochrome P450 (CYP)
Famille d'enzymes catalysant le métabolisme des médicaments ; le CYP3A4 et le CYP2D6 métabolisent la rispéridone et l'aripiprazole ; le bergapten (dans la bergamote) inhibe le CYP3A4, peut augmenter les concentrations de médicaments.
Dopamine (DA)
Catécholamine neurotransmetteur; médiatise le traitement de la récompense, la motivation, le contrôle moteur; chez les TSA, activation striatale réduite pour les récompenses sociales, densité modifiée des transporteurs de dopamine; l'ylang-ylang module le métabolisme de la DA dans des modèles précliniques.
DSM-5 (Manuel diagnostique et statistique des troubles mentaux, 5e édition)
Système de classification de l'American Psychiatric Association ; définit les TSA par deux domaines principaux : (1) déficits persistants dans la communication/interaction sociale, (2) modèles de comportement restreints et répétitifs.
Dysbiose
Déséquilibre du microbiote intestinal ; chez les personnes atteintes de TSA, réduction de la diversité microbienne, augmentation du rapport Firmicutes/Bactérodètes, réduction des Bifidobactéries et des Prevotelles ; corrélé à la gravité des symptômes.
Déséquilibre E/I (Déséquilibre Excitateur-Inhibiteur)
Déséquilibre entre la neurotransmission excitatrice (glutamatergique) et inhibitrice (GABAergique) ; hypothèse pathophysiologique centrale dans les TSA ; conduit à une hyperexcitabilité, à une perturbation du filtrage sensoriel et à une altération du traitement des informations sociales.
Électroacupuncture
Acupuncture avec stimulation électrique ; des études précliniques montrent une amélioration des comportements de type TSA chez la souris VPA via des mécanismes vagaux et la modulation du microbiome.
Épilepsie
Neurologische Erkrankung mit rekurrenten Anfällen; 10–30 % der ASD-Patienten haben komorbide Epilepsie; campherhaltige ätherische Öle (Kampfer, Rosmarin-Campher-Chemotyp, Salbei) sind kontraindiziert.
Greffe de microbiote fécal (GMF)
Transfer de microbiote intestinal de donneurs sains à des receveurs; des études précliniques montrent une amélioration des comportements similaires à ceux de l'autisme chez des modèles murins; une étude clinique ouverte chez des enfants autistes a montré des améliorations des symptômes gastro-intestinaux et du comportement.
Flumazénil
Antagoniste des benzodiazépines, se lie au site de liaison des benzodiazépines du récepteur GABA-A ; bloque les effets anxiolytiques du linalol et du 1,8-cinéole, ce qui confirme leur interaction avec ce site.
GABA (acide γ-aminobutyrique)
Neurotransmetteur inhibiteur principal du SNC ; se lie aux récepteurs GABA-A (ionotropes) et GABA-B (métabotropes) ; fonction GABAergique réduite, niveaux de GABA altérés, inversion du switch GABAergique pendant le développement dans les TSA.
Récepteur GABA-A
Canal chlorure ligand-dépendant ; activation par le GABA entraîne un influx de chlorure et une hyperpolarisation (inhibition) ; contient un site de liaison des benzodiazépines ; le linalol, le 1,8-cinéole et l'α-pinène modulent les récepteurs GABA-A.
GABA-Switch
Transition développementale de l'action excitatrice à inhibitrice du GABA ; médiatisée par le passage de l'expression du co-transporteur NKCC1 à KCC2 ; retardée dans l'autisme ; l'ocytocine et le bumétanide peuvent normaliser le switch GABAergique.
GAD65/GAD67 (Glutamate Décarboxylase 65/67)
Enzymes qui convertissent le glutamate en GABA ; chez les TSA, expression réduite de GAD65/67 dans le cortex préfrontal et le cervelet, entraînant une synthèse réduite de GABA.
Chromatographie en phase gazeuse couplée à la spectrométrie de masse (GC/MS)
Technique analytique pour l'identification et la quantification des composants volatils ; étalon-or pour la caractérisation chimique des huiles essentielles ; permet la détection des adultérations, des contaminants et de la variabilité d'un lot à l'autre.
Glutamate (Glu)
Neurotransmetteur excitateur principal du SNC ; se lie aux récepteurs ionotropes (NMDA, AMPA, Kainate) et métabotropes (mGluR1-8) ; taux de glutamate altérés dans l'autisme, gènes de synapse glutamatergique perturbés (GRIN2B, GRIA1), transmission glutamatergique excessive.
Glutathion (GSH)
Tripeptide (γ-Glutamyl-Cystéinyl-Glycine), antioxydant intracellulaire primaire ; chez les TSA, taux réduits de GSH, augmentation du glutathion oxydé (GSSG), ratio GSH/GSSG réduit ; variantes génétiques des enzymes de synthèse du GSH (GCLC, GSS) associées aux TSA.
Axe intestin-cerveau
Communication bidirectionnelle entre le tractus gastro-intestinal et le SNC par des voies neuronales (nerf vague), endocriniennes (axe HPA), immunologiques et métaboliques ; dans le TSA dysbiose, production altérée de précurseurs de neurotransmetteurs, voies de signalisation intestin-cerveau perturbées.
Hème oxygénase-1 (HO-1)
Enzyme qui dégrade l'hème en biliverdine (antioxydante), monoxyde de carbone (anti-inflammatoire) et fer ; régulé par Nrf2 ; les acides boswelliques augmentent l'expression de HO-1 ; l'induction de HO-1 protège contre le stress oxydatif et la neuroinflammation.
Hippocampe
Structure cérébrale du lobe temporal médian; médiatise la mémoire déclarative, la navigation spatiale, le traitement contextuel; chez les TSA, hypertrophie pendant l'enfance, connectivité altérée, extinction conditionnée à la peur contextuelle perturbée.
Hypersérotominémie
Erhöhte periphere Serotonin-Spiegel; bei 25–50 % der ASD-Patienten nachgewiesen; Beziehung zu zentralen 5-HT-Spiegeln unklar; möglicherweise durch gestörte Plättchen-Serotonin-Aufnahme oder erhöhte periphere Synthese.
Interleukine-6 (IL-6)
Cytokine pro-inflammatoire ; taux accrus d'IL-6 dans le plasma et le LCR chez les personnes atteintes de TSA ; l'activation immunitaire maternelle avec production d'IL-6 produit des phénotypes similaires à ceux des TSA dans des modèles de souris ; l'IL-6 module la transmission synaptique et le développement.
Cervelet
Structure cérébrale dans le rhombencéphale ; traditionnellement associée au contrôle moteur, elle joue également des rôles dans les processus cognitifs, la prédiction sensorielle et l'apprentissage social ; dans le TSA, perte de cellules de Purkinje, volume vermien réduit, connectivité cérébello-corticale perturbée.
Lavande (Lavandula angustifolia)
Aromatische Pflanze, ätherisches Öl enthält 25–45 % Linalool und Linalylacetat; kleine Pilotstudien berichten verbesserte ABA-Compliance und geteilte Aufmerksamkeit bei ASD-Kindern; präklinische Evidenz für GABAerge Modulation, serotonerge Regulation und oxytonerge Aktivierung.
Linalol
Alcool monoterpénique, composant principal de la lavande, de la coriandre, de la bergamote ; module les récepteurs GABA-A au niveau du site de liaison des benzodiazépines (sensible au flumazénil), affecte les niveaux de sérotonine, augmente le calcium intracellulaire dans les neurones à ocytocine, présente des effets anti-inflammatoires.
Acétate de linalyle
Ester de linalol et d'acide acétique ; composant principal de la lavande (25–45 %) et de la bergamote ; contribue aux effets anxiolytiques et sédatifs ; est hydrolysé en linalol.
Potentiation à long terme (LTP) / Dépression à long terme (LTD)
Mécanismes cellulaires de la plasticité synaptique ; LTP : renforcement durable de la transmission synaptique après stimulation à haute fréquence ; LTD : affaiblissement durable après stimulation à basse fréquence ; chez le TSA, déséquilibre LTP/LTD perturbé dans de multiples régions cérébrales.
Spectroscopie par résonance magnétique (SRM)
Technique d'imagerie non invasive pour la quantification des métabolites (glutamate, GABA, N-acétylaspartate, créatine) in vivo ; chez les TSA, la MRS montre des altérations régionales des concentrations de glutamate et de GABA.
Activation immunitaire maternelle (AIM)
Modèle préclinique dans lequel des animaux gestantes sont traitées avec des immunostimulants (Poly(I:C), LPS) ; la descendance présente des comportements similaires à ceux des TSA, une augmentation des cytokines pro-inflammatoires, un développement synaptique perturbé ; modélise un facteur de risque environnemental pour les TSA.
Mélatonine
Hormone produit par la glande pinéale ; régule le rythme circadien et le sommeil ; des troubles du sommeil sont fréquents chez les personnes autistes ; la supplémentation en mélatonine améliore la latence et la durée du sommeil ; des méta-analyses montrent une efficacité modérée.
Microglie
Cellules immunitaires résidentes du SNC ; régulent l'élagage synaptique, le développement neuronal, la surveillance immunitaire ; chez l'autisme, microglie activée (expression accrue d'Iba1, morphologie amiboïde) dans le cortex préfrontal, le cervelet ; libèrent des cytokines pro-inflammatoires et des ROS.
Dysfonctionnement mitochondrial
Dysfonctionnement mitochondrial (activité réduite de la chaîne respiratoire, augmentation du lactate, synthèse d'ATP réduite) ; chez 5 à 30 % des patients atteints de TSA ; entraîne une production accrue d'ROS, un stress oxydatif, une homéostasie calcique perturbée.
Neuroligine (NLGN)
Molécules d'adhésion cellulaire postsynaptiques (NLGN1-4) ; interagissent avec les neurexines présynaptiques ; régulent la différenciation, la maturation et la fonction synaptiques ; mutations dans NLGN3 et NLGN4X chez des patients atteints de TSA ; les souris NLGN3-R451C présentent une transmission inhibitrice accrue et des phénotypes de type TSA.
Neurexine (NRXN)
Molécules d'adhésion cellulaire présynaptiques (NRXN1-3) ; interagissent avec les neuroligines postsynaptiques ; régulent l'organisation synaptique ; mutations de NRXN1 chez les patients atteints de TSA ; délétions de NRXN1 associées aux TSA, à la schizophrénie et à la déficience intellectuelle.
Neuroinflammation
Réaction inflammatoire dans le SNC ; caractérisée par l'activation des microglies et des astrocytes, une augmentation des cytokines pro-inflammatoires (TNF-α, IL-6, IL-1β), une perturbation de la barrière hémato-encéphalique ; dans l'autisme, une neuroinflammation chronique dans de multiples régions cérébrales.
NF-κB (Facteur Nucléaire kappa B)
Facteur de transcription qui régule les gènes pro-inflammatoires (TNF-α, IL-6, IL-1β, COX-2) ; activation accrue de NF-κB dans l'autisme ; le β-cariopphylène et les acides de boswellia inhibent les voies de signalisation de NF-κB.
Récepteur NMDA (récepteur N-méthyl-D-aspartate)
Récepteur ionotropique du glutamate, canal perméable au calcium ; central pour la plasticité synaptique (LTP/LTD), l'apprentissage et la mémoire ; expression altérée des sous-unités du récepteur NMDA (GRIN2A, GRIN2B) dans l'autisme, fonction altérée du récepteur NMDA dans des souris invalidées pour SHANK2.
Facteur 2 apparenté au facteur nucléaire des érythroïdes 2 (Nrf2)
Facteur de transcription, régulateur principal de la réponse antioxydante ; induit l'expression de HO-1, NQO1, glutathion S-transférases, d'autres enzymes antioxydantes ; les acides de boswellia activent Nrf2 ; les activateurs de Nrf2 (sulforaphane) montrent des améliorations dans l'ASC dans de petites études.
Stress oxydatif
Déséquilibre entre la production de ROS et la défense antioxydante ; chez les TSA, une peroxydation lipidique accrue, une carbonylation protéique, une oxydation de l'ADN, une capacité antioxydante réduite (GSH, SOD, catalase) ; contribue aux lésions et dysfonctionnements neuronaux.
Ocytocine (OT)
Neuropeptide, produit dans l'hypothalamus; rôle central dans la liaison sociale, la confiance, la cognition sociale, la régulation du stress; chez les TSA, réduction des taux plasmatiques d'OT, expression modifiée du récepteur d'ocytocine (OXTR); l'OT intranasale donne des résultats mitigés; l'OT régule le développement GABAergique dans des modèles précliniques.
Interneurone parvalbumine-positif
Sous-type d'interneurone GABAergique, exprimant la protéine liant le calcium parvalbumine ; médie une inhibition rapide et synchrone ; densité et fonction réduites des interneurones à parvalbumine dans le cortex préfrontal chez les TSA.
Syndrome de Phelan-McDermid
Syndrome génétique dû à une délétion 22q13, comprenant le gène SHANK3; caractérisé par des TSA, une déficience intellectuelle, des troubles du langage, une hypotonie; démontre le rôle causal de SHANK3 dans la pathogenèse des TSA.
Cortex préfrontal (CPF)
Région frontale du cerveau ; médiatise les fonctions exécutives, la mémoire de travail, la flexibilité cognitive, la cognition sociale, la théorie de l'esprit ; chez les TSA, activation réduite du PFC pendant les tâches de cognition sociale, connectivité PFC perturbée, déficits GABAergiques.
Propionate
Acide gras à chaîne courte, produit par le microbiote intestinal ; taux de propionate potentiellement élevés dans l'autisme ; exposition au propionate dans des modèles de rongeurs induit des comportements de type autisme, une neuroinflammation, un stress oxydatif.
Espèces réactives de l'oxygène (ERO)
Molécules hautement réactives (superoxyde, peroxyde d'hydrogène, radical hydroxyle) ; se forment comme sous-produits de la respiration mitochondriale ; à des concentrations excessives, les ROS provoquent des dommages oxydatifs aux lipides, aux protéines, à l'ADN ; production accrue de ROS dans l'autisme.
Risperidone
Antipsychotique atypique, antagoniste dopaminergique D2 et sérotoninergique 5-HT2A ; approuvé par la FDA pour l'irritabilité chez les TSA ; effets secondaires : prise de poids, hyperprolactinémie, symptômes extrapyramidaux, syndrome métabolique ; métabolisé par le CYP2D6.
Sérotonine (5-HT, 5-Hydroxytryptamine)
Neurotransmetteur monoaminergique ; module l'humeur, l'anxiété, le sommeil, l'appétit, la cognition sociale ; dans les TSA, hypersérotoninémie (périphérique), synthèse centrale réduite de sérotonine, variants génétiques dans 5-HTT et TPH2 ; le linalol et l'ylang-ylang modulent les systèmes sérotoninergiques.
Protéine SHANK (domaine SH3 et domaines répétitive ankyrine multiples)
Protéines du squelette postsynaptique (SHANK1-3) ; organisent les récepteurs du glutamate, le cytosquelette d'actine, les molécules de signalisation ; mutations dans SHANK2 et SHANK3 dans l'ASD ; les souris SHANK3 knock-out présentent une densité d'épines réduite, une transmission synaptique perturbée, des comportements de type ASD.
Striatum
Structure sous-corticale des ganglions de la base (noyau caudé, putamen, noyau accumbens) ; intervient dans le traitement de la récompense, l'apprentissage des habitudes, le contrôle moteur ; chez les personnes autistes, hypertrophie du striatum, activation réduite lors des récompenses sociales, connectivité cortico-striatale perturbée.
Élagage synaptique
Processus de biologie du développement au cours duquel les synapses excédentaires sont éliminées ; médiatisé par les microglies, le système du complément ; chez les TSA, un élagage potentiellement perturbé (trop ou pas assez), entraînant des densités synaptiques et une connectivité modifiées.
Terpène
Classe diverse de produits naturels, composés d'unités d'isoprène (C5H8) ; principaux composants des huiles essentielles ; monoterpènes (C10) : linalol, 1,8-cinéole, α-pinène ; sesquiterpènes (C15) : β-caryophyllène, cédrol ; triterpènes (C30) : acides boswelliques.
TNF-α (Facteur de Nécrose Tumorale-α)
Cytokine pro-inflammatoire ; taux de TNF-α élevés dans le plasma, le LCR et le tissu cérébral post-mortem chez les personnes atteintes de TSA ; activation immunitaire maternelle avec une augmentation du TNF-α produisant des phénotypes similaires à ceux des TSA ; le TNF-α module la transmission synaptique, réduit l'inhibition GABAergique.
Protéine translocatrice (TSPO)
Protéine mitochondriale, fortement régulée dans les microglies activées ; les ligands TEP (par ex. [11C]-PBR28) se lient à la TSPO et permettent l'imagerie in vivo de l'activation microgliale ; augmentation de la liaison TSPO dans de multiples régions cérébrales chez les personnes atteintes de TSA.
Tryptophane
Acide aminé essentiel, précurseur de la sérotonine et de la mélatonine ; métabolisme du tryptophane potentiellement perturbé dans le TSA ; le microbiote intestinal influence la disponibilité et le métabolisme du tryptophane via les voies de la kynurénine et de la sérotonine.
Acide valproïque (AVP)
Antiepileptique ; l'exposition prénatale au VPA est un facteur de risque de TSA chez l'homme ; modèle de souris TSA induit par le VPA : des souris gestantes reçoivent du VPA, la progéniture présente des comportements semblables aux TSA, une neuroinflammation et un stress oxydatif ; modèle préclinique largement utilisé.
Principe de Venturi
Principe physique (Effet Bernoulli) : Réduction de la pression dans un fluide lorsqu'il traverse un rétrécissement ; dans le nébuliseur d'arômes organiques Organik Aromas 3.0, l'air comprimé est généré par une buse, créant une dépression qui aspire l'huile essentielle et la pulvérise en fines gouttelettes (nébulisation à froid).
Vétiver (Vetiveria zizanioides)
Herbe tropicale, huile essentielle contenant du vétivérol, du khusimol, de l'α-vétivone ; rapports anecdotiques sur les effets sur l'attention et l'hyperactivité, mais études contrôlées chez les TSA absentes ; preuves scientifiques des mécanismes insuffisantes.
Encens (Boswellia)
Résine d'espèces de Boswellia; l'huile essentielle et les extraits contiennent des acides boswelliques; preuves précliniques d'effets anti-neuroinflammatoires, antioxydants (Nrf2/HO-1) et neuroprotecteurs; aucune étude clinique sur les TSC identifiée.
Bois de cèdre (Cedrus atlantica, Juniperus virginiana)
L'huile essentielle contient du cèdre, de l'α-cèdrène, du thujopsène ; traditionnellement utilisée pour la sédation et la réduction de l'anxiété, mais les preuves scientifiques des mécanismes GABAergiques ou de l'efficacité clinique dans le TSA font défaut.
Rythme circadien
Rythme endogène d'environ 24 heures, régule le cycle veille-sommeil, la sécrétion hormonale, la température corporelle ; chez les personnes atteintes de TSA, les rythmes circadiens et les troubles du sommeil sont souvent perturbés ; la mélatonine régule le rythme circadien et améliore le sommeil chez les personnes atteintes de TSA.