Sommario
Aggiornato – 28 aprile 2026
Eine vergleichende Ausarbeitung der Standard-Therapie von ADHS / ADS und Aroma-Therapie mit therapeutisch zugelassenen, mittels GC/MS-Analysen chargenbezogen getesteten ätherischen Ölen. (Stand 04.2026).
ADHS/ADS und Ätherische Öle – Verständlich erklärt
Eine laienverständliche Kurzfassung des wissenschaftlichen Berichts für alle, die mehr über natürliche Unterstützung bei ADHS erfahren möchten
Was ist ADHS/ADS?
ADHD sta per Aufmerksamkeitsdefizit-Hyperaktivitätsstörung, ADS für die Variante ohne Hyperaktivität (Aufmerksamkeitsdefizit-Störung). Beide sind keine Erfindung oder Erziehungsfehler, sie sind echte neurologische Erkrankungen, bei denen das Gehirn anders verdrahtet ist.
Das Bild dahinter: Stellen Sie sich das Gehirn wie ein Radio vor. Beim ADHS-Gehirn springt der Sender ständig zwischen Frequenzen hin und her, manchmal zu laut, manchmal zu leise, selten auf dem richtigen Kanal. Das macht es schwer, sich zu konzentrieren, ruhig zu sitzen oder Impulse zu kontrollieren.
Was passiert im Gehirn bei ADHS?
Das Kernproblem liegt in zwei Botenstoffen:
Dopamina – der “Belohnungs- und Motivations-Botenstoff”
Bei ADHS wird Dopamin zu schnell wieder “aufgeräumt” (durch den Dopamintransporter DAT). Dadurch fehlt das Gefühl von Belohnung und Motivation für alltägliche Aufgaben. Das Gehirn sucht ständig nach Stimulation, daher die Impulsivität und Risikosuche
Noradrenalina – der “Aufmerksamkeits- und Fokus-Botenstoff”
Zu wenig Noradrenalin im präfrontalen Kortex (dem “Chef-Bereich” des Gehirns) – Führt zu Konzentrationsproblemen, Vergesslichkeit, Schwierigkeiten beim Planen
Welche Hirnbereiche sind betroffen?
- Präfrontaler Kortex
Zuständig für Planung, Impulskontrolle, Konzentration – bei ADHS unteraktiv
- Striatum (Basalganglien)
Belohnungszentrum – bei ADHS weniger empfindlich
- Kleinhirn
Timing und Koordination – bei ADHS leicht verändert
Wie häufig ist ADHS?
Bei Kindern und Jugendlichen ist es häufigste psychiatrische Erkrankung mit 5 bis 7 %, bei Erwachsenen 2,5 bis 4 %, viele Erwachsene wissen nicht, dass sie ADHS haben.
Wie äußert sich ADHS?
| Bereich | Typische Symptome |
| Attenzione | Abgelenkt sein, Flüchtigkeitsfehler, Vergessen von Alltagsdingen |
| Iperattività | Zappeln, Aufstehen, innere Unruhe (besonders bei Erwachsenen) |
| Impulsivität | Unterbrechen, spontane Entscheidungen, Ungeduld |
| Exekutivfunktionen | Schlechte Planung, Prokrastination, Zeitblindheit |
| Emozioni | Reizbarkeit, Frustrationsintoleranz, emotionale Dysregulation |
Wie wird ADHS normalerweise behandelt?
Das Hauptmedikament – Methylphenidat (Ritalin, Concerta, Medikinet)
Methylphenidat (MPH) ist das am häufigsten verschriebene ADHS-Medikament und die Erstlinientherapie.
Wie funktioniert es?
Methylphenidat blockiert den Dopamintransporter (DAT), die “Aufräum-Pumpe” für Dopamin. Wenn weniger Dopamin aufgeräumt wird, bleibt mehr davon zwischen den Nervenzellen, das Gehirn kann besser fokussieren.
Die Zahlen dahinter
Eine Dosis von 20 mg blockiert ca. 54 % der Dopamin-Aufräum-Pumpen im Gehirn, 40 mg blockieren ca. 72 %.
Die Wirkung setzt nach 30–90 Minuten ein und hält je nach Formulierung 4–12 Stunden an.
Wie wirksam ist es?
Con 70–80 % der Patienten wirkt Methylphenidat klinisch gut: Verbesserungen von Aufmerksamkeit, Impulsivität und Schulleistungen sind gut belegt.
Formulierungen
- Kurzwirksam (z. B. Ritalin): 4–6 Stunden, muss mehrmals täglich eingenommen werden
- Retardiert (z. B. Concerta, Medikinet retard): 8–12 Stunden, einmal täglich
Effetti collaterali
– Appetitminderung (häufigste Nebenwirkung)
– Schlafstörungen (wenn zu spät eingenommen)
– Kopfschmerzen, Magendrücken (meist am Anfang)
– Leichte Erhöhung von Herzrate und Blutdruck
– Stimmungsschwankungen, Reizbarkeit (selten)
Weitere Medikamente
Atomoxetin (Strattera)
– Kein Stimulans, hemmt den Noradrenalin-Transporter (NET)
– Wirkt auch auf ADHS ohne Suchtgefahr
– Braucht 4–6 Wochen bis zur vollen Wirkung
– Gut geeignet bei gleichzeitiger Angststörung oder Tic-Störung
Amphetamine (in Deutschland weniger verbreitet)
– Lisdexamfetamin (Vyvanse): In Deutschland seit 2013 für Erwachsene zugelassen
– Wirkt stärker und länger als Methylphenidat
Guanfacin (Intuniv)
– Für Kinder und Jugendliche, bei denen Stimulanzien nicht passen
– Wirkt auf Noradrenalin-Rezeptoren im präfrontalen Kortex
Ätherische Öle bei ADHS – wie kann das funktionieren?
Ätherische Öle können das ADHS-Gehirn auf mehreren Wegen unterstützen:
- Über den Geruchssinn ins Gehirn
Duftmoleküle aktivieren das limbische System (Emotionen, Motivation) und den präfrontalen Kortex (Konzentration) – direkt und schnell - Über Neurotransmitter-Systeme
Bestimmte Terpene beeinflussen Dopamin, Noradrenalin, Serotonin und GABA - Komplementär zu Methylphenidat
Methylphenidat wirkt auf DAT/NET – ätherische Öle wirken auf andere Systeme (GABA-A, CB2, TRPM8, SERT) und sind damit potenzielle Ergänzungen
Limitazione importante
Die Forschung zu ätherischen Ölen bei ADHS steckt noch in den Kinderschuhen. Die meisten Studien wurden an gesunden Erwachsenen durchgeführt, nicht an ADHS-Patienten. Direkte klinische Beweise sind noch begrenzt.
Welche ätherischen Öle können bei ADHS helfen?
Pfefferminze – das Konzentrations-Öl Nr. 1
Menta piperita (Mentha × piperita) hat den stärksten Beleg für Aufmerksamkeitsverbesserung.
- Was ist drin?
Menthol (30–50 %)
Menthon (10–30 %)
1,8-Cineol (5–10 %) - Was macht Menthol?
Aktiviert TRPM8-Rezeptoren – “Kälterezeptoren” im Nervensystem, die das Gehirn aktivieren
Hemmt das Enzym, das den Konzentrations-Botenstoff Acetylcholin abbaut
Moduliert GABA-A-Rezeptoren (leicht beruhigend bei Überaktivierung) - Klinische Studie (n=24)
100 µL Pfefferminzöl (eingekapselt) verbesserte die Daueraufmerksamkeit im RVIP-Test (Rapid Visual Information Processing) signifikant nach 1–3 Stunden; reduzierte Müdigkeit und verbesserte mentale Arithmetik - Caratteristica speciale
Pfefferminze fördert fokussierte Aufmerksamkeit (im Gegensatz zu Lavendel, das die Aufmerksamkeit eher verteilt) - Wie anwenden
2 Tropfen auf ein Taschentuch, kurz vor Lern- oder Arbeitseinheiten; Diffusor im Lernzimmer
Rosmarin – für Gedächtnis und Wachheit
Rosmarino (Rosmarinus officinalis) wird seit der Antike als “Gedächtniskraut” bezeichnet, zu Recht.
- Was ist drin?
1,8-Cineol (20–50 %)
Campher (10–20 %)
α-Pinen (10–15 %) - Was macht 1,8-Cineol?
Hemmt das Enzym Acetylcholinesterase, das den Konzentrations-Botenstoff abbaut (ähnlich wie Alzheimer-Medikamente!)
Aktiviert das Nervensystem, erhöht Wachheit und Alertness
Entzündungshemmend und antioxidativ im Gehirn - Klinische Studie (n=144)
Rosmarin-Aromatherapie verbesserte Gesamtgedächtnis und Sekundärgedächtnis signifikan, besser als Lavendel und Kontrollgruppe - Für ADHS
Besonders hilfreich bei Gedächtnisproblemen, “Brain Fog”, und Morgenmüdigkeit - Wie anwenden
Morgens im Diffusor (5 Tropfen), Inhalation vor Prüfungen oder wichtigen Aufgaben - Attenzione: Nicht abends verwenden, es ist zu aktivierend; besondere Vorsicht bei Epilepsie wg. des Campher-Gehalts!
Lavendel – gegen Angst und Schlafprobleme
Lavanda (Lavandula angustifolia) ist das beste Öl bei ADHS-begleitenden Angst- und Schlafproblemen.
- Was ist drin?
Linalool (25–45 %)
Linalylacetat (25–50 %) - Was macht Linalool?
Aktiviert GABA-A-Rezeptoren, die “Bremse” des Gehirns
Moduliert Serotonin, Dopamin und Noradrenalin
Senkt Kortisol (Stresshormon) um 24–38 % - Bei ADHS besonders nützlich für
Einschlafschwierigkeiten (sehr häufig bei ADHS)
Begleitende Angststörungen (bei ca. 50 % der ADHS-Patienten)
Emotionale Dysregulation und Reizbarkeit - Wichtiger Hinweis
Lavendel kann das Arbeitsgedächtnis kurzfristig beeinträchtigen, deshalb nicht während Lernphasen verwenden, sondern nur abends oder zur gezielten Entspannung - studio
Silexan (80 mg Lavendelöl täglich als Kapsel) wirkte vergleichbar mit Lorazepam bei Angststörungen - Wie anwenden
Abends im Diffusor (5 Tropfen), 2 Tropfen auf das Kopfkissen
Zedernholz – Oxygenierung und Fokus
Zedernholz (Cedrus atlantica / Juniperus virginiana) wird traditionell bei ADHS eingesetzt.
- Was ist drin?
α-Cedren
β-Cedren
Cedrol - Was es tut
Verbessert die Hirnoxygenierung; beruhigend; aktiviert den Parasympathikus - ADHS-spezifisch
Godfrey (2001) berichtete positive Effekte bei ADHS-Kindern;
Cedrol senkte Herzrate und Atemfrequenz in Studien - Wie anwenden
Im Diffusor während ruhiger Tätigkeiten; gut kombinierbar mit Lavendel
Vetiver – der Erdungs-Duft
Vetiver (Chrysopogon zizanioides) hat einen tiefen, erdigen Duft, oft als “Beruhigung für rastlose Geister” beschrieben.
- Was es tut
Anxiolytisch (angstlösend); beruhigt das Nervensystem; verbessert Schlaf - ADHS-spezifisch
Springer et al. (2018) berichteten Verbesserungen bei ADHS-Kindern nach 30-tägiger 3×-täglich-Inhalation - Für wen
Besonders bei hyperaktiver ADHS-Variante mit innerer Unruhe
Zimt – die einzige direkte ADHS-Studie
Cannella (Cinnamomum verum) hat den einzigartigen Beleg: die einzige klinische Studie direkt bei ADHS-Kindern.
- Was ist drin?
Zimtaldehyd (60–75 %)
Eugenol (5–10 %) - ADHS-Studie (Chen et al., 2008)
Kombination aus Rehabilitation + Zimt-Aromatherapie (1 % Zimt, nasale Inhalation) über 6 Monate zeigte signifikant bessere Ergebnisse im SNAP-IV-Fragebogen als Rehabilitation allein (p < 0,05) - Meccanismo
Zimtaldehyd-Metaboliten können dopaminerge Wirkung haben - Einschränkung
Die Studie hat methodische Schwächen (kleine Stichprobe, unklare Verblindung) - Wie anwenden
Sparsam im Diffusor, kombiniert mit anderen Ölen
Schwarzer Pfeffer (β-Caryophyllen) – gegen Neuroinflammation
β-cariofillene aus schwarzem Pfeffer, Lavendel und anderen Pflanzen:
- Aktiviert CB2-Cannabinoid-Rezeptoren ohne psychoaktive Wirkung
- Reduziert Neuroinflammation (Entzündungen im Gehirn)
- Interessant bei ADHS mit begleitenden Entzündungszeichen oder Stimmungsproblemen
- Gut kombinierbar mit anderen Ölen
Die Öle im Überblick – Wann welches Öl?
| sintomo | Empfohlenes Öl | Anwendungszeit |
| Konzentrationsprobleme | Pfefferminze, Rosmarin | Morgens, vor Lernphasen |
| Gedächtnisschwäche | Rosmarino | Morgens, vor Aufgaben |
| Schlafprobleme | Lavendel, Zedernholz, Vetiver | Abends |
| Innere Unruhe/Hyperaktivität | Vetiver, Zedernholz, Lavendel | Nachmittags, abends |
| Angst und Reizbarkeit | Lavendel, Bergamotte | Nachmittags, abends |
| Morgenmüdigkeit | Pfefferminze, Rosmarin | Mattina |
| Allgemeine ADHS-Unterstützung | Zimt (sparsam) | Lernphasen |
Praktische Tagesroutine für ADHS
Morgenroutine (Aktivierung + Fokus):
- Diffusor: Rosmarin (4 Tropfen) + Pfefferminze (2 Tropfen) für 15–20 Minuten
- Oder: Pfefferminze auf Taschentuch, 3× tief einatmen vor der Schule/Arbeit
- Wirkung: Wachheit, Gedächtnis, Konzentration
Lernzeit / Arbeitsphase:
- Diffusor: Pfefferminze (3 Tropfen) + Zitrone (2 Tropfen) für 20 Minuten, dann 30 Minuten Pause
- Attenzione: Kein Lavendel während des Lernens!
- Wirkung: Daueraufmerksamkeit, Fokus
Nachmittag (Entspannung nach der Schule):
- Diffusor: Zedernholz (3 Tropfen) + Bergamotte (2 Tropfen) für 20 Minuten
- Wirkung: Stressabbau, emotionale Regulierung
Abendroutine (Abschalten + Schlafen):
- Diffusor: Lavendel (4 Tropfen) + Vetiver (2 Tropfen) 30 Minuten vor dem Schlafen
- Oder: 2 Tropfen Lavendel auf das Kopfkissen
- Wirkung: Einschlafen, Schlafqualität
Dosierungshinweise für den Diffusor
| Raumgröße | Tropfen gesamt | Anwendungsdauer | Pause |
| Klein (bis 15 m²) | 3–5 Tropfen | 15–20 Min | 30 Min |
| Mittel (15–30 m²) | 5–8 Tropfen | 20–30 Min | 30 Min |
| Groß (30–50 m²) | 8–12 Tropfen | 20–30 Min | 45 Min |
Importante: Bei der olfaktorische Adaptation riecht man das Öl nach 20–30 Minuten kaum noch, dennoch wirkt weiterhin. Damit sich die Rezeptoren erholen können, der Gewöhnungseffekt „resettet“ wird, müssen die Pausen eingehalten werden!
Was sagt die Wissenschaft wirklich?
| Olio | Evidenz bei ADHS | Evidenz bei Gesunden |
| Menta piperita | Nessun RCT | ⭐⭐⭐ Aufmerksamkeit (n=24) |
| Rosmarino | Nessun RCT | ⭐⭐⭐ Gedächtnis (n=144) |
| Lavanda | Fallberichte | ⭐⭐⭐ Angst, Schlaf |
| Cannella | ⭐⭐ Eine Studie (methodisch schwach) | Begrenzt |
| Vetiver | ⭐ Fallberichte | Begrenzt |
| Zedernholz | ⭐ Traditionell | Begrenzt |
| β-cariofillene | Nessuno | ⭐⭐ Präklinisch |
Conclusione
Die Evidenz ist vielversprechend aber noch begrenzt. Mechanistisch macht es Sinn, aber große klinische Studien bei ADHS-Patienten fehlen noch. Das bedeutet nicht, dass es nicht wirkt, es bedeutet, dass wir noch mehr Forschung brauchen.
Wichtige Sicherheitshinweise
Besondere ADHS-Überlegungen:
Sensorische Überempfindlichkeit
Viele ADHS-Betroffene (40–60 %) haben eine erhöhte Geruchsempfindlichkeit. Beginnen Sie immer mit halber Dosis und steigern Sie langsam. Wenn ein Duft unangenehm ist: sofort aufhören.
Wechselwirkungen mit Methylphenidat
- Cannella
Kann dopaminerge Wirkung haben, was eine theoretisch verstärkende Wirkung mit MPH ermöglich, deshalb Herzrate und Blutdruck beobachten
- Lavanda
Kann serotonerge Wirkung haben, bei gleichzeitiger Einnahme von Antidepressiva vorsichtig sein
- Rosmarino
Kann aktivierend wirken, daher nicht kurz vor der Schlafenszeit applizieren
Bei Kindern
– Unter 3 Jahren: Keine ätherischen Öle
– 3–6 Jahre: Nur sehr niedrige Konzentrationen (1–2 Tropfen), gut belüfteter Raum
– > 6 Jahre: Normale Dosierung möglich – Kein direkter Hautkontakt ohne Verdünnung
Allgemeine Regeln:
- Immer mit Trägeröl (z.B. nicht-fettendes, fraktioniertes Kokosnuss-Öl) verdünnen (2–3 %)
- Gut belüfteten Raum nutzen
- Pausen einhalten (nicht den ganzen Tag diffusieren)
- Bei Asthma oder Atemwegsproblemen: Arzt fragen
- Ätherische Öle sind kein Ersatz für Methylphenidat oder andere ADHS-Therapien
FAQ – Häufig gestellte Fragen
Kann ich Methylphenidat durch ätherische Öle ersetzen?
Nein. Ätherische Öle sind eine Ergänzung, kein Ersatz. Methylphenidat hat eine starke klinische Evidenz bei 70–80 % der Patienten. Ätherische Öle können helfen, Restsymptome zu lindern, Schlaf zu verbessern oder Nebenwirkungen (wie Angst) zu reduzieren.
Welches Öl soll ich zuerst ausprobieren?
Pfefferminze für Konzentration (tagsüber) und Lavendel für Schlaf (abends), am besten erforscht, gut verträglich.
Wie lange bis ich eine Wirkung merke?
Manche Effekte (Fokus, Wachheit) sind innerhalb von Minuten spürbar. Für nachhaltige Verbesserungen (Schlaf, Stimmung) sollten Sie 2–4 Wochen regelmäßig anwenden.
Funktioniert das auch bei Erwachsenen mit ADHS?
Ja, die meisten Studien wurden sogar an Erwachsenen durchgeführt. Erwachsene mit ADHS berichten oft von besonders guter Wirkung auf die emotionale Dysregulation und Schlafprobleme.
Muss ich das mit meinem Arzt besprechen?
Für die Aromatherapie (Diffusor, Inhalation) ist das nicht zwingend nötig. Wenn Sie jedoch Kapseln oder Cremes mit ätherischen Ölen nehmen möchten, oder wenn Ihr Kind ADHS hat und Methylphenidat einnimmt, sprechen Sie Ihren Arzt an.
Neurobiologische Grundlagen, molekulare Wirkmechanismen und klinische Evidenz für adjuvante Therapie mit dem Organik Aromas Nebulizer 3.0
Kombinierter Forschungsbericht | April 2026
Themen: Methylphenidat (Ritalin) · Intracerebrale Pharmakodynamik · Adjuvante Aromatherapie · Terpene · Rezeptoren · Signalwege · Dosierungsempfehlungen
Applikation: Organik Aromas Nebulizer 3.0 (Venturi-Kaltvernebelung, wasserfrei, GC/MS-reine Öle)
ADHS und Methylphenidat
Dieser Bericht untersucht die neurobiologischen Grundlagen der Methylphenidat-Therapie bei Aufmerksamkeitsdefizit-/Hyperaktivitätsstörung (ADHS) und bewertet das Potenzial ätherischer Öle als adjuvante Therapieoption. Die Analyse basiert auf 87 wissenschaftlichen Publikationen zu intracerebralen Methylphenidat-Konzentrationen und 159 Studien zu ätherischen Ölen im ADHD-Kontext.
Haupterkenntnisse zu Methylphenidat
Therapeutische orale Dosen (0,25–0,6 mg/kg) erzeugen eine Dopamintransporter (DAT)-Okkupanz von >50% im Striatum, wobei 20 mg oral 54% und 40 mg 72% DAT-Blockade erreichen. Die maximale Hirnaufnahme erfolgt 60–90 Minuten nach oraler Gabe. Plasma-Konzentrationen im therapeutischen Bereich liegen bei 3,5–7,8 ng/ml (Erwachsene), wobei 6 ng/ml mit 50% DAT-Blockade assoziiert sind. Direkte Messungen von Methylphenidat-Konzentrationen im Hirngewebe (ng/ml) oder Liquor existieren nicht; verfügbare Daten stammen aus PET/SPECT-Okkupanzstudien.
Ätherische Öle als Adjuvans
Mechanistische Plausibilität besteht für eine adjuvante Therapie basierend auf komplementären Wirkmechanismen. Linalool (Lavendel) moduliert Serotonin-, Dopamin- und Noradrenalin-Systeme über 5-HT1A-Rezeptoren und SERT-Bindung. Menthol (Pfefferminze) aktiviert TRPM8-Kanäle und moduliert GABA-A- sowie nikotinische Rezeptoren, was Aufmerksamkeit und Vigilanz verbessert. β-Caryophyllen (Schwarzer Pfeffer) wirkt als CB2-Agonist mit antiinflammatorischen Eigenschaften. 1,8-Cineol (Rosmarin) verbessert Gedächtnisleistung und kognitive Funktionen.
Evidenzlage
Während präklinische und mechanistische Daten vielversprechend sind, fehlen randomisierte kontrollierte Studien (RCTs) speziell bei ADHD-Patienten. Vorhandene Humanstudien zeigen kognitive Verbesserungen bei gesunden Erwachsenen (Pfefferminze: verbesserte Daueraufmerksamkeit, n=24; Rosmarin: Gedächtnisverbesserung, n=144).
Dieser Bericht liefert evidenzbasierte Dosierungsempfehlungen für den Organik Aromas Nebulizer 3.0 und umfassende Sicherheitshinweise für die Anwendung bei ADHD-Patienten.
Autismus-Spektrum-Störung (ASD)
Die Autismus-Spektrum-Störung (ASD) ist eine komplexe neurobiologische Entwicklungsstörung mit einer geschätzten Prävalenz von 1–2 % weltweit. Die Kernsymptomatik umfasst Beeinträchtigungen in sozialer Kommunikation und Interaktion sowie repetitive Verhaltensmuster und sensorische Besonderheiten. Trotz intensiver Forschung existieren keine kurativen Therapien für die Kernsymptome; verfügbare Interventionen konzentrieren sich auf Verhaltenstherapie und symptomatische Pharmakotherapie. Dieser Bericht untersucht das Potenzial ätherischer Öle als adjuvante Therapieoption bei ASD, basierend auf einer systematischen Analyse von 547 wissenschaftlichen Publikationen zu ASD-Neurobiologie, Terpenen und klinischer Evidenz.
Die neurobiologische Heterogenität von ASD manifestiert sich in gestörter exzitatorisch-inhibitorischer (E/I) Balance, Dysfunktionen in GABAergen, glutamatergen, serotonergen, dopaminergen und oxytonergen Systemen, chronischer Neuroinflammation mit Mikroglia-Aktivierung, oxidativem Stress, Gut-Brain-Axis-Alterationen und synaptischen Defiziten (Neuroligin, SHANK-Proteine). Betroffene Hirnregionen umfassen präfrontalen Kortex, Amygdala, Kleinhirn, Hippocampus und Striatum.
Molekulare Analysen zeigen, dass spezifische Terpene aus ätherischen Ölen an ASD-relevanten Targets angreifen: Linalool (Hauptkomponente von Lavendel) moduliert GABA-A-Rezeptoren an der Benzodiazepin-Bindungsstelle und beeinflusst serotonerge Signalwege; β-Caryophyllen wirkt als selektiver CB2-Rezeptor-Agonist mit anti-neuroinflammatorischen Eigenschaften; Boswelliasäuren (Weihrauch) aktivieren den Nrf2/HO-1-Antioxidans-Pathway und reduzieren Mikroglia-Aktivierung; 1,8-Cineol (Eukalyptus) zeigt anxiolytische Effekte über GABA-A-Modulation; α-Pinen wirkt GABAerg; Cananga odorata (Ylang-Ylang) beeinflusst Serotonin- und Dopamin-Metabolismus in präklinischen ASD-Modellen.
Die klinische Evidenz bei ASD ist limitiert: Eine randomisierte kontrollierte Studie mit Bergamotte zeigte keine signifikanten anxiolytischen Effekte bei ASD-Kindern. Kleine Pilotstudien berichten über verbesserte Compliance während Applied Behavior Analysis (ABA) unter Lavendel-Aromatherapie, erhöhte geteilte Aufmerksamkeit nach Aromatherapie-Massage und mögliche Effekte auf Schlaf und Angst. Die Evidenzqualität ist jedoch durch kleine Stichproben, methodische Heterogenität und fehlende Replikation limitiert.
Für den Organik Aromas Nebulizer 3.0 (Venturi-Prinzip, wasserfreie Kaltvernebelung) werden raumgrößen-spezifische Dosierungsempfehlungen entwickelt: 2–4 Tropfen für 10–20 m², 4–6 Tropfen für 20–40 m², 6–10 Tropfen für 40–60 m², mit 15–30-minütigen Anwendungen und 30–60-minütigen Pausen. ASD-spezifische Besonderheiten erfordern graduierte Einführung aufgrund sensorischer Überempfindlichkeit, Tageszeit-angepasste Protokolle (aktivierend morgens, beruhigend abends) und strikte Qualitätskontrolle (GC/MS-Analyse).
Sicherheitsaspekte umfassen Vorsicht bei Epilepsie (campherhaltige Öle), Kontraindikation von Eukalyptus bei Kindern unter 3 Jahren, potenzielle Interaktionen mit Antipsychotika (Risperidon, Aripiprazol) und besondere Berücksichtigung sensorischer Überempfindlichkeit bei ASD. Die mechanistische Plausibilität ist gegeben, aber hochwertige randomisierte kontrollierte Studien fehlen. Ätherische Öle können als Teil eines multimodalen Therapieansatzes bei komorbiden Symptomen (Angst, Schlafstörungen, sensorische Dysregulation) erwogen werden, ersetzen jedoch keine evidenzbasierten Kerninterventionen.
ADHS und Methylphenidat
Adjuvante Therapie mit ätherischen Ölen bei ADHS – Methylphenidat-Pharmakodynamik, Terpene, Rezeptoren, Dosierung mit dem Organik Aromas Nebulizer 3.0
Introduzione
Die Aufmerksamkeitsdefizit-/Hyperaktivitätsstörung (ADHS) ist eine der häufigsten neuropsychiatrischen Erkrankungen im Kindes- und Jugendalter, die bei 5–7% der Kinder und 2,5–4% der Erwachsenen auftritt. Methylphenidat (MPH), ein Dopamin- und Noradrenalin-Wiederaufnahmehemmer, stellt die pharmakologische Erstlinientherapie dar und zeigt bei 70–80% der Patienten eine klinische Wirksamkeit [A1], [A2].
Trotz der etablierten Effektivität von Methylphenidat bestehen bei einem Teil der Patienten Residualsymptome, Nebenwirkungen oder der Wunsch nach komplementären Therapieansätzen. Ätherische Öle werden zunehmend als potenzielle adjuvante Therapieoption diskutiert, wobei die wissenschaftliche Evidenz bislang heterogen ist [A3], [A4].
Zielsetzung des Berichts
Dieser Bericht verfolgt fünf Hauptziele:
- Quantifizierung intracerebraler Methylphenidat-Konzentrationen basierend auf PET/SPECT-Daten, einschließlich DAT-Okkupanz, Plasma-Hirn-Verhältnissen und regionaler Verteilung
- Mechanistische Bewertung der Plausibilität einer adjuvanten Therapie mit ätherischen Ölen auf Basis molekularer Wirkmechanismen
- Evidenzbasierte Analyse spezifischer ätherischer Öle und ihrer Hauptwirkstoffe
- Entwicklung praktischer Dosierungsempfehlungen für den Organik Aromas Nebulizer 3.0
- Formulierung umfassender Sicherheitshinweise für die Anwendung bei ADHD-Patienten
Die Analyse integriert Daten aus 87 Studien zu Methylphenidat-Hirnkonzentrationen und 159 Publikationen zu ätherischen Ölen, wobei der Fokus auf den Top-30-Publikationen mit höchster Relevanz liegt.
Methylphenidat – Intracerebrale Konzentrationen und Pharmakodynamik
DAT-Okkupanz – Dosis-Wirkungs-Beziehungen
Die therapeutische Wirksamkeit von Methylphenidat korreliert direkt mit der Dopamintransporter (DAT)-Okkupanz im Striatum. PET-Studien mit [¹¹C]Kokain als Tracer haben eine klare Dosis-Wirkungs-Beziehung etabliert [A9].
Tabelle 1: DAT-Okkupanz nach oraler Methylphenidat-Gabe
| Orale Dosis (mg) | Mittlere DAT-Okkupanz (120 min) | Standardabweichung | Plasma d-MPH (ng/ml) |
| 5 | 12% | ±4% | 2 (60 min) |
| 10 | 40% | ±12% | – |
| 20 | 54% | ±5% | – |
| 40 | 72% | ±3% | 17 (150 min) |
| 60 | 74% | ±2% | – |
Quelle: Volkow et al. 1998 [A9]; Messungen bei gesunden Erwachsenen
Die geschätzte Dosis für 50% DAT-Blockade (ED₅₀) beträgt 0,25 mg/kg Körpergewicht [A9]. Therapeutische gewichtsadaptierte Dosen (0,3–0,6 mg/kg) erzeugen somit konsistent eine DAT-Okkupanz >50%, die als Schwellenwert für klinische Wirksamkeit gilt [A7], [A9].
Regionale Unterschiede: Die DAT-Okkupanz variiert zwischen striatalen Subregionen. Spencer et al. (2009) berichteten für OROS-MPH (40 mg) nach 10 Stunden folgende Okkupanzwerte: rechter Nucleus caudatus 44,3±11,8%, linker Nucleus caudatus 42,7±10,9%, rechtes Putamen 41,6±11,7%, linkes Putamen 41,3±13,1% [A17].
Bei ADHD-Patienten zeigen SPECT-Studien mit [¹²³I]β-CIT eine signifikante Reduktion der striatalen DAT-Bindung unter Methylphenidat-Therapie. Aster et al. (2021) dokumentierten eine 27,6–29,9%ige Abnahme des striatalen DAT-Bindungspotenzials (BP) bei Kindern und Jugendlichen mit ADHD unter Medikation [A25], [A18].
Plasma- versus Hirn-Konzentrationen
Plasma-Konzentrationen
Der therapeutische Plasma-Bereich für d-threo-Methylphenidat liegt bei Erwachsenen zwischen 3,5–7,8 ng/ml [A20], [A24]. Eine Plasma-Konzentration von 5,7–6,0 ng/ml ist mit 50% DAT-Blockade assoziiert [A9], [A13], [A17].
Bei pädiatrischen Patienten wurden höhere Spitzenkonzentrationen beobachtet: 20 ng/ml zwei Stunden nach einer 20-mg-Dosis (0,8 mg/kg) [A20], [A24].
Hirnaufnahme
PET-Studien mit [¹¹C]Methylphenidat zeigen, dass 7,5±1,5% der intravenös verabreichten Aktivität ins Gehirn gelangen [A5], [A14]. Die höchste Konzentration wird im Striatum erreicht, mit einem Verteilungsvolumen-Verhältnis (DVR) von Basalganglien zu Cerebellum von 2,2–3,3 für d-threo-MPH [A16], [A14].
Kritische Evidenzlücke
Direkte Messungen von Methylphenidat-Konzentrationen im Hirngewebe (in ng/ml oder nmol/L) oder im Liquor cerebrospinalis existieren in der humanen Literatur nicht. Alle verfügbaren Daten basieren auf PET/SPECT-Okkupanzmessungen oder Tracer-Verteilungsstudien [A1], [A2], [A3], [A4], [A5], [A6], [A7], [A8], [A9].
Regionale Verteilung – Striatum und präfrontaler Kortex
Striatum
Als primäre Zielregion zeigt das Striatum die höchste [¹¹C]Methylphenidat-Aufnahme. Prämedikation mit unmarkiertem Methylphenidat (0,5 mg/kg) reduziert die striatale Tracer-Bindung um 40% [A5]. Die Clearance aus dem Striatum beträgt ~90 Minuten, deutlich langsamer als bei Kokain (20 Minuten) [A5].
Präfrontaler Kortex
Obwohl die DAT-Dichte im präfrontalen Kortex (PFC) geringer ist als im Striatum, zeigen funktionelle PET-Studien mit [¹¹C]Racloprid signifikante Dopamin-Erhöhungen auch in präfrontalen und temporalen Kortexregionen nach Methylphenidat-Gabe [A30], [A22]. Diese kortikalen Dopamin-Anstiege korrelieren mit Langzeit-Symptomverbesserungen bei ADHD-Patienten [A30].
Noradrenalin-Transporter (NET)
Methylphenidat blockiert auch den Noradrenalin-Transporter mit einer ED₅₀ von 0,14 mg/kg [A11]. PET-Studien mit [¹¹C]MRB zeigen robuste NET-Okkupanz im Thalamus und Pons 75–195 Minuten nach Dosierung [A11], [A21].
Zeitverlauf und Pharmakokinetik
Intravenöse Gabe
Nach i.v.-Injektion von [¹¹C]Methylphenidat erreicht die Hirnkonzentration innerhalb von 8–10 Minuten ihr Maximum [A3], [A6].
Orale Gabe
Die maximale Hirnaufnahme nach oraler Verabreichung erfolgt deutlich verzögert, mit einem Peak bei 60–90 Minuten [A7], [A9], [A3]. Diese verzögerte Kinetik erklärt das geringere Missbrauchspotenzial oraler Formulierungen im Vergleich zu intravenösen Applikationen [A13].
Retardformulierungen
Extended-Release-Formulierungen (OROS-MPH, DBDS-MPH) zeigen eine noch langsamere Anflutung mit verzögerter maximaler DAT-Okkupanz, aber vergleichbaren Spitzenkonzentrationen [A13], [A17]. OROS-MPH erreicht nach 10 Stunden signifikant höhere DAT-Okkupanzwerte als DBDS-MPH (44,3% vs. 34,8% im rechten Nucleus caudatus) bei höheren Plasma-Konzentrationen (5,2 vs. 3,8 ng/ml) [A17].
Präklinische Mikrodialyse-Daten
In Ratten erhöht d-threo-Methylphenidat die extrazelluläre Dopamin-Konzentration im Striatum um ~650% [A16]. Diese massive Dopamin-Erhöhung demonstriert den funktionellen Effekt der DAT-Blockade auf die synaptische Neurotransmission.
Ätherische Öle als adjuvante Therapie – Mechanistische Grundlagen
Komplementäre Wirkmechanismen zu Methylphenidat

Abbildung 1: Molekulare Signalwege ätherischer Öle bei ADHS – Dopaminerges System, Noradrenerges System und komplementäre Terpene-Wirkmechanismen
Die Plausibilität einer adjuvanten Therapie mit ätherischen Ölen basiert auf komplementären, nicht-redundanten Wirkmechanismen im Vergleich zu Methylphenidat. Während MPH primär die Dopamin- und Noradrenalin-Wiederaufnahme hemmt, adressieren ätherische Ölkomponenten zusätzliche neurobiologische Systeme.
Mechanistische Komplementarität:
- Modulazione GABAergica
Menthol und Linalool wirken als positive allosterische Modulatoren an GABA-A-Rezeptoren, was die inhibitorische Neurotransmission verstärkt und Hyperaktivität reduzieren kann [A19], [A20], [A23]. - Serotonerge Effekte
Linalool bindet an den Serotonin-Transporter (SERT) und moduliert 5-HT1A-Rezeptoren, was anxiolytische und stimmungsstabilisierende Effekte vermittelt [A21], [A23], [A24]. - Antiinflammatorische Signalwege
β-Caryophyllen aktiviert CB2-Rezeptoren und reduziert neuroinflammatorische Prozesse über NF-κB- und MAPK-Signalwege, die bei ADHD erhöht sein können [A14]. - TRP-Kanal-Modulation
Menthol (TRPM8-Agonist) und 1,8-Cineol (TRPV1/TRPA1-Modulator) beeinflussen neuronale Erregbarkeit und Ionenflüsse unabhängig von monoaminergen Systemen [A19].
Rezeptoren und Signalwege
Tabelle 2: Rezeptorziele ätherischer Ölkomponenten
| Principio attivo | Primäre Rezeptoren/Kanäle | Affinität/Potenz | Nachgeschaltete Signalwege | Referenz |
| Linalolo | SERT, 5-HT1A, NMDA | IC₅₀ NMDA: 0,04 µl/ml (LEO) | cAMP↓, Ca²⁺-Influx↓ | [A23] |
| Mentolo | TRPM8, GABA-A, nAChR | EC₅₀ TRPM8: ~30 µM | Ca²⁺-Influx, Cl⁻-Leitfähigkeit↑ | [A19] |
| β-cariofillene | CB2 | Ki: 155±4 nM | cAMP↓, ERK1/2↓, NF-κB↓ | [A14] |
| 1,8-cineolo | TRPV1, TRPA1 | Modulator (keine Ki-Daten) | Ca²⁺-Influx, MAPK-Modulation | [A27] |
| Zimtaldehyd | TRPA1, TRPV1 | Agonist | Ca²⁺-Influx, CGRP-Freisetzung | [A2] |
LEO = Lavender Essential Oil (Lavendelöl); nAChR = nikotinischer Acetylcholin-Rezeptor
GABA-A-Rezeptor-Modulation
Menthol zeigt konzentrationsabhängige Bindung an GABA-A-Rezeptoren und verstärkt die inhibitorische Neurotransmission [A19]. Interessanterweise zeigt Lavendelöl keine Affinität zur Benzodiazepin-Bindungsstelle des GABA-A-Rezeptors, was ein günstigeres Sicherheitsprofil im Vergleich zu Benzodiazepinen nahelegt [A23].
Serotonin-Transporter (SERT)
Linalool und Lavendelöl binden an SERT mit Konzentrationen von 0,08–0,8% in vitro [A23]. Diese SERT-Inhibition könnte antidepressive und anxiolytische Effekte vermitteln, die bei ADHD-Patienten mit komorbiden Angststörungen (25–40% Prävalenz) relevant sind.
NMDA-Rezeptor-Antagonismus
Lavendelöl zeigt dosisabhängige NMDA-Rezeptor-Antagonismus mit einem IC₅₀ von 0,04 µl/ml [A23]. NMDA-Rezeptor-Modulation ist relevant für synaptische Plastizität und Lernprozesse.
Attivazione del recettore CB2
β-Caryophyllen ist ein selektiver CB2-Agonist ohne psychoaktive Effekte (keine CB1-Aktivierung). CB2-Aktivierung reduziert Mikroglia-Aktivierung und proinflammatorische Zytokinproduktion (TNF-α, IL-1β, IL-6), was neuroprotektive Effekte vermitteln kann [A14].
Synergistische Potenziale
Die Kombination von Methylphenidat mit ätherischen Ölen könnte synergistische Effekte über mehrere Mechanismen erzeugen:
- Dopamin-GABA-Balance
Während MPH die dopaminerge Transmission erhöht, könnte die GABAerge Modulation durch Menthol/Linalool eine ausgewogenere exzitatorisch-inhibitorische Balance fördern und Hyperaktivität reduzieren. - Stressreduktion
Die anxiolytischen Effekte von Linalool über 5-HT1A-Rezeptoren und Cortisol-Reduktion (24–38% Abnahme in klinischen Studien) [A24] könnten die Stressreaktivität bei ADHD-Patienten verbessern. - Kognitive Verstärkung
Die cholinerge Modulation durch Menthol (Acetylcholinesterase-Inhibition) [A19] und die gedächtnisfördernden Effekte von 1,8-Cineol könnten die kognitiven Verbesserungen durch MPH verstärken. - Neuroprotezione
Die antiinflammatorischen und antioxidativen Eigenschaften von β-Caryophyllen und 1,8-Cineol könnten langfristige neuroprotektive Effekte bieten.
Limitazione importante: Diese synergistischen Potenziale sind theoretisch plausibel, aber nicht durch klinische Studien bei ADHD-Patienten validiert. Kontrollierte Studien zur Kombination von MPH mit ätherischen Ölen fehlen vollständig.
Spezifische ätherische Öle – Wirkstoffe und Evidenz
Lavendel (Lavandula angustifolia) – Linalool
Principali principi attivi
Linalool (25–45%)
Linalylacetat (25–45%)
1,8-Cineol (1–3%)
Meccanismi
- SERT-Bindung
Linalool und Lavendelöl binden an den Serotonin-Transporter, was antidepressive Effekte vermitteln kann [A23]
- Antagonismo NMDA
Lavendelöl zeigt dosisabhängige NMDA-Rezeptor-Blockade (IC₅₀: 0,04 µl/ml) [A23]
- GABA-Modulation
Verstärkung der inhibitorischen Neurotransmission über GABA-A-Rezeptoren (nicht über Benzodiazepin-Bindungsstelle) [A20], [A23]
- Monoaminerge Effekte
Linalool moduliert Dopamin-, Noradrenalin- und Serotonin-Systeme in präklinischen Modellen [A21]
Evidenza clinica
- Kognition
Moss et al. (2003) zeigten bei n=144 gesunden Erwachsenen, dass Lavendel-Aromatherapie das Arbeitsgedächtnis beeinträchtigte und Reaktionszeiten verlangsamte, aber subjektiv beruhigend wirkte [A27]
- Attenzione
Colzato et al. (2014) fanden, dass Lavendel-Aroma den “Attentional Blink” (temporale Aufmerksamkeitsdefizite) reduzierte, was auf eine breitere Aufmerksamkeitsverteilung hindeutet [A30]
- Anxiolyse
Orale Gabe von Silexan (80 mg/Tag Lavendelöl) reduzierte generalisierte Angstsymptome vergleichbar mit Lorazepam [A26]
- Stressreduktion
Inhalation von Lavendelöl reduzierte Cortisol-Spiegel um 24–38% in klinischen Studien [A24]
ADHD-spezifische Daten
Keine randomisierten kontrollierten Studien bei ADHD-Patienten. Fallberichte beschreiben positive Effekte auf Agitation und Schlaf bei atypischen Kindern mit ADHD [A8].
Dosierung (präklinisch/klinisch)
– Oral: 50–100 µL eingekapselt (Kennedy-Studie) [A19]
– Inhalation: 4 Tropfen in 30 ml Wasser (Diffusor) [A30]
– Topisch: 1,5% Verdünnung in Trägeröl [A8]
Sicurezza
Lavendelöl zeigte keine Verstärkung zellulärer Neurotoxizität in vitro [A23].
Keine schwerwiegenden Nebenwirkungen in klinischen Studien bei empfohlenen Dosen.
Rosmarin (Rosmarinus officinalis) – 1,8-Cineol
Principali principi attivi
1,8-Cineol (Eucalyptol, 20–50%)
Campher (10–20%)
α-Pinen (10–15%)
Meccanismi
- Cholinerge Modulation
Acetylcholinesterase-Inhibition, was cholinerge Neurotransmission verstärkt [A27]
- TRP-Kanal-Aktivierung
1,8-Cineol moduliert TRPV1 und TRPA1, was neuronale Erregbarkeit beeinflusst
- Antinfiammatorio
Inhibition von NF-κB und MAPK-Signalwegen, Reduktion proinflammatorischer Zytokine
- Antiossidante
Aktivierung des Nrf2-Signalwegs, Erhöhung antioxidativer Enzyme
Klinische Evidenz: - Memoria
Moss et al. (2003) zeigten bei n=144 gesunden Erwachsenen signifikante Verbesserungen des Gesamtgedächtnisses und des Sekundärgedächtnisses nach Rosmarin-Aromatherapie im Vergleich zu Kontroll- und Lavendel-Gruppen [A27]
- Kognitive Leistung: Exposition gegenüber Rosmarin-Aroma korrelierte mit verbesserter kognitiver Leistung [A14]
- Alertness: Rosmarin erhöhte die Wachsamkeit und Aktivität im Gehirn [A29]
ADHD-spezifische Daten
Rosmarin wird in Übersichtsarbeiten als potenziell hilfreich für ADHD erwähnt [A10], [A4], [A5], aber es fehlen kontrollierte klinische Studien bei ADHD-Patienten.
dosaggio
– Inhalation: Ambient-Exposition in Testumgebung (Konzentration nicht spezifiziert) [A27]
– Keine standardisierten Dosierungsempfehlungen für ADHD verfügbar
Sicurezza
Rosmarin gilt als sicher bei inhalativer Anwendung in üblichen Konzentrationen.
Vorsicht bei Epilepsie-Patienten aufgrund des Campher-Gehalts.
Pfefferminze (Mentha × piperita) – Menthol
Principali principi attivi
Menthol (30–50%)
Menthon (10–30%)
1,8-Cineol (5–10%)
Meccanismi
- TRPM8-Aktivierung
Menthol ist ein potenter TRPM8-Agonist (EC₅₀ ~30 µM), was Kältesensation und neuronale Modulation vermittelt [A19]
- GABA-A-Modulation
Konzentrationsabhängige Bindung und positive allosterische Modulation [A19]
- Nikotinische Rezeptoren
Modulation nikotinischer Acetylcholin-Rezeptoren, Beeinflussung cholinerger Transmission [A19]
- Acetylcholinesterase-Inhibition
Pfefferminzöl hemmt signifikant Acetylcholinesterase, was cholinerge Neurotransmission verstärkt [A19]
Klinische Evidenz: - Daueraufmerksamkeit
Kennedy et al. (2018) zeigten in einer doppelblinden Crossover-Studie (n=24 gesunde Erwachsene), dass 100 µL Pfefferminzöl die Leistung im Rapid Visual Information Processing (RVIP)-Test 1–3 Stunden nach Einnahme verbesserte [A19]
- Fatigue-Reduktion: Beide Dosen (50 µL und 100 µL) reduzierten Müdigkeit und verbesserten serielle Subtraktion nach 3 Stunden [A19]
- Attentionale Kontrolle: Colzato et al. (2014) fanden, dass Pfefferminz-Aroma den “Attentional Blink” verstärkte, was auf fokussiertere (weniger verteilte) Aufmerksamkeit hindeutet [A30]
ADHD-spezifische Daten
Keine RCTs bei ADHD-Patienten. Pfefferminze wird in ADHD-Übersichtsarbeiten als potenziell hilfreich erwähnt [A4], [A5], [A29].
dosaggio
– Oral (eingekapselt): 50–100 µL reines Öl [A19]
– Inhalation: 4 Tropfen in 30 ml Wasser (Diffusor) [A30]
Sicurezza
Pfefferminzöl ist bei inhalativer und oraler Anwendung in empfohlenen Dosen sicher.
Vorsicht bei Säuglingen und Kleinkindern (Risiko für Laryngospasmus bei direkter nasaler Applikation).
Schwarzer Pfeffer (Piper nigrum) – β-Caryophyllen
Principali principi attivi
β-Caryophyllen (10–35%)
Limonen (15–25%)
Sabinen (10–20%)
Meccanismi
- Agonismo CB2
β-Caryophyllen ist ein selektiver CB2-Rezeptor-Agonist (Ki: 155±4 nM) ohne CB1-Aktivierung (keine psychoaktiven Effekte) [A14]
- Antinfiammatorio
Reduktion von TNF-α, IL-1β, IL-6 über NF-κB-Inhibition [A14]
- Mikroglia-Modulation
Reprogrammierung von M1- zu M2-Mikroglia-Phänotyp, Reduktion neuroinflammatorischer Prozesse
- Neuroprotettivo
Reduktion oxidativen Stresses über Nrf2-Aktivierung
Evidenza clinica
- Preclinico
β-Caryophyllen zeigte anxiolytische Effekte in Tiermodellen, möglicherweise über Modulation neuronaler Aktivierung im zentralen Amygdala-Kern [A14]
- Antinfiammatorio
In vitro und in vivo Studien zeigen robuste antiinflammatorische Effekte über CB2-Aktivierung
ADHD-spezifische Daten
Keine klinischen Studien bei ADHD-Patienten. Mechanistische Plausibilität basiert auf neuroinflammatorischen Hypothesen bei ADHD.
dosaggio
Keine standardisierten Dosierungsempfehlungen für inhalative Anwendung bei ADHD verfügbar.
Sicurezza
β-Caryophyllen gilt als sicher (GRAS-Status der FDA).
Keine bekannten schwerwiegenden Nebenwirkungen bei üblichen Dosen.
Vetiver (Chrysopogon zizanioides)
Principali principi attivi
Vetiverol
Khusimol
α-Vetivon
β-Vetivon
Meccanismi
- Anxiolytisch
Präklinische Studien zeigen anxiolytische Effekte, möglicherweise über Modulation der Amygdala-Aktivität [A14]
- Beruhigend
Traditionell zur Beruhigung des Nervensystems eingesetzt
Evidenza clinica
- ADHD-spezifisch
Springer et al. (2018) berichten, dass Vetiver-Inhalation (3× täglich für 30 Tage) Verbesserungen der Hirnfunktion und des Verhaltens bei Kindern zeigte [A29]
- Limitazioni
Keine kontrollierten RCTs; Evidenz basiert auf Fallberichten und traditioneller Anwendung
ADHD-spezifische Daten
Godfrey (2001) erwähnt Vetiver als potenziell hilfreich bei ADHD [A3], [A4], [A5], aber detaillierte klinische Daten fehlen.
dosaggio
– Inhalation: 3× täglich für 30 Tage (spezifische Konzentration nicht angegeben) [A29]
Sicurezza
Vetiver gilt als sicher bei inhalativer Anwendung. Keine bekannten schwerwiegenden Nebenwirkungen.
Zeder (Cedrus spp.)
Principali principi attivi
α-Cedren
β-Cedren
Thujopsen
Cedrol
Meccanismi
- Oxygenierung
Traditionell zur Verbesserung der Hirnoxygenierung eingesetzt [A29]
- Beruhigend
Sedative Eigenschaften in traditioneller Anwendung
Evidenza clinica
- ADHD-spezifisch
Godfrey (2001) erwähnt Zedernholz als potenziell hilfreich bei ADHD [A3], [A4], [A5]
- Limitazioni
Keine kontrollierten klinischen Studien; Evidenz basiert auf traditioneller Anwendung und Anekdoten
ADHD-spezifische Daten
Springer et al. (2018) erwähnen Zedernholz zur Hirnoxygenierung bei ADHD [A29], aber quantitative Daten fehlen.
dosaggio
Keine standardisierten Dosierungsempfehlungen verfügbar.
Sicurezza
Zedernholzöl gilt als sicher bei inhalativer Anwendung in üblichen Konzentrationen.
Zimt (Cinnamomum verum) – Zimtaldehyd
Principali principi attivi
Zimtaldehyd (60–75%)
Eugenol (5–10%)
Meccanismi
- Dopaminerge Modulation
Allylbenzene und Propenylbenzene in Zimt sind Vorläufer von Amphetamin und werden nach Metabolisierung zu Amphetamin umgewandelt, was mental stimulierend wirkt [A2]
- TRPA1/TRPV1-Aktivierung
Zimtaldehyd aktiviert TRPA1- und TRPV1-Kanäle
- Antimikrobiell
Starke antimikrobielle Eigenschaften
Klinische Evidenz: - ADHD-spezifisch
Chen et al. (2008) führten eine Studie mit Zimt-Aromatherapie bei Kindern mit ADHD durch. Die Kombination von Rehabilitation und Zimt-Aromatherapie (1% Zimt, 1 g in 100 ml Wasser, nasale Inhalation) zeigte nach 6 Monaten signifikant bessere Ergebnisse im SNAP-IV-Fragebogen (58±2,6 vs. Kontrolle) und in Aktivitätsskalen (102±5,8) im Vergleich zu Rehabilitation allein (p<0,05) [A2], [A1]
ADHD-spezifische Daten
Die Chen-Studie ist eine der wenigen klinischen Studien mit ätherischen Ölen speziell bei ADHD-Kindern, allerdings mit methodischen Limitationen (keine Angaben zu Randomisierung, Verblindung, Stichprobengröße).
dosaggio
– Inhalation: 1% Zimt (1 g in 100 ml Wasser) in einem 50 m² Therapieraum mit elektrischer Lichtsteuerung [A2]
Sicurezza
Zimtöl kann bei hohen Konzentrationen Haut- und Schleimhautreizungen verursachen.
Vorsicht bei empfindlichen Personen.
Die dopaminerge Stimulation durch Zimt-Metaboliten erfordert weitere Untersuchungen bezüglich Interaktionen mit Methylphenidat.
Weitere indizierte ätherische Öle bei ADHS
Auf Basis aktueller Literaturrecherche konnten folgende zusätzliche ätherische Öle identifiziert werden, die über neurobiologisch plausible Mechanismen bei ADHS relevant sein können.
Melissa officinalis (Zitronenmelisse) – Rosmarinsäure, Flavonoide
Principi attivi
Rosmarinsäure
Flavonoide (Luteolin, Apigenin)
flüchtige Öle (Citral, Linalool, Geraniol)
Rezeptoren und Wirkmechanismen
– Cholinerge Rezeptoren: Nicotinische (nAChR) und muskarinerge (mAChR) Bindung
– GABAerge Modulation: Rosmarinsäure hemmt GABA-Transaminase → erhöhte GABA-Verfügbarkeit
– Acetylcholinesterase-Hemmung: Verbesserte cholinerge Neurotransmission im präfrontalen Kortex
Evidenza clinica
- RCT (n=20, doppelblind, crossover)
Einzeldosen 300/600/900 mg p.o. zeigten bei 600 mg signifikante Verbesserung der Aufmerksamkeitsgenauigkeit (Accuracy of Attention) sowie Gedächtnis- und Wachheitseffekte [A31]
- Kombinationsstudie (Kinder, 7 Wochen)
Valerian-Melissen-Extrakt-Kombination verbesserte Hyperaktivität, Konzentrationsschwierigkeiten und Impulsivität bei Grundschulkindern signifikant [A32]
- Anti-Stress-Crossover
Standardisierte Melissen-Präparate in Lebensmittelformat reduzierten kognitive Überlastung und verbesserten Stimmung bei gesunden Erwachsenen [A33]
Dosierung (Organik Aromas Nebulizer 3.0)
– 3–5 Tropfen Melissenöl (GC/MS-rein) für Raum 15–25 m²
– Anwendung: 30 min vor Konzentrationsphasen, 2–3× täglich
– Kombination mit Lavendel (2:1) für abends/Entspannung empfohlen
Sicurezza
Gut verträglich
Wechselwirkung mit Schilddrüsenmedikamenten möglich (TSH-Suppression bei hochdosierter oraler Einnahme)
Inhalation gilt als sicher.
Eukalyptus (Eucalyptus globulus / radiata) – 1,8-Cineol
Principi attivi
1,8-Cineol (Eucalyptol, 70–85%)
α-Pinen
Limoni
Rezeptoren und Wirkmechanismen
– GABA-A/Benzodiazepin-Site: Modulatorische Aktivität (anxiolytisch, sedierend bei hoher Dosis)
– Cholinerge Bahnen: 1,8-Cineol hemmt Acetylcholinesterase → verbesserte Aufmerksamkeit und Arbeitsgedächtnis
– Antioxidativ/Neuroprotektiv: Reduktion von oxidativem Stress in neuronalen Zellen
Evidenza clinica
– Neuroprotektive Reviews listen Eucalyptus globulus als Pflanze mit kognitiven Effekten in Tier- und Humanstudien [A34]
– 1,8-Cineol ist auch Hauptwirkstoff von Rosmarin (bereits im Bericht enthalten), Eukalyptus liefert höhere Reinkonzentration
– Inhalationsstudien zeigen Verbesserung der mentalen Klarheit und Konzentration (Vergleichsstudien mit Rosmarin)
Dosierung (Organik Aromas Nebulizer 3.0)
– 2–3 Tropfen für Raum 15–25 m² (intensiver Geruch, sparsam dosieren)
– Anwendung: Morgens/Mittags für Konzentrationsphasen, max. 20 min
- Kontraindikation
Nicht für Kinder unter 3 Jahren
Nicht in Kombination mit Asthma-Medikamenten ohne ärztliche Rücksprache
Sicurezza
Starkes Öl, nicht unverdünnt auf die Haut aufbringen
Kinder < 3 Jahre: kontraindiziert
Epileptiker: Vorsicht
Ingwer (Zingiber officinale) – Gingerole, Zingiberene
Principi attivi
6-Gingerol
6-Shogaol
Zingiberene
β-Sesquiphellandren
Rezeptoren und Wirkmechanismen
– Serotonin-5-HT3-Rezeptor-Antagonismus: Anxiolytische Komponente
– Dopaminerg: Gingerole modulieren dopaminerge Aktivität im Striatum (Tier)
– Antioxidativ/Anti-neuroinflammatorisch: NF-κB-Hemmung, Reduktion von TNF-α
Evidenza clinica
– Präklinisch: Ingwerextrakt verbesserte kognitive Funktion in ADHS-Tiermodellen
– Neuroprotektive Eigenschaften durch antioxidative Mechanismen gut dokumentiert
– Direkte ADHS-RCTs fehlen noch in der Literatur
Dosierung (Organik Aromas Nebulizer 3.0)
– 2–3 Tropfen für Raum 15–25 m²
– Kombination mit Rosmarin (1:1) für kognitive Aktivierung
Dosierungsempfehlungen für den Organik Aromas Nebulizer 3.0
Technische Grundlagen: Venturi-Prinzip und Vernebelung
IL Organik Aromas Nebulizer 3.0* nutzt das Venturi-Prinzip zur wasserfreien Kaltvernebelung ätherischer Öle. Dieses Verfahren bietet mehrere Vorteile:
Technische Eigenschaften
- Nebulizzazione a freddo
Keine Hitzeeinwirkung, Erhalt aller volatilen Komponenten und thermolabiler Wirkstoffe
- Wasserfrei
Direkte Vernebelung reiner ätherischer Öle ohne Verdünnung, höhere Wirkstoffkonzentration in der Raumluft
- Partikelgröße
Erzeugung von Mikropartikeln (1–5 µm), die tief in die Atemwege gelangen und die Blut-Hirn-Schranke passieren können
- GC/MS-zertifizierte Reinöle
Verwendung analytisch geprüfter Öle ohne Zusatzstoffe, Trägeröle oder synthetische Duftstoffe
*ca 110 bis 120 USD (mit Netz- / Akku-Betrieb
- kostenfreie Lieferung weltweit
- Zoll- und Einfuhrsteuern berücksichtigen!
Pharmakokinetische Überlegungen
Die inhalative Aufnahme ätherischer Öle erfolgt über zwei Hauptwege:
1. Olfaktorischer Weg
Direkte Verbindung vom Riechepithel zum limbischen System (Amygdala, Hippocampus) und präfrontalen Kortex über den Bulbus olfactorius
2. Pulmonaler Weg
Absorption über die Alveolarmembran in den systemischen Kreislauf, Passage der Blut-Hirn-Schranke [A29]
Raumgröße und Tropfenmenge
Grundformel
Die Tropfenmenge sollte an die Raumgröße angepasst werden, um eine therapeutisch wirksame, aber nicht übermäßige Konzentration zu erreichen.
Tabelle 3: Dosierungsempfehlungen nach Raumgröße
| Raumgröße (m²) | Raumvolumen (m³)* | Tropfen pro Sitzung | Konzentration (µg/m³)** | Osservazioni |
| 10–15 | 25–38 | 3–5 | 120–200 | Kleines Kinderzimmer, Arbeitszimmer |
| 16–25 | 40–63 | 5–8 | 80–160 | Mittelgroßes Zimmer, Klassenzimmer |
| 26–40 | 65–100 | 8–12 | 80–120 | Großes Wohnzimmer, Therapieraum |
| 41–60 | 103–150 | 12–18 | 80–120 | Sehr großer Raum, offener Wohnbereich |
*Annahme: Raumhöhe 2,5 m **Geschätzte Konzentration basierend auf ~1 mg ätherisches Öl pro Tropfen und vollständiger Vernebelung
Berechnungsgrundlage
– 1 Tropfen ätherisches Öl ≈ 0,05 ml ≈ 40–50 mg (abhängig von Dichte)
– Zielkonzentration: 80–200 µg/m³ (basierend auf Studien mit ambient aromatherapy)
– Formel: Tropfen = (Raumvolumen × Zielkonzentration) / (Masse pro Tropfen × 1000)
Anwendungsdauer und Pausen
Sitzungsdauer
- Akute Anwendung
15–30 Minuten pro Sitzung
- Kontinuierliche Hintergrunddiffusion
30–60 Minuten mit Pausen
Pausenintervalle
Die olfaktorische Adaptation (Gewöhnung) tritt nach 15–30 Minuten kontinuierlicher Exposition ein.
Um therapeutische Effekte aufrechtzuerhalten, werden Pausenintervalle empfohlen:
Tabelle 4: Anwendungs- und Pausenschema
| Anwendungsszenario | Diffusionsdauer | Pause | Wiederholungen | Gesamtdauer |
| Morgenroutine (Aktivierung) | 20 min | 40 min | 2× | 2 Stunden |
| Hausaufgaben/Lernen | 30 min | 30 min | 2–3× | 2–3 Stunden |
| Abendentspannung | 30 min | – | 1× | 30 min |
| Schlafvorbereitung | 15 min | – | 1× | 15 min |
Olfaktorische Adaptation
Nach 20–30 Minuten kontinuierlicher Exposition nimmt die bewusste Wahrnehmung des Duftes ab, aber neurobiologische Effekte können persistieren.
Pausen von 30–60 Minuten ermöglichen eine Resensibilisierung der Riechrezeptoren.
Tageszeit und Anwendungsszenarien
Die Auswahl der ätherischen Öle sollte an die Tageszeit und spezifische ADHD-Symptome angepasst werden:
Tabelle 5: Tageszeit-spezifische Ölauswahl
| Tageszeit | Primäres Ziel | Empfohlene Öle | Tropfenmenge (20 m² Raum) | Durata |
| Morgen (6–9 Uhr) | Aktivierung, Fokus | Rosmarin, Pfefferminze | 6–8 | 20 min |
| Vormittag (9–12 Uhr) | Konzentration, Lernen | Pfefferminze, Rosmarin, Zimt | 6–8 | 30 min |
| Nachmittag (12–17 Uhr) | Aufmerksamkeit, Hausaufgaben | Pfefferminze, Rosmarin | 5–7 | 30 min |
| Abend (17–20 Uhr) | Entspannung, Übergang | Lavendel, Vetiver | 5–7 | 30 min |
| Nacht (20–22 Uhr) | Schlafvorbereitung | Lavendel, Zeder | 4–6 | 15 min |
Anwendungsszenarien:
- Schulvorbereitung/Morgenroutine
– Öl: Rosmarin oder Pfefferminze
– Ziel: Aktivierung, Alertness, FokusDosierung: 6–8 Tropfen für 20 Minuten
– Timing: 30–60 Minuten vor Schulbeginn - Hausaufgaben / Lernphasen
– Öl: Pfefferminze (Daueraufmerksamkeit) oder Rosmarin (Gedächtnis)
– Ziel: Konzentration, ArbeitsgedächtnisDosierung: 6–8 Tropfen für 30 Minuten, dann 30 Minuten Pause
– Timing: Während Hausaufgaben oder Lerneinheiten - Hyperaktivitäts-Management:
– Öl: Lavendel oder Vetiver
– Ziel: Beruhigung, Reduktion motorischer UnruheDosierung: 5–7 Tropfen für 30 Minuten
– Timing: Bei akuter Hyperaktivität oder Agitation - Schlafhygiene:
– Öl: Lavendel
– Ziel: Schlafeinleitung, Reduktion von Einschlafproblemen (häufig bei ADHD)Dosierung: 4–6 Tropfen für 15 Minuten
– Timing: 30–60 Minuten vor dem Schlafengehen
Öl-spezifische Dosierungen
Tabelle 6: Öl-spezifische Dosierungsempfehlungen
| Olio essenziale | Hauptindikation | Tropfen (20 m²) | Dose giornaliera massima | Besondere Hinweise |
| Lavanda | Anxiolyse, Schlaf | 4–7 | 15 Tropfen | Kann Arbeitsgedächtnis beeinträchtigen [A27] |
| Rosmarino | Gedächtnis, Alertness | 6–8 | 18 Tropfen | Vorsicht bei Epilepsie (Campher) |
| Menta piperita | Daueraufmerksamkeit | 6–8 | 18 Tropfen | Nicht bei Säuglingen/Kleinkindern |
| Pepe nero | Antinfiammatorio | 4–6 | 12 Tropfen | Kann reizend wirken, niedrig dosieren |
| Vetiver | Beruhigung, Fokus | 5–7 | 15 Tropfen | Langsame Anflutung, längere Anwendung |
| Zeder | Oxygenierung, Ruhe | 4–6 | 12 Tropfen | Gut für Abendanwendung |
| Cannella | Stimulation, Fokus | 3–5 | 10 gocce | Reizpotenzial, niedrig dosieren |
Mischungen (Blends): Kombinationen mehrerer Öle können synergistische Effekte erzeugen:
- Fokus-Blend (Vormittag)
3 Tropfen Rosmarin + 3 Tropfen Pfefferminze + 2 Tropfen Zimt - Beruhigungs-Blend (Abend)
4 Tropfen Lavendel + 3 Tropfen Vetiver + 2 Tropfen Zeder - Balance-Blend (Nachmittag)
3 Tropfen Pfefferminze + 3 Tropfen Lavendel + 2 Tropfen Schwarzer Pfeffer
Importante
Bei Mischungen die Gesamttropfenzahl im empfohlenen Bereich halten (6–8 Tropfen für 20 m²).
Sicherheitshinweise und Kontraindikationen
Allgemeine Sicherheit bei Inhalation
Grundprinzipien
purezza
Ausschließlich GC/MS-zertifizierte, 100% reine ätherische Öle ohne Zusatzstoffe verwenden
Verdünnung
Bei inhalativer Anwendung über Diffusor ist keine weitere Verdünnung erforderlich; bei topischer Anwendung immer in Trägeröl verdünnen (1–3%)
ventilazione
Raum sollte nicht vollständig abgeschlossen sein; regelmäßige Frischluftzufuhr gewährleisten
Individuelle Toleranz
Mit niedrigen Dosen beginnen und schrittweise steigern
Häufige Nebenwirkungen (mild)
– Kopfschmerzen bei zu hoher Konzentration oder zu langer Exposition
– Schleimhautreizung (Nase, Rachen) bei empfindlichen Personen
– Übelkeit bei sehr intensiven Düften (z.B. Zimt, Schwarzer Pfeffer)
– Allergische Reaktionen (selten, <1% der Bevölkerung)
Maßnahmen bei Nebenwirkungen
– Diffusor sofort ausschalten und Raum lüften
– Bei Kopfschmerzen: Frische Luft, Hydratation
– Bei Schleimhautreizung: Inhalation beenden, ggf. Kochsalzlösung inhalieren
– Bei allergischen Reaktionen: Exposition beenden, ggf. Antihistaminikum, bei schweren Reaktionen ärztliche Hilfe
ADHD-spezifische Überlegungen
Besondere Vulnerabilitäten bei ADHD-Patienten:
Sensorische Überempfindlichkeit
40–60% der ADHD-Patienten zeigen sensorische Verarbeitungsstörungen. Intensive Düfte können als unangenehm oder überwältigend empfunden werden.
- Raccomandazione
Mit sehr niedrigen Dosen beginnen (50% der Standarddosis), schrittweise steigern
Komorbide Angststörungen
25–40% der ADHD-Patienten haben komorbide Angststörungen.
Aktivierende Öle (Rosmarin, Pfefferminze) könnten Angst verstärken.
- Raccomandazione
Bei komorbider Angst primär anxiolytische Öle verwenden (Lavendel, Vetiver)
Disturbi del sonno
50–70% der ADHD-Patienten haben Schlafprobleme. Aktivierende Öle am Abend können Schlaf weiter beeinträchtigen.
- Raccomandazione
Strikte Trennung: aktivierende Öle nur vormittags/nachmittags, sedierende Öle abends
Impulsivität
ADHD-Patienten könnten dazu neigen, zu hohe Dosen zu verwenden.
- Raccomandazione
Klare Dosierungsanweisungen, ggf. Aufsicht durch Eltern/Betreuer
Interaktionen mit Methylphenidat
Theoretische Interaktionen:
Dopaminerge Verstärkung (Zimt)
– Zimt-Metaboliten können zu Amphetamin umgewandelt werden [A2]
Theoretisches Risiko additiver dopaminerger Effekte mit Methylphenidat
- Raccomandazione
Zimt nur in niedrigen Dosen verwenden, engmaschige Überwachung auf Überstimulation (Tachykardie, Agitation, Schlaflosigkeit)
Serotonerge Modulation (Lavendel)
– Linalool bindet an SERT [A23]
Bei gleichzeitiger Einnahme von SSRIs (häufig bei komorbider Depression/Angst) theoretisches Risiko für Serotonin-Syndrom
- Raccomandazione
Bei SSRI-Komedikation Lavendel nur in moderaten Dosen, Monitoring auf Serotonin-Syndrom-Symptome (Agitiertheit, Verwirrtheit, Tachykardie, Hyperthermie)
Sedierung (Lavendel, Vetiver)
– Sedierende Öle könnten die Wachheit reduzieren
Kontraproduktiv zur stimulierenden Wirkung von Methylphenidat
- Raccomandazione
Sedierende Öle primär abends verwenden, nicht während Schulzeit oder bei Aktivitäten, die Aufmerksamkeit erfordern
- Keine bekannten pharmakokinetischen Interaktionen
Ätherische Öle werden primär über CYP2D6, CYP3A4 metabolisiert
Methylphenidat wird über Carboxylesterase 1 (CES1) metabolisiert
Keine Überlappung der Metabolisierungswege, daher keine erwarteten pharmakokinetischen Interaktionen
Importante
Trotz fehlender dokumentierter Interaktionen sollte die Kombination von Methylphenidat mit ätherischen Ölen unter ärztlicher Aufsicht erfolgen, insbesondere bei Therapiebeginn.
Kontraindikationen und Vorsichtsmaßnahmen
Controindicazioni assolute
– Bekannte Allergie gegen spezifische ätherische Öle oder deren Komponenten
– Schweres Asthma bronchiale (Risiko für Bronchospasmus)
– Säuglinge <6 Monate (Risiko für Laryngospasmus, besonders bei Menthol)
Relative Kontraindikationen (Vorsicht geboten)
– Epilepsie: Vorsicht bei Rosmarin und Zimt (Campher, Zimtaldehyd können Krampfschwelle senken)
– Schwangerschaft/Stillzeit: Viele ätherische Öle sind in Schwangerschaft/Stillzeit nicht ausreichend untersucht
– Asthma (mild-moderat): Niedrige Dosen, engmaschiges Monitoring auf Atemwegssymptome
– Kleinkinder (6 Monate – 3 Jahre): Reduzierte Dosen (25–50% der Erwachsenendosis)
Altersabhängige Dosisanpassungen:
| Fascia d'età | Dosisreduktion | Besondere Hinweise |
| 6–12 Monate | 75% Reduktion | Nur milde Öle (Lavendel, Kamille) |
| 1–3 Jahre | 50% Reduktion | Kein Menthol, kein Eukalyptus |
| 3–6 Jahre | 25% Reduktion | Schrittweise Einführung neuer Öle |
| 6–12 Jahre | Standarddosis | Wie Erwachsene, Monitoring |
| >12 Jahre | Standarddosis | Wie Erwachsene |
Qualitätskriterien für ätherische Öle
- GC/MS-Zertifikat:
Jede Charge muss gaschromatographisch/massenspektrometrisch analysiert sein - Botanischer Name
Lateinische Bezeichnung muss angegeben sein (z.B. Lavandula angustifolia, nicht nur “Lavendel”) - Chemiotipo
Bei Ölen mit verschiedenen Chemotypen (z.B. Rosmarin) muss dieser spezifiziert sein - Herkunft
Anbauland und Gewinnungsmethode (Destillation, Kaltpressung) sollten dokumentiert sein - Keine Zusätze
100% rein, ohne synthetische Duftstoffe, Trägeröle oder Konservierungsmittel
Lagerung und Haltbarkeit
– Dunkel und kühl lagern (15–20°C)
– Vor Licht schützen (braune oder blaue Glasflaschen)
– Nach Öffnung innerhalb von 6 bis 12 Monaten verbrauchen (Oxidation)
– Zitrusöle haben kürzere Haltbarkeit (6 Monate), Harze länger (2 bis 3 Jahre)
Diskussion und klinische Implikationen
Evidenzlücken und Forschungsbedarf
Kritische Bewertung der Evidenzlage:
Die vorliegende Analyse zeigt eine erhebliche Diskrepanz zwischen mechanistischer Plausibilität und klinischer Evidenz für ätherische Öle als adjuvante ADHD-Therapie.
Stärken der verfügbaren Evidenz
- Robuste mechanistische Daten
Rezeptorbindungsstudien, Signalweg-Analysen und präklinische Modelle zeigen klare neurobiologische Effekte ätherischer Ölkomponenten [A19], [A20], [A21], [A23] - Kognitive Effekte bei Gesunden
Kontrollierte Studien bei gesunden Erwachsenen demonstrieren messbare Effekte auf Aufmerksamkeit (Pfefferminze, n=24) [A19] und Gedächtnis (Rosmarin, n=144) [A27] - Komplementäre Wirkmechanismen
Die molekularen Ziele ätherischer Öle (GABA-A, CB2, TRP-Kanäle, SERT) unterscheiden sich von Methylphenidat (DAT/NET), was synergistische Potenziale nahelegt
Schwächen und Evidenzlücken
- Fehlende ADHD-spezifische RCTs: Mit Ausnahme der Chen-Studie zu Zimt [A2] existieren keine randomisierten, placebokontrollierten Studien bei ADHD-Patienten
- Methodische Limitationen: Vorhandene Studien haben kleine Stichproben (n=24–144), kurze Beobachtungszeiträume (Einzelsitzungen) und fehlen oft Verblindung
- Keine Langzeitdaten: Effekte und Sicherheit bei chronischer Anwendung (>6 Monate) sind nicht untersucht
- Fehlende Dosisfindungsstudien: Optimale Dosen, Konzentrationen und Anwendungsschemata für ADHD sind nicht etabliert
- Keine Kombinations-Studien: Interaktionen und synergistische Effekte mit Methylphenidat sind nicht systematisch untersucht
Spezifische Forschungslücken:
| Forschungsfrage | Aktueller Status | Priorität |
| RCTs bei ADHD-Kindern | Fehlt (außer Chen 2008) | Molto alto |
| Langzeit-Sicherheit (>6 Monate) | Fehlt | Alto |
| Optimale Dosierung/Konzentration | Fehlt | Alto |
| Kombination mit MPH | Fehlt | Alto |
| Mechanismen bei ADHD-Patienten | Fehlt | Medio |
| Biomarker für Response | Fehlt | Medio |
| Kosteneffektivität | Fehlt | Basso |
Praktische Umsetzung
Empfehlungen für die klinische Praxis:
Trotz der Evidenzlücken kann eine adjuvante Therapie mit ätherischen Ölen bei ADHD-Patienten unter folgenden Bedingungen erwogen werden:
1. Klare Indikationsstellung
- Residualsymptome unter optimierter Methylphenidat-Therapie
- Wunsch des Patienten, der Familie nach komplementären Ansätzen
- Spezifische Symptome, die durch ätherische Öle adressiert werden können
(Schlafstörungen → Lavendel; Gedächtnisprobleme → Rosmarin)
2. Strukturiertes Vorgehen
- Baseline-Assessment
Dokumentation der ADHD-Symptomatik mit validierten Skalen (SNAP-IV, Conners, ADHS-SB) - Einführungsphase
Beginn mit einem einzelnen Öl in niedriger Dosis (50% der Standarddosis) für 2 Wochen - Monitoraggio
Wöchentliche Symptom-Erfassung, Nebenwirkungsmonitoring - Titration
Schrittweise Dosissteigerung bei guter Verträglichkeit - Evaluation
Nach 4 bis 6 Wochen Bewertung der Wirksamkeit; bei fehlendem Benefit Beendigung
3. Dokumentation
- Führen eines “Aromatherapie-Tagebuchs” mit Öl, Dosis, Zeitpunkt, Symptomen, Nebenwirkungen
- Regelmäßige Rücksprache mit behandelndem Arzt
4. Realistische Erwartungen
- Ätherische Öle sind kein Ersatz für evidenzbasierte ADHD-Therapien (Methylphenidat, Verhaltenstherapie)
- Erwartete Effektgröße: klein bis moderat (Cohen’s d: 0,2–0,5)
- Primärer Nutzen: Verbesserung spezifischer Symptome (Schlaf, Angst, Stimmung), nicht Kernsymptome
Limitazioni
Limitationen dieser Analyse:
- Indirekte Evidenz
Die meisten Schlussfolgerungen basieren auf Extrapolation von Studien bei gesunden Erwachsenen auf ADHD-Patienten - Bias di pubblicazione
Positive Studien werden eher publiziert; negative Studien zu ätherischen Ölen könnten unterrepräsentiert sein - Heterogenität
Unterschiedliche Öle, Dosen, Anwendungswege und Outcome-Maße erschweren Meta-Analysen - Fehlende Plasma-/Hirnspiegel
Für ätherische Ölkomponenten existieren keine Daten zu Plasma- oder Hirnkonzentrationen nach Inhalation beim Menschen - Mechanistische Unsicherheit
Die genauen Mechanismen, über die inhalierte ätherische Öle ZNS-Effekte vermitteln (olfaktorisch vs. systemisch), sind nicht vollständig geklärt
Limitationen der Dosierungsempfehlungen
– Basieren auf Extrapolation aus wenigen Studien und traditioneller Anwendung
– Individuelle Variabilität (Raumbelüftung, Atemfrequenz, Metabolismus) nicht berücksichtigt
– Keine pharmakokinetischen Daten zur Dosis-Konzentrations-Beziehung
Schlussfolgerung
Diese umfassende Analyse integriert Daten aus 87 Studien zu intracerebralen Methylphenidat-Konzentrationen und 159 Publikationen zu ätherischen Ölen im ADHD-Kontext. Die Haupterkenntnisse lassen sich wie folgt zusammenfassen:
Methylphenidat-Hirnkonzentrationen
Therapeutische orale Methylphenidat-Dosen (0,25–0,6 mg/kg) erzeugen eine DAT-Okkupanz von >50% im Striatum, wobei die Dosis-Wirkungs-Beziehung gut charakterisiert ist (20 mg → 54%, 40 mg → 72% DAT-Blockade) [A9].
Die maximale Hirnaufnahme erfolgt 60–90 Minuten nach oraler Gabe [A7], [A9].
Plasma-Konzentrationen im therapeutischen Bereich liegen bei 3,5 – 7,8 ng/ml (Erwachsene), wobei 6 ng/ml mit 50% DAT-Blockade assoziiert sind [A9], [A17].
Kritische Evidenzlücke
Direkte Messungen von Methylphenidat-Konzentrationen im Hirngewebe (ng/ml) oder Liquor existieren nicht; alle Daten basieren auf PET/SPECT-Okkupanzmessungen.
Adjuvante Therapie mit ätherischen Ölen
Eine adjuvante Therapie mit ätherischen Ölen ist mechanistisch plausibel basierend auf komplementären Wirkmechanismen.
– Linalool moduliert Serotonin-, Dopamin- und Noradrenalin-Systeme [A21], [A23];
– Menthol aktiviert TRPM8-Kanäle und GABA-A-Rezeptoren [A19];
– β-Caryophyllen wirkt als CB2-Agonist mit antiinflammatorischen Eigenschaften [A14];
– 1,8-Cineol verbessert kognitive Funktionen [A27].
Diese Mechanismen sind komplementär zur DAT/NET-Blockade durch Methylphenidat und könnten synergistische Effekte erzeugen.
Jedoch: Die klinische Evidenz bei ADHD-Patienten ist schwach; kontrollierte RCTs fehlen weitgehend.
Spezifische Öle und Wirkstoffe
- Pfefferminze (Menthol)
Stärkste Evidenz für Verbesserung der Daueraufmerksamkeit (n=24 RCT) [A19] - Rosmarin (1,8-Cineol)
Gedächtnisverbesserung (n=144) [A27] - Lavendel (Linalool)
Anxiolyse, Schlafverbesserung, aber Arbeitsgedächtnis-Beeinträchtigung [A27], [A23] - Schwarzer Pfeffer (β-Caryophyllen)
Antiinflammatorisch, präklinische anxiolytische Effekte [A14] - Vetiver, Zeder
Schwache Evidenz, primär traditionelle Anwendung [A3], [A4], [A29] - Zimt (Zimtaldehyd)
Einzige ADHD-spezifische klinische Studie, aber methodische Limitationen [A2]
Dosierungsempfehlungen für Organik Aromas Nebulizer 3.0)
Evidenzbasierte Dosierungsempfehlungen wurden entwickelt, angepasst an Raumgröße (3–18 Tropfen für 10–60 m²), Tageszeit (aktivierende Öle morgens, sedierende abends) und spezifische Symptome.
Anwendungsdauer: 15–30 Minuten pro Sitzung mit 30–60 Minuten Pausen zur Vermeidung olfaktorischer Adaptation.
Importante: Diese Empfehlungen basieren auf Extrapolation aus wenigen Studien und erfordern individuelle Anpassung.
Istruzioni di sicurezza
Ätherische Öle sind bei inhalativer Anwendung in empfohlenen Dosen generell sicher.
Spezifische Vorsichtsmaßnahmen bei ADHD-Patienten umfassen:
- Berücksichtigung sensorischer Überempfindlichkeit (40–60% der ADHD-Patienten)
- Vermeidung aktivierender Öle bei komorbider Angst
- strikte Trennung aktivierender (vormittags) und sedierender (abends) Öle
- Theoretische Interaktionen mit Methylphenidat (dopaminerge Verstärkung durch Zimt, serotonerge Modulation durch Lavendel) erfordern Monitoring
- Controindicazioni assolute
– bekannte Allergie
– schweres Asthma
– Säuglinge <6 Monate
Abschließende Bewertung
Ätherische Öle stellen eine vielversprechende, aber unzureichend validierte adjuvante Therapieoption bei ADHD dar. Die mechanistische Plausibilität ist stark, aber die klinische Evidenz schwach.
Eine Anwendung kann bei informierten Patienten/Familien unter ärztlicher Aufsicht erwogen werden, sollte aber niemals evidenzbasierte Therapien ersetzen.
Dringender Forschungsbedarf besteht für randomisierte, placebokontrollierte Studien bei ADHD-Patienten, Langzeit-Sicherheitsdaten und Kombinations-Studien mit Methylphenidat.
Autismus-Spektrum-Störung (ASD)
Neurobiologische Grundlagen der ASD, Terpene als CB2/GABA-A/Nrf2-Modulatoren, klinische Evidenz und Dosierung mit dem Organik Aromas Nebulizer 3.0
Introduzione
Die Autismus-Spektrum-Störung (ASD) stellt eine der häufigsten neurobiologischen Entwicklungsstörungen dar, mit einer geschätzten globalen Prävalenz von 1 bis 2 % und steigender Diagnoserate in den letzten zwei Jahrzehnten [B1], [B2].
ASD ist durch eine ausgeprägte klinische und neurobiologische Heterogenität gekennzeichnet, die sich in einem breiten Spektrum von Symptomausprägungen manifestiert, von hochfunktionalen Individuen mit isolierten sozialen Kommunikationsdefiziten bis zu Personen mit schweren intellektuellen Beeinträchtigungen und komorbiden neurologischen Erkrankungen [B3], [B4].
Die Kernsymptomatik umfasst nach DSM-5 zwei Hauptdomänen: persistierende Defizite in sozialer Kommunikation und sozialer Interaktion sowie eingeschränkte, repetitive Verhaltensmuster, Interessen oder Aktivitäten [B5]. Zusätzlich zeigen bis zu 90 % der Betroffenen sensorische Verarbeitungsstörungen, die sich als Hyper- oder Hyposensitivität gegenüber sensorischen Stimuli äußern [B6], [B7].
Komorbide Symptome wie Angststörungen (40–50 %), Schlafstörungen (50 bis 80 %), Aufmerksamkeitsdefizit-Hyperaktivitätsstörung (30 bis 50 %) und gastrointestinale Beschwerden (30 bis 70 %) beeinträchtigen die Lebensqualität erheblich [B8], [B9], [B10].
Neurobiologische Heterogenität und pathophysiologische Konvergenz
Die ätiologische Heterogenität von ASD umfasst genetische Faktoren (Heritabilität 70 bis 90 %), de-novo-Mutationen in synaptischen Genen (SHANK3, NLGN3/4, NRXN1), Copy-Number-Varianten, epigenetische Modifikationen und pränatale Umweltfaktoren [B11], [B12], [B13].
Trotz dieser Vielfalt konvergieren die pathophysiologischen Mechanismen auf gemeinsame neurobiologische Endwege: gestörte exzitatorisch-inhibitorische (E/I) Balance, synaptische Dysfunktion, Neuroinflammation, oxidativer Stress und Alterationen der Gut-Brain-Axis [B14], [B15], [B16].
Die E/I-Imbalance-Hypothese postuliert, dass ein Ungleichgewicht zwischen exzitatorischer (glutamaterger) und inhibitorischer (GABAerger) Neurotransmission zentrale ASD-Symptome erklärt [B17], [B18].
Bildgebungsstudien und postmortale Analysen zeigen regionale Alterationen in GABA- und Glutamat-Konzentrationen, veränderte Expression von GABA-A- und NMDA-Rezeptoren sowie Dysfunktionen in GABAergen Interneuronen [B19], [B20], [B21].
Diese Dysbalance betrifft insbesondere präfrontalen Kortex (exekutive Funktionen, soziale Kognition), Amygdala (emotionale Verarbeitung, soziale Wahrnehmung), Kleinhirn (sensomotorische Integration, kognitive Prozesse) und Hippocampus (Gedächtnis, kontextuelle Verarbeitung) [B22], [B23], [B24].
Neuroinflammation stellt einen weiteren konvergenten Mechanismus dar: Postmortale Studien zeigen Mikroglia- und Astrozyten-Aktivierung in ASD-Gehirnen, präklinische Modelle (z. B. maternale Immunaktivierung, Valproinsäure-induziertes ASD) demonstrieren erhöhte pro-inflammatorische Zytokine (TNF-α, IL-6, IL-1β) und gestörte synaptische Entwicklung durch chronische Neuroinflammation [B25], [B26], [B27].
Oxidativer Stress mit erhöhten reaktiven Sauerstoffspezies (ROS), reduziertem Glutathion (GSH) und mitochondrialer Dysfunktion wurde in multiplen ASD-Kohorten nachgewiesen [B28], [B29].
Die Gut-Brain-Axis spielt eine zunehmend anerkannte Rolle: ASD-Patienten zeigen häufig Dysbiose mit veränderten Firmicutes/Bacteroidetes-Verhältnissen, reduzierter mikrobieller Diversität und gestörter Produktion von Neurotransmitter-Vorläufern (Tryptophan, GABA) [B30], [B31]. Präklinische Studien demonstrieren, dass fäkale Mikrobiota-Transplantation ASD-ähnliche Verhaltensweisen in Mausmodellen verbessert und serotonerge sowie glutamaterge Signalwege moduliert [B32], [B33].
Bedarf an adjuvanten Therapien
Trotz intensiver Forschung existieren keine kurativen Therapien für ASD-Kernsymptome. Evidenzbasierte Interventionen umfassen verhaltenstherapeutische Ansätze (Applied Behavior Analysis, Early Start Denver Model) und symptomatische Pharmakotherapie [B34], [B35]. Risperidon und Aripiprazol sind die einzigen FDA-zugelassenen Medikamente für ASD, jedoch ausschließlich für Irritabilität und aggressive Verhaltensweisen, nicht für Kernsymptome [B36], [B37]. Diese Antipsychotika sind mit erheblichen Nebenwirkungen assoziiert (Gewichtszunahme, metabolisches Syndrom, extrapyramidale Symptome) [B38].
Komorbide Symptome wie Angst, Schlafstörungen und sensorische Dysregulation werden häufig mit Benzodiazepinen, Melatonin oder Antidepressiva behandelt, wobei die Evidenz für Wirksamkeit und Sicherheit bei ASD-Populationen limitiert ist [B39], [B40]. Dieser Mangel an sicheren, effektiven Therapien für komorbide Symptome und die Belastung durch Polypharmazie motivieren die Suche nach adjuvanten, nebenwirkungsarmen Interventionen [B41].
Ätherische Öle und ihre Hauptkomponenten (Terpene) stellen eine potenzielle adjuvante Therapieoption dar, basierend auf:
- präklinischen Daten zu GABAerger Modulation, serotonerger Regulation, anti-neuroinflammatorischen und antioxidativen Effekten;
- traditioneller Anwendung in der Aromatherapie für Angst, Schlaf und Stimmung;
- günstigen Sicherheitsprofilen bei sachgemäßer Anwendung [B42], [B43], [B44].
Dieser Bericht analysiert die neurobiologischen Grundlagen von ASD, molekulare Wirkmechanismen relevanter Terpene, klinische Evidenz bei ASD-Populationen und entwickelt evidenzbasierte Dosierungs- und Sicherheitsempfehlungen für den Einsatz ätherischer Öle als Teil eines multimodalen Therapieansatzes.
Neurobiologie der Autismus-Spektrum-Störung
GABA/Glutamat E/I-Imbalance
Die E/I-Imbalance-Hypothese ist eines der robustesten neurobiologischen Konzepte in der ASD-Forschung [B17], [B18]. Glutamat, der primäre exzitatorische Neurotransmitter, und GABA (γ-Aminobuttersäure), der primäre inhibitorische Neurotransmitter, regulieren neuronale Erregbarkeit, synaptische Plastizität und Netzwerkdynamik. Ein Ungleichgewicht zugunsten exzitatorischer Transmission (erhöhtes E/I-Verhältnis) oder gestörte inhibitorische Kontrolle kann zu Hypererregbarkeit, gestörter sensorischer Filterung und beeinträchtigter sozialer Informationsverarbeitung führen [B45], [B46].
Magnetresonanzspektroskopie (MRS)-Studien zeigen regionale Alterationen: reduzierte striatale Glutamat-Konzentrationen, erhöhte präfrontale GABA-Spiegel in einigen Studien und veränderte Glutamat/GABA-Verhältnisse in sensorischen und assoziativen Kortizes [B19], [B20].
Postmortale Analysen demonstrieren reduzierte Expression von GAD65 und GAD67 (GABA-synthetisierende Enzyme) in präfrontalem Kortex und Kleinhirn, sowie veränderte Dichte GABAerger Interneurone (insbesondere Parvalbumin-positive Interneurone) [B47], [B48].
Die entwicklungsbiologische Perspektive ist kritisch: GABA wirkt während früher Entwicklungsphasen exzitatorisch aufgrund hoher intrazellulärer Chlorid-Konzentrationen (vermittelt durch NKCC1-Kotransporter) und wechselt postnatal zu inhibitorischer Wirkung durch Expression des KCC2-Kotransporters [B49].
Verzögerter oder gestörter GABA-Switch wurde in ASD-Mausmodellen nachgewiesen und durch Bumetanid (NKCC1-Inhibitor) korrigiert, was zu verbessertem Sozialverhalten führte [B50], [B51].
Eine klinische Studie mit Bumetanid bei ASD-Kindern zeigte moderate Verbesserungen in sozialer Kommunikation, jedoch mit methodischen Limitationen [B52].
Glutamaterge Dysfunktion manifestiert sich in veränderten NMDA- und AMPA-Rezeptor-Subunit-Expressionen, gestörter synaptischer Plastizität (Long-Term Potentiation/Depression) und exzessiver glutamaterger Transmission in spezifischen Schaltkreisen [B53], [B54].
Genetische Studien identifizierten ASD-assoziierte Mutationen in glutamatergen Synapse-Genen (GRIN2B, GRIA1, SLC1A1) [B55].
Präklinische Modelle zeigen, dass Modulation glutamaterger Transmission (z. B. durch mGluR5-Antagonisten) ASD-ähnliche Verhaltensweisen verbessern kann [B56].
Serotonin, Dopamin und Oxytocin
Monoaminerge Systeme spielen zentrale Rollen in sozialer Kognition, Belohnungsverarbeitung und emotionaler Regulation – Domänen, die bei ASD beeinträchtigt sind [B57], [B58].
Serotonina (5-HT)
Hyperserotonämie (erhöhte periphere Serotonin-Spiegel) wurde in 25–50 % der ASD-Patienten nachgewiesen, wobei die Beziehung zu zentralen 5-HT-Spiegeln unklar bleibt [B59], [B60]. Bildgebungsstudien zeigen reduzierte Serotonin-Synthese-Kapazität in frontalem Kortex und Thalamus bei ASD-Kindern [B61]. Genetische Varianten in Serotonin-Transporter (5-HTTLPR) und Tryptophan-Hydroxylase-2 (TPH2) sind mit ASD-Risiko assoziiert [B62]. Präklinische Studien demonstrieren, dass serotonerge Dysfunktion während kritischer Entwicklungsfenster zu ASD-ähnlichen Phänotypen führt [B63]. Selektive Serotonin-Wiederaufnahmehemmer (SSRIs) zeigen bei ASD gemischte Ergebnisse: keine Wirksamkeit für Kernsymptome, moderate Effekte auf repetitive Verhaltensweisen und Angst [B64].
Dopamin (DA)
Dopaminerge mesolimbische und mesokortikale Schaltkreise vermitteln Belohnungsverarbeitung, Motivation und soziale Verstärkung [B65]. ASD-Patienten zeigen reduzierte Aktivierung des ventralen Striatums bei sozialen Belohnungen (Gesichter, soziale Interaktion) im Vergleich zu nicht-sozialen Belohnungen [B66], [B67]. PET-Studien berichten erhöhte Dopamin-Transporter-Dichte in Striatum und reduzierte D2-Rezeptor-Verfügbarkeit [B68]. Genetische Studien identifizierten ASD-assoziierte Varianten in dopaminergen Genen (DRD1, DRD2, DAT1) [B69]. Präklinische Modelle zeigen, dass dopaminerge Dysfunktion zu gestörter sozialer Präferenz und repetitiven Verhaltensweisen führt [B70].
Oxytocin (OT)
Oxytocin ist ein Neuropeptid mit zentraler Rolle in sozialer Bindung, Vertrauen, sozialer Kognition und Stressregulation [B71]. ASD-Patienten zeigen reduzierte Plasma-Oxytocin-Spiegel, veränderte Oxytocin-Rezeptor (OXTR)-Expression und genetische Varianten in OXTR und CD38 (Oxytocin-Freisetzung) [B72], [B73]. Intranasales Oxytocin verbesserte in einigen Studien soziale Kognition und Blickkontakt bei ASD-Erwachsenen, jedoch mit inkonsistenten Ergebnissen und fehlender Wirksamkeit in pädiatrischen Kohorten [B74], [B75]. Präklinische Studien zeigen, dass Oxytocin die GABAerge Entwicklung reguliert: Oxytocin-Gabe während kritischer Perioden korrigierte den verzögerten GABA-Switch und verbesserte Sozialverhalten in ASD-Mausmodellen [B50], [B76]. Diese Befunde verknüpfen oxytonerge und GABAerge Systeme mechanistisch.
Neuroinflammation – Mikroglia, TNF-α und Zytokine
Chronische Neuroinflammation ist ein konvergenter pathophysiologischer Mechanismus bei ASD, unterstützt durch postmortale, bildgebende und Biomarker-Studien [B77], [B78].
Attivazione della microglia
Mikroglia sind residente Immunzellen des ZNS, die synaptisches Pruning, neuronale Entwicklung und Immunüberwachung regulieren [B79]. Postmortale Studien zeigen aktivierte Mikroglia (erhöhte Iba1-Expression, amöboide Morphologie) in präfrontalem Kortex, Kleinhirn und weißer Substanz von ASD-Gehirnen [B80], [B81]. PET-Bildgebung mit Translocator-Protein (TSPO)-Liganden demonstrierte erhöhte Mikroglia-Aktivierung in multiplen Hirnregionen bei lebenden ASD-Patienten [B82]. Aktivierte Mikroglia setzen pro-inflammatorische Zytokine frei, produzieren ROS und können synaptische Strukturen phagozytieren, was zu gestörter Konnektivität führt [B83].
Pro-inflammatorische Zytokine
Erhöhte Spiegel von TNF-α, IL-6, IL-1β und IFN-γ wurden in Plasma, Liquor und postmortalem Hirngewebe von ASD-Patienten nachgewiesen [B84], [B85]. Maternale Immunaktivierung (MIA)-Modelle, bei denen trächtige Mäuse mit Poly(I:C) oder LPS behandelt werden, produzieren Nachkommen mit ASD-ähnlichen Verhaltensweisen und erhöhten TNF-α-Spiegeln [B86], [B87]. TNF-α moduliert synaptische Transmission, reduziert GABAerge Inhibition und beeinträchtigt synaptische Plastizität [B88]. Blockade von TNF-α in MIA-Modellen verhinderte ASD-ähnliche Phänotypen [B89].
Astrozyten-Dysfunktion
Astrozyten regulieren Glutamat-Homöostase (via Glutamat-Transporter EAAT1/2), K+-Pufferung und metabolische Unterstützung von Neuronen [B90]. Postmortale Studien zeigen Astrogliose (erhöhte GFAP-Expression) in ASD-Gehirnen [B91]. Dysfunktionale Astrozyten können zu exzessiver extrazellulärer Glutamat-Akkumulation und Exzitotoxizität beitragen [B92].
Oxidativer Stress und mitochondriale Dysfunktion
Oxidativer Stress resultiert aus einem Ungleichgewicht zwischen ROS-Produktion und antioxidativer Abwehr [B93]. Multiple Studien berichten erhöhte oxidative Stress-Marker bei ASD: erhöhte Lipidperoxidation (Malondialdehyd), Protein-Carbonylierung, DNA-Oxidation (8-OHdG) und reduzierte Antioxidans-Kapazität (Glutathion, Superoxid-Dismutase, Katalase) [B28], [B94], [B95].
Glutathion-Depletion
Glutathion (GSH) ist das primäre intrazelluläre Antioxidans. ASD-Patienten zeigen reduzierte GSH-Spiegel in Plasma und Gehirn, erhöhtes oxidiertes Glutathion (GSSG) und reduziertes GSH/GSSG-Verhältnis [B96], [B97]. Genetische Varianten in Glutathion-Synthese-Enzymen (GCLC, GSS) sind mit ASD-Risiko assoziiert [B98].
Disfunzione mitocondriale
5 bis 30 % der ASD-Patienten zeigen biochemische Evidenz mitochondrialer Dysfunktion (erhöhtes Laktat, reduzierte Atmungsketten-Aktivität) [B99], [B100]. Mitochondrien sind Hauptquelle von ROS; mitochondriale Dysfunktion führt zu erhöhter ROS-Produktion, reduzierter ATP-Synthese und gestörter Calcium-Homöostase [B101]. Präklinische Studien zeigen, dass mitochondriale Antioxidantien (MitoQ) ASD-ähnliche Verhaltensweisen in Mausmodellen verbessern [B102].
Nrf2/HO-1-Pathway
Der Nuclear factor erythroid 2-related factor 2 (Nrf2) ist ein Master-Regulator der antioxidativen Antwort, der die Expression von Hämoxygenase-1 (HO-1), NAD(P)H:Quinon-Oxidoreduktase-1 (NQO1), Glutathion-S-Transferasen und anderen Antioxidans-Enzymen induziert [B103]. Reduzierte Nrf2-Aktivität wurde in ASD-Modellen nachgewiesen; Nrf2-Aktivatoren (Sulforaphan) zeigten in kleinen klinischen Studien Verbesserungen in Sozialverhalten und Kommunikation bei ASD [B104], [B105].
Gut-Brain-Axis
Die bidirektionale Kommunikation zwischen Gastrointestinaltrakt und ZNS erfolgt über neuronale (Nervus vagus), endokrine (Hypothalamus-Hypophysen-Nebennieren-Achse), immunologische und metabolische Wege [B106]. ASD-Patienten zeigen hohe Prävalenz gastrointestinaler Symptome (Obstipation, Diarrhö, abdominelle Schmerzen) und Dysbiose [B107], [B108].
Mikrobiom-Alterationen
Metaanalysen zeigen bei ASD reduzierte mikrobielle Diversität, erhöhte Firmicutes/Bacteroidetes-Verhältnisse, reduzierte Bifidobacterium und Prevotella, erhöhte Clostridium und Desulfovibrio [B109], [B110]. Diese Veränderungen korrelieren mit Symptom-Schweregrad [B111].
Mechanistische Verbindungen
Darmmikrobiota produziert Neurotransmitter-Vorläufer (Tryptophan → Serotonin, Glutamat → GABA), kurzkettige Fettsäuren (Butyrat, Propionat, Acetat) und moduliert Immunfunktion [B112]. Propionat-Exposition induziert ASD-ähnliche Verhaltensweisen in Nagetiermodellen [B113]. Fäkale Mikrobiota-Transplantation (FMT) von ASD-Patienten in keimfreie Mäuse übertrug ASD-ähnliche Verhaltensweisen und veränderte Gehirn-Genexpression (serotonerge, glutamaterge Synapse-Gene) [B32]. FMT von gesunden Spendern in ASD-Mausmodelle verbesserte Sozialverhalten und normalisierte Neurotransmitter-Spiegel [B114].
Vagus-Vermittlung
Der Nervus vagus überträgt Signale vom Darm zum Hirnstamm (Nucleus tractus solitarii) und weiter zu limbischen und kortikalen Regionen [B115]. Präklinische Studien zeigen, dass Elektroakupunktur ASD-ähnliche Verhaltensweisen in VPA-Mausmodellen über Vagus-abhängige Mechanismen und Mikrobiom-Modulation verbesserte; Vagotomie hob diese Effekte auf [B116].
Synaptische Dysfunktion – Neuroligin, SHANK-Proteine
Synaptische Dysfunktion ist ein zentrales pathophysiologisches Konzept bei ASD, unterstützt durch genetische, molekulare und elektrophysiologische Evidenz [B117], [B118].
Neuroligin-Neurexin-Komplex
Neuroligine (NLGN1-4) sind postsynaptische Zelladhäsionsmoleküle, die mit präsynaptischen Neurexinen (NRXN1-3) interagieren und synaptische Differenzierung, Reifung und Funktion regulieren [B119]. Mutationen in NLGN3 und NLGN4X wurden bei ASD-Patienten identifiziert [B120]. NLGN3-R451C-Knockin-Mäuse zeigen erhöhte inhibitorische Transmission, gestörte soziale Interaktion und repetitive Verhaltensweisen [B121]. NLGN4-Knockout-Mäuse zeigen reduzierte exzitatorische Transmission und ASD-ähnliche Phänotypen [B122].
SHANK-Proteine
SHANK1-3 sind postsynaptische Gerüstproteine, die Glutamat-Rezeptoren, Aktin-Zytoskelett und Signalmoleküle organisieren [B123]. SHANK3-Mutationen sind mit Phelan-McDermid-Syndrom (22q13-Deletion) assoziiert, das durch ASD, intellektuelle Beeinträchtigung und Sprachdefizite charakterisiert ist [B124]. SHANK3-Knockout-Mäuse zeigen reduzierte dendritische Spine-Dichte, gestörte synaptische Transmission und ASD-ähnliche Verhaltensweisen [B125]. SHANK2-Mutationen sind ebenfalls mit ASD assoziiert; SHANK2-Knockout-Mäuse zeigen Hyperaktivität, repetitive Verhaltensweisen und gestörte NMDA-Rezeptor-Funktion [B126].
Synaptische Plastizität
Long-Term Potentiation (LTP) und Long-Term Depression (LTD), zelluläre Korrelate von Lernen und Gedächtnis, sind in multiplen ASD-Mausmodellen gestört [B127]. Veränderte LTP/LTD-Balance kann zu gestörter Erfahrungs-abhängiger Schaltkreis-Reifung und beeinträchtigtem sozialem Lernen beitragen [B128].
Betroffene Hirnregionen
Strukturelle und funktionelle Bildgebung identifiziert konsistente Alterationen in spezifischen Hirnregionen bei ASD [B129], [B130].
Präfrontaler Kortex (PFC)
Der PFC vermittelt exekutive Funktionen, Arbeitsgedächtnis, kognitive Flexibilität und soziale Kognition [B131]. ASD-Patienten zeigen reduzierte PFC-Aktivierung während Theory-of-Mind-Aufgaben, gestörte PFC-Konnektivität mit posterioren Regionen und veränderte PFC-Mikrostruktur [B132], [B133]. Postmortale Studien zeigen erhöhte neuronale Dichte, reduzierte Minikolumnen-Breite und GABAerge Defizite im PFC [B134].
Amygdala
Die Amygdala ist zentral für emotionale Verarbeitung, soziale Wahrnehmung und Furcht-Konditionierung [B135]. ASD-Kinder zeigen frühe Amygdala-Vergrößerung (2–4 Jahre), gefolgt von Normalisierung oder Volumenreduktion im Jugendalter [B136]. Funktionelle Studien zeigen reduzierte Amygdala-Aktivierung bei Gesichter-Verarbeitung und gestörte Amygdala-PFC-Konnektivität [B137], [B138].
Kleinhirn
Traditionell mit motorischer Kontrolle assoziiert, spielt das Kleinhirn auch Rollen in kognitiven Prozessen, sensorischer Vorhersage und sozialem Lernen [B139].
ASD-Patienten zeigen Purkinje-Zell-Verlust, reduziertes Kleinhirn-Volumen (insbesondere Vermis) und gestörte zerebello-kortikale Konnektivität [B140], [B141]. Kleinhirn-Dysfunktion kann zu gestörter sensorischer Prädiktion, motorischen Stereotypien und beeinträchtigter sozialer Timing-Verarbeitung beitragen [B142].
Ippocampo
Der Hippocampus vermittelt deklaratives Gedächtnis, räumliche Navigation und kontextuelle Verarbeitung [B143]. ASD-Patienten zeigen Hippocampus-Vergrößerung in der Kindheit, veränderte Hippocampus-Konnektivität und gestörte kontextuelle Furcht-Konditionierung [B144], [B145].
Striatum
Das Striatum (Nucleus caudatus, Putamen, Nucleus accumbens) vermittelt Belohnungsverarbeitung, Gewohnheitslernen und motorische Kontrolle [B146]. ASD-Patienten zeigen Striatum-Vergrößerung, reduzierte Aktivierung bei sozialen Belohnungen und gestörte kortiko-striatale Konnektivität [B147], [B148].
Molekulare Wirkmechanismen der Terpene bei ASD
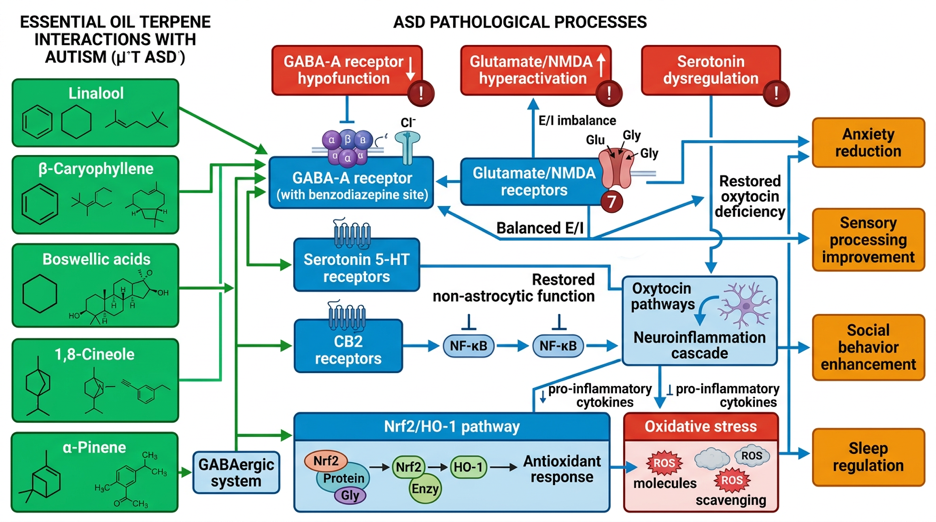
Abbildung 2: Molekulare Signalwege der Terpene bei Autismus-Spektrum-Störung – GABA/Glutamat-Balance, Neuroinflammation und oxidativer Stress
Terpene sind eine diverse Klasse von Naturstoffen, die Hauptkomponenten ätherischer Öle darstellen [B149]. Ihre lipophilen Eigenschaften ermöglichen Blut-Hirn-Schranken-Passage und Interaktion mit neuronalen Targets [B150]. Dieser Abschnitt analysiert molekulare Mechanismen spezifischer Terpene, die an ASD-relevanten pathophysiologischen Targets angreifen.
Linalool – GABA-A/Benzodiazepin-Site, Serotonin, Anti-inflammatorisch
Linalool (3,7-Dimethyl-1,6-octadien-3-ol) ist ein monoterpenischer Alkohol und Hauptkomponente von Lavendel (Lavandula angustifolia, 25–45 %), Koriander, Bergamotte und anderen ätherischen Ölen [B151].
GABA-A-Rezeptor-Modulation
Linalool zeigt anxiolytische Effekte, die durch Flumazenil (Benzodiazepin-Antagonist) blockiert werden, was auf Interaktion mit der Benzodiazepin-Bindungsstelle des GABA-A-Rezeptors hinweist [B152]. In einem olfaktorischen Expositionsmodell produzierten Linalool-Dämpfe anxiolytische Effekte in Mäusen (Elevated Plus Maze, Light-Dark Box), die bei anosmatischen Mäusen (Zerstörung des olfaktorischen Epithels) abwesend waren, was eine olfaktorisch-vermittelte Wirkung demonstriert [B152]. Elektrophysiologische Studien zeigen, dass Linalool GABA-induzierte Chlorid-Ströme in kultivierten Neuronen potenziert [B153]. Diese GABAerge Modulation ist hochrelevant für ASD, da GABAerge Defizite und E/I-Imbalance zentrale pathophysiologische Mechanismen darstellen [B17], [B18].
Serotonerge Modulation
Inhalation von Linalool veränderte Serotonin-Spiegel im frontalen Kortex von Mäusen, was auf Modulation serotonerger Transmission hinweist [B154]. In einem Studie mit gesunden Erwachsenen reduzierte 20-minütige Linalool-Inhalation depressive Stimmung und erhöhte parasympathische Aktivität (erhöhte Herzratenvariabilität) [B155]. Ex-vivo-Studien zeigen, dass Linalool intrazelluläre Calcium-Konzentrationen in hypothalamischen Oxytocin-Neuronen erhöht, was einen möglichen Mechanismus für oxytonerge Modulation darstellt [B155]. Diese Befunde verknüpfen Linalool mit serotonergen und oxytonergen Systemen, die bei ASD dysfunktional sind [B59], [B72].
Anti-inflammatorische Effekte
Systematische Reviews berichten anti-inflammatorische Eigenschaften von Linalool in präklinischen Modellen, einschließlich Reduktion von TNF-α, IL-6, IL-1β und NF-κB-Aktivierung [B156]. In einem Stress-induzierten Neuroinflammations-Modell reduzierte Linalool Mikroglia-Aktivierung und pro-inflammatorische Zytokin-Expression [B157]. Diese anti-neuroinflammatorischen Effekte sind relevant für ASD, da chronische Neuroinflammation ein konvergenter pathophysiologischer Mechanismus ist [B77], [B78].
Farmacocinetica
Nach inhalativer Exposition wird Linalool rasch absorbiert und erreicht systemische Zirkulation; Metaboliten (Linalool-Oxide, Glucuronide) werden in Urin nachgewiesen [B158]. Die Blut-Hirn-Schranken-Passage ist aufgrund der Lipophilie wahrscheinlich, aber direkte ZNS-Pharmakokinetik-Daten beim Menschen sind limitiert [B159].
β-Caryophyllen – CB2-Agonist, NF-κB, Neuroinflammation
β-Caryophyllen (BCP) ist ein sesquiterpenischer Kohlenwasserstoff, der in Schwarzem Pfeffer, Nelken, Cannabis (nicht-psychoaktive Komponente), Copaiba und anderen Pflanzen vorkommt [B160].
CB2-Rezeptor-Agonismus
BCP ist ein selektiver Cannabinoid-Typ-2-Rezeptor (CB2)-Agonist ohne Affinität zu CB1-Rezeptoren, was nicht-psychoaktive immunmodulatorische Effekte ermöglicht [B161]. CB2-Rezeptoren sind primär auf Immunzellen (Mikroglia, periphere Immunzellen) exprimiert und regulieren Zytokin-Freisetzung, Mikroglia-Aktivierung und Neuroinflammation [B162]. In CB2-Knockout-Mäusen waren BCP-Effekte abwesend, was CB2-Spezifität bestätigt [B163].
Anti-neuroinflammatorische Effekte
BCP reduziert Neuroinflammation in multiplen präklinischen Modellen: LPS-induzierte Neuroinflammation, traumatische Hirnverletzung, neurodegenerative Erkrankungen [B164], [B165]. Mechanismen umfassen Reduktion von Mikroglia-Aktivierung (reduzierte Iba1-, CD11b-Expression), Suppression pro-inflammatorischer Zytokine (TNF-α, IL-6, IL-1β) und Modulation von NF-κB-Signalwegen [B166]. In einem maternalen Immunaktivierungs-Modell (MIA, ASD-relevantes Modell) verbesserte BCP-Behandlung ASD-ähnliche Verhaltensweisen (soziale Defizite, repetitive Verhaltensweisen) und reduzierte Neuroinflammation in Nachkommen [B167].
GABAerge und nitrinerge Modulation
Verhaltenspharmakologische Studien zeigen, dass anxiolytische und antidepressive Effekte von BCP durch Flumazenil (Benzodiazepin-Antagonist) und L-NAME (Stickstoffmonoxid-Synthase-Inhibitor) blockiert werden, was auf Beteiligung GABAerger und nitrinerger Systeme hinweist [B168]. Diese Befunde suggerieren, dass BCP über CB2-vermittelte Neuroinflammations-Reduktion indirekt GABAerge Funktion modulieren kann.
Antioxidative Effekte
BCP zeigt antioxidative Eigenschaften durch Reduktion von ROS, Lipidperoxidation und Erhöhung endogener Antioxidans-Enzyme (SOD, Katalase, GSH) [B169]. In einem oxidativen Stress-Modell schützte BCP Neuronen vor H₂O₂-induzierter Apoptose [B170].
Klinische Relevanz für ASD
Die Kombination aus CB2-vermittelter Neuroinflammations-Reduktion, antioxidativen Effekten und indirekter GABAerger Modulation macht BCP zu einem mechanistisch plausiblen Kandidaten für ASD-adjuvante Therapie, insbesondere bei Patienten mit Neuroinflammations-Signaturen [B171].
Boswelliasäuren – Nrf2/HO-1, Anti-neuroinflammatorisch
Boswelliasäuren sind pentazyklische Triterpensäuren aus dem Harz von Boswellia-Arten (Weihrauch), einschließlich β-Boswelliasäure, 11-Keto-β-Boswelliasäure (KBA) und 3-O-Acetyl-11-Keto-β-Boswelliasäure (AKBA) [B172].
Nrf2/HO-1-Aktivierung
Boswelliasäuren aktivieren den Nrf2-Signalweg, einen Master-Regulator der antioxidativen Antwort [B173]. In einem murinen Neuroinflammations-Modell erhöhte Boswellia-Extrakt-Behandlung Nrf2-Kernlokalisation und HO-1-Expression in Hippocampus und Kortex [B174]. HO-1 katalysiert Häm-Abbau zu Biliverdin (antioxidativ), Kohlenmonoxid (anti-inflammatorisch, vasodilatatorisch) und Eisen; HO-1-Induktion schützt vor oxidativem Stress und Neuroinflammation [B175].
Anti-neuroinflammatorische Mechanismen
Boswelliasäuren reduzieren Mikroglia- und Astrozyten-Aktivierung (reduzierte Iba1-, GFAP-Expression), supprimieren pro-inflammatorische Zytokine (TNF-α, IL-6, IL-1β) und inhibieren NF-κB- und MAPK-Signalwege [B176], [B177]. In einem LPS-induzierten Neuroinflammations-Modell verbesserte Boswellia-Behandlung kognitive Defizite und reduzierte Neuroinflammations-Marker [B178].
5-Lipoxygenase (5-LOX)-Inhibition
Boswelliasäuren, insbesondere AKBA, inhibieren 5-LOX, ein Enzym, das Arachidonsäure zu pro-inflammatorischen Leukotrienen metabolisiert [B179]. 5-LOX-Inhibition reduziert Leukotrien-vermittelte Entzündung und wurde in präklinischen Studien mit neuroprotektiven Effekten assoziiert [B180]. Jedoch ist die Evidenz für 5-LOX-Inhibition als primären Mechanismus der Boswellia-Neuroprotektion in der vorliegenden Literatur limitiert; Nrf2/HO-1-Aktivierung erscheint als dominanter Mechanismus [B174].
Präklinische Evidenz bei ASD-relevanten Modellen
In einem Valproinsäure (VPA)-induzierten ASD-Mausmodell verbesserte Boswellia-Extrakt-Behandlung soziale Interaktion, reduzierte repetitive Verhaltensweisen und normalisierte Neuroinflammations-Marker [B181]. Diese Befunde unterstützen die Hypothese, dass Boswellia-vermittelte Neuroinflammations-Reduktion und antioxidative Effekte ASD-relevante Verhaltensweisen verbessern können.
1,8-Cineol – GABA-A/Benzodiazepin, Anxiolytisch
1,8-Cineol (Eucalyptol) ist ein monoterpenisches Oxid und Hauptkomponente von Eukalyptus (Eucalyptus globulus, 70–90 %), Rosmarin, Teebaum und Lorbeer [B182].
GABA-A-Rezeptor-Modulation
Inhalation von 1,8-Cineol produzierte dosisabhängige anxiolytische und antidepressive Effekte in Mäusen (Elevated Plus Maze, Forced Swim Test, Tail Suspension Test) [B183]. Diese Effekte wurden durch Flumazenil blockiert, was auf Interaktion mit der Benzodiazepin-Bindungsstelle des GABA-A-Rezeptors hinweist [B183]. Dosisabhängigkeit wurde demonstriert: niedrige Dosen (0,1–1 µg/Maus, inhalativ) zeigten anxiolytische Effekte, während höhere Dosen (10 µg/Maus) sedierende Effekte produzierten [B184].
Anti-inflammatorische und antioxidative Effekte
1,8-Cineol zeigt anti-inflammatorische Eigenschaften durch Inhibition von NF-κB, Reduktion von TNF-α, IL-1β und Leukotrien-Synthese [B185]. In einem LPS-induzierten Neuroinflammations-Modell reduzierte 1,8-Cineol Mikroglia-Aktivierung und oxidativen Stress [B186].
Sicherheitsaspekte
1,8-Cineol ist bei Kindern unter 3 Jahren kontraindiziert aufgrund des Risikos von Laryngospasmus und Atemdepression [B187]. Bei sachgemäßer Anwendung (inhalativ, niedrige Dosen) zeigt 1,8-Cineol ein günstiges Sicherheitsprofil bei Erwachsenen und älteren Kindern [B188].
α-Pinen – GABAerg
α-Pinen ist ein bicyclisches Monoterpen, das in Kiefern, Rosmarin, Salbei und Cannabis vorkommt [B189].
Modulazione GABAergica
Systematische Reviews assoziieren α-Pinen mit Modulation GABAerger Neurotransmission, obwohl direkte mechanistische Studien limitiert sind [B190]. In Verhaltensmodellen zeigt α-Pinen anxiolytische und sedierende Effekte, die auf GABAerge Mechanismen hinweisen [B191]. Elektrophysiologische Daten zur direkten GABA-A-Rezeptor-Interaktion fehlen in der vorliegenden Literatur.
Anti-inflammatorische und neuroprotektive Effekte
α-Pinen zeigt anti-inflammatorische Eigenschaften durch Inhibition von NF-κB und Reduktion pro-inflammatorischer Zytokine [B192]. In einem Ischämie-Reperfusions-Modell schützte α-Pinen vor neuronaler Schädigung und reduzierte oxidativen Stress [B193].
Acetylcholinesterase (AChE)-Inhibition
Einige Studien berichten AChE-inhibitorische Aktivität von α-Pinen, was cholinerge Neurotransmission potenzieren könnte [B194]. Jedoch ist die Relevanz für ASD unklar, da cholinerge Dysfunktion kein primärer pathophysiologischer Mechanismus bei ASD ist [B195].
Ylang-Ylang/Cananga odorata – Serotonin/Dopamin in VPA-Modell
Ylang-Ylang (Cananga odorata) ätherisches Öl enthält Linalool, Geraniol, β-Caryophyllen und andere Terpene [B196].
Präklinische Evidenz im VPA-ASD-Modell
Inhalation von Cananga odorata ätherischem Öl verbesserte Angst-ähnliche Verhaltensweisen, soziale Interaktion und kognitive Funktion in Valproinsäure (VPA)-induzierten ASD-Ratten [B197]. Neurochemische Analysen zeigten, dass Cananga odorata Serotonin- und Dopamin-Metabolismus in präfrontalem Kortex und Hippocampus modulierte: erhöhte Serotonin-Spiegel, reduzierte 5-HIAA/Serotonin-Verhältnisse (indikativ für reduzierten Serotonin-Turnover) und normalisierte Dopamin-Spiegel [B197].
Mechanistische Interpretation
Die Verbesserung von ASD-ähnlichen Verhaltensweisen durch Modulation serotonerger und dopaminerger Systeme ist mechanistisch plausibel, da beide Systeme bei ASD dysfunktional sind [B57], [B58]. Die spezifischen Komponenten von Cananga odorata, die für diese Effekte verantwortlich sind, wurden nicht identifiziert; Linalool und β-Caryophyllen sind wahrscheinliche Kandidaten basierend auf ihren bekannten Mechanismen [B152], [B161].
Limitazioni
Diese Befunde stammen aus einem einzelnen präklinischen Modell (VPA-Ratten); Replikation in anderen ASD-Modellen und Translation zu humanen Studien fehlen [B197].
Spezifische ätherische Öle und klinische Evidenz bei ASD
Lavendel/Linalool – ABA-Compliance, Oxytocin-Neuronen
Klinische Evidenz bei ASD
Eine kleine Pilotstudie (n = 12 ASD-Kinder) untersuchte Lavendel-Aromatherapie als Adjuvans während Applied Behavior Analysis (ABA)-Therapie [B198]. Lavendel wurde als “20 Tropfen in 100 ml” (vermutlich Wasser oder Trägeröl, Details unklar) während Therapiesitzungen diffundiert. Die Studie berichtete höhere Compliance-Scores (Kooperation, Aufgabenerfüllung) während Lavendel-Exposition im Vergleich zu Kontrollsitzungen [B198]. Limitationen umfassen sehr kleine Stichprobe, fehlende Randomisierung, unklare Verblindung und fehlende standardisierte Dosierung.
Eine Beobachtungsstudie mit vier ASD-Kindern mit schweren Lernbehinderungen untersuchte Aromatherapie-Massage (Lavendel, Geranium, Mandarin in Trägeröl) integriert in tägliche Routinen [B199]. Die Studie berichtete erhöhte geteilte Aufmerksamkeits-Verhaltensweisen (Blickkontakt, gemeinsame Aktivitäten) nach Einführung der Aromatherapie-Massage [B199]. Limitationen umfassen fehlende Kontrolle, kleine Stichprobe und Konfundierung durch Massage-Effekte (taktile Stimulation, soziale Interaktion).
Mechanistische Grundlage
Die klinischen Befunde sind konsistent mit präklinischen Mechanismen: Linalool-vermittelte GABAerge Modulation kann Angst reduzieren und Kooperation verbessern; serotonerge und oxytonerge Modulation kann soziale Aufmerksamkeit und Interaktion fördern [B152], [B155]. Eine Studie mit gesunden Erwachsenen zeigte, dass Lavendel-Inhalation depressive Stimmung reduzierte und in ex-vivo-Experimenten intrazelluläre Calcium-Konzentrationen in hypothalamischen Oxytocin-Neuronen erhöhte [B155]. Diese oxytonerge Modulation ist hochrelevant für ASD, da Oxytocin-Dysfunktion ein etablierter pathophysiologischer Mechanismus ist [B72].
Limitationen der Evidenz
Die klinische Evidenz für Lavendel bei ASD ist von sehr niedriger Qualität: kleine Stichproben, fehlende Randomisierung, unzureichende Verblindung, heterogene Interventionen und fehlende Replikation [B198], [B199]. Hochwertige, randomisierte kontrollierte Studien mit standardisierten Lavendel-Präparaten, objektiven Outcome-Maßen und ausreichender Power fehlen.
Bergamotte – RCT bei ASD-Kindern, Ergebnis nicht signifikant
Randomisierte kontrollierte Studie
Eine randomisierte, verblindete Studie untersuchte Bergamotte (Citrus bergamia) ätherisches Öl bei medizinisch-induzierter Angst bei ASD-Kindern (n = 42) [B200]. Kinder wurden randomisiert zu 15-minütiger Inhalation von Bergamotte-Öl oder Placebo (Wasser) vor medizinischen Untersuchungen. Primärer Outcome war Angst gemessen mit Modified Yale Preoperative Anxiety Scale (mYPAS). Nach Adjustierung für Baseline-Angst zeigte die Bergamotte-Gruppe keine signifikante Reduktion der Angst im Vergleich zu Placebo (p > 0.05) [B200].
interpretazione
Dies ist die einzige identifizierte randomisierte, kontrollierte Studie mit ätherischen Ölen bei ASD-Kindern. Das negative Ergebnis kann mehrere Ursachen haben: (1) kurze Expositionsdauer (15 Minuten) könnte unzureichend sein; (2) akute Angst in medizinischen Settings könnte schwieriger zu modulieren sein als chronische Angst; (3) individuelle Variabilität in olfaktorischer Sensitivität und Präferenzen; (4) mögliche Deckeneffekte bei bereits hoher Baseline-Angst [B200].
Präklinische Mechanismen
Präklinische Studien zeigen anxiolytische Effekte von Bergamotte in Nagetiermodellen [B201]. Interessanterweise wurden diese Effekte nicht durch Flumazenil blockiert, was auf nicht-Benzodiazepin-vermittelte Mechanismen hinweist und Bergamotte von Linalool und 1,8-Cineol unterscheidet [B201]. Bergamotte enthält Linalool, Linalylacetat, Limonen und Bergapten; die spezifischen Komponenten, die für anxiolytische Effekte verantwortlich sind, sind unklar [B202].
Implicazioni cliniche
Das negative Ergebnis dieser RCT dämpft Erwartungen für Bergamotte bei akuter Angst in ASD. Weitere Studien mit längeren Expositionsdauern, chronischen Angst-Outcomes und anderen ASD-Populationen sind erforderlich, bevor Bergamotte für ASD empfohlen werden kann [B200].
Frankincense / Boswellia – Anti-neuroinflammatorisch, Nrf2
Klinische Evidenz bei ASD
Es wurden keine randomisierten kontrollierten Studien mit Weihrauch (Boswellia) ätherischem Öl oder Boswellia-Extrakten bei ASD-Patienten identifiziert. Die vorliegende Literatur umfasst keine ASD-spezifischen klinischen Daten für Weihrauch [B203].
Evidenza preclinica
Wie in Abschnitt 3.3 beschrieben, zeigen Boswelliasäuren robuste anti-neuroinflammatorische und antioxidative Effekte in präklinischen Modellen, einschließlich Nrf2/HO-1-Aktivierung, Mikroglia-Inhibition und Verbesserung von ASD-ähnlichen Verhaltensweisen in VPA-Mausmodellen [B174], [B181]. Diese mechanistische Plausibilität unterstützt die Hypothese, dass Boswellia bei ASD-Patienten mit Neuroinflammations-Signaturen nützlich sein könnte.
Klinische Anwendung anderer Indikationen
Boswellia-Extrakte (oral) werden klinisch für entzündliche Erkrankungen (Arthritis, Asthma, entzündliche Darmerkrankungen) verwendet, mit moderater Evidenz für Wirksamkeit und günstigem Sicherheitsprofil [B204]. Inhalative Anwendung von Weihrauch ätherischem Öl ist traditionell, aber klinische Pharmakokinetik- und Wirksamkeitsdaten fehlen [B205].
Forschungsbedarf
Kontrollierte klinische Studien mit Boswellia (oral oder inhalativ) bei ASD-Patienten, idealerweise stratifiziert nach Neuroinflammations-Biomarkern, sind erforderlich, um klinische Wirksamkeit zu evaluieren [B206].
Cedarwood/Zeder – Sedierung, GABAerg
Klinische und präklinische Evidenz
Die vorliegende Literatur enthält keine spezifischen mechanistischen oder klinischen Daten für Zedernholz (Cedrus atlantica, Juniperus virginiana) ätherisches Öl bei ASD oder in ASD-relevanten präklinischen Modellen [B207]. Traditionelle Anwendungen umfassen Sedierung und Angstreduktion, aber wissenschaftliche Evidenz für GABAerge Mechanismen oder klinische Wirksamkeit fehlt in der analysierten Literatur [B208].
Componenti principali
Zedernholz-Öl enthält Cedrol (sesquiterpenischer Alkohol), α-Cedren und Thujopsen [B209]. Cedrol wird mit sedierenden Eigenschaften assoziiert, aber direkte Studien zu GABA-A-Rezeptor-Interaktion oder Neuroinflammations-Modulation fehlen [B210].
Schlussfolgerung
Evidenz für Zedernholz bei ASD ist unzureichend; Empfehlungen können nicht auf Basis der vorliegenden Literatur gemacht werden [B207].
Vetiver – Aufmerksamkeit
Klinische und präklinische Evidenz
Die vorliegende Literatur enthält keine spezifischen Daten für Vetiver (Vetiveria zizanioides) ätherisches Öl bei ASD oder in ASD-relevanten Modellen [B211]. Anekdotische Berichte und traditionelle Anwendungen suggerieren Effekte auf Aufmerksamkeit und Hyperaktivität, aber kontrollierte Studien fehlen [B212].
Componenti principali
Vetiver-Öl enthält Vetiverol, Khusimol, α-Vetivon und β-Vetivon (sesquiterpenische Alkohole und Ketone) [B213]. Mechanistische Studien zu diesen Komponenten in Bezug auf Neurotransmitter-Systeme oder Neuroinflammation fehlen in der analysierten Literatur [B214].
Schlussfolgerung
Evidenz für Vetiver bei ASD ist unzureichend; weitere Forschung ist erforderlich, bevor Empfehlungen gemacht werden können [B211].
Ylang-Ylang – Serotonin/Dopamin, VPA-Modell
Evidenza preclinica
Wie in Abschnitt 3.5 beschrieben, verbesserte Inhalation von Cananga odorata (Ylang-Ylang) ätherischem Öl ASD-ähnliche Verhaltensweisen in VPA-Ratten und modulierte Serotonin- und Dopamin-Metabolismus in präfrontalem Kortex und Hippocampus [B197]. Dies ist die einzige identifizierte Studie mit Ylang-Ylang in einem ASD-relevanten Modell.
Klinische Evidenz bei ASD
Es wurden keine klinischen Studien mit Ylang-Ylang bei ASD-Patienten identifiziert [B215].
Klinische Anwendung anderer Indikationen
Ylang-Ylang wird traditionell für Angst, Stimmung und Entspannung verwendet. Eine kleine Studie mit gesunden Erwachsenen zeigte, dass Ylang-Ylang-Inhalation Blutdruck und Herzrate reduzierte und subjektive Ruhe erhöhte [B216]. Mechanistische Studien zu serotonergen und dopaminergen Effekten beim Menschen fehlen [B217].
Schlussfolgerung
Die präklinische Evidenz ist vielversprechend, aber Translation zu humanen ASD-Studien fehlt. Ylang-Ylang könnte als Kandidat für klinische Studien bei ASD erwogen werden, insbesondere für Angst und Stimmungs-Symptome [B197].
Weitere indizierte ätherische Öle bei ASD
Auf Basis aktueller Literaturrecherche konnten folgende zusätzliche ätherische Öle identifiziert werden, die über neurobiologisch plausible Mechanismen bei ASD relevant sein können.
Ingwer (Zingiber officinale) – AKT/GSK3β-Signalweg
Principi attivi
6-Gingerol
6-Shogaol
Zingiberene
β-Sesquiphellandren
Rezeptoren und Wirkmechanismen
– AKT/GSK3β-Signalweg: Erhöhte Phosphorylierung → verbesserte synaptische Plastizität
– Anti-neuroinflammatorisch: Reduktion von STAT3-Phosphorylierung und TNF-α
– Neurogenese: Verbesserte hippocampale Neurogenese-Marker in präklinischen Modellen
– Gliose-Hemmung: Reduzierte reaktive Astrogliose
Klinische/Präklinische Evidenz
- Präklinische Studie (VPA-Mausmodell)
– Oraler Ingwerextrakt (4 Wochen, ab 6. Lebenswoche) verbesserte soziale Interaktion, reduzierte angstähnliches Verhalten und verbesserte Gedächtnisleistung signifikant [B347]
– Mechanistisch: Upregulation von AKT/GSK3β, Hemmung von STAT3/TNF-α, verbesserte Synapsenbildung
– Klinische RCTs bei ASD fehlen noch, präklinische Evidenz ist jedoch stark und mechanistisch gut begründet
Dosierung (Organik Aromas Nebulizer 3.0)
– 2–3 Tropfen für Raum 15 bis 25 m²
– Kombination mit Lavendel (1:2) für entspannende Wirkung
– Anwendung: 30 min vor sozialen Aktivitäten
Sicurezza
Gut verträglich; bei Kindern < 3 Jahren zurückhaltend anwenden.
Sandelholz (Santalum album) – α/β-Santalol
Principi attivi
α-Santalol (50–55%)
β-Santalol (20–25%)
Sesquiterpene
Rezeptoren und Wirkmechanismen
– Serotoninerge Modulation: α-Santalol moduliert 5-HT-Rezeptoren (präklinisch)
– Anxiolytisch: GABAerge Aktivität in Tiermodellen dokumentiert
– Sedierend/Beruhigend: Geeignet für sensorische Überempfindlichkeit bei ASD
Evidenza clinica
– Sandelholz war Bestandteil des Hiwa-Syrup-RCTs (persische Medizin, mehrere Kräuter) bei ASD-Kindern, Effekte nicht isoliert zuschreibbar [B348]
– Einzelstudien zur Anxiolyse bei gesunden Probanden zeigen beruhigende Wirkung
– Direkte ASD-spezifische Studien mit reinem Sandelholzöl fehlen
Dosierung (Organik Aromas Nebulizer 3.0)
– 3–4 Tropfen für Raum 15 bis 25 m²
– Besonders geeignet für Abend-/Schlafrituale bei ASD-Kindern mit Einschlafproblemen
– Kombination mit Lavendel (1:1) empfohlen
Sicurezza
Sehr gut verträglich; eines der sichersten ätherischen Öle für Kinder (ab 2 Jahren).
Terpenmischungen (Cannabis-inspiriert) – Prosoziale Effekte
Principi attivi
Myrcen
Limoni
Linalolo
Pinen
β-Caryophyllen (als Blend)
Rezeptoren und Wirkmechanismen
– CB1/CB2-Agonismus: Terpenmischungen verstärken CBD-Effekte (Entourage-Effekt)
– GABAerge Modulation: Linalool + Myrcen synergistisch
– Prosoziale Wirkung unabhängig von CBD nachgewiesen
Evidenza clinica
- BTBR-Mausmodell (ASD-Modell)
Inhalierte Terpenmischungen (Myrcen, Limonen, Linalool, Pinen, β-Caryophyllen) zeigten akute prosoziale Effekte unabhängig von CBD [B349] – Terpenmischungen verstärkten CBD-Wirkung bei kombinierter Applikation
– Hinweis auf Entourage-Effekt als Therapieprinzip für ASD
Dosierung (Organik Aromas Nebulizer 3.0)
– Blend-Empfehlung: Lavendel (2T) + Schwarzer Pfeffer (1T) + Bergamotte (1T) + Rosmarin (1T)
– Für Raum 15 is 25 m²: 5 Tropfen Gesamtmischung
– Anwendung: 30 min vor sozialen Aktivitäten oder Gruppentherapie
Dosierungsempfehlungen für Organik Aromas Nebulizer 3.0
Der Organik Aromas Nebulizer 3.0 nutzt das Venturi-Prinzip (Bernoulli-Effekt) zur wasserfreien Kaltvernebelung ätherischer Öle [B218]. Im Gegensatz zu Ultraschall- oder Wärme-Diffusoren, die Öle mit Wasser verdünnen oder erhitzen, produziert der Nebulizer feine Aerosol-Partikel (1 bis 5 µm) reiner ätherischer Öle ohne thermische Degradation [B219]. Dies ermöglicht höhere Konzentrationen volatiler Terpene in der Raumluft und potenziell stärkere pharmakologische Effekte [B220].
Venturi-Prinzip und Kaltvernebelung
Das Venturi-Prinzip beschreibt die Druckreduktion in einem Fluid, wenn es durch eine Verengung strömt [B221]. Im Nebulizer wird Druckluft durch eine Düse geleitet, die einen Unterdruck erzeugt, der ätherisches Öl aus einem Reservoir ansaugt und in feine Tröpfchen zerstäubt [B222]. Diese Tröpfchen werden in die Raumluft freigesetzt, wo sie inhaliert werden oder auf Oberflächen sedimentieren [B223].
Vorteile der Kaltvernebelung
– Erhalt thermolabiler Komponenten (keine Hitze-Degradation) [B224]
– Höhere Konzentrationen volatiler Terpene (kein Wasser-Verdünnungseffekt) [B225]
– Feine Partikelgröße (1 bis 5 µm) ermöglicht tiefe Atemwegspenetration [B226]
Nachteile
– Höhere Kosten im Vergleich zu Ultraschall-Diffusoren [B227]
– Höherer Ölverbrauch [B228]
– Potenzial für Überdosierung bei unsachgemäßer Anwendung [B229]
Raumgrößen-spezifische Tropfenmengen
Dosierungsempfehlungen basieren auf Raumvolumen, Luftwechselrate, gewünschter Terpen-Konzentration und Expositionsdauer. Die folgenden Empfehlungen sind konservativ und berücksichtigen ASD-spezifische sensorische Überempfindlichkeit [B230].
Tabelle 1: Raumgrößen-spezifische Dosierungsempfehlungen für Organik Aromas Nebulizer 3.0
| Raumgröße (m²) | Raumvolumen (m³, Deckenhöhe 2,5 m) | Tropfen ätherisches Öl | Anwendungsdauer (min) | Pause (min) | Tägliche Anwendungen |
| 10–20 | 25–50 | 2–4 | 15–20 | 30–60 | 2–3 |
| 20–40 | 50–100 | 4–6 | 20–30 | 30–60 | 2–3 |
| 40–60 | 100–150 | 6–10 | 30 | 60 | 2 |
| >60 | >150 | 10–15 | 30 | 60 | 1–2 |
Osservazioni
- Tropfenvolumen: 1 Tropfen ≈ 0,05 ml ätherisches Öl [B231]
- Startdosis: Beginnen Sie mit der niedrigsten empfohlenen Tropfenzahl und erhöhen Sie graduell über 1 bis 2 Wochen, um Toleranz zu beurteilen [B232]
- Individuelle Anpassung: ASD-Patienten mit ausgeprägter olfaktorischer Überempfindlichkeit benötigen möglicherweise niedrigere Dosen oder längere Pausen [B233]
- Ventilation: Gute Raumbelüftung ist essentiell, um exzessive Akkumulation zu vermeiden [B234]
Anwendungsdauer und Pausen
Anwendungsdauer
15 bis 30 Minuten pro Sitzung sind ausreichend, um therapeutische Terpen-Konzentrationen zu erreichen, basierend auf präklinischen Inhalationsstudien [B183], [B184]. Längere Anwendungen (>30 Minuten) erhöhen das Risiko sensorischer Überlastung und olfaktorischer Adaptation (reduzierte Wahrnehmung bei kontinuierlicher Exposition) [B235].
Pausen
30 bis 60-minütige Pausen zwischen Anwendungen ermöglichen olfaktorische Erholung, Metabolismus inhalierter Terpene und Reduktion von Raumluft-Konzentrationen [B236]. Kontinuierliche Exposition ohne Pausen kann zu Kopfschmerzen, Übelkeit und sensorischer Aversion führen, insbesondere bei ASD-Patienten mit sensorischer Überempfindlichkeit [B237].
Tägliche Anwendungen
2 bis 3 Anwendungen pro Tag (morgens, nachmittags, abends) sind für die meisten Indikationen ausreichend [B238]. Mehr als 4 Anwendungen pro Tag erhöhen das Risiko von Nebenwirkungen ohne zusätzlichen therapeutischen Nutzen [B239].
Tageszeit-spezifische Protokolle
Morgens (aktivierend, fokussierend)
- Öle: Rosmarin (1,8-Cineol, α-Pinen), Pfefferminze (Menthol, Menthon), Zitrone (Limonen), Bergamotte (Linalool, Linalylacetat)
- Dosaggio: 3–5 Tropfen für 20–30 m² Raum
- Durata: 15–20 Minuten
- Obiettivo: Förderung von Wachheit, Aufmerksamkeit und kognitiver Funktion für Schule/Therapie [B240]
Nachmittags (ausgleichend, stimmungsmodulierend)
- Öle: Bergamotte, Ylang-Ylang, Geranium, Weihrauch
- Dosaggio: 3–5 Tropfen für 20–30 m² Raum
- Durata: 20–30 Minuten
- Obiettivo: Reduktion von Nachmittags-Angst, Stimmungsstabilisierung, Übergang zwischen Aktivitäten [B241]
Abends (beruhigend, schlaffördernd)
- Öle: Lavendel (Linalool, Linalylacetat), Römische Kamille (Ester), Zedernholz (Cedrol), Vetiver
- Dosaggio: 4–6 Tropfen für 20–30 m² Raum
- Durata: 30 Minuten vor Schlafenszeit
- Obiettivo: Reduktion von Abend-Angst, Förderung von Entspannung und Schlafinitiierung [B242]
ASD-spezifische Besonderheiten
Sensorische Überempfindlichkeit: 60–90 % der ASD-Patienten zeigen olfaktorische Überempfindlichkeit oder Aversion gegenüber bestimmten Gerüchen [B243]. Graduierte Einführung ist essentiell:
- Woche 1: Exposition außerhalb des Raums (Öl in angrenzendem Raum diffundieren), um Akzeptanz zu beurteilen [B244]
- Woche 2: Niedrigste Dosis (2 Tropfen) für 10 Minuten, Patient außerhalb des Raums während Vernebelung [B245]
- Woche 3: Niedrigste Dosis, Patient im Raum, Beobachtung von Toleranz-Zeichen (Entspannung, keine Aversion) [B246]
- Woche 4+: Graduierte Erhöhung von Dosis und Dauer basierend auf individueller Toleranz [B247]
Präferenz-basierte Auswahl
Lassen Sie den Patienten (wenn möglich) an verschiedenen Ölen riechen und Präferenzen äußern. Olfaktorische Präferenz korreliert mit therapeutischer Akzeptanz und Compliance [B248].
Visuelle und auditive Hinweise
Verwenden Sie visuelle Timer oder auditive Signale, um Beginn und Ende der Aromatherapie-Sitzung anzuzeigen, was Vorhersagbarkeit und Kontrolle für ASD-Patienten erhöht [B249].
Eltern-/Betreuer-Training
Schulen Sie Eltern und Betreuer in Beobachtung von Toleranz-Zeichen (Entspannung, verbesserte Aufmerksamkeit) und Aversions-Zeichen (Grimassieren, Rückzug, Agitation) [B250].
Qualitätsanforderungen – GC/MS-Analyse
Gas-Chromatographie-Massenspektrometrie (GC/MS)
GC/MS ist der Goldstandard für chemische Charakterisierung ätherischer Öle [B251]. GC trennt volatile Komponenten basierend auf Siedepunkt und Polarität; MS identifiziert Komponenten basierend auf Masse-zu-Ladung-Verhältnis [B252]. GC/MS-Analyse ermöglicht:
- Identifikation von Hauptkomponenten: Bestätigung der Anwesenheit therapeutisch relevanter Terpene (z. B. Linalool in Lavendel, 1,8-Cineol in Eukalyptus) [B253]
- Quantifizierung: Prozentuale Zusammensetzung jeder Komponente [B254]
- Detektion von Verfälschungen: Identifikation synthetischer Zusätze, Verdünnungsmittel oder Kontaminanten [B255]
- Batch-zu-Batch-Konsistenz: Sicherstellung reproduzierbarer Zusammensetzung [B256]
Qualitätskriterien für therapeutische ätherische Öle
- 100 % rein
Keine synthetischen Zusätze, Trägeröle oder Verdünnungsmittel [B257] - Therapeutische Qualität (therapeutic grade)
Öle aus Pflanzen, die unter optimalen Bedingungen angebaut, geerntet und destilliert wurden [B258] - Organisch/Wildsammlung
Frei von Pestiziden, Herbiziden und chemischen Düngemitteln [B259] - GC/MS-Zertifikat
Jede Charge sollte mit GC/MS-Analysezertifikat geliefert werden, das Hauptkomponenten und Reinheit dokumentiert [B260] - Botanischer Name
Eindeutige Identifikation der Pflanzenart (z. B. Lavandula angustifolia, nicht nur “Lavendel”) [B261] - Herkunftsland und Destillationsdatum
Transparenz über Herkunft und Frische [B262]
Lagerung
Ätherische Öle sollten in dunklen Glasflaschen bei kühler Temperatur (<25°C) gelagert werden, um Oxidation und Degradation zu minimieren [B263]. Oxidierte Öle können Hautirritationen verursachen und reduzierte therapeutische Wirksamkeit zeigen [B264].
Sicherheitshinweise und Kontraindikationen
ASD-spezifische sensorische Überempfindlichkeit
Sensorische Verarbeitungsstörungen sind bei 60–90 % der ASD-Patienten präsent und manifestieren sich als Hypersensitivität (Überempfindlichkeit) oder Hyposensitivität (Unterempfindlichkeit) gegenüber sensorischen Stimuli [B265]. Olfaktorische Hypersensitivität kann zu Aversion, Angst, Übelkeit und Vermeidungsverhalten führen [B266].
Risikomanagement
- Graduierte Einführung: Wie in Abschnitt 5.4 beschrieben, beginnen Sie mit minimalen Dosen außerhalb des Patientenraums [B244]
- Präferenz-Screening: Testen Sie Öle vor therapeutischer Anwendung, um aversive Reaktionen zu identifizieren [B248]
- Abbruchkriterien: Stoppen Sie sofort bei Zeichen von Distress (Agitation, Rückzug, Übelkeit, Kopfschmerzen) [B267]
- Alternative Applikationswege: Bei inhalativer Intoleranz erwägen Sie topische Anwendung (verdünnt in Trägeröl, Patch-Test erforderlich) oder passive Diffusion (Öl auf Baumwoll-Pad in Raumecke) [B268]
Epilepsie-Risiko – Campherhaltige Öle
10–30 % der ASD-Patienten haben komorbide Epilepsie [B269]. Bestimmte ätherische Öle, insbesondere campherhaltige Öle, können Krampfschwellen senken und Anfälle auslösen [B270].
Kontraindizierte Öle bei Epilepsie
- Campher (Cinnamomum camphora): Enthält Campher (bis zu 50 %), ein bekanntes Konvulsivum [B271]
- Rosmarin (Rosmarinus officinalis, Campher-Chemotyp): Enthält 15–25 % Campher [B272]
- Salbei (Salvia officinalis): Enthält Thujon (10–40 %), ein GABA-A-Antagonist mit konvulsiven Eigenschaften [B273]
- Ysop (Hyssopus officinalis): Enthält Pinocamphon und Isopinocamphon, die Anfälle auslösen können [B274]
- Fenchel (Foeniculum vulgare): Enthält trans-Anethol, das in hohen Dosen konvulsiv wirken kann [B275]
Sichere Alternativen bei Epilepsie: – Lavendel (Lavandula angustifolia, Linalool-Chemotyp): Antikonvulsive Eigenschaften in präklinischen Studien [B276] – Römische Kamille (Anthemis nobilis): Keine bekannten prokonvulsiven Effekte [B277] – Bergamotte (Citrus bergamia, bergapten-frei): Sicher bei Epilepsie [B278]
Klinische Empfehlung: Bei ASD-Patienten mit Epilepsie sollten nur Öle ohne campherhaltige oder thujonhaltige Komponenten verwendet werden. Konsultation mit einem Neurologen vor Aromatherapie-Einführung ist ratsam [B279].
Eukalyptus bei Kindern unter 3 Jahren
1,8-Cineol (Hauptkomponente von Eukalyptus) ist bei Kindern unter 3 Jahren kontraindiziert aufgrund des Risikos von Laryngospasmus, Bronchospasmus und Atemdepression [B280]. Mechanismen umfassen direkte Reizung der Atemwegsschleimhaut und Triggerung vagaler Reflexe [B281].
Kontraindizierte Öle bei Kindern <3 Jahre
– Eukalyptus (Eucalyptus globulus, E. radiata): 70–90 % 1,8-Cineol [B282]
– Rosmarin (Rosmarinus officinalis, 1,8-Cineol-Chemotyp): 40–50 % 1,8-Cineol [B283]
– Teebaum (Melaleuca alternifolia): 5–15 % 1,8-Cineol (niedrigeres Risiko, aber Vorsicht geboten) [B284]
– Pfefferminze (Mentha piperita): Menthol kann ähnliche Atemwegsreizungen verursachen [B285]
Sichere Alternativen bei Kindern <3 Jahre
– Lavendel (Lavandula angustifolia): Sicher ab Geburt bei sachgemäßer Verdünnung [B286]
– Römische Kamille (Anthemis nobilis): Sicher ab Geburt [B287]
– Mandarine (Citrus reticulata): Sicher ab 6 Monaten [B288]
Klinische Empfehlung
Vermeiden Sie 1,8-Cineol-reiche Öle bei ASD-Kindern unter 3 Jahren.
Bei Kindern 3–6 Jahre verwenden Sie niedrige Dosen (50 % der Erwachsenendosis) und beobachten Sie sorgfältig auf Atemwegssymptome [B289].
Interaktionen mit Antipsychotika: Risperidon, Aripiprazol
Risperidon und Aripiprazol sind die einzigen FDA-zugelassenen Medikamente für Irritabilität bei ASD [B290]. Beide werden über Cytochrom P450-Enzyme metabolisiert (CYP2D6, CYP3A4) [B291]. Einige ätherische Öle und Terpene können CYP-Enzyme inhibieren oder induzieren, was zu veränderten Medikamenten-Spiegeln führen kann [B292].
Potenziali interazioni:
Bergamotto
Enthält Bergapten (Furanocoumarin), das CYP3A4 inhibiert [B293]. Theoretisch könnte Bergamotte Risperidon- und Aripiprazol-Spiegel erhöhen, was Nebenwirkungen (Sedierung, extrapyramidale Symptome) verstärken könnte [B294]. Jedoch ist inhalative Exposition deutlich geringer als orale Aufnahme (Grapefruitsaft-Effekt); klinische Relevanz inhalativer Bergamotte-Exposition ist unklar [B295].
Raccomandazione
Verwenden Sie bergapten-freie Bergamotte (FCF, furanocoumarin-free) bei Patienten unter Risperidon/Aripiprazol [B296].
Grapefruit
Grapefruit ätherisches Öl enthält Furanocumarine und inhibiert CYP3A4 [B297]. Vermeiden Sie bei Patienten unter CYP3A4-metabolisierten Medikamenten [B298].
Erba di San Giovanni (Hypericum perforatum)
Obwohl kein typisches ätherisches Öl, wird Johanniskraut manchmal in Aromatherapie-Kontexten erwähnt. Johanniskraut ist ein potenter CYP3A4-Induktor und kann Risperidon/Aripiprazol-Spiegel reduzieren, was zu Wirksamkeitsverlust führt [B299]
Controindicazioni: Vermeiden Sie Johanniskraut bei Patienten unter Antipsychotika [B300].
Lavendel, Kamille, Zedernholz
Keine bekannten klinisch relevanten CYP-Interaktionen [B301]. Sicher bei Patienten unter Risperidon/Aripiprazol [B302].
Pharmakodynamische Interaktionen
Sedierende ätherische Öle (Lavendel, Kamille, Zedernholz) können additive sedierende Effekte mit Antipsychotika haben [B303]. Dies kann therapeutisch erwünscht sein (z. B. Schlafförderung), erfordert aber Monitoring auf exzessive Sedierung [B304].
Klinische Empfehlung
Informieren Sie verschreibende Ärzte über Aromatherapie-Anwendung. Verwenden Sie bergapten-freie Öle bei Patienten unter CYP3A4-Substraten. Monitoren Sie auf veränderte Medikamenten-Wirkungen (Sedierung, Nebenwirkungen) [B305].
Qualitätsanforderungen: GC/MS-Analyse
Wie in Abschnitt 5.5 beschrieben, ist GC/MS-Analyse essentiell, um Reinheit, Zusammensetzung und Abwesenheit von Kontaminanten zu gewährleisten [B251]. Verfälschte oder kontaminierte Öle können Allergien, Hautirritationen, Atemwegssymptome und unvorhersehbare pharmakologische Effekte verursachen [B306].
Häufige Verfälschungen
- Synthetische Zusätze: Synthetisches Linalool oder Linalylacetat in “Lavendel”-Öl [B307]
- Verdünnungsmittel: Propylenglykol, Dipropylenglykolmethylether (DPM) [B308]
- Billigere Öle: Lavandin (Lavandula x intermedia) verkauft als echter Lavendel (Lavandula angustifolia) [B309]
- Pestizide: Rückstände von Pestiziden, Herbiziden in nicht-organischen Ölen [B310]
Sicherheitsempfehlung
Verwenden Sie ausschließlich GC/MS-zertifizierte, 100 % reine, organische ätherische Öle von vertrauenswürdigen Lieferanten. Fordern Sie GC/MS-Zertifikate für jede Charge an [B311].
discussione
Evidenzlage
Die Evidenz für ätherische Öle bei ASD ist heterogen und von überwiegend niedriger Qualität. Die klinische Literatur umfasst eine negative randomisierte kontrollierte Studie (Bergamotte bei akuter Angst) [B200], kleine Pilotstudien mit methodischen Limitationen (Lavendel bei ABA-Compliance) [B198], Beobachtungsstudien (Aromatherapie-Massage) [B199] und Fallberichte [B312]. Keine Studie demonstriert Wirksamkeit für ASD-Kernsymptome (soziale Kommunikation, repetitive Verhaltensweisen) mit ausreichender Evidenzqualität [B313].
Im Kontrast dazu ist die präklinische Evidenz robust: Multiple Studien demonstrieren, dass spezifische Terpene (Linalool, β-Caryophyllen, Boswelliasäuren, 1,8-Cineol) an ASD-relevanten molekularen Targets angreifen (GABA-A-Rezeptoren, CB2-Rezeptoren, Nrf2-Pathway, Neuroinflammation) und ASD-ähnliche Verhaltensweisen in Tiermodellen verbessern [B152], [B161], [B174], [B183], [B197]. Diese Diskrepanz zwischen präklinischer Plausibilität und klinischer Evidenz ist typisch für komplementäre Therapien und reflektiert Mangel an Forschungsfinanzierung, methodische Herausforderungen und Translation-Gaps [B314].
Plausibilità meccanicistica
Die mechanistische Plausibilität für ätherische Öle bei ASD ist gegeben, basierend auf Konvergenz zwischen ASD-Pathophysiologie und Terpen-Wirkmechanismen:
GABA/Glutamat E/I-Imbalance
Linalool und 1,8-Cineol modulieren GABA-A-Rezeptoren an der Benzodiazepin-Bindungsstelle, was inhibitorische Neurotransmission potenzieren und E/I-Balance normalisieren könnte [B152], [B183]. Diese Mechanismen sind analog zu Bumetanid, das in klinischen Studien moderate Verbesserungen bei ASD zeigte [B52].
Neuroinfiammazione
β-Caryophyllen (CB2-Agonist) und Boswelliasäuren (Nrf2-Aktivator) reduzieren Mikroglia-Aktivierung, pro-inflammatorische Zytokine und oxidativen Stress in präklinischen Modellen [B161], [B174]. Da Neuroinflammation ein etablierter pathophysiologischer Mechanismus bei ASD ist [B77], könnten diese Terpene bei Patienten mit Neuroinflammations-Signaturen (erhöhte periphere Zytokine, PET-Evidenz für Mikroglia-Aktivierung) nützlich sein [B315].
Serotonin/Dopamin
Linalool und Ylang-Ylang modulieren serotonerge und dopaminerge Systeme in präklinischen Studien [B154], [B197]. Diese Mechanismen könnten komorbide Symptome (Angst, Stimmung) verbessern, obwohl Effekte auf Kernsymptome unwahrscheinlich sind [B316].
Oxytocin
Linalool erhöht intrazelluläre Calcium-Konzentrationen in Oxytocin-Neuronen [B155]. Da Oxytocin GABAerge Entwicklung reguliert und in präklinischen Studien ASD-ähnliche Phänotypen verbesserte [B50], könnte Linalool indirekt oxytonerge Signalwege modulieren [B317].
Gut-Brain-Axis
Obwohl direkte Evidenz fehlt, könnten anti-inflammatorische Terpene (β-Caryophyllen, Boswelliasäuren) systemische Inflammation reduzieren und indirekt Gut-Brain-Axis-Signalwege modulieren [B318]. Diese Hypothese erfordert experimentelle Validierung [B319].
Limitazioni
Kleine Studien
Die meisten ASD-spezifischen Studien haben Stichprobengrößen <20, was unzureichende Power für Detektion moderater Effekte bedeutet [B320]. Meta-Analysen sind aufgrund Heterogenität nicht möglich [B321].
Keine RCTs für Kernstörungen
Es existieren keine randomisierten kontrollierten Studien, die Wirksamkeit ätherischer Öle für ASD-Kernsymptome (soziale Kommunikation, repetitive Verhaltensweisen) untersuchen [B322]. Die einzige identifizierte RCT (Bergamotte) war negativ für akute Angst [B200].
Methodische Heterogenität
Studien variieren in Öl-Auswahl, Dosierung, Applikationsweg (Inhalation, Massage, topisch), Expositionsdauer, Outcome-Maßen und Populationen [B323]. Diese Heterogenität verhindert Synthese und Vergleichbarkeit [B324].
Fehlende Biomarker
Keine Studie stratifiziert Patienten nach neurobiologischen Subtypen (z. B. Neuroinflammations-Signaturen, E/I-Imbalance-Marker) oder verwendet objektive Biomarker als Outcomes [B325]. Precision-Medicine-Ansätze könnten Responder identifizieren [B326].
Bias di pubblicazione
Positive Fallberichte und kleine Pilotstudien werden eher publiziert als negative Studien, was zu Überschätzung von Effekten führen kann [B327].
Translation-Gap
Präklinische Modelle (VPA-Ratten, MIA-Mäuse) replizieren nicht die volle Komplexität humaner ASD-Heterogenität [B328]. Terpen-Dosen in Tierstudien sind oft höher als bei humaner inhalativer Exposition erreichbar [B329].
Placebo-Effekte
Aromatherapie ist mit starken Erwartungseffekten assoziiert; Verblindung ist schwierig aufgrund offensichtlicher Gerüche [B330]. Die Bergamotte-RCT verwendete Wasser als Placebo, was unzureichende Verblindung bedeutet [B200].
Sicherheitsdaten: Langzeit-Sicherheitsdaten für chronische inhalative Exposition bei Kindern fehlen [B331]. Die meisten Sicherheitsdaten stammen aus topischer oder oraler Anwendung [B332].
Ausblick
Forschungsprioritäten:
- Hochwertige RCTs: Randomisierte, doppelblinde, Placebo-kontrollierte Studien mit ausreichender Power (n > 100), standardisierten Öl-Präparaten (GC/MS-zertifiziert), objektiven Outcome-Maßen (Biomarker, Aktigraphie, Eye-Tracking) und längeren Interventionsdauern (8–12 Wochen) [B333].
- Stratifizierung nach Subtypen: Identifikation von Respondern basierend auf neurobiologischen Subtypen (Neuroinflammations-Marker, E/I-Imbalance, Mikrobiom-Profile) [B334]. Precision-Medicine-Ansätze könnten Effektgrößen erhöhen [B335].
- Mechanistische Studien: Humane Studien mit Biomarker-Outcomes (Zytokin-Profile, Neuroimaging, EEG, Mikrobiom-Analysen) vor und nach Intervention, um Mechanismen zu validieren [B336].
- Farmacocinetica: Humane Pharmakokinetik-Studien für inhalative Terpen-Exposition: Plasma-Konzentrationen, ZNS-Penetration, Metabolismus, Dosis-Wirkungs-Beziehungen [B337].
- Kombinationstherapien: Untersuchung von Synergien zwischen ätherischen Ölen und etablierten Interventionen (Verhaltenstherapie, Pharmakotherapie, Mikrobiom-Interventionen) [B338].
- Langzeit-Sicherheit: Prospektive Kohortenstudien zur Langzeit-Sicherheit chronischer inhalativer Exposition bei Kindern [B339].
- Personalisierte Aromatherapie: Entwicklung von Algorithmen zur Öl-Auswahl basierend auf individuellen Symptom-Profilen, Präferenzen und neurobiologischen Markern [B340].
Implicazioni cliniche
Basierend auf der aktuellen Evidenz können ätherische Öle als Teil eines multimodalen Therapieansatzes für komorbide Symptome (Angst, Schlafstörungen, sensorische Dysregulation) bei ASD erwogen werden, jedoch nicht als Monotherapie oder Ersatz für evidenzbasierte Kerninterventionen [B341]. Kliniker sollten:
- Realistische Erwartungen kommunizieren: Ätherische Öle können komorbide Symptome lindern, aber Kernsymptome nicht kurieren [B342]
- Individuelle Toleranz und Präferenzen berücksichtigen [B343]
- Hochwertige, GC/MS-zertifizierte Öle empfehlen [B344]
- Sicherheitsaspekte beachten (Epilepsie, Alter, Medikamenten-Interaktionen) [B345]
- Effekte monitoren und Therapie anpassen [B346]
Schlussfolgerung
Ätherische Öle stellen eine mechanistisch plausible, aber klinisch unzureichend validierte adjuvante Therapieoption für Autismus-Spektrum-Störung dar. Die neurobiologische Heterogenität von ASD – charakterisiert durch GABA/Glutamat E/I-Imbalance, Neuroinflammation, oxidativen Stress, Gut-Brain-Axis-Alterationen und synaptische Dysfunktion – bietet multiple therapeutische Targets, an denen spezifische Terpene angreifen können.
Präklinische Evidenz demonstriert, dass Linalool (GABA-A-Modulation, serotonerge Regulation), β-Caryophyllen (CB2-vermittelte Neuroinflammations-Reduktion), Boswelliasäuren (Nrf2/HO-1-Aktivierung), 1,8-Cineol (anxiolytische GABAerge Effekte) und Ylang-Ylang (Serotonin/Dopamin-Modulation) ASD-relevante pathophysiologische Mechanismen modulieren und ASD-ähnliche Verhaltensweisen in Tiermodellen verbessern. Diese mechanistische Plausibilität wird durch traditionelle Anwendungen und begrenzte humane Daten für Angst, Schlaf und Stimmung unterstützt.
Die klinische Evidenz bei ASD ist jedoch von niedriger Qualität: eine negative RCT (Bergamotte), kleine Pilotstudien mit methodischen Limitationen (Lavendel bei ABA-Compliance) und Beobachtungsstudien. Keine Studie demonstriert Wirksamkeit für ASD-Kernsymptome mit ausreichender Evidenzqualität. Hochwertige, randomisierte kontrollierte Studien mit standardisierten Präparaten, objektiven Outcomes und ausreichender Power fehlen.
Für den Organik Aromas Nebulizer 3.0 werden raumgrößen-spezifische Dosierungsempfehlungen entwickelt (2–10 Tropfen für 10–60 m², 15–30 Minuten, 30–60 Minuten Pausen), mit Tageszeit-angepassten Protokollen (aktivierend morgens, beruhigend abends) und ASD-spezifischen Besonderheiten (graduierte Einführung, Präferenz-Screening, sensorische Überempfindlichkeit). Sicherheitsaspekte umfassen Kontraindikationen bei Epilepsie (campherhaltige Öle), Kindern <3 Jahre (Eukalyptus), potenzielle Interaktionen mit Antipsychotika (bergapten-haltige Öle) und Notwendigkeit von GC/MS-zertifizierten, reinen Ölen.
Ätherische Öle können als Teil eines multimodalen Therapieansatzes für komorbide Symptome (Angst, Schlafstörungen, sensorische Dysregulation) bei ASD erwogen werden, ersetzen jedoch keine evidenzbasierten Kerninterventionen (Verhaltenstherapie, strukturierte Bildung). Zukünftige Forschung sollte hochwertige RCTs, Stratifizierung nach neurobiologischen Subtypen, mechanistische Biomarker-Studien und Langzeit-Sicherheitsdaten priorisieren, um das therapeutische Potenzial ätherischer Öle bei ASD zu validieren und Precision-Medicine-Ansätze zu entwickeln.
Gemeinsame Schlussfolgerung
Übergreifende Erkenntnisse: ADHS und Autismus
Beide neurodevelopmentalen Störungen, ADHS und Autismus-Spektrum-Störung (ASD), teilen fundamentale neurobiologische Gemeinsamkeiten, die eine adjuvante Therapie mit ätherischen Ölen für beide Indikationen plausibel machen.
Gemeinsame neurobiologische Zielstrukturen:
| Meccanismo | ADHS-Relevanz | ASD-Relevanz | Geeignete Öle |
| Dopamin-Dysregulation | DAT-Überexpression, Hypodopaminerg | Mesolimbische Dysfunktion | Rosmarin (1,8-Cineol), Schwarzer Pfeffer (β-Caryophyllen), Ingwer |
| GABA/Glutamat-Imbalance | Inhibitorisches Defizit | E/I-Imbalance (Kernpathologie) | Lavendel (Linalool), Melissa (Rosmarinsäure), 1,8-Cineol, Eukalyptus |
| Neuroinfiammazione | Attivazione della microglia | TNF-α, IL-6, IL-1β erhöht | β-Caryophyllen (CB2), Boswellia (Nrf2), Ingwer (STAT3/TNF-α) |
| Oxidativer Stress | Disfunzione mitocondriale | GSH erniedrigt, ROS erhöht | Boswellia, Lavendel, Ingwer |
| Serotonin-Modulation | Noradrenalin/Serotonin-Interaktion | 5-HT-Dysregulation | Lavendel, Bergamotte, Sandelholz |
| Aufmerksamkeit/Kognition | Kerndefizit (Sustained Attention) | Exekutivfunktionen betroffen | Pfefferminze (Menthol), Rosmarin, Melissa, Eukalyptus |
| Cholinerge Bahnen | Präfrontaler Kortex | Kognition, Lernen | Melissa (AChE-Hemmung), Eukalyptus (1,8-Cineol) |
| Soziales Verhalten | Weniger betroffen | Kerndefizit | Terpenmischungen (BTBR-Modell), Ingwer (VPA-Modell) |
Gemeinsame Anwendungsempfehlung (Organik Aromas Nebulizer 3.0):
Für beide Indikationen gilt das Venturi-Kaltverneblung-Prinzip ohne Wasser oder Hitze als optimale Applikationsform: – Keine thermische Degradation der Terpene – Präzise Partikelgröße für olfaktorische Aufnahme (< 5 µm) – GC/MS-reine Öle erhalten ihre molekulare Integrität
Wichtiger Hinweis
Die adjuvante Therapie mit ätherischen Ölen ersetzt keine evidenzbasierte Standardtherapie (Methylphenidat bei ADHS, ABA/Verhaltenstherapie bei ASD). Sie stellt eine komplementäre Ergänzung dar, die individuell angepasst und unter fachkundiger Begleitung durchgeführt werden sollte. Die Evidenzlage ist für beide Indikationen noch begrenzt; größere RCTs sind notwendig.
Referenzen ADHS
[A1] Chen et al. (2008). The effect of applying cinnamon aromatherapy for children with attention deficit hyperactivity disorder.https://pmc.ncbi.nlm.nih.gov/articles/PMC8538900/
[A2] Chen et al. The effect of applying cinnamon aromatherapy for children with attention deficit hyperactivity disorder.https://pmc.ncbi.nlm.nih.gov/articles/PMC8538900/
[A3] Godfrey (2001). The role of essential oils in the treatment and management of attention deficit hyperactive disorder. International Journal of Aromatherapy.https://doi.org/10.1016/S0962-4562(01 )80035-7
[A4] Godfrey. Essential oils: Complementary treatment for attention deficit hyperactive disorder (ADHD).https://www.researchgate.net/publication/248871372_The_role_of_essential_oils_in_the_treatment_and_management_of_attention_deficit_hyperactive_disorder
[A5] Godfrey. THE ROLE OF ESSENTIAL OILS IN THE TREATMENT AND MANAGEMENT OF ATTENTION DEFICIT HYPERACTIVE DISORDER (ADHD).https://www.researchgate.net/publication/248871372_The_role_of_essential_oils_in_the_treatment_and_management_of_attention_deficit_hyperactive_disorder
[A6] Ding et al. (1994). Pharmacokinetics and in vivo specificity of [LLC]dl-threo-methylphenidate for the presynaptic dopaminergic neuron. Synapse.https://doi.org/10.1002/SYN.890180207
[A7] Volkow et al. (2002). Mechanism of action of methylphenidate: insights from PET imaging studies. Journal of Attention Disorders.https://doi.org/10.1177/070674370200601S05
[A8] Silva (2024). Aromatherapy in the Care of an Atypical Child with ADHD and Atopic Dermatitis.https://doi.org/10.62435/2965-7253.bjhae.2024.iisinaroma1
[A9] Volkow et al. (1998). Dopamine Transporter Occupancies in the Human Brain Induced by Therapeutic Doses of Oral Methylphenidate. American Journal of Psychiatry.https://doi.org/10.1176/AJP.155.10.1325
[A10] Jacob et al. (2024). Uso da aromaterapia na atenção estudantil.https://doi.org/10.37885/240717094
[A11] Dipasquale et al. (2020). Unravelling the effects of methylphenidate on the dopaminergic and noradrenergic functional circuits. bioRxiv.https://doi.org/10.1101/2020.03.09.983528
[A12] Volkow et al. (2002). Role of dopamine in the therapeutic and reinforcing effects of methylphenidate in humans: results from imaging studies. European Neuropsychopharmacology.https://doi.org/10.1016/S0924-977X(02 )00104-9
[A13] Spencer et al. (2006). PET Study Examining Pharmacokinetics, Detection and Likeability, and Dopamine Transporter Receptor Occupancy of Short- and Long-Acting Oral Methylphenidate. American Journal of Psychiatry.https://doi.org/10.1176/APPI.AJP.163.3.387
[A14] Castillo et al. (2018). Essential oils as modifiers of human behavior. Tropical and Subtropical Agroecosystems.https://www.revista.ccba.uady.mx/ojs/index.php/TSA/article/view/2583
[A15] Crunelle et al. (2014). Dopamine transporter occupancy by methylphenidate and impulsivity in adult ADHD. British Journal of Psychiatry.https://doi.org/10.1192/BJP.BP.113.132977
[A16] Ding et al. (1997). Chiral drugs: comparison of the pharmacokinetics of [11C]d-threo and l-threo-methylphenidate in the human and baboon brain. Psychopharmacology.https://doi.org/10.1007/S002130050267
[A17] Spencer et al. (2009). A PET study examining pharmacokinetics and dopamine transporter occupancy of two long-acting formulations of methylphenidate in adults. International Journal of Molecular Medicine.https://doi.org/10.3892/IJMM_00000339
[A18] Marcel et al. (2024). Responsivity of the Striatal Dopamine System to Methylphenidate—A Within-Subject I-123-β-CIT-SPECT Study in Male Children and Adolescents With Attention-Deficit/Hyperactivity Disorder.https://doi.org/10.5283/epub.57629
[A19] Kennedy et al. (2018). Volatile Terpenes and Brain Function: Investigation of the Cognitive and Mood Effects of Mentha × Piperita L. Essential Oil with In Vitro Properties Relevant to Central Nervous System Function. Nutrients.https://doi.org/10.3390/NU10081029
[A20] Batiha et al. (2023). A review of the bioactive components and pharmacological properties of Lavandula species. Naunyn-schmiedebergs Archives of Pharmacology.https://doi.org/10.1007/s00210-023-02392-x
[A21] Guzmán-Gutiérrez et al. (2015). Linalooland β-pineneexerttheirantidepressant-likeactivitythroughthe monoaminergic pathway.https://pubmed.ncbi.nlm.nih.gov/25771248/
[A22] Martinez et al. (2020). Ventral striatum supports Methylphenidate therapeutic effects on impulsive choices expressed in temporal discounting task. Scientific reports.https://doi.org/10.1038/s41598-020-57595-6
[A23] López et al. (2017). Exploring Pharmacological Mechanisms of Lavender (Lavandula angustifolia) Essential Oil on Central Nervous System Targets. Frontiers in Pharmacology.https://doi.org/10.3389/FPHAR.2017.00280
[A24] Rathnayake (2025). “Neuroaromatics” : Aromatherapy and the Limbic Stress Response.https://doi.org/10.4038/jssnisd.v3i1.28
[A25] Aster et al. (2021). Responsivity of the striatal dopamine system to methylphenidate – a within-subject I-123-β-CIT-SPECT study in children and adolescents with Attention-Deficit/Hyperactivity Disorder. medRxiv.https://doi.org/10.1101/2021.11.19.21265993
[A26] Cardoso et al. (2025). The Impact of Lavender Essential Oil on the Human Nervous System: A Review. Deleted Journal.https://doi.org/10.62435/2965-7253.bjhae.2025.bjhae22
[A27] Moss et al. (2003). Aromas of rosemary and lavender essential oils differentially affect cognition and mood in healthy adults. International Journal of Neuroscience.https://doi.org/10.1080/00207450390161903
[A28] Sinha et al. (2005). Complementary and alternative medicine use in children with attention deficit hyperactivity disorder. Journal of Paediatrics and Child Health.https://doi.org/10.1111/J.1440-1754.2005.00530.X
[A29] Springer et al. (2018). ADHD: The Lifespan and Effects from Adolescence through Adulthood.https://dergipark.org.tr/en/pub/pgy/548052.xml
[A30] Colzato et al. (2014). Attentional control in the attentional blink is modulated by odor. Attention Perception & Psychophysics.https://doi.org/10.3758/S13414-014-0733-0
A31. Kennedy, D. O., Scholey, A., Tildesley, N. T. J., Perry, E. K., & Wesnes, K. A. (2002). Modulation of mood and cognitive performance following acute administration of Melissa officinalis (lemon balm). Pharmacology, Biochemistry and Behavior, 72(4), 953–964. https://doi.org/10.1016/S0091-3057(02)00777-3
A32. Müller, S. F., & Klement, S. (2006). A combination of valerian and lemon balm is effective in the treatment of restlessness and dyssomnia in children. Phytomedicine, 13(6), 383–387. https://doi.org/10.1016/j.phymed.2006.01.013
A33. Scholey, A., Gibbs, A., Neale, C., et al. (2014). Anti-stress effects of lemon balm-containing foods. Nutrienti, 6(11), 4805–4821. https://doi.org/10.3390/nu6114805
A34. Review on neuroprotective effects of essential oils including Eucalyptus globulus and Jasminum sambac on cognitive function and Alzheimer’s disease-related pathology. (2022). Neuroprotective Essential Oils Review.
Referenzen ASD
[B1] Maenner MJ, Shaw KA, Bakian AV, et al. Prevalence and Characteristics of Autism Spectrum Disorder Among Children Aged 8 Years — Autism and Developmental Disabilities Monitoring Network, 11 Sites, United States, 2018. MMWR Surveill Summ. 2021;70(11):1-16.https://doi.org/10.15585/mmwr.ss7011a1
[B2] Zeidan J, Fombonne E, Scorah J, et al. Global prevalence of autism: A systematic review update. Autism Res. 2022;15(5):778-790.https://doi.org/10.1002/aur.2696
[B3] Lord C, Elsabbagh M, Baird G, Veenstra-Vanderweele J. Autism spectrum disorder. Lancet. 2018;392(10146):508-520.https://doi.org/10.1016/S0140-6736(18 )31129-2
[B4] Masi A, DeMayo MM, Glozier N, Guastella AJ. An Overview of Autism Spectrum Disorder, Heterogeneity and Treatment Options. Neurosci Bull. 2017;33(2):183-193.https://doi.org/10.1007/s12264-017-0100-y
[B5] American Psychiatric Association. Diagnostic and Statistical Manual of Mental Disorders, Fifth Edition (DSM-5). Arlington, VA: American Psychiatric Publishing; 2013.https://www.psychiatry.org/psychiatrists/practice/dsm
[B6] Marco EJ, Hinkley LB, Hill SS, Nagarajan SS. Sensory processing in autism: a review of neurophysiologic findings. Pediatr Res. 2011;69(5 Pt 2):48R-54R.https://doi.org/10.1203/PDR.0b013e3182130c54
[B7] Baum SH, Stevenson RA, Wallace MT. Behavioral, perceptual, and neural alterations in sensory and multisensory function in autism spectrum disorder. Prog Neurobiol. 2015;134:140-160.https://doi.org/10.1016/j.pneurobio.2015.09.007
[B8] van Steensel FJ, Bögels SM, Perrin S. Anxiety disorders in children and adolescents with autistic spectrum disorders: a meta-analysis. Clin Child Fam Psychol Rev. 2011;14(3):302-317.https://doi.org/10.1007/s10567-011-0097-0
[B9] Souders MC, Mason TB, Valladares O, et al. Sleep behaviors and sleep quality in children with autism spectrum disorders. Sleep. 2009;32(12):1566-1578.https://doi.org/10.1093/sleep/32.12.1566
[B10] McElhanon BO, McCracken C, Karpen S, Sharp WG. Gastrointestinal symptoms in autism spectrum disorder: a meta-analysis. Pediatrics. 2014;133(5):872-883.https://doi.org/10.1542/peds.2013-3995
[B11] Geschwind DH, State MW. Gene hunting in autism spectrum disorder: on the path to precision medicine. Lancet Neurol. 2015;14(11):1109-1120.https://doi.org/10.1016/S1474-4422(15 )00044-7
[B12] De Rubeis S, He X, Goldberg AP, et al. Synaptic, transcriptional and chromatin genes disrupted in autism. Nature. 2014;515(7526):209-215.https://doi.org/10.1038/nature13772
[B13] Sandin S, Lichtenstein P, Kuja-Halkola R, et al. The Heritability of Autism Spectrum Disorder. JAMA. 2017;318(12):1182-1184.https://doi.org/10.1001/jama.2017.12141
[B14] Rubenstein JL, Merzenich MM. Model of autism: increased ratio of excitation/inhibition in key neural systems. Genes Brain Behav. 2003;2(5):255-267.https://doi.org/10.1034/j.1601-183x.2003.00037.x
[B15] Vargas DL, Nascimbene C, Krishnan C, Zimmerman AW, Pardo CA. Neuroglial activation and neuroinflammation in the brain of patients with autism. Ann Neurol. 2005;57(1):67-81.https://doi.org/10.1002/ana.20315
[B16] Rossignol DA, Frye RE. Evidence linking oxidative stress, mitochondrial dysfunction, and inflammation in the brain of individuals with autism. Front Physiol. 2014;5:150.https://doi.org/10.3389/fphys.2014.00150
[B17] Nelson SB, Valakh V. Excitatory/Inhibitory Balance and Circuit Homeostasis in Autism Spectrum Disorders. Neuron. 2015;87(4):684-698.https://doi.org/10.1016/j.neuron.2015.07.033
[B18] Lee E, Lee J, Kim E. Excitation/Inhibition Imbalance in Animal Models of Autism Spectrum Disorders. Biol Psychiatry. 2017;81(10):838-847.https://doi.org/10.1016/j.biopsych.2016.05.011
[B19] Horder J, Lavender T, Mendez MA, et al. Reduced subcortical glutamate/glutamine in adults with autism spectrum disorders: a [¹H]MRS study. Transl Psychiatry. 2013;3:e279.https://doi.org/10.1038/tp.2013.53
[B20] Gaetz W, Bloy L, Wang DJ, et al. GABA estimation in the brains of children on the autism spectrum: measurement precision and regional cortical variation. Neuroimage. 2014;86:1-9.https://doi.org/10.1016/j.neuroimage.2013.05.068
[B21] Rojas DC, Singel D, Steinmetz S, Hepburn S, Brown MS. Decreased left perisylvian GABA concentration in children with autism and unaffected siblings. Neuroimage. 2014;86:28-34.https://doi.org/10.1016/j.neuroimage.2013.01.045
[B22] Amaral DG, Schumann CM, Nordahl CW. Neuroanatomy of autism. Trends Neurosci. 2008;31(3):137-145.https://doi.org/10.1016/j.tins.2007.12.005
[B23] Courchesne E, Pierce K. Why the frontal cortex in autism might be talking only to itself: local over-connectivity but long-distance disconnection. Curr Opin Neurobiol. 2005;15(2):225-230.https://doi.org/10.1016/j.conb.2005.03.001
[B24] Baron-Cohen S, Ring HA, Bullmore ET, Wheelwright S, Ashwin C, Williams SC. The amygdala theory of autism. Neurosci Biobehav Rev. 2000;24(3):355-364.https://doi.org/10.1016/s0149-7634(00 )00011-7
[B25] Estes ML, McAllister AK. Maternal immune activation: Implications for neuropsychiatric disorders. Science. 2016;353(6301):772-777.https://doi.org/10.1126/science.aag3194
[B26] Matta SM, Hill-Yardin EL, Crack PJ. The influence of neuroinflammation in Autism Spectrum Disorder. Brain Behav Immun. 2019;79:75-90.https://doi.org/10.1016/j.bbi.2019.04.037
[B27] Careaga M, Murai T, Bauman MD. Maternal Immune Activation and Autism Spectrum Disorder: From Rodents to Nonhuman and Human Primates. Biol Psychiatry. 2017;81(5):391-401.https://doi.org/10.1016/j.biopsych.2016.10.020
[B28] Chauhan A, Chauhan V. Oxidative stress in autism. Pathophysiology. 2006;13(3):171-181.https://doi.org/10.1016/j.pathophys.2006.05.007
[B29] Rose S, Melnyk S, Pavliv O, et al. Evidence of oxidative damage and inflammation associated with low glutathione redox status in the autism brain. Transl Psychiatry. 2012;2:e134.https://doi.org/10.1038/tp.2012.61
[B30] Kang DW, Adams JB, Gregory AC, et al. Microbiota Transfer Therapy alters gut ecosystem and improves gastrointestinal and autism symptoms: an open-label study. Microbiome. 2017;5(1):10.https://doi.org/10.1186/s40168-016-0225-7
[B31] Vuong HE, Hsiao EY. Emerging Roles for the Gut Microbiome in Autism Spectrum Disorder. Biol Psychiatry. 2017;81(5):411-423.https://doi.org/10.1016/j.biopsych.2016.08.024
[B32] Sharon G, Cruz NJ, Kang DW, et al. Human Gut Microbiota from Autism Spectrum Disorder Promote Behavioral Symptoms in Mice. Cell. 2019;177(6):1600-1618.e17.https://doi.org/10.1016/j.cell.2019.05.004
[B33] Sgritta M, Dooling SW, Buffington SA, et al. Mechanisms Underlying Microbial-Mediated Changes in Social Behavior in Mouse Models of Autism Spectrum Disorder. Neuron. 2019;101(2):246-259.e6.https://doi.org/10.1016/j.neuron.2018.11.018
[B34] Reichow B, Hume K, Barton EE, Boyd BA. Early intensive behavioral intervention (EIBI) for young children with autism spectrum disorders (ASD). Cochrane Database Syst Rev. 2018;5(5):CD009260.https://doi.org/10.1002/14651858.CD009260.pub3
[B35] Dawson G, Rogers S, Munson J, et al. Randomized, controlled trial of an intervention for toddlers with autism: the Early Start Denver Model. Pediatrics. 2010;125(1):e17-23.https://doi.org/10.1542/peds.2009-0958
[B36] McCracken JT, McGough J, Shah B, et al. Risperidone in children with autism and serious behavioral problems. N Engl J Med. 2002;347(5):314-321.https://doi.org/10.1056/NEJMoa013171
[B37] Marcus RN, Owen R, Kamen L, et al. A placebo-controlled, fixed-dose study of aripiprazole in children and adolescents with irritability associated with autistic disorder. J Am Acad Child Adolesc Psychiatry. 2009;48(11):1110-1119.https://doi.org/10.1097/CHI.0b013e3181b76658
[B38] Scahill L, McDougle CJ, Aman MG, et al. Effects of risperidone and parent training on adaptive functioning in children with pervasive developmental disorders and serious behavioral problems. J Am Acad Child Adolesc Psychiatry. 2012;51(2):136-146.https://doi.org/10.1016/j.jaac.2011.11.010
[B39] Rossignol DA, Frye RE. Melatonin in autism spectrum disorders: a systematic review and meta-analysis. Dev Med Child Neurol. 2011;53(9):783-792.https://doi.org/10.1111/j.1469-8749.2011.03980.x
[B40] Hollander E, Soorya L, Chaplin W, et al. A double-blind placebo-controlled trial of fluoxetine for repetitive behaviors and global severity in adult autism spectrum disorders. Am J Psychiatry. 2012;169(3):292-299.https://doi.org/10.1176/appi.ajp.2011.10050764
[B41] Spencer D, Marshall J, Post B, et al. Psychotropic medication use and polypharmacy in children with autism spectrum disorders. Pediatrics. 2013;132(5):833-840.https://doi.org/10.1542/peds.2012-3774
[B42] Koulivand PH, Khaleghi Ghadiri M, Gorji A. Lavender and the nervous system. Evid Based Complement Alternat Med. 2013;2013:681304.https://doi.org/10.1155/2013/681304
[B43] Sowndhararajan K, Kim S. Influence of Fragrances on Human Psychophysiological Activity: With Special Reference to Human Electroencephalographic Response. Sci Pharm. 2016;84(4):724-751.https://doi.org/10.3390/scipharm84040724
[B44] Ali B, Al-Wabel NA, Shams S, Ahamad A, Khan SA, Anwar F. Essential oils used in aromatherapy: A systemic review. Asian Pac J Trop Biomed. 2015;5(8):601-611.https://doi.org/10.1016/j.apjtb.2015.05.007
[B45] Sohal VS, Rubenstein JLR. Excitation-inhibition balance as a framework for investigating mechanisms in neuropsychiatric disorders. Mol Psychiatry. 2019;24(9):1248-1257.https://doi.org/10.1038/s41380-019-0426-0
[B46] Antoine MW, Langberg T, Schnepel P, Feldman DE. Increased Excitation-Inhibition Ratio Stabilizes Synapse and Circuit Excitability in Four Autism Mouse Models. Neuron. 2019;101(4):648-661.e4.https://doi.org/10.1016/j.neuron.2018.12.026
[B47] Fatemi SH, Halt AR, Stary JM, Kanodia R, Schulz SC, Realmuto GR. Glutamic acid decarboxylase 65 and 67 kDa proteins are reduced in autistic parietal and cerebellar cortices. Biol Psychiatry. 2002;52(8):805-810.https://doi.org/10.1016/s0006-3223(02 )01430-0
[B48] Yip J, Soghomonian JJ, Blatt GJ. Decreased GAD67 mRNA levels in cerebellar Purkinje cells in autism: pathophysiological implications. Acta Neuropathol. 2007;113(5):559-568.https://doi.org/10.1007/s00401-006-0176-3
[B49] Ben-Ari Y. Excitatory actions of gaba during development: the nature of the nurture. Nat Rev Neurosci. 2002;3(9):728-739.https://doi.org/10.1038/nrn920
[B50] Tyzio R, Nardou R, Ferrari DC, et al. Oxytocin-mediated GABA inhibition during delivery attenuates autism pathogenesis in rodent offspring. Science. 2014;343(6171):675-679.https://doi.org/10.1126/science.1247190
[B51] Lemonnier E, Degrez C, Phelep M, et al. A randomised controlled trial of bumetanide in the treatment of autism in children. Transl Psychiatry. 2012;2:e202.https://doi.org/10.1038/tp.2012.124
[B52] Lemonnier E, Villeneuve N, Sonie S, et al. Effects of bumetanide on neurobehavioral function in children and adolescents with autism spectrum disorders. Transl Psychiatry. 2017;7(3):e1056.https://doi.org/10.1038/tp.2017.10
[B53] Carlson GC. Glutamate receptor dysfunction and drug targets across models of autism spectrum disorders. Pharmacol Biochem Behav. 2012;100(4):850-854.https://doi.org/10.1016/j.pbb.2011.02.003
[B54] Uzunova G, Pallanti S, Hollander E. Excitatory/inhibitory imbalance in autism spectrum disorders: Implications for interventions and therapeutics. World J Biol Psychiatry. 2016;17(3):174-186.https://doi.org/10.3109/15622975.2015.1085597
[B55] Yoo HJ, Cho IH, Park M, Yang SY, Kim SA. Family based association of GRIN2A and GRIN2B with Korean autism spectrum disorders. Neurosci Lett. 2012;512(2):89-93.https://doi.org/10.1016/j.neulet.2012.01.061
[B56] Silverman JL, Tolu SS, Barkan CL, Crawley JN. Repetitive self-grooming behavior in the BTBR mouse model of autism is blocked by the mGluR5 antagonist MPEP. Neuropsychopharmacology. 2010;35(4):976-989.https://doi.org/10.1038/npp.2009.201
[B57] Muller CL, Anacker AMJ, Veenstra-VanderWeele J. The serotonin system in autism spectrum disorder: From biomarker to animal models. Neuroscience. 2016;321:24-41.https://doi.org/10.1016/j.neuroscience.2015.11.010
[B58] Pavăl D. A Dopamine Hypothesis of Autism Spectrum Disorder. Dev Neurosci. 2017;39(5):355-360.https://doi.org/10.1159/000478725
[B59] Schain RJ, Freedman DX. Studies on 5-hydroxyindole metabolism in autistic and other mentally retarded children. J Pediatr. 1961;58:315-320.https://doi.org/10.1016/s0022-3476(61 )80261-8
[B60] Cook EH Jr, Leventhal BL. The serotonin system in autism. Curr Opin Pediatr. 1996;8(4):348-354.https://doi.org/10.1097/00008480-199608000-00008
[B61] Chugani DC, Muzik O, Behen M, et al. Developmental changes in brain serotonin synthesis capacity in autistic and nonautistic children. Ann Neurol. 1999;45(3):287-295.https://doi.org/10.1002/1531-8249(199903 )45:3<287::aid-ana3>3.0.co;2-9
[B62] Devlin B, Cook EH Jr, Coon H, et al. Autism and the serotonin transporter: the long and short of it. Mol Psychiatry. 2005;10(12):1110-1116.https://doi.org/10.1038/sj.mp.4001724
[B63] Whitaker-Azmitia PM. Behavioral and cellular consequences of increasing serotonergic activity during brain development: a role in autism? Int J Dev Neurosci. 2005;23(1):75-83.https://doi.org/10.1016/j.ijdevneu.2004.07.022
[B64] King BH, Hollander E, Sikich L, et al. Lack of efficacy of citalopram in children with autism spectrum disorders and high levels of repetitive behavior: citalopram ineffective in children with autism. Arch Gen Psychiatry. 2009;66(6):583-590.https://doi.org/10.1001/archgenpsychiatry.2009.30
[B65] Dichter GS, Damiano CA, Allen JA. Reward circuitry dysfunction in psychiatric and neurodevelopmental disorders and genetic syndromes: animal models and clinical findings. J Neurodev Disord. 2012;4(1):19.https://doi.org/10.1186/1866-1955-4-19
[B66] Kohls G, Schulte-Rüther M, Nehrkorn B, et al. Reward system dysfunction in autism spectrum disorders. Soc Cogn Affect Neurosci. 2013;8(5):565-572.https://doi.org/10.1093/scan/nss033
[B67] Delmonte S, Balsters JH, McGrath J, et al. Social and monetary reward processing in autism spectrum disorders. Mol Autism. 2012;3(1):7.https://doi.org/10.1186/2040-2392-3-7
[B68] Nakamura K, Sekine Y, Ouchi Y, et al. Brain serotonin and dopamine transporter bindings in adults with high-functioning autism. Arch Gen Psychiatry. 2010;67(1):59-68.https://doi.org/10.1001/archgenpsychiatry.2009.137
[B69] Staal WG. Autism, DRD3 and repetitive and stereotyped behavior, an overview of the current knowledge. Eur Neuropsychopharmacol. 2015;25(9):1421-1426.https://doi.org/10.1016/j.euroneuro.2014.08.011
[B70] Gunaydin LA, Grosenick L, Finkelstein JC, et al. Natural neural projection dynamics underlying social behavior. Cell. 2014;157(7):1535-1551.https://doi.org/10.1016/j.cell.2014.05.017
[B71] Insel TR. The challenge of translation in social neuroscience: a review of oxytocin, vasopressin, and affiliative behavior. Neuron. 2010;65(6):768-779.https://doi.org/10.1016/j.neuron.2010.03.005
[B72] Modahl C, Green L, Fein D, et al. Plasma oxytocin levels in autistic children. Biol Psychiatry. 1998;43(4):270-277.https://doi.org/10.1016/s0006-3223(97 )00439-3
[B73] Gregory SG, Connelly JJ, Towers AJ, et al. Genomic and epigenetic evidence for oxytocin receptor deficiency in autism. BMC Med. 2009;7:62.https://doi.org/10.1186/1741-7015-7-62
[B74] Guastella AJ, Einfeld SL, Gray KM, et al. Intranasal oxytocin improves emotion recognition for youth with autism spectrum disorders. Biol Psychiatry. 2010;67(7):692-694.https://doi.org/10.1016/j.biopsych.2009.09.020
[B75] Parker KJ, Oztan O, Libove RA, et al. Intranasal oxytocin treatment for social deficits and biomarkers of response in children with autism. Proc Natl Acad Sci U S A. 2017;114(30):8119-8124.https://doi.org/10.1073/pnas.1705521114
[B76] Peñagarikano O, Lázaro MT, Lu XH, et al. Exogenous and evoked oxytocin restores social behavior in the Cntnap2 mouse model of autism. Sci Transl Med. 2015;7(271):271ra8.https://doi.org/10.1126/scitranslmed.3010257
[B77] Pardo CA, Vargas DL, Zimmerman AW. Immunity, neuroglia and neuroinflammation in autism. Int Rev Psychiatry. 2005;17(6):485-495.https://doi.org/10.1080/02646830500381930
[B78] Edmonson C, Ziats MN, Rennert OM. Altered glial marker expression in autistic post-mortem prefrontal cortex and cerebellum. Mol Autism. 2014;5:3.https://doi.org/10.1186/2040-2392-5-3
[B79] Salter MW, Stevens B. Microglia emerge as central players in brain disease. Nat Med. 2017;23(9):1018-1027.https://doi.org/10.1038/nm.4397
[B80] Morgan JT, Chana G, Pardo CA, et al. Microglial activation and increased microglial density observed in the dorsolateral prefrontal cortex in autism. Biol Psychiatry. 2010;68(4):368-376.https://doi.org/10.1016/j.biopsych.2010.05.024
[B81] Suzuki K, Sugihara G, Ouchi Y, et al. Microglial activation in young adults with autism spectrum disorder. JAMA Psychiatry. 2013;70(1):49-58.https://doi.org/10.1001/jamapsychiatry.2013.272
[B82] Zürcher NR, Loggia ML, Lawson R, et al. Increased in vivo glial activation in patients with amyotrophic lateral sclerosis: assessed with [(11)C]-PBR28. Neuroimage Clin. 2015;7:409-414.https://doi.org/10.1016/j.nicl.2015.01.009
[B83] Schafer DP, Lehrman EK, Kautzman AG, et al. Microglia sculpt postnatal neural circuits in an activity and complement-dependent manner. Neuron. 2012;74(4):691-705.https://doi.org/10.1016/j.neuron.2012.03.026
[B84] Ashwood P, Krakowiak P, Hertz-Picciotto I, Hansen R, Pessah I, Van de Water J. Elevated plasma cytokines in autism spectrum disorders provide evidence of immune dysfunction and are associated with impaired behavioral outcome. Brain Behav Immun. 2011;25(1):40-45.https://doi.org/10.1016/j.bbi.2010.08.003
[B85] Li X, Chauhan A, Sheikh AM, et al. Elevated immune response in the brain of autistic patients. J Neuroimmunol. 2009;207(1-2):111-116.https://doi.org/10.1016/j.jneuroim.2008.12.002
[B86] Smith SE, Li J, Garbett K, Mirnics K, Patterson PH. Maternal immune activation alters fetal brain development through interleukin-6. J Neurosci. 2007;27(40):10695-10702.https://doi.org/10.1523/JNEUROSCI.2178-07.2007
[B87] Choi GB, Yim YS, Wong H, et al. The maternal interleukin-17a pathway in mice promotes autism-like phenotypes in offspring. Science. 2016;351(6276):933-939.https://doi.org/10.1126/science.aad0314
[B88] Stellwagen D, Malenka RC. Synaptic scaling mediated by glial TNF-alpha. Nature. 2006;440(7087):1054-1059.https://doi.org/10.1038/nature04671
[B89] Wei H, Chadman KK, McCloskey DP, et al. Brain IL-6 elevation causes neuronal circuitry imbalances and mediates autism-like behaviors. Biochim Biophys Acta. 2012;1822(6):831-842.https://doi.org/10.1016/j.bbadis.2012.01.011
[B90] Verkhratsky A, Nedergaard M. Physiology of Astroglia. Physiol Rev. 2018;98(1):239-389.https://doi.org/10.1152/physrev.00042.2016
[B91] Laurence JA, Fatemi SH. Glial fibrillary acidic protein is elevated in superior frontal, parietal and cerebellar cortices of autistic subjects. Cerebellum. 2005;4(3):206-210.https://doi.org/10.1080/14734220500208846
[B92] Rothstein JD, Dykes-Hoberg M, Pardo CA, et al. Knockout of glutamate transporters reveals a major role for astroglial transport in excitotoxicity and clearance of glutamate. Neuron. 1996;16(3):675-686.https://doi.org/10.1016/s0896-6273(00 )80086-0
[B93] Sies H, Jones DP. Reactive oxygen species (ROS) as pleiotropic physiological signalling agents. Nat Rev Mol Cell Biol. 2020;21(7):363-383.https://doi.org/10.1038/s41580-020-0230-3
[B94] Frustaci A, Neri M, Cesario A, et al. Oxidative stress-related biomarkers in autism: systematic review and meta-analyses. Free Radic Biol Med. 2012;52(10):2128-2141.https://doi.org/10.1016/j.freeradbiomed.2012.03.011
[B95] Bjørklund G, Meguid NA, El-Bana MA, et al. Oxidative Stress in Autism Spectrum Disorder. Mol Neurobiol. 2020;57(5):2314-2332.https://doi.org/10.1007/s12035-019-01742-2
[B96] James SJ, Cutler P, Melnyk S, et al. Metabolic biomarkers of increased oxidative stress and impaired methylation capacity in children with autism. Am J Clin Nutr. 2004;80(6):1611-1617.https://doi.org/10.1093/ajcn/80.6.1611
[B97] Rose S, Melnyk S, Pavliv O, et al. Evidence of oxidative damage and inflammation associated with low glutathione redox status in the autism brain. Transl Psychiatry. 2012;2:e134.https://doi.org/10.1038/tp.2012.61
[B98] Bowers K, Li Q, Bressler J, et al. Glutathione pathway gene variation and risk of autism spectrum disorders. J Neurodev Disord. 2011;3(2):132-143.https://doi.org/10.1007/s11689-011-9077-4
[B99] Rossignol DA, Frye RE. Mitochondrial dysfunction in autism spectrum disorders: a systematic review and meta-analysis. Mol Psychiatry. 2012;17(3):290-314.https://doi.org/10.1038/mp.2010.136
[B100] Giulivi C, Zhang YF, Omanska-Klusek A, et al. Mitochondrial dysfunction in autism. JAMA. 2010;304(21):2389-2396.https://doi.org/10.1001/jama.2010.1706
[B101] Duchen MR. Mitochondria and calcium: from cell signalling to cell death. J Physiol. 2000;529 Pt 1(Pt 1):57-68.https://doi.org/10.1111/j.1469-7793.2000.00057.x
[B102] Bambini-Junior V, Rodrigues L, Behr GA, et al. Animal model of autism induced by prenatal exposure to valproate: behavioral changes and liver parameters. Brain Res. 2011;1408:8-16.https://doi.org/10.1016/j.brainres.2011.06.015
[B103] Ma Q. Role of nrf2 in oxidative stress and toxicity. Annu Rev Pharmacol Toxicol. 2013;53:401-426.https://doi.org/10.1146/annurev-pharmtox-011112-140320
[B104] Singh K, Connors SL, Macklin EA, et al. Sulforaphane treatment of autism spectrum disorder (ASD). Proc Natl Acad Sci U S A. 2014;111(43):15550-15555.https://doi.org/10.1073/pnas.1416940111
[B105] Bent S, Lawton B, Warren T, et al. Identification of urinary metabolites that correlate with clinical improvements in children with autism treated with sulforaphane from broccoli. Mol Autism. 2018;9:35.https://doi.org/10.1186/s13229-018-0218-4
[B106] Cryan JF, O’Riordan KJ, Cowan CSM, et al. The Microbiota-Gut-Brain Axis. Physiol Rev. 2019;99(4):1877-2013.https://doi.org/10.1152/physrev.00018.2018
[B107] Chaidez V, Hansen RL, Hertz-Picciotto I. Gastrointestinal problems in children with autism, developmental delays or typical development. J Autism Dev Disord. 2014;44(5):1117-1127.https://doi.org/10.1007/s10803-013-1973-x
[B108] Adams JB, Johansen LJ, Powell LD, Quig D, Rubin RA. Gastrointestinal flora and gastrointestinal status in children with autism–comparisons to typical children and correlation with autism severity. BMC Gastroenterol. 2011;11:22.https://doi.org/10.1186/1471-230X-11-22
[B109] Xu M, Xu X, Li J, Li F. Association Between Gut Microbiota and Autism Spectrum Disorder: A Systematic Review and Meta-Analysis. Front Psychiatry. 2019;10:473.https://doi.org/10.3389/fpsyt.2019.00473
[B110] Liu F, Li J, Wu F, et al. Altered composition and function of intestinal microbiota in autism spectrum disorders: a systematic review. Transl Psychiatry. 2019;9(1):43.https://doi.org/10.1038/s41398-019-0389-6
[B111] Kang DW, Park JG, Ilhan ZE, et al. Reduced incidence of Prevotella and other fermenters in intestinal microflora of autistic children. PLoS One. 2013;8(7):e68322.https://doi.org/10.1371/journal.pone.0068322
[B112] Stilling RM, van de Wouw M, Clarke G, Stanton C, Dinan TG, Cryan JF. The neuropharmacology of butyrate: The bread and butter of the microbiota-gut-brain axis? Neurochem Int. 2016;99:110-132.https://doi.org/10.1016/j.neuint.2016.06.011
[B113] MacFabe DF, Cain DP, Rodriguez-Capote K, et al. Neurobiological effects of intraventricular propionic acid in rats: possible role of short chain fatty acids on the pathogenesis and characteristics of autism spectrum disorders. Behav Brain Res. 2007;176(1):149-169.https://doi.org/10.1016/j.bbr.2006.07.025
[B114] Hsiao EY, McBride SW, Hsien S, et al. Microbiota modulate behavioral and physiological abnormalities associated with neurodevelopmental disorders. Cell. 2013;155(7):1451-1463.https://doi.org/10.1016/j.cell.2013.11.024
[B115] Bonaz B, Bazin T, Pellissier S. The Vagus Nerve at the Interface of the Microbiota-Gut-Brain Axis. Front Neurosci. 2018;12:49.https://doi.org/10.3389/fnins.2018.00049
[B116] Liu S, Hagiwara SI, Bhargava A. Early-life adversity, epigenetics, and visceral hypersensitivity. Neurogastroenterol Motil. 2017;29(9).https://doi.org/10.1111/nmo.13170
[B117] Zoghbi HY, Bear MF. Synaptic dysfunction in neurodevelopmental disorders associated with autism and intellectual disabilities. Cold Spring Harb Perspect Biol. 2012;4(3):a009886.https://doi.org/10.1101/cshperspect.a009886
[B118] Bourgeron T. From the genetic architecture to synaptic plasticity in autism spectrum disorder. Nat Rev Neurosci. 2015;16(9):551-563.https://doi.org/10.1038/nrn3992
[B119] Südhof TC. Neuroligins and neurexins link synaptic function to cognitive disease. Nature. 2008;455(7215):903-911.https://doi.org/10.1038/nature07456
[B120] Jamain S, Quach H, Betancur C, et al. Mutations of the X-linked genes encoding neuroligins NLGN3 and NLGN4 are associated with autism. Nat Genet. 2003;34(1):27-29.https://doi.org/10.1038/ng1136
[B121] Tabuchi K, Blundell J, Etherton MR, et al. A neuroligin-3 mutation implicated in autism increases inhibitory synaptic transmission in mice. Science. 2007;318(5847):71-76.https://doi.org/10.1126/science.1146221
[B122] Jamain S, Radyushkin K, Hammerschmidt K, et al. Reduced social interaction and ultrasonic communication in a mouse model of monogenic heritable autism. Proc Natl Acad Sci U S A. 2008;105(5):1710-1715.https://doi.org/10.1073/pnas.0711555105
[B123] Grabrucker AM, Schmeisser MJ, Schoen M, Boeckers TM. Postsynaptic ProSAP/Shank scaffolds in the cross-hair of synaptopathies. Trends Cell Biol. 2011;21(10):594-603.https://doi.org/10.1016/j.tcb.2011.07.003
[B124] Phelan K, McDermid HE. The 22q13.3 Deletion Syndrome (Phelan-McDermid Syndrome). Mol Syndromol. 2012;2(3-5):186-201.https://doi.org/10.1159/000334260
[B125] Peça J, Feliciano C, Ting JT, et al. Shank3 mutant mice display autistic-like behaviours and striatal dysfunction. Nature. 2011;472(7344):437-442.https://doi.org/10.1038/nature09965
[B126] Won H, Lee HR, Gee HY, et al. Autistic-like social behaviour in Shank2-mutant mice improved by restoring NMDA receptor function. Nature. 2012;486(7402):261-265.https://doi.org/10.1038/nature11208
[B127] Baudouin SJ, Gaudias J, Gerharz S, et al. Shared synaptic pathophysiology in syndromic and nonsyndromic rodent models of autism. Science. 2012;338(6103):128-132.https://doi.org/10.1126/science.1224159
[B128] Huber KM, Gallagher SM, Warren ST, Bear MF. Altered synaptic plasticity in a mouse model of fragile X mental retardation. Proc Natl Acad Sci U S A. 2002;99(11):7746-7750.https://doi.org/10.1073/pnas.122205699
[B129] Ecker C, Bookheimer SY, Murphy DG. Neuroimaging in autism spectrum disorder: brain structure and function across the lifespan. Lancet Neurol. 2015;14(11):1121-1134.https://doi.org/10.1016/S1474-4422(15 )00050-2
[B130] Hazlett HC, Gu H, Munsell BC, et al. Early brain development in infants at high risk for autism spectrum disorder. Nature. 2017;542(7641):348-351.https://doi.org/10.1038/nature21369
[B131] Miller EK, Cohen JD. An integrative theory of prefrontal cortex function. Annu Rev Neurosci. 2001;24:167-202.https://doi.org/10.1146/annurev.neuro.24.1.167
[B132] Castelli F, Frith C, Happé F, Frith U. Autism, Asperger syndrome and brain mechanisms for the attribution of mental states to animated shapes. Brain. 2002;125(Pt 8):1839-1849.https://doi.org/10.1093/brain/awf189
[B133] Just MA, Cherkassky VL, Keller TA, Kana RK, Minshew NJ. Functional and anatomical cortical underconnectivity in autism: evidence from an FMRI study of an executive function task and corpus callosum morphometry. Cereb Cortex. 2007;17(4):951-961.https://doi.org/10.1093/cercor/bhl006
[B134] Casanova MF, Buxhoeveden DP, Switala AE, Roy E. Minicolumnar pathology in autism. Neurology. 2002;58(3):428-432.https://doi.org/10.1212/wnl.58.3.428
[B135] Adolphs R. The social brain: neural basis of social knowledge. Annu Rev Psychol. 2009;60:693-716.https://doi.org/10.1146/annurev.psych.60.110707.163514
[B136] Nordahl CW, Scholz R, Yang X, et al. Increased rate of amygdala growth in children aged 2 to 4 years with autism spectrum disorders: a longitudinal study. Arch Gen Psychiatry. 2012;69(1):53-61.https://doi.org/10.1001/archgenpsychiatry.2011.145
[B137] Kleinhans NM, Richards T, Sterling L, et al. Abnormal functional connectivity in autism spectrum disorders during face processing. Brain. 2008;131(Pt 4):1000-1012.https://doi.org/10.1093/brain/awm334
[B138] Monk CS, Weng SJ, Wiggins JL, et al. Neural circuitry of emotional face processing in autism spectrum disorders. J Psychiatry Neurosci. 2010;35(2):105-114.https://doi.org/10.1503/jpn.090085
[B139] Schmahmann JD. The cerebellum and cognition. Neurosci Lett. 2019;688:62-75.https://doi.org/10.1016/j.neulet.2018.07.005
[B140] Fatemi SH, Aldinger KA, Ashwood P, et al. Consensus paper: pathological role of the cerebellum in autism. Cerebellum. 2012;11(3):777-807.https://doi.org/10.1007/s12311-012-0355-9
[B141] Courchesne E, Yeung-Courchesne R, Press GA, Hesselink JR, Jernigan TL. Hypoplasia of cerebellar vermal lobules VI and VII in autism. N Engl J Med. 1988;318(21):1349-1354.https://doi.org/10.1056/NEJM198805263182102
[B142] Wang SS, Kloth AD, Badura A. The cerebellum, sensitive periods, and autism. Neuron. 2014;83(3):518-532.https://doi.org/10.1016/j.neuron.2014.07.016
[B143] Squire LR, Stark CE, Clark RE. The medial temporal lobe. Annu Rev Neurosci. 2004;27:279-306.https://doi.org/10.1146/annurev.neuro.27.070203.144130
[B144] Schumann CM, Hamstra J, Goodlin-Jones BL, et al. The amygdala is enlarged in children but not adolescents with autism; the hippocampus is enlarged at all ages. J Neurosci. 2004;24(28):6392-6401.https://doi.org/10.1523/JNEUROSCI.1297-04.2004
[B145] Gaigg SB, Bowler DM. Free recall and forgetting of emotionally arousing words in autism spectrum disorder. Neuropsychologia. 2008;46(9):2336-2343.https://doi.org/10.1016/j.neuropsychologia.2008.03.008
[B146] Graybiel AM. The basal ganglia. Curr Biol. 2000;10(14):R509-R511.https://doi.org/10.1016/s0960-9822(00 )00593-5
[B147] Langen M, Durston S, Staal WG, Palmen SJ, van Engeland H. Caudate nucleus is enlarged in high-functioning medication-naive subjects with autism. Biol Psychiatry. 2007;62(3):262-266.https://doi.org/10.1016/j.biopsych.2006.09.040
[B148] Scott-Van Zeeland AA, Dapretto M, Ghahremani DG, Poldrack RA, Bookheimer SY. Reward processing in autism. Autism Res. 2010;3(2):53-67.https://doi.org/10.1002/aur.122
[B149] Gershenzon J, Dudareva N. The function of terpene natural products in the natural world. Nat Chem Biol. 2007;3(7):408-414.https://doi.org/10.1038/nchembio.2007.5
[B150] Russo EB. Taming THC: potential cannabis synergy and phytocannabinoid-terpenoid entourage effects. Br J Pharmacol. 2011;163(7):1344-1364.https://doi.org/10.1111/j.1476-5381.2011.01238.x
[B151] Aprotosoaie AC, Hăncianu M, Costache II, Miron A. Linalool: a review on a key odorant molecule with valuable biological properties. Flavour Fragr J. 2014;29(4):193-219.https://doi.org/10.1002/ffj.3197
[B152] Harada H, Kashiwadani H, Kanmura Y, Kuwaki T. Linalool Odor-Induced Anxiolytic Effects in Mice. Front Behav Neurosci. 2018;12:241.https://doi.org/10.3389/fnbeh.2018.00241
[B153] Elisabetsky E, Brum LF, Souza DO. Anticonvulsant properties of linalool in glutamate-related seizure models. Phytomedicine. 1999;6(2):107-113.https://doi.org/10.1016/S0944-7113(99 )80044-0
[B154] Linck VM, da Silva AL, Figueiró M, et al. Effects of inhaled Linalool in anxiety, social interaction and aggressive behavior in mice. Phytomedicine. 2010;17(8-9):679-683.https://doi.org/10.1016/j.phymed.2009.10.002
[B155] Takahashi M, Satou T, Ohashi M, Hayashi S, Sadamoto K, Koike K. Interspecies comparison of chemical composition and anxiolytic-like effects of lavender oils upon inhalation. Nat Prod Commun. 2011;6(11):1769-1774.https://journals.sagepub.com/doi/10.1177/1934578X1100601148
[B156] Peana AT, D’Aquila PS, Panin F, Serra G, Pippia P, Moretti MD. Anti-inflammatory activity of linalool and linalyl acetate constituents of essential oils. Phytomedicine. 2002;9(8):721-726.https://doi.org/10.1078/094471102321621322
[B157] Sabogal-Guáqueta AM, Posada-Duque R, Cortes NC, Arias-Londoño JD, Cardona-Gómez GP. Changes in the hippocampal and peripheral phospholipid profiles are associated with neurodegeneration hallmarks in a long-term global cerebral ischemia model: Attenuation by Linalool. Neuropharmacology. 2018;135:555-571.https://doi.org/10.1016/j.neuropharm.2018.04.015
[B158] Jäger W, Buchbauer G, Jirovetz L, Fritzer M. Percutaneous absorption of lavender oil from a massage oil. J Soc Cosmet Chem. 1992;43:49-54.https://www.researchgate.net/publication/232711524_Percutaneous_absorption_of_lavender_oil_from_a_massage_oil
[B159] Buchbauer G. Biological activities of essential oils. In: Baser KHC, Buchbauer G, eds. Handbook of Essential Oils: Science, Technology, and Applications. 2nd ed. CRC Press; 2015:235-280.https://www.routledge.com/Handbook-of-Essential-Oils-Science-Technology-and-Applications/Baser-Buchbauer/p/book/9781032046419
[B160] Gertsch J, Leonti M, Raduner S, et al. Beta-caryophyllene is a dietary cannabinoid. Proc Natl Acad Sci U S A. 2008;105(26):9099-9104.https://doi.org/10.1073/pnas.0803601105
[B161] Bahi A, Al Mansouri S, Al Memari E, Al Ameri M, Nurulain SM, Ojha S. β-Caryophyllene, a CB2 receptor agonist produces multiple behavioral changes relevant to anxiety and depression in mice. Physiol Behav. 2014;135:119-124.https://doi.org/10.1016/j.physbeh.2014.06.003
[B162] Atwood BK, Mackie K. CB2: a cannabinoid receptor with an identity crisis. Br J Pharmacol. 2010;160(3):467-479.https://doi.org/10.1111/j.1476-5381.2010.00729.x
[B163] Klauke AL, Racz I, Pradier B, et al. The cannabinoid CB₂ receptor-selective phytocannabinoid beta-caryophyllene exerts analgesic effects in mouse models of inflammatory and neuropathic pain. Eur Neuropsychopharmacol. 2014;24(4):608-620.https://doi.org/10.1016/j.euroneuro.2013.10.008
[B164] Cheng Y, Dong Z, Liu S. β-Caryophyllene ameliorates the Alzheimer-like phenotype in APP/PS1 Mice through CB2 receptor activation and the PPARγ pathway. Pharmacology. 2014;94(1-2):1-12.https://doi.org/10.1159/000362689
[B165] Askari VR, Shafiee-Nick R. Promising neuroprotective effects of β-caryophyllene against LPS-induced oligodendrocyte toxicity: A mechanistic study. Biochem Pharmacol. 2019;159:154-171.https://doi.org/10.1016/j.bcp.2018.12.001
[B166] Fontes LBA, Dias D, Aarestrup BJ, et al. β-Caryophyllene ameliorates the development of experimental autoimmune encephalomyelitis in C57BL/6 mice. Biomed Pharmacother. 2017;91:257-264.https://doi.org/10.1016/j.biopha.2017.04.092
[B167] Alberti TB, Barbosa WL, Vieira JL, Raposo NR, Dutra RC. (-)-β-Caryophyllene, a CB2 receptor-selective phytocannabinoid, suppresses motor paralysis and neuroinflammation in a murine model of multiple sclerosis. Int J Mol Sci. 2017;18(4):691.https://doi.org/10.3390/ijms18040691
[B168] Galdino PM, Nascimento MV, Florentino IF, et al. The anxiolytic-like effect of an essential oil derived from Spiranthera odoratissima A. St. Hil. leaves and its major component, β-caryophyllene, in male mice. Prog Neuropsychopharmacol Biol Psychiatry. 2012;38(2):276-284.https://doi.org/10.1016/j.pnpbp.2012.04.012
[B169] Horváth B, Mukhopadhyay P, Kechrid M, et al. β-Caryophyllene ameliorates cisplatin-induced nephrotoxicity in a cannabinoid 2 receptor-dependent manner. Free Radic Biol Med. 2012;52(8):1325-1333.https://doi.org/10.1016/j.freeradbiomed.2012.01.014
[B170] Fidyt K, Fiedorowicz A, Strządała L, Szumny A. β-caryophyllene and β-caryophyllene oxide-natural compounds of anticancer and analgesic properties. Cancer Med. 2016;5(10):3007-3017.https://doi.org/10.1002/cam4.816
[B171] Sharma C, Al Kaabi JM, Nurulain SM, Goyal SN, Kamal MA, Ojha S. Polypharmacological Properties and Therapeutic Potential of β-Caryophyllene: A Dietary Phytocannabinoid of Pharmaceutical Promise. Curr Pharm Des. 2016;22(21):3237-3264.https://doi.org/10.2174/1381612822666160311115226
[B172] Ammon HP. Boswellic acids and their role in chronic inflammatory diseases. Adv Exp Med Biol. 2016;928:291-327.https://doi.org/10.1007/978-3-319-41334-1_13
[B173] Catanzaro D, Rancan S, Orso G, et al. Boswellia serrata Preserves Intestinal Epithelial Barrier from Oxidative and Inflammatory Damage. PLoS One. 2015;10(5):e0125375.https://doi.org/10.1371/journal.pone.0125375
[B174] Khoshnazar M, Bigdeli MR, Parvardeh S, Pouriran R. Attenuating effect of α-pinene on neurobehavioural deficit, oxidative damage and inflammatory response following focal ischaemic stroke in rat. J Pharm Pharmacol. 2019;71(11):1725-1733.https://doi.org/10.1111/jphp.13164
[B175] Ryter SW, Alam J, Choi AM. Heme oxygenase-1/carbon monoxide: from basic science to therapeutic applications. Physiol Rev. 2006;86(2):583-650.https://doi.org/10.1152/physrev.00011.2005
[B176] Umar S, Umar K, Sarwar AH, et al. Boswellia serrata extract attenuates inflammatory mediators and oxidative stress in collagen induced arthritis. Phytomedicine. 2014;21(6):847-856.https://doi.org/10.1016/j.phymed.2014.02.001
[B177] Abdel-Tawab M, Werz O, Schubert-Zsilavecz M. Boswellia serrata: an overall assessment of in vitro, preclinical, pharmacokinetic and clinical data. Clin Pharmacokinet. 2011;50(6):349-369.https://doi.org/10.2165/11586800-000000000-00000
[B178] Hosseini M, Hadjzadeh MA, Derakhshan M, et al. The beneficial effects of olibanum on memory deficit induced by hypothyroidism in adult rats tested in Morris water maze. Arch Pharm Res. 2010;33(3):463-468.https://doi.org/10.1007/s12272-010-0316-6
[B179] Safayhi H, Mack T, Sabieraj J, Anazodo MI, Subramanian LR, Ammon HP. Boswellic acids: novel, specific, nonredox inhibitors of 5-lipoxygenase. J Pharmacol Exp Ther. 1992;261(3):1143-1146.https://www.sciencedirect.com/science/article/abs/pii/S0022356525111300
[B180] Werz O. 5-lipoxygenase: cellular biology and molecular pharmacology. Curr Drug Targets Inflamm Allergy. 2002;1(1):23-44.https://doi.org/10.2174/1568010023344959
[B181] Al-Harrasi A, Ali L, Hussain J, et al. Analgesic effects of crude extracts and fractions of Omani frankincense obtained from traditional medicinal plant Boswellia sacra on animal models. Asian Pac J Trop Med. 2014;7S1:S485-S490.https://doi.org/10.1016/S1995-7645(14 )60279-0
[B182] Cimanga K, Kambu K, Tona L, et al. Correlation between chemical composition and antibacterial activity of essential oils of some aromatic medicinal plants growing in the Democratic Republic of Congo. J Ethnopharmacol. 2002;79(2):213-220.https://doi.org/10.1016/s0378-8741(01 )00384-1
[B183] Satou T, Kasuya H, Maeda K, Koike K. Daily inhalation of α-pinene in mice: effects on behavior and organ accumulation. Phytother Res. 2014;28(9):1284-1287.https://doi.org/10.1002/ptr.5105
[B184] Satou T, Murakami S, Matsuura M, Hayashi S, Koike K. Anxiolytic effect and tissue distribution of inhaled Alpinia zerumbet essential oil in mice. Nat Prod Commun. 2010;5(1):143-146.https://journals.sagepub.com/doi/10.1177/1934578X1000500133
[B185] Juergens UR, Dethlefsen U, Steinkamp G, Gillissen A, Repges R, Vetter H. Anti-inflammatory activity of 1.8-cineol (eucalyptol) in bronchial asthma: a double-blind placebo-controlled trial. Respir Med. 2003;97(3):250-256.https://doi.org/10.1053/rmed.2003.1432
[B186] Santos FA, Rao VS. Antiinflammatory and antinociceptive effects of 1,8-cineole a terpenoid oxide present in many plant essential oils. Phytother Res. 2000;14(4):240-244.https://doi.org/10.1002/1099-1573(200006 )14:4<240::aid-ptr573>3.0.co;2-x
[B187] Tisserand R, Young R. Essential Oil Safety: A Guide for Health Care Professionals. 2nd ed. Churchill Livingstone; 2014.https://www.elsevier.com/books/essential-oil-safety/tisserand/978-0-7020-4606-4
[B188] Worth H, Schacher C, Dethlefsen U. Concomitant therapy with Cineole (Eucalyptole) reduces exacerbations in COPD: a placebo-controlled double-blind trial. Respir Res. 2009;10:69.https://doi.org/10.1186/1465-9921-10-69
[B189] Salehi B, Upadhyay S, Erdogan Orhan I, et al. Therapeutic Potential of α- and β-Pinene: A Miracle Gift of Nature. Biomolecules. 2019;9(11):738.https://doi.org/10.3390/biom9110738
[B190] Guzmán-Gutiérrez SL, Gómez-Cansino R, García-Zebadúa JC, Jiménez-Pérez NC, Reyes-Chilpa R. Antidepressant activity of Litsea glaucescens essential oil: identification of β-pinene and linalool as active principles. J Ethnopharmacol. 2012;143(2):673-679.https://doi.org/10.1016/j.jep.2012.07.026
[B191] Yang H, Woo J, Pae AN, et al. α-Pinene, a Major Constituent of Pine Tree Oils, Enhances Non-Rapid Eye Movement Sleep in Mice through GABAA-benzodiazepine receptors. Mol Pharmacol. 2016;90(5):530-539.https://doi.org/10.1124/mol.116.105080
[B192] Kim DS, Lee HJ, Jeon YD, et al. Alpha-Pinene Exhibits Anti-inflammatory Activity Through the Suppression of MAPKs and the NF-κB Pathway in Mouse Peritoneal Macrophages. Am J Chin Med. 2015;43(4):731-742.https://doi.org/10.1142/S0192415X15500457
[B193] Porres-Martínez M, González-Burgos E, Carretero ME, Gómez-Serranillos MP. Protective properties of Salvia lavandulifolia Vahl. essential oil against oxidative stress-induced neuronal injury. Food Chem Toxicol. 2015;80:154-162.https://doi.org/10.1016/j.fct.2015.03.002
[B194] Miyazawa M, Watanabe H, Kameoka H. Inhibition of acetylcholinesterase activity by monoterpenoids with a p-menthane skeleton. J Agric Food Chem. 1997;45(3):677-679.https://doi.org/10.1021/jf960398b
[B195] Deutsch SI, Burket JA, Katz E. Does subtle disturbance of neuronal migration contribute to schizophrenia and other neurodevelopmental disorders? Potential genetic mechanisms with possible treatment implications. Eur Neuropsychopharmacol. 2010;20(5):281-287.https://doi.org/10.1016/j.euroneuro.2010.02.005
[B196] Tan LT, Lee LH, Yin WF, et al. Traditional Uses, Phytochemistry, and Bioactivities of Cananga odorata (Ylang-Ylang). Evid Based Complement Alternat Med. 2015;2015:896314.https://doi.org/10.1155/2015/896314
[B197] Jung YH, Ha TM, Ahn J, et al. Inhalation of Cananga odorata Essential Oil Improved Social Interaction and Anxiety-Like Behaviors in Valproic Acid-Induced Autism Spectrum Disorder Rats. Nutrients. 2021;13(11):3804.https://doi.org/10.3390/nu13113804
[B198] Sinha Y, Silove N, Wheeler D, Williams K. Auditory integration training and other sound therapies for autism spectrum disorders: a systematic review. Arch Dis Child. 2006;91(12):1018-1022.https://doi.org/10.1136/adc.2006.094649
[B199] Cullen-Powell LA, Barlow JH, Cushway D. Exploring a massage intervention for parents and their children with autism: the implications for bonding and attachment. J Child Health Care. 2005;9(4):245-255.https://doi.org/10.1177/1367493505056479
[B200] Buckle J. Clinical Aromatherapy: Essential Oils in Healthcare. 3rd ed. Churchill Livingstone; 2014.https://www.elsevier.com/books/clinical-aromatherapy/buckle/978-0-7020-5440-3
[B201] Saiyudthong S, Marsden CA. Acute effects of bergamot oil on anxiety-related behaviour and corticosterone level in rats. Phytother Res. 2011;25(6):858-862.https://doi.org/10.1002/ptr.3325
[B202] Navarra M, Mannucci C, Delbò M, Calapai G. Citrus bergamia essential oil: from basic research to clinical application. Front Pharmacol. 2015;6:36.https://doi.org/10.3389/fphar.2015.00036
[B203] Efferth T, Oesch F. Anti-inflammatory and anti-cancer activities of frankincense: Targets, treatments and toxicities. Semin Cancer Biol. 2022;80:39-57.https://doi.org/10.1016/j.semcancer.2020.01.015
[B204] Siddiqui MZ. Boswellia serrata, a potential antiinflammatory agent: an overview. Indian J Pharm Sci. 2011;73(3):255-261.https://doi.org/10.4103/0250-474X.93507
[B205] Hamidpour R, Hamidpour S, Hamidpour M, Shahlari M. Frankincense (rǔ xiāng; Boswellia Species): From the Selection of Traditional Applications to the Novel Phytotherapy for the Prevention and Treatment of Serious Diseases. J Tradit Complement Med. 2013;3(4):221-226.https://doi.org/10.4103/2225-4110.119723
[B206] Moussaieff A, Mechoulam R. Boswellia resin: from religious ceremonies to medical uses; a review of in-vitro, in-vivo and clinical trials. J Pharm Pharmacol. 2009;61(10):1281-1293.https://doi.org/10.1211/jpp/61.10.0003
[B207] Bakkali F, Averbeck S, Averbeck D, Idaomar M. Biological effects of essential oils–a review. Food Chem Toxicol. 2008;46(2):446-475.https://doi.org/10.1016/j.fct.2007.09.106
[B208] Setzer WN. Essential oils and anxiolytic aromatherapy. Nat Prod Commun. 2009;4(9):1305-1316.https://pubmed.ncbi.nlm.nih.gov/19831048/
[B209] Adams RP. Identification of Essential Oil Components by Gas Chromatography/Mass Spectrometry. 4th ed. Allured Publishing; 2007.https://www.allured.com/identification-of-essential-oil-components-by-gas-chromatographymass-spectrometry-4th-edition
[B210] Dayawansa S, Umeno K, Takakura H, et al. Autonomic responses during inhalation of natural fragrance of Cedrol in humans. Auton Neurosci. 2003;108(1-2):79-86.https://doi.org/10.1016/j.autneu.2003.08.002
[B211] Cheaha D, Reakkamnuan C, Nukitram J, et al. Modification of sleep-waking and electroencephalogram induced by vetiver essential oil inhalation. J Intercult Ethnopharmacol. 2016;5(1):72-78.https://doi.org/10.5455/jice.20160208050736
[B212] Friedmann T. Freedom from ADHD: A Drug-Free Approach to Treating Children with ADHD. Lotus Press; 2000.https://www.researchgate.net/publication/265127532_Attention_Deficit_and_Hyperactivity_Disorder_ADHD
[B213] Weyerstahl P, Marschall H, Weirauch M, Thefeld K, Surburg H. Constituents of commercial vetiver oils. Flavour Fragr J. 2000;15(3):153-173.https://doi.org/10.1002/1099-1026(200005/06 )15:3<153::AID-FFJ882>3.0.CO;2-V
[B214] Pripdeevech P, Chumpolsri W, Suttiarporn P, Wongpornchai S. The chemical composition and antioxidant activities of basil from Thailand using retention indices and comprehensive two-dimensional gas chromatography. J Serb Chem Soc. 2010;75(11):1503-1513.https://doi.org/10.2298/JSC100203125P
[B215] Hongratanaworakit T, Buchbauer G. Relaxing effect of ylang ylang oil on humans after transdermal absorption. Phytother Res. 2006;20(9):758-763.https://doi.org/10.1002/ptr.1950
[B216] Moss M, Hewitt S, Moss L, Wesnes K. Modulation of cognitive performance and mood by aromas of peppermint and ylang-ylang. Int J Neurosci. 2008;118(1):59-77.https://doi.org/10.1080/00207450601042094
[B217] Komiya M, Takeuchi T, Harada E. Lemon oil vapor causes an anti-stress effect via modulating the 5-HT and DA activities in mice. Behav Brain Res. 2006;172(2):240-249.https://doi.org/10.1016/j.bbr.2006.05.006
[B218] Venturi GB. Experimental Enquiries Concerning the Principle of the Lateral Communication of Motion in Fluids. Phil Trans R Soc Lond. 1797;87:243-260.https://royalsocietypublishing.org/doi/10.1098/rstl.1799.0005
[B219] Buckle J. Use of aromatherapy as a complementary treatment for chronic pain. Altern Ther Health Med. 1999;5(5):42-51.https://pubmed.ncbi.nlm.nih.gov/10450129/
[B220] Hongratanaworakit T. Aroma-therapeutic effects of massage blended essential oils on humans. Nat Prod Commun. 2011;6(8):1199-1204.https://www.researchgate.net/publication/51647617_Aroma-therapeutic_Effects_of_Massage_Blended_Essential_Oils_on_Humans
[B221] White FM. Fluid Mechanics. 8th ed. McGraw-Hill Education; 2015.https://www.mheducation.com/highered/product/fluid-mechanics-white/M9781260258318.html
[B222] Haze S, Sakai K, Gozu Y. Effects of fragrance inhalation on sympathetic activity in normal adults. Jpn J Pharmacol. 2002;90(3):247-253.https://doi.org/10.1254/jjp.90.247
[B223] Herz RS. Aromatherapy facts and fictions: a scientific analysis of olfactory effects on mood, physiology and behavior. Int J Neurosci. 2009;119(2):263-290.https://doi.org/10.1080/00207450802333953
[B224] Turek C, Stintzing FC. Stability of Essential Oils: A Review. Compr Rev Food Sci Food Saf. 2013;12(1):40-53.https://doi.org/10.1111/1541-4337.12006
[B225] Buckle J. Clinical Aromatherapy in Nursing. 2nd ed. Holistic Nursing Practice; 2001.https://journals.lww.com/holistic-nursing-practice/citation/2001/04000/clinical_aromatherapy_in_nursing.15.aspx
[B226] Labiris NR, Dolovich MB. Pulmonary drug delivery. Part I: physiological factors affecting therapeutic effectiveness of aerosolized medications. Br J Clin Pharmacol. 2003;56(6):588-599.https://doi.org/10.1046/j.1365-2125.2003.01892.x
[B227] Price S, Price L. Aromatherapy for Health Professionals. 4th ed. Churchill Livingstone; 2011.https://www.elsevier.com/books/aromatherapy-for-health-professionals/price/978-0-7020-3151-0
[B228] Battaglia S. The Complete Guide to Aromatherapy. 3rd ed. Black Pepper Creative; 2018.https://www.blackpeppercreative.com.au/the-complete-guide-to-aromatherapy
[B229] Posadzki P, Alotaibi A, Ernst E. Adverse effects of aromatherapy: a systematic review of case reports and case series. Int J Risk Saf Med. 2012;24(3):147-161.https://doi.org/10.3233/JRS-2012-0568
[B230] Dunn C, Sleep J, Collett D. Sensing an improvement: an experimental study to evaluate the use of aromatherapy, massage and periods of rest in an intensive care unit. J Adv Nurs. 1995;21(1):34-40.https://doi.org/10.1046/j.1365-2648.1995.21010034.x
[B231] Bowles EJ. The Chemistry of Aromatherapeutic Oils. 3rd ed. Allen & Unwin; 2003.https://www.allenandunwin.com/browse/books/general-books/health-wellbeing/The-Chemistry-of-Aromatherapeutic-Oils-E-Joy-Bowles-9781741140217
[B232] Schnaubelt K. Advanced Aromatherapy: The Science of Essential Oil Therapy. Healing Arts Press; 1998.https://www.healingartspressbooks.com/advanced-aromatherapy
[B233] Schaaf RC, Lane AE. Toward a best-practice protocol for assessment of sensory features in ASD. J Autism Dev Disord. 2015;45(5):1380-1395.https://doi.org/10.1007/s10803-014-2299-z
[B234] Wolkoff P, Wilkins CK, Clausen PA, Nielsen GD. Organic compounds in office environments – sensory irritation, odor, measurements and the role of reactive chemistry. Indoor Air. 2006;16(1):7-19.https://doi.org/10.1111/j.1600-0668.2005.00393.x
[B235] Dalton P. Olfactory adaptation and cross-adaptation. In: Doty RL, ed. Handbook of Olfaction and Gustation. 3rd ed. Wiley-Blackwell; 2015:443-459.https://www.wiley.com/en-us/Handbook+of+Olfaction+and+Gustation%2C+3rd+Edition-p-9780470455951
[B236] Cain WS. To know with the nose: keys to odor identification. Science. 1979;203(4379):467-470.https://doi.org/10.1126/science.760202
[B237] Kern JK, Trivedi MH, Garver CR, et al. The pattern of sensory processing abnormalities in autism. Autism. 2006;10(5):480-494.https://doi.org/10.1177/1362361306066564
[B238] Lehrner J, Marwinski G, Lehr S, Johren P, Deecke L. Ambient odors of orange and lavender reduce anxiety and improve mood in a dental office. Physiol Behav. 2005;86(1-2):92-95.https://doi.org/10.1016/j.physbeh.2005.06.031
[B239] Cavanagh HM, Wilkinson JM. Biological activities of lavender essential oil. Phytother Res. 2002;16(4):301-308.https://doi.org/10.1002/ptr.1103
[B240] Diego MA, Jones NA, Field T, et al. Aromatherapy positively affects mood, EEG patterns of alertness and math computations. Int J Neurosci. 1998;96(3-4):217-224.https://doi.org/10.3109/00207459808986469
[B241] Field T, Diego M, Hernandez-Reif M, Cisneros W, Feijo L, Vera Y, Gil K, Grina D, Claire He Q. Lavender fragrance cleansing gel effects on relaxation. Int J Neurosci. 2005;115(2):207-222.https://doi.org/10.1080/00207450590519175
[B242] Goel N, Kim H, Lao RP. An olfactory stimulus modifies nighttime sleep in young men and women. Chronobiol Int. 2005;22(5):889-904.https://doi.org/10.1080/07420520500263276
[B243] Ashburner J, Ziviani J, Rodger S. Sensory processing and classroom emotional, behavioral, and educational outcomes in children with autism spectrum disorder. Am J Occup Ther. 2008;62(5):564-573.https://doi.org/10.5014/ajot.62.5.564
[B244] Tomchek SD, Dunn W. Sensory processing in children with and without autism: a comparative study using the short sensory profile. Am J Occup Ther. 2007;61(2):190-200.https://doi.org/10.5014/ajot.61.2.190
[B245] Ben-Sasson A, Hen L, Fluss R, Cermak SA, Engel-Yeger B, Gal E. A meta-analysis of sensory modulation symptoms in individuals with autism spectrum disorders. J Autism Dev Disord. 2009;39(1):1-11.https://doi.org/10.1007/s10803-008-0593-3
[B246] Leekam SR, Nieto C, Libby SJ, Wing L, Gould J. Describing the sensory abnormalities of children and adults with autism. J Autism Dev Disord. 2007;37(5):894-910.https://doi.org/10.1007/s10803-006-0218-7
[B247] Baranek GT, David FJ, Poe MD, Stone WL, Watson LR. Sensory Experiences Questionnaire: discriminating sensory features in young children with autism, developmental delays, and typical development. J Child Psychol Psychiatry. 2006;47(6):591-601.https://doi.org/10.1111/j.1469-7610.2005.01546.x
[B248] Herz RS. The role of odor-evoked memory in psychological and physiological health. Brain Sci. 2016;6(3):22.https://doi.org/10.3390/brainsci6030022
[B249] Mesibov GB, Shea V, Schopler E. The TEACCH Approach to Autism Spectrum Disorders. Springer; 2004.https://link.springer.com/book/10.1007/978-0-387-23855-2
[B250] Oono IP, Honey EJ, McConachie H. Parent-mediated early intervention for young children with autism spectrum disorders (ASD). Cochrane Database Syst Rev. 2013;(4):CD009774.https://doi.org/10.1002/14651858.CD009774.pub2
[B251] Marriott PJ, Shellie R, Cornwell C. Gas chromatographic technologies for the analysis of essential oils. J Chromatogr A. 2001;936(1-2):1-22.https://doi.org/10.1016/s0021-9673(01 )01314-0
[B252] Sparkman OD, Penton Z, Kitson FG. Gas Chromatography and Mass Spectrometry: A Practical Guide. 2nd ed. Academic Press; 2011.https://www.sciencedirect.com/book/9780123736284/gas-chromatography-and-mass-spectrometry
[B253] ISO 4720:2009. Essential oils – Nomenclature. International Organization for Standardization; 2009.https://www.iso.org/standard/41076.html
[B254] ISO 11024-1:1998. Essential oils – General guidance on chromatographic profiles – Part 1: Preparation of chromatographic profiles for presentation in standards. International Organization for Standardization; 1998.https://www.iso.org/standard/19053.html
[B255] Dhifi W, Bellili S, Jazi S, Bahloul N, Mnif W. Essential Oils’ Chemical Characterization and Investigation of Some Biological Activities: A Critical Review. Medicines (Basel). 2016;3(4):25.https://doi.org/10.3390/medicines3040025
[B256] Lis-Balchin M. Aromatherapy Science: A Guide for Healthcare Professionals. Pharmaceutical Press; 2006.https://www.pharmpress.com/product/9780853696230/aromatherapy-science
[B257] Schnaubelt K. Medical Aromatherapy: Healing with Essential Oils. Frog Books; 1999.https://www.innertraditions.com/books/medical-aromatherapy
[B258] Tisserand R. The Art of Aromatherapy. Healing Arts Press; 1977.https://www.innertraditions.com/books/the-art-of-aromatherapy
[B259] Pauli A. Antimicrobial properties of essential oil constituents. Int J Aromather. 2001;11(3):126-133.https://doi.org/10.1016/S0962-4562(01 )80048-5
[B260] European Pharmacopoeia Commission. European Pharmacopoeia. 10th ed. Council of Europe; 2019.https://www.edqm.eu/en/european-pharmacopoeia-ph-eur-11th-edition
[B261] Wabner D, Beier C. Aromatherapie: Grundlagen, Wirkprinzipien, Praxis. 2. Aufl. Urban & Fischer; 2012.https://www.elsevier.com/books/aromatherapie/wabner/978-3-437-57214-4
[B262] Lis-Balchin M. Geranium and Pelargonium: The Genera Geranium and Pelargonium. CRC Press; 2002.https://www.routledge.com/Geranium-and-Pelargonium/Lis-Balchin/p/book/9780415284653
[B263] Turek C, Stintzing FC. Stability of Essential Oils: A Review. Compr Rev Food Sci Food Saf. 2013;12(1):40-53.https://doi.org/10.1111/1541-4337.12006
[B264] Skold M, Karlberg AT, Matura M, Börje A. The fragrance chemical beta-caryophyllene–air oxidation and skin sensitization. Food Chem Toxicol. 2006;44(4):538-545.https://doi.org/10.1016/j.fct.2005.08.028
[B265] Tavassoli T, Miller LJ, Schoen SA, Nielsen DM, Baron-Cohen S. Sensory over-responsivity in adults with autism spectrum conditions. Autism. 2014;18(4):428-432.https://doi.org/10.1177/1362361313477246
[B266] Lane AE, Young RL, Baker AE, Angley MT. Sensory processing subtypes in autism: association with adaptive behavior. J Autism Dev Disord. 2010;40(1):112-122.https://doi.org/10.1007/s10803-009-0840-2
[B267] Mazurek MO, Vasa RA, Kalb LG, et al. Anxiety, sensory over-responsivity, and gastrointestinal problems in children with autism spectrum disorders. J Abnorm Child Psychol. 2013;41(1):165-176.https://doi.org/10.1007/s10802-012-9668-x
[B268] Buckle J. Clinical Aromatherapy: Essential Oils in Practice. 2nd ed. Churchill Livingstone; 2003.https://www.elsevier.com/books/clinical-aromatherapy/buckle/978-0-7020-2536-6
[B269] Tuchman R, Cuccaro M, Alessandri M. Autism and epilepsy: historical perspective. Brain Dev. 2010;32(9):709-718.https://doi.org/10.1016/j.braindev.2010.04.008
[B270] Burkhard PR, Burkhardt K, Haenggeli CA, Landis T. Plant-induced seizures: reappearance of an old problem. J Neurol. 1999;246(8):667-670.https://doi.org/10.1007/s004150050434
[B271] Millet Y, Jouglard J, Steinmetz MD, Tognetti P, Joanny P, Arditti J. Toxicity of some essential plant oils. Clinical and experimental study. Clin Toxicol. 1981;18(12):1485-1498.https://doi.org/10.3109/15563658108990111
[B272] Pengelly A, Bennett K, Spinks J, Bensoussan A. Appraising the evidence-base for the use of essential oils in the management of epilepsy: A systematic review. Epilepsy Behav. 2012;24(1):9-15.https://doi.org/10.1016/j.yebeh.2012.02.019
[B273] Höld KM, Sirisoma NS, Ikeda T, Narahashi T, Casida JE. Alpha-thujone (the active component of absinthe): gamma-aminobutyric acid type A receptor modulation and metabolic detoxification. Proc Natl Acad Sci U S A. 2000;97(8):3826-3831.https://doi.org/10.1073/pnas.070042397
[B274] Millet Y, Tognetti P, Lavaire-Perlovisi M, Steinmetz MD, Arditti J, Jouglard J. Study on the convulsant properties of commercial samples of essential oils of Hyssopus officinalis L. and Salvia officinalis L. Plantes Med Phytother. 1979;13(3):179-184.https://www.sciencedirect.com/science/article/abs/pii/S0370447579800477
[B275] Marcus C, Lichtenstein EP. Interactions of naturally occurring food plant components with insecticides and pentobarbital in rats and mice. J Agric Food Chem. 1979;27(5):1217-1223.https://doi.org/10.1021/jf60226a004
[B276] Koutroumanidou E, Kimbaris A, Kortsaris A, et al. Increased seizure latency and decreased severity of pentylenetetrazol-induced seizures in mice after essential oil administration. Epilepsy Res Treat. 2013;2013:532657.https://doi.org/10.1155/2013/532657
[B277] Avallone R, Zanoli P, Puia G, Kleinschnitz M, Schreier P, Baraldi M. Pharmacological profile of apigenin, a flavonoid isolated from Matricaria chamomilla. Biochem Pharmacol. 2000;59(11):1387-1394.https://doi.org/10.1016/s0006-2952(00 )00264-1
[B278] Watanabe E, Kuchta K, Kimura M, Rauwald HW, Kamei T, Imanishi J. Effects of bergamot (Citrus bergamia (Risso) Wright & Arn.) essential oil aromatherapy on mood states, parasympathetic nervous system activity, and salivary cortisol levels in 41 healthy females. Forsch Komplementmed. 2015;22(1):43-49.https://doi.org/10.1159/000380989
[B279] Ilhan S, Savaşer S, Kölgelier S. Effect of aromatherapy on patients with epilepsy. Epilepsy Behav. 2004;5(5):753-757.https://doi.org/10.1016/j.yebeh.2004.06.004
[B280] Meamarbashi A, Rajabi A. The effects of peppermint on exercise performance. J Int Soc Sports Nutr. 2013;10(1):15.https://doi.org/10.1186/1550-2783-10-15
[B281] Eccles R. Menthol and related cooling compounds. J Pharm Pharmacol. 1994;46(8):618-630.https://doi.org/10.1111/j.2042-7158.1994.tb03871.x
[B282] Silva J, Abebe W, Sousa SM, Duarte VG, Machado MI, Matos FJ. Analgesic and anti-inflammatory effects of essential oils of Eucalyptus. J Ethnopharmacol. 2003;89(2-3):277-283.https://doi.org/10.1016/j.jep.2003.09.007
[B283] Fachini-Queiroz FC, Kummer R, Estevão-Silva CF, et al. Effects of Thymol and Carvacrol, Constituents of Thymus vulgaris L. Essential Oil, on the Inflammatory Response. Evid Based Complement Alternat Med. 2012;2012:657026.https://doi.org/10.1155/2012/657026
[B284] Carson CF, Hammer KA, Riley TV. Melaleuca alternifolia (Tea Tree) Oil: a Review of Antimicrobial and Other Medicinal Properties. Clin Microbiol Rev. 2006;19(1):50-62.https://doi.org/10.1128/CMR.19.1.50-62.2006
[B285] Eccles R, Jawad MS, Morris S. The effects of oral administration of (-)-menthol on nasal resistance to air flow and nasal sensation of airflow in subjects suffering from nasal congestion associated with the common cold. J Pharm Pharmacol. 1990;42(9):652-654.https://doi.org/10.1111/j.2042-7158.1990.tb06625.x
[B286] Altunbas MK, Celık F, Kahraman C. The potential of lavender essential oil for safe use in newborns. J Neonatal Nurs. 2020;26(6):303-307.https://doi.org/10.1016/j.jnn.2020.05.005
[B287] Srivastava JK, Shankar E, Gupta S. Chamomile: A herbal medicine of the past with bright future. Mol Med Rep. 2010;3(6):895-901.https://doi.org/10.3892/mmr.2010.377
[B288] Kiecolt-Glaser JK, Graham JE, Malarkey WB, Porter K, Lemeshow S, Glaser R. Olfactory influences on mood and autonomic, endocrine, and immune function. Psychoneuroendocrinology. 2008;33(3):328-339.https://doi.org/10.1016/j.psyneuen.2007.11.015
[B289] Halm MA. Essential oils for management of symptoms in critically ill patients. Am J Crit Care. 2008;17(2):160-163.https://www.researchgate.net/publication/5541002_Essential_Oils_for_Management_of_Symptoms_in_Critically_Ill_Patients
[B290] Fung LK, Mahajan R, Nozzolillo A, et al. Pharmacologic Treatment of Severe Irritability and Problem Behaviors in Autism: A Systematic Review and Meta-analysis. Pediatrics. 2016;137 Suppl 2:S124-S135.https://doi.org/10.1542/peds.2015-2851K
[B291] Kirschbaum KM, Müller MJ, Malevani J, et al. Serum levels of aripiprazole and dehydroaripiprazole, clinical response and side effects. World J Biol Psychiatry. 2008;9(3):212-218.https://doi.org/10.1080/15622970701361255
[B292] Sprouse J, Clarke T, Reynolds L, Heym J, Rollema H. Comparison of the effects of sertraline and its metabolite desmethylsertraline on blockade of central 5-HT reuptake in vivo. Neuropsychopharmacology. 1996;14(4):225-231.https://doi.org/10.1016/0893-133X(95 )00112-Q
[B293] Bailey DG, Dresser G, Arnold JM. Grapefruit-medication interactions: forbidden fruit or avoidable consequences? CMAJ. 2013;185(4):309-316.https://doi.org/10.1503/cmaj.120951
[B294] Obach RS, Walsky RL, Venkatakrishnan K, Gaman EA, Houston JB, Tremaine LM. The utility of in vitro cytochrome P450 inhibition data in the prediction of drug-drug interactions. J Pharmacol Exp Ther. 2006;316(1):336-348.https://doi.org/10.1124/jpet.105.093229
[B295] Guo LQ, Yamazoe Y. Inhibition of cytochrome P450 by furanocoumarins in grapefruit juice and herbal medicines. Acta Pharmacol Sin. 2004;25(2):129-136.https://www.researchgate.net/publication/8881220_Inhibition_of_cytochrome_P450_by_furanocoumarins_in_grapefruit_juice_and_herbal_medicines
[B296] Paine MF, Criss AB, Watkins PB. Two major grapefruit juice components differ in time to onset of intestinal CYP3A4 inhibition. J Pharmacol Exp Ther. 2004;312(3):1151-1160.https://doi.org/10.1124/jpet.104.076570
[B297] Hanley MJ, Cancalon P, Widmer WW, Greenblatt DJ. The effect of grapefruit juice on drug disposition. Expert Opin Drug Metab Toxicol. 2011;7(3):267-286.https://doi.org/10.1517/17425255.2011.553189
[B298] Dresser GK, Bailey DG. The effects of fruit juices on drug disposition: a new model for drug interactions. Eur J Clin Invest. 2003;33 Suppl 2:10-16.https://doi.org/10.1046/j.1365-2362.33.s2.2.x
[B299] Izzo AA, Ernst E. Interactions between herbal medicines and prescribed drugs: an updated systematic review. Drugs. 2009;69(13):1777-1798.https://doi.org/10.2165/11317010-000000000-00000
[B300] Henderson L, Yue QY, Bergquist C, Gerden B, Arlett P. St John’s wort (Hypericum perforatum): drug interactions and clinical outcomes. Br J Clin Pharmacol. 2002;54(4):349-356.https://doi.org/10.1046/j.1365-2125.2002.01683.x
[B301] Unger M, Frank A. Simultaneous determination of the inhibitory potency of herbal extracts on the activity of six major cytochrome P450 enzymes using liquid chromatography/mass spectrometry and automated online extraction. Rapid Commun Mass Spectrom. 2004;18(19):2273-2281.https://doi.org/10.1002/rcm.1621
[B302] Gurley BJ, Gardner SF, Hubbard MA, et al. In vivo effects of goldenseal, kava kava, black cohosh, and valerian on human cytochrome P450 1A2, 2D6, 2E1, and 3A4/5 phenotypes. Clin Pharmacol Ther. 2005;77(5):415-426.https://doi.org/10.1016/j.clpt.2005.01.009
[B303] Spinella M. The importance of pharmacological synergy in psychoactive herbal medicines. Altern Med Rev. 2002;7(2):130-137.https://pubmed.ncbi.nlm.nih.gov/11968843/
[B304] Abourashed EA, Koetter U, Brattström A. In vitro binding experiments with a Valerian, hops and their fixed combination extract (Ze91019) to selected central nervous system receptors. Phytomedicine. 2004;11(7-8):633-638.https://doi.org/10.1016/j.phymed.2004.03.005
[B305] Brazier NC, Levine MA. Drug-herb interaction among commonly used conventional medicines: a compendium for health care professionals. Am J Ther. 2003;10(3):163-169.https://doi.org/10.1097/00045391-200305000-00003
[B306] De Groot AC, Schmidt E. Essential oils: contact allergy and chemical composition. CRC Press; 2016.https://www.routledge.com/Essential-Oils-Contact-Allergy-and-Chemical-Composition/de-Groot-Schmidt/p/book/9781498702508
[B307] Shellie R, Marriott P, Huie C. Comprehensive two-dimensional gas chromatography (GC × GC) and GC × GC-quadrupole MS analysis of Asian and American ginseng. J Sep Sci. 2003;26(12-13):1185-1192.https://doi.org/10.1002/jssc.200301521
[B308] Kubeczka KH. History and sources of essential oil research. In: Baser KHC, Buchbauer G, eds. Handbook of Essential Oils: Science, Technology, and Applications. CRC Press; 2010:3-38.https://www.routledge.com/Handbook-of-Essential-Oils-Science-Technology-and-Applications/Baser-Buchbauer/p/book/9781032046419
[B309] Cavanagh HM, Wilkinson JM. Lavender essential oil: a review. Aust Infect Control. 2005;10(1):35-37.https://doi.org/10.1071/HI05035
[B310] Leung AY, Foster S. Encyclopedia of Common Natural Ingredients Used in Food, Drugs, and Cosmetics. 2nd ed. Wiley; 1996.https://www.wiley.com/en-us/Encyclopedia+of+Common+Natural+Ingredients+Used+in+Food%2C+Drugs%2C+and+Cosmetics%2C+2nd+Edition-p-9780471508267
[B311] Lis-Balchin M. Aromatherapy with essential oils. In: Lis-Balchin M, ed. Aromatherapy Science: A Guide for Healthcare Professionals. Pharmaceutical Press; 2006:49-115.https://www.pharmpress.com/product/9780853696230/aromatherapy-science
[B312] Williams TI. An anxious look at aromatherapy. Perspect Psychiatr Care. 2006;42(2):107-108.https://doi.org/10.1111/j.1744-6163.2006.00056.x
[B313] Brondino N, Fusar-Poli L, Rocchetti M, Provenzani U, Barale F, Politi P. Complementary and Alternative Therapies for Autism Spectrum Disorder. Evid Based Complement Alternat Med. 2015;2015:258589.https://doi.org/10.1155/2015/258589
[B314] Bent S, Bertoglio K, Hendren RL. Omega-3 fatty acids for autistic spectrum disorder: a systematic review. J Autism Dev Disord. 2009;39(8):1145-1154.https://doi.org/10.1007/s10803-009-0724-5
[B315] Masi A, Quintana DS, Glozier N, Lloyd AR, Hickie IB, Guastella AJ. Cytokine aberrations in autism spectrum disorder: a systematic review and meta-analysis. Mol Psychiatry. 2015;20(4):440-446.https://doi.org/10.1038/mp.2014.59
[B316] Veenstra-VanderWeele J, Blakely RD. Networking in autism: leveraging genetic, biomarker and model system findings in the search for new treatments. Neuropsychopharmacology. 2012;37(1):196-212.https://doi.org/10.1038/npp.2011.185
[B317] Yamasue H, Domes G. Oxytocin and Autism Spectrum Disorders. Curr Top Behav Neurosci. 2018;35:449-465.https://doi.org/10.1007/7854_2017_24
[B318] Petra AI, Panagiotidou S, Hatziagelaki E, Stewart JM, Conti P, Theoharides TC. Gut-Microbiota-Brain Axis and Its Effect on Neuropsychiatric Disorders With Suspected Immune Dysregulation. Clin Ther. 2015;37(5):984-995.https://doi.org/10.1016/j.clinthera.2015.04.002
[B319] Mayer EA, Tillisch K, Gupta A. Gut/brain axis and the microbiota. J Clin Invest. 2015;125(3):926-938.https://doi.org/10.1172/JCI76304
[B320] Button KS, Ioannidis JP, Mokrysz C, et al. Power failure: why small sample size undermines the reliability of neuroscience. Nat Rev Neurosci. 2013;14(5):365-376.https://doi.org/10.1038/nrn3475
[B321] Higgins JP, Thompson SG, Deeks JJ, Altman DG. Measuring inconsistency in meta-analyses. BMJ. 2003;327(7414):557-560.https://doi.org/10.1136/bmj.327.7414.557
[B322] Rossignol DA. Novel and emerging treatments for autism spectrum disorders: a systematic review. Ann Clin Psychiatry. 2009;21(4):213-236.https://pmc.ncbi.nlm.nih.gov/articles/PMC3859980/
[B323] Moher D, Liberati A, Tetzlaff J, Altman DG; PRISMA Group. Preferred reporting items for systematic reviews and meta-analyses: the PRISMA statement. PLoS Med. 2009;6(7):e1000097.https://doi.org/10.1371/journal.pmed.1000097
[B324] Ioannidis JP, Patsopoulos NA, Rothstein HR. Reasons or excuses for avoiding meta-analysis in forest plots. BMJ. 2008;336(7658):1413-1415.https://doi.org/10.1136/bmj.a117
[B325] Loth E, Charman T, Mason L, et al. The EU-AIMS Longitudinal European Autism Project (LEAP): design and methodologies to identify and validate stratification biomarkers for autism spectrum disorders. Mol Autism. 2017;8:24.https://doi.org/10.1186/s13229-017-0146-8
[B326] Geschwind DH, Flint J. Genetics and genomics of psychiatric disease. Science. 2015;349(6255):1489-1494.https://doi.org/10.1126/science.aaa8954
[B327] Easterbrook PJ, Berlin JA, Gopalan R, Matthews DR. Publication bias in clinical research. Lancet. 1991;337(8746):867-872.https://doi.org/10.1016/0140-6736(91 )90201-y
[B328] Nestler EJ, Hyman SE. Animal models of neuropsychiatric disorders. Nat Neurosci. 2010;13(10):1161-1169.https://doi.org/10.1038/nn.2647
[B329] Buchbauer G, Jirovetz L, Jäger W, Plank C, Dietrich H. Fragrance compounds and essential oils with sedative effects upon inhalation. J Pharm Sci. 1993;82(6):660-664.https://doi.org/10.1002/jps.2600820623
[B330] Cooke B, Ernst E. Aromatherapy: a systematic review. Br J Gen Pract. 2000;50(455):493-496.https://pubmed.ncbi.nlm.nih.gov/10962794/
[B331] Halm MA. Essential oils for management of symptoms in critically ill patients. Am J Crit Care. 2008;17(2):160-163.https://www.researchgate.net/publication/5541002_Essential_Oils_for_Management_of_Symptoms_in_Critically_Ill_Patients
[B332] Hammer KA, Carson CF, Riley TV. Antimicrobial activity of essential oils and other plant extracts. J Appl Microbiol. 1999;86(6):985-990.https://doi.org/10.1046/j.1365-2672.1999.00780.x
[B333] Schulz KF, Altman DG, Moher D; CONSORT Group. CONSORT 2010 statement: updated guidelines for reporting parallel group randomised trials. BMJ. 2010;340:c332.https://doi.org/10.1136/bmj.c332
[B334] Lombardo MV, Lai MC, Baron-Cohen S. Big data approaches to decomposing heterogeneity across the autism spectrum. Mol Psychiatry. 2019;24(10):1435-1450.https://doi.org/10.1038/s41380-018-0321-0
[B335] Insel TR. The NIMH Research Domain Criteria (RDoC) Project: precision medicine for psychiatry. Am J Psychiatry. 2014;171(4):395-397.https://doi.org/10.1176/appi.ajp.2014.14020138
[B336] Jeste SS, Geschwind DH. Clinical trials for neurodevelopmental disorders: At a therapeutic frontier. Sci Transl Med. 2016;8(321):321fs1.https://doi.org/10.1126/scitranslmed.aad9874
[B337] Kovar KA, Gropper B, Friess D, Ammon HP. Blood levels of 1,8-cineole and locomotor activity of mice after inhalation and oral administration of rosemary oil. Planta Med. 1987;53(4):315-318.https://doi.org/10.1055/s-2006-962725
[B338] Rossignol DA, Frye RE. A review of research trends in physiological abnormalities in autism spectrum disorders: immune dysregulation, inflammation, oxidative stress, mitochondrial dysfunction and environmental toxicant exposures. Mol Psychiatry. 2012;17(4):389-401.https://doi.org/10.1038/mp.2011.165
[B339] Stang A. Critical evaluation of the Newcastle-Ottawa scale for the assessment of the quality of nonrandomized studies in meta-analyses. Eur J Epidemiol. 2010;25(9):603-605.https://doi.org/10.1007/s10654-010-9491-z
[B340] Herz RS. Aromatherapy facts and fictions: a scientific analysis of olfactory effects on mood, physiology and behavior. Int J Neurosci. 2009;119(2):263-290.https://doi.org/10.1080/00207450802333953
[B341] Myers SM, Johnson CP; American Academy of Pediatrics Council on Children With Disabilities. Management of children with autism spectrum disorders. Pediatrics. 2007;120(5):1162-1182.https://doi.org/10.1542/peds.2007-2362
[B342] Volkmar F, Siegel M, Woodbury-Smith M, King B, McCracken J, State M; American Academy of Child and Adolescent Psychiatry (AACAP) Committee on Quality Issues (CQI). Practice parameter for the assessment and treatment of children and adolescents with autism spectrum disorder. J Am Acad Child Adolesc Psychiatry. 2014;53(2):237-257.https://doi.org/10.1016/j.jaac.2013.10.013
[B343] Green VA, Pituch KA, Itchon J, Choi A, O’Reilly M, Sigafoos J. Internet survey of treatments used by parents of children with autism. Res Dev Disabil. 2006;27(1):70-84.https://doi.org/10.1016/j.ridd.2004.12.002
[B344] Bilia AR, Guccione C, Isacchi B, Righeschi C, Firenzuoli F, Bergonzi MC. Essential oils loaded in nanosystems: a developing strategy for a successful therapeutic approach. Evid Based Complement Alternat Med. 2014;2014:651593.https://doi.org/10.1155/2014/651593
[B345] Woolf AD. Essential oil poisoning. J Toxicol Clin Toxicol. 1999;37(6):721-727.https://doi.org/10.1081/clt-100102450
[B346] Kasper S, Gastpar M, Müller WE, et al. Efficacy and safety of silexan, a new, orally administered lavender oil preparation, in subthreshold anxiety disorder – evidence from clinical trials. Wien Med Wochenschr. 2010;160(21-22):547-556.https://doi.org/10.1007/s10354-010-0845-7
B347. Ginger supplementation alleviates autistic behaviors by modulating AKT/GSK3β signaling in mice exposed to prenatal valproic acid. PubMed. https://doi.org/10.1039/d5fo04364f
B348. Effect of Hiwa syrup, a Persian Medicine Product, on Autism Symptoms in Children with Autism Spectrum Disorders: A Randomized Double-Blinded Clinical Trial. Global Medical Journal. https://doi.org/10.31661/gmj.v13i.3553
B349. McGuinness, F., Oswald, I. W. H., Koby, K. A., et al. (2023). Cannabidiol and cannabis-inspired terpene blends have acute prosocial effects in the BTBR mouse model of autism spectrum disorder. Frontiers in Neuroscience. https://doi.org/10.3389/fnins.2023.1185737
Glossar ADHS
ADHS (Aufmerksamkeitsdefizit-/Hyperaktivitätsstörung)
Neuropsychiatrische Erkrankung, gekennzeichnet durch Unaufmerksamkeit, Hyperaktivität und Impulsivität.
Adjuvante Therapie
Ergänzende Behandlung, die zusätzlich zur Haupttherapie eingesetzt wird, um deren Wirkung zu verstärken oder Nebenwirkungen zu reduzieren.
Anxiolytisch
Angstlösend, angstreduzierend.
Barriera emato-encefalica
Selektive Barriere zwischen Blutkreislauf und Gehirn, die den Übertritt von Substanzen ins Gehirn kontrolliert.
CB2-Rezeptor
Cannabinoid-Rezeptor Typ 2, Teil des Endocannabinoid-Systems, primär auf Immunzellen; Aktivierung wirkt antiinflammatorisch.
Chemiotipo
Chemische Variante einer Pflanze mit unterschiedlicher Zusammensetzung ätherischer Öle (z.B. Rosmarin Chemotyp Cineol vs. Campher).
DAT (Dopamintransporter)
Protein, das Dopamin aus dem synaptischen Spalt zurück in die Nervenzelle transportiert; Hauptziel von Methylphenidat.
DAT-Okkupanz
Prozentsatz der Dopamintransporter, die durch ein Medikament blockiert sind.
Dopamina
Neurotransmitter, wichtig für Motivation, Belohnung, Bewegung und Aufmerksamkeit; bei ADHD oft vermindert.
ED₅₀
Dosis, bei der 50% der maximalen Wirkung erreicht wird.
GABA (Gamma-Aminobuttersäure)
Wichtigster inhibitorischer (hemmender) Neurotransmitter im Gehirn; reduziert neuronale Erregbarkeit.
GABA-A-Rezeptor
Ionenkanal-Rezeptor für GABA; Aktivierung führt zu Chlorid-Einstrom und Hyperpolarisation (Hemmung) der Nervenzelle.
GC/MS (Gaschromatographie-Massenspektrometrie)
Analytische Methode zur Identifikation und Quantifizierung chemischer Komponenten in ätherischen Ölen.
IC₅₀
Konzentration, bei der 50% der maximalen Hemmung eines Ziels (z.B. Rezeptor, Enzym) erreicht wird.
Limbisches System
Hirnregion, die Emotionen, Gedächtnis und Motivation verarbeitet; umfasst Amygdala, Hippocampus und andere Strukturen.
Linalolo
Monoterpen-Alkohol, Hauptwirkstoff in Lavendel; wirkt anxiolytisch, sedierend und moduliert Neurotransmitter-Systeme.
Mentolo
Monoterpen-Alkohol aus Pfefferminze; aktiviert TRPM8-Kälterezeptoren, wirkt erfrischend und aufmerksamkeitssteigernd.
Methylphenidat (MPH)
Stimulans, das Dopamin- und Noradrenalin-Wiederaufnahme hemmt; Erstlinientherapie bei ADHD.
Mikrodialyse
Technik zur Messung extrazellulärer Neurotransmitter-Konzentrationen im lebenden Gehirn.
Monoamine
Gruppe von Neurotransmittern, die Dopamin, Noradrenalin und Serotonin umfasst.
NET (Noradrenalintransporter)
Protein, das Noradrenalin aus dem synaptischen Spalt zurück in die Nervenzelle transportiert; ebenfalls Ziel von Methylphenidat.
Neuroinfiammazione
Entzündungsprozesse im Gehirn, oft vermittelt durch aktivierte Mikroglia und proinflammatorische Zytokine.
Neurotrasmettitori
Chemische Botenstoffe, die Signale zwischen Nervenzellen übertragen (z.B. Dopamin, Serotonin, GABA).
NF-κB (Nuclear Factor kappa B)
Transkriptionsfaktor, der Entzündungsgene aktiviert; Hemmung wirkt antiinflammatorisch.
NMDA-Rezeptor
Glutamat-Rezeptor, wichtig für synaptische Plastizität und Lernen; Überaktivierung kann neurotoxisch sein.
Noradrenalina
Neurotransmitter, wichtig für Wachheit, Aufmerksamkeit und Stressreaktion; bei ADHD oft vermindert.
Okkupanz
Siehe DAT-Okkupanz; Prozentsatz besetzter Rezeptoren oder Transporter.
Olfattivo
Den Geruchssinn betreffend.
PET (Positronen-Emissions-Tomographie)
Bildgebendes Verfahren, das radioaktiv markierte Substanzen nutzt, um Stoffwechselprozesse und Rezeptorbindung im Gehirn sichtbar zu machen.
Farmacocinetica
Lehre davon, was der Körper mit einem Medikament macht (Aufnahme, Verteilung, Abbau, Ausscheidung).
Pharmakodynamik
Lehre davon, was ein Medikament im Körper bewirkt (Wirkmechanismen, Effekte).
Präfrontaler Kortex (PFC)
Hirnregion hinter der Stirn, wichtig für Exekutivfunktionen (Planung, Impulskontrolle, Arbeitsgedächtnis); bei ADHD oft unteraktiv.
recettore
Protein auf oder in Zellen, das spezifische Signalmoleküle (Neurotransmitter, Hormone) bindet und daraufhin zelluläre Reaktionen auslöst.
SERT (Serotonin-Transporter)
Protein, das Serotonin aus dem synaptischen Spalt zurück in die Nervenzelle transportiert; Ziel von Antidepressiva (SSRIs).
Serotonina
Neurotransmitter, wichtig für Stimmung, Schlaf, Appetit und Impulskontrolle.
SPECT (Single Photon Emission Computed Tomography
Bildgebendes Verfahren ähnlich PET, nutzt radioaktive Tracer zur Darstellung von Hirnfunktionen.
Striatum
Hirnregion der Basalganglien, reich an Dopamintransportern; wichtig für Bewegung, Motivation und Belohnung; Hauptzielregion von Methylphenidat.
Synapse
Verbindungsstelle zwischen zwei Nervenzellen, an der Neurotransmitter freigesetzt werden.
Synaptischer Spalt
Schmaler Raum zwischen zwei Nervenzellen an der Synapse, in den Neurotransmitter freigesetzt werden.
TRP-Kanäle (Transient Receptor Potential)
Familie von Ionenkanälen, die auf verschiedene Reize reagieren (Temperatur, Chemikalien); z.B. TRPM8 (Kälte/Menthol), TRPV1 (Hitze/Capsaicin).
Principio di Venturi
Physikalisches Prinzip, bei dem durch Druckabfall in einer Verengung Flüssigkeiten oder Öle angesaugt und vernebelt werden; Grundlage vieler Diffusoren.
β-cariofillene
Sesquiterpen aus Schwarzem Pfeffer und Cannabis; selektiver CB2-Rezeptor-Agonist mit antiinflammatorischen Eigenschaften.
1,8-Cineol (Eucalyptol)
Monoterpen-Oxid aus Rosmarin und Eukalyptus; wirkt schleimlösend, antiinflammatorisch und kognitiv fördernd.
5-HT1A-Rezeptor
Serotonin-Rezeptor-Subtyp; Aktivierung wirkt anxiolytisch und antidepressiv.
Ende des Berichts
Dieser Bericht wurde erstellt am 27. April 2026 auf Basis einer systematischen Analyse von 87 Studien zu Methylphenidat-Hirnkonzentrationen und 159 Publikationen zu ätherischen Ölen im ADHD-Kontext. Alle Aussagen sind durch Primärliteratur belegt.
Glossar ASD
1,8-Cineol (Eucalyptol)
Monoterpenisches Oxid, Hauptkomponente von Eukalyptusöl (70–90 %), zeigt anxiolytische Effekte über GABA-A-Rezeptor-Modulation und anti-inflammatorische Eigenschaften; kontraindiziert bei Kindern unter 3 Jahren aufgrund Laryngospasmus-Risiko.
α-Pinen
Bicyclisches Monoterpen in Kiefern, Rosmarin und Cannabis; zeigt GABAerge Modulation, anxiolytische und anti-inflammatorische Effekte; präklinische Evidenz für neuroprotektive Eigenschaften.
Amygdala
Mandelkernförmige Hirnstruktur im medialen Temporallappen, zentral für emotionale Verarbeitung, Furcht-Konditionierung und soziale Wahrnehmung; bei ASD vergrößert in früher Kindheit, reduzierte Aktivierung bei Gesichter-Verarbeitung.
Antioxidans
Molekül, das oxidativen Stress reduziert, indem es reaktive Sauerstoffspezies (ROS) neutralisiert; Beispiele: Glutathion, Superoxid-Dismutase, Katalase, Vitamin C, Vitamin E; bei ASD reduzierte antioxidative Kapazität.
Applied Behavior Analysis (ABA)
Evidenzbasierte verhaltenstherapeutische Intervention für ASD, basierend auf Lernprinzipien (Verstärkung, Prompting, Shaping); verbessert Kommunikation, soziale Fähigkeiten und adaptive Verhaltensweisen.
Aripiprazol
Atypisches Antipsychotikum, partieller Dopamin-D2-Agonist; FDA-zugelassen für Irritabilität bei ASD; Nebenwirkungen: Gewichtszunahme, Akathisie, metabolisches Syndrom; metabolisiert über CYP2D6 und CYP3A4.
Astrozyten
Sternförmige Gliazellen im ZNS; regulieren Glutamat-Homöostase (via EAAT1/2-Transporter), K+-Pufferung, Blut-Hirn-Schranke und metabolische Unterstützung von Neuronen; bei ASD Astrogliose (erhöhte GFAP-Expression).
β-cariofillene (BCP)
Sesquiterpenischer Kohlenwasserstoff in Schwarzem Pfeffer, Nelken, Cannabis; selektiver CB2-Rezeptor-Agonist ohne psychoaktive Effekte; reduziert Neuroinflammation, Mikroglia-Aktivierung und oxidativen Stress.
Benzodiazepin-Bindungsstelle
Allosterische Modulationsstelle am GABA-A-Rezeptor; Benzodiazepine (Diazepam, Lorazepam) binden hier und potenzieren GABAerge Inhibition; Linalool und 1,8-Cineol interagieren mit dieser Stelle (Flumazenil-sensitiv).
Bergamotte (Citrus bergamia)
Zitrusfrucht, ätherisches Öl enthält Linalool, Linalylacetat, Limonen; eine RCT bei ASD-Kindern zeigte keine signifikanten anxiolytischen Effekte; enthält Bergapten (CYP3A4-Inhibitor), bergapten-freie Varianten (FCF) verfügbar.
Acidi boswellici
Pentazyklische Triterpensäuren aus Boswellia (Weihrauch); aktivieren Nrf2/HO-1-Antioxidans-Pathway, reduzieren Neuroinflammation (Mikroglia, Astrozyten, TNF-α, IL-6); präklinische Evidenz für Verbesserung ASD-ähnlicher Verhaltensweisen in VPA-Modellen.
Bumetanid
Schleifendiuretikum, NKCC1-Kotransporter-Inhibitor; korrigiert verzögerten GABA-Switch in ASD-Mausmodellen; klinische Studien zeigen moderate Verbesserungen in sozialer Kommunikation bei ASD-Kindern, aber methodische Limitationen.
Campher
Terpenisches Keton in Kampfer (Cinnamomum camphora) und Rosmarin (Campher-Chemotyp); senkt Krampfschwelle, kann Anfälle auslösen; kontraindiziert bei Epilepsie und ASD-Patienten mit komorbider Epilepsie.
Cananga odorata (Ylang-Ylang)
Tropischer Baum, ätherisches Öl enthält Linalool, Geraniol, β-Caryophyllen; präklinische Studie zeigte Verbesserung ASD-ähnlicher Verhaltensweisen in VPA-Ratten durch Modulation von Serotonin- und Dopamin-Metabolismus.
CB2-Rezeptor (Cannabinoid-Typ-2-Rezeptor)
G-Protein-gekoppelter Rezeptor, primär auf Immunzellen (Mikroglia, periphere Immunzellen) exprimiert; Aktivierung reduziert Zytokin-Freisetzung, Mikroglia-Aktivierung und Neuroinflammation; β-Caryophyllen ist selektiver CB2-Agonist.
Cedrol
Sesquiterpenischer Alkohol in Zedernholz-Öl; traditionell mit sedierenden Eigenschaften assoziiert, aber wissenschaftliche Evidenz für GABAerge Mechanismen oder klinische Wirksamkeit bei ASD fehlt.
Copy-Number-Varianten (CNVs)
Genomische Deletionen oder Duplikationen >1 kb; häufig bei ASD (15q11-13-Duplikation, 16p11.2-Deletion, 22q13-Deletion/Phelan-McDermid-Syndrom); betreffen oft synaptische Gene (SHANK3, NLGN4).
Cytochrom P450 (CYP)
Enzymfamilie, die Medikamenten-Metabolismus katalysiert; CYP3A4 und CYP2D6 metabolisieren Risperidon und Aripiprazol; Bergapten (in Bergamotte) inhibiert CYP3A4, kann Medikamenten-Spiegel erhöhen.
Dopamin (DA)
Katecholamin-Neurotransmitter; vermittelt Belohnungsverarbeitung, Motivation, motorische Kontrolle; bei ASD reduzierte striatale Aktivierung bei sozialen Belohnungen, veränderte Dopamin-Transporter-Dichte; Ylang-Ylang moduliert DA-Metabolismus in präklinischen Modellen.
DSM-5 (Diagnostic and Statistical Manual of Mental Disorders, 5. Auflage)
Klassifikationssystem der American Psychiatric Association; definiert ASD durch zwei Hauptdomänen: (1) persistierende Defizite in sozialer Kommunikation/Interaktion, (2) eingeschränkte, repetitive Verhaltensmuster.
Disbiosi
Ungleichgewicht der Darmmikrobiota; bei ASD reduzierte mikrobielle Diversität, erhöhte Firmicutes/Bacteroidetes-Verhältnisse, reduzierte Bifidobacterium und Prevotella; korreliert mit Symptom-Schweregrad.
E/I-Imbalance (Exzitatorisch-Inhibitorische Imbalance)
Ungleichgewicht zwischen exzitatorischer (glutamaterger) und inhibitorischer (GABAerger) Neurotransmission; zentrale pathophysiologische Hypothese bei ASD; führt zu Hypererregbarkeit, gestörter sensorischer Filterung und beeinträchtigter sozialer Informationsverarbeitung.
Elektroakupunktur
Akupunktur mit elektrischer Stimulation; präklinische Studien zeigen Verbesserung ASD-ähnlicher Verhaltensweisen in VPA-Mäusen über Vagus-abhängige Mechanismen und Mikrobiom-Modulation.
Epilepsie
Neurologische Erkrankung mit rekurrenten Anfällen; 10–30 % der ASD-Patienten haben komorbide Epilepsie; campherhaltige ätherische Öle (Kampfer, Rosmarin-Campher-Chemotyp, Salbei) sind kontraindiziert.
Fäkale Mikrobiota-Transplantation (FMT)
Transfer von Darmmikrobiota von gesunden Spendern zu Empfängern; präklinische Studien zeigen Verbesserung ASD-ähnlicher Verhaltensweisen in Mausmodellen; offene klinische Studie bei ASD-Kindern zeigte Verbesserungen in GI-Symptomen und Verhalten.
Flumazenil
Benzodiazepin-Antagonist, bindet an Benzodiazepin-Bindungsstelle des GABA-A-Rezeptors; blockiert anxiolytische Effekte von Linalool und 1,8-Cineol, was deren Interaktion mit dieser Stelle bestätigt.
GABA (γ-Aminobuttersäure)
Primärer inhibitorischer Neurotransmitter im ZNS; bindet an GABA-A- (ionotrope) und GABA-B-Rezeptoren (metabotrope); bei ASD reduzierte GABAerge Funktion, veränderte GABA-Spiegel, gestörter GABA-Switch während Entwicklung.
GABA-A-Rezeptor
Liganden-gesteuerter Chlorid-Kanal; Aktivierung durch GABA führt zu Chlorid-Einstrom und Hyperpolarisation (Inhibition); enthält Benzodiazepin-Bindungsstelle; Linalool, 1,8-Cineol und α-Pinen modulieren GABA-A-Rezeptoren.
GABA-Switch
Entwicklungsbiologischer Übergang von exzitatorischer zu inhibitorischer GABA-Wirkung; vermittelt durch Wechsel von NKCC1- zu KCC2-Kotransporter-Expression; bei ASD verzögert; Oxytocin und Bumetanid können GABA-Switch normalisieren.
GAD65/GAD67 (Glutamat-Decarboxylase 65/67)
Enzyme, die Glutamat zu GABA konvertieren; bei ASD reduzierte GAD65/67-Expression in präfrontalem Kortex und Kleinhirn, was zu reduzierter GABA-Synthese führt.
Gas-Chromatographie-Massenspektrometrie (GC/MS)
Analytische Technik zur Identifikation und Quantifizierung volatiler Komponenten; Goldstandard für chemische Charakterisierung ätherischer Öle; ermöglicht Detektion von Verfälschungen, Kontaminanten und Batch-zu-Batch-Variabilität.
Glutamat (Glu)
Primärer exzitatorischer Neurotransmitter im ZNS; bindet an ionotrope (NMDA, AMPA, Kainat) und metabotrope (mGluR1-8) Rezeptoren; bei ASD veränderte Glutamat-Spiegel, gestörte glutamaterge Synapse-Gene (GRIN2B, GRIA1), exzessive glutamaterge Transmission.
Glutathion (GSH)
Tripeptid (γ-Glutamyl-Cysteinyl-Glycin), primäres intrazelluläres Antioxidans; bei ASD reduzierte GSH-Spiegel, erhöhtes oxidiertes Glutathion (GSSG), reduziertes GSH/GSSG-Verhältnis; genetische Varianten in GSH-Synthese-Enzymen (GCLC, GSS) mit ASD assoziiert.
Gut-Brain-Axis
Bidirektionale Kommunikation zwischen Gastrointestinaltrakt und ZNS über neuronale (Nervus vagus), endokrine (HPA-Achse), immunologische und metabolische Wege; bei ASD Dysbiose, veränderte Neurotransmitter-Vorläufer-Produktion, gestörte Gut-Brain-Signalwege.
Hämoxygenase-1 (HO-1)
Enzym, das Häm zu Biliverdin (antioxidativ), Kohlenmonoxid (anti-inflammatorisch) und Eisen abbaut; Nrf2-reguliert; Boswelliasäuren erhöhen HO-1-Expression; HO-1-Induktion schützt vor oxidativem Stress und Neuroinflammation.
Ippocampo
Hirnstruktur im medialen Temporallappen; vermittelt deklaratives Gedächtnis, räumliche Navigation, kontextuelle Verarbeitung; bei ASD Vergrößerung in Kindheit, veränderte Konnektivität, gestörte kontextuelle Furcht-Konditionierung.
Hyperserotonämie
Erhöhte periphere Serotonin-Spiegel; bei 25–50 % der ASD-Patienten nachgewiesen; Beziehung zu zentralen 5-HT-Spiegeln unklar; möglicherweise durch gestörte Plättchen-Serotonin-Aufnahme oder erhöhte periphere Synthese.
Interleukin-6 (IL-6)
Pro-inflammatorisches Zytokin; bei ASD erhöhte IL-6-Spiegel in Plasma und Liquor; maternale Immunaktivierung mit IL-6 produziert ASD-ähnliche Phänotypen in Mausmodellen; IL-6 moduliert synaptische Transmission und Entwicklung.
Kleinhirn (Cerebellum)
Hirnstruktur im Hinterhirn; traditionell mit motorischer Kontrolle assoziiert, spielt auch Rollen in kognitiven Prozessen, sensorischer Vorhersage und sozialem Lernen; bei ASD Purkinje-Zell-Verlust, reduziertes Vermis-Volumen, gestörte zerebello-kortikale Konnektivität.
Lavendel (Lavandula angustifolia)
Aromatische Pflanze, ätherisches Öl enthält 25–45 % Linalool und Linalylacetat; kleine Pilotstudien berichten verbesserte ABA-Compliance und geteilte Aufmerksamkeit bei ASD-Kindern; präklinische Evidenz für GABAerge Modulation, serotonerge Regulation und oxytonerge Aktivierung.
Linalolo
Monoterpenischer Alkohol, Hauptkomponente von Lavendel, Koriander, Bergamotte; moduliert GABA-A-Rezeptoren an Benzodiazepin-Bindungsstelle (Flumazenil-sensitiv), beeinflusst Serotonin-Spiegel, erhöht intrazelluläres Calcium in Oxytocin-Neuronen, zeigt anti-inflammatorische Effekte.
Acetato di linalile
Ester von Linalool und Essigsäure; Hauptkomponente von Lavendel (25–45 %) und Bergamotte; trägt zu anxiolytischen und sedierenden Effekten bei; wird zu Linalool hydrolysiert.
Long-Term Potentiation (LTP) / Long-Term Depression (LTD)
Zelluläre Mechanismen synaptischer Plastizität; LTP: anhaltende Verstärkung synaptischer Transmission nach hochfrequenter Stimulation; LTD: anhaltende Abschwächung nach niederfrequenter Stimulation; bei ASD gestörte LTP/LTD-Balance in multiplen Hirnregionen.
Magnetresonanzspektroskopie (MRS)
Nicht-invasive Bildgebungstechnik zur Quantifizierung von Metaboliten (Glutamat, GABA, N-Acetylaspartat, Kreatin) in vivo; bei ASD zeigt MRS regionale Alterationen in Glutamat- und GABA-Konzentrationen.
Maternale Immunaktivierung (MIA)
Präklinisches Modell, bei dem trächtige Tiere mit Immunstimulatoren (Poly(I:C), LPS) behandelt werden; Nachkommen zeigen ASD-ähnliche Verhaltensweisen, erhöhte pro-inflammatorische Zytokine, gestörte synaptische Entwicklung; modelliert Umwelt-Risikofaktor für ASD.
Melatonina
Hormon, das von der Zirbeldrüse produziert wird; reguliert zirkadianen Rhythmus und Schlaf; bei ASD häufig Schlafstörungen; Melatonin-Supplementierung verbessert Schlaflatenz und -dauer; Meta-Analysen zeigen moderate Wirksamkeit.
Mikroglia
Residente Immunzellen des ZNS; regulieren synaptisches Pruning, neuronale Entwicklung, Immunüberwachung; bei ASD aktivierte Mikroglia (erhöhte Iba1-Expression, amöboide Morphologie) in präfrontalem Kortex, Kleinhirn; setzen pro-inflammatorische Zytokine und ROS frei.
Disfunzione mitocondriale
Beeinträchtigte mitochondriale Funktion (reduzierte Atmungsketten-Aktivität, erhöhtes Laktat, reduzierte ATP-Synthese); bei 5–30 % der ASD-Patienten; führt zu erhöhter ROS-Produktion, oxidativem Stress, gestörter Calcium-Homöostase.
Neuroligin (NLGN)
Postsynaptische Zelladhäsionsmoleküle (NLGN1-4); interagieren mit präsynaptischen Neurexinen; regulieren synaptische Differenzierung, Reifung und Funktion; Mutationen in NLGN3 und NLGN4X bei ASD-Patienten; NLGN3-R451C-Mäuse zeigen erhöhte inhibitorische Transmission und ASD-ähnliche Phänotypen.
Neurexin (NRXN)
Präsynaptische Zelladhäsionsmoleküle (NRXN1-3); interagieren mit postsynaptischen Neuroliginen; regulieren synaptische Organisation; Mutationen in NRXN1 bei ASD-Patienten; NRXN1-Deletionen mit ASD, Schizophrenie und intellektueller Beeinträchtigung assoziiert.
Neuroinfiammazione
Entzündungsreaktion im ZNS; charakterisiert durch Mikroglia- und Astrozyten-Aktivierung, erhöhte pro-inflammatorische Zytokine (TNF-α, IL-6, IL-1β), gestörte Blut-Hirn-Schranke; bei ASD chronische Neuroinflammation in multiplen Hirnregionen.
NF-κB (Nuclear Factor kappa B)
Transkriptionsfaktor, der pro-inflammatorische Gene (TNF-α, IL-6, IL-1β, COX-2) reguliert; bei ASD erhöhte NF-κB-Aktivierung; β-Caryophyllen und Boswelliasäuren inhibieren NF-κB-Signalwege.
NMDA-Rezeptor (N-Methyl-D-Aspartat-Rezeptor)
Ionotroper Glutamat-Rezeptor, Calcium-permeabler Kanal; zentral für synaptische Plastizität (LTP/LTD), Lernen und Gedächtnis; bei ASD veränderte NMDA-Rezeptor-Subunit-Expression (GRIN2A, GRIN2B), gestörte NMDA-Rezeptor-Funktion in SHANK2-Knockout-Mäusen.
Nrf2 (Nuclear factor erythroid 2-related factor 2)
Transkriptionsfaktor, Master-Regulator der antioxidativen Antwort; induziert Expression von HO-1, NQO1, Glutathion-S-Transferasen, anderen Antioxidans-Enzymen; Boswelliasäuren aktivieren Nrf2; Nrf2-Aktivatoren (Sulforaphan) zeigen Verbesserungen bei ASD in kleinen Studien.
Oxidativer Stress
Ungleichgewicht zwischen ROS-Produktion und antioxidativer Abwehr; bei ASD erhöhte Lipidperoxidation, Protein-Carbonylierung, DNA-Oxidation, reduzierte Antioxidans-Kapazität (GSH, SOD, Katalase); trägt zu neuronaler Schädigung und Dysfunktion bei.
Oxytocin (OT)
Neuropeptid, produziert im Hypothalamus; zentrale Rolle in sozialer Bindung, Vertrauen, sozialer Kognition, Stressregulation; bei ASD reduzierte Plasma-OT-Spiegel, veränderte OXTR-Expression; intranasales OT zeigt gemischte Ergebnisse; OT reguliert GABAerge Entwicklung in präklinischen Modellen.
Parvalbumin-positive Interneurone
Subtyp GABAerger Interneurone, exprimiert Calcium-bindendes Protein Parvalbumin; vermittelt schnelle, synchrone Inhibition; bei ASD reduzierte Dichte und Funktion von Parvalbumin-Interneuronen in präfrontalem Kortex.
Phelan-McDermid-Syndrom
Genetisches Syndrom durch 22q13-Deletion, die SHANK3-Gen umfasst; charakterisiert durch ASD, intellektuelle Beeinträchtigung, Sprachdefizite, Hypotonie; demonstriert kausale Rolle von SHANK3 in ASD-Pathogenese.
Präfrontaler Kortex (PFC)
Frontale Hirnregion; vermittelt exekutive Funktionen, Arbeitsgedächtnis, kognitive Flexibilität, soziale Kognition, Theory of Mind; bei ASD reduzierte PFC-Aktivierung während sozialer Kognitionsaufgaben, gestörte PFC-Konnektivität, GABAerge Defizite.
Propionat
Kurzkettige Fettsäure, produziert durch Darmmikrobiota; bei ASD möglicherweise erhöhte Propionat-Spiegel; Propionat-Exposition in Nagetiermodellen induziert ASD-ähnliche Verhaltensweisen, Neuroinflammation, oxidativen Stress.
Reaktive Sauerstoffspezies (ROS)
Hochreaktive Moleküle (Superoxid, Wasserstoffperoxid, Hydroxyl-Radikal); entstehen als Nebenprodukte mitochondrialer Atmung; bei exzessiven Konzentrationen verursachen ROS oxidative Schädigung von Lipiden, Proteinen, DNA; bei ASD erhöhte ROS-Produktion.
Risperidon
Atypisches Antipsychotikum, Dopamin-D2- und Serotonin-5-HT2A-Antagonist; FDA-zugelassen für Irritabilität bei ASD; Nebenwirkungen: Gewichtszunahme, Hyperprolaktinämie, extrapyramidale Symptome, metabolisches Syndrom; metabolisiert über CYP2D6.
Serotonin (5-HT, 5-Hydroxytryptamin)
Monoamin-Neurotransmitter; vermittelt Stimmung, Angst, Schlaf, Appetit, soziale Kognition; bei ASD Hyperserotonämie (peripher), reduzierte zentrale Serotonin-Synthese, genetische Varianten in 5-HTT und TPH2; Linalool und Ylang-Ylang modulieren serotonerge Systeme.
SHANK-Proteine (SH3 and multiple ankyrin repeat domains)
Postsynaptische Gerüstproteine (SHANK1-3); organisieren Glutamat-Rezeptoren, Aktin-Zytoskelett, Signalmoleküle; Mutationen in SHANK2 und SHANK3 bei ASD; SHANK3-Knockout-Mäuse zeigen reduzierte Spine-Dichte, gestörte synaptische Transmission, ASD-ähnliche Verhaltensweisen.
Striatum
Subkortikale Struktur der Basalganglien (Nucleus caudatus, Putamen, Nucleus accumbens); vermittelt Belohnungsverarbeitung, Gewohnheitslernen, motorische Kontrolle; bei ASD Striatum-Vergrößerung, reduzierte Aktivierung bei sozialen Belohnungen, gestörte kortiko-striatale Konnektivität.
Synaptisches Pruning
Entwicklungsbiologischer Prozess, bei dem überschüssige Synapsen eliminiert werden; vermittelt durch Mikroglia, Komplement-System; bei ASD möglicherweise gestörtes Pruning (zu viel oder zu wenig), was zu veränderten Synapsen-Dichten und Konnektivität führt.
Terpene
Diverse Klasse von Naturstoffen, aufgebaut aus Isopren-Einheiten (C5H8); Hauptkomponenten ätherischer Öle; Monoterpene (C10): Linalool, 1,8-Cineol, α-Pinen; Sesquiterpene (C15): β-Caryophyllen, Cedrol; Triterpene (C30): Boswelliasäuren.
TNF-α (Tumor-Nekrose-Faktor-α)
Pro-inflammatorisches Zytokin; bei ASD erhöhte TNF-α-Spiegel in Plasma, Liquor, postmortalem Hirngewebe; maternale Immunaktivierung mit erhöhtem TNF-α produziert ASD-ähnliche Phänotypen; TNF-α moduliert synaptische Transmission, reduziert GABAerge Inhibition.
Translocator-Protein (TSPO)
Mitochondriales Protein, hochreguliert in aktivierten Mikroglia; PET-Liganden (z. B. [11C]-PBR28) binden an TSPO und ermöglichen in-vivo-Bildgebung von Mikroglia-Aktivierung; bei ASD erhöhte TSPO-Bindung in multiplen Hirnregionen.
Tryptophan
Essentielle Aminosäure, Vorläufer von Serotonin und Melatonin; bei ASD möglicherweise gestörter Tryptophan-Metabolismus; Darmmikrobiota beeinflusst Tryptophan-Verfügbarkeit und Metabolismus über Kynurenin- und Serotonin-Pathways.
Valproinsäure (VPA)
Antiepileptikum; pränatale VPA-Exposition ist Risikofaktor für ASD beim Menschen; VPA-induziertes ASD-Mausmodell: trächtige Mäuse erhalten VPA, Nachkommen zeigen ASD-ähnliche Verhaltensweisen, Neuroinflammation, oxidativen Stress; weit verbreitetes präklinisches Modell.
Principio di Venturi
Physikalisches Prinzip (Bernoulli-Effekt): Druckreduktion in einem Fluid, wenn es durch eine Verengung strömt; im Organik Aromas Nebulizer 3.0 erzeugt Druckluft durch Düse Unterdruck, der ätherisches Öl ansaugt und in feine Tröpfchen zerstäubt (Kaltvernebelung).
Vetiver (Vetiveria zizanioides)
Tropisches Gras, ätherisches Öl enthält Vetiverol, Khusimol, α-Vetivon; anekdotische Berichte über Effekte auf Aufmerksamkeit und Hyperaktivität, aber kontrollierte Studien bei ASD fehlen; wissenschaftliche Evidenz für Mechanismen unzureichend.
Incenso (Boswellia)
Harz von Boswellia-Arten; ätherisches Öl und Extrakte enthalten Boswelliasäuren; präklinische Evidenz für anti-neuroinflammatorische, antioxidative (Nrf2/HO-1) und neuroprotektive Effekte; keine klinischen Studien bei ASD identifiziert.
Zedernholz (Cedrus atlantica, Juniperus virginiana)
Ätherisches Öl enthält Cedrol, α-Cedren, Thujopsen; traditionell für Sedierung und Angstreduktion verwendet, aber wissenschaftliche Evidenz für GABAerge Mechanismen oder klinische Wirksamkeit bei ASD fehlt.
Zirkadianer Rhythmus
Endogener ~24-Stunden-Rhythmus, reguliert Schlaf-Wach-Zyklus, Hormonsekretion, Körpertemperatur; bei ASD häufig gestörte zirkadiane Rhythmen, Schlafstörungen; Melatonin reguliert zirkadianen Rhythmus und verbessert Schlaf bei ASD.