Sisällysluettelo
Päivitetty – 30. huhtikuuta 2026
Vertailu ADHD/ADS:n standardihoidon ja aromaterapian välillä terapeuttisesti hyväksytyillä, GC/MS-analysoiduilla ja eräkohtaisesti testatuilla eteerisillä öljyillä. (Tilanne 04/2026).
ADHD/ADS ja eteeriset öljyt – selitetty ymmärrettävästi
Tieteellisen raportin yleistajuinen tiivistelmä kaikille, jotka haluavat oppia lisää luonnollisesta tuesta ADHD:hen
Mikä on ADHD/ADD?
ADHD tarkoittaa Tarkkaavuus- ja ylivilkkaushäiriö, Ilmoitukset yhdistyy hyperaktiivisuutta esiintymättömään muotoon (tarkkaavuushäiriö). Kumpikaan ei ole keksintö tai kasvatusvirhe, vaan ne ovat todellisia neurologisia sairauksia, joissa aivot ovat erilainen.
Kuva sen takana: Ajattele aivoja kuin radiota. ADHD-aivoissa lähetin hyppii jatkuvasti taajuudelta toiselle, joskus liian kovaa, joskus liian hiljaa, harvoin oikealla kanavalla. Tämä vaikeuttaa keskittymistä, paikallaan pysymistä tai impulssien hallintaa.
Mitä aivoissa tapahtuu ADHD:ssä?
Ydinasia on kahdessa välittäjäaineessa:
Dopamiini – palkkio- ja motivaatiovälittäjäaine“
ADHD:ssa dopamiini “siivotaan” liian nopeasti takaisin (dopamiinitransportteri DAT:n kautta). Tämän seurauksena arkiaskareiden tuottama palkitsemisen ja motivaation tunne puuttuu. Aivot etsivät jatkuvasti stimulaatiota, mistä johtuvat impulsiivisuus ja riskienhaku.
Noradrenaliini – tarkkaavaisuuden ja keskittymisen välittäjäaine“
Liian vähän noradrenaliinia etuotsalohkossa (aivojen “johtoalueella”) – aiheuttaa keskittymisvaikeuksia, unohtelua, vaikeuksia suunnittelussa
Mitkä aivoalueet ovat mukana?
- Etuaivokuoren otsalohko
Vastuussa suunnittelusta, impulssikontrollista, keskittymisestä – ADHD:ssa vajaatoimintaa
- Tyvitumakkeet (striatum)
Palkitsemisjärjestelmä – vähemmän herkkä ADHD:ssa
- Pikkuaivot
Ajoitus ja koordinaatio – lievästi muuttuneet ADHD:ssa
Kuinka yleinen ADHD on?
Lapsilla ja nuorilla se on yleisin psykiatrinen sairaus, johon liittyy 5–7 %, aikuisilla 2,5 - 4 %, monet aikuiset eivät tiedä, että heillä on ADHD.
ADHD ilmenee monin eri tavoin, mutta yleisimpiä oireita ovat keskittymisvaikeudet, ylivilkkaus ja impulsiivisuus.
Miten ADHD:ta yleensä hoidetaan?
Pääasiallinen lääke – metyylifenidaatti (Ritalin, Concerta, Medikinet)
Metylfenidaatti (MPH) on yleisimmin määrätty ADHD-lääke ja ensisijainen hoito.
Miten se toimii?
Metylfenidaatti estää dopamiinitransporteria (DAT), joka on dopamiinin “siivouspumppu”. Kun vähemmän dopamiinia siivotaan, sitä jää enemmän hermosolujen väliin, ja aivot voivat keskittyä paremmin.
Numerot sen takana
20 mg:n annos estää noin. 54 % aivot puhdistumassa dopamiinista, 40 mg estää noin. 72 %.
Vaikutus alkaa 30–90 minuutin kuluttua ja kestää valmisteesta riippuen 4–12 tuntia.
Kuinka tehokasta se on?
Osoitteessa 70–80 % Potilailla metyylifenidaatti tehoaa kliinisesti hyvin: huomiokyvyn, impulssikontrollin ja koulusuoritusten parantumista koskeva näyttö on vahvaa.
Muotoilut
- Lyhytvaikutteinen (esim. Ritalin): 4–6 tuntia, otettava useita kertoja päivässä
- Kituliäs (esim. Concerta, Medikinet retard): 8–12 tuntia, kerran päivässä
Sivuvaikutukset
– Ruokahalun heikkeneminen (yleisin sivuvaikutus)
– Unihäiriöt (jos otetaan liian myöhään)
– Päänsärky, vatsakipu (yleensä alussa)
– Sydämen sykkeen ja verenpaineen lievä nousu
– Mielialanvaihtelut, ärtyisyys (harvinainen)
Lisää lääkkeitä
Atomoksetiini (Strattera)
– Kein Stimulans, estää noradrenaliinin kuljettajaa (NET)
– Vaikuttaa myös ADHD:hen ilman riippuvuusriskiä
– Kestää 4–6 viikkoa täyden tehon saavuttamiseen
– Soveltuu hyvin samanaikaisen ahdistuneisuushäiriön tai Touretten oireyhtymän kanssa
Amfetamiini (Saksassa vähemmän yleinen)
– Lisdeksamfetamiini (Vyvanse): Myönnetty myyntilupa aikuisille Saksassa vuonna 2013
– Vaikuttaa vahvemmin ja pidempään kuin metyylifenidaatti
Guanfasiini (Intuniv)
– Lapsille ja nuorille, joille stimulantit eivät sovi
Vaikuttaa noradrenaliinireseptoreihin aivokuoren etuosassa
Eteeriset öljyt ADHD:n hoidossa – miten se voi toimia?
Eteeriset öljyt voivat tukea ADHD-aivoja useilla tavoilla:
- Hajuaistin kautta aivoihin
Tuoksumolekyylit aktivoivat limbistä järjestelmää (tunteet, motivaatio) ja aivokuoren etulohkoa (keskittyminen) – suoraan ja nopeasti - Hermovälittäjäainejärjestelmät
Tietyt terpeenit vaikuttavat dopamiiniin, noradrenaliiniin, serotoniiniin ja GABA:han - Komplementaarinen metyylifenidaatille
Metyylifenidaatti vaikuttaa DAT/NETiin – eteeriset öljyt vaikuttavat muihin järjestelmiin (GABA-A, CB2, TRPM8, SERT) ja ovat siten mahdollisia lisähoitoja.
Tärkeä rajoitus
Eteeristen öljyjen tutkimus ADHD:n hoidossa on vielä lapsenkengissään. Useimmat tutkimukset on tehty terveillä aikuisilla, ei ADHD-potilailla. Suorat kliiniset todisteet ovat vielä rajallisia.
Mit welchen ätherischen Ölen kann man ADHS behandeln?
Piparminttu – keskittymisöljy nro 1
Piparminttu (Piparminttu) on vahvin näyttö huomiokyvyn paranemisesta.
- Mitä sisällä on?
Mentoli (30–50 %)
Mentonista (10–30 %)
1,8-sineoli (5–10 %) - Mitä mentoli tekee?
Aktivoi TRPM8-reseptorit – hermoston “kylmäreseptorit”, jotka aktivoivat aivoja
Estää entsyymiä, joka hajottaa välittäjäainetta asetyylikoliinia
Moduloi GABA-A-reseptoreita (lievästi rauhoittava yliaktiivisuudessa) - Kliininen tutkimus (n=24)
100 µL piparminttuöljyä (kapseloituna) paransi merkittävästi jatkuvaa tarkkaavaisuutta RVIP-testissä (nopea visuaalisen informaation käsittely) 1–3 tunnin kuluttua; vähensi väsymystä ja paransi henkistä laskentaa - Erikoisominaisuus
Piparminttu edistää kohdennettu Huomio (toisin kuin laventeli, joka hajottaa huomiota) - Kuinka käyttää
2 tippaa nenäliinaan, juuri ennen opiskelu- tai työskentelyjaksoja; diffuusori opiskeluhuoneeseen
Rosmariini – muistille ja vireydelle
Rosemary (Rosmariini) on jo antiikin ajoista lähtien oikeutetusti tunnettu “muistiyrttinä”.
- Mitä sisällä on?
1,8-Kineoli (20–50 %)
Kamferi (10–20 %)
α-pineeni (10–15 %) - Mitä 1,8-sineoli tekee?
Estää entsyymiä asetyylikoliiniesteraasia, joka hajottaa välittäjäainetta (samankaltaista kuin Alzheimerin lääkkeitä!)
Aktivoi hermoston, lisää valveillaoloa ja tarkkaavaisuutta
Tulehdusta ehkäisevä ja antioksidanttinen aivoissa - Kliininen tutkimus (n=144)
Rosmariiniaromaterapia paransi merkittävästi kokonaismuistia ja jälkimuistia, paremmin kuin laventeli ja kontrolliryhmä - ADHD:lle
Erityisen hyödyllinen muistiongelmiin, “aivosumuun” ja aamuturhauteen. - Kuinka käyttää
Aamulla diffuusoriin (5 tippaa), inhalaatio ennen kokeita tai tärkeitä tehtäviä - Huomio: Älä käytä iltaisin, se on liian virkistävää; erityistä varovaisuutta epilepsiassa kamferipitoisuuden vuoksi!
Laventeli – ahdistusta ja univaikeuksia vastaan
Laventeli (Lavandula angustifolia) on paras öljy ADHD-oireisiin liittyvään ahdistukseen ja unettomuuteen.
- Mitä sisällä on?
Linalooli (25–45 %)
Linalyyliasetaatti (25–50 %) - Mitä linalooli tekee?
Aktivoi GABA-A-reseptoreja, aivojen “jarru”
Moduloi serotoniinia, dopamiinia ja noradrenaliinia
Laske kortisolin (stressihormonin) tasoa 24–38 % - ADHD:n kohdalla erityisen hyödyllinen
Nukahtamisvaikeudet (erittäin yleisiä ADHD:ssa)
Liitännäishäiriöt (noin 50 %:lla % ADHD-potilaista)
Tunteiden säätelyn vaikeudet ja ärtyneisyys - Tärkeä huomautus
Laventeli pystyy siihen Lyhytaikaisesti heikentää työmuistia, siksi älä käytä oppimisvaiheiden aikana, vaan vain illalla tai tarkoitukselliseen rentoutumiseen - Tutkimus
Silexan (80 mg laventeliöljyä päivässä kapselina) oli verrattavissa loratsepaamiin ahdistuneisuushäiriöiden hoidossa - Kuinka käyttää
Illalla diffuusiin (5 tippaa), 2 tippaa tyynylle
Sederpuu – Hapetus ja fokus
Setripuu (AtlaskSetri / Virginianpunapuu) käytetään perinteisesti ADHD:n hoidossa.
- Mitä sisällä on?
α-cedreen
β-cedreen
Cedrol - Mitä se tekee
Parantaa aivojen hapetusta; rauhoittava; aktivoi parasympaattisen hermoston - ADHD-spesifinen
Godfrey (2001) raportoi positiivisia vaikutuksia ADHD-lapsilla;
Cedrol alensi sydämen sykettä ja hengitystiheyttä tutkimuksissa - Kuinka käyttää
Diffuusorissa kevyiden toimintojen aikana; sopii hyvin yhteen laventelin kanssa
Vetiver – Maadoittava tuoksu
Vetiver (Vetiveria zizanioides) tuoksuu syvältä ja maanläheisesti, ja sitä kuvataan usein “rauhoittavaksi levottomille sieluille”.
- Mitä se tekee
Anksiolyyttinen (ahdistusta lievittävä); rauhoittaa hermostoa; parantaa unta - ADHD-spesifinen
Springer ym. (2018) raportoivat parannuksia ADHD-lapsilla 30 päivän 3 kertaa päivässä tapahtuneen inhalaation jälkeen - Kenelle
Erityisesti hyperaktiivisella ADHD-variantilla, johon liittyy sisäistä levottomuutta
Kaneli – ainoa suora ADHD-tutkimus
Kaneli (Cinnamomum verum) on ainutlaatuinen todiste: ainoa kliininen tutkimus suoraan ADHD-lapsilla.
- Mitä sisällä on?
Zimtaldehydi (60–75 %)
Eugenoli (5–10 %) - ADHD-tutkimus (Chen et al., 2008)
Rehabilitointi + kaneliaromaterapian (1 % kaneli, nenähengitys) yhdistelmä 6 kuukauden ajan osoitti merkittävästi parempia tuloksia SNAP-IV-kyselyssä kuin pelkkä kuntoutus (p < 0,05) - Mekanismi
Sinnilde-metaboliiteilla voi olla dopaminergisia vaikutuksia - Rajoitus
Tutkimuksessa on metodologisia heikkouksia (pieni otoskoko, epäselvä sokkoutus) - Kuinka käyttää
Säästäväinen diffuusorissa, yhdistettynä muihin öljyihin
Mustapippuri (β-karyofylleen) – neuroinflammaatiota vastaan
β-karyofylleeni mustapippurista, laventelista ja muista kasveista:
- Aktivoi CB2-kannabinoidireseptoreita ilman psykoaktiivisia vaikutuksia
- Vähentää neuroinflammaatiota (aivotulehdusta)
- Mielenkiintoista ADHD:ssa, johon liittyy tulehdusmerkkejä tai mielialahäiriöitä
- Hyvin yhdisteltävissä muihin öljyihin
Öljyt pähkinänkuoressa – Milloin mitäkin öljyä?
Käytännöllinen päivittäinen rutiini ADHD:lle
Aamurutiini (aktivointi + fokus):
- Diffuusori Rosmariini (4 tippaa) + piparminttu (2 tippaa) 15–20 minuutiksi
- Tai: piparminttua nenäliinaan, hengitä syvään 3 kertaa ennen koulua/töitä
- Vaikutus Valppaus, muisti, keskittyminen
Oppimisaika / Työskentelyvaihe
- Diffuusori Piparminttu (3 tippaa) + sitruuna (2 tippaa) 20 minuutiksi, sitten 30 minuutin tauko
- Huomio: Ei laventelia opiskelun aikana!
- Vaikutus Jatkuva tarkkaavaisuus, keskittyminen
Iltapäivä (rentoutuminen koulun jälkeen):
- Diffuusori Setripuu (3 tippaa) + bergamotti (2 tippaa) 20 minuutiksi
- Vaikutus Stressin lievitys, tunteiden säätely
Iltaohjelma (Rentoutuminen + Nukkuminen):
- Diffuusori Laventeli (4 tippaa) + Vetiver (2 tippaa) 30 minuuttia ennen nukkumaanmenoa
- Tai: 2 tippaa laventelia tyynylle
- Vaikutus Nukahtaminen, unenlaatu
Annosteluohjeet diffuuserille
Tärkeää: Hajuaistin sopeutuessa öljyä ei enää tunnu juuri lainkaan 20–30 minuutin kuluttua, mutta se vaikuttaa silti. Jotta reseptorit voivat toipua ja totutteluefekti „nollautua“, taukoja on noudatettava!
Mitä tiede todella sanoo?
Päätelmä
Todisteet ovat lupaava mutta vielä rajallinen. Mekanismin kannalta se on järkevää, mutta suuria kliinisiä tutkimuksia ADHD-potilailla puuttuu vielä. Se ei tarkoita, ettei se tehoaisi, se tarkoittaa, että tarvitsemme lisää tutkimusta.
Tärkeitä turvallisuusohjeita
Erityisiä ADHD-huomioita:
Aistiyliherkkyys
Monilla ADHD-henkilöillä (40–60 %) on kohonnut hajuherkkyys. Aloita aina puoli annosta ja pidennä annostelua vähitellen. Jos haju on epämiellyttävä: lopeta heti.
Yhteisvaikutukset metyylifenidaatin kanssa
- Kaneli
Dopaminergisella vaikutuksella voi olla teoreettisesti vahvistava vaikutus MPH:iin, joten sydämen sykettä ja verenpainetta tulisi tarkkailla.
- Laventeli
Voi olla serotoniinivaikutteinen, ole varovainen käyttäessäsi samanaikaisesti masennuslääkkeitä
- Rosemary
Voi vaikuttaa piristävästi, joten älä levitä sitä juuri ennen nukkumaanmenoa
Lasten kanssa
– Alle vähintään 3 vuotta: Ei eteerisiä öljyjä
– 3–6 vuotta: Vain hyvin pieniä pitoisuuksia (1–2 tippaa), hyvin ilmastoitu tila
– > 6 vuotta: Normaali annostus mahdollinen – Ei suoraa ihokosketusta ilman laimennusta
Yleiset säännöt:
- Laimentaa aina kantajaöljyn kanssa (esim. ei-rasvoittuva, fraktioitu kookosöljy) (2–3 %)
- Käytä hyvin ilmastoitua tilaa
- Pitää taukoja (ei hajottaa koko päivää)
- Astman tai hengitystieongelmien yhteydessä: kysy lääkäriltä
- Eteeriset öljyt ovat ei korvausta metyylifenidaatille tai muille ADHD-hoidoille
UKK – Usein kysytyt kysymykset
Voinko korvata metyylifenidaatin eteerisillä öljyillä?
Ei. Eteeriset öljyt ovat täydennys, eivät korvike. Metyylifenidaatilla on vahva kliininen näyttö 70–80 % potilaista. Eteeriset öljyt voivat auttaa lievittämään jäännösoireita, parantamaan unta tai vähentämään sivuvaikutuksia (kuten ahdistusta).
Mitä öljyä minun pitäisi kokeilla ensin?
Pipparminttu keskittymiseen (päivisin) ja laventeli uneen (iltaisin), parhaiten tutkitut, hyvin siedetyt.
Kuinka kauan kestää, että huomaan vaikutuksen?
Jotkut vaikutukset (keskittyminen, vireys) tuntuvat minuuttien sisällä. Pitkäkestoisia parannuksia (uni, mieliala) varten käytä säännöllisesti 2–4 viikkoa.
Toimiiko tämä myös aikuisilla, joilla on ADHD?
Kyllä, useimmat tutkimukset on itse asiassa tehty aikuisilla. ADH:ta sairastavat aikuiset raportoivat usein erityisen hyvistä vaikutuksista tunne-elämän epäsäätelyyn ja univaikeuksiin.
Täytyykö minun ostaa kalliita öljyjä?
Laatu on tärkeää: Kiinnitä huomiota 100 % luonnolliseen eteeriseen öljyyn, mieluiten analyysitodistuksella (GC/MS) eräkohtaisesti.
Edullisilla parfyymiöljyillä tai synteettisillä tuoksuilla ei ole terapeuttisia vaikutuksia, ja synteettisten ainesosien vuoksi ne voivat olla terveydelle haitallisia ja aiheuttaa päänsärkyä, pahoinvointia jne.
Ne, jotka haluavat saada lisätietoa eteeristen öljyjen valinnasta ja laadusta, löytävät sitä artikkelista „Eteeriset öljyt – Etsinnän odysseia“löytöretkeilijä.
Toinen artikkeli lainaa Ruhr-yliopiston Bochumin professoria, tohtori tohtori tohtori lääketieteen tohtori Hanns Hattia, joka videossaan „Parantaminen tuoksuilla“käsiteltään eteeristen öljyjen vaikutusta ihmiskehoon mielenkiintoisella, viihdyttävällä mutta silti tieteellisellä tavalla.
Pitäisikö minun keskustella tästä lääkärini kanssa?
Aromaterapiaan (diffuusori, inhalaatio) sitä ei välttämättä tarvita. Jos kuitenkin haluat käyttää kapseleita tai voiteita eteerisillä öljyillä tai jos lapsellasi on ADHD ja hän käyttää metyylifenidaattia, ota yhteyttä lääkäriin.
Neurobiologiset perusteet, molekulaariset toimintamekanismit ja kliininen näyttö orgaanisen aromalaitteen Nebulizer 3.0:n liitännäishoidolle
Yhdistetty tutkimusraportti Huhtikuu 2026
Aiheet: Metyylifenidaatti (Ritalin) · Aivojen sisäinen farmakodynamiikka · Adjuvantti aromaterapia · Terpeenit · Reseptorit · Signaalireitit · Annostussuositukset
Sovellus Organik Aromas Nebulizer 3.0 (Venturi-kylmäsumutin, vedetön, GC/MS-puhdasta öljyä)
ADHD ja metyylifenidaatti
Tämä raportti tutkii metyylifenidaatti-hoidon neurobiologisia perusteita tarkkaavaisuus- ja ylivilkkaushäiriössä (ADHD) ja arvioi eteeristen öljyjen potentiaalia liitännäishoidon vaihtoehtona. Analyysi perustuu 87 tieteelliseen julkaisuun aivojen sisäisistä metyylifenidaattipitoisuuksista ja 159 eteerisiä öljyjä koskevaan tutkimukseen ADHD-kontekstissa.
Keskeiset havainnot metyylifenidaatista
Terapeuttiset oraaliset annokset (0,25–0,6 mg/kg) tuottavat striatumissa yli 50% dopamiinitransporterin (DAT) okkupanssia, ja 20 mg oraalisesti saavutettuna 54% ja 40 mg 72% DAT-estäytymistä. Suurin aivojen otto tapahtuu 60–90 minuuttia oraalisen annon jälkeen. Terapeuttisella alueella olevat plasman pitoisuudet ovat 3,5–7,8 ng/ml (aikuiset), ja 6 ng/ml liittyy 50% DAT-estäytymiseen. Methylphenidat-pitoisuuksista aivokudoksessa (ng/ml) tai aivo-selkäydinnesteessä ei ole suoria mittauksia; saatavilla olevat tiedot perustuvat PET/SPECT-okkupanssitutkimuksiin.
Eteeriset öljyt apuaineina
Mekaaninen uskottavuus on olemassa adjuvantille terapialle, joka perustuu täydentäviin toimintamekanismeihin. Linalool (laventeli) vaikuttaa serotoniini-, dopamiini- ja noradrenaliinijärjestelmiin 5-HT1A-reseptorien ja SERT-sitoutumisen kautta. Mentoli (piparminttu) aktivoi TRPM8-kanavat ja vaikuttaa GABA-A- sekä nikotiinireseptoreihin, parantaen tarkkaavaisuutta ja valveutuneisuutta. β-karyofylleeni (mustapippuri) toimii CB2-agonistina tulehdusta ehkäisevin ominaisuuksin. 1,8-sineoli (rosmariini) parantaa muistisuorituskykyä ja kognitiivisia toimintoja.
Näyttö
Vaikka prekliiniset ja mekaaniset tiedot ovat lupaavia, satunnaistettuja kontrolloituja tutkimuksia (RCT) erityisesti ADHD-potilailla puuttuu. Olemassa olevat ihmistutkimukset osoittavat kognitiivisia parannuksia terveillä aikuisilla (piparminttu: parantunut jatkuva tarkkaavaisuus, n=24; rosmariini: muistin parantuminen, n=144).
Tämä raportti tarjoaa näyttöön perustuvia annostussuosituksia Organik Aromas Nebulizer 3.0 ja kattavat turvallisuusohjeet ADHD-potilaiden käyttöön.
Autismin kirjon häiriö
Autismin kirjosiirtohäiriö (ASD) on monimutkainen neurobiologinen kehityshäiriö, jonka arvioitu esiintyvyys maailmanlaajuisesti on 1–2 %. Ydinoireita ovat sosiaalisen kommunikaation ja vuorovaikutuksen vaikeudet sekä toistuvat käyttäytymismallit ja aistierikoisuudet. Huolimatta intensiivisestä tutkimuksesta ydinoireisiin ei ole parantavia hoitoja; käytettävissä olevat interventiot keskittyvät käyttäytymisterapiaan ja oireenmukaiseen lääkehoitoon. Tässä raportissa tarkastellaan eteeristen öljyjen potentiaalia ASD:n liitännäishoito-vaihtoehtona perustuen 547 tieteellisen julkaisun systemaattiseen analyysiin ASD-neurobiologiasta, terpeeneistä ja kliinisestä näytöstä.
ASD:n neurobiologinen heterogeenisyys ilmenee häiriintyneenä eksitatoris-inhibitorisena (E/I) tasapainona, GABAergisten, glutamatergisten, serotergisten, dopaminergisten ja oksytorergisten järjestelmien toimintahäiriöinä, kroonisena neuroinflammaationa mikroglias aktivaation myötä, oksidatiivisena stressinä, suoli-aivoakselin muutoksina ja synapsivajeina (neuroligiinit, SHANK-proteiinit). Vaikuttavia aivoalueita ovat etuotsalohko, mantelitumake, pikkuaivot, hippokampus ja tyvitumakkeet.
Molekyylianalyysit osoittavat, että eteeristen öljyjen spesifiset terpeenit kohdistuvat ASD:hen liittyviin kohteisiin: Linalool (laventelin pääkomponentti) moduloi GABA-A-reseptoreita bentsodiatsepiinin sitoutumiskohdassa ja vaikuttaa serotergisiin signalointireitteihin; β-karyofylleeni toimii selektiivisenä CB2-reseptoriagonistina, jolla on neuroinflammaatiota ehkäiseviä ominaisuuksia; Boswelliahapot (suitsuke) aktivoivat Nrf2/HO-1-antioksidanttireitin ja vähentävät mikrogliasolujen aktivaatiota; 1,8-sineoli (eukalyptus) osoittaa ahdistusta lievittäviä vaikutuksia GABA-A-modulaation kautta; α-pineeni toimii GABAergisesti; Cananga odorata (ylang-ylang) vaikuttaa serotoniinin ja dopamiinin aineenvaihduntaan prekliinisissä ASD-malleissa.
Kliininen näyttö autismikirjon häiriöissä (ASD) on rajallista: Satunnaistetussa, kontrolloidussa bergamottitutkimuksessa ei havaittu merkittäviä ahdistusta lievittäviä vaikutuksia ASD-lapsilla. Pienet pilottitutkimukset raportoivat parantuneesta hoitomyöntyvyydestä sovelletun käyttäytymisanalyysin (ABA) aikana laventeliaromaterapialla, lisääntyneestä jaetusta tarkkaavaisuudesta aromaterapiahieronnan jälkeen sekä mahdollisista vaikutuksista uneen ja ahdistukseen. Näytön laatu on kuitenkin rajallinen pienten otoskokojen, metodologisen heterogeenisyyden ja uusintatutkimusten puutteen vuoksi.
Organik Aromas Nebulizer 3.0:lle (Venturi-periaate, vesitön kylmäsumutus) kehitetään tilakohtaisia annostelusuosituksia: 2–4 tippaa 10–20 m²:lle, 4–6 tippaa 20–40 m²:lle, 6–10 tippaa 40–60 m²:lle, käyttöajat 15–30 minuuttia ja tauot 30–60 minuuttia. ASD-spesifiset piirteet edellyttävät asteittaista aloittamista sensorisen yliherkkyyden vuoksi, vuorokausirytmiin mukautettuja protokollia (aktivoiva aamuisin, rauhoittava iltaisin) ja tiukkaa laadunvalvontaa (GC/MS-analyysi).
Turvallisuusnäkökohdat sisältävät varovaisuuden epilepsiassa (kamferia sisältävät öljyt), eukalyptuksen vasta-aiheisuuden alle 3-vuotiailla lapsilla, mahdolliset yhteisvaikutukset antipsykoottien (risperidoni, aripipratsoli) kanssa ja sensorisen yliherkkyyden erityishuomion ASD:ssä. Mekanistinen uskottavuus on olemassa, mutta laadukkaita, satunnaistettuja, kontrolloituja tutkimuksia puuttuu. Eteerisiä öljyjä voidaan harkita osana monimuotoista hoitomenetelmää samanaikaisten oireiden (ahdistus, unihäiriöt, sensorinen dysregulaatio) hoidossa, mutta ne eivät korvaa näyttöön perustuvia perushoitoja.
ADHD ja metyylifenidaatti
Apuhoito eteerisillä öljyillä ADHD:ssä – metyylifenidaatin farmakodynamiikka, terpeenit, reseptorit, annostelu Organik Aromas Nebulizer 3.0 -laitteella
Johdanto
Tarkkaavaisuus- ja ylivilkkaushäiriö (ADHD) on yksi yleisimmistä lapsuuden ja nuoruuden neuropsykiatrisista häiriöistä, ja se esiintyy 5–7% lapsista ja 2,5–4% aikuisista. Metylfenidaatti (MPH), dopamiinin ja noradrenaliinin takaisinoton estäjä, on farmakologinen ensilinjan hoito ja osoittaa kliinistä tehoa 70–80% potilaista. [A1], [A2].
Huolimatta metyylifenidaatin vakiintuneesta tehokkuudesta osalla potilaista esiintyy jäännös-oireita, sivuvaikutuksia tai halua täydentäviin hoitomuotoihin. Eteerisiä öljyjä pohditaan yhä enemmän mahdollisena lisähoitovaihtoehtona, vaikkakin tieteellinen näyttö on tähän mennessä ollut hajanaista. [A3], [A4].
Raportin tavoite
Tämä raportti pyrkii saavuttamaan viisi päätavoitetta:
- Intrakraniaalisten metyylifenidaattipitoisuuksien kvantifiointi PET/SPECT-tietojen perusteella, mukaan lukien DAT-saturaatio, plasma-aivo-suhteet ja alueellinen jakauma
- Mekanisminen arviointi Eteeristen öljyjen liitännäishoidon uskottavuus molekyylitason vaikutusmekanismien perusteella
- Näyttöön perustuva analyysi erityisiä eteerisiä öljyjä ja niiden pääkomponentteja
- Käytännöllisten annostussuositusten kehittäminen Organik Aromas sumuttimeen 3.0
- Yleisten turvallisuusohjeiden laatiminen ADHD-potilaiden hoitoon
Analyysi integroi tietoja 87 metyylifenidaattia koskevasta aivopitoisuustutkimuksesta ja 159 eteerisiä öljyjä koskevasta julkaisusta, keskittyen 30 asiaankuuluvimpaan julkaisuun.
Metyylifenidaatti – Aivonsisäiset pitoisuudet ja farmakodynamiikka
DAT-vartija – Annos-vaikutussuhteet
Metyylifenidaatin terapeuttinen tehokkuus korreloi suoraan dopamiinitransportterin (DAT) sitoutumisen kanssa striatumissa. PET-tutkimukset [¹¹C]kokaiinin avulla ovat osoittaneet selkeän annos-vaste-suhteen. [A9].
Taulukko 1: DAT-okkupanssi metyylifenidaatin suun kautta annon jälkeen
Lähde: Volkow et al. 1998 [A9]; Mittaukset terveillä aikuisilla
Arvioitu annos 50% DAT-estäytymiseen (ED₅₀) on 0,25 mg/kg kehonpainoa [A9]. Terapeuttiset painoon mukautetut annokset (0,3–0,6 mg/kg) tuottavat siten johdonmukaisesti >50 % DAT-okkupanssin (%), jota pidetään kliinisen tehokkuuden kynnysarvona [A7], [A9].
Alueelliset erot DAT-sitoutuvuus vaihtelee striatumin aliregioiden välillä. Spencer ym. (2009) raportoivat OROS-MPH:n (40 mg) 10 tunnin jälkeen seuraavat sitoutuvuusarvot: oikea nucleus caudatus 44,3±11,8%, vasen nucleus caudatus 42,7±10,9%, oikea putamen 41,6±11,7%, vasen putamen 41,3±13,1% [A17].
ADHD-potilailla SPECT-tutkimukset [¹²³I]β-CIT:llä osoittavat merkittävän striataalisen DAT-sitoutumisen vähenemisen metyylifenidaattihoidon aikana. Aster et al. (2021) dokumentoivat 27,6–29,9%vähenemisen striataalisessa DAT-sitoutumispotentiaalissa (BP) lääkitystä saavilla lapsilla ja nuorilla, joilla oli ADHD. [A25], [A18].
Plasman ja aivojen pitoisuudet
Plasman pitoisuudet
Aikuisten terapeuttinen plasmapitoisuusalue d-treo-metyylifenidaatille on 3,5–7,8 ng/ml [A20], [A24]. 5,7–6,0 ng/ml:n plasmapitoisuus liittyy 50% DAT-estäjä. [A9], [A13], [A17].
Pediatrisilla potilailla havaittiin korkeampia huippupitoisuuksia: 20 ng/ml kaksi tuntia 20 mg annoksen (0,8 mg/kg) jälkeen [A20], [A24].
Aivojen kuvantaminen
PET-tutkimukset [¹¹C]metyylif Eenidaatilla osoittavat, että 7,5±1,5% suonensisäisesti annetusta aktiivisuudesta pääsee aivoihin [A5], [A14]. Korkein pitoisuus saavutetaan striatumissa, ja d-treo-MPH:lle basaaliganglioiden ja pikkuaivojen jakaumatilavuussuhde (DVR) on 2,2–3,3. [A16], [A14].
Kriittinen näyttöaukko
Metaanietyylifenidaattipitoisuuksien suorat mittaukset aivokudoksessa (ng/ml tai nmol/l) tai selkäydinnesteessä puuttuvat ihmiskirjallisuudesta. Kaikki saatavilla olevat tiedot perustuvat PET/SPECT-havaittavuusmittauksiin tai jälkiaineiden jakautumistutkimuksiin. [A1], [A2], [A3], [A4], [A5], [A6], [A7], [A8], [A9].
Alueellinen jakautuminen – tyvitumakkeet ja etuotsalohko
Tyvitumakkeet
Striatum näyttää ensisijaisena kohdealueena korkeimman [¹¹C]metyylifenidaatin otaksunnan. Esilääkitys merkitsemättömällä metyylifenidaatilla (0,5 mg/kg) vähentää striataalista jäljittimen sitoutumista 40% [A5]. Striatumin puhdistuma on noin 90 minuuttia, huomattavasti hitaampi kuin kokaiinin (20 minuuttia) [A5].
Etuaivokuoren otsalohko
Vaikka DAT-tiheys on pienempi etuotsalohkossa (PFC) kuin tyvitumakkeessa, toiminnalliset PET-tutkimukset [¹¹C]rakloridilla osoittavat merkittävää dopamiinin lisääntymistä myös etuotsalohkon ja ohimolohkon alueilla metyylifenidaatin jälkeen. [A30], [A22]. Nämä aivokuoren dopamiinin lisääntymiset korreloivat pitkäaikaisten oireiden paranemisen kanssa ADHD-potilailla [A30].
Noradrenaliinin kuljettaja (NET)
Metyylifenidaatti estää myös noradrenaliinin takaisinoton ED₅₀-arvolla 0,14 mg/kg [A11]. PET-tutkimukset [¹¹C]MRB:llä osoittavat vahvaa NET-peittyvyyttä talamuksessa ja ponsissa 75–195 minuuttia annostelun jälkeen [A11], [A21].
Aikasarja ja farmakokinetiikka
Suonensisäinen anto
[¹¹C]metyylifeniiddaatin i.v.-injektion jälkeen aivojen pitoisuus saavuttaa huippunsa 8–10 minuutissa [A3], [A6].
Selvä juttu Gabe
Aivojen maksimaalinen imeytyminen suun kautta annosteltuna tapahtuu huomattavasti viivästyneenä, huippu saavutetaan 60–90 minuutin kuluttua [A7], [A9], [A3]. Tämä viivästynyt kinetiikka selittää suun kautta otettavien valmisteiden vähäisemmän väärinkäyttöpotentiaalin verrattuna suonensisäisiin annosteluihin. [A13].
Retardointikaavoitukset
Pitkävaikutteiset valmisteet (OROS-MPH, DBDS-MPH) osoittavat vielä hitaampaa alkua viivästyneellä DAT-okklusiolla maksimiin, mutta verrattavilla huippukonssentraatioilla [A13], [A17]. OROS-MPH saavuttaa 10 tunnin kuluttua merkittävästi korkeampia DAT-sitoutumisasteita kuin DBDS-MPH (44,3% vs. 34,8% oikeassa caudatus-tumakkeessa) korkeammilla pitoisuuksilla plasmassa (5,2 vs. 3,8 ng/ml) [A17].
Nähdeukliniset mikrodialyysitiedot
Rotissa d-treo-metyylifenidaatti lisää dopamiinin solunulkoista pitoisuutta tyvitumakkeessa ~650% [A16]. Tämä massiivinen dopamiinin lisääntyminen osoittaa DAT-estäjän funktionaalisen vaikutuksen synaptiseen välitykseen.
Eteeriset öljyt lisähoitona – Mekanistiset perusteet
Komplementaariset toimintamekanismit metyylifenidaatille

Kuva 1: Eteeristen öljyjen molekulaariset signalointireitit ADHD:ssä – Dopaminerginen järjestelmä, Noradrenerginen järjestelmä ja täydentävät terpeenien vaikutusmekanismit
Eteeristen öljyjen liitännäishoidon uskottavuus perustuu täydentäviin, ei-päällekkäisiin vaikutusmekanismeihin verrattuna metyylifenidaattiin. Vaikka MPH estää ensisijaisesti dopamiinin ja noradrenaliinin takaisinottoa, eteeristen öljyjen komponentit vaikuttavat lisäksi neurobiologisiin järjestelmiin.
Mekaaninen komplementaarisuus
- GABAerginen modulaatio
Mentoli ja linalooli toimivat positiivisina allosteerisina modulaattoreina GABA-A-reseptoreissa, mikä vahvistaa inhiboivaa neurotransmissiota ja voi vähentää hyperaktiivisuutta. [A19], [A20], [A23]. - Serotonerge effektit
Linalooli sitoutuu serotoniinin kuljettajaproteiiniin (SERT) ja moduloi 5-HT1A-reseptoreita, mikä välittää ahdistusta lievittäviä ja mielialaa tasapainottavia vaikutuksia. [A21], [A23], [A24]. - Anti-inflammatoriset signaalireitit
β-karyofylleeni aktivoi CB2-reseptoreita ja vähentää neuroinflammatorisia prosesseja NF-κB- ja MAPK-signalointireittien kautta, jotka voivat olla koholla ADHD:ssä [A14]. - TRP-kanavan modulaatio
Mentoli (TRPM8-agonisti) ja 1,8-sineoli (TRPV1/TRPA1-modulaattori) vaikuttavat neuronien ärtyvyyteen ja ionivirtoihin monoaminergisistä järjestelmistä riippumatta [A19].
Reseptorit ja signalointireitit
Taulukko 2: Eteeristen öljykomponenttien reseptorikohteet
LEO = Laventeliöljy; nAChR = nikotiininen asetyylikoliinireseptori
GABA-A-reseptorin modulaatio
Mentoli sitoutuu GABA-A-reseptoreihin pitoisuusriippuvaisesti ja vahvistaa inhibitoivaa neurotransmissiota [A19]. Mielenkiintoista kyllä, laventeliöljy ei osoita affiniteettia GABA-A-reseptorin bentsodiatsepiin-sitoutumiskohdalle, mikä viittaa suotuisampaan turvallisuusprofiiliin verrattuna bentsodiatsepiineihin. [A23].
Serotoniinin transkportteri (SERT)
Linalooli ja laventeliöljy sitoutuvat SERT:iin pitoisuuksilla 0,08–0,8% in vitro [A23]. Tämä SERT-inhibointi saattaa välittää masennusta ja ahdistusta lievittäviä vaikutuksia, jotka ovat merkityksellisiä ADHD-potilailla, joilla on samanaikaisia ahdistuneisuushäiriöitä (25–40% esiintyvyys).
NMDA-reseptoriantagonismi
Laventeliöljy osoittaa annosriippuvaista NMDA-reseptoriantagonismia, jonka IC₅₀ on 0,04 µl/ml [A23]. NMDA-reseptorien modulaatio on relevantti synaptisen plastisuuden ja oppimisprosessien kannalta.
CB2-reseptorin aktivoituminen
β-karyofylleeni on selektiivinen CB2-agonisti ilman psykoaktiivisia vaikutuksia (ei CB1-aktivaatiota). CB2-aktivaatio vähentää mikrogliasolujen aktivaatiota ja proinflammatoristen sytokiinien tuotantoa (TNF-α, IL-1β, IL-6), mikä voi välittää neuroprotektiivisia vaikutuksia. [A14].
Synergiapotentiaalit
Metylfenidaatin ja eteeristen öljyjen yhdistelmä voi tuottaa synergisiä vaikutuksia useilla mekanismeilla:
- Dopamiini-GABA-tasapaino
Vaikka MPH lisää dopaminergista transmissiota, mentolin/linaloolin GABAergisen modulaation kautta voitaisiin edistää tasapainoisempaa kiihottumis-estäytymiskyvyn tasapainoa ja vähentää hyperaktiivisuutta. - Stressin vähennys
Linaloolin ahdistusta lievittävät vaikutukset 5-HT1A-reseptorien kautta ja kortisolin väheneminen (24–38% vähennys kliinisissä tutkimuksissa) [A24] voisivat parantaa ADHD-potilaiden stressireaktiivisuutta. - Kognitiivinen vahvistaminen
Mentolin kolinerginen modulaatio (asetyylikoliiniesteraasin estyminen) [A19] ja 1,8-cineolin muistia edistävät vaikutukset voivat vahvistaa MPH:n kognitiivisia parannuksia. - Neuroprotektio
β-karyofylleeni ja 1,8-kineoli tarjoavat tulehdusta ehkäisevien ja antioksidanttisten ominaisuuksiensa ansiosta mahdollisesti pitkäaikaisia neuroprotektiivisia vaikutuksia.
Tärkeä rajoitus: Nämä synergistiset potentiaalit ovat teoreettisesti uskottavia, mutta niitä ei ole validoitu kliinisissä tutkimuksissa ADHD-potilailla. MPH:n ja eteeristen öljyjen yhdistelmää koskevia kontrolloituja tutkimuksia puuttuu kokonaan.
Erityiset eteeriset öljyt – vaikuttavat aineet ja todisteet
Laventeli (Lavandula angustifolia) – Linalooli
Tärkeimmät vaikuttavat aineet
Linalool (25–45%)
Linalyyliasetaatti (25–45%)
1,8-Sineoli (1–3%)
Mekanismit
- SERT-sitoutuminen
Linalooli ja laventeliöljy sitoutuvat serotoniinin kuljettajaproteiiniin, mikä voi välittää masennuslääkkeitä. [A23]
- NMDA-antagonismi
Laventeliöljy estää annoksesta riippuen NMDA-reseptoreita (IC₅₀: 0,04 µl/ml) [A23]
- GABA-Modulaatio
Inhibitorisen hermovälityksen vahvistaminen GABA-A-reseptorien kautta (ei bentsodiatsepiinisitoutumispaikan kautta) [A20], [A23]
- Monoaminergiset vaikutukset
Linalool moduloi dopamin-, noradrenaliini- ja serotoniinijärjestelmiä prekliinisissä malleissa [A21]
Kliininen näyttö
- Kognitio
Moss et al. (2003) osoittivat 144 terveen aikuisen otoksella, että laventelin aromaterapia heikensi työmuistia ja hidasti reaktioaikoja, mutta vaikutti subjektiivisesti rauhoittavasti. [A27]
- Huomio
Colzato ym. (2014) havaitsivat, että laventelin tuoksu vähensi “attentional blink” -ilmiötä (ajallisia tarkkaavaisuuspuutteita), mikä viittaa laajempaan tarkkaavaisuuden jakaumaan. [A30]
- Ahdistuksen lievitys
Oraalinen Silexan (80 mg/vrk laventeliöljyä) vähensi yleistyneitä ahdistusoireita verrattavissa loratsepaamiin [A26]
- Stressin vähennys
Laventeliöljyn hengittäminen laski kortisolin tasoa 24–38% kliinisissä tutkimuksissa [A24]
ADHD-spesifistä dataa
Ei satunnaistettuja kontrolloituja tutkimuksia ADHD-potilailla. Tapausselostukset kuvaavat positiivisia vaikutuksia agitaatioon ja uneen epätyypillisillä lapsilla, joilla on ADHD. [A8].
Annostus (prekliininen/kliininen)
– Suun kautta: 50–100 µl kapseloituna (Kennedy-tutkimus) [A19]
– Hengitys: 4 tippaa 30 ml:aan vettä (diffuuseri) [A30]
– Paikallinen: 1,5% laimennus kantajaöljyyn [A8]
Turvallisuus
Laventeliöljy ei osoittanut solujen neurotoksisuuden vahvistumista in vitro [A23].
Ei vakavia sivuvaikutuksia kliinisissä tutkimuksissa suositelluilla annoksilla.
Rosmariini (Rosmarinus officinalis) – 1,8-kineoli
Tärkeimmät vaikuttavat aineet
1,8-sineoli (eukalyptoli, 20–50%)
Kamferi (10–20%)
α-pineniä (10–15%)
Mekanismit
- Kolinerginen Modulaatio
Asetyylikoliiniesteraasin esto, joka vahvistaa kolinergistä neurotransmissiota [A27]
- TRP-kanavan aktivointi
1,8-Kineoli moduloi TRPV1:tä ja TRPA1:tä, mikä vaikuttaa hermosolujen ärtyvyyteen
- Anti-inflammatoriset
NF-κB:n ja MAPK-signalointireittien esto, tulehdusta edistävien sytokiinien väheneminen
- Antioksidantti
Nrf2-signalointireitin aktivointi, antioksidatiivisten entsyymien lisääntyminen
Kliininen näyttö - Muisti
Moss et al. (2003) osoittivat n=144 terveellä aikuisella merkitseviä parannuksia kokonaismuistissa ja sekundäärimuistissa rosmariiniaromaterapian jälkeen verrattuna kontrolli- ja laventeliryhmiin. [A27]
- Kognitiivinen suorituskyky Rosmariinin tuoksulle altistuminen korreloi parantuneen kognitiivisen suorituskyvyn kanssa [A14]
- Valppaus Rosmariini lisäsi valppautta ja aktiivisuutta aivoissa [A29]
ADHD-spesifistä dataa
Rosmariinia mainitaan yleiskatsauksissa potentiaalisesti hyödyllisenä ADHD:lle. [A10], [A4], [A5], mutta ADHD-potilailla ei ole kontrolloituja kliinisiä tutkimuksia.
Annostus
– Hengitys: Ympäristöaltistus testimiljöössä (pitoisuutta ei määritellä) [A27]
– ADHD:lle ei ole standardoituja annostussuosituksia
Turvallisuus
Rosmariinia pidetään turvallisena inhaloituna tavanomaisina pitoisuuksina.
Varoitus epilepsiapotilaille kamferipitoisuuden vuoksi.
Piparminttu (Mentha × piperita) – Mentoli
Tärkeimmät vaikuttavat aineet
Mentoli (30–50%)
Menthoni (10–30%)
1,8-Kineoli (5–10%)
Mekanismit
- TRPM8-aktivaatio
Mentoli on voimakas TRPM8-agonisti (EC₅₀ ~30 µM), joka välittää kylmyysaistimusta ja hermostollista modulaatiota [A19]
- GABA-A-modulaatio
Konsentraatiosta riippuva sitoutuminen ja positiivinen allosteerinen modulaatio [A19]
- Nikotiinireseptorit
Nikotiinisten asetyylikoliinireseptorien modulaatio, kolinergisen transission vaikuttaminen [A19]
- Asetyylikoliiniesteraasin esto
Piparminttuöljy estää merkittävästi asetyylikoliiniesteraasia, mikä vahvistaa kolinergistä neurotransmissiota. [A19]
Kliininen näyttö - Keskittymiskyky
Kennedy ym. (2018) osoittivat kaksoissokkotutkimuksessa (n=24 terveitä aikuisia), että 100 µL piparminttuöljyä paransi suoriutumista Rapid Visual Information Processing (RVIP) -testissä 1–3 tuntia nauttimisen jälkeen. [A19]
- Väsymyksen vähennys Molemmat annokset (50 µL ja 100 µL) vähensivät väsymystä ja paransivat sarjasubtraktiota 3 tunnin jälkeen. [A19]
- Tarkkaavaisuuden säätely Colzato et al. (2014) havaitsivat, että piparminttuaromi voimisti “tarkkaavaisuushäiriötä”, mikä viittaa keskittyneempään (vähemmän hajautuneeseen) tarkkaavaisuuteen. [A30]
ADHD-spesifistä dataa
Ei satunnaistettuja kontrolloituja tutkimuksia ADHD-potilailla. Piparminttua mainitaan ADHD:ta koskevissa katsausartikkeleissa mahdollisesti hyödyllisenä. [A4], [A5], [A29].
Annostus
– Suun kautta (kapseloitu): 50–100 µl puhdasta öljyä [A19]
– Hengitys: 4 tippaa 30 ml:aan vettä (diffuuseri) [A30]
Turvallisuus
Piparminttuöljy on turvallista inhalaatio- ja suun kautta nautittuna suositeltujen annosten mukaan.
Varoitus imilla ja pienillä lapsilla (kurkunpään kouristuksen riski suorassa nenään annostelussa).
Mustapippuri (Piper nigrum) – β-karyofylleeni
Tärkeimmät vaikuttavat aineet
β-Karyofylleeni (10–35%)
Limonen (15–25%)
Sabinen (10–20%)
Mekanismit
- CB2-agonismi
β-karyofylleeni on selektiivinen CB2-reseptoriagonisti (Ki: 155±4 nM) ilman CB1-aktivaatiota (ei psykoaktiivisia vaikutuksia) [A14]
- Anti-inflammatoriset
TNF-α:n, IL-1β:n ja IL-6:n väheneminen NF-κB-inhibition kautta [A14]
- Mikrogliasäätely
M1-mikroglian ohjelmointi uudelleen M2-mikrogliafenotyypiksi, hermotulehdusprosessien vähentäminen
- Neuroprotektiivinen
Oksidatiivisen stressin väheneminen Nrf2:n aktivaation kautta
Kliininen näyttö
- Präkliininen
Beeta-karyofylleeni osoitti ahdistusta lievittäviä vaikutuksia eläinmalleissa, mahdollisesti muuttamalla neuronien aktiivisuutta keskusamygdalan ytimessä. [A14]
- Anti-inflammatoriset
In vitro- ja in vivo -tutkimukset osoittavat vahvoja anti-inflammatorisia vaikutuksia CB2-aktivaation kautta.
ADHD-spesifistä dataa
Ei kliinisiä tutkimuksia ADHD-potilailla. Mekanistinen uskottavuus perustuu neuroinflammatorisiin hypoteeseihin ADHD:ssä.
Annostus
Inhalatiiviseen käyttöön ADHD:lle ei ole saatavilla standardoituja annostussuosituksia.
Turvallisuus
β-karyofylleeniä pidetään turvallisena (FDA:n GRAS-status).
Ei tunnettuja vakavia sivuvaikutuksia tavanomaisilla annoksilla.
Vetiver (Chrysopogon zizanioides)
Tärkeimmät vaikuttavat aineet
Vetiveroli
Khusimoli
α-Vetivoni
β-Vetivoni
Mekanismit
- Anksiolyyttinen
Prekliiniset tutkimukset osoittavat anksiolyyttisiä vaikutuksia, mahdollisesti amygdalan aktiivisuuden modulaation kautta [A14]
- Rauhoittava
Perinteisesti käytetty hermoston rauhoittamiseen
Kliininen näyttö
- ADHD-spesifinen
Springer et al. (2018) raportoivat, että vetiveriinhalaatio (3 kertaa päivässä 30 päivän ajan) osoitti parannuksia lasten aivojen toiminnassa ja käyttäytymisessä. [A29]
- Rajoitukset
Ei kontrolloituja satunnaistettuja tutkimuksia; näytön perusteena tapausselostukset ja perinteinen käyttö
ADHD-spesifistä dataa
Godfrey (2001) mainitsee vetiverin mahdollisesti hyödyllisenä ADHD:n hoidossa. [A3], [A4], [A5], mutta yksityiskohtaiset kliiniset tiedot puuttuvat.
Annostus
– Inhalaatio: 3 kertaa päivässä 30 päivän ajan (tarkkaa pitoisuutta ei määritelty) [A29]
Turvallisuus
Vetiveriä pidetään turvallisena hengitettynä. Ei tunnettuja vakavia sivuvaikutuksia.
Seder (Cedrus spp.)
Tärkeimmät vaikuttavat aineet
α-cedreen
β-cedreen
Tuijopseeni
Cedrol
Mekanismit
- Hapetus
Perinteisesti käytetty aivojen hapettumisen parantamiseen [A29]
- Rauhoittava
Sedatiiviset ominaisuudet perinteisessä käytössä
Kliininen näyttö
- ADHD-spesifinen
Godfrey (2001) mainitsee setripuun mahdollisesti hyödyllisenä ADHD:n hoidossa [A3], [A4], [A5]
- Rajoitukset
Ei kontrolloituja kliinisiä tutkimuksia; näyttö perustuu perinteiseen käyttöön ja anekdootteihin
ADHD-spesifistä dataa
Springer et al. (2018) mainitsevat setripuuta aivojen hapetukseen ADHD:ssä [A29], mutta kvantitatiivista dataa puuttuu.
Annostus
Ei standardoituja annostussuosituksia saatavilla.
Turvallisuus
Setripuun eteeristä öljyä pidetään turvallisena sisäänhengityskäytössä tavanomaisina pitoisuuksina.
Kaneli (Cinnamomum verum) – Kanelaldehydi
Tärkeimmät vaikuttavat aineet
Sinnambi (60–75%)
Eugenoli (5–10%)
Mekanismit
- Dopamiininen modulaatio
Kanelin allyylibentseeni ja propenyylibentseeni ovat amfetamiinin esiasteita ja muuttuvat metaboloitumisen jälkeen amfetamiiniksi, jolla on piristävä vaikutus. [A2]
- TRPA1/TRPV1-aktivaatio
Sinneldehydi aktivoi TRPA1- ja TRPV1-kanavia
- Antimikrobinen
Vahvat antimikrobiset ominaisuudet
Kliininen näyttö - ADHD-spesifinen
Chen ym. (2008) tekivät tutkimuksen kaneli-aromaterapiasta ADHD-lapsilla. kuntoutuksen ja kaneli-aromaterapian (1% kanelia, 1 g 100 ml:ssa vettä, nenähengitys) yhdistelmä näytti 6 kuukauden jälkeen merkittävästi parempia tuloksia SNAP-IV-kyselyssä (58±2,6 vs. kontrolli) ja aktiivisuustasoissa (102±5,8) verrattuna pelkkään kuntoutukseen (p<0,05). [A2], [A1]
ADHD-spesifistä dataa
Chenin tutkimus on yksi harvoista, nimenomaan ADHD-lapsilla tehtyistä eteerisillä öljyillä toteutetuista kliinisistä tutkimuksista, mutta siinä on metodologisia rajoituksia (ei tietoa satunnaistamisesta, sokkouttamisesta tai otoskoosta).
Annostus
– Hengitys: 1% kanelia (1 g 100 ml:ssa vettä) 50 m² hoitohuoneessa sähköisellä valonohjauksella [A2]
Turvallisuus
Kaneliöljy voi korkeina pitoisuuksina aiheuttaa iho- ja limakalvoärsytystä.
Varo herkkiä henkilöitä.
Kanelin metaboliittien dopaminerginen stimulaatio vaatii lisätutkimuksia metyylifenidaatin yhteisvaikutusten osalta.
Lisää ADHD:lle osoitettuja eteerisiä öljyjä
Viimeisimmän kirjallisuuskatsauksen perusteella voitiin tunnistaa seuraavia lisäeetterisiä öljyjä, jotka voivat olla relevantteja ADHD:n hoidossa neurobiologisesti uskottavien mekanismien kautta.
Melissa officinalis (sitruunamelissa) – rosmariinihappo, flavonoidit
Aktiiviset ainesosat
Rosmariinihappo
Flavonoidit (Luteoliini, Apigeniini)
haihtuvat öljyt (sitraali, linalooli, geranioli)
Reseptorit ja toimintamekanismit
– Kolinergiset reseptorit: Nikotiiniset (nAChR) ja muskariiniset (mAChR) sitoutuminen
– GABAerginen modulaatio: Rosmariinihappo estää GABA-transaminaasia → lisääntynyt GABA-saatavuus
– Asetyylikoliiniesteraasin estäminen: Parantunut kolinerginen hermovälitys aivokuoren etulohkossa
Kliininen näyttö
- RCT (n=20, kaksoissokko, ristiinaseteltu)
Yksittäisannokset 300/600/900 mg p.o. osoittivat 600 mg:n annoksella merkittävää tarkkaavaisuuden tarkkuuden (Accuracy of Attention) paranemista sekä muistiin ja virkeyteen liittyviä vaikutuksia [A31]
- Kombinaatiotutkimus (Lapset, 7 viikkoa)
Valeriaana-melissauuteyhdistelmä paransi merkittävästi ylivilkkautta, keskittymisvaikeuksia ja impulsiivisuutta ala-asteikäisillä lapsilla [A32]
- Antistress-ristikko
Standardoidut sitruunamelissavalmisteet elintintarvikemuodossa vähensivät kognitiivista ylikuormitusta ja paransivat mielialaa terveillä aikuisilla [A33]
Annostus (Organik Aromas Nebulizer 3.0)
– 3–5 tippaa sitruunamelissaa (GC/MS-puhdasta) 15–25 m² tilaan
– Käyttö: 30 minuuttia ennen keskittymistä vaativia vaiheita, 2–3 kertaa päivässä
– Yhdistelmä laventelin kanssa (2:1) suositeltu iltaisin/rentoutumiseen
Turvallisuus
Hyvin siedetty
Mahdollinen yhteisvaikutus kilpirauhaslääkkeiden kanssa (TSH-suppressio suurilla suun kautta otettavilla annoksilla)
Inhalointi katsotaan turvalliseksi.
Eukalyptus (Eucalyptus globulus / radiata) – 1,8-kineoli
Aktiiviset ainesosat
1,8-Sineoli (Eukalyptoli, 70–85%)
α-pineeni
Limes
Reseptorit ja toimintamekanismit
– GABA-A/Bentsodiatsepiinikohta: Modulatorinen aktiivisuus (ahdistusta lievittävä, sedatiivinen suuressa annoksessa)
– Kolinergiset reitit: 1,8-sineoli estää asetylkolinesteraasia → parantunut tarkkaavaisuus ja työmuisti
– Antioksidanttinen/neuroprotektiivinen: Oksidatiivisen stressin vähentäminen hermosoluissa
Kliininen näyttö
– Neuroprotektive Reviews listaa Eucalyptus globulus -kasvin kognitiivisia vaikutuksia eläin- ja ihmistutkimuksissa [A34]
– 1,8-kineoli on myös rosmariinin (jo raportissa) pääainesosa, eukalyptuksessa pitoisuus on suurempi.
– Inhalaatiotutkimukset osoittavat mielen selkeyden ja keskittymiskyvyn paranemista (vertailututkimukset rosmariinin kanssa)
Annostus (Organik Aromas Nebulizer 3.0)
– 2–3 tippaa tiloille 15–25 m² (voimakas tuoksu, annostele säästeliäästi)
– Käyttö: Aamulla/päivällä keskittymisjaksoihin, enintään 20 min
- Vasta-aihe
Ei alle hidas 3-vuotiaille
Ei yhdessä astmalääkkeiden kanssa ilman lääkärin neuvoa
Turvallisuus
Vahva öljy, älä levitä laimentamattomana iholle
Lapset < 3 vuotta: vasta-aiheinen
Epileptikko: Varo
Inkivääri (Zingiber officinale) – Gingeroli, Zingiberiini
Aktiiviset ainesosat
6-Gingeroli
6-Shogaoli
Singeberen
β-Seskvifellandreeni
Reseptorit ja toimintamekanismit
Serotoniini-5-HT3-reseptoriantagonismi: ahdistusta lievittävä komponentti
– Dopaminerg: Inkivääri vaikuttavat dopaminergiseen aktiivisuuteen tyvitumakkeessa (eläin)
– Antioksidantti/anti-neuroinflammatorinen: NF-κB:n esto, TNF-α:n vähentäminen
Kliininen näyttö
– Prekliiniset tutkimukset: Inkivääriuute paransi kognitiivisia toimintoja ADHD-eläinmalleissa
– Neuroprotektiiviset ominaisuudet hyvin dokumentoitu antioksidatiivisten mekanismien kautta
– Suoria ADHD:ta koskevia satunnaistettuja kontrolloituja tutkimuksia puuttuu vielä kirjallisuudesta
Annostus (Organik Aromas Nebulizer 3.0)
– 2–3 tippaa tiloihin 15–25 m²
– Yhdistelmä rosmariinin kanssa (1:1) kognitiiviseen aktivointiin
Annostussuositukset Organik Aromas Nebulizer 3.0 -laitteelle
Tekniset perusteet: Venturi-periaate ja sumutus
The Organik Aromas Nebulizer 3.0* hyödyntää Venturi-periaatetta vedettömään kylmäsumutukseen eteerisistä öljyistä. Tämä menetelmä tarjoaa useita etuja:
Tekniset ominaisuudet
- Kylmäsumutus
Ei lämpövaikutusta, kaikki haihtuvat komponentit ja lämpöherkät vaikuttavat aineet säilyvät
- Vesivapaa
Puhtaiden eteeristen öljyjen suora sumuttaminen laimentamatta, korkeampi vaikuttavien aineiden pitoisuus huoneilmassa
- Partikkelikoko
Mikropartikkelien (1–5 µm) tuottaminen, jotka pääsevät syvälle hengitysteihin ja voivat läpäistä veri-aivoesteen
- GC/MS-sertifioidut puhtaat öljyt
Analyyttisesti testattujen, lisäaineettomien, kantajaöljyjen tai synteettisten tuoksujen käyttö
noin 110–120 USD (verkko-/akkukäyttöinen)
- ilmainen toimitus maailmanlaajuisesti
- Huomioi tulli- ja maahantuontiverot!
Farmakokineettiset näkökohdat
Eteeristen öljyjen inhalaatio tapahtuu kahta pääreittiä pitkin:
1. Hajureitti
Suora yhteys hajuepiteelistä limbiseen järjestelmään (amygdala, hippokampus) ja otsalohkon etuosan aivokuoreen hajukäämin kautta
2. Keuhkoreitti
Imeytyminen alveolikalvon läpi systeemiseen verenkiertoon, veri-aivoesteen ylitys [A29]
Huoneen koko ja tippamäärä
Peruskaava
Tippojen määrä tulisi sovittaa tilan kokoon terapeuttisesti tehokkaan, mutta ei liiallisen pitoisuuden saavuttamiseksi.
Taulukko 3: Annostussuositukset huonekoon mukaan
*Oletus: Huonekorkeus 2,5 m **Arvioitu pitoisuus perustuen ~1 mg eteeristä öljyä per tippa ja täydelliseen sumutukseen
Laskentaperuste
– 1 tippa eteeristä öljyä ≈ 0,05 ml ≈ 40–50 mg (tiheydestä riippuen)
– Kohdekonsentraatio: 80–200 µg/m³ (perustuu ambient-aromaterapiatutkimuksiin)
– Kaava: Tipat = (Tilan tilavuus × Tavoitepitoisuus) / (Massa per tippa × 1000)
Käyttöaika ja tauot
Istunnon kesto
- Akuutti käyttö
15–30 minuuttia per istunto
- Jatkuva taustahajonta
30–60 minuuttia taukoineen
Taukovälit
Hajuaistiin sopeutuminen (tottuminen) tapahtuu 15–30 minuutin jatkuvan altistuksen jälkeen.
Hoitovaikutusten ylläpitämiseksi suositellaan taukovälejä:
Taulukko 4: Käyttö- ja taukoaikataulu
Hajuaistillinen sopeutuminen
Kun altistuminen on jatkunut 20–30 minuuttia, hajuaistin tietoinen havaitseminen vähenee, mutta neurobiologiset vaikutukset voivat säilyä.
30–60 minuutin tauot mahdollistavat hajureseptorien herkistymisen uudelleen.
Vuorokaudenaika ja käyttöskenaariot
Eteeristen öljyjen valinta tulisi räätälöidä vuorokaudenajan ja ADHD:n erityisoireiden mukaan:
Taulukko 5: Vuorokaudenajan mukainen öljynvalinta
Käyttötapaukset
- Schulvorbereitung/Morgenroutine
– Olut: Rosmariini tai piparminttu
– Tavoite: Aktivoituminen, virkeys, keskittyminen Annostus: 6–8 tippaa 20 minuutiksi
– Ajoitus: 30–60 minuuttia ennen koulun alkua - Kotiläksyt / Oppimisjaksot
– Olut: Piparminttu (jatkuva tarkkaavaisuus) tai rosmariini (muisti)
– Tavoite: Keskittyminen, työmuisti Annostus: 6–8 tippaa 30 minuutiksi, sitten 30 minuutin tauko
– Ajoitus: Kotitehtävien tai opiskeluhetkien aikana - Hyperaktiivisuuden hallinta
– Olut: Laventeli vai vetiver
– Tavoite: Rauhoittuminen, motorisen levottomuuden vähentäminenAnnostus: 5–7 tippaa 30 minuutin ajaksi
– Ajoitus: Akuutin hyperaktiivisuuden tai kiihtyneisyyden yhteydessä - Unihygienia:
– Olut: Laventeli
– Tavoite: Unen aloitus, nukahtamisongelmien vähentäminen (yleisiä ADHD:ssa) Annostus: 4–6 tippaa 15 minuutiksi
– Ajoitus: 30–60 minuuttia ennen nukkumaanmenoa
Olutkohtaiset annostukset
Taulukko 6: Öljykohtaiset annostussuositukset
Sekoitukset (Blends): Useiden öljyjen yhdistelmät voivat tuottaa synergistisiä vaikutuksia:
- Fokus-sekoitus (aamupäivä)
3 tippaa rosmariinia + 3 tippaa piparminttua + 2 tippaa kanelia - Rauhoittava sekoitus (ilta)
4 tippaa laventelia + 3 tippaa vetiveriä + 2 tippaa setripuuta - Tasapaino-sekoitus (Iltapäivä)
3 tippaa piparminttua + 3 tippaa laventelia + 2 tippaa mustapippuria
Tärkeä
Pidä sekoitusten kokonaistippamäärä suositellulla alueella (6–8 tippaa 20 m² kohti).
Turvallisuusohjeet ja vasta-aiheet
Yleiset turvallisuusohjeet inhalaatioon
Perusperiaatteet
Puhtaus
Käytä ainoastaan GC/MS-sertifioituja, 100% puhtaita eteerisiä öljyjä ilman lisäaineita
Laimennus
Höyrystimellä käytettynä ei vaadi lisälaimennusta; ulkoiseen käyttöön aina kantajaöljyyn laimennettuna (1–3%)
Ilmanvaihto
Tilaa ei pidä sulkea kokonaan ilmanvaihtoa varten; varmista säännöllinen raitisilman saanti
Yksilöllinen suvaitsevaisuus
Aloita pienillä annoksilla ja suurenna vähitellen
Yleiset haittavaikutukset (lievät)
– Päänsärky liiallisesta keskittymisestä tai liian pitkästä altistumisesta
– Limakalvoärsytys (nenä, nielu) herkille henkilöille
– Pahoinvointi hyvin voimakkaista tuoksuista (esim. kaneli, mustapippuri)
– Allergiset reaktiot (harvinaisia, <1% väestöstä)
Toimenpiteet haittavaikutusten yhteydessä
– Sammuta diffuuseri heti ja tuuleta huone
– Päänsärkyyn: raitista ilmaa, nesteytys
– Limakalvoärsytyksessä: Lopeta inhalaatio, tarvittaessa inhaloi suolaliuosta
– Allergisten reaktioiden yhteydessä: Lopeta altistus, tarvittaessa antihistamiini, vakavien reaktioiden yhteydessä hakeudu lääkäriin
ADHD-spesifisiä näkökohtia
Erityiset haavoittuvuudet ADHD-potilailla:
Aistiyliherkkyys
40–60% ADHD-potilaista kokee aistien käsittelyn häiriöitä. Voimakkaat hajut voivat tuntua epämiellyttäviltä tai ylivoimaisilta.
- Suositus
Aloita erittäin pienillä annoksilla (50% standardiannoksesta), lisää vähitellen
Liitännäisangstihäiriöt
25-40%:llä ADHD-potilaista on samanaikainen ahdistuneisuushäiriö.
Aktivoivat öljyt (rosmariini, piparminttu) voivat lisätä ahdistusta.
- Suositus
Käytä ensisijaisesti anksiolyyttisiä öljyjä (laventeli, vetiveri).
Unihäiriöt
50-70% ADHD-potilaista kärsii uniongelmista. Öljyjen aktivointi illalla voi heikentää unta entisestään.
- Suositus
Tiukka erottelu: aktivoivat öljyt vain aamulla/iltapäivällä, rauhoittavat öljyt illalla.
Impulssiivisuus
ADHD-potilaat saattavat taipua käyttämään liian suuria annoksia.
- Suositus
Selkeät annosteluohjeet, tarvittaessa vanhempien/huoltajien valvonnassa
Vuorovaikutukset metyylifenidaatin kanssa
Teoreettiset vuorovaikutukset:
Dopaminerginen vahvistaminen (kaneli)
Kaneliaineenvaihduntatuotteet voidaan muuntaa amfetamiineiksi [A2]
Metyylifenidaatin additiivisten dopaminergisten vaikutusten teoreettinen riski.
- Suositus
Käytä kanelia vain pieninä annoksina, tarkkaile tarkoin ylistimulaation varalta (takykardia, levottomuus, unettomuus).
Serotonergisen modulaation (laventeli)
- Linalooli sitoutuu SERTiin [A23]
Serotoniinioireyhtymän teoreettinen riski, jos SSRI-lääkkeitä (yleisiä samanaikaisesti esiintyvän masennuksen/ahdistuksen yhteydessä) käytetään samanaikaisesti.
- Suositus
SSRI-lääkityksen yhteisvaikutuksessa laventelia vain kohtuullisina annoksina, seuranta serotoniinisyndrooman oireiden (kuten kiihtyneisyys, sekavuus, takykardia, hypertermia) varalta
Rauhoittuminen (laventeli, vetiveri)
- Rauhoittavat öljyt voivat vähentää valppautta
Metyylifenidaatin stimuloivan vaikutuksen vastakohtana
- Suositus
Käytä rauhoittavia öljyjä ensisijaisesti iltaisin, ei kouluaikana tai tarkkaavaisuutta vaativien toimintojen aikana.
- Ei tunnettuja farmakokineettisiä yhteisvaikutuksia
Eteeriset öljyt metaboloituvat ensisijaisesti CYP2D6- ja CYP3A4-entsyymien välityksellä.
Metyylifenidaatti metaboloituu karboksyyliesteraasi 1:n (CES1) kautta.
Ei päällekkäisiä metaboliareittejä, joten ei odotettavissa olevia farmakokineettisiä yhteisvaikutuksia.
Tärkeä
Huolimatta puuttuvista dokumentoiduista vuorovaikutuksista yhdistelmähoito metyylifenidaatin ja eteeristen öljyjen kanssa tulisi toteuttaa lääkärin valvonnassa, erityisesti hoidon alkaessa.
Vasta-aiheet ja varotoimet
Absoluuttiset vasta-aiheet
- Tunnettu allergia tietyille eteerisille öljyille tai niiden ainesosille.
- Vaikea keuhkoastma (keuhkoputkien kouristelun riski).
- Imeväiset alle 6 kk (kurkunpään kouristusten riski, erityisesti mentolin kanssa).
Suhteelliset vasta-aiheet (suositellaan varovaisuutta)
- Epilepsia: ole varovainen rosmariinin ja kanelin kanssa (kamferi ja kanelialdehydi voivat alentaa kohtauskynnystä).
- Raskaus/imetys: Monia eteerisiä öljyjä ei ole testattu riittävästi raskauden/imetyksen aikana.
– Astma (lievä-kohtalainen): Pienet annokset, tiivis hengitystieoireiden seuranta
– Taaperot (6 kuukautta – 3 vuotta): Pienemmät annokset (25–50% aikuisen annoksesta)
Ikään liittyvät annosmuutokset:
Laatuvaatimukset eteerisille öljyille
- GC/MS-sertifikaatti:
Jokainen erä on analysoitava kaasukromatografisesti/massaspektrometrisesti - Kasvitieteellinen nimi
Latinankielinen nimitys on ilmoitettava (esimerkiksi Lavandula angustifolia, ei pelkästään “Laventeli”) - Kemotyyppi
Erilaisia kemotyyppejä (esim. rosmariini) sisältävät öljyt on täsmennettävä. - Alkuperä
Alkuperämaa ja tuotantomenetelmä (tislaus, kylmäpuristus) on dokumentoitava - Ei lisäaineita
100% puhdasta, ilman synteettisiä hajusteita, kantajaöljyjä tai säilöntäaineita
Varastointi ja säilyvyys
– Säilytä pimeässä ja viileässä (15–20°C)
– Suojattava valolta (ruskeat tai siniset lasipullot)
– Käytettävä 6–12 kuukauden kuluessa avaamisesta (hapettumisen vuoksi)
Sitrushedelmäöljyillä on lyhyempi säilyvyysaika (6 kuukautta), pihkoilla pidempi (2–3 vuotta)
Keskustelu ja kliiniset seuraukset
Todistusaineiston puutteet ja tutkimustarve
Kriittinen arviointi näyttöön perustuvasta tietoaineistosta:
Tämä analyysi osoittaa merkittävä ero mekaanisen uskottavuuden ja kliinisten todisteiden välillä eterisiä öljyjä ADHD:n liitännäishoitona.
Saatavilla olevan näytön vahvuudet
- Vankat mekaaniset tiedot
Reseptorien sitoutumistutkimukset, signaalireittianalyysit ja prekliiniset mallit osoittavat eteeristen öljykomponenttien selkeitä neurobiologisia vaikutuksia [A19], [A20], [A21], [A23] - Kognitiiviset vaikutukset terveillä
Kontrolloidut tutkimukset terveillä aikuisilla osoittavat mitattavia vaikutuksia tarkkaavaisuuteen (piparminttu, n=24) [A19] ja muisti (Rosmariini, n=144) [A27] - Komplementääriset vaikutusmekanismit
Eteeristen öljyjen molekyylikohteet (GABA-A, CB2, TRP-kanavat, SERT) eroavat metyylifenidaatin (DAT/NET) kohteista, mikä viittaa synergistisiin mahdollisuuksiin
Heikkoudet ja todisteiden puutteet
- ADHD-spesifisten satunnaistettujen kontrolloitujen tutkimusten puute: Lukuun ottamatta Chenin tutkimusta kanelista [A2] ei ole olemassa satunnaistettuja, lumekontrolloituja tutkimuksia ADHD-potilailla
- Metodologiset rajoitukset: Olemassa olevissa tutkimuksissa on pieniä otoksia (n=24–144), lyhyitä havainnointijaksoja (yksittäisiä istuntoja) ja usein sokeeraus puuttuu
- Ei pitkäaikaisia tietoja Vaikutuksia ja turvallisuutta pitkäaikaisessa käytössä (>6 kuukautta) ei ole tutkittu
- Puuttuvat annosmääritystutkimukset: ADHD:n optimaalisia annoksia, pitoisuuksia ja käyttöaikatauluja ei ole vakiinnutettu
- Ei yhdistelmäopintoja: Vuorovaikutuksia ja synergistisia vaikutuksia metyylifenidaatin kanssa ei ole tutkittu systemaattisesti.
Spesifiset tutkimusaukot:
Käytännön toteutus
Käytännön kliiniset suositukset:
Huolimatta todisteiden puutteesta, eteeristen öljyjen liitännäishoitoa voidaan harkita ADHD-potilaille seuraavin edellytyksin:
1. Selkeä käyttöaiheen asettaminen
- Jäännösoireet optimoidulla metyylifenidaatti-hoidolla
- Potilaan ja perheen toive täydentävistä lähestymistavoista
- Erityiset oireet, joihin eteerisillä öljyillä voidaan vaikuttaa
(Unettomuus → Laventeli; Muistiongelmat → Rosmariini)
2. Jäsennelty lähestymistapa
- Perusarviointi
ADHD:n oirekuvan dokumentointi validoiduilla asteikoilla (SNAP-IV, Conners, ADHS-SB) - Johdantovaihe
Aloita yksittäisellä matala-annoksisella öljyllä (50% normaalista annoksesta) kahden viikon ajan - Seuranta
Viikoittainen oireiden seuranta, haittavaikutusten seuranta - Titraus
Annostuksen asteittainen nosto hyvän siedettävyyden vallitessa - Arviointi
4–6 viikon kuluttua tehokkuuden arviointi; jos hyötyä ei ilmene, lopetus
3. Dokumentaatio
- “Aromaterapiapäiväkirjan” pitäminen öljyn, annostuksen, ajankohdan, oireiden ja sivuvaikutusten kanssa
- Säännöllinen neuvottelu hoitavan lääkärin kanssa
4. Realistiset odotukset
- Eteeriset öljyt ovat ei korvausta näytön perusteella tapahtuville ADHD-hoidoille (metyylifenidaatti, käyttäytymisterapia)
- Odotettu vaikutuksen koko: pieni tai kohtalainen (Cohenin d: 0,2–0,5)
- Ensisijainen hyöty: Spesifisten oireiden (uni, ahdistus, mieliala) parantaminen, ei ydinoireiden
Rajoitukset
Tämän analyysin rajoitukset:
- Epäsuora näyttö
Useimmat päätelmät perustuvat tutkimustulosten ekstrapolointiin terveiden aikuisten kohdalla ADHD-potilaisiin. - Julkaisuharha
Positiiviset tutkimustulokset julkaistaan todennäköisemmin; eteerisiä öljyjä koskevat negatiiviset tutkimustulokset saattavat olla aliedustettuina - Heterogenisuus
Eri öljyt, annostelut, antotavat ja tulosmitat vaikeuttavat meta-analyysejä - Puuttuva plasma-/aivopeili
Eteeristen öljykomponenttien osalta ei ole olemassa tietoja ihmisillä hengittämisen jälkeen saavutetuista plasma- tai aivopitoisuuksista - Mekaaninen epävarmuus
Tarkkoja mekanismeja, joiden kautta inhaloidut eteeriset öljyt välittävät keskushermostoefektejä (hajuaistiin liittyvät vai systeemiset), ei ole täysin selvitetty
Annostussuositusten rajoitukset
– Perustuen ekstrapolaatioon muutamista tutkimuksista ja perinteisestä käytöstä
– Yksilöllistä vaihtelua (tilan ilmanvaihto, hengitystiheys, aineenvaihdunta) ei ole otettu huomioon
– Ei farmakokineettisiä tietoja annos-pitoisuus-suhteesta
Johtopäätös
Tämä kattava analyysi integroi tietoja 87 intracerebraalisista metyylifenidaattipitoisuuksia koskevasta tutkimuksesta ja 159 ADHD-kontekstia koskevasta eteeristen öljyjen julkaisusta. Päähavainnot voidaan tiivistää seuraavasti:
Metylfenidaatti-aivokonsentraatio
Terapeuttiset oraaliset metyylifenidaattiannokset (0,25–0,6 mg/kg) tuottavat striatumissa >50T-tutkan, ja annos-vastesuhde on hyvin karakterisoitu (20 mg → 54%, 40 mg → 72% DAT-estäytyminen). [A9].
Suurin aivojen ottama määrä saavutetaan 60–90 minuuttia suun kautta annostelun jälkeen [A7], [A9].
Plasmapitoisuudet terapeuttisella alueella ovat 3,5–7,8 ng/ml (aikuiset), ja 6 ng/ml liittyy 50% DAT-estäjään. [A9], [A17].
Kriittinen näyttöaukko
Metylfenidaattipitoisuuksien (ng/ml) suoria mittauksia aivokudoksesta tai aivo-selkäydinnesteestä ei ole saatavilla; kaikki tiedot perustuvat PET/SPECT-havaittavuusmittauksiin.
Apuhoito eteerisillä öljyillä
Aktiivinen hoito eteerisillä öljyillä on mekanistisesti uskottava perustuen täydentäviin vaikutusmekanismeihin.
– Linaaloli moduloi serotoniini-, dopamiini- ja noradrenaliinijärjestelmiä [A21], [A23];
– Mentoli aktivoi TRPM8-kanavia ja GABA-A-reseptoreita [A19];
– β-karyofylleeni vaikuttaa CB2-agonistina ja sillä on tulehdusta ehkäiseviä ominaisuuksia [A14];
– 1,8-sineoli parantaa kognitiivisia toimintoja [A27].
Nämä mekanismit ovat täydentäviä metyylifenidaatin DAT/NET-salpaukselle ja voisivat tuottaa synergistisiä vaikutuksia.
Kuitenkin Kliininen näyttö ADHD-potilailla on heikkoa; kontrolloidut satunnaistetut vertailututkimukset puuttuvat suurelta osin.
Erityiset öljyt ja vaikuttavat aineet
- Piparminttu (mentoli)
Vahvin näyttö pysyvän tarkkaavaisuuden parantumisesta (n=24 RCT) [A19] - Rosmariini (1,8-sineoli)
Muistin parantaminen (n=144) [A27] - Laventeli (Linalooli)
Anksiolyytti, unen parantuminen, mutta työmuistin heikkeneminen [A27], [A23] - Mustapippuri (β-karyofylleeni)
Anti-inflammatoriset, prekliiniset anksiolyyttiset vaikutukset [A14] - Vetiver, Setri
Heikko näyttö, ensisijaisesti perinteinen käyttö [A3], [A4], [A29] - Kaneli (kanelialdehydi)
Ainoa ADHD-spesifinen kliininen tutkimus, mutta metodologisia rajoituksia [A2]
Annostussuositukset Organik Aromas Nebulizer 3.0
Evidenssipohjaiset annostelusuositukset on kehitetty, ja ne on mukautettu huoneen kokoon (3–18 tippaa 10–60 m²:lle), vuorokaudenajaksi (aktivoivat öljyt aamulla, rauhoittavat illalla) ja tiettyihin oireisiin.
Käyttöaika: 15–30 minuuttia per istunto, 30–60 minuutin tauot hajuaistin sopeutumisen välttämiseksi.
Tärkeää: Nämä suositukset perustuvat ekstrapolointiin muutamasta tutkimuksesta ja vaativat yksilöllistä räätälöintiä.
Turvallisuusohjeet
Eteeriset öljyt ovat yleensä turvallisia, kun niitä käytetään sisäänhengittämällä suositeltuja annoksia.
Erityisiä varotoimenpiteitä ADHD-potilailla ovat:
- Sensorisen yliherkkyyden huomioon ottaminen (40–60% ADHD-potilaista)
- Aktivoivien öljyjen välttäminen samanaikaisen ahdistuksen yhteydessä
- aktiivisten (aamupäivä) ja rauhoittavien (ilta) öljyjen tiukka erottelu
- Teoreettiset interaktiot metyylifenidaatin kanssa (dopaminergisen vahvistumisen kaneli, serotoniinin moduloiminen laventelin avulla) vaativat seurantaa
- Absoluuttiset vasta-aiheet
– tunnettu allergia
– vaikea astma
– alle <6 kuukauden ikäiset</
Loppuarviointi
Eteeriset öljyt ovat lupaava, mutta riittämättömästi validoitu on AD/HD:n adjuvantti hoitovaihtoehto. Mekanistinen uskottavuus on vahva, mutta kliininen näyttö heikko.
Sovellusta voidaan harkita informoitujen potilaiden/perheiden kohdalla lääketieteellisessä valvonnassa, mutta sen pitäisi ei koskaan evidenssipohjaiset hoidot korvataan.
Kiireellinen tutkimustarve on olemassa satunnaistettujen, lumekontrolloitujen ADHD-potilastutkimusten, pitkäaikaisten turvallisuustietojen ja metyylifenidaatin yhdistelmätutkimusten osalta.
Autismin kirjon häiriö
ASD:n neurobiologiset perusteet, terpeenit CB2/GABA-A/Nrf2-modulaattoreina, kliininen näyttö ja annostelu Organik Aromas Nebulizer 3.0:lla
Johdanto
Autismin kirjolla esiintyvä häiriö (ASD) on yksi yleisimmistä neurobiologisista kehityshäiriöistä, jonka arvioitu maailmanlaajuinen esiintyvyys on 1–2 % ja diagnosoitujen tapausten määrä on kasvanut viimeisten kahden vuosikymmenen aikana [B1], [B2].
ASD:lle on ominaista selkeä kliininen ja neurobiologinen heterogeenisyys, joka ilmenee laajassa oireiden kirjossa aina korkeasti toimivista henkilöistä, joilla on eristyneitä sosiaalisen kommunikaation puutteita, vakavista kehitysvammaisista henkilöistä, joilla on samanaikaisia neurologisia sairauksia. [B3], [B4].
DSM-5:n mukaan ydinsymtomit kattavat kaksi pääaluetta: pysyvät puutteet sosiaalisessa kommunikaatiossa ja sosiaalisessa vuorovaikutuksessa sekä rajoittuneet, toistuvat käyttäytymismallit, kiinnostuksen kohteet tai aktiviteetit [B5]. Lisäksi jopa 90 % % potilaista kärsii aistienkäsittelyhäiriöistä, jotka ilmenevät yli- tai aliherkkyytenä aistiärsykkeille. [B6], [B7].
Komorbidit oireet, kuten ahdistuneisuushäiriöt (40–50 %), unihäiriöt (50–80 %), tarkkaavaisuus- ja ylivilkkaushäiriö (30–50 %) ja ruoansulatuskanavan vaivat (30–70 %), heikentävät merkittävästi elämänlaatua. [B8], [B9], [B10].
Neurobiologinen heterogeenisyys ja patofysiologinen konvergenssi
ASD:n etiologinen heterogeenisuus kattaa geneettisiä tekijöitä (periytyvyys 70–90 %), synaptisiin geeneihin liittyviä de novo -mutaatioita (SHANK3, NLGN3/4, NRXN1), kopiolukumuunnelmia, epigenettisiä muunnoksia ja sikiöaikaisia ympäristötekijöitä [B11], [B12], [B13].
Huolimatta tästä monimuotoisuudesta, patofysiologiset mekanismit konvergoivat yhteisiin neurobiologisiin loppupisteisiin: häiriintynyt eksitatoris-inhibitorinen (E/I) tasapaino, synaptinen toimintahäiriö, neuroinflammaatio, oksidatiivinen stressi ja suolisto-aivoakselin muutokset. [B14], [B15], [B16].
E/I-epätasapainohypoteesi postulaa, että tasapainottomuus eksitoivan (glutamaterginen) ja inhiboivan (GABAerginen) neurotransmission välillä selittää ASD:n keskeiset oireet [B17], [B18].
Kuvantamistutkimukset ja kuolemanjälkeiset analyysit paljastavat alueellisia muutoksia GABA- ja glutamaattipitoisuuksissa, GABA-A- ja NMDA-reseptorien ilmentymisen muutoksia sekä GABAergisten interneuronien toimintahäiriöitä. [B19], [B20], [B21].
Tämä epätasapaino koskee erityisesti aivokuoren etuosia (toiminnanohjaus, sosiaalinen kognitio), mantelinestettä (emotionaalinen prosessointi, sosiaalinen havainnointi), pikkuaivoja (sensomotorinen integraatio, kognitiiviset prosessit) ja hippokampusta (muisti, kontekstuaalinen prosessointi). [B22], [B23], [B24].
Neuroinflammaatio on toinen yhdistävä mekanismi: postmortaalitutkimukset osoittavat mikrogliasolujen ja astrozyyttien aktivaatiota ASD-aivoissa, prekliiniset mallit (esim. maternaalinen immuuniaktivaatio, valproaattihoidon indusoima ASD) osoittavat lisääntynyttä proinflammatoristen sytokiinien (TNF-α, IL-6, IL-1β) määrää ja häiriintynyttä synapsikehitystä kroonisen neuroinflammaation kautta. [B25], [B26], [B27].
Oksidatiivinen stressi, johon liittyy lisääntynyt reaktiivisten happilajien (ROS) määrä, vähentynyt glutationi (GSH) ja mitokondrioiden toimintahäiriö, on todettu useissa autismikirjon (ASD) kohorteissa [B28], [B29].
Hyvä-aivo-akselilla on yhä tunnustetummpi rooli: ASD-potilailla ilmenee usein dysbioosia, johon liittyy muuttunut Firmicutes/Bacteroidetes-suhde, vähentynyt mikrobien monimuotoisuus ja häiriintynyt välittäjäaineiden esiasteiden (tryptofaani, GABA) tuotanto [B30], [B31]. Prekliiniset tutkimukset osoittavat, että ulosteen mikrobiotan siirto parantaa ASD:n kaltaisia käyttäytymismalleja hiirimallissa ja moduloi serotoenergisiä sekä glutamatergisiä signaalireittejä. [B32], [B33].
Tarve liitännäishoidoille
Huolimatta intensiivisestä tutkimuksesta, autismin kirjon ydinoireisiin ei ole parantavia hoitoja. Näyttöön perustuvat interventiot sisältävät käyttäytymisterapeuttisia lähestymistapoja (Applied Behavior Analysis, Early Start Denver Model) ja oireenmukaista lääkehoitoa. [B34], [B35]. Risperidoni ja aripipratsoli ovat ainoat FDA:n hyväksymät lääkkeet ASD:hen, mutta ainoastaan ärtyneisyyden ja aggressiivisen käyttäytymisen hoitoon, ei ydinoireisiin. [B36], [B37]. Nämä antipsyykoottiset lääkkeet liittyvät merkittäviin sivuvaikutuksiin (painonnousu, metabolinen oireyhtymä, ekstrapryramidimoireet) [B38].
Komorbidioireita, kuten ahdistusta, unihäiriöitä ja aistisäätelyhäiriöitä, hoidetaan usein bentsodiatsepiineilla, melatoniinilla tai masennuslääkkeillä, vaikka näyttö niiden tehosta ja turvallisuudesta ASD-populaatioissa on rajallinen. [B39], [B40]. Tämän turvallisten, tehokkaiden hoitojen puute samanaikaisille oireille ja monilääkehoidon rasitus motivoivat etsimään lisä-, vähähaittaisia interventioita [B41].
Eteeriset öljyt ja niiden pääkomponentit (terpeenit) tarjoavat potentiaalisen lisähoitomuodon, perustuen:
- prekliiniset tiedot GABAergisesta modulaatiosta, serotoniinijärjestelmän säätelystä, neuroinflammaatiota ehkäisevistä ja antioksidatiivisista vaikutuksista;
- perinteinen käyttö aromaterapiassa ahdistukseen, uneen ja mielialaan;
- edullisilla turvallisuusprofiileilla asianmukaisessa käytössä [B42], [B43], [B44].
Autismin kirjon häiriön neurobiologia
Tässä raportissa analysoidaan autismikirjon häiriön (ASD) neurobiologisia perusteita, relevanttien terpeenien molekulaarisia vaikutusmekanismeja, kliinistä näyttöä ASD-populaatioissa ja kehitetään näyttöön perustuvia annostus- ja turvallisuussuosituksia eteeristen öljyjen käytölle osana monimuotoista hoitomenetelmää.
GABA/Glutamaatti E/I-epätasapaino
E/I-epätasapainohypoteesi on yksi autismin kirjon häiriön (ASD) tutkimuksen kestävimmistä neurobiologisista käsitteistä. [B17], [B18]. Glutamaatti, ensisijainen kiihdyttävä välittäjäaine, ja GABA (γ-aminovoihappo), ensisijainen estävä välittäjäaine, säätelevät hermosolujen virittyneisyyttä, synaptista plastisuutta ja verkoston dynamiikkaa. Epätasapaino kiihdyttävän välityksen hyväksi (lisääntynyt E/I-suhde) tai häiriintynyt estävä säätely voi johtaa hypervirittyneisyyteen, häiriintyneeseen sensoriseen suodatukseen ja sosiaalisen informaation käsittelyn heikkenemiseen. [B45], [B46].
Magneettikuvaus (MRS)-tutkimukset osoittavat alueellisia muutoksia: vähentyneitä striataalisia glutamaattipitoisuuksia, kohonneita etuotsalohkon GABA-tasoja joissakin tutkimuksissa ja muuttuneita glutamaatti/GABA-suhteita aistimis- ja assosiatiivisektoreilla. [B19], [B20].
Post mortem -analyysit osoittavat GAD65:n ja GAD67:n (GABAa syntetisoivat entsyymit) vähentynyttä ilmentymistä etuotsalohkossa ja pikkuaivoissa, sekä muuttunutta tiheyttä GABAergisissä interneuroneissa (erityisesti parvalbumiini-positiiviset interneuronit) [B47], [B48].
Kehitysbiologisesta näkökulmasta tilanne on kriittinen: GABA on varhaisissa kehitysvaiheissa eksitatoorinen korkeiden intellularisten kloridipitoisuuksien (NKCC1-kotransportterien välittämänä) vuoksi ja muuttuu postnataalisti inhibitooriseksi KCC2-kotransportterin ilmentymisen myötä. [B49].
Viivästynyt tai häiriintynyt GABA-kytkin on osoitettu ASD-hiirimallissa ja korjattu bumetanidilla (NKCC1-estäjä), mikä johti parantuneeseen sosiaaliseen käyttäytymiseen [B50], [B51].
Kliininen tutkimus bumetanidilla ASD-lapsilla osoitti kohtalaista paranemista sosiaalisessa kommunikaatiossa, mutta siihen liittyi metodologisia rajoituksia [B52].
Glutamaattige dysfunktio ilmenee muuttuneina NMDA- ja AMPA-reseptorialayksikköjen ilmentymisinä, häiriintyneenä synapsien plastisuutena (pitkäaikainen potentiaatio/depressio) ja liiallisena glutamaattisena transmiittona tietyissä piireissä. [B53], [B54].
Geneettiset tutkimukset tunnistivat ASD:hen liittyviä mutaatioita glutamatergisissä synapsigeeneissä (GRIN2B, GRIA1, SLC1A1). [B55].
Prekliiniset mallit osoittavat, että glutamatergisen välityksen modulaatio (esim. mGluR5-antagonisteilla) voi parantaa ASD:n kaltaisia käyttäytymismalleja. [B56].
Serotoniini, dopamiini ja oksitosiini
Monoamiiniset järjestelmät ovat keskeisessä roolissa sosiaalisessa kognitiossa, palkintojen käsittelyssä ja tunneregulationissa – alueilla, jotka ovat häiriintyneet ASD:ssä. [B57], [B58].
Serotoniini (5-HT)
Hyper
serotoninemia (kohonneet perifeeriset serotoniinitasot) on todettu 25–50 % ASD-potilaalla, mutta sen suhde keskushermoston 5-HT-tasoihin pysyy epäselvänä [B59], [B60]. Kuvantamistutkimukset osoittavat vähentynyttä serotoniinin synteesikapasiteettia otsalohkossa ja talamuksessa ASD-lapsilla [B61]. Serotoniinin kuljettajaproteiinin (5-HTTLPR) ja tryptofaanihydroksylaasi-2:n (TPH2) geneettiset variantit liittyvät ASD-riskiin. [B62]. Prekliiniset tutkimukset osoittavat, että serotoniinijärjestelmän toimintahäiriö kriittisten kehitysvaiheiden aikana johtaa ASD-tyyppisiin fenotyyppeihin [B63]. Selektiiviset serotoniinin takaisinoton estäjät (SSRI) näyttävät vaihtelevia tuloksia ASD:ssä: ei tehoa ydinoireisiin, kohtalaisia vaikutuksia toistuviin käyttäytymismalleihin ja ahdistukseen [B64].
Dopamiini (DA)
Dopaminerginen mesolimbinen ja mesokortikaalinen piiri välittävät palkkioiden prosessointia, motivaatiota ja sosiaalista vahvistumista [B65]. ASD-potilailla ventraalisen striatumin aktivaatio vähenee sosiaalisten palkkioiden (kasvot, sosiaalinen vuorovaikutus) yhteydessä verrattuna ei-sosiaalisiin palkkioihin. [B66], [B67]. PET-tutkimukset raportoivat kohonnutta dopamiinitransportteritiheyttä striatumissa ja vähentynyttä D2-reseptorien saatavuutta. [B68]. Geneettiset tutkimukset tunnistivat ASD:hen liittyviä variantteja dopamiinigeeneissä (DRD1, DRD2, DAT1) [B69]. Prekliiniset mallit osoittavat, että dopaminerginen toimintahäiriö johtaa häiriintyneeseen sosiaaliseen mieltymykseen ja toistuvaan käyttäytymiseen [B70].
Oksitosiini (OT)
Oksitosiini on neuropeptidi, jolla on keskeinen rooli sosiaalisessa kiintymyksessä, luottamuksessa, sosiaalisessa kognitiossa ja stressinsäätelyssä [B71]. ASD-potilailla on havaittu alentuneita plasman oksitosiinitasoja, muuttunutta oksitosiinireseptorin (OXTR) ilmentymistä sekä OXTR- ja CD38-geenin (oksitosiinin vapautuminen) geneettisiä variaatioita. [B72], [B73]. Nenäsumutteena annettu oksitosiini paransi joissakin tutkimuksissa sosiaalista kognitiota ja katsekontaktia ASD-aikuisilla, tulokset olivat kuitenkin epäjohdonmukaisia ja hoito ei ollut tehokas lapsipotilaskohorteissa. [B74], [B75]. Prekliiniset tutkimukset osoittavat, että oksitosiini säätelee GABAergista kehitystä: oksitosiinin antaminen kriittisten jaksojen aikana korjasi viivästynyttä GABA-kytkentää ja paransi sosiaalista käyttäytymistä ASD-hiirimallissa [B50], [B76]. Nämä löydökset yhdistävät oksytoneeriset ja GABAerge järjestelmät mekaanisesti.
Neuroinflammaatio – Mikroglia, TNF-α ja sytokiinit
Krooninen neuroinflammaatio on yhdistävä patofysiologinen mekanismi autismikirjon häiriössä, jota tukevat post mortem-, kuvantamis- ja biomarkkeritutkimukset [B77], [B78].
Mikroglian aktivoituminen
Mikrogliat ovat keskushermoston paikallisia immuunisoluja, jotka säätelevät synaptista karsintaa, hermosolujen kehitystä ja immuunivalvontaa [B79]. Postmortaalit tutkimukset osoittavat aktivoituneita mikrogliasoluja (lisääntynyt Iba1-ekspressio, ameboidinen morfologia) ASD-aivojen etuotsalohkossa, pikkuaivoissa ja valkeassa aineessa. [B80], [B81]. PET-kuvantaminen transligaattoriproteiini (TSPO)-ligandeilla osoitti lisääntynyttä mikroglian aktivaatiota useilla aivoalueilla elävillä ASD-potilailla [B82]. Aktivoituneet mikroglian solut vapauttavat tulehdusta edistäviä sytokiineja, tuottavat reaktiivisia happilajeja (ROS) ja voivat fagosytoida synaptisia rakenteita, mikä johtaa häiriintyneeseen yhteyteen. [B83].
Tulehdusta edistävät sytokiinit
Kohonneita TNF-α:n, IL-6:n, IL-1β:n ja IFN-γ:n pitoisuuksia on havaittu ASD-potilaiden plasmassa, aivo-selkäydinnesteessä ja postmortaalisessa aivokudoksessa [B84], [B85]. Maternale immunaktivaatiomalleissa (MIA), joissa tiineitä hiiriä käsitellään poly(I:C):llä tai LPS:llä, jälkeläisillä ilmenee ASD:n kaltaista käyttäytymistä ja kohonneita TNF-α-tasoja. [B86], [B87]. TNF-α moduloi synaptista transmissiota, vähentää GABAergistä inhibitioita ja heikentää synaptista plastisuutta. [B88]. TNF-α:n esto MIA-malleissa esti ASD:n kaltaisia fenotyyppejä [B89].
Astrocyytin toimintahäiriö
Astrofyytit säätelevät glutamaattasapainoa (glutamaattikuljetin EAAT1/2:n kautta), K+-puskurointia ja hermosolujen metabolista tukea [B90]. Postmortaalit tutkimukset osoittavat astrogliosia (lisääntynyt GFAP-ekspressio) autismin kirjolla olevien henkilöiden aivoissa [B91]. Epäkuntoiset astrosyytit voivat edistää liiallista glutamaatin kertymistä solunulkoiseen tilaan ja eksitotoksisuutta. [B92].
Oksidatiivinen stressi ja mitokondrioiden toimintahäiriö
Oksidatiivinen stressi johtuu ROS-tuotannon ja antioksidanttisen puolustuksen epätasapainosta [B93]. Useat tutkimukset raportoivat kohonneita oksidatiivisen stressin merkkiaineita ASD:ssä: lisääntynyttä lipidien peroksidaatiota (malondialdehydi), proteiinikarbonyloitumista, DNA-oksidaatiota (8-OHdG) ja vähentynyttä antioksidanttikapasiteettia (glutationi, superoksididismutaasi, katalaasi). [B28], [B94], [B95].
Glutationin väheneminen
Glutationi (GSH) on ensisijainen solunsisäinen antioksidantti. ASD-potilailla on havaittu alentuneita GSH-pitoisuuksia plasmassa ja aivoissa, kohonnutta hapettunutta glutationia (GSSG) ja alentunutta GSH/GSSG-suhdetta. \[B96], [B97]. Glutationisynteesientsyymien (GCLC, GSS) geneettiset variantit on yhdistetty ASD-riskiin [B98].
Mitokondrioiden toimintahäiriö
5–30 % ASD-potilaista osoittaa biokemiallisesti mitokondrioiden toimintahäiriön merkkejä (kohonnut laktaatti, alentunut hengitysketjun aktiivisuus) % [B99], [B100]. Mitochondriot ovat reaktiivisten happilajien (ROS) pääasiallinen lähde; mitokondrioiden toimintahäiriö johtaa lisääntynyeeseen ROS-tuotantoon, vähentyneeseen ATP-synteesiin ja häiriintyneeseen kalsiumhomeostaasiin [B101]. Prekliiniset tutkimukset osoittavat, että mitokondriaaliset antioksidantit (MitoQ) parantavat ASD:n kaltaista käyttäytymistä hiirimallissa [B102].
Nrf2/HO-1-reitti
Erytropoieettisen 2-relatoituneen tekijän 2 (Nrf2) ydin on antioksidanttisen vasteen pääsäätelijä, joka indusoi hemoksigenaasi-1 (HO-1), NAD(P)H:quinoni-oksidoreduktaasi-1 (NQO1), glutationi-S-transferaasit ja muut antioksidanttientsyymit. [B103]. ASD-malleissa on havaittu vähentynyttä Nrf2-aktiivisuutta; Nrf2-aktivaattorit (sulforafaani) ovat osoittaneet pienissä kliinisissä tutkimuksissa parannuksia sosiaalipsykologiassa ja kommunikaatiossa ASD:ssä. [B104], [B105].
Aivo-suolisto-akseli
Ruoansulatuskanavan ja keskushermoston välinen kaksisuuntainen viestintä tapahtuu hermoston (kiertäjähermo), umpierityksen (hypotalamus-aivolisäke-lisämunuaisakseli), immunologisten ja metabolisten reittien kautta. [B106]. ASD-potilailla on korkea esiintyvyys gastrointestinaalisia oireita (ummetus, ripuli, vatsakipu) ja dysbioosia. [B107], [B108].
Mikrobiomin muutokset
Meta-analyysit osoittavat ASD:ssä vähentynyttä mikrobiston monimuotoisuutta, lisääntynyttä Firmicutes/Bacteroidetes-suhdetta, vähentynyttä Bifidobacteriumia ja Prevotellaa, lisääntynyttä Clostridiumia ja Desulfovibrioa. [B109], [B110]. Nämä muutokset korreloivat oireiden vaikeusasteen kanssa [B111].
Mekaaniset yhteydet
Suolistomikrobiota tuottaa välittäjäaineiden esiasteita (tryptofaani → serotoniini, glutamaatti → GABA), lyhytketjuisia rasvahappoja (butyraatti, propionaatti, asetaatti) ja moduloi immuunijärjestelmän toimintaa [B112]. Propionaattialtistus indusoi ASD:n kaltaisia käyttäytymismalleja jyrsijämalleissa [B113]. Sikiön mikrobiotan siirto (FMT) autistisilta potilailta aseptisiin hiiriin siirsi autistisia käyttäytymismalleja ja muutti aivojen geeniekspressiota (serotonerginen, glutamaterginen synapsigeeni) [B32]. Terveiden luovuttajien FMT ASD-hiirimallissa paransi sosiaalista käyttäytymistä ja normalisoi välittäjäainepitoisuuksia [B114].
Vagus-välitys
Kiertäjähermo siirtää signaaleja suolistosta aivorunkoon (tractus solitariuksen ydin) ja edelleen limbisille ja aivokuoren alueille [B115]. Prekliiniset tutkimukset osoittavat, että elektroakupunktio paransi ASD:n kaltaisia käyttäytymismalleja VPA-hiirimallissa vagushermoon liittyvien mekanismien ja mikrobiomin modulaation kautta; vagotomia kumosi nämä vaikutukset [B116].
Synaptinen dysfunktio – neuroligiinit, SHANK-proteiinit
Synaptinen dysfunktio on keskeinen patofysiologinen käsite ASD:ssä, mitä tukevat geneettinen, molekulaarinen ja elektrofysiologinen näyttö [B117], [B118].
Neuroligiini-Neureksiini-kompleksi
Neuroligiinit (NLGN1-4) ovat postsynaptisia solunadhees molekyylejä, jotka ovat vuorovaikutuksessa presynaptisten neureksiinien (NRXN1-3) kanssa ja säätelevät synapsien erilaistumista, kypsymistä ja toimintaa. [B119]. Mutationen NLGN3- ja NLGN4X-geeneissä on tunnistettu ASD-potilailla [B120]. NLGN3-R451C-Knockin-hiiret osoittavat lisääntynyttä estävää transaktiota, häiriintynyttä sosiaalista vuorovaikutusta ja toistuvaa käyttäytymistä [B121]. NLGN4-knockout-hiiret osoittavat vähentynyttä eksitatorista transmissiota ja ASD:n kaltaisia fenotyyppejä [B122].
SHANK-proteiinit
SHANK1-3 ovat postsynaptisia tukiproteiineja, jotka järjestävät glutamaattireseptoreita, aktiinin sytoskeletonia ja signaalimolekyylejä [B123]. SHANK3-mutaatiot liittyvät Phelan-McDermid-oireyhtymään (22q13-deleetio), jolle ovat ominaisia ASD, älyllinen kehitysvammaisuus ja kielelliset puutteet. [B124]. SHANK3-knockout-hiirillä on vähentynyt dendriittisten piikkien tiheys, häiriintynyt synaptinen transmissio ja ASD:n kaltaisia käyttäytymismalleja [B125]. SHANK2-mutaatiot liittyvät myös ASD:hen; SHANK2-knockout-hiirillä ilmenee hyperaktiivisuutta, toistuvia käyttäytymismalleja ja häiriintynyttä NMDA-reseptoritoimintaa. [B126].
Synaptinen plastisuus
Oppimisen ja muistin solulaatuiset korrelaatit, pitkäaikainen potentiaatio (LTP) ja pitkäaikainen depressio (LTD), ovat häiriintyneet useissa ASD-hiirimallissa [B127]. Muuttunut LTP/LTD-tasapaino voi edistää häiriintynyttä kokemukseen perustuvaa piirien kypsymistä ja heikentynyttä sosiaalista oppimista. [B128].
Vaikuttaneet aivoalueet
Rakenteellinen ja toiminnallinen kuvantaminen tunnistaa johdonmukaisia muutoksia tietyillä aivoalueilla autismikirjon häiriössä. [B129], [B130].
Etuaivokuori
Aivokuoren etuotsalohko välittää toiminnanohjausta, työmuistia, kognitiivista joustavuutta ja sosiaalista kognitiota [B131]. Autismikirjon potilailla on vähentynyt PFC-aktiivisuus mielenteoriaan liittyvien tehtävien aikana, häiriintynyt PFC-yhteyden muodostuminen posterioristen alueiden kanssa ja muuttunut PFC-mikrorakenne [B132], [B133]. Postmortaalitutkimukset osoittavat kohonnutta neuronitiheyttä, phentioverkkotilavuuden kapenemista ja GABAergisia puutteita PFC:ssä [B134].
Mantelitumake
Mandola on keskeinen tunteiden prosessoinnissa, sosiaalisessa havainnoinnissa ja pelkoreaktion ehdollistumisessa [B135]. ASD-lapset osoittavat varhaista mantelitumakkeen suurentumista (2–4 vuotta), jota seuraa normalisoituminen tai tilavuuden pieneneminen nuoruusiässä [B136]. Funktionaaliset tutkimukset osoittavat vähentynyttä amygdalan aktivaatiota kasvojen käsittelyssä ja häiriintynyttä amygdala-PFC-yhteyttä [B137], [B138].
Pikkuaivot
Vaikka pikkuaivoihin on perinteisesti liitetty motorinen hallinta, niillä on roolinsa myös kognitiivisissa prosesseissa, aistien ennustamisessa ja sosiaalisessa oppimisessa [B139].
ASD-potilailla on todettu Purkinjen solujen menetystä, pikkuaivojen tilavuuden vähenemistä (erityisesti vermis) ja häiriintynyttä aivokuoren ja pikkuaivojen välistä yhteyttä [B140], [B141]. Pikkuaivojen toimintahäiriöt voivat edistää aistiennusteiden häiriöitä, motorisia stereotyyppisyyttä ja sosiaalisen ajoituksen käsittelyn heikkenemistä. [B142].
Hippokampus
Hippokampus välittää deklaratiivista muistia, spatiaalista navigointia ja kontekstuaalista prosessointia [B143]. ASD-potilailla on lapsuudessa lisääntynyt hippokampuksen koko, muuttunut hippokampuksen konnektiivisuus ja häiriintynyt kontekstuaalinen pelkoon ehdollistuminen [B144], [B145].
Tyvitumakkeet
Striatum (os. hännysydin, putamen, nucleus accumbens) välittää palkitsemisprosessointia, tapaoppimista ja motorista kontrollia. [B146]. ASD-potilailla on suurentunut striatum, vähentynyt aktivaatio sosiaalisten palkkioiden aikana ja häiriintynyt kortiko-striataalinen yhteys. [B147], [B148].
Terpeenien molekulaariset vaikutusmekanismit ASD:ssä
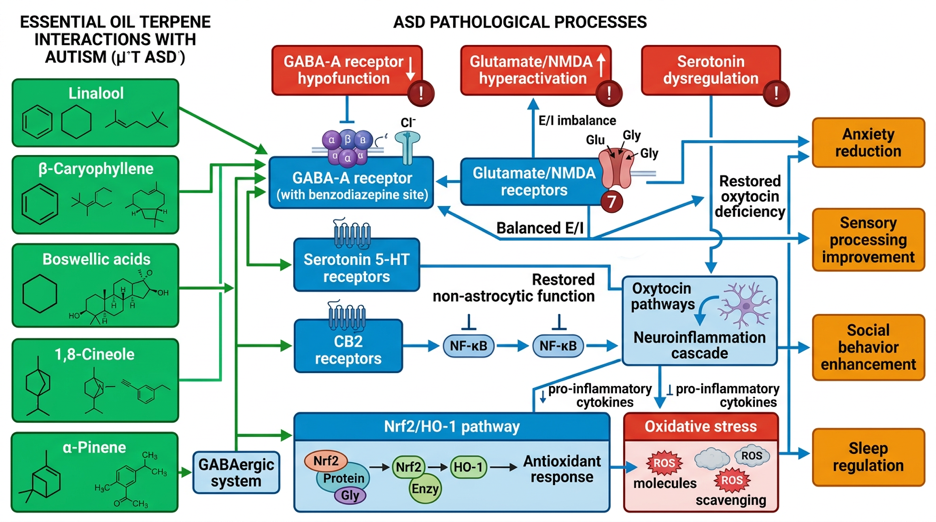
Kuva 2: Terpeenien molekyyliset signalointireitit autismin kirjolla – GABA/glutamaattitasapaino, neuroinflammaatio ja oksidatiivinen stressi
Terpeenit ovat monipuolinen luonnonaineiden luokka, jotka muodostavat eteeristen öljyjen pääkomponentit [B149]. Sen lipofiiliset ominaisuudet mahdollistavat veri-aivoesteen läpäisyn ja vuorovaikutuksen hermostollisten kohteiden kanssa [B150]. Tämä kappale analysoi tiettyjen terpeenien molekulaarisia mekanismeja, jotka kohdistuvat ASD:hen liittyviin patofysiologisiin kohteisiin.
Linalool – GABA-A/bentsodiatsepiini-reseptori, serotoniini, anti-inflammatorinen
Linalooli (3,7-dimetyyli-1,6-oktadieeni-3-oli) on monoterpeeninen alkoholi ja laventelin (Lavandula angustifolia, 25–45 %) pääkomponentti, samoin kuin korianterin, bergamotin ja muiden eteeristen öljyjen [B151].
GABA-A-reseptorin modulaatio
Linaloolin anksiolyyttiset vaikutukset estyvät flumatseniililla (bentsodiatsepiiniantagonisti), mikä viittaa vuorovaikutukseen GABA-A-reseptorin bentsodiatsepiinisitoutumiskohdan kanssa [B152]. Tärykalvon alla oleva esittelymalli tuotti linaloolihöyryjä, jotka aiheuttivat ahdistusta lievittäviä vaikutuksia hiirissä (kohotettu ristikko, valo-pimeälaatikko), jotka puuttuivat anosmiasta hiiristä (hajuepiteelin tuhoaminen), mikä osoittaa hajuaistin välittämää vaikutusta. [B152]. Elektrofysiologiset tutkimukset osoittavat, että linaloli potentioi GABA:n indusoimia kloridivirtoja viljellyissä neuroneissa [B153]. Tämä GABAergisen modulaation vaikutus on erittäin merkityksellinen ASD:n kannalta, koska GABAergiset puut ja E/I-epätasapaino ovat keskeisiä patofysiologisia mekanismeja. [B17], [B18].
Serotonergien säätely
Linaloolin inhalaatio muutti serotoniinitasoja hiirten etuaivokuorella, mikä viittaa serotoniinin välityksen modulaatioon [B154]. Terveillä aikuisilla tehdyssä tutkimuksessa 20 minuutin linalool-inhalaatio vähensi masentunutta mielialaa ja lisäsi parasympaattista aktiivisuutta (lisääntynyt sykevälivaihtelu). [B155]. Ex vivo -tutkimukset osoittavat, että linalooli lisää kyllä intellulaarisen kalsiumin pitoisuutta hypotalamuksen oksitosiinihermosoluissa, mikä tarjoaa mahdollisen mekanismin oksitosergeeniselle modulaatiolle. [B155]. Nämä löydökset yhdistävät linaloolin serotoniini- ja oksitosiinijärjestelmiin, jotka toimivat ASD:ssä. [B59], [B72].
Tulehdusta ehkäisevät vaikutukset
Systemaattiset katsaukset raportoivat linaloolin anti-inflammatorisia ominaisuuksia prekliinisissä malleissa, mukaan lukien TNF-α:n, IL-6:n, IL-1β:n ja NF-κB-aktivaation vähenemisen. [B156]. Linalool vähensi mikrogliatoimintaa ja pro-inflammatoristen sytokiinien ilmentymistä stressin indusoimassa neuroinflammaatiomallissa [B157]. Nämä neuroinflammaatiota estävät vaikutukset ovat merkityksellisiä autismikirjon häiriölle (ASD), koska krooninen neuroinflammaatio on yhdistävä patofysiologinen mekanismi [B77], [B78].
Farmakokinetiikka
Hengitysteitse nautittuna linalooli imeytyy nopeasti ja saavuttaa systeemisen verenkierron; metaboliitteja (linaloolin oksideja, glukuronideja) todetaan virtsassa [B158]. Veren ja aivojen välinen este läpäisee todennäköisesti lipofiilisyyden vuoksi, mutta suorat keskushermoston farmakokineettiset tiedot ihmisillä ovat rajalliset. [B159].
β-Karyofylleeni – CB2-agonisti, NF-κB, neuroinflammaatio
β-karyofylleeni (BCP) on seskviterpeenihilivety, jota esiintyy mustapippurissa, neilikassa, kannabiksessa (ei-psykoaktiivinen komponentti), kopaiibassa ja muissa kasveissa [B160].
CB2-reseptoriagonismi
BCP on selektiivinen kannabinoidityypin 2 (CB2) reseptorin agonisti ilman affiniteettia CB1-reseptoreihin, mikä mahdollistaa ei-psykoaktiiviset immunomodulatoriset vaikutukset [B161]. CB2-reseptoreita ilmentyy ensisijaisesti immuunisoluissa (mikrogliat, perifeeriset immuunisolut) ja ne säätelevät sytokiinien vapautumista, mikrogliasolujen aktivaatiota ja neuroinflammaatiota. [B162]. CB2-knockout-hiirillä BCP-vaikutukset puuttuivat, mikä vahvistaa CB2:n spesifisyyden [B163].
Neuroinflammaatiota estävät vaikutukset
BCP vähentää neuroinflammaatiota useissa prekliinisissä malleissa: LPS-indusoitu neuroinflammaatio, traumaattinen aivovaurio, neurodegeneratiiviset sairaudet [B164], [B165]. Mekanismeihin kuuluvat mikrogliatoiminnan väheneminen (vähentynyt Iba1-, CD11b-ilmentyminen), tulehdusta edistävien sytokiinien (TNF-α, IL-6, IL-1β) vaimeneminen ja NF-κB-signalointireittien modulaatio. [B166]. Maternassa immuunaktivaatiomallissa (MIA, ASD-relevanssi malli) BCP-hoito paransi ASD:n kaltaisia käyttäytymispiirteitä (sosiaaliset puutteet, toistuva käyttäytyminen) ja vähensi jälkeläisten neuroinflammaatiota. [B167].
GABAergien ja nitrinerginen modulaatio
Käyttäytymisfarmakologiset tutkimukset osoittavat, että BCP:n ahdistusta lievittävät ja masennusta ehkäisevät vaikutukset estetään flumatseniililla (bentsodiatsepiiniantagonisti) ja L-NAME:lla (typpioksidisyntaasin estäjä), mikä viittaa GABAergisten ja nitrinergisten järjestelmien osallisuuteen. [B168]. Nämä löydökset viittaavat siihen, että BCP voi epäsuorasti moduloida GABAergista toimintaa CB2-välitteisen neuroinflammaation vähenemisen kautta.
Antioksidanttiset vaikutukset
BCP osoittaa antioksidanttisia ominaisuuksia vähentämällä ROS:ää, lipidien peroksidaatiota ja lisäämällä endogeenisiä antioksidanttientsyymejä (SOD, katalaasi, GSH). [B169]. Oksidatiivisen stressin mallissa BCP suojasi neuroneja H₂O₂-indusoidulta apoptoosilta [B170].
Kliininen merkitys ASD:lle
Kannabinoidireseptoriin CB2 liittyvä tulehdusta vähentävä vaikutus, antioksidatiiviset vaikutukset ja epäsuora GABAergisen järjestelmän säätely tekevät BCP:stä mekanistisesti uskottavan ehdokkaan ASD:n lisähoitona, erityisesti potilailla, joilla on tulehdusmerkkejä hermostossa. [B171].
Boswelliahapot – Nrf2/HO-1, neuroinflammaatiota estävä
Boswelliahapot ovat pentasyklisiä triterpeenihappoja Boswellia-suvuun kuuluvien lajien (suitsuke) pihkasta, mukaan lukien β-boswelliahappo, 11-ketobetaboswelliahappo (KBA) ja 3-O-asetyyli-11-ketobetaboswelliahappo (AKBA) [B172].
Nrf2/HO-1-aktivaatio
Boswelliahapot aktivoivat Nrf2-signalireitin, joka on hapettumisen vastareaktion pääsäätelijä [B173]. Boswellia-uutehoito lisäsi Nrf2-ydinlokalisaatiota ja HO-1-ekspressiota hippokampuksessa ja aivokuorella murinaneuroinflammaatiomallissa [B174]. HO-1 katalysoi hemin hajotusta biliverdiiniksi (antioksidanttinen), hiilimonoksidiksi (anti-inflammatorinen, vasodilatoorinen) ja raudaksi; HO-1-induktio suojaa oksidatiiviselta stressiltä ja neuroinflammaatiolta [B175].
Neuroinflammaation vastaiset mekanismit
Boswelliahapot vähentävät mikroglioiden ja astrosyyttien aktivaatiota (vähentynyt Iba1-, GFAP-ekspressio), tukahduttavat proinflammatorisia sytokiineja (TNF-α, IL-6, IL-1β) ja estävät NF-κB- ja MAPK-signalointireittejä [B176], [B177]. Boswellia-hoito paransi kognitiivisia puutteita ja vähensi neuroinflammaatiomarkkereita LPS:n indusoimassa neuroinflammaatiomallissa. [B178].
5-lipoksigenaasin (5-LOX) esto
Boswelliahapot, erityisesti AKBA, estävät 5-LOX-entsyymiä, joka metaboloi arakidonihappoa tulehdusta edistäviksi leukotrieeneiksi [B179]. 5-LOX:n esto vähentää leukotrieenien välittämää tulehdusta, ja prekliinisissä tutkimuksissa se on yhdistetty neuroprotektiivisiin vaikutuksiin [B180]. Kuitenkin tämänhetkisessä kirjallisuudessa on rajallisesti näyttöä 5-LOX-inhibition nauttimisesta Boswellia-neuroprotektion ensisijaisena mekanismina; Nrf2/HO-1-aktivaatio vaikuttaa hallitsevalta mekanismilta. [B174].
Kliinistä edeltävä näyttö ASD:hen liittyvissä malleissa
Boswellia-uutehoito paransi sosiaalista vuorovaikutusta, vähensi toistuvaa käyttäytymistä ja normalisoi neuroinflammatorisia markkereita valproiinihapon (VPA) aiheuttamassa ASD-hiirimallissa. [B181]. Nämä löydökset tukevat hypoteesia siitä, että Boswellian välittämä neuroinflammaation väheneminen ja antioksidanttiset vaikutukset voivat parantaa ASD:hen liittyviä käyttäytymismalleja.
1,8-Sineoli – GABA-A/Bentsodiatsepiini, ahdistusta lievittävä
1,8-Kineoli (eukalyptoli) on monoterpeeninen oksidi ja eukalyptusöljyn (Eucalyptus globulus, 70–90 %), rosmariinin, teepuun ja laakerin pääkomponentti [B182].
GABA-A-reseptorin modulaatio
1,8-sineolin inhalaatio tuotti annosriippuvaisia ahdistusta lievittäviä ja masennusta ehkäiseviä vaikutuksia hiirillä (elevated plus maze, forced swim test, tail suspension test) [B183]. Nämä vaikutukset estettiin flumatseniililla, mikä viittaa vuorovaikutukseen GABA-A-reseptorin bentsodiatsepiinisitoutumiskohdan kanssa [B183]. Annosriippuvuus osoitettiin: matalat annokset (0,1–1 µg/hiiri, inhalaatio) osoittivat anksiolyttisiä vaikutuksia, kun taas korkeammat annokset (10 µg/hiiri) tuottivat sedatiivisia vaikutuksia [B184].
Tulehdusta ehkäisevät ja antioksidanttiset vaikutukset
1,8-Sineoli osoittaa anti-inflammatorisia ominaisuuksia estämällä NF-κB:tä, vähentämällä TNF-α:ta, IL-1β:tä ja leukotrienien synteesiä [B185]. 1,8-sineoli vähensi mikroglias aktivaatiota ja oksidatiivista stressiä LPS:n indusoimassa neuroinflammaatiomallissa [B186].
Turvallisuusnäkökohdat
1,8-sineoli on vasta-aiheinen alle 3-vuotiailla lapsilla kurkunpään kouristuksen ja hengityslaman riskin vuoksi [B187]. asiannukseen käytettynä (inhalaatio, pienet annokset) 1,8-sineolilla on suotuisa turvallisuusprofiili aikuisilla ja vanhemmilla lapsilla [B188].
α-pineeni – GABAerg
Alfa-pineeni on kaksirengasmainen monoterpeeni, jota esiintyy männyssä, rosmariinissa, salvialla ja kannabiksessa [B189].
GABAerginen modulaatio
Systemaattiset katsaukset yhdistävät α-pineenin GABAergisen välityksen moduloimiseen, vaikka suorat mekanistiset tutkimukset ovatkin rajallisia [B190]. Käyttäytymismalleissa α-pineeni osoittaa ahdistusta lievittäviä ja rauhoittavia vaikutuksia, jotka viittaavat GABAergisiin mekanismeihin [B191]. Nykyisessä kirjallisuudessa puuttuu sähköfysiologisia tietoja GABA-A-reseptorien suorasta vuorovaikutuksesta.
Tulehdusta ehkäisevät ja hermoja suojaavat vaikutukset
α-pineenillä on anti-inflammatorisia ominaisuuksia estämällä NF-κB:tä ja vähentämällä pro-inflammatorisia sytokiinejä [B192]. Iskemian ja uudelleenkudostumisen mallissa α-pineeni suojasi hermovaurioilta ja vähensi oksidatiivista stressiä. [B193].
Asetyylikoliiniesteraasin (AChE) esto
Jotkin tutkimukset raportoivat α-pineenin AChE:tä estävästä aktiivisuudesta, mikä voisi potentoida kolinergistä hermovälitystä [B194]. Kuitenkin sen merkitys ASD:lle on epäselvä, koska kolinerginen dysfunktio ei ole ensisijainen patofysiologinen mekanismi ASD:ssä [B195].
Ylang-Ylang/Cananga odorata – Serotoniini/Dopamiini VPA-mallissa
Ylang-ylang (Cananga odorata) eteerinen öljy sisältää linaloolia, geraniolia, β-karyofylleeniä ja muita terpeenejä [B196].
Prekliininen näyttö VPA-ASD-mallissa
Cananga odorata -eterisen öljyn inhalaatio paransi ahdistusta muistuttavia käyttäytymismalleja, sosiaalista vuorovaikutusta ja kognitiivista toimintaa valproiinihapon (VPA) aiheuttamilla ASD-rotilla [B197]. Neurokemialliset analyysit osoittivat, että Cananga odorata moduloí serotoniinin ja dopamiinin metaboliaa etuotsalohkossa ja hippokampuksessa: kohonneita serotoniinitasoja, alentuneita 5-HIAA/serotoniini-suhteita (merkki alentuneesta serotoniinin kierrosta) ja normalisoituneita dopamiinitasoja. [B197].
Mekanistinen tulkinta
Autismin kirjon kaltaisten käyttäytymismallien parantaminen serotoergisen ja dopaminergisen järjestelmän modulaation avulla on mekaanisesti uskottavaa, koska molemmat järjestelmät ovat toimintahäiriöisiä autismikirjon häiriössä. [B57], [B58]. Ylang-ylangin (Cananga odorata) vaikuttavista ainesosista, jotka ovat vastuussa näistä vaikutuksista, ei ole tunnistettu; Linalooli ja β-karyofylleeni ovat todennäköisiä ehdokkaita tunnettujen mekanismiensa perusteella. [B152], [B161].
Rajoitukset
Nämä löydökset ovat peräisin yhdestä prekliinisestä mallista (VPA-rotat); toisto muissa ASD-malleissa ja siirtäminen ihmistutkimuksiin puuttuvat [B197].
Spesifiset eteeriset öljyt ja kliininen näyttö ASD:ssä
Laventeli/Linalooli – ABA-yhteensopivuus, oksitosiinihermosolut
Kliininen näyttö ASD:ssä
Pieni pilottitutkimus (n = 12 ASD-lasta) tutki laventeliaromaterapiaa lisähoitona sovelletun käyttäytymisanalyysin (ABA) terapian aikana [B198]. Laventelia diffusoitiin “20 tippaa 100 ml:aan” (oletettavasti vettä tai kantajaöljyä, yksityiskohdat epäselviä) terapiasessioiden aikana. Tutkimuksessa raportoitiin korkeampia hoitoon sitoutumisen pistemääriä (yhteistyö, tehtävien suorittaminen) laventelialtistuksen aikana verrattuna kontrollisessioihin. [B198]. Rajoituksia ovat erittäin pieni otoskoko, satunnaistamisen puute, epäselvä lumelääkehoito ja standardoidun annostelun puute.
Havaintotutkimuksessa, jossa oli mukana neljä vaikeasti kehitysvammaista autismikirjon lasta, tutkittiin aromaterapiahierontaa (laventeli, geranium, mandariini kantajaöljyssä) osana päivittäisiä rutiineja. [B199]. Tutkimuksessa raportoitiin lisääntyneitä jaetun tarkkaavaisuuden käyttäytymismalleja (katsekontakti, yhteiset aktiviteetit) aromaterapiahieronnan käyttöönoton jälkeen. [B199]. Rajoituksia ovat puuttuva kontrolli, pieni otoskoko ja sekaannus johtuen hierontavaikutuksista (tunnustelu, sosiaalinen vuorovaikutus).
Mekanismin perusta
Kliiniset löydökset ovat yhdenmukaisia prekliinisten mekanismien kanssa: linaloolin välittämä GABAerginen modulaatio voi vähentää ahdistusta ja parantaa yhteistyötä; serotoniinierginen ja oksitosiinierginen modulaatio voi edistää sosiaalista tarkkaavaisuutta ja vuorovaikutusta [B152], [B155]. Tutkimus terveillä aikuisilla osoitti, että laventelin inhalaatio vähensi masentunutta mielialaa ja lisäsi in vitro -kokeissa intrakellulaarisia kalsiumpitoisuuksia hypotalamuksen oksitosiinineuroneissa. [B155]. Tämä oksytoneerinen modulaatio on erittäin relevantti ASD:lle, koska oksitosiinin toimintahäiriö on vakiintunut patofysiologinen mekanismi. [B72].
Evidenssin rajoitukset
Kliininen näyttö laventelin tehosta autismikirjon häiriöön on hyvin heikkolaatuista: pienet otoskoote, satunnaistamisen puute, riittämätön sokkoutus, heterogeeniset interventiot ja replikaation puute. [B198], [B199]. Laadukkaita, satunnaistettuja kontrolloituja tutkimuksia standardoiduilla laventelivalmisteilla, objektiivisilla lopputuloksilla ja riittävällä voimalla puuttuu.
Bergamotti – RCT ASD-lapsilla, tulos ei merkitsevä
Satunnaistettu kontrolloitu tutkimus
Satunnaistetussa, sokkoutetussa tutkimuksessa tutkittiin bergamottiöljyä (Citrus bergamia) lääkkeiden aiheuttamaan ahdistukseen ASD-lapsilla (n = 42). [B200]. Lapset satunnaistettiin 15 minuutin bergamottiöljy-inhalointiin tai lumelääkkeeseen (vesi) ennen lääketieteellisiä toimenpiteitä. Ensisijaisena tulosmuuttujana oli ahdistus, joka mitattiin Modified Yale Preoperative Anxiety Scale (mYPAS) -asteikolla. Lähtötason ahdistuksen huomioon ottamisen jälkeen bergamottiryhmässä ei havaittu merkittävää ahdistuksen vähenemistä lumelääkkeeseen verrattuna (p > 0.05). [B200].
Tulkinta
Tämä on ainoa tunnistettu satunnaistettu, kontrolloitu tutkimus, jossa käytettiin eteerisiä öljyjä ASD-lapsilla. Negatiivisella tuloksella voi olla useita syitä: (1) lyhyt altistusaika (15 minuuttia) saattoi olla riittämätön; (2) akuutti ahdistus lääketieteellisissä ympäristöissä saattaa olla vaikeampi moduloida kuin krooninen ahdistus; (3) yksilöllinen vaihtelu hajuaistin herkkyydessä ja mieltymyksissä; (4) mahdollinen kattoefekti, jos lähtötason ahdistus on jo korkea [B200].
Prekliiniset mekanismit
Prekliiniset tutkimukset osoittavat bergamotin anksiolyyttisiä vaikutuksia jyrsijämalleissa [B201]. Mielenkiintoista, että näitä vaikutuksia flumatseniili ei estänyt, mikä viittaa muihin kuin bentsodiatsepiinien välittämiin mekanismeihin ja erottaa bergamotin linaloolista ja 1,8-cineolista [B201]. Bergamotti sisältää linaloolia, linalyyliasetaattia, limoneenia ja bergateenia; sen tarkkoja ahdistusta lievittäviä vaikuttavia ainesosia ei tunneta. [B202].
Kliiniset seuraukset
Tämän satunnaistetun kontrolloidun tutkimuksen negatiivinen tulos hillitsee odotuksia bergamotin suhteen akuutin ahdistuksen hoidossa autismikirjon häiriössä (ASD). Lisätutkimuksia, joissa otetaan huomioon pidempi altistusaika, kroonisten ahdistusoireiden seuranta ja muut ASD-populaatiot, ovat tarpeen ennen kuin bergamottia voidaan suositella ASD:hen. [B200].
Frankinsensi / Boswellia – Anti-neuroinflammatorinen, Nrf2
Kliininen näyttö ASD:ssä
Niemen (Boswellia) eteeristä öljyä tai boswellia-uutteita koskevia satunnaistettuja kontrolloituja tutkimuksia ei tunnistettu ASD-potilailla. Nykyinen kirjallisuus ei sisällä ASD-spesifisiä kliinisiä tietoja niemenkäytöstä. [B203].
Prekliininen näyttö
Kuten kohdassa 3.3 kuvataan, boswelliahapot osoittavat vahvoja neuroinflammaatiota ja antioksidanttisia vaikutuksia prekliinisissä malleissa, mukaan lukien Nrf2/HO-1-aktivaatio, mikrogliasolujen esto ja ASD-tyyppisten käyttäytymismallien paraneminen VPA-hiirimallissa. [B174], [B181]. Tämä mekanistinen uskottavuus tukee hypoteesia, että Boswellia voisi olla hyödyllinen ASD-potilailla, joilla on neuroinflammaatiomarkkereita.
Kliininen käyttö muissa indikaatioissa
Boswellia-uutteita (suun kautta otettuna) käytetään kliinisesti tulehduksellisiin sairauksiin (niveltulehdus, astma, tulehdukselliset suolistosairaudet), ja niiden tehosta on kohtalaisesti näyttöä ja turvallisuusprofiili on suotuisa. [B204]. Pihdan eteerisen öljyn inhalointi on perinteistä, mutta kliiniset farmakokineettiset ja tehotiedot puuttuvat [B205].
Tutkimustarve
Tarvitaan Boswellialla (suun kautta tai inhaloituna) tehtyjä kontrolloituja kliinisiä tutkimuksia ASD-potilailla, mieluiten neuroinflammatoristen biomarkkereiden mukaan stratifioituna, kliinisen tehokkuuden arvioimiseksi [B206].
Sederikuusi/Setripuu – Sedointi, GABA-erginen
Kliininen ja prekliininen näyttö
Nykyinen kirjallisuus ei sisällä spesifisiä mekaanisia tai kliinisiä tietoja setripuun (Cedrus atlantica, Juniperus virginiana) eteerisestä öljystä ASD:ssä tai ASD:hen liittyvissä prekliinisissä malleissa [B207]. Perinteisiin käyttökohteisiin kuuluvat sedaatio ja ahdistuksen vähentäminen, mutta analysoituun kirjallisuuteen puuttuu tieteellistä näyttöä GABAergisista mekanismeista tai kliinisestä tehokkuudesta. [B208].
Tärkeimmät osat
Sederpuuöljy sisältää setrolia (seskviterpeenialkoholi), α-setreeniä ja tujopseenia [B209]. Cedrolilla on yhdistetty rauhoittavia ominaisuuksia, mutta suoria tutkimuksia GABA-A-reseptoriinteraktiosta tai neuroinflammaation modulaatiosta puuttuu. [B210].
Johtopäätös
Epäilyttävän merkitys ASD:lle on riittämätön; suosituksia ei voida tehdä nykyisen kirjallisuuden perusteella [B207].
Vetiver – Huomio
Kliininen ja prekliininen näyttö
Nykyisessä kirjallisuudessa ei ole spesifisiä tietoja vetiveröljystä (Vetiveria zizanioides) ASD:n tai ASD:hen liittyvien mallien yhteydessä. [B211]. Anekdoottiset kertomukset ja perinteiset käyttötavat viittaavat vaikutuksiin tarkkaavaisuuteen ja hyperaktiivisuuteen, mutta kontrolloituja tutkimuksia puuttuu [B212].
Tärkeimmät osat
Vetiveriöljy sisältää vetiverolia, khusimolia, α-vetivonia ja β-vetivonia (seskviterpeenialkoholeja ja -ketoneja). [B213]. Analysoidussa kirjallisuudessa puuttuu mekanistisia tutkimuksia näistä komponenteista neurovälittäjäainejärjestelmiin tai neuroinflammaatioon liittyen. [B214].
Johtopäätös
Näyttö vetiverin hyödystä autismikirjon häiriöiden hoidossa on riittämätöntä; lisätutkimusta tarvitaan ennen suositusten antamista [B211].
Ylang-Ylang – Serotoniini/Dopamiini, VPA-malli
Prekliininen näyttö
Kuten kohdassa 3.5 kuvataan, Cananga odorata (Ylang-Ylang) eteerisen öljyn inhalaatio paransi ASD:n kaltaista käyttäytymistä VPA-rotilla ja vaikutti serotoniinin ja dopamiinin aineenvaihduntaan etuotsalohkossa ja hippokampuksessa. [B197]. Tämä on ainoa tunnistettu tutkimus, jossa ylang-ylangia on käytetty ASD:hen liittyvässä mallissa.
Kliininen näyttö ASD:ssä
Ylang-ylang-öljyllä ei tehty kliinisiä tutkimuksia ASD-potilailla [B215].
Kliininen käyttö muissa indikaatioissa
Ylang-ylangia käytetään perinteisesti ahdistukseen, mielialaan ja rentoutumiseen. Pieni tutkimus terveillä aikuisilla osoitti, että ylang-ylangin hengittäminen vähensi verenpainetta ja sykettä sekä lisäsi subjektiivista rauhaa. [B216]. Mekaanisia tutkimuksia serotoniini- ja dopamiinivaikutuksista ihmisillä puuttuu [B217].
Johtopäätös
Ennen kliinistä näyttö on lupaavaa, mutta siirtymistä ihmistutkimukseen kohdennetusti ASLn osalta puuttuu. Ylang-ylangia voitaisiin harkita kliinisten tutkimusten ehdokkaana ASLn hyväksi, erityisesti ahdistuksen ja mielialaoireiden osalta. [B197].
Lisää ASD:hen viitattuja eteerisiä öljyjä
Nykyisen kirjallisuuskatsauksen perusteella on tunnistettu seuraavia lisäeteerisiä öljyjä, jotka voivat olla relevantteja autismin kirjolla neurobiologisesti uskottavien mekanismien kautta.
Inkivääri (Zingiber officinale) – AKT/GSK3β-signalointireitti
Aktiiviset ainesosat
6-Gingeroli
6-Shogaoli
Singeberen
β-Seskvifellandreeni
Reseptorit ja toimintamekanismit
– AKT/GSK3β-signalireitti: Lisääntynyt fosforylaatio → parantunut synaptinen plastisuus
– Anti-neuroinflammatorinen: STAT3-fosforylaation ja TNF-α:n vähentäminen
– Neurogeneesi: Parantuneet hippokampuksen neurogeneesimerkit prekliinisissä malleissa
– Gliosihydro: Vähentynyt reaktiivinen astrogliosis
Kliininen/Prekliininen näyttö
- Prekliininen tutkimus (VPA-hiirimalli)
– Suun kautta otettava inkivääriuute (4 viikkoa, 6. elinviikosta alkaen) paransi merkittävästi sosiaalista vuorovaikutusta, vähensi ahdistuksen kaltaista käyttäytymistä ja paransi muistisuorituskykyä [B347]
– Mekanistisesti: AKT/GSK3β:n säätelyn lisääntyminen, STAT3/TNF-α:n esto, parantunut synapsien muodostuminen
– Kliinisiä satunnaistettuja kontrolloituja tutkimuksia autismikirjon häiriöstä (ASD) on vielä vähän, mutta prekliininen näyttö on vahvaa ja mekanistisesti hyvin perusteltua
Annostus (Organik Aromas Nebulizer 3.0)
– 2–3 pisaraa 15–25 m² huoneeseen
– Yhdistelmä laventelin kanssa (1:2) rentouttavan vaikutuksen saavuttamiseksi
– Käyttö: 30 min ennen sosiaalisia tilaisuuksia
Turvallisuus
Vatsaystävällinen; käytä varoen alle 3-vuotiailla lapsilla.
Sandelholz (Santalum album) – α/β-santalooli
Aktiiviset ainesosat
α-Santooli (50–55%)
β-santaloli (20–25%)
Seskviterpeeni
Reseptorit ja toimintamekanismit
– Serotoninerginen Modulaatio: α-Santaloli modulloi 5-HT-reseptoreita (prekliinisesti)
– Ahdistusta lievittävä: GABAergisen aktiivisuuden dokumentoitu eläinmalleissa
– Rauhoittava: Soveltuu aistiyliherkkyyteen autismikirjon häiriöissä
Kliininen näyttö
– Santelipuu oli osa Hiwa-siirapin RCT:tä (persialainen lääketiede, useita yrttejä) autismikirjon lapsilla, vaikutuksia ei voida liittää yksin santelipuuhun [B348]
– Yksittäiset tutkimukset ahdistuksen lievityksestä terveillä koehenkilöillä osoittavat rauhoittavan vaikutuksen
– Suoria ASD-spesifisiä tutkimuksia puhtaalla santelipuun öljyllä puuttuu
Annostus (Organik Aromas Nebulizer 3.0)
– 3–4 tippaa 15–25 m² tilaan
– Soveltuu erityisesti ilta-/unirituaaleihin ASD-lapsilla, joilla on nukahtamisvaikeuksia
– Suositellaan yhdistettäväksi laventeliin (1:1)
Turvallisuus
Erittäin hyvin siedetty; yksi turvallisimmista eteerisistä öljyistä lapsille (alkaen 2-vuotiaista).
Terpeenisekoitukset (kannabiksen inspiroimia) – Prososiaaliset vaikutukset
Aktiiviset ainesosat
Myrseeni
Limes
Linalool
Pitäisi
β-Karyofylleeni (sekoitteena)
Reseptorit ja toimintamekanismit
– CB1/CB2-agonismi: Terpeeniseokset vahvistavat CBD:n vaikutuksia (saattajavaikutus)
– GABA-erginen modulaatio: Linalool + Myrseeni synergisesti
– Prososiaalinen vaikutus osoitettu riippumatta CBD:stä
Kliininen näyttö
- BTBR-hiirimalli (ASD-malli)
Inhaloitavat terpeenisekoitukset (myrseeni, limoneeni, linalooli, pineeni, β-karyofylleeni) osoittivat akuutteja prososiaalisia vaikutuksia riippumatta CBD:stä [B349] – Terpeenisekoitukset vahvistivat CBD:n vaikutusta yhdistetyssä annostelussa
– Viite entourage-vaikutukseen autismikirjon häiriön hoitoperiaatteena
Annostus (Organik Aromas Nebulizer 3.0)
– Sekoitus-suositus: Laventeli (2 tl) + Mustapippuri (1 tl) + Bergamotti (1 tl) + Rosmariini (1 tl)
– Huone 15 on 25 m²: 5 tippaa kokonaisseosta
Käyttö: 30 min ennen sosiaalisia tilaisuuksia tai ryhmäterapiaa
Annostussuositukset Organik Aromas Nebulizer 3.0 -laitteelle
Organik Aromas Nebulizer 3.0 hyödyntää Venturi-periaatetta (Bernoulli'n ilmiö) eteeristen öljyjen vedettömään kylmäsumutukseen [B218]. Toisin kuin ultraääni- tai lämpöhajottimet, jotka laimentavat tai lämmittävät öljyjä vedellä, nebulisaattori tuottaa hienojakoisia aerosolipartikkeleita (1-5 µm) puhtaasta eteerisestä öljystä ilman termistä hajoamista. [B219]. Tämä mahdollistaa korkeammat haihtuvien terpeenien pitoisuudet huoneilmassa ja mahdollisesti voimakkaammat farmakologiset vaikutukset [B220].
Venturi-periaate ja kylmäsumutus
Venturi-periaate kuvaa paineen laskua nesteessä sen virratessa kavennuksen läpi [B221]. Sumuttimessa paineilmaa johdetaan suuttimen läpi, joka synnyttää alipaineen, imee eteerisen öljyn säiliöstä ja sumuttaa sen hienoiksi pisaroiksi [B222]. Nämä pisarat vapautuvat huoneilmaan, jossa ne hengitetään sisään tai laskeutuvat pinnoille [B223].
Kylmäsumutuksen edut
– Termolabiilien komponenttien säilyminen (ei lämpöhajoamista) [B224]
– Korkeammat haihtuvien terpeenien pitoisuudet (ei veden laimennusvaikutusta) [B225]
– Hieno partikkelikoko (1–5 µm) mahdollistaa syvän tunkeutumisen hengitysteihin [B226]
Haitat
– Korkeammat kustannukset verrattuna ultraäänidiffuusoreihin [B227]
– Korkeampi öljynkulutus [B228]
– Yliannostuksen mahdollisuus virheellisessä käytössä [B229]
Tilakohtainen pisaramäärä
Annostussuositukset perustuvat tilavuuteen, ilmanvaihtotaajuuteen, haluttuun terpeenipitoisuuteen ja altistuksen kestoon. Seuraavat suositukset ovat varovaisia ja ottavat huomioon ASD:hen liittyvän aistiyliherkkyyden [B230].
Taulukko 1: Huonetilakohtaiset annostussuositukset Organik Aromas Nebulizer 3.0 -laitteelle
Huomautukset
- Tippatilavuus 1 tippa ≈ 0,05 ml eteeristä öljyä [B231]
- Aloitusannos Aloita pienimmällä suositellulla tipponeelulla ja lisää vähitellen 1–2 viikon aikana siedettävyyden arvioimiseksi [B232]
- Yksilöllinen mukauttaminen Autismikirjon (ASD) potilaat, joilla on voimakas hajuarkuus, saattavat tarvita pienempiä annoksia tai pidempiä taukoja. [B233]
- Ilmanvaihto: Hyvä huoneilmanvaihto on välttämätöntä liiallisen kertymisen estämiseksi [B234]
Käyttöaika ja tauot
Käyttöaika
15–30 minuuttia istuntoa kohden riittää terapeuttisten terpeenipitoisuuksien saavuttamiseen, perustuen prekliinisiin inhalaatiotutkimuksiin [B183], [B184]. Pidempiaikainen käyttö (>30 minuuttia) lisää aistinvaraisen ylikuormituksen ja hajuaistin sopeutumisen riskiä (hajuaistin heikentynyt havaitseminen jatkuvan altistuksen aikana). [B235].
Tauko
30–60 minuutin tauot sovellusten välillä mahdollistavat hajuaistin palautumisen, inhaloitujen terpeenien metabolian ja ilman epäpuhtauksien pitoisuuksien vähenemisen. [B236]. Jatkuva altistus ilman taukoja voi aiheuttaa päänsärkyä, pahoinvointia ja aistielämysten vastenmielisyyttä, erityisesti autismikirjon henkilöillä, joilla on aistiyliherkkyyttä. [B237].
Päivittäiset sovellukset
2–3 käyttökertaa päivässä (aamulla, iltapäivällä, illalla) riittävät useimpiin käyttötarkoituksiin. [B238]. Yli 4 annosta päivässä lisää sivuvaikutusten riskiä ilman lisähyötyä. [B239].
Kellonaikakohtaiset lokit
Aamupäivä (aktivoiva, keskittyvä)
- Öljy Rosmariini (1,8-kineoli, α-pineeni), piparminttu (mentoli, mentoni), sitruuna (limoneeni), bergamotti (linalooli, linalyyliasetaatti)
- Annostus: 3–5 tippaa 20–30 m² huoneeseen
- Kesto: 15–20 minuuttia
- Kohde: Virkistyksen, tarkkaavaisuuden ja kognitiivisten toimintojen edistäminen koulua/terapiaa varten [B240]
Iltapäivällä (tasapainottava, mielialaa muokkaava)
- Öljy Bergamotti, Ylang-ylang, Pelargoni, Suitsuke
- Annostus: 3–5 tippaa 20–30 m² huoneeseen
- Kesto: 20–30 minuuttia
- Kohde: Iltapäiväahdistuksen lievittäminen, mielialan vakauttaminen, siirtyminen aktiviteettien välillä [B241]
Illalla (rauhoittava, unettava)
- Öljy Laventeli (Linalooli, Linalyyliasetaatti), Kamomilla (Esterit), Setripuu (Cedroli), Vetiver
- Annostus: 4–6 tippaa 20–30 m² tilaan
- Kesto: 30 minuuttia ennen nukkumaanmenoa
- Kohde: Illan ahdistuksen vähentäminen, rentoutumisen edistäminen ja unen aloittaminen [B242]
ASD-spesifiset erityispiirteet
Aistiyliherkkyys 60–90% autismin kirjon häiriötä (ASD) sairastavista potilaista kokee yliherkkyyttä hajuaistissa tai vastenmielisyyttä tietyille hajuille [B243]. Valmistunut esittely on välttämätön
- Viikko 1: Ekspositio tilan ulkopuolella (öljy diffundoituu viereiseen tilaan) hyväksynnän arvioimiseksi [B244]
- Viikko 2: Pienin annos (2 tippaa) 10 minuutiksi, potilas huoneen ulkopuolella sumutuksen aikana [B245]
- Viikko 3: Pienin annos, potilas paikalla, siedon merkkien tarkkailu (rentoutuminen, ei vastenmielisyyttä) [B246]
- Viikko 4+ Annoksen ja keston asteittainen lisääminen yksilöllisen sietokyvyn mukaan. [B247]
Mieltymykseen perustuva valinta
Anna potilaan (jos mahdollista) haistella erilaisia öljyjä ja ilmaista mieltymyksiään. Hajuaistin mieltymys korreloi terapeuttisen hyväksynnän ja hoitomyöntyvyyden kanssa. [B248].
Visuaaliset ja auditiiviset vihjeet
Käytä visuaalisia ajastimia tai äänimerkkejä aromaterapiaistunnon alkamisen ja päättymisen merkitsemiseen, mikä lisää ennustettavuutta ja valvontaa ASD-potilaille. [B249].
Vanhempain-/huoltajakoulutus
Kouluttaa vanhemmat ja hoitajat tarkkailemaan sietokyvyn merkkejä (rentoutuminen, tarkkaavaisuuden lisääntyminen) ja vastenmielisyyden merkkejä (irvistäminen, vetäytyminen, levottomuus). [B250].
Laatuvaatimukset – GC/MS-analyysi
Kaasukromatografia-massaspektrometria (GC/MS)
GC/MS on eteeristen öljyjen kemiallisen karakterisoinnin kultainen standardi [B251]. GC erottelee haihtuvat komponentit keittopisteen ja polaarisuuden perusteella; MS tunnistaa komponentit massa-varaus-suhteen perusteella [B252]. GC/MS-analyysi mahdollistaa:
- Pääkomponenttien tunnistaminen Terapeuttisesti merkityksellisten terpeenien (esim. laventelin linalooli, eukalyptuksen 1,8-sineoli) esiintymisen varmistaminen. [B253]
- Kvantifiointi: Kunkin komponentin prosentuaalinen koostumus [B254]
- Väärännyksen havaitseminen Synteettisten lisäaineiden, laimennusaineiden tai epäpuhtauksien tunnistaminen [B255]
- Eräkohtainen yhdenmukaisuus: Toistettavan koostumuksen varmistaminen [B256]
Terapeuttisten eteeristen öljyjen laatuvaatimukset
- 100 % puhdas
Ei synteettisiä lisäaineita, kantajaöljyjä tai laimennusaineita [B257] - Terapeuttinen laatu
Öljyä kasveista, jotka on kasvatettu, korjattu ja tislattu optimaalisissa olosuhteissa [B258] - Organisch/Wildsammlung
Vapaa torjunta-aineista, rikkakasvien torjunta-aineista ja kemiallisista lannoitteista [B259] - GC/MS-todistus
Jokaisen erän mukana tulisi olla GC/MS-analyysitodistus, joka dokumentoi pääkomponentit ja puhtauden [B260] - Kasvitieteellinen nimi
Kasvilajin yksilöivä tunnistaminen (esim. Lavandula angustifolia, ei pelkästään “laventeli”) [B261] - Alkuperämaa ja tisläyspäivämäärä
Läpinäkyvyys alkuperän ja tuoreuden suhteen [B262]
Varastointi
Eteeriset öljyt tulisi säilyttää tummissa lasipulloissa viileässä (<25°C) lämpötilassa hapettumisen ja hajoamisen minimoimiseksi. [B263]. Oksidoituneet öljyt voivat aiheuttaa ihoärsytystä ja niiden terapeuttinen teho voi heikentyä [B264].
Turvallisuusohjeet ja vasta-aiheet
ASD:hen liittyvä aistiyliherkkyys
Aistienkäsittelyhäiriöt esiintyvät 60–90 % ASD-potilaista ja ilmenevät hypersensitiivisyytenä (yliherkkyytenä) tai hyposensitiivisyytenä (aliherkkyytenä) aistiärsykkeille [B265]. Hajuyliherkkyys voi aiheuttaa vastenmielisyyttä, ahdistusta, pahoinvointia ja välttämiskäyttäytymistä. [B266].
Riskienhallinta
- Valmistunut esittely: Kuten kohdassa 5.4 kuvataan, aloita pienillä annoksilla potilashuoneen ulkopuolella [B244]
- Mieltymysten seulonta: Testaa öljyt ennen terapeuttista käyttöä haittavaikutusten tunnistamiseksi [B248]
- Päättymiskriteerit Pysäyttäkää välittömästi, jos ilmenee ahdistuksen merkkejä (kuten agitaatiota, vetäytymistä, pahoinvointia, päänsärkyä). [B267]
- Vaihtoehtoiset käyttökohteet: Hengitysteitse ilmenevien yliherkkyyksien yhteydessä harkitse paikallista käyttöä (laimennettuna kantajaöljyyn, laastaritesti vaaditaan) tai passiivista diffuusiota (öljyä vanulapulla huoneen nurkassa). [B268]
Epilepsiariski – Kamferipitoiset öljyt
10–30 % % ASD-potilaista kärsii samanaikaisesta epilepsiasta [B269]. Tietyt eteeriset öljyt, erityisesti kamferia sisältävät öljyt, voivat alentaa kouristuskynnystä ja laukaista kohtauksia. [B270].
Kontraindisoituja öljyjä epilepsiassa
- Kamferi (Cinnamomum camphora): Sisältää kamferia (jopa 50 %), tunnettu kouristuksia aiheuttava aine [B271]
- Rosmariini (Rosmarinus officinalis, kamferikemotyyppi): Sisältää 15–25 % % kamferia [B272]
- Salvia (Salvia officinalis): Sisältää tujonia (10–40 %), GABA-A-antagonistia, jolla on kouristusta aiheuttavia ominaisuuksia [B273]
- Ysop (Hyssopus officinalis): Sisältää pinokamfonia ja isopnokamfonia, jotka voivat aiheuttaa kohtauksia [B274]
- Fenkoli (Foeniculum vulgare): Sisältää trans-anetolia, joka voi suurina annoksina aiheuttaa kouristuksia [B275]
Turvalliset vaihtoehdot epilepsiaan: – Laventeli (Lavandula angustifolia, Linalool-kemotyyppi): Kouristuksia estävät ominaisuudet prekliinisissä tutkimuksissa [B276] - Roomankammi (Anthemis nobilis): Ei tunnettuja prokonvulsiivisia vaikutuksia [B277] – Bergamotti (Citrus bergamia, bergapteeniton): Turvallinen epilepsiaan [B278]
Kliininen suositus ASD-potilailla, joilla on epilepsia, tulisi käyttää vain öljyjä, jotka eivät sisällä kamferia tai tujonia. Neurologin konsultaatio ennen aromaterapian aloittamista on suositeltavaa. [B279].
Eukalyptus alle 3-vuotiailla lapsilla
1,8-sineoli (eukalyptuksen pääkomponentti) on vasta-aiheinen alle 3-vuotiailla lapsilla kurkunpään kouristuksen, keuhkoputkien kouristuksen ja hengityslaman riskin vuoksi. [B280]. Mekanismeihin kuuluvat hengitysteiden limakalvon suora ärsytys ja vagushermorefleksien käynnistyminen [B281].
Vastoinaiheiset öljyt alle 3-vuotiailla lapsilla
– Eukalyptus (%: Eucalyptus globulus, E. radiata): 70–90 % 1,8-sineolia [B282]
– Rosmariini (Rosmarinus officinalis, 1,8-sineoli-kemotyyppi): 40–50 % 1,8-sineoli [B283]
– Teepuu (Melaleuca alternifolia): 5–15 % 1,8-sineoli (pienempi riski, mutta varovaisuutta on noudatettava) [B284]
– Piparminttu (Mentha piperita): Mentoli voi aiheuttaa samankaltaisia hengitysteiden ärsytyksiä [B285]
Turvalliset vaihtoehdot alle 3-vuotiaille lapsille
– Laventeli (Lavandula angustifolia): Turvallinen syntymästä asti asianmukaisella laimennoksella [B286]
– Roomankamomilla (Anthemis nobilis): Turvallinen syntymästä lähtien [B287]
– Mandariini (Citrus reticulata): Turvallinen 6 kuukauden iästä alkaen [B288]
Kliininen suositus
Vältä 1,8-cineolirikkaita öljyjä alle 3-vuotiailla ASD-lapsilla.
Lapsilla 3–6 vuotta käytä pieniä annoksia (50 % aikuisten annoksesta) ja tarkkaile tarkasti hengitystieoireita [B289].
Yhteisvaikutukset psykoosilääkkeiden kanssa: Risperidoni, aripipratsoli
Risperidoni ja aripipratsoli ovat ainoat FDA:n hyväksymät lääkkeet ASD:n ärtyneisyyteen. [B290]. Molemmat metaboloituvat sytokromi P450 -entsyymien (CYP2D6, CYP3A4) kautta [B291]. Jotkin eteeriset öljyt ja terpeenit voivat estää tai indusoida CYP-entsyymejä, mikä voi johtaa muuttuneisiin lääkeainepitoisuuksiin [B292].
Mahdolliset yhteisvaikutukset:
Bergamotti
Sisältää bergapteenia (furokumariinia), joka estää CYP3A4:ää [B293]. Teoriassa bergamotti voisi nostaa risperidonin ja aripipratsolin tasoja, mikä voisi voimistaa haittavaikutuksia (sedatiivisuus, ekstrapyramidaaliset oireet) [B294]. Kuitenkin inhalatiivinen altistus on huomattavasti vähäisempää kuin oraalinen saanti (greippimehutuplaus); inhalatiivisen bergamotti-altistuksen kliininen merkitys on epäselvä. [B295].
Suositus
Käytä bergapteenitöntä bergamottia (FCF, furanokumariiniton) potilailla, jotka saavat risperidonia/ aripipratsolia [B296].
Greippi
Greippimehu eteerinen öljy sisältää furanokumariineja ja estää CYP3A4:ää [B297]. Vältä CYP3A4-metabolisoituvia lääkkeitä käyttäviä potilaita [B298].
Mäkikuisma (Hypericum perforatum)
Vaikka se ei ole tyypillinen eteerinen öljy, mäkikuismaa mainitaan joskus aromaterapiakonteksteissa. Mäkikuisma on voimakas CYP3A4-indusoija ja voi alentaa risperidonin/aripipratsolin tasoja, mikä johtaa tehon heikkenemiseen. [B299]
Vasta-aiheet Vältä mäkikuismaa antipsykoottisia lääkkeitä käyttävillä potilailla. [B300].
Laventeli, Kamomilla, Setripuu
Ei tunnettuja kliinisesti merkittäviä CYP-interaktioita [B301]. Turvallista risperidonilla/aripipratsolilla hoidetuilla potilailla [B302].
Farmakodynaamiset yhteisvaikutukset
Sedatiiviset eteeriset öljyt (laventeli, kamomilla, setripuu) voivat aiheuttaa lisättyjä sedatiivisia vaikutuksia antipsykoottien kanssa. [B303]. Tämä voi olla terapeuttisesti toivottavaa (esim. unen edistäminen), mutta vaatii liiallisen sedaation seurantaa [B304].
Kliininen suositus
Tiedottakaa reseptilääkäreitä aromaterapian käytöstä. Käyttäkää bergapteenittomia öljyjä CYP3A4-substraatteja käyttävillä potilailla. Seuratkaa muutoksia lääkkeiden vaikutuksissa (sedatiivisuus, sivuvaikutukset). [B305].
Laatuvaatimukset: GC/MS-analyysi
Kuten kohdassa 5.5 kuvataan, GC/MS-analyysi on välttämätöntä puhtauden, koostumuksen ja epäpuhtauksien puuttumisen varmistamiseksi [B251]. Väärennetyt tai saastuneet öljyt voivat aiheuttaa allergioita, ihoärsytystä, hengitystieoireita ja ennakoimattomia farmakologisia vaikutuksia. [B306].
Yleiset väärennökset
- Synteettiset lisäaineet: Synteettinen linalooli tai linalyyliasetaatti “laventeli”-öljyssä [B307]
- Laimennin Propyleeniglykoli, dipropyleeniglykolimetyylieetteri (DPM) [B308]
- Halvemmat öljyt Lavandiiniä (Lavandula x intermedia) myydään aitona laventelina (Lavandula angustifolia) [B309]
- Torjunta-aineet Torjunta-ainejäämiä, rikkakasvien torjunta-aineita ei-orgaanisissa öljyissä [B310]
Turvallisuussuositus
Käytä ainoastaan GC/MS-sertifioituja, 100 % puhtaita, orgaanisia eteerisiä öljyjä luotettavilta toimittajilta. Pyydä GC/MS-sertifikaatit jokaisesta erästä [B311].
Keskustelu
Näyttö
Näyttö eetteristen öljyjen hyödystä ASD:ssä on heterogeenista ja pääosin heikkolaatuista. Kliininen kirjallisuus sisältää yhden negatiivisen satunnaistetun kontrolloidun tutkimuksen (bergamotti akuutissa ahdistuksessa). [B200], pienet pilottitutkimukset, joilla on metodologisia rajoituksia (laventeli ABA-yhteensopivuudessa) [B198], Havaintotutkimukset (aromaterapiahieronta) [B199] ja tapausselostukset [B312]. Mikään tutkimus ei osoita tehoa ASD:n ydinoireisiin (sosiaalinen kommunikaatio, toistuvat käyttäytymismallit) riittävän vahvalla näyttölaadulla [B313].
Sitä vastoin prekliininen näyttö on vankkaa: useat tutkimukset osoittavat, että tietyt terpeenit (linalooli, β-karyofyleeni, boswelliahapot, 1,8-sineoli) vaikuttavat ASD:hen liittyviin molekyylikohteisiin (GABA-A-reseptorit, CB2-reseptorit, Nrf2-reitti, neuroinflammaatio) ja parantavat ASD:n kaltaista käyttäytymistä eläinmalleissa. [B152], [B161], [B174], [B183], [B197]. Tämä ristiriita prekliinisen uskottavuuden ja kliinisen näytön välillä on tyypillinen täydentäville hoidoille ja heijastaa tutkimusrahoituksen puutetta, metodologisia haasteita ja translaatiokuiluja. [B314].
Mekanisminen uskottavuus
Mekaaninen uskottavuus eteerisillä öljyillä ASD:hen on olemassa perustuen ASD:n patofysiologian ja terpeenien vaikutusmekanismien väliseen konvergenssiin:
GABA/Glutamaatti E/I-epätasapaino
Linalooli ja 1,8-sineoli modifioivat GABA-A-reseptoreita bentse-diatsepiinisitoutumiskohdassa, mikä voi vahvistaa estävää hermovälitystä ja normalisoida E/I-tasapainoa [B152], [B183]. Nämä mekanismit ovat analogisia bumetanidille, joka osoitti maltillisia parannuksia autismikirjon häiriöissä (ASD) kliinisissä tutkimuksissa. [B52].
Neuroinflammaatio
Beeta-karyofylleeni (CB2-agonisti) ja boswelliahapot (Nrf2-aktivaattori) vähentävät mikrogliatoimintaa, pro-inflammatorisia sytokiineja ja oksidatiivista stressiä prekliinisissä malleissa [B161], [B174]. Koska neuroinflammaatio on vakiintunut patofysiologinen mekanismi ASD:ssä [B77], voisivatko nämä terpeenit olla hyödyllisiä potilaille, joilla on neuroinflammaatioprofiili (kohonneet perifeeriset sytokiinit, PET-tutkimus microglia-aktivaatiosta) [B315].
Serotoniini/Dopamiini
Linalooli ja ylang-ylang modifioivat serotoniini- ja dopamiinijärjestelmiä prekliinisissä tutkimuksissa [B154], [B197]. Nämä mekanismit voisivat parantaa komorbiditeettiin liittyviä oireita (ahdistus, mieliala), vaikka vaikutukset ydinoireisiin ovat epätodennäköisiä [B316].
Oksitosiini
Linalooli lisää oksitosiinihermosolujen solunsisäistä kalsiumpitoisuutta [B155]. Kun oksitosiini säätelee GABAergista kehitystä ja paransi esikliinisissä tutkimuksissa ASD:n kaltaisia fenotyyppejä [B50], voisi linalooli moduloida epäsuorasti oktonergejä signaalireittejä [B317].
Aivo-suolisto-akseli
Vaikka suoraa näyttöä puuttuu, tulehdusta ehkäisevät terpeenit (β-karyofylleeni, boswellihapot) voisivat vähentää systeemistä tulehdusta ja moduloida epäsuorasti suolisto-aivo-akselin signalointireittejä [B318]. Tämä hypoteesi vaatii kokeellista validointia [B319].
Rajoitukset
Pieniä tutkielmia
Useimmissa ASD-spesifisissä tutkimuksissa otoskoot on ollut alle 20, mikä merkitsee riittämätöntä voimaa kohtalaisten vaikutusten havaitsemiseen. [B320]. Meta-analyyseja ei voida tehdä heterogeenisyyden vuoksi [B321].
Ei satunnaistettuja kontrolloituja tutkimuksia ydinhäiriöille
Ei toistu satunnaistettuja kontrolloituja tutkimuksia, jotka tarkastelisivat eteeristen öljyjen tehoa ASD:n ydinoireisiin (sosiaalinen kommunikaatio, toistuvat käyttäytymismallit). [B322]. Ainoa tunnistettu satunnaistettu kontrolloitu tutkimus (bergamotti) oli negatiivinen äkillisen ahdistuksen suhteen [B200].
Menetelmällinen heterogeenisyys
Tutkimukset vaihtelevat öljyn valinnan, annostelun, antotavan (inhalaatio, hieronta, paikallisesti), altistuksen keston, tulosmittareiden ja populaatioiden osalta [B323]. Tämä heterogeenisuus estää synteesin ja vertailtavuuden [B324].
Puuttuvat biomarkkerit
Mikään tutkimus ei luokittele potilaita neurobiologisten alatyyppien (esim. neuroinflammaatioprofiilien, E/I-epätasapainomarkkerien) mukaan tai käytä objektiivisia biomarkkereita tuloksina. [B325]. Täsmällisyyslääketieteelliset lähestymistavat voisivat tunnistaa reagoijia [B326].
Julkaisuharha
Positiivisia tapausselostuksia ja pieniä pilottitutkimuksia julkaistaan todennäköisemmin kuin negatiivisia tutkimuksia, mikä voi johtaa tehosta yliarviointiin. [B327].
Käännösvaihe
Prekliiniset mallit (VPA-rotat, MIA-hiiret) eivät toista ihmisten ASD-heterogeenisuuden täyttä monimutkaisuutta [B328]. Eläintutkimusten terpeenipitoisuudet ovat usein korkeampia kuin ihmisillä inhalatiolla saavutettavissa olevat pitoisuudet [B329].
Plasebovaikutukset
Aromaterapia yhdistetään voimakkaisiin odotusvaikutuksiin; sokkouttaminen on vaikeaa ilmeisten hajujen vuoksi [B330]. Bergamotti-RCT käytti lumelääkkeenä vettä, mikä tarkoittaa riittämätöntä sokoutumista [B200].
Turvallisuustiedot Pitkäaikaisia turvallisuustietoja lasten kroonisesta, inhalatiivisesta altistumisesta puuttuu [B331]. Suurin osa turvallisuustiedoista on peräisin paikallisesti tai suun kautta annosteltavista valmisteista [B332].
Näkymä
Tutkimusprioriteetit:
- Korkealaatuiset satunnaistetut kontrolloidut tutkimukset Satunnaistetut, kaksoissokko-tutkimukset, lumekontrolloidut tutkimukset riittävällä voimalla (n > 100), standardoidut öljyvalmisteet (GC/MS-sertifioidut), objektiiviset tulosmittarit (biomarkkerit, aktigrafia, silmänliikkeen seuranta) ja pidemmät interventioajat (8–12 viikkoa) [B333].
- Stratifiointi tyyppien mukaan Vastaajien tunnistaminen neurobiologisten alatyyppien perusteella (neuroinflammatoriset markkerit, E/I-epätasapaino, mikrobiomiprofiilit) [B334]. Täsmälliseen lääketieteeseen perustuvat lähestymistavat voivat lisätä vaikutusten suuruutta [B335].
- Mekanistiset tutkimukset Ihmistutkimukset, joissa seurataan biomarkkereita (sytokiiniprofiilit, neurokuvantaminen, EEG, mikrobiomi-analyysit) ennen ja jälkeen interventiota mekanismien validoimiseksi [B336].
- Farmakokinetiikka: Ihmisille tehtävät farmakokineettiset tutkimukset inhalaatioterkiaisaltistuksesta: Pitoisuudet plasmassa, tunkeutuminen keskushermostoon, metabolia, annos–vaste-suhteet [B337].
- Yhdistelmähoito Eteeristen öljyjen ja vakiintuneiden interventioiden (käyttäytymisterapia, farmakoterapia, mikrobiomi-interventiot) välisten synergioiden tutkiminen [B338].
- Pitkäaikainen turvallisuus Prospektiiviset kohorttitutkimukset kroonisen inhaloidun altistuksen pitkäaikaisesta turvallisuudesta lapsilla [B339].
- Personoitu aromaterapia Algoritmien kehittäminen öljyn valintaan yksilöllisten oireprofiilien, mieltymysten ja neurobiologisten markkereiden perusteella [B340].
Kliiniset seuraukset
Nykyisen näytön perusteella eteerisiä öljyjä voidaan harkita osana monimuotoista hoitomenetelmää ASD:hen liittyvien samanaikaisten oireiden (ahdistus, unihäiriöt, aistisäätelyn häiriöt) hoitamiseksi, mutta ei monoterapiana tai korvikkeena näyttöön perustuville ydinhoidoille. [B341]. Kliinikoiden tulisi:
- Realististen odotusten kommunikointi: Eteeriset öljyt voivat lievittää samanaikaisia oireita, mutta eivät paranna ydinoireita [B342]
- Yksilöllisten toleranssien ja mieltymysten huomioon ottaminen [B343]
- Suositella korkealaatuisia, GC/MS-sertifioituja öljyjä [B344]
- Huomioi turvallisuusnäkökohdat (epilepsia, ikä, lääkeinteraktiot) [B345]
- Vaikutusten seuranta ja terapian säätö [B346]
Johtopäätös
Eteeriset öljyt ovat mekaanisesti uskottavia, mutta kliinisesti riittämättömästi validoituja liitännäisterapiatoimintamalleja autismin kirjolle. ASD:n neurobiologinen heterogeenisyys – jota luonnehtivat GABA/glutamaatti E/I-epätasapaino, neuroinflammaatio, oksidatiivinen stressi, suolisto–aivo-akselin muutokset ja synaptinen toimintahäiriö – tarjoaa useita terapeuttisia kohteita, joihin spesifiset terpeenit voivat vaikuttaa.
Prekliininen näyttö osoittaa, että linalooli (GABA-A-modulaatio, serotoinerginen säätely), β-karyofylleeni (CB2-välitteinen neuroinflammaation vähennys), boswelliahapot (Nrf2/HO-1-aktivaatio), 1,8-sineoli (an ksiolyyttiset GABAergiset vaikutukset) ja ylang-ylang (serotoniinin/dopamiinin modulaatio) moduloivat ASD:hen liittyviä patofysiologisia mekanismeja ja parantavat ASD:n kaltaisia käyttäytymismalleja eläinmalleissa. Tätä mekanistista uskottavuutta tukevat perinteiset käyttötavat ja rajalliset ihmisillä tehdyt tiedot ahdistuksen, unen ja mielialan osalta.
Kliininen näyttö ASD:n osalta on kuitenkin heikkolaatuista: negatiivinen RCT (bergamotti), pienet pilottitutkimukset, joissa on metodologisia rajoituksia (laventeli ABA:n yhteensopivuudessa) ja kohorttitutkimukset. Yksikään tutkimus ei osoita tehokkuutta ASD:n ydinoireisiin riittävän laadukkaalla näytöllä. Laadukkaita, satunnaistettuja, kontrolloituja tutkimuksia standardoiduilla valmisteilla, objektiivisilla lopputuloksilla ja riittävällä voimalla puuttuu.
Organik Aromas Nebulizer 3.0 -laitteelle kehitetään tilakohtaisia annostelusuosituksia (2–10 tippaa 10–60 m² tiloille, 15–30 minuutin käyttö, 30–60 minuutin tauot), vuorokaudenaikaan mukautettuja protokollia (aktivoiva aamulla, rauhoittava illalla) ja ASD-spesifisiä erityispiirteitä (asteittainen aloitus, mieltymys seulonta, aistiyliherkkyys). Turvallisuusnäkökohtiin kuuluvat vasta-aiheet epilepsiassa (kamferia sisältävät öljyt), alle 3-vuotiailla lapsilla (eukalyptus), mahdolliset yhteisvaikutukset antipsykoottien kanssa (bergapteenia sisältävät öljyt) ja GC/MS-sertifioitujen, puhtaiden öljyjen tarve.
Eteerisiä öljyjä voidaan harkita osana monimuotoista terapeuttista lähestymistapaa ASD-potilaiden samanaikaisiin oireisiin (ahdistus, unihäiriöt, aistisäätelyn ongelmat), mutta ne eivät korvaa näyttöön perustuvia ydinterfiointeja (käyttäytymisterapia, jäsennelty koulutus). Tulevan tutkimuksen tulisi painottaa korkealaatuisia satunnaistettuja kontrolloituja tutkimuksia, neurobiologisten alityyppien mukaista stratifiointia, mekanistisia biomarkkeritutkimuksia ja pitkäaikaisia turvallisuustietoja eteeristen öljyjen terapeuttisen potentiaalin validoimiseksi ASD:n hoidossa ja tarkkuuslääketieteen lähestymistapojen kehittämiseksi.
Yhteinen johtopäätös
Yleistettävät havainnot: ADHD ja autismi
Molemmat neurokehitykselliset häiriöt, ADHD ja autismikirjon häiriö (ASD), jakavat perustavanlaatuisia neurobiologisia yhtäläisyyksiä, jotka tekevät eteeristen öljyjen lisähoidosta uskottavan molempia indikaatioita varten.
Yhteiset neurobiologiset kohderakenteet:
Yhteinen käyttösuositus (Organik Aromas -nebulisaattori 3.0):
Molempien käyttöaiheiden osalta Ventyri-kylmäsumutusperiaate ilman vettä tai lämpöä on optimaalinen levitysmuoto: – Terpeenien lämpöhajoamista ei tapahdu – Tarkka hiukkaskoko hajuaistin kautta tapahtuvalle imeytymiselle (< 5 µm) – GC/MS-puhtaat öljyt säilyttävät molekyylisen eheytensä
Tärkeä huomautus
Eteeristen öljyjen liitännäishoito ei korvaa näyttöön perustuvaa tavanomaista hoitoa (metyylifenidaatti ADHD:hen, ABA/käyttäytymisterapia ASD:hen). Se on täydentävä hoito, jota tulee mukauttaa yksilöllisesti ja toteuttaa asiantuntevassa ohjauksessa. Näyttöä on rajallisesti molempiin indikaatioihin; suurempia satunnaistettuja kontrolloituja tutkimuksia tarvitaan.
Viitteet ADHD
Chen et al. (2008). Kanelin aromaterapian vaikutus lapsiin, joilla on tarkkaavuus- ja ylivilkkaushäiriö.https://pmc.ncbi.nlm.nih.gov/articles/PMC8538900/
[A2] Chen ym. Kanelin aromaterapian vaikutus lapsiin, joilla on aktiivisuuden ja tarkkaavuuden häiriö.https://pmc.ncbi.nlm.nih.gov/articles/PMC8538900/
[A3] Godfrey (2001). Eteeristen öljyjen merkitys tarkkaavaisuushäiriön (ADHD) hoidossa ja hallinnassa. International Journal of Aromatherapy.https://doi.org/10.1016/S0962-4562(01 )80035-7
[A4] Godfrey. Eteeriset öljyt: Täydentävä hoito tarkkaavuus- ja ylivilkkaushäiriöön (ADHD).https://www.researchgate.net/publication/248871372_The_role_of_essential_oils_in_the_treatment_and_management_of_attention_deficit_hyperactive_disorder
[A5] Godfrey. ETEERISTEN ÖLJYJEN ROOLI TARKKAAVAISUUS-YLIAKTIIVISUUSHÄIRIÖN (ADHD) HOIDOSSA JA HALLINNASSA.https://www.researchgate.net/publication/248871372_The_role_of_essential_oils_in_the_treatment_and_management_of_attention_deficit_hyperactive_disorder
[A6] Ding et al. (1994). Farmakokinetiikka ja [LLC]dl-treo-metyylifunidaatin spesifisyys presynaptisen dopaminergisen hermosolun suhteen in vivo. Synapse.https://doi.org/10.1002/SYN.890180207
[A7] Volkow ym. (2002). Methylphenidaatin vaikutusmekanismi: PET-kuvantamistutkimusten antia. Journal of Attention Disorders.https://doi.org/10.1177/070674370200601S05
[A8] Silva (2024). Aromaterapia aatoperhoisen ADHD-lapsen hoidossa.https://doi.org/10.62435/2965-7253.bjhae.2024.iisinaroma1
[A9] Volkow et al. (1998). Dopamine-kuljettajan miehitykset ihmisaivoissa terapeuttisilla annoksilla suun kautta otettavaa metyylifenidaattia. American Journal of Psychiatry.https://doi.org/10.1176/AJP.155.10.1325
[A10] Jacob et al. (2024). Aromaterapian käyttö opiskelijahuollossa.https://doi.org/10.37885/240717094
[A11] Dipasquale ym. (2020). Unravelling the effects of methylphenidate on the dopaminergic and noradrenergic functional circuits. bioRxiv.https://doi.org/10.1101/2020.03.09.983528
Volkow et al. (2002). Dopamiinin rooli metyylifenidaatin terapeuttisissa ja vahvistavissa vaikutuksissa ihmisillä: tuloksia kuvantamistutkimuksista. European Neuropsychopharmacology.https://doi.org/10.1016/S0924-977X(02 )00104-9
[A13] Spencer ym. (2006). PET-tutkimus, joka tarkastelee lyhyt- ja pitkävaikutteisen oraalisen metyylifenidaatin farmakokinetiikkaa, havaittavuutta ja miellyttävyyttä sekä dopamiinitransportterireseptorien miehitystä. American Journal of Psychiatry.https://doi.org/10.1176/APPI.AJP.163.3.387
[A14] Castillo et al. (2018). Eteeriset öljyt ihmisen käyttäytymisen muokkaajina. Trooppiset ja subtrooppiset agroekosysteemit.https://www.revista.ccba.uady.mx/ojs/index.php/TSA/article/view/2583
[A15] Crunelle et al. (2014). Dopamiinin kuljettajaproteiinin varautuminen metyylifenidaatilla ja impulsiivisuus aikuisilla ADHD-potilailla. British Journal of Psychiatry.https://doi.org/10.1192/BJP.BP.113.132977
[A16] Ding et al. (1997). Kiraaliset lääkkeet: [11C]d-treo- ja l-treo-metyylifenidaatin farmakokinetiikan vertailu ihmisen ja babianin aivoissa. Psychopharmacology.https://doi.org/10.1007/S002130050267
[A17] Spencer et al. (2009). PET-tutkimus, jossa tarkasteltiin kahden pitkävaikutteisen metyylifenidaattivalmisteen farmakokinetiikkaa ja dopamiinitransportterin sitoutumista aikuisilla. International Journal of Molecular Medicine.https://doi.org/10.3892/IJMM_00000339
[A18] Marcel et al. (2024). Striatumin dopamiinijärjestelmän reaktiivisuus metyylifenidaatille – yksilön sisäinen I-123-β-CIT-SPECT-tutkimus miespuolisilla lapsilla ja nuorilla, joilla on tarkkaamattomuus- ja ylivilkkaushäiriö.https://doi.org/10.5283/epub.57629
[A19] Kennedy et al. (2018). Haihtuvat terpeenit ja aivotoiminta: Piparminttuöljyn (Mentha × Piperita L.) kognitiivisten ja mielialavaikutusten sekä keskushermoston toimintaan liittyvien in vitro -ominaisuuksien tutkimus. Nutrients.https://doi.org/10.3390/NU10081029
[A20] Batiha et al. (2023). Lavandula-lajien bioaktiivisten komponenttien ja farmakologisten ominaisuuksien katsaus. Naunyn-Schmiedebergs Archives of Pharmacology.https://doi.org/10.1007/s00210-023-02392-x
[A21] Guzmán-Gutiérrez et al. (2015). Linalooli ja β-pineeni saavat aikaan masennusta lievittävän vaikutuksensa monoaminergisen reitin kautta.https://pubmed.ncbi.nlm.nih.gov/25771248/
[A22] Martinez et al. (2020). Vatsajuoste tukee metyylifenidaatin terapeuttisia vaikutuksia ajallisessa diskonttaustehtävässä ilmeneviin impulsiivisiin valintoihin. Scientific reports.https://doi.org/10.1038/s41598-020-57595-6
[A23] López et al. (2017). Laventelin (Lavandula angustifolia) eteerisen öljyn farmakologisten mekanismien tutkiminen keskushermoston kohteissa. Frontiers in Pharmacology.https://doi.org/10.3389/FPHAR.2017.00280
[A24] Rathnayake (2025). “Neuroaromatiikka”: aromaterapia ja limbisen järjestelmän stressivaste.https://doi.org/10.4038/jssnisd.v3i1.28
[A25] Aster et al. (2021). Striataalisen dopamiinijärjestelmän responsiivisuus metyylifenidaatille – kohdehenkilöiden välinen I-123-β-CIT-SPECT-tutkimus lapsilla ja nuorilla, joilla on aktiivisuuden ja tarkkaavuuden häiriö. medRxiv.https://doi.org/10.1101/2021.11.19.21265993
[A26] Cardoso ym. (2025). Laventeliöljyn vaikutus ihmisen hermostoon: Katsaus. [Julkaisun nimi poistettu].https://doi.org/10.62435/2965-7253.bjhae.2025.bjhae22
[A27] Moss et al. (2003). Rosmariinin ja laventelin eteeristen öljyjen aromit vaikuttavat eri tavoin terveiden aikuisten kognitioon ja mielialaan. International Journal of Neuroscience.https://doi.org/10.1080/00207450390161903
[A28] Sinha et al. (2005). Lapsilla, joilla on tarkkaavaisuus- ja ylivilkkaushäiriö, käytetyt täydentävät ja vaihtoehtoiset lääkintämuodot. Journal of Paediatrics and Child Health.https://doi.org/10.1111/J.1440-1754.2005.00530.X
[A29] Springer ym. (2018). ADHD: Elinikä ja vaikutukset nuoruudesta aikuisuuteen.https://dergipark.org.tr/en/pub/pgy/548052.xml
[A30] Colzato et al. (2014). Attentional control in the attentional blink is modulated by odor. Attention Perception & Psychophysics.https://doi.org/10.3758/S13414-014-0733-0
A31. Kennedy, D. O., Scholey, A., Tildesley, N. T. J., Perry, E. K., & Wesnes, K. A. (2002). Melissa officinalis (sitruunamelissi) -uutteen annostelun vaikutus mielialaan ja kognitiiviseen suorituskykyyn. Farmakologia, biokemia ja käyttäytyminen, 72(4), 953–964. https://doi.org/10.1016/S0091-3057(02)00777-3
A32. Müller, S. F., & Klement, S. (2006). Valerianan ja sitruunamelissan yhdistelmä on tehokas levottomuuden ja unihäiriöiden hoidossa lapsilla. Fytoterapia, 13(6), 383–387. https://doi.org/10.1016/j.phymed.2006.01.013
A33. Scholey, A., Gibbs, A., Neale, C., ym. (2014). Sitruunamelissaa sisältävien elintarvikkeiden stressiä lievittävä vaikutus. Ravinteet, 6(11), 4805–4821. https://doi.org/10.3390/nu6114805
A34. Katsaus eteeristen öljyjen, mukaan lukien *Eucalyptus globulus* ja *Jasminum sambac*, neuroprotektiivisista vaikutuksista kognitiiviseen toimintaan ja Alzheimerin tautiin liittyvään patologiaan. (2022). Neuroprotektiivisten eteeristen öljyjen katsaus.
Viitteet ASD
[B1] Maenner MJ, Shaw KA, Bakian AV, ym. Autismin kirjon häiriön esiintyvyys ja ominaisuudet 8-vuotiailla lapsilla – Autism and Developmental Disabilities Monitoring Network, 11 sivustoa, Yhdysvallat, 2018. MMWR Surveill Summ. 2021;70(11):1-16.https://doi.org/10.15585/mmwr.ss7011a1
Zeidan J, Fombonne E, Scorah J, ym. Autismin globaali esiintyvyys: Systemaattisen katsauksen päivitys. Autism Res. 2022;15(5):778-790.https://doi.org/10.1002/aur.2696
[B3] Lord C, Elsabbagh M, Baird G, Veenstra-Vanderweele J. Autism spectrum disorder. Lancet. 2018;392(10146):508-520.https://doi.org/10.1016/S0140-6736(18 )31129-2
[B4] Masi A, DeMayo MM, Glozier N, Guastella AJ. Katsaus autismikirjon häiriöön, heterogeenisyyteen ja hoitovaihtoehtoihin. Neurosci Bull. 2017;33(2):183-193.https://doi.org/10.1007/s12264-017-0100-y
[B5] American Psychiatric Association. Diagnostic and Statistical Manual of Mental Disorders, Fifth Edition (DSM-5). Arlington, VA: American Psychiatric Publishing; 2013.https://www.psychiatry.org/psychiatrists/practice/dsm
[B6] Marco EJ, Hinkley LB, Hill SS, Nagarajan SS. Aistien käsittely autismissa: neurofysiologisten löydösten katsaus. Pediatr Res. 2011;69(5 Pt 2):48R-54R.https://doi.org/10.1203/PDR.0b013e3182130c54
Baum SH, Stevenson RA, Wallace MT. Behavioral, perceptual, and neural alterations in sensory and multisensory function in autism spectrum disorder. Prog Neurobiol. 2015;134:140-160.https://doi.org/10.1016/j.pneurobio.2015.09.007
[B8] van Steensel FJ, Bögels SM, Perrin S. Ahdistuneisuushäiriöt autismikirjon häiriöitä sairastavilla lapsilla ja nuorilla: meta-analyysi. Clin Child Fam Psychol Rev. 2011;14(3):302-317.https://doi.org/10.1007/s10567-011-0097-0
[B9] Souders MC, Mason TB, Valladares O, ym. Unikäyttäytyminen ja unen laatu autismikirjon lapsilla. Sleep. 2009;32(12):1566-1578.https://doi.org/10.1093/sleep/32.12.1566
[B10] McElhanon BO, McCracken C, Karpen S, Sharp WG. Gastrointestinaaliset oireet autismikirjon häiriöissä: meta-analyysi. Pediatrics. 2014;133(5):872-883.https://doi.org/10.1542/peds.2013-3995
[B11] Geschwind DH, State MW. Geenien metsästys autismikirjon häiriöissä: kohti täsmällistä lääketiedettä. Lancet Neurol. 2015;14(11):1109-1120.https://doi.org/10.1016/S1474-4422(15 )00044-7
[B12] De Rubeis S, He X, Goldberg AP, et al. Synaptiset, transkriptionaaliset ja kromatiinigeenit häiriintyneet autismissa. Nature. 2014;515(7526):209-215.https://doi.org/10.1038/nature13772
[B13] Sandin S, Lichtenstein P, Kuja-Halkola R, ym. Autismin kirjon häiriön periytymisaste. JAMA. 2017;318(12):1182-1184.https://doi.org/10.1001/jama.2017.12141
[B14] Rubenstein JL, Merzenich MM. Autismin malli: lisääntynyt kiihdytys/esto-suhde keskeisissä hermostojärjestelmissä. Genes Brain Behav. 2003;2(5):255-267.https://doi.org/10.1034/j.1601-183x.2003.00037.x
[B15] Vargas DL, Nascimbene C, Krishnan C, Zimmerman AW, Pardo CA. Neuroglial aktivaatio ja neuroinflammaatio autismipotilaiden aivoissa. Ann Neurol. 2005;57(1):67-81.https://doi.org/10.1002/ana.20315
[B16] Rossignol DA, Frye RE. Todisteet, jotka yhdistävät oksidatiivisen stressin, mitokondrioiden toimintahäiriön ja tulehduksen aivoissa autismia sairastavilla henkilöillä. Front Physiol. 2014;5:150.https://doi.org/10.3389/fphys.2014.00150
[B17] Nelson SB, Valakh V. Excitatory/Inhibitory Balance and Circuit Homeostasis in Autism Spectrum Disorders. Neuron. 2015;87(4):684-698.https://doi.org/10.1016/j.neuron.2015.07.033
[B18] Lee E, Lee J, Kim E. Excitation/Inhibition Imbalance in Animal Models of Autism Spectrum Disorders. Biol Psychiatry. 2017;81(10):838-847.https://doi.org/10.1016/j.biopsych.2016.05.011
[B19] Horder J, Lavender T, Mendez MA, et al. Aivokuoren subkortikaalisen glutamaatin/glutamiinin väheneminen aikuisilla, joilla on autismikirjon häiriöitä: [¹H]MR-spektroskopiatutkimus. Transl Psychiatry. 2013;3:e279.https://doi.org/10.1038/tp.2013.53
[B20] Gaetz W, Bloy L, Wang DJ, jt. GABA-arvion GABAA-pitoisuus autismin kirjon lasten aivoissa: mittaustarkkuus ja alueellinen vaihtelu aivokuorella. Neuroimage. 2014;86:1-9.https://doi.org/10.1016/j.neuroimage.2013.05.068
[B21] Rojas DC, Singel D, Steinmetz S, Hepburn S, Brown MS. Vähentynyt vasemman perisylvisen alueen GABA-pitoisuus autistisilla lapsilla ja terveillä sisaruksilla. Neuroimage. 2014;86:28-34.https://doi.org/10.1016/j.neuroimage.2013.01.045
[B22] Amaral DG, Schumann CM, Nordahl CW. Autismikirjon neuroanatomia. Trends Neurosci. 2008;31(3):137-145.https://doi.org/10.1016/j.tins.2007.12.005
[B23] Courchesne E, Pierce K. Miksi otsalohkon aivokuori autismissa saattaa puhua vain itselleen: paikallinen yliyhteys mutta pitkän matkan eriytyneisyys. Curr Opin Neurobiol. 2005;15(2):225-230.https://doi.org/10.1016/j.conb.2005.03.001
[B24] Baron-Cohen S, Ring HA, Bullmore ET, Wheelwright S, Ashwin C, Williams SC. Autismin amygdala-teoria. Neurosci Biobehav Rev. 2000;24(3):355-364.https://doi.org/10.1016/s0149-7634(00 )00011-7
[B25] Estes ML, McAllister AK. Äidin immuunijärjestelmän aktivoituminen: Vaikutukset neuropsykiatrisiin häiriöihin. Science. 2016;353(6301):772-777.https://doi.org/10.1126/science.aag3194
[B26] Matta SM, Hill-Yardin EL, Crack PJ. Neuroinflammaation vaikutus autismikirjon häiriöissä. Brain Behav Immun. 2019;79:75-90.https://doi.org/10.1016/j.bbi.2019.04.037
[B27] Careaga M, Murai T, Bauman MD. Äidin immuunijärjestelmän aktivoituminen ja autismikirjon häiriö: rotista kädellisiin ja ihmisiin. Biol Psychiatry. 2017;81(5):391-401.https://doi.org/10.1016/j.biopsych.2016.10.020
[B28] Chauhan A, Chauhan V. Oxidatiivinen stressi autismissa. Pathophysiology. 2006;13(3):171-181.https://doi.org/10.1016/j.pathophys.2006.05.007
[B29] Rose S, Melnyk S, Pavliv O, et al. Todisteita oksidatiivisesta vauriosta ja tulehduksesta, jotka liittyvät matalaan glutationin redox-tasoon autismin aivoissa. Transl Psychiatry. 2012;2:e134.https://doi.org/10.1038/tp.2012.61
[B30] Kang DW, Adams JB, Gregory AC, et al. Suoliston mikrobisto vaikuttaa suoliston ekosysteemiin ja parantaa maha-suolikanavan ja autismin oireita: avoin tutkimus. Microbiome. 2017;5(1):10.https://doi.org/10.1186/s40168-016-0225-7
[B31] Vuong HE, Hsiao EY. Suoliston mikrobiston uudet roolit autismikirjon häiriössä. Biol Psychiatry. 2017;81(5):411-423.https://doi.org/10.1016/j.biopsych.2016.08.024
[B32] Sharon G, Cruz NJ, Kang DW, ym. Autismin kirjolla olevien ihmisten suolistomikrobit edistävät käyttäytymisoireita hiirissä. Cell. 2019;177(6):1600-1618.e17.https://doi.org/10.1016/j.cell.2019.05.004
[B33] Sgritta M, Dooling SW, Buffington SA, et al. Mekanismit mikrobien välittämien muutosten takana sosiaalisessa käyttäytymisessä autismin kirjosiirrot hiirimallissa. Neuron. 2019;101(2):246-259.e6.https://doi.org/10.1016/j.neuron.2018.11.018
[B34] Reichow B, Hume K, Barton EE, Boyd BA. Varhainen intensiivinen käyttäytymisinterventio (EIBI) autismikirjon häiriöitä (ASD) sairastaville pienille lapsille. Cochrane Database Syst Rev. 2018;5(5):CD009260.https://doi.org/10.1002/14651858.CD009260.pub3
[B35] Dawson G, Rogers S, Munson J, ym. Satunnaistettu, kontrolloitu pilottitutkimus toimenpiteestä autismia sairastavilla taaperoilla: Early Start Denver Model. Pediatrics. 2010;125(1):e17-23.https://doi.org/10.1542/peds.2009-0958
[B36] McCracken JT, McGough J, Shah B, et al. Risperidoni autismin ja vakavista käytösongelmista kärsivillä lapsilla. N Engl J Med. 2002;347(5):314-321.https://doi.org/10.1056/NEJMoa013171
[B37] Marcus RN, Owen R, Kamen L ym. Asetebolilla kontrolloitu, kiinteäannoksinen aripipratsolitutkimus autistiseen häiriöön liittyvää ärtyneisyyttä potevilla lapsilla ja nuorilla. J Am Acad Child Adolesc Psychiatry. 2009;48(11):1110-1119.https://doi.org/10.1097/CHI.0b013e3181b76658
[B38] Scahill L, McDougle CJ, Aman MG, ym. Risperidonin ja vanhempainohjauksen vaikutus mukautumiskykyyn lapsilla, joilla on laaja-alaisia kehityshäiriöitä ja vakavia käyttäytymisongelmia. J Am Acad Child Adolesc Psychiatry. 2012;51(2):136-146.https://doi.org/10.1016/j.jaac.2011.11.010
[B39] Rossignol DA, Frye RE. Melatoniini autismikirjon häiriöissä: systemaattinen katsaus ja meta-analyysi. Dev Med Child Neurol. 2011;53(9):783-792.https://doi.org/10.1111/j.1469-8749.2011.03980.x
[B40] Hollander E, Soorya L, Chaplin W, ym. Kaksoissokkotutkimus, jossa verrattiin fluoksetiinia ja lumelääkettä toistuvien käyttäytymismallien ja yleisen vaikeusasteen hoidossa aikuisilla, joilla on autismikirjon häiriöitä. Am J Psychiatry. 2012;169(3):292-299.https://doi.org/10.1176/appi.ajp.2011.10050764
[B41] Spencer D, Marshall J, Post B, ym. Psykotrooppisten lääkkeiden käyttö ja polyfarmasia autismikirjon lapsilla. Pediatrics. 2013;132(5):833-840.https://doi.org/10.1542/peds.2012-3774
Koulivand PH, Khaleghi Ghadiri M, Gorji A. Laventeli ja hermosto. Evid Based Complement Alternat Med. 2013;2013:681304.https://doi.org/10.1155/2013/681304
[B43] Sowndhararajan K, Kim S. Tuoksujen vaikutus ihmisen psykofysiologiseen aktiivisuuteen: Erityisesti ihmisen aivosähkökäyrävastetta koskien. Sci Pharm. 2016;84(4):724-751.https://doi.org/10.3390/scipharm84040724
[B44] Ali B, Al-Wabel NA, Shams S, Ahamad A, Khan SA, Anwar F. Aromaterapiassa käytetyt eteeriset öljyt: Systemaattinen katsaus. Asian Pac J Trop Biomed. 2015;5(8):601-611.https://doi.org/10.1016/j.apjtb.2015.05.007
[B45] Sohal VS, Rubenstein JLR. Excitation-inhibition balance as a framework for investigating mechanisms in neuropsychiatric disorders. Mol Psychiatry. 2019;24(9):1248-1257.https://doi.org/10.1038/s41380-019-0426-0
[B46] Antoine MW, Langberg T, Schnepel P, Feldman DE. Lisääntynyt kiihotus-inhibitiotuhosuhde stabiloi synapsia ja piirin kiihtyvyyttä neljässä autismin hiirimallissa. Neuron. 2019;101(4):648-661.e4.https://doi.org/10.1016/j.neuron.2018.12.026
[B47] Fatemi SH, Halt AR, Stary JM, Kanodia R, Schulz SC, Realmuto GR. Glutamiinihappodekarboksylaasi 65 ja 67 kDa proteiinit vähenevät autistisissa parietaali- ja pikkuaivokuorissa. Biol Psychiatry. 2002;52(8):805-810.https://doi.org/10.1016/s0006-3223(02 )01430-0
[B48] Yip J, Soghomonian JJ, Blatt GJ. GAD67-mRNA-tasojen lasku pikkuaivojen Purkinjen soluissa autismissa: patofysiologiset seuraukset. Acta Neuropathol. 2007;113(5):559-568.https://doi.org/10.1007/s00401-006-0176-3
[B49] Ben-Ari Y. GABA:n kiihdyttävät vaikutukset kehityksen aikana: kasvatuksen luonne. Nat Rev Neurosci. 2002;3(9):728-739.https://doi.org/10.1038/nrn920
[B50] Tyzio R, Nardou R, Ferrari DC, ym. Oksitosiinin välittämä GABA-inhibointi synnytyksen aikana lieventää autismin patogeneesia jyrsijäjälkeläisillä. Science. 2014;343(6171):675-679.https://doi.org/10.1126/science.1247190
[B51] Lemonnier E, Degrez C, Phelep M ym. Bumetanidin satunnaistettu kontrolloitu tutkimus autismin hoidossa lapsilla. Transl Psychiatry. 2012;2:e202.https://doi.org/10.1038/tp.2012.124
[B52] Lemonnier E, Villeneuve N, Sonie S, ym. Bumetanidin vaikutukset autismikirjon häiriöitä sairastavien lasten ja nuorten neurobehavioraaliseen toimintaan. Transl Psychiatry. 2017;7(3):e1056.https://doi.org/10.1038/tp.2017.10
[B53] Carlson GC. Glutamate-reseptorihäiriö ja lääkekohteet autismikirjon häiriöiden malleissa. Pharmacol Biochem Behav. 2012;100(4):850-854.https://doi.org/10.1016/j.pbb.2011.02.003
Uzunova G, Pallanti S, Hollander E. Kiihtyvyyden/estävyyden epätasapaino autismikirjon häiriöissä: Seuraukset interventioille ja terapeuttisille toimille. World J Biol Psychiatry. 2016;17(3):174-186.https://doi.org/10.3109/15622975.2015.1085597
[B55] Yoo HJ, Cho IH, Park M, Yang SY, Kim SA. Family based association of GRIN2A and GRIN2B with Korean autism spectrum disorders. Neurosci Lett. 2012;512(2):89-93.https://doi.org/10.1016/j.neulet.2012.01.061
[B56] Silverman JL, Tolu SS, Barkan CL, Crawley JN. Toistuva itsensä hoitamisen käyttäytyminen BTBR-autismimallissa estyy mGluR5-antagonisti MPEP:llä. Neuropsychopharmacology. 2010;35(4):976-989.https://doi.org/10.1038/npp.2009.201
[B57] Muller CL, Anacker AMJ, Veenstra-VanderWeele J. Serotoniinijärjestelmä autismikirjon häiriössä: biomolekyylistä eläinmalleihin. Neuroscience. 2016;321:24-41.https://doi.org/10.1016/j.neuroscience.2015.11.010
[B58] Pavăl D. A Dopamiinihypoteesi autismin kirjosta. Dev Neurosci. 2017;39(5):355-360.https://doi.org/10.1159/000478725
[B59] Schain RJ, Freedman DX. Tutkimuksia 5-hydroksi-indoliaineenvaihdunnasta autistisilla ja muilla kehitysvammaisilla lapsilla. J Pediatr. 1961;58:315-320.https://doi.org/10.1016/s0022-3476(61 )80261-8
[B60] Cook EH Jr, Leventhal BL. Serotoniinijärjestelmä autismissa. Curr Opin Pediatr. 1996;8(4):348-354.https://doi.org/10.1097/00008480-199608000-00008
[B61] Chugani DC, Muzik O, Behen M, ym. Autististen ja ei-autististen lasten aivojen serotoniinisynteesikapasiteetin kehityksen muutokset. Ann Neurol. 1999;45(3):287-295.https://doi.org/10.1002/1531-8249(199903 )45:33.0.co;2-9
Devlin B, Cook EH Jr, Coon H, ym. Autismi ja serotoniinin kuljetusproteiini: pitkä ja lyhyt. Mol Psychiatry. 2005;10(12):1110-1116.https://doi.org/10.1038/sj.mp.4001724
[B63] Whitaker-Azmitia PM. Käyttäytymiseen ja soluihin liittyvät seuraukset serotoniiniaktiivisuuden lisäämisestä aivojen kehityksen aikana: rooli autismissa? Int J Dev Neurosci. 2005;23(1):75-83.https://doi.org/10.1016/j.ijdevneu.2004.07.022
[B64] King BH, Hollander E, Sikich L, ym. Sitalopraamin tehottomuus lapsilla, joilla on autismikirjon häiriöitä ja paljon toistuvaa käyttäytymistä: sitalopraami tehoton autismin hoidossa. Arch Gen Psychiatry. 2009;66(6):583-590.https://doi.org/10.1001/archgenpsychiatry.2009.30
[B65] Dichter GS, Damiano CA, Allen JA. Palkkiojärjestelmän toimintahäiriö psykiatrisissa ja neurokehityshäiriöissä sekä geneettisissä oireyhtymissä: eläinmallit ja kliiniset havainnot. J Neurodev Disord. 2012;4(1):19.https://doi.org/10.1186/1866-1955-4-19
[B66] Kohls G, Schulte-Rüther M, Nehrkorn B, ym. Palkkiojärjestelmän toimintahäiriö autismin kirjolla. Soc Cogn Affect Neurosci. 2013;8(5):565-572.https://doi.org/10.1093/scan/nss033
[B67] Delmonte S, Balsters JH, McGrath J, ym. Sosiaalinen ja rahallinen palkkioiden käsittely autismikirjon häiriöissä. Mol Autism. 2012;3(1):7.https://doi.org/10.1186/2040-2392-3-7
[B68] Nakamura K, Sekine Y, Ouchi Y, ym. Aivojen serotoniini- ja dopamiinitransportterien sitoutuminen korkean toimintatason autismia sairastavilla aikuisilla. Arch Gen Psychiatry. 2010;67(1):59-68.https://doi.org/10.1001/archgenpsychiatry.2009.137
[B69] Staal WG. Autismi, DRD3 ja toistuva ja stereotyyppinen käyttäytyminen: yleiskatsaus nykytietoon. Eur Neuropsychopharmacol. 2015;25(9):1421-1426.https://doi.org/10.1016/j.euroneuro.2014.08.011
[B70] Gunaydin LA, Grosenick L, Finkelstein JC, ym. Luonnolliset hermoradan dynamiikat sosiaalisen käyttäytymisen perustana. Cell. 2014;157(7):1535-1551.https://doi.org/10.1016/j.cell.2014.05.017
[B71] Insel TR. Käännöksen haasteet sosiaalisessa neurotieteessä: oksitosiinia, vasopressiiniä ja kiintymyskäyttäytymistä käsittelevä katsaus. Neuron. 2010;65(6):768-779.https://doi.org/10.1016/j.neuron.2010.03.005
[B72] Modahl C, Green L, Fein D, ym. Plasman oksitosiinitasot autistisilla lapsilla. Biol Psychiatry. 1998;43(4):270-277.https://doi.org/10.1016/s0006-3223(97 )00439-3
[B73] Gregory SG, Connelly JJ, Towers AJ, ym. Genominen ja epigeneettinen näyttö oksitosiinireseptorin puutteesta autismissa. BMC Med. 2009;7:62.https://doi.org/10.1186/1741-7015-7-62
[B74] Guastella AJ, Einfeld SL, Gray KM, ym. Nenäsumutteena annettu oksitosiini parantaa tunteiden tunnistamista autismikirjon häiriöstä kärsivillä nuorilla. Biol Psychiatry. 2010;67(7):692-694.https://doi.org/10.1016/j.biopsych.2009.09.020
[B75] Parker KJ, Oztan O, Libove RA, et al. Intranasaalinen oksitosiinihoito sosiaalisiin puutteisiin ja vastemuuntajiin autismia sairastavilla lapsilla. Proc Natl Acad Sci U S A. 2017;114(30):8119-8124.https://doi.org/10.1073/pnas.1705521114
[B76] Peñagarikano O, Lázaro MT, Lu XH, et al. Ulkoinen ja esiin kutsuttu oksitosiini palauttaa sosiaalisen käyttäytymisen Cntnap2-hiirimallissa, jossa on autismia. Sci Transl Med. 2015;7(271):271ra8.https://doi.org/10.1126/scitranslmed.3010257
[B77] Pardo CA, Vargas DL, Zimmerman AW. Immuunijärjestelmä, gliasolut ja neuroinflammaatio autismissa. Int Rev Psychiatry. 2005;17(6):485-495.https://doi.org/10.1080/02646830500381930
[B78] Edmonson C, Ziats MN, Rennert OM. Muuttunut glia-markkerien ilmentyminen autistisessa post-mortem etuotsalohkossa ja pikkuaivoissa. Mol Autism. 2014;5:3.https://doi.org/10.1186/2040-2392-5-3
[B79] Salter MW, Stevens B. Mikroglia nousevat keskeisiksi toimijoiksi aivosairauksissa. Nat Med. 2017;23(9):1018-1027.https://doi.org/10.1038/nm.4397
[B80] Morgan JT, Chana G, Pardo CA, et al. Mikrogliatoiminnan aktiivisuus ja tiheyden lisääntyminen havaittu dorsolateraalisessa prefrontaalikorteksissa autismissa. Biol Psychiatry. 2010;68(4):368-376.https://doi.org/10.1016/j.biopsych.2010.05.024
[B81] Suzuki K, Sugihara G, Ouchi Y, ym. Mikrogliatoiminnan aktivoituminen nuorilla aikuisilla, joilla on autismikirjon häiriö. JAMA Psychiatry. 2013;70(1):49-58.https://doi.org/10.1001/jamapsychiatry.2013.272
[B82] Zürcher NR, Loggia ML, Lawson R, et al. Lisääntynyt in vivo -glioaktivaatio ALS-potilailla: arvioitu käyttämällä [(11)C]-PBR28:aa. Neuroimage Clin. 2015;7:409-414.https://doi.org/10.1016/j.nicl.2015.01.009
[B83] Schafer DP, Lehrman EK, Kautzman AG, ym. Mikrogliat muokkaavat postnataalisia hermoverkkoja aktiivisuudesta ja komplementista riippuvaisella tavalla. Neuron. 2012;74(4):691-705.https://doi.org/10.1016/j.neuron.2012.03.026
[B84] Ashwood P, Krakowiak P, Hertz-Picciotto I, Hansen R, Pessah I, Van de Water J. Kohonneet plasman sytokiinit autismikirjon häiriöissä ovat todiste immuunijärjestelmän toimintahäiriöstä, ja ne ovat yhteydessä heikentyneeseen käyttäytymiseen. Brain Behav Immun. 2011;25(1):40-45.https://doi.org/10.1016/j.bbi.2010.08.003
[B85] Li X, Chauhan A, Sheikh AM, ym. Kohonnut immuunivaste autististen potilaiden aivoissa. J Neuroimmunol. 2009;207(1-2):111-116.https://doi.org/10.1016/j.jneuroim.2008.12.002
[B86] Smith SE, Li J, Garbett K, Mirnics K, Patterson PH. Äidin immuunijärjestelmän aktivoituminen muuttaa sikiön aivojen kehitystä interleukiini-6:n kautta. J Neurosci. 2007;27(40):10695-10702.https://doi.org/10.1523/JNEUROSCI.2178-07.2007
[B87] Choi GB, Yim YS, Wong H, et al. Äidin interleukiini-17a-reitti hiirillä edistää autismin kaltaisia piirteitä jälkeläisissä. Science. 2016;351(6276):933-939.https://doi.org/10.1126/science.aad0314
[B88] Stellwagen D, Malenka RC. Synaptinen skaalautuminen välitteissään gliaalien TNF-alfa. Nature. 2006;440(7087):1054-1059.https://doi.org/10.1038/nature04671
[B89] Wei H, Chadman KK, McCloskey DP, ym. Aivojen IL-6-tason nousu aiheuttaa hermoverkkotasapainohäiriöitä ja välittää autismin kaltaisia käyttäytymismalleja. Biochim Biophys Acta. 2012;1822(6):831-842.https://doi.org/10.1016/j.bbadis.2012.01.011
[B90] Verkhratsky A, Nedergaard M. Astroglioiden fysiologia. Physiol Rev. 2018;98(1):239-389.https://doi.org/10.1152/physrev.00042.2016
[B91] Laurence JA, Fatemi SH. Gliafilamenttiproteiini (GFAP) on kohonnut autismikirjon henkilöiden aivokuoren yläpuolisilla, päälaen ja pikkuaivojen alueilla. Cerebellum. 2005;4(3):206-210.https://doi.org/10.1080/14734220500208846
[B92] Rothstein JD, Dykes-Hoberg M, Pardo CA, ym. Glutamattransporterien poistaminen paljastaa astrosyyttien kuljetuksen suuren roolin eksitotoksisuudessa ja glutamaatin poistossa. Neuron. 1996;16(3):675-686.https://doi.org/10.1016/s0896-6273(00 )80086-0
[B93] Sies H, Jones DP. Reactive oxygen species (ROS) as pleiotropic physiological signalling agents. Nat Rev Mol Cell Biol. 2020;21(7):363-383.https://doi.org/10.1038/s41580-020-0230-3
[B94] Frustaci A, Neri M, Cesario A, ym. Oksidatiiviseen stressiin liittyvät biomarkkerit autismissa: systemaattinen katsaus ja meta-analyysi. Free Radic Biol Med. 2012;52(10):2128-2141.https://doi.org/10.1016/j.freeradbiomed.2012.03.011
[B95] Bjørklund G, Meguid NA, El-Bana MA, et al. Oksidatiivinen stressi autismikirjon häiriössä. Mol Neurobiol. 2020;57(5):2314-2332.https://doi.org/10.1007/s12035-019-01742-2
[B96] James SJ, Cutler P, Melnyk S, ym. Metabolic biomarkers of increased oxidative stress and impaired methylation capacity in children with autism. Am J Clin Nutr. 2004;80(6):1611-1617.https://doi.org/10.1093/ajcn/80.6.1611
[B97] Rose S, Melnyk S, Pavliv O, et al. Todisteita oksidatiivisesta vauriosta ja tulehduksesta, jotka liittyvät matalaan glutationin redox-tilaan autismia sairastavan aivossa. Transl Psychiatry. 2012;2:e134.https://doi.org/10.1038/tp.2012.61
[B98] Bowers K, Li Q, Bressler J, et al. Glutationipolun geenivariantit ja autismin kirjon häiriöiden riski. J Neurodev Disord. 2011;3(2):132-143.https://doi.org/10.1007/s11689-011-9077-4
[B99] Rossignol DA, Frye RE. Mitokondrioiden toimintahäiriöt autismikirjon häiriöissä: systemaattinen katsaus ja meta-analyysi. Mol Psychiatry. 2012;17(3):290-314.https://doi.org/10.1038/mp.2010.136
[B100] Giulivi C, Zhang YF, Omanska-Klusek A, et al. Mitokondrioiden toimintahäiriö autismissa. JAMA. 2010;304(21):2389-2396.https://doi.org/10.1001/jama.2010.1706
[B101] Duchen MR. Mitokondriot ja kalsium: solun signaloinnista solukuolemaan. J Physiol. 2000;529 Pt 1(Pt 1):57-68.https://doi.org/10.1111/j.1469-7793.2000.00057.x
[B102] Bambini-Junior V, Rodrigues L, Behr GA, et al. Animal model of autism induced by prenatal exposure to valproate: behavioral changes and liver parameters. Brain Res. 2011;1408:8-16.https://doi.org/10.1016/j.brainres.2011.06.015
[B103] Ma Q. Nrf2:n rooli oksidatiivisessa stressissä ja toksisuudessa. Annu Rev Pharmacol Toxicol. 2013;53:401-426.https://doi.org/10.1146/annurev-pharmtox-011112-140320
[B104] Singh K, Connors SL, Macklin EA, et al. Sulforafaanihoito autismin kirjon häiriössä (ASD). Proc Natl Acad Sci U S A. 2014;111(43):15550-15555.https://doi.org/10.1073/pnas.1416940111
[B105] Bent S, Lawton B, Warren T, et al. Virtsan aineenvaihduntatuotteiden tunnistaminen, jotka korreloivat kliinisten parannusten kanssa autistisilla lapsilla, joita hoidetaan parsakaalista saatavalla sulforafaanilla. Mol Autism. 2018;9:35.https://doi.org/10.1186/s13229-018-0218-4
[B106] Cryan JF, O'Riordan KJ, Cowan CSM, et al. The Microbiota-Gut-Brain Axis. Physiol Rev. 2019;99(4):1877-2013.https://doi.org/10.1152/physrev.00018.2018
[B107] Chaidez V, Hansen RL, Hertz-Picciotto I. Ruoansulatuskanavan ongelmat lapsilla, joilla on autismia, kehitysviivästymiä tai tyypillistä kehitystä. J Autism Dev Disord. 2014;44(5):1117-1127.https://doi.org/10.1007/s10803-013-1973-x
[B108] Adams JB, Johansen LJ, Powell LD, Quig D, Rubin RA. Ruoansulatuskanavan mikrobisto ja ruoansulatuskanavan tila autismin kirjolla olevilla lapsilla – vertailu tyypillisesti kehittyneisiin lapsiin ja korrelaatio autismin vaikeusasteen kanssa. BMC Gastroenterol. 2011;11:22.https://doi.org/10.1186/1471-230X-11-22
[B109] Xu M, Xu X, Li J, Li F. Assosiaatio suoliston mikrobiston ja autismin kirjon häiriön välillä: systemaattinen katsaus ja meta-analyysi. Front Psychiatry. 2019;10:473.https://doi.org/10.3389/fpsyt.2019.00473
[B110] Liu F, Li J, Wu F, et al. Muuttunut suoliston mikrobiston koostumus ja toiminta autismikirjon häiriöissä: systemaattinen kirjallisuuskatsaus. Transl Psychiatry. 2019;9(1):43.https://doi.org/10.1038/s41398-019-0389-6
[B111] Kang DW, Park JG, Ilhan ZE, et al. Prevotellan ja muiden fermentoijien vähentynyt esiintyminen autististen lasten suoliston mikrofloorassa. PLoS One. 2013;8(7):e68322.https://doi.org/10.1371/journal.pone.0068322
[B112] Stilling RM, van de Wouw M, Clarke G, Stanton C, Dinan TG, Cryan JF. Butyraatin neurofarmakologia: Mikrobiotan-suoliston-aivojen akselin perusta? Neurochem Int. 2016;99:110-132.https://doi.org/10.1016/j.neuint.2016.06.011
[B113] MacFabe DF, Cain DP, Rodriguez-Capote K, et al. Intraventrikulaarisen propionihapon neurobiologiset vaikutukset rotilla: lyhytketjuisten rasvahappojen mahdollinen rooli autismin kirjon häiriöiden patogeneesissä ja ominaisuuksissa. Behav Brain Res. 2007;176(1):149-169.https://doi.org/10.1016/j.bbr.2006.07.025
[B114] Hsiao EY, McBride SW, Hsien S, et al. Microbiota modulate behavioral and physiological abnormalities associated with neurodevelopmental disorders. Cell. 2013;155(7):1451-1463.https://doi.org/10.1016/j.cell.2013.11.024
[B115] Bonaz B, Bazin T, Pellissier S. Vagushermo mikrobiotan-suoliston-aivojen akseleiden rajapinnassa. Front Neurosci. 2018;12:49.https://doi.org/10.3389/fnins.2018.00049
[B116] Liu S, Hagiwara SI, Bhargava A. Early-life adversity, epigenetics, and visceral hypersensitivity. Neurogastroenterol Motil. 2017;29(9).https://doi.org/10.1111/nmo.13170
[B117] Zoghbi HY, Bear MF. Synaptic dysfunction in neurodevelopmental disorders associated with autism and intellectual disabilities. Cold Spring Harb Perspect Biol. 2012;4(3):a009886.https://doi.org/10.1101/cshperspect.a009886
[B118] Bourgeron T. Geneettisestä arkkitehtuurista synaptiseen plastisuuteen autismin kirjon häiriössä. Nat Rev Neurosci. 2015;16(9):551-563.https://doi.org/10.1038/nrn3992
[B119] Südhof TC. Neuroligiinit ja neureksiinit yhdistävät synaptisen toiminnan kognitiivisiin sairauksiin. Nature. 2008;455(7215):903-911.https://doi.org/10.1038/nature07456
[B120] Jamain S, Quach H, Betancur C, et al. Neuroligiineja NLGN3 ja NLGN4 koodaavien X-sidonnaisten geenien mutaatiot liittyvät autismiin. Nat Genet. 2003;34(1):27-29.https://doi.org/10.1038/ng1136
[B121] Tabuchi K, Blundell J, Etherton MR, ym. Autismiin liittyvä neuroligiini-3-mutaatio lisää inhibitiivista synaptista transaktiota hiirillä. Science. 2007;318(5847):71-76.https://doi.org/10.1126/science.1146221
[B122] Jamain S, Radyushkin K, Hammerschmidt K, et al. Vähentynyt sosiaalinen vuorovaikutus ja ultraääniviestintä autismin monogeenisessa periytyvässä hiirimallissa. Proc Natl Acad Sci U S A. 2008;105(5):1710-1715.https://doi.org/10.1073/pnas.0711555105
Grabrucker AM, Schmeisser MJ, Schoen M, Boeckers TM. Postsynaptiset ProSAP/Shank-telineet synaptopatioiden ristitulessa. Trends Cell Biol. 2011;21(10):594-603.https://doi.org/10.1016/j.tcb.2011.07.003
[B124] Phelan K, McDermid HE. 22q13.3 deleetiöoireyhtymä (Phelan-McDermidin oireyhtymä). Mol Syndromol. 2012;2(3-5):186-201.https://doi.org/10.1159/000334260
[B125] Peça J, Feliciano C, Ting JT, ym. Shank3-mutanttimyyrillä ilmenee autismin kaltaisia käyttäytymismalleja ja striatumin toimintahäiriöitä. Nature. 2011;472(7344):437-442.https://doi.org/10.1038/nature09965
[B126] Won H, Lee HR, Gee HY, et al. Autistiset käyttäytymismallit hiirillä, joilla on Shank2-mutaatio, paranevat NMDA-reseptoritoiminnon palauttamisella. Nature. 2012;486(7402):261-265.https://doi.org/10.1038/nature11208
[B127] Baudouin SJ, Gaudias J, Gerharz S, ym. Synaptisen patofysiologian samanaikaisuus autismin syndromallisissa ja ei-syndromallisissa jyrsijämalleissa. Science. 2012;338(6103):128-132.https://doi.org/10.1126/science.1224159
[B128] Huber KM, Gallagher SM, Warren ST, Bear MF. Muuntunut synaptinen plastisuus hiirimallissa fragiilista X-kromosomin hidastuneen kehityksen retardation. Proc Natl Acad Sci U S A. 2002;99(11):7746-7750.https://doi.org/10.1073/pnas.122205699
[B129] Ecker C, Bookheimer SY, Murphy DG. Neuroimaging in autism spectrum disorder: brain structure and function across the lifespan. Lancet Neurol. 2105;14(11):1121-1134.https://doi.org/10.1016/S1474-4422(15 )00050-2
[B130] Hazlett HC, Gu H, Munsell BC ym. Varhainen aivojen kehitys autismin kirjon häiriön suuressa riskissä olevilla vauvoilla. Nature. 2017;542(7641):348-351.https://doi.org/10.1038/nature21369
[B131] Miller EK, Cohen JD. Prefrontaalikorteksin toimintaa käsittelevä integroiva teoria. Annu Rev Neurosci. 2001;24:167-202.https://doi.org/10.1146/annurev.neuro.24.1.167
[B132] Castelli F, Frith C, Happé F, Frith U. Autismi, Aspergerin oireyhtymä ja aivomekanismit mielentilojen liittämiseksi animoituihin muotoihin. Brain. 2002;125(Pt 8):1839-1849.https://doi.org/10.1093/brain/awf189
[B133] Just MA, Cherkassky VL, Keller TA, Kana RK, Minshew NJ. Autismissa toiminnallinen ja anatominen kortikaalinen aliyhteydellisyys: todisteita aivojen magneettikuvauksen (fMRI) tutkimuksesta, joka koskee suorituskykytehtävää ja corpus callosumin morfometriaa. Cereb Cortex. 2007;17(4):951-961.https://doi.org/10.1093/cercor/bhl006
[B134] Casanova MF, Buxhoeveden DP, Switala AE, Roy E. Minikolumnipatologia autismissa. Neurology. 2002;58(3):428-432.https://doi.org/10.1212/wnl.58.3.428
[B135] Adolphs R. The social brain: neural basis of social knowledge. Annu Rev Psychol. 2009;60:693-716.https://doi.org/10.1146/annurev.psych.60.110707.163514
[B136] Nordahl CW, Scholz R, Yang X, ym. Päärynän kasvun lisääntynyt tahti 2-4-vuotiailla lapsilla, joilla on autismikirjon häiriöitä: pitkittäistutkimus. Arch Gen Psychiatry. 2012;69(1):53-61.https://doi.org/10.1001/archgenpsychiatry.2011.145
[B137] Kleinhans NM, Richards T, Sterling L, et al. Poikkeava toiminnallinen konnektiivisuus autismikirjon häiriöissä kasvojen prosessoinnin aikana. Brain. 2008;131(Pt 4):1000-1012.https://doi.org/10.1093/brain/awm334
[B138] Monk CS, Weng SJ, Wiggins JL, ym. Emotionaalisten kasvojen käsittelyn hermoverkostot autismikirjon häiriöissä. J Psychiatry Neurosci. 2010;35(2):105-114.https://doi.org/10.1503/jpn.090085
[B139] Schmahmann JD. Cerebellum ja kognitio. Neurosci Lett. 2019;688:62-75.https://doi.org/10.1016/j.neulet.2018.07.005
[B140] Fatemi SH, Aldinger KA, Ashwood P, ym. Yhteisymmärryspaperi: pikkuaivojen patologinen rooli autismissa. Cerebellum. 2012;11(3):777-807.https://doi.org/10.1007/s12311-012-0355-9
[B141] Courchesne E, Yeung-Courchesne R, Press GA, Hesselink JR, Jernigan TL. Pikkuaivojen etulohkojen VI ja VII hypoplasia autismissa. N Engl J Med. 1988;318(21):1349-1354.https://doi.org/10.1056/NEJM198805263182102
[B142] Wang SS, Kloth AD, Badura A. Pikkuaivot, herkkyyskaudet ja autismi. Neuron. 2014;83(3):518-532.https://doi.org/10.1016/j.neuron.2014.07.016
[B143] Squire LR, Stark CE, Clark RE. Mediaalinen ohimolohko. Annu Rev Neurosci. 2004;27:279-306.https://doi.org/10.1146/annurev.neuro.27.070203.144130
[B144] Schumann CM, Hamstra J, Goodlin-Jones BL, ym. Talamus on suurentunut lapsilla, mutta ei nuorilla autismissa; hippokampus on suurentunut kaikilla ikäryhmillä. J Neurosci. 2004;24(28):6392-6401.https://doi.org/10.1523/JNEUROSCI.1297-04.2004
[B145] Gaigg SB, Bowler DM. Vapaa-samankaltaisuus ja unohtaminen emotionaalisesti kiihottavista sanoista autismikirjon häiriössä. Neuropsychologia. 2008;46(9):2336-2343.https://doi.org/10.1016/j.neuropsychologia.2008.03.008
[B146] Graybiel AM. Tyvitumakkeet. Curr Biol. 2000;10(14):R509-R511.https://doi.org/10.1016/s0960-9822(00 )00593-5
[B147] Langen M, Durston S, Staal WG, Palmen SJ, van Engeland H. Caudateryhmä on suurentunut korkean toimintatason lääkkeettömillä autismia sairastavilla henkilöillä. Biol Psychiatry. 2007;62(3):262-266.https://doi.org/10.1016/j.biopsych.2006.09.040
[B148] Scott-Van Zeeland AA, Dapretto M, Ghahremani DG, Poldrack RA, Bookheimer SY. Palkitsemiskäsittely autismissa. Autism Res. 2010;3(2):53-67.https://doi.org/10.1002/aur.122
[B149] Gershenzon J, Dudareva N. Terpeenien luonnontuotteiden merkitys luonnossa. Nat Chem Biol. 2007;3(7):408-414.https://doi.org/10.1038/nchembio.2007.5
[B150] Russo EB. Taming THC: potential cannabis synergy and phytocannabinoid-terpenoid entourage effects. Br J Pharmacol. 2011;163(7):1344-1364.https://doi.org/10.1111/j.1476-5381.2011.01238.x
[B151] Aprotosoaie AC, Hăncianu M, Costache II, Miron A. Linalooli: katsaus keskeiseen tuoksumolekyyliin, jolla on arvokkaita biologisia ominaisuuksia. Flavour Fragr J. 2014;29(4):193-219.https://doi.org/10.1002/ffj.3197
[B152] Harada H, Kashiwadani H, Kanmura Y, Kuwaki T. Linaloolin hajuindusoidut ahdistusta lievittävät vaikutukset hiirillä. Front Behav Neurosci. 2018;12:241.https://doi.org/10.3389/fnbeh.2018.00241
[B153] Elisabetsky E, Brum LF, Souza DO. Linaloolin antikolvusiiviset ominaisuudet glutamaattiin liittyvissä kouristusmalleissa. Phytomedicine. 1999;6(2):107-113.https://doi.org/10.1016/S0944-7113(99 )80044-0
[B154] Linck VM, da Silva AL, Figueiró M, ym. Inhaloitavan linaloolin vaikutukset ahdistuneisuuteen, sosiaaliseen vuorovaikutukseen ja aggressiiviseen käyttäytymiseen hiirillä. Phytomedicine. 2010;17(8-9):679-683.https://doi.org/10.1016/j.phymed.2009.10.002
[B155] Takahashi M, Satou T, Ohashi M, Hayashi S, Sadamoto K, Koike K. Laventeliöljyjen kemiallisen koostumuksen ja anksiolyyttis-kaltaisten vaikutusten lajienväliset vertailut inhalaation yhteydessä. Nat Prod Commun. 2011;6(11):1769-1774.https://journals.sagepub.com/doi/10.1177/1934578X1100601148
[B156] Peana AT, D’Aquila PS, Panin F, Serra G, Pippia P, Moretti MD. Linaloolin ja linalyyliasetaatin, eteeristen öljyjen yhdisteiden, anti-inflammatorinen aktiivisuus. Phytomedicine. 2002;9(8):721-726.https://doi.org/10.1078/094471102321621322
[B157] Sabogal-Guáqueta AM, Posada-Duque R, Cortes NC, Arias-Londoño JD, Cardona-Gómez GP. Hippokampuksen ja perifeeristen fosfolipidiprofiilien muutokset liittyvät neurodegeneraation tunnusmerkkeihin pitkäaikaisessa globaalin aivoverenkierron iskemian mallissa: Linaloolin vaimennus. Neuropharmacology. 2018;135:555-571.https://doi.org/10.1016/j.neuropharm.2018.04.015
[B158] Jäger W, Buchbauer G, Jirovetz L, Fritzer M. Laventeliöljyn perkutaaninen imeytyminen hierontaöljystä. J Soc Cosmet Chem. 1992;43:49-54.https://www.researchgate.net/publication/232711524_Percutaneous_absorption_of_lavender_oil_from_a_massage_oil
[B159] Buchbauer G. Biological activities of essential oils. Teoksessa: Baser KHC, Buchbauer G, toim. Handbook of Essential Oils: Science, Technology, and Applications. 2. painos. CRC Press; 2015:235-280.https://www.routledge.com/Handbook-of-Essential-Oils-Science-Technology-and-Applications/Baser-Buchbauer/p/book/9781032046419
[B160] Gertsch J, Leonti M, Raduner S, ym. Beetä-karyofylleeni on ruokavalion kannabinoidi. Proc Natl Acad Sci U S A. 2008;105(26):9099-9104.https://doi.org/10.1073/pnas.0803601105
[B161] Bahi A, Al Mansouri S, Al Memari E, Al Ameri M, Nurulain SM, Ojha S. β-Karyofylleeni, CB2-reseptoriagonisti, tuottaa hiirillä useita ahdistukseen ja masennukseen liittyviä käyttäytymismuutoksia. Physiol Behav. 2014;135:119-124.https://doi.org/10.1016/j.physbeh.2014.06.003
[B162] Atwood BK, Mackie K. CB2: kannabinoidireseptori identiteettikriisissä. Br J Pharmacol. 2010;160(3):467-479.https://doi.org/10.1111/j.1476-5381.2010.00729.x
[B163] Klauke AL, Racz I, Pradier B, ym. Kannabinoidi CB₂ -reseptorille valikoivasti vaikuttava fytokannabinoidi beeta-karyofylleeni tuottaa kipua lievittäviä vaikutuksia tulehduksellisen ja neuropaattisen kivun hiirimalleissa. Eur Neuropsychopharmacol. 2014;24(4):608-620.https://doi.org/10.1016/j.euroneuro.2013.10.008
[B164] Cheng Y, Dong Z, Liu S. β-Karyofylleeni lievittää Alzheimerin kaltaista fenotyyppiä APP/PS1 hiirissä CB2-reseptorin aktivaation ja PPARγ-reitin kautta. Pharmacology. 2014;94(1-2):1-12.https://doi.org/10.1159/000362689
[B165] Askari VR, Shafiee-Nick R. β-karyofyleenin lupaavat neuroprotektiiviset vaikutukset LPS:n indusoimaa oligodendrosyyttitoksisuutta vastaan: Mekanistinen tutkimus. Biochem Pharmacol. 2019;159:154-171.https://doi.org/10.1016/j.bcp.2018.12.001
[B166] Fontes LBA, Dias D, Aarestrup BJ, et al. β-Caryofylleeni lieventää kokeellisen autoimmuunisen enkefalomyeliitin kehittymistä C57BL/6-hiirillä. Biomed Pharmacother. 2017;91:257-264.https://doi.org/10.1016/j.biopha.2017.04.092
[B167] Alberti TB, Barbosa WL, Vieira JL, Raposo NR, Dutra RC. (-)-β-Caryofylleeni, CB2-reseptoriin selektiivinen fytokannabinoidi, vähentää motorista halvausta ja neuroinflammaatiota hiirimallissa multippeliskleroosia. Int J Mol Sci. 2017;18(4):691.https://doi.org/10.3390/ijms18040691
[B168] Galdino PM, Nascimento MV, Florentino IF, et al. Spiranthera odoratissima A. St. Hil. -lehdistä peräisin olevan eteerisen öljyn ja sen pääkomponentin, β-karyofyleenin, ahdistusta lievittävä vaikutus koirailla hiirillä. Prog Neuropsychopharmacol Biol Psychiatry. 2012;38(2):276-284.https://doi.org/10.1016/j.pnpbp.2012.04.012
[B169] Horváth B, Mukhopadhyay P, Kechrid M, et al. β-Karyofylleeni lievittää sisplatiinin aiheuttamaa munuaisvauriota kannabinoidi 2 -reseptoririippuvaisella tavalla. Free Radic Biol Med. 2012;52(8):1325-1333.https://doi.org/10.1016/j.freeradbiomed.2012.01.014
[B170] Fidyt K, Fiedorowicz A, Strządała L, Szumny A. β-caryofylleen ja β-caryofylleenoksidi – luonnolliset yhdisteet, joilla on syöpää ehkäiseviä ja kipua lievittäviä ominaisuuksia. Cancer Med. 2016;5(10):3007-3017.https://doi.org/10.1002/cam4.816
[B171] Sharma C, Al Kaabi JM, Nurulain SM, Goyal SN, Kamal MA, Ojha S. Beeta-karyofylleeni:n monilääkinnälliset ominaisuudet ja terapeuttinen potentiaali: ruokavalioperäinen fytokannabinoidi, jolla on farmaseuttista potentiaalia. Curr Pharm Des. 2016;22(21):3237-3264.https://doi.org/10.2174/1381612822666160311115226
[B172] Ammon HP. Boswellihapot ja niiden rooli kroonisissa tulehdussairauksissa. Adv Exp Med Biol. 2016;928:291-327.https://doi.org/10.1007/978-3-319-41334-1_13
[B173] Catanzaro D, Rancan S, Orso G, et al. Boswellia serrata Preserves Intestinal Epithelial Barrier from Oxidative and Inflammatory Damage. PLoS One. 2015;10(5):e0125375.https://doi.org/10.1371/journal.pone.0125375
[B174] Khoshnazar M, Bigdeli MR, Parvardeh S, Pouriran R. α-pineenin vaimentava vaikutus fokaalisen iskeemisen aivohalvauksen jälkeiseen neurokäyttäytymisen puutteeseen, oksidatiiviseen vaurioon ja inflammatoriseen vasteeseen rotassa. J Pharm Pharmacol. 2019;71(11):1725-1733.https://doi.org/10.1111/jphp.13164
[B175] Ryter SW, Alam J, Choi AM. Heme oxygenaasi-1/hiilimonoksidi: perusteista terapeuttisiin sovelluksiin. Physiol Rev. 2006;86(2):583-650.https://doi.org/10.1152/physrev.00011.2005
[B176] Umar S, Umar K, Sarwar AH, ym. Boswellia serrata -uute vaimentaa tulehduksellisia välittäjäaineita ja oksidatiivista stressiä kollageenin aiheuttamassa artriitissa. Phytomedicine. 2014;21(6):847-856.https://doi.org/10.1016/j.phymed.2014.02.001
[B177] Abdel-Tawab M, Werz O, Schubert-Zsilavecz M. Boswellia serrata: kokonaisarviointi in vitro-, prekliinisistä, farmakokineettisistä ja kliinisistä tiedoista. Clin Pharmacokinet. 2011;50(6):349-369.https://doi.org/10.2165/11586800-000000000-00000
[B178] Hosseini M, Hadjzadeh MA, Derakhshan M ym. Olibaanumin hyödylliset vaikutukset kilpirauhasen vajaatoiminnan aiheuttamaan muistin heikkenemiseen aikuisilla rotilla Morrisin vesi-labyrinttitestiä käytettäessä. Arch Pharm Res. 2010;33(3):463-468.https://doi.org/10.1007/s12272-010-0316-6
[B179] Safayhi H, Mack T, Sabieraj J, Anazodo MI, Subramanian LR, Ammon HP. Boswellihapot: uudet, spesifiset, ei-redoksinen 5-lipoksigenaasin estäjät. J Pharmacol Exp Ther. 1992;261(3):1143-1146.https://www.sciencedirect.com/science/article/abs/pii/S0022356525111300
[B180] Werz O. 5-lipoxygenase: solubiologia ja molekyylifarmakologia. Curr Drug Targets Inflamm Allergy. 2002;1(1):23-44.https://doi.org/10.2174/1568010023344959
[B181] Al-Harrasi A, Ali L, Hussain J, ym. Osa- ja raakauutteiden sekä Boswellia sacra -kasvista perinteisessä lääkinnässä saatavan suitsukkeen kivunlievitysvaikutukset eläinmalleilla. Asian Pac J Trop Med. 2014;7S1:S485-S490.https://doi.org/10.1016/S1995-7645(14 )60279-0
[B182] Cimanga K, Kambu K, Tona L, ym. Correlation between chemical composition and antibacterial activity of essential oils of some aromatic medicinal plants growing in the Democratic Republic of Congo. J Ethnopharmacol. 2002;79(2):213-220.https://doi.org/10.1016/s0378-8741(01 )00384-1
[B183] Satou T, Kasuya H, Maeda K, Koike K. Päivittäinen α-pineenin inhalaatio hiirillä: vaikutukset käyttäytymiseen ja elinkohtaan kertymiseen. Phytother Res. 2014;28(9):1284-1287.https://doi.org/10.1002/ptr.5105
[B184] Satou T, Murakami S, Matsuura M, Hayashi S, Koike K. Anksiolyyttinen vaikutus ja kudosten jakautuminen hengitetyn Alpinia zerumbet -eteerisen öljyn hiirillä. Nat Prod Commun. 2010;5(1):143-146.https://journals.sagepub.com/doi/10.1177/1934578X1000500133
[B185] Juergens UR, Dethlefsen U, Steinkamp G, Gillissen A, Repges R, Vetter H. 1,8-cineolin (eukalyptolin) anti-inflammatorinen vaikutus keuhkoastmassa: kaksoissokkotutkimus lumelääkkeellä. Respir Med. 2003;97(3):250-256.https://doi.org/10.1053/rmed.2003.1432
[B186] Santos FA, Rao VS. 1,8-sineolin, monien kasvien eteerisissä öljyissä esiintyvän terpeenihappo-oksidin tulehdusta ja kipua lievittävät vaikutukset. Phytother Res. 2000;14(4):240-244.https://doi.org/10.1002/1099-1573(200006 )14:43.0.co;2-x
[B187] Tisserand R, Young R. Essential Oil Safety: A Guide for Health Care Professionals. 2. painos. Churchill Livingstone; 2014.https://www.elsevier.com/books/essential-oil-safety/tisserand/978-0-7020-4606-4
[B188] Worth H, Schacher C, Dethlefsen U. Samanaikainen terapeuttinen hoito sineolilla (eukalyptolilla) vähentää KOLS-pahenemisvaiheita: lumekontrolloitu kaksoissokkotutkimus. Respir Res. 2009;10:69.https://doi.org/10.1186/1465-9921-10-69
[B189] Salehi B, Upadhyay S, Erdogan Orhan I, ym. Alfan ja betan pineenin terapeuttinen potentiaali: Luonnon ihmeellinen lahja. Biomolecules. 2019;9(11):738.https://doi.org/10.3390/biom9110738
[B190] Guzmán-Gutiérrez SL, Gómez-Cansino R, García-Zebadúa JC, Jiménez-Pérez NC, Reyes-Chilpa R. Litsea glaucescens -eteerisen öljyn masennuslääkevaikutus: β-pineenin ja linaloolin tunnistaminen vaikuttaviksi aineiksi. J Ethnopharmacol. 2012;143(2):673-679.https://doi.org/10.1016/j.jep.2012.07.026
[B191] Yang H, Woo J, Pae AN, ym. α-Pineeni, männynöljyjen pääkomponentti, parantaa hiirten ei-REM-unta GABAA-bentsodiatsepiinireseptorien kautta. Mol Pharmacol. 2016;90(5):530-539.https://doi.org/10.1124/mol.116.105080
[B192] Kim DS, Lee HJ, Jeon YD, ym. Alfa-pineeni ilmentää anti-inflammatorista aktiivisuutta estämällä MAPKin ja NF-κB-reitin aktivoitumista hiiren peritoneaalimakrofageissa. Am J Chin Med. 2015;43(4):731-742.https://doi.org/10.1142/S0192415X15500457
[B193] Porres-Martínez M, González-Burgos E, Carretero ME, Gómez-Serranillos MP. Salvia lavandulifolia Vahl. -rohtoöljyn suojaavat ominaisuudet oksidatiivisen stressin aiheuttamaa hermovauriota vastaan. Food Chem Toxicol. 2015;80:154-162.https://doi.org/10.1016/j.fct.2015.03.002
[B194] Miyazawa M, Watanabe H, Kameoka H. Monoterpenoidien, joilla on p-mentaanirunko, asetyylikoliiniesteraasiaktiivisuutta estävä vaikutus. J Agric Food Chem. 1997;45(3):677-679.https://doi.org/10.1021/jf960398b
[B195] Deutsch SI, Burket JA, Katz E. Myötävaikuttavatko hermosolujen migraation hienovaraiset häiriöt skitsofreniaan ja muihin neurokehityshäiriöihin? Mahdolliset geneettiset mekanismit ja mahdolliset hoitovaikutukset. Eur Neuropsychopharmacol. 2010;20(5):281-287.https://doi.org/10.1016/j.euroneuro.2010.02.005
[B196] Tan LT, Lee LH, Yin WF, et al. Perinteiset käyttötavat, fytokemia ja bioaktiivisuudet Cananga odoratassa (Ylang-Ylang). Evid Based Complement Alternat Med. 2015;2015:896314.https://doi.org/10.1155/2015/896314
[B197] Jung YH, Ha TM, Ahn J, et al. Väylä Ylang Ylang -öljyn hengittäminen paransi sosiaalista vuorovaikutusta ja ahdistuneisuuteen liittyvää käyttäytymistä valproiinihapon indusoiman autismikirjon häiriön rotilla. Nutrients. 2021;13(11):3804.https://doi.org/10.3390/nu13113804
[B198] Sinha Y, Silove N, Wheeler D, Williams K. Auditiorinen integraatiokoulutus ja muut äänihoitomuodot autismikirjon häiriöihin: systemaattinen kirjallisuuskatsaus. Arch Dis Child. 2006;91(12):1018-1022.https://doi.org/10.1136/adc.2006.094649
[B199] Cullen-Powell LA, Barlow JH, Cushway D. Tutkimus hierontahoidosta autismilasten ja heidän vanhempiensa kanssa: vaikutukset kiintymyssuhteeseen. J Child Health Care. 2005;9(4):245-255.https://doi.org/10.1177/1367493505056479
[B200] Buckle J. Clinical Aromatherapy: Essential Oils in Healthcare. 3. painos. Churchill Livingstone; 2014.https://www.elsevier.com/books/clinical-aromatherapy/buckle/978-0-7020-5440-3
[B201] Saiyudthong S, Marsden CA. Bergioöljyn akuutit vaikutukset ahdistukseen liittyvään käyttäytymiseen ja kortikosteronitasoon rotilla. Phytother Res. 2011;25(6):858-862.https://doi.org/10.1002/ptr.3325
[B202] Navarra M, Mannucci C, Delbò M, Calapai G. Citrus bergamia -eteerinen öljy: perustutkimuksesta kliiniseen sovellukseen. Front Pharmacol. 2015;6:36.https://doi.org/10.3389/fphar.2015.00036
[B203] Efferth T, Oesch F. Frankinsensin anti-inflammatoriset ja syöpää ehkäisevät vaikutukset: kohteet, hoidot ja toksisuudet. Semin Cancer Biol. 2022;80:39-57.https://doi.org/10.1016/j.semcancer.2020.01.015
[B204] Siddiqui MZ. Boswellia serrata, potentiaalinen tulehdusta ehkäisevä aine: yleiskatsaus. Indian J Pharm Sci. 2011;73(3):255-261.https://doi.org/10.4103/0250-474X.93507
[B205] Hamidpour R, Hamidpour S, Hamidpour M, Shahlari M. Frankincense (rǔ xiāng; Boswellia Species): From the Selection of Traditional Applications to the Novel Phytotherapy for the Prevention and Treatment of Serious Diseases. J Tradit Complement Med. 2013;3(4):221-226.https://doi.org/10.4103/2225-4110.119723
[B206] Moussaieff A, Mechoulam R. Boswellia-hartsit: uskonnollisista seremonioista lääketieteellisiin käyttötarkoituksiin; katsaus in vitro-, in vivo- ja kliinisiin tutkimuksiin. J Pharm Pharmacol. 2009;61(10):1281-1293.https://doi.org/10.1211/jpp/61.10.0003
[B207] Bakkali F, Averbeck S, Averbeck D, Idaomar M. Biological effects of essential oils–a review. Food Chem Toxicol. 2008;46(2):446-475.https://doi.org/10.1016/j.fct.2007.09.106
[B208] Setzer WN. Eteeriset öljyt ja ahdistusta lievittävä aromaterapia. Nat Prod Commun. 2009;4(9):1305-1316.https://pubmed.ncbi.nlm.nih.gov/19831048/
[B209] Adams RP. Identification of Essential Oil Components by Gas Chromatography/Mass Spectrometry. 4. painos. Allured Publishing; 2007.https://www.allured.com/identification-of-essential-oil-components-by-gas-chromatographymass-spectrometry-4th-edition
[B210] Dayawansa S, Umeno K, Takakura H, ym. Autonomiset vasteet ihmisillä sedrolin luonnollisen tuoksun hengittämisen aikana. Auton Neurosci. 2003;108(1-2):79-86.https://doi.org/10.1016/j.autneu.2003.08.002
[B211] Cheaha D, Reakkamnuan C, Nukitram J, ym. Vetiveröljyn inhaloinnin aiheuttamat muutokset unirytmissä ja aivosähkökäyrässä. J Intercult Ethnopharmacol. 2016;5(1):72-78.https://doi.org/10.5455/jice.20160208050736
[B212] Friedmann T. Vapautuminen ADHD:stä: lääkkeetön lähestymistapa ADHD-lasten hoitoon. Lotus Press; 2000.https://www.researchgate.net/publication/265127532_Attention_Deficit_and_Hyperactivity_Disorder_ADHD
[B213] Weyerstahl P, Marschall H, Weirauch M, Thefeld K, Surburg H. Kaupallisten vetiveröljyjen ainesosat. Flavour Fragr J. 2000;15(3):153-173.https://doi.org/10.1002/1099-1026(200005/06 )15:33.0.CO;2-V
[B214] Pripdeevech P, Chumpolsri W, Suttiarporn P, Wongpornchai S. Basilien kemiallinen koostumus ja antioksidatiivinen aktiivisuus Thaimaasta käyttäen retentioindeksejä ja kattavaa kaksiulotteista kaasukromatografiaa. J Serb Chem Soc. 2010;75(11):1503-1513.https://doi.org/10.2298/JSC100203125P
[B215] Hongratanaworakit T, Buchbauer G. Ylang ylang -öljyn rentouttava vaikutus ihmisiin transdermaalisen imeytymisen jälkeen. Phytother Res. 2006;20(9):758-763.https://doi.org/10.1002/ptr.1950
[B216] Moss M, Hewitt S, Moss L, Wesnes K. Piparmintun ja ylang-ylangin aromien vaikutus kognitiiviseen suorituskykyyn ja mielialaan. Int J Neurosci. 2008;118(1):59-77.https://doi.org/10.1080/00207450601042094
[B217] Komiya M, Takeuchi T, Harada E. Sitruunaöljyhöyry aiheuttaa stressiä lievittävän vaikutuksen moduloimalla 5-HT:n ja DA:n aktiivisuutta hiirissä. Behav Brain Res. 2006;172(2):240-249.https://doi.org/10.1016/j.bbr.2006.05.006
[B218] Venturi GB. Experimental Enquiries Concerning the Principle of the Lateral Communication of Motion in Fluids. Phil Trans R Soc Lond. 1797;87:243-260.https://royalsocietypublishing.org/doi/10.1098/rstl.1799.0005
[B219] Buckle J. Aromaterapian käyttö kroonisen kivun täydentävänä hoitona. Altern Ther Health Med. 1999;5(5):42-51.https://pubmed.ncbi.nlm.nih.gov/10450129/
[B220] Hongratanaworakit T. Aromaterapeuttiset vaikutukset ihmisiin hieronnan ja sekoitettujen eteeristen öljyjen avulla. Nat Prod Commun. 2011;6(8):1199-1204.https://www.researchgate.net/publication/51647617_Aroma-therapeutic_Effects_of_Massage_Blended_Essential_Oils_on_Humans
[B221] Valkoinen FM. Virtausmekaniikka. 8. painos. McGraw-Hill Education; 2015.https://www.mheducation.com/highered/product/fluid-mechanics-white/M9781260258318.html
[B222] Haze S, Sakai K, Gozu Y. Tuoksujen hengittämisen vaikutukset sympaattiseen aktiivisuuteen terveillä aikuisilla. Jpn J Pharmacol. 2002;90(3):247-253.https://doi.org/10.1254/jjp.90.247
[B223] Herz RS. Aromaterapia: tosiasiat ja fiktiot – tieteellinen analyysi hajuaistimusten vaikutuksista mielialaan, fysiologiaan ja käyttäytymiseen. Int J Neurosci. 2009;119(2):263-290.https://doi.org/10.1080/00207450802333953
[B224] Turek C, Stintzing FC. Stabiilisuus välttämättömien öljyjen: Katsaus. Compr Rev Food Sci Food Saf. 2013;12(1):40-53.https://doi.org/10.1111/1541-4337.12006
[B225] Buckle J. Clinical Aromatherapy in Nursing. 2. painos. Holistic Nursing Practice; 2001.https://journals.lww.com/holistic-nursing-practice/citation/2001/04000/clinical_aromatherapy_in_nursing.15.aspx
[B226] Labiris NR, Dolovich MB. Keuhkojen lääkeannostelu. Osa I: fysiologiset tekijät, jotka vaikuttavat aerosolisoitujen lääkkeiden terapeuttiseen tehokkuuteen. Br J Clin Pharmacol. 2003;56(6):588-599.https://doi.org/10.1046/j.1365-2125.2003.01892.x
Kirja-arvio. Aromaterapia terveydenhuollon ammattilaisille. 4. painos. Churchill Livingstone; 2011.https://www.elsevier.com/books/aromatherapy-for-health-professionals/price/978-0-7020-3151-0
[B228] Battaglia S. The Complete Guide to Aromatherapy. 3. painos. Black Pepper Creative; 2018.https://www.blackpeppercreative.com.au/the-complete-guide-to-aromatherapy
[B229] Posadzki P, Alotaibi A, Ernst E. Aromaterapian haittavaikutukset: systemaattinen katsaus tapausselostuksiin ja tapaussarjoihin. Int J Risk Saf Med. 2012;24(3):147-161.https://doi.org/10.3233/JRS-2012-0568
[B230] Dunn C, Sleep J, Collett D. Parannuksen aistiminen: koe, jolla arvioitiin aromaterapian, hieronnan ja lepojaksojen käyttöä teho-osastolla. J Adv Nurs. 1995;21(1):34-40.https://doi.org/10.1046/j.1365-2648.1995.21010034.x
[B231] Bowles EJ. Aromaterapeuttisten öljyjen kemia. 3. painos. Allen & Unwin; 2003.https://www.allenandunwin.com/browse/books/general-books/health-wellbeing/The-Chemistry-of-Aromatherapeutic-Oils-E-Joy-Bowles-9781741140217
[B232] Schnaubelt K. Advanced Aromatherapy: The Science of Essential Oil Therapy. Healing Arts Press; 1998.https://www.healingartspressbooks.com/advanced-aromatherapy
[B233] Schaaf RC, Lane AE. Kohti parhaiden käytäntöjen protokollaa aistiominaisuuksien arviointiin ASD:ssä. J Autism Dev Disord. 2015;45(5):1380-1395.https://doi.org/10.1007/s10803-014-2299-z
[B234] Wolkoff P, Wilkins CK, Clausen PA, Nielsen GD. Orgaaniset yhdisteet toimistoympäristöissä – aistiärsytys, haju, mittaukset ja reaktiivisen kemian rooli. Indoor Air. 2006;16(1):7-19.https://doi.org/10.1111/j.1600-0668.2005.00393.x
[B235] Dalton P. Olfactory adaptation and cross-adaptation. Teoksessa: Doty RL, toim. Handbook of Olfaction and Gustation. 3. painos. Wiley-Blackwell; 2015:443-459.https://www.wiley.com/en-us/Handbook+of+Olfaction+and+Gustation%2C+3rd+Edition-p-9780470455951
[B236] Cain WS. Nenällä tietäminen: avaimia hajun tunnistamiseen. Science. 1979;203(4379):467-470.https://doi.org/10.1126/science.760202
[B237] Kern JK, Trivedi MH, Garver CR, et al. Autismin aistien prosessoinnin poikkeavuuksien malli. Autism. 2006;10(5):480-494.https://doi.org/10.1177/1362361306066564
[B238] Lehrner J, Marwinski G, Lehr S, Johren P, Deecke L. Appiamalliset appelsiinin ja laventelin tuoksut vähentävät ahdistusta ja parantavat mielialaa hammaslääkäriasemalla. Physiol Behav. 2005;86(1-2):92-95.https://doi.org/10.1016/j.physbeh.2005.06.031
[B239] Cavanagh HM, Wilkinson JM. Laventeliöljyn biologiset vaikutukset. Phytother Res. 2002;16(4):301-308.https://doi.org/10.1002/ptr.1103
[B240] Diego MA, Jones NA, Field T, et al. Aromaterapia vaikuttaa positiivisesti mielialaan, vireystilan EEG-malleihin ja matemaattisiin laskutehtäviin. Int J Neurosci. 1998;96(3-4):217-224.https://doi.org/10.3109/00207459808986469
[B241] Field T, Diego M, Hernandez-Reif M, Cisneros W, Feijo L, Vera Y, Gil K, Grina D, Claire He Q. Laventelin tuoksuisen puhdistusgeelin vaikutukset rentoutumiseen. Int J Neurosci. 2005;115(2):207-222.https://doi.org/10.1080/00207450590519175
[B242] Goel N, Kim H, Lao RP. Hajuaistiärsyke muuttaa yöunta nuorilla miehillä ja naisilla. Chronobiol Int. 2005;22(5):889-904.https://doi.org/10.1080/07420520500263276
[B243] Ashburner J, Ziviani J, Rodger S. Sensorinen prosessointi ja luokkahuoneen emotionaaliset, käyttäytymiseen liittyvät ja koulutukselliset tulokset autismikirjon häiriötä sairastavilla lapsilla. Am J Occup Ther. 2008;62(5):564-573.https://doi.org/10.5014/ajot.62.5.564
[B244] Tomchek SD, Dunn W. Aistien käsittely autistisilla ja tyypillisesti kehittyvillä lapsilla: vertaileva tutkimus lyhyen aistiprofiilin avulla. Am J Occup Ther. 2007;61(2):190-200.https://doi.org/10.5014/ajot.61.2.190
[B245] Ben-Sasson A, Hen L, Fluss R, Cermak SA, Engel-Yeger B, Gal E. Meta-analyysi aistien säätelyn oireyksistä autismikirjon henkilöillä. J Autism Dev Disord. 2009;39(1):1-11.https://doi.org/10.1007/s10803-008-0593-3
[B246] Leekam SR, Nieto C, Libby SJ, Wing L, Gould J. Aistihäiriöiden kuvaus autismikirjon lapsilla ja aikuisilla. J Autism Dev Disord. 2007;37(5):894-910.https://doi.org/10.1007/s10803-006-0218-7
[B247] Baranek GT, David FJ, Poe MD, Stone WL, Watson LR. Sensory Experiences Questionnaire: aistien kokemuksia erittelevä kyselylomake lapsilla, joilla on autismi, kehitysviiveitä ja tyypillistä kehitystä. J Child Psychol Psychiatry. 2006;47(6):591-601.https://doi.org/10.1111/j.1469-7610.2005.01546.x
[B248] Herz RS. Hajumuistien rooli psyykkisessä ja fysiologisessa terveydessä. Brain Sci. 2016;6(3):22.https://doi.org/10.3390/brainsci6030022
[B249] Mesibov GB, Shea V, Schopler E. The TEACCH Approach to Autism Spectrum Disorders. Springer; 2004.https://link.springer.com/book/10.1007/978-0-387-23855-2
[B250] Oono IP, Honey EJ, McConachie H. Vanhemman välittämä varhainen interventio autismikirjon häiriöitä sairastaville pienille lapsille. Cochrane Database Syst Rev. 2013;(4):CD009774.https://doi.org/10.1002/14651858.CD009774.pub2
[B251] Marriott PJ, Shellie R, Cornwell C. Kaasukromatografiset tekniikat eteeristen öljyjen analyyseissä. J Chromatogr A. 2001;936(1-2):1-22.https://doi.org/10.1016/s0021-9673(01 )01314-0
[B252] Sparkman OD, Penton Z, Kitson FG. Kaasukromatografia ja massaspektrometria: käytännön opas. 2. painos. Academic Press; 2011.https://www.sciencedirect.com/book/9780123736284/gas-chromatography-and-mass-spectrometry
[B253] ISO 4720:2009. Eteeriset öljyt – Nimikkeistö. International Organization for Standardization; 2009.https://www.iso.org/standard/41076.html
[B254] ISO 11024-1:1998. Eteeriset öljyt – Yleisohjeita kromatografisille profiileille – Osa 1: Kromatografisten profiilien laatiminen esitettäväksi standardeissa. International Organization for Standardization; 1998.https://www.iso.org/standard/19053.html
[B255] Dhifi W, Bellili S, Jazi S, Bahloul N, Mnif W. Eteeristen öljyjen kemiallinen karakterisointi ja joidenkin biologisten aktiivisuuksien tutkimus: kriittinen katsaus. Medicines (Basel). 2016;3(4):25.https://doi.org/10.3390/medicines3040025
Lis-Balchin M. Aromatherapy Science: A Guide for Healthcare Professionals. Pharmaceutical Press; 2006.https://www.pharmpress.com/product/9780853696230/aromatherapy-science
[B257] Schnaubelt K. Lääketieteellinen aromaterapia: parantaminen eteerisillä öljyillä. Frog Books; 1999.https://www.innertraditions.com/books/medical-aromatherapy
[B258] Tisserand R. Aromaterapian taide. Healing Arts Press; 1977.https://www.innertraditions.com/books/the-art-of-aromatherapy
[B259] Pauli A. Eteeristen öljyjen ainesosien antimikrobiset ominaisuudet. Int J Aromather. 2001;11(3):126-133.https://doi.org/10.1016/S0962-4562(01 )80048-5
[B260] Euroopan farmakopeian komissio. Eurooppalainen farmakopea. 10. painos. Euroopan neuvosto; 2019.https://www.edqm.eu/en/european-pharmacopoeia-ph-eur-11th-edition
[B261] Wabner D, Beier C. Aromaterapia: perusteet, toimintaperiaatteet, käytäntö. 2. painos. Urban & Fischer; 2012.https://www.elsevier.com/books/aromatherapie/wabner/978-3-437-57214-4
[B262] Lis-Balchin M. Geranium and Pelargonium: The Genera Geranium and Pelargonium. CRC Press; 2002.https://www.routledge.com/Geranium-and-Pelargonium/Lis-Balchin/p/book/9780415284653
Turek C, Stintzing FC. Eteeristen öljyjen stabiilisuus: Katsaus. Compr Rev Food Sci Food Saf. 2013;12(1):40-53.https://doi.org/10.1111/1541-4337.12006
[B264] Skold M, Karlberg AT, Matura M, Börje A. Beta-karyofylliini-hajuste kemikaali – ilman hapetus ja ihon herkistyminen. Food Chem Toxicol. 2006;44(4):538-545.https://doi.org/10.1016/j.fct.2005.08.028
[B265] Tavassoli T, Miller LJ, Schoen SA, Nielsen DM, Baron-Cohen S. Sensory over-responsivity in adults with autism spectrum conditions. Autism. 2014;18(4):428-432.https://doi.org/10.1177/1362361313477246
[B266] Lane AE, Young RL, Baker AE, Angley MT. Aistiinputin käsittelyn alatyyppit autismin kirjossa: yhteys adaptiiviseen käyttäytymiseen. J Autism Dev Disord. 2010;40(1):112-122.https://doi.org/10.1007/s10803-009-0840-2
[B267] Mazurek MO, Vasa RA, Kalb LG, ym. Ahdistuneisuus, aistiyliherkkyys ja ruoansulatuskanavan ongelmat autismikirjon häiriöitä sairastavilla lapsilla. J Abnorm Child Psychol. 2013;41(1):165-176.https://doi.org/10.1007/s10802-012-9668-x
[B268] Buckle J. Kliininen aromaterapia: eteeriset öljyt käytännössä. 2. painos. Churchill Livingstone; 2003.https://www.elsevier.com/books/clinical-aromatherapy/buckle/978-0-7020-2536-6
[B269] Tuchman R, Cuccaro M, Alessandri M. Autismi ja epilepsia: historiallinen katsaus. Brain Dev. 2010;32(9):709-718.https://doi.org/10.1016/j.braindev.2010.04.008
[B270] Burkhard PR, Burkhardt K, Haenggeli CA, Landis T. Kasvien aiheuttamat kohtaukset: vanhan ongelman uudelleen ilmestyminen. J Neurol. 1999;246(8):667-670.https://doi.org/10.1007/s004150050434
[B271] Millet Y, Jouglard J, Steinmetz MD, Tognetti P, Joanny P, Arditti J. Myrkyllisyys eräille eteerisille kasviöljyille. Kliininen ja kokeellinen tutkimus. Clin Toxicol. 1981;18(12):1485-1498.https://doi.org/10.3109/15563658108990111
[B272] Pengelly A, Bennett K, Spinks J, Bensoussan A. Appraising the evidence-base for the use of essential oils in the management of epilepsy: A systematic review. Epilepsy Behav. 2012;24(1):9-15.https://doi.org/10.1016/j.yebeh.2012.02.019
[B273] Höld KM, Sirisoma NS, Ikeda T, Narahashi T, Casida JE. Alfa-tujoni (absintin vaikuttava aine): gamma-aminovoihappo tyyppi A -reseptorin modulaatio ja metabolinen detoksifikaatio. Proc Natl Acad Sci U S A. 2000;97(8):3826-3831.https://doi.org/10.1073/pnas.070042397
[B274] Millet Y, Tognetti P, Lavaire-Perlovisi M, Steinmetz MD, Arditti J, Jouglard J. Tutkimus isopin ja salvian eteeristen öljyjen kaupallisten näytteiden kouristuksia aiheuttavista ominaisuuksista. Plantes Med Phytother. 1979;13(3):179-184.https://www.sciencedirect.com/science/article/abs/pii/S0370447579800477
[B275] Marcus C, Lichtenstein EP. Luonnossa esiintyvien ravintokasvien komponenttien ja hyönteismyrkkyjen sekä pentobarbitaalin yhteisvaikutukset rotilla ja hiirillä. J Agric Food Chem. 1979;27(5):1217-1223.https://doi.org/10.1021/jf60226a004
[B276] Koutroumanidou E, Kimbaris A, Kortsaris A, ym. Pentyleenitetratsolin aiheuttamien kouristusten kohtauslatenssin lisääntyminen ja vakavuuden väheneminen rotilla eteerisen öljyn annon jälkeen. Epilepsy Res Treat. 2013;2013:532657.https://doi.org/10.1155/2013/532657
[B277] Avallone R, Zanoli P, Puia G, Kleinschnitz M, Schreier P, Baraldi M. Apigeniinin farmakologinen profiili, matricaria chamomilla -kasvista eristetty flavonoidi. Biochem Pharmacol. 2000;59(11):1387-1394.https://doi.org/10.1016/s0006-2952(00 )00264-1
[B278] Watanabe E, Kuchta K, Kimura M, Rauwald HW, Kamei T, Imanishi J. Bergamotin (Citrus bergamia (Risso) Wright & Arn.) eteerisen öljyn aromaterapian vaikutukset mielialatiloihin, parasympaattisen hermoston aktiivisuuteen ja syljen kortisolitasoihin 41 terveellä naisella. Forsch Komplementmed. 2015;22(1):43-49.https://doi.org/10.1159/000380989
[B279] Ilhan S, Savaşer S, Kölgelier S. Aromaterapian vaikutus epilepsiapotilaisiin. Epilepsy Behav. 2004;5(5):753-757.https://doi.org/10.1016/j.yebeh.2004.06.004
[B280] Meamarbashi A, Rajabi A. Piparmintun vaikutukset urheilusuoritukseen. J Int Soc Sports Nutr. 2013;10(1):15.https://doi.org/10.1186/1550-2783-10-15
[B281] Eccles R. Mentoli ja siihen liittyvät viilentävät yhdisteet. J Pharm Pharmacol. 1994;46(8):618–630.https://doi.org/10.1111/j.2042-7158.1994.tb03871.x
[B282] Silva J, Abebe W, Sousa SM, Duarte VG, Machado MI, Matos FJ. Eucalyptus-eteteeristen öljyjen analgeettiset ja anti-inflammatoriset vaikutukset. J Ethnopharmacol. 2003;89(2-3):277-283.https://doi.org/10.1016/j.jep.2003.09.007
[B283] Fachini-Queiroz FC, Kummer R, Estevão-Silva CF, ym. Thymolin ja karvakrolin, Thymus vulgaris L. eteerisen öljyn ainesosien, vaikutukset tulehdusvasteeseen. Evid Based Complement Alternat Med. 2012;2012:657026.https://doi.org/10.1155/2012/657026
[B284] Carson CF, Hammer KA, Riley TV. Melaleuca alternifolia (Tea Tree) Oil: a Review of Antimicrobial and Other Medicinal Properties. Clin Microbiol Rev. 2006;19(1):50-62.https://doi.org/10.1128/CMR.19.1.50-62.2006
[B285] Eccles R, Jawad MS, Morris S. (-)-Mentolin oraalisen antamisen vaikutukset nenän ilmanvirtauskestävyyteen ja nenän ilmanvirtauksen tunteeseen flunssan aiheuttamasta nenän tukkoisuudesta kärsivillä henkilöillä. J Pharm Pharmacol. 1990;42(9):652-654.https://doi.org/10.1111/j.2042-7158.1990.tb06625.x
[B286] Altunbas MK, Celık F, Kahraman C. Laventeliöljyn potentiaali turvalliseen käyttöön vastasyntyneillä. J Neonatal Nurs. 2020;26(6):303-307.https://doi.org/10.1016/j.jnn.2020.05.005
[B287] Srivastava JK, Shankar E, Gupta S. Kamomilla: Yrttilääke menneisyydestä loistava tulevaisuus. Mol Med Rep. 2010;3(6):895-901.https://doi.org/10.3892/mmr.2010.377
[B288] Kiecolt-Glaser JK, Graham JE, Malarkey WB, Porter K, Lemeshow S, Glaser R. Hajuaistivaikutukset mielialaan ja autonomiseen, endokriiniseen ja immuunitoimintaan. Psychoneuroendocrinology. 2008;33(3):328-339.https://doi.org/10.1016/j.psyneuen.2007.11.015
[B289] Halm MA. Eteeriset öljyt kriittisesti sairaiden potilaiden oireiden hoidossa. Am J Crit Care. 2008;17(2):160-163.https://www.researchgate.net/publication/5541002_Essential_Oils_for_Management_of_Symptoms_in_Critically_Ill_Patients
[B290] Fung LK, Mahajan R, Nozzolillo A, ym. Lääkehoito vaikeaan ärtyneisyyteen ja ongelmakäyttäytymiseen autismissa: systemaattinen katsaus ja meta-analyysi. Pediatrics. 2016;137 Suppl 2:S124-S135.https://doi.org/10.1542/peds.2015-2851K
[B291] Kirschbaum KM, Müller MJ, Malevani J, ym. Aripipratsolin ja dehydroaripipratsolin seerumitasot, kliininen vaste ja sivuvaikutukset. World J Biol Psychiatry. 2008;9(3):212-218.https://doi.org/10.1080/15622970701361255
[B292] Sprouse J, Clarke T, Reynolds L, Heym J, Rollema H. Sertraliinin ja sen metaboliitin desmetyylisertraliinin vaikutusten vertailu keskushermoston 5-HT:n takaisinoton salpauksessa in vivo. Neuropsychopharmacology. 1996;14(4):225-231.https://doi.org/10.1016/0893-133X(95 )00112-Q
[B293] Bailey DG, Dresser G, Arnold JM. Greippimehu-lääkeinteraktiot: kielletty hedelmä vai vältettävissä olevat seuraukset? CMAJ. 2013;185(4):309-316.https://doi.org/10.1503/cmaj.120951
[B294] Obach RS, Walsky RL, Venkatakrishnan K, Gaman EA, Houston JB, Tremaine LM. In vitro -tutkimusten sytokromi P450 -inhibitiotietojen käyttökelpoisuus lääkeaineiden yhteisvaikutusten ennustamisessa. J Pharmacol Exp Ther. 2006;316(1):336-348.https://doi.org/10.1124/jpet.105.093229
[B295] Guo LQ, Yamazoe Y. Sytokromi P450:n estyminen greippimehun ja rohdosvalmisteiden furanokumariineilla. Acta Pharmacol Sin. 2004;25(2):129-136.https://www.researchgate.net/publication/8881220_Inhibition_of_cytochrome_P450_by_furanocoumarins_in_grapefruit_juice_and_herbal_medicines
[B296] Paine MF, Criss AB, Watkins PB. Kaksi greippimehun merkittävää ainesosaa eroavat suoliston CYP3A4-inhiboitumisen alkamisajan suhteen. J Pharmacol Exp Ther. 2004;312(3):1151-1160.https://doi.org/10.1124/jpet.104.076570
[B297] Hanley MJ, Cancalon P, Widmer WW, Greenblatt DJ. Grapefruitin mehun vaikutus lääkeaineiden metaboliaan. Expert Opin Drug Metab Toxicol. 2011;7(3):267-286.https://doi.org/10.1517/17425255.2011.553189
[B298] Dresser GK, Bailey DG. Hedelmämehujen vaikutukset lääkkeiden poistumiseen: uusi malli lääkeaineiden yhteisvaikutuksille. Eur J Clin Invest. 2003;33 Suppl 2:10-16.https://doi.org/10.1046/j.1365-2362.33.s2.2.x
[B299] Izzo AA, Ernst E. Vuorovaikutukset yrttilääkkeiden ja määrättyjen lääkkeiden välillä: päivitetty systemaattinen katsaus. Drugs. 2009;69(13):1777-1798.https://doi.org/10.2165/11317010-000000000-00000
[B300] Henderson L, Yue QY, Bergquist C, Gerden B, Arlett P. Johannesjuoma (Hypericum perforatum): yhteisvaikutukset lääkkeiden kanssa ja kliiniset tulokset. Br J Clin Pharmacol. 2002;54(4):349-356.https://doi.org/10.1046/j.1365-2125.2002.01683.x
[B301] Unger M, Frank A. Kuuden merkittävän CYP-entsyymin aktiivisuuden estopotenssin samanaikainen määrittäminen yrttiuutteista nestekromatografialla/massaspektrometrialla ja automaattisella online-uuttamisella. Rapid Commun Mass Spectrom. 2004;18(19):2273-2281.https://doi.org/10.1002/rcm.1621
[B302] Gurley BJ, Gardner SF, Hubbard MA ja muut. Goldensealin, kava kavan, mustakoisimon ja rohtovirmajuuren in vivo -vaikutukset ihmisen sytokromi P450 1A2:n, 2D6:n, 2E1:n ja 3A4/5:n fenotyyppeihin. Clin Pharmacol Ther. 2005;77(5):415-426.https://doi.org/10.1016/j.clpt.2005.01.009
Spinella M. Psykoaktiivisten yrttilääkkeiden farmakologisen synergian merkitys. Altern Med Rev. 2002;7(2):130-137.https://pubmed.ncbi.nlm.nih.gov/11968843/
[B304] Abourashed EA, Koetter U, Brattström A. In vitro -sitoutumiskokeet valeriaanan, humalan ja niiden kiinteän yhdistelmän uutteella (Ze91019) valittuihin keskushermoston reseptoreihin. Phytomedicine. 2004;11(7-8):633-638.https://doi.org/10.1016/j.phymed.2004.03.005
[B305] Brazier NC, Levine MA. Lääke-yrttivuorovaikutukset yleisesti käytettyjen tavanomaisten lääkkeiden joukossa: seloste terveydenhuollon ammattilaisille. Am J Ther. 2003;10(3):163-169.https://doi.org/10.1097/00045391-200305000-00003
[B306] De Groot AC, Schmidt E. Essential oils: contact allergy and chemical composition. CRC Press; 2016.https://www.routledge.com/Essential-Oils-Contact-Allergy-and-Chemical-Composition/de-Groot-Schmidt/p/book/9781498702508
[B307] Shellie R, Marriott P, Huie C. Kattava kaksiulotteinen kaasukromatografinen (GC × GC) ja GC × GC-kvadrupolimassaspektrometianalyysi aasian- ja amerikkalaisesta ginsengistä. J Sep Sci. 2003;26(12-13):1185-1192.https://doi.org/10.1002/jssc.200301521
[B308] Kubeczka KH. Eteeristen öljyjen tutkimuksen historia ja lähteet. Teoksessa: Baser KHC, Buchbauer G, toim. Handbook of Essential Oils: Science, Technology, and Applications. CRC Press; 2010:3-38.https://www.routledge.com/Handbook-of-Essential-Oils-Science-Technology-and-Applications/Baser-Buchbauer/p/book/9781032046419
[B309] Cavanagh HM, Wilkinson JM. Laventeliöljy: katsaus. Aust Infect Control. 2005;10(1):35-37.https://doi.org/10.1071/HI05035
[B310] Leung AY, Foster S. Encyclopedia of Common Natural Ingredients Used in Food, Drugs, and Cosmetics. 2. painos. Wiley; 1996.https://www.wiley.com/en-us/Encyclopedia+of+Common+Natural+Ingredients+Used+in+Food%2C+Drugs%2C+and+Cosmetics%2C+2nd+Edition-p-9780471508267
[B311] Lis-Balchin M. Aromaterapia eteerisillä öljyillä. Teoksessa: Lis-Balchin M, toim. Aromatherapy Science: A Guide for Healthcare Professionals. Pharmaceutical Press; 2006:49-115.https://www.pharmpress.com/product/9780853696230/aromatherapy-science
[B312] Williams TI. Ahdistunut katsaus aromaterapiaan. Perspect Psychiatr Care. 2006;42(2):107-108.https://doi.org/10.1111/j.1744-6163.2006.00056.x
[B313] Brondino N, Fusar-Poli L, Rocchetti M, Provenzani U, Barale F, Politi P. Komplementääriset ja vaihtoehtoiset hoidot autismikirjon häiriöön. Evid Based Complement Alternat Med. 2015;2015:258589.https://doi.org/10.1155/2015/258589
Bent S, Bertoglio K, Hendren RL. Omega-3-rasvahapot autismin kirjolla: systemaattinen kirjallisuuskatsaus. J Autism Dev Disord. 2009;39(8):1145-1154.https://doi.org/10.1007/s10803-009-0724-5
[B315] Masi A, Quintana DS, Glozier N, Lloyd AR, Hickie IB, Guastella AJ. Sytokiiniaberraatiot autismikirjon häiriössä: systemaattinen katsaus ja meta-analyysi. Mol Psychiatry. 2015;20(4):440-446.https://doi.org/10.1038/mp.2014.59
[B316] Veenstra-VanderWeele J, Blakely RD. Verkostoyhteydet autismissa: geneettisen, biomerkki- ja mallijärjestelmälöydösten hyödyntäminen uusien hoitojen etsinnässä. Neuropsychopharmacology. 2012;37(1):196-212.https://doi.org/10.1038/npp.2011.185
[B317] Yamasue H, Domes G. Oksitosiini ja autismikirjon häiriöt. Curr Top Behav Neurosci. 2018;35:449-465.https://doi.org/10.1007/7854_2017_24
[B318] Petra AI, Panagiotidou S, Hatziagelaki E, Stewart JM, Conti P, Theoharides TC. Suolisto-mikrobisto-aivoakseli ja sen vaikutus immuunihäiriöitä epäileviin psykiatrisiin häiriöihin. Clin Ther. 2015;37(5):984-995.https://doi.org/10.1016/j.clinthera.2015.04.002
[B319] Mayer EA, Tillisch K, Gupta A. Suolisto/aivoakseli ja mikrobiota. J Clin Invest. 2015;125(3):926-938.https://doi.org/10.1172/JCI76304
[B320] Painike KS, Ioannidis JP, Mokrysz C, ym. Tehon pettäminen: miksi pieni otoskoko heikentää neurotieteen luotettavuutta. Nat Rev Neurosci. 2013;14(5):365-376.https://doi.org/10.1038/nrn3475
[B321] Higgins JP, Thompson SG, Deeks JJ, Altman DG. Mittaa epäjohdonmukaisuutta meta-analyyseissä. BMJ. 2003;327(7414):557-560.https://doi.org/10.1136/bmj.327.7414.557
[B322] Rossignol DA. Uudet ja kehittyvät hoidot autismikirjon häiriöihin: systemaattinen katsaus. Ann Clin Psychiatry. 2009;21(4):213-236.https://pmc.ncbi.nlm.nih.gov/articles/PMC3859980/
[B323] Moher D, Liberati A, Tetzlaff J, Altman DG; PRISMA Group. Preferred reporting items for systematic reviews and meta-analyses: the PRISMA statement. PLoS Med. 2009;6(7):e1000097.https://doi.org/10.1371/journal.pmed.1000097
[B324] Ioannidis JP, Patsopoulos NA, Rothstein HR. Syitä tai tekosyitä meta-analyysin välttämiseen forest plot -kaavioissa. BMJ. 2008;336(7658):1413-1415.https://doi.org/10.1136/bmj.a117
[B325] Loth E, Charman T, Mason L, ym. EU-AIMS Longitudinal European Autism Project (LEAP): suunnittelu ja menetelmät stratifiointibiomarkkereiden tunnistamiseksi ja validoimiseksi autismikirjon häiriöissä. Mol Autism. 2017;8:24.https://doi.org/10.1186/s13229-017-0146-8
[B326] Geschwind DH, Flint J. Psykiatristen sairauksien genetiikka ja genomiikka. Science. 2015;349(6255):1489-1494.https://doi.org/10.1126/science.aaa8954
[B327] Easterbrook PJ, Berlin JA, Gopalan R, Matthews DR. Publication bias in clinical research. Lancet. 1991;337(8746):867-872.https://doi.org/10.1016/0140-6736(91 )90201-y
[B328] Nestler EJ, Hyman SE. Animal models of neuropsychiatric disorders. Nat Neurosci. 2010;13(10):1161-1169.https://doi.org/10.1038/nn.2647
[B329] Buchbauer G, Jirovetz L, Jäger W, Plank C, Dietrich H. Rauhoittavia tuoksu-yhdisteitä ja eteerisiä öljyjä inhalaation yhteydessä. J Pharm Sci. 1993;82(6):660-664.https://doi.org/10.1002/jps.2600820623
[B330] Cooke B, Ernst E. Aromaterapia: systemaattinen katsaus. Br J Gen Pract. 2000;50(455):493-496.https://pubmed.ncbi.nlm.nih.gov/10962794/
[B331] Halm MA. Eteeriset öljyt kriittisesti sairaiden potilaiden oireiden hallinnassa. Am J Crit Care. 2008;17(2):160-163.https://www.researchgate.net/publication/5541002_Essential_Oils_for_Management_of_Symptoms_in_Critically_Ill_Patients
[B332] Hammer KA, Carson CF, Riley TV. Antimikrobinen aktiivisuus eteerisillä öljyillä ja muilla kasviuutteilla. J Appl Microbiol. 1999;86(6):985-990.https://doi.org/10.1046/j.1365-2672.1999.00780.x
[B333] Schulz KF, Altman DG, Moher D; CONSORT Group. CONSORT 2010 -lausunto: päivitetyt ohjeet rinnakkaisryhmävilvittelytutkimusten raportointiin. BMJ. 2010;340:c332.https://doi.org/10.1136/bmj.c332
[B334] Lombardo MV, Lai MC, Baron-Cohen S. Big data approaches to decomposing heterogeneity across the autism spectrum. Mol Psychiatry. 2019;24(10):1435-1450.https://doi.org/10.1038/s41380-018-0321-0
[B335] Insel TR. NIMH:n tutkimusalan kriteerit (RDoC) -projekti: psykiatrian täsmällinen lääketiede. Am J Psychiatry. 2014;171(4):395-397.https://doi.org/10.1176/appi.ajp.2014.14020138
[B336] Jeste SS, Geschwind DH. Kliiniset kokeet neurokehityshäiriöissä: Terapeuttisella rajaseudulla. Sci Transl Med. 2016;8(321):321fs1.https://doi.org/10.1126/scitranslmed.aad9874
[B337] Kovar KA, Gropper B, Friess D, Ammon HP. Veren tasot 1,8-kineolia ja hiirten liikkumisaktiivisuutta rosmariiniöljyn inhalaation ja oraalisen annon jälkeen. Planta Med. 1987;53(4):315-318.https://doi.org/10.1055/s-2006-962725
[B338] Rossignol DA, Frye RE. Katsaus tutkimustrendeihin fysiologisissa poikkeavuuksissa autismin kirjolla: immuunijärjestelmän säätelyhäiriöt, tulehdus, oksidatiivinen stressi, mitokondrioiden toimintahäiriöt ja ympäristömyrkkyaltistukset. Mol Psychiatry. 2012;17(4):389-401.https://doi.org/10.1038/mp.2011.165
[B339] Stang A. Newcastle-Ottawan asteikon kriittinen arviointi satunnaistamattomien tutkimusten laadun arvioinnissa meta-analyyseissä. Eur J Epidemiol. 2010;25(9):603-605.https://doi.org/10.1007/s10654-010-9491-z
[B340] Herz RS. Aromaterapiafaktoja ja -fiktioita: tieteellinen analyysi hajuaistivaikutuksista mielialaan, fysiologiaan ja käyttäytymiseen. Int J Neurosci. 2009;119(2):263-290.https://doi.org/10.1080/00207450802333953
[B341] Myers SM, Johnson CP; American Academy of Pediatrics Council on Children With Disabilities. Autismin kirjon häiriöitä sairastavien lasten hoito. Pediatrics. 2007;120(5):1162-1182.https://doi.org/10.1542/peds.2007-2362
[B342] Volkmar F, Siegel M, Woodbury-Smith M, King B, McCracken J, State M; American Academy of Child and Adolescent Psychiatry (AACAP) Committee on Quality Issues (CQI). Käytäntöohje autismikirjon häiriöiden arviointiin ja hoitoon lapsilla ja nuorilla. J Am Acad Child Adolesc Psychiatry. 2014;53(2):237-257.https://doi.org/10.1016/j.jaac.2013.10.013
[B343] Green VA, Pituch KA, Itchon J, Choi A, O’Reilly M, Sigafoos J. Internet survey of treatments used by parents of children with autism. Res Dev Disabil. 2006;27(1):70-84.https://doi.org/10.1016/j.ridd.2004.12.002
[B344] Bilia AR, Guccione C, Isacchi B, Righeschi C, Firenzuoli F, Bergonzi MC. Eteeriset öljyt nanokantajissa: kehittyvä strategia onnistuneeseen terapeuttiseen lähestymistapaan. Evid Based Complement Alternat Med. 2014;2014:651593.https://doi.org/10.1155/2014/651593
[B345] Woolf AD. Eteeristen öljyjen myrkytys. J Toxicol Clin Toxicol. 1999;37(6):721-727.https://doi.org/10.1081/clt-100102450
[B346] Kasper S, Gastpar M, Müller WE, ym. Silexan, uuden suun kautta annosteltavan laventeliöljyvalmisteen teho ja turvallisuus subkliinisessä ahdistuneisuushäiriössä – kliinisten tutkimusten näyttö. Wien Med Wochenschr. 2010;160(21-22):547-556.https://doi.org/10.1007/s10354-010-0845-7
B347. Inkiväärilisä lievittää autistisia käyttäytymismalleja moduloimalla AKT/GSK3β-signalointia hiirillä, jotka on altistettu raskaudenaikaiselle valproaateille. PubMed. https://doi.org/10.1039/d5fo04364f
B348. Hiwa-siirapin, persialaisen lääketuotteen, vaikutus autismin oireisiin autismin kirjolla olevilla lapsilla: satunnaistettu kaksoissokkoutettu kliininen tutkimus. Maailman lääketieteellinen aikakauslehti. https://doi.org/10.31661/gmj.v13i.3553
B349. McGuinness, F., Oswald, I. W. H., Koby, K. A. ym. (2023). Kannabidiolilla ja kannabista muistuttavilla terpeeniseoksilla on akuutteja sosiaalisia vaikutuksia autismin kirjon häiriön BTBR-hiirimallissa. Frontiers in Neuroscience. https://doi.org/10.3389/fnins.2023.1185737
ADHD-lyhennesanasto
ADHD (tarkkaavuus- ja ylivilkkaushäiriö)
ADHD.
Adjuvanttihoito
Täydentävä hoito, jota käytetään pääasiallisen hoidon rinnalla sen tehon vahvistamiseksi tai sivuvaikutusten vähentämiseksi.
Anksiolyyttinen
Ahdistusta lievittävä, ahdistusta vähentävä.
Veri-aivoeste
Valikoiva este verenkiertoon ja aivoihin, joka säätelee aineiden siirtymistä aivoihin.
CB2-reseptori
Kannabinoidireseptori tyyppi 2, osa endokannabinoidijärjestelmää, löytyy ensisijaisesti immuunisoluista; aktivaatio vaikuttaa tulehdusta ehkäisevästi.
Kemotyyppi
Kasvin kemiallinen muunnos, jolla on erilainen eteeristen öljyjen koostumus (esim. Rosmariini kemotyyppi Cineoli vs. kamferi).
DAT (dopamiininkuljettaja)
Proteiini, joka kuljettaa dopamiinia synapsiraosta takaisin hermosoluun; metyylifenidaatin pääkohde.
DAT-Okkupanz
Dopamiinitransporterien prosentti, jotka lääke on estänyt.
Dopamiini
Dopamiini, tärkeä motivaatiolle, palkitsemiselle, liikkeelle ja tarkkaavaisuudelle; ADHD:ssa usein alentunut.
ED₅₀
Annos, jolla saavutetaan 50% maksimivaikutuksesta.
GABA (gamma-aminovoihappo)
Aivojen tärkein estävä (inhibitorinen) välittäjäaine; vähentää hermosolujen ärtyvyyttä.
GABA-A-reseptori
GABA-ionikanavareseptori; aktivaatio johtaa kloridi-ionien virtaukseen sisään ja hermosolun hyperpolarisaatioon (inhibitiota).
GC/MS (kaasukromatografinen-massaspektrometria)
Analyyttinen menetelmä eteeristen öljyjen kemiallisten komponenttien tunnistamiseen ja kvantifiointiin.
IC₅₀
Konsentraatio, jolla saavutetaan 50% kohteelle (esim. reseptori, entsyymi) aiheutuvasta maksimaalisesta estosta.
Limbinen järjestelmä
Aivoalue, joka käsittelee tunteita, muistia ja motivaatiota; sisältää amygdalan, hippokampuksen ja muita rakenteita.
Linalool
Monoterpeenialkoholi, laventelin pääasiallinen vaikuttava aine; vaikuttaa ahdistusta lievittävästi, rauhoittavasti ja moduloi välittäjäainejärjestelmiä.
Mentoli
Monoterpeenialkoholi piparmintusta; aktivoi TRPM8-kylmäreseptorit, virkistää ja parantaa vireystilaa.
Metylfenidaatti (MPH)
Stimulantti, joka estää dopamiinin ja noradrenaliinin takaisinottoa; ensilinjan hoito ADHD:hen.
Mikrodialyysi
Tekniikka elävän aivojen ekstrasellulaaristen välittäjäainepitoisuuksien mittaamiseen.
monoamiini
Neurotransmitter-ryhmä, johon kuuluvat dopamiini, noradrenaliini ja serotoniini.
NET (noradrenaliinin kuljetusproteiini)
Proteiini, joka kuljettaa noradrenaliinia synapsivakosta takaisin hermosoluun; myös metyylifenidaatin kohde.
Neuroinflammaatio
Tulehdusprosessit aivoissa, jotka välittyvät usein aktivoituneiden mikroglian ja proinflammatoristen sytokiinien avulla.
Neurotransmitterit
Kemialliset välittäjäaineet, jotka välittävät signaaleja hermosolujen välillä (esim. dopamiini, serotoniini, GABA).
NF-κB (tumatekijä kappa B)
Transkriptiotekijä, joka aktivoi tulehdusgeenejä; sen estäminen on anti-inflammatorista.
NMDA-reseptori
Glutamaattireseptori, tärkeä synaptiselle plastisuudelle ja oppimiselle; yliaktiivisuus voi olla neurotoksista.
Noradrenaliini
Välittäjäaine, tärkeä vireystilan, tarkkaavaisuuden ja stressireaktion kannalta; ADHD:ssa usein vähentynyt.
Okupanz
KATSO DAT-okupanssi; reseptoreiden tai kuljettajien varattujen prosenttiosuus.
Haju
Hajuun liittyvä.
PET (positroniemissiotomografia)
Kuvantamismenetelmä, joka hyödyntää radioaktiivisesti leimattuja aineita aineenvaihduntaprosessien ja reseptorisitoutumisen visualisointiin aivoissa.
Farmakokinetiikka
Opi siitä, mitä elimistö tekee lääkkeelle (imeytyminen, jakautuminen, metabolia, erittyminen).
Lääkeainefarmakodynamiikka
Opi, mitä lääke tekee elimistössä (vaikutusmekanismit, vaikutukset).
Etuaivokuori
Aivojen otsan takainen alue, joka on tärkeä toiminnanohjaukselle (suunnittelu, impulssikontrolli, työmuisti); ADHD:ssa usein aliaktiivinen.
Reseptori
Solukalvolla tai solun sisällä olevat proteiinit, jotka sitovat spesifisiä signaalimolekyylejä (välittäjäaineita, hormoneja) ja käynnistävät niiden seurauksena solun reaktioita.
SERT (serotoniinin kuljettajaproteiini)
Proteiini, joka kuljettaa serotoniinia synapsiraosta takaisin hermosoluun; masennuslääkkeiden (SSRI-lääkkeiden) kohde.
Serotoniini
Välittäjäaine, tärkeä mielialalle, unelle, ruokahalulle ja impulssikontrollille.
SPECT (Single Photon Emission Computed Tomography)
Kuvantamismenetelmä, joka muistuttaa PETiä ja käyttää radioaktiivisia jäljitysaineita aivojen toimintojen kuvaamiseen.
Tyvitumakkeet
Tyvitumakkeiden aivoalue, joka on runsaasti dopamiinitransporttereita; tärkeä liikkumiselle, motivaatiolle ja palkkiolle; metyylifenidaatin pääkohdealue.
Synapsi
Synapsi.
Synapsikostama
Synapsikuilu.
TRP-kanavat (Transient Receptor Potential)
Ionikanavien perheet, jotka reagoivat eri ärsykkeisiin (lämpötila, kemikaalit); esim. TRPM8 (kylmä/mentoli), TRPV1 (kuuma/kapsaisiini).
Venturi-periaate
Fysikaalinen periaate, jossa paineen lasku ahtaumassa imee nesteitä tai öljyjä ja sumuttaa ne; monien diffuusorien perusta.
β-karyofylleeni
Seskviterpeenit mustapippurista ja kannabiksesta; selektiivinen CB2-reseptoriagonisti, jolla on anti-inflammatorisia ominaisuuksia.
1,8-Kineoli (Eukalyptoli)
Monoterpeenioksidi rosmariinista ja eukalyptuksesta; limaa irrottava, tulehdusta lievittävä ja kognitiota edistävä vaikutus.
5-HT1A-reseptori
Serotoniini-reseptorialatyyppi; aktivaatio on ahdistusta lievittävä ja masennusta ehkäisevä.
Raportin loppu
Tämä raportti on laadittu 27. huhtikuuta 2026 perustuen 87 metyylifenidaattia koskevan aivokonsentraatiotutkimuksen ja 159 ADHD-kontekstissa esiintyvää eteerisiä öljyjä koskevan julkaisun systemaattiseen analyysiin. Kaikki väitteet on todistettu primaarilähdekirjallisuudella.
ASD-sanasto
1,8-Kineoli (Eukalyptoli)
Monoterpeenioksidi, eukalyptusöljyn pääkomponentti (70–90 %), osoittaa ahdistusta lievittäviä vaikutuksia GABA-A-reseptorien modulaation kautta ja sillä on anti-inflammatorisia ominaisuuksia; vasta-aiheinen alle 3-vuotiailla lapsilla kurkunpään kouristuksen riskin vuoksi.
α-pineeni
Bisyklinen monoterpeenin havupuissa, rosmariinissa ja kannabiksessa; osoittaa GABAergistä modulaatiota, ahdistusta lievittäviä ja tulehdusta ehkäiseviä vaikutuksia; prekliininen näyttö neuroprotektiivisista ominaisuuksista.
Mantelitumake
Mantelin muotoinen aivojen rakenne mediaalisessa ohimolohkossa, keskeinen tunteiden käsittelylle, pelkokonditionoinnille ja sosiaaliselle havainnoinnille; autismin kirjolla suurentunut varhaislapsuudessa, vähentynyt aktivaatio kasvojen käsittelyssä.
Antioksidantti
Molekyyli, joka vähentää oksidatiivista stressiä neutraloimalla reaktiivisia happilajeja (ROS); esimerkkejä: glutationi, superoksididismutaasi, katalaasi, C-vitamiini, E-vitamiini; ASD:ssä vähentynyt antioksidanttikapasiteetti.
Soveltava käyttäytymisanalyysi (ABA)
Näyttöön perustuva käyttäytymisterapeuttinen interventio ASD:lle, perustuu oppimisperiaatteisiin (vahvistaminen, kehotus, muokkaaminen); parantaa kommunikaatiota, sosiaalisia taitoja ja adaptiivisia käyttäytymismalleja.
Aripipratsoli
Epätyypillinen antipsykootti, osittainen dopamiini-D2-agonisti; FDA-hyväksytty ASD:n ärtyneisyyteen; haittavaikutukset: painonnousu, akatisia, metabolinen oireyhtymä; metaboloituu CYP2D6:n ja CYP3A4:n kautta.
Astrocyytit
Tähdenmuotoiset gliasolut keskushermostossa; säätelevät glutamaatin homeostaasia (EAAT1/2-kuljettajien kautta), K+-puskurointia, veri-aivoestettä ja neuronien metabolista tukea; ASD:ssä astrogliosis (kohonnut GFAP-ekspressio).
β-karyofylleeni (BCP)
Seskviterpeenhiilivety mustapippurissa, neilikassa, kannabiksessa; selektiivinen CB2-reseptoriagonisti ilman psykoaktiivisia vaikutuksia; vähentää neuroinflammaatiota, mikroglian aktivaatiota ja oksidatiivista stressiä.
Bentsodiatsepiinin sitoutumispaikka
Allosteerinen modulaatiokohta GABA-A-reseptorissa; bentsodiatsepiinit (diatsepaami, loratsepaami) sitoutuvat tähän ja potentioivat GABAergista inhibitiota; linalooli ja 1,8-sineoli ovat vuorovaikutuksessa tämän kohdan kanssa (flumatseniiliherkkä).
Bergamotti (Citrus bergamia)
Sitrushedelmä, eteerinen öljy sisältää linaloolia, linalyyliasetaattia, limoneenia; RCT ASD-lapsilla ei osoittanut merkittäviä anksiolyyttisiä vaikutuksia; sisältää bergapteenia (CYP3A4-inhibiittori), bergapteenittomia variantteja (FCF) saatavilla.
Boswelliinihapot
Boswellian (suitsutus) pentasykliset triterpeenihapot; aktivoivat Nrf2/HO-1-antioksidanttireitin, vähentävät neuroinflammaatiota (mikrogliat, astrosyytit, TNF-α, IL-6); prekliininen näyttö ASD-tyyppisten käyttäytymismallien parantumisesta VPA-malleissa.
Bumetanidi
Kuokinta-diureetti, NKCC1-kotransportterin estäjä; korjaa viivästynyttä GABA-kytkentää ASD-hiirimallissa; kliiniset tutkimukset osoittavat kohtalaista parannusta sosiaalisessa kommunikaatiossa ASD-lapsilla, mutta menetelmällisiä rajoituksia.
Kamferi
Terpeeniketoni kamferissa (Cinnamomum camphora) ja rosmariinissa (kamferikemotyyppi); laskee kouristuskynnystä, voi laukaista kouristuksia; vasta-aiheinen epilepsiapotilailla ja ASD-potilailla, joilla on samanaikainen epilepsia.
Cananga odorata (Ylang-Ylang)
Trooppinen puu, eteerinen öljy sisältää linaloolia, geraniolia, β-karyofyleeniä; prekliininen tutkimus osoitti VPA-rotta-mallissa parannusta ASD:tä muistuttavissa käyttäytymismalleissa moduloimalla serotoniini- ja dopamiiniaineenvaihduntaa.
CB2-reseptori (kannabinoidityyppinen 2 -reseptori)
G-proteiinikytkentäinen reseptori, jota ilmentyy ensisijaisesti immuunisoluissa (mikrogliat, perifeeriset immuunisolut); aktivaatio vähentää sytokiinien vapautumista, mikrogliatoimintaa ja neuroinflammaatiota; β-karyofylleeni on selektiivisempi CB2-agonisti.
Cedrol
Seskviterpeenialkoholi setripuuöljyssä; perinteisesti yhdistetty rauhoittaviin ominaisuuksiin, mutta tieteellinen näyttö GABAergisistä mekanismeista tai ASD:n kliinisestä tehosta puuttuu.
Kopiomäärävariaatiot (CNV:t)
Genomiset deleetiot tai duplikaatiot >1 kb; yleisiä ASD:ssä (15q11-13-duplikaatio, 16p11.2-deleetio, 22q13-deleetio/Phelan-McDermidin oireyhtymä); vaikuttavat usein synaptisiin geeneihin (SHANK3, NLGN4).
Sytokromi P450 (CYP)
Entsyymiperhe, joka katalysoi lääkeaineiden metaboliaa; CYP3A4 ja CYP2D6 metabolisoivat risperidonia ja aripipratsolia; Bergapteeni (bergamottiöljyssä) estää CYP3A4:ää, voi nostaa lääkeainepitoisuuksia.
Dopamiini (DA)
Katekoliamiini-välittäjäaine; välittää palkitsemiskäsittelyä, motivaatiota, motorista kontrollia; autismikirjon häiriössä vähentynyt striatumin aktivaatio sosiaalisista palkinnoista, muuttunut dopamiinitransportterin tiheys; Ylang-Ylang modulii DA-metaboliaa prekliinisissä malleissa.
DSM-5 (Diagnostic and Statistical Manual of Mental Disorders, 5. painos)
American Psychiatric Associationin luokitusjärjestelmä; määrittelee ASD:n kahden pääalueen kautta: (1) jatkuvat puutteet sosiaalisessa kommunikaatiossa/vuorovaikutuksessa, (2) rajoittuneet, toistuvat käyttäytymismallit.
Dysbioosi
Suolen mikrobiotan epätasapaino; ASD:ssä vähentynyt mikrobiston monimuotoisuus, lisääntynyt Firmicutes/Bacteroidetes-suhde, vähentynyt Bifidobacterium ja Prevotella; korreloi oireiden vakavuuden kanssa.
E/I-epätasapaino (kiihtyvä-estävä epätasapaino)
Epätasapaino eksitatorisen (glutamatergisen) ja inhiboivan (GABAergisen) hermovälityksen välillä; autismin kirjon häiriön keskeinen patofysiologinen hypoteesi; johtaa yliärtyneisyyteen, häiriintyneeseen aistisuodatukseen ja sosiaalisen informaation käsittelyn heikkenemiseen.
Elektroakupunktio
Akupunktio sähköstimulaatiolla; prekliiniset tutkimukset osoittavat ASD-tyyppisten käyttäytymismallien paranemista VPA-hiirillä vagushermoon vaikuttavien mekanismien ja mikrobiomin muokkauksen kautta.
Epilepsia
Neurologische Erkrankung mit rekurrenten Anfällen; 10–30 % der ASD-Patienten haben komorbide Epilepsie; campherhaltige ätherische Öle (Kampfer, Rosmarin-Campher-Chemotyp, Salbei) sind kontraindiziert.
Fekaalinen mikrobiotasiirto (FMT)
Suoliston mikrobiston siirto terveiltä luovuttajilta vastaanottajille; prekliiniset tutkimukset osoittivat ASD-kaltaisten käyttäytymismallien paranemista hiirimallissa; avoin kliininen tutkimus ASD-lapsilla osoitti parannusta GI-oireissa ja käyttäytymisessä.
Flumatseniili
Bentsodiatsepiiniantagonisti, sitoutuu GABA-A-reseptorin bentsodiatsepiinisidospaikkaan; estää linaloolin ja 1,8-cineolin anksiolyyttisiä vaikutuksia, mikä vahvistaa niiden vuorovaikutusta tämän paikan kanssa.
GABA (γ-aminovoihappo)
Primaarinen inhiboiva välittäjäaine keskushermostossa; sitoutuu GABA-A- (ionotrooppisiin) ja GABA-B-reseptoreihin (metabotrooppisiin); ASD:ssä vähentynyt GABAergisen järjestelmän toiminta, muuttuneet GABA-tasot, häiriintynyt GABA-kytkentä kehityksen aikana.
GABA-A-reseptori
Ligandi-ohjattu kloridikanava; aktivoituminen GABA:lla johtaa kloridin virtaukseen ja hyperpolarisaatioon (inhibointi); sisältää bentsodiatsepiinisitoutumispaikan; linalooli, 1,8-sineoli ja α-pineeni moduloivat GABA-A-reseptoreita.
GABA-kytkin
Kehitysbiologinen siirtymä eksitatorisesta inhiboivaksi GABA-vaikutukseksi; välittyy NKCC1- ja KCC2-kotransportteriekspressionin vaihtuessa; ASD:ssa viivästynyt; oksitosiini ja bumetanidi voivat normalisoida GABA-kytkimen.
GAD65/GAD67 (Glutamaattidekarboksylaasi 65/67)
Entsyymi, joka muuntaa glutamaatin GABA:ksi; ASD:ssä vähentynyt GAD65/67:n ilmentyminen etuotsalohkossa ja pikkuaivoissa, mikä johtaa vähentyneeseen GABA-synteesiin.
Kaasukromatografia-massaspektrometria (GC/MS)
Analyyttinen tekniikka haihtuvien komponenttien tunnistamiseen ja kvantifiointiin; kultastandardi eteeristen öljyjen kemiallisessa karakterisoinnissa; mahdollistaa väärennösten, epäpuhtauksien ja erien välisen vaihtelun havaitsemisen.
Glutamaatit (Glu)
Keskeinen kiihdyttävä välittäjäaine keskushermostossa; sitoutuu ionotrooppisiin (NMDA, AMPA, kainaaatti) ja metabotrooppisiin (mGluR1-8) reseptoreihin; tunne-elämän ja sosiaalisten taitojen häiriössä (ASD) muuttuneet glutamaattitasot, häiriintyneet glutamaattisynapsien geenit (GRIN2B, GRIA1), liiallinen glutamaattitransmissio.
Glutationi (GSH)
Tripeptidi (γ-Glutamyyli-Kysteynyyli-Glysiini), ensisijainen solunsisäinen antioksidantti; ASD:ssä (autismikirjon häiriö) alentuneet GSH-tasot, kohonnut hapetettu glutationi (GSSG), alentunut GSH/GSSG-suhde; GSH-synteesientsyymien (GCLC, GSS) geenivariantit assosioituneet ASD:hen.
Aivo-suolisto-akseli
Kaksisuuntainen viestintä ruoansulatuskanavan ja keskushermoston välillä hermoston (Vagushermo), endokriinisten (HPA-akseli), immunologisten ja aineenvaihdunnan reittien kautta; ASD:ssä dysbioosi, muuttunut välittäjäaineiden esiasteiden tuotanto, häiriintyneet suoli-aivo-signalointireitit.
Himeeoksigenaasi-1 (HO-1)
Entsyymi, joka hajottaa hemiä biliverdiiniksi (antioksidantti), hiilimonoksidiksi (anti-inflammatorinen) ja raudaksi; Nrf2-säädelty; bosweliinihapot lisäävät HO-1:n ilmentymistä; HO-1:n induktio suojaa oksidatiiviselta stressiltä ja neuroinflammatiolta.
Hippokampus
Aivorakenne mediaalisessa ohimolohkossa; välittää deklaratiivista muistia, spatiaalista navigointia, kontekstuaalista prosessointia; autismissa suurentunut lapsuudessa, muuttunut konnektiivisuus, häiriintynyt kontekstuaalinen pelkoehdollistuminen.
Hyperserotonemia
Lisääntynyt perifeerinen serotoniinipitoisuus; havaittu 25-50 %:llä ASD-potilaista; suhde keskushermoston 5-HT-pitoisuuksiin epäselvä; johtuu mahdollisesti verihiutaleiden heikentyneestä serotoniinin otosta tai lisääntyneestä perifeerisestä synteesistä.
Interleukiini-6 (IL-6)
Proinflammatorinen sytokiini; ASD:ssä kohonneet IL-6-tasot plasmassa ja likvorissa; äidin immuuniaktivaatio IL-6-tuotannolla tuottaa ASD-tyyppisiä fenotyyppejä hiirimallintoeisiin; IL-6 moduloi synaptista transmissiota ja kehitystä.
Pikkuaivot
Aivojen takaosa; perinteisesti yhdistetty motoriseen kontrolliin, mutta sillä on rooleja myös kognitiivisissa prosesseissa, aistien ennakoimisessa ja sosiaalisessa oppimisessa; ASD:ssä Purkinjen solujen menetys, pienempi vermis-tilavuus, häiriintynyt aivojen ja aivokuoren välinen yhteys.
Laventeli (Lavandula angustifolia)
Aromaattinen kasvi, eteerinen öljy sisältää 25-45 % linaloolia ja linalyyliasetaattia; pienissä pilottitutkimuksissa on raportoitu parantuneesta ABA:n noudattamisesta ja jaetusta tarkkaavaisuudesta ASD-lapsilla; prekliinistä näyttöä GABAergisesta modulaatiosta, serotonergisesta säätelystä ja oksitonergisestä aktivoinnista.
Linalool
Monoterpeeninen alkoholi, laventelin, korianterin ja bergamotin pääkomponentti; moduloi GABA-A-reseptoreita bentsodiatsepiinien sitoutumiskohdassa (flumatseniiliherkkä), vaikuttaa serotoniinitasoihin, lisää solunsisäistä kalsiumia oksitosiinineuroneissa, vaikuttaa tulehdusta ehkäisevästi.
Linalyyliasetaatti
Esteriä linaloolista ja etikkahaposta; laventelin (25–45 %) ja bergamotin pääkomponentti; edistää ahdistusta lievittäviä ja rauhoittavia vaikutuksia; hydrolysoituu linalooliksi.
Pitkäaikainen potentiaatio (LTP) / Pitkäaikainen depressio (LTD)
Synaptisen plastisuuden solu-mekanismit; LTP: pitkäaikainen synaptisen transissionin vahvistuminen korkeataajuisen stimulaation jälkeen; LTD: pitkäaikainen heikkeneminen matalataajuisen stimulaation jälkeen; ASD:ssa häiriintynyt LTP/LTD-tasapaino useilla aivoalueilla.
Magneettikuvaus (MRS)
Ei-invasiivinen kuvantamismenetelmä metabolian (glutamaatti, GABA, N-asetyyliaspartaatti, kreatiini) in vivo -kvantifiointiin; ASD:ssä MRS osoittaa alueellisia muutoksia glutamaatti- ja GABA-pitoisuuksissa.
Äidin immuunijärjestelmän aktivointi
Prekliininen malli, jossa tiineitä eläimiä hoidetaan immuunistimulaattoreilla (Poly(I:C), LPS); jälkeläisillä ilmenee autismin kirjon häiriöihin (ASD) viittaavia käyttäytymismalleja, kohonneita proinflammatorisia sytokiineja, häiriintynyttä synaptista kehitystä; mallintaa ympäristöön liittyvää ASD:n riskitekijää.
Melatoniini
Käpyrauhasen tuottama hormoni; säätelee vuorokausirytmiä ja unta; unihäiriöt yleisiä ASD:ssä; melatoniinilisä parantaa unen latenssia ja kestoa; meta-analyysit osoittavat kohtalaista tehoa.
Mikrogliat
Keskihermoston residentit immuunisolut; säätelevät synaptista karsintaa, neuraalista kehitystä, immuunitarkkailua; ASD:ssä aktivoituneet mikroglian solut (lisääntynyt Iba1-ekspressio, ameboidi morfologia) etuotsalohkossa, pikkuaivoissa; vapauttavat pro-inflammatorisia sytokiinejä ja ROS:ta.
Mitokondrioiden toimintahäiriö
Heikentynyt mitokondrioiden toiminta (hengitysketjun aktiivisuuden väheneminen, lisääntynyt laktaatti, vähentynyt ATP-synteesi); 5–30 % ASD-potilaista; johtaa lisääntyeeseen ROS-tuotantoon, oksidatiiviseen stressiin, häiriintyneeseen kalsium-homeostaasiin.
Neuroligiini (NLGN)
Postsynaptiset solujen adheesiomolekyylit (NLGN1-4); vuorovaikutuksessa presynaptisten neureksiinien kanssa; säätelevät synaptista erilaistumista, kypsymistä ja toimintaa; NLGN3:n ja NLGN4X:n mutaatiot ASD-potilailla; NLGN3-R451C-hiirillä on lisääntynyt inhibitorinen transmissio ja ASD:n kaltaisia fenotyyppejä.
Neureksiini (NRXN)
Presynaptiset solujen adheesiomolekyylit (NRXN1-3); vuorovaikutuksessa postsynaptisten neuroligiinien kanssa; säätelevät synaptista organisoitumista; NRXN1:n mutaatiot ASD-potilailla; NRXN1-deleetioihin liittyy ASD, skitsofrenia ja älyllinen kehitysvammaisuus.
Neuroinflammaatio
Tulehdusreaktio keskushermostossa, jolle on ominaista mikroglian ja astrosyyttien aktivoituminen, lisääntyneet pro-inflammatoriset sytokiinit (TNF-α, IL-6, IL-1β), heikentynyt veri-aivoeste; ASD:ssä krooninen neuroinflammatio useilla aivoalueilla.
NF-κB (tumatekijä kappa B)
Transkriptiotekijä, joka säätelee pro-inflammatorisia geenejä (TNF-α, IL-6, IL-1β, COX-2); lisääntynyt NF-κB:n aktivoituminen ASD:ssä; β-karyofylyleeni ja bosweliinihapot estävät NF-κB-signalointireittejä.
NMDA-reseptori (N-metyyli-D-asparataattireseptori)
Ionotrooppinen glutamaattireseptori, kalsiumia läpäisevä kanava; keskeinen synaptisen plastisuuden (LTP/LTD), oppimisen ja muistin kannalta; muuttunut NMDA-reseptorin alayksikön ilmentyminen ASD:ssä (GRIN2A, GRIN2B), heikentynyt NMDA-reseptorin toiminta SHANK2:n tyrmäävissä hiirissä.
Nrf2 (tumatekijä erytroidi 2:een liittyvä tekijä 2)
Transkriptiotekijä, antioksidanttivasteen pääsäätelijä; indusoi HO-1:n, NQO1:n, glutationi-S-transferaasien ja muiden antioksidanttisten entsyymien ilmentymistä; boswelliinihapot aktivoivat Nrf2:ta; Nrf2:n aktivaattorit (sulforafaani) osoittavat pienissä tutkimuksissa parannuksia ASD:ssä.
Oksidatiivinen stressi
Epätasapaino ROS-tuotannon ja antioksidatiivisen puolustuksen välillä; ASD:ssä lisääntynyt lipidien peroksidaatio, proteiinien karbonylointi, DNA-oksidaatio, vähentynyt antioksidanttikapasiteetti (GSH, SOD, katalyysi); edistää hermosolujen vaurioitumista ja toimintahäiriöitä.
Oksitosiini (OT)
Neuropeptidi, jota syntetisoidaan hypotalamuksessa; keskeinen rooli sosiaalisessa kiintymyksessä, luottamuksessa, sosiaalisessa kognitiossa, stressinsäätelyssä; ASD:ssä vähentyneet plasma-OT-tasot, muuttunut OXTR-ilmentyminen; nenäsumutteena annettu OT antaa vaihtelevia tuloksia; OT säätelee GABAergista kehitystä prekliinisissä malleissa.
Parvalbumiini-positiiviset interneuronit
GABAergisen interneuronin alatyyppi, joka ilmentää kalsiumia sitovaa proteiinia parvalbumiinia; välittää nopeaa, synkronista estymistä; ASD:ssä parvalbumiini-interneuronien tiheys ja toiminta vähentyneet etuotsalohkossa.
Phelan-McDermid-oireyhtymä
Geneettinen syndrooma, joka johtuu 22q13-deleetistä, joka sisältää SHANK3-geenin; luonteenomaisia piirteitä ovat autismikirjon häiriöt, älyllinen kehitysvammaisuus, puheen puutteet, hypotonia; osoittaa SHANK3:n kausaalisen roolin autismin patogeneesissä.
Etuaivokuori
Aivokuoren etulohko; välittää toiminnanohjausta, työmuistia, kognitiivista joustavuutta, sosiaalista kognitiota, mielen teoriaa; ASD:ssä vähentynyt etulohkon aktivaatio sosiaalisen kognition tehtävissä, häiriintynyt etulohkon konnektiivisuus, GABAergiset puut.
Propionaatti
Lyhytketjuinen rasvahappo, jonka suolistomikrobisto tuottaa; ASD:ssä mahdollisesti kohonneet propionaattitasot; propionaattialtistus jyrsijämalleissa indusoi ASD:n kaltaisia käyttäytymismalleja, neuroinflammaatiota, oksidatiivista stressiä.
Reaktiiviset happilajit (ROS)
Erittäin reaktiiviset molekyylit (superoksidi, vetyperoksidi, hydroksyyliradikaali); syntyvät mitokondriaalisen hengityksen sivutuotteina; liiallisina pitoisuuksina ROS aiheuttavat lipideille, proteiineille ja DNA:lle oksidatiivista vauriota; ASD:ssä lisääntynyttä ROS-tuotantoa.
Risperidoni
Epätyypillinen antipsykootti, dopamiini-D2- ja serotoniini-5-HT2A-antagonisti; FDA:n hyväksymä ASD:n ärtyneisyyteen; haittavaikutukset: painonnousu, hyperprolaktinemia, ekstrapulmonaaliset oireet, metabolinen oireyhtymä; metabolisoituu CYP2D6:n kautta.
Serotoniini (5-HT, 5-hydroksitryptamiini)
Monoamiini-välittäjäaine; välittää mielialaa, ahdistusta, unta, ruokahalua, sosiaalista kognitiota; ASD:ssä hypertoninen serotoniini (perifeerinen), alentunut keskushermoston serotoniinisynteesi, geenivariantit 5-HTT:ssä ja TPH2:ssa; Linaool ja Ylang-ylang moduloivat serotoniinijärjestelmää.
SHANK-proteiinit (SH3- ja useat ankyriinirepeiinidomeenit)
Postsynaptiset tukiproteiinit (SHANK1-3); järjestävät glutamattireseptoreita, aktiinisytoskelettia, signalointimolekyylejä; mutaatiot SHANK2:ssa ja SHANK3:ssa ASD:ssä; SHANK3-knockout-hiiret osoittavat vähentynyttä piikkitiheyttä, häiriintynyttä synaptista transmissiota, ASD-tyyppisiä käyttäytymismalleja.
Tyvitumakkeet
Tyvitumakkeiden subkortikaaliset rakenteet (häntätumake, putamen, accumbens-tumake); välittää palkkionkäsittelyä, tottumisen oppimista, motorista kontrollia; ASD:ssä striatumin suureneminen, pienentynyt aktivaatio sosiaalisissa palkkioissa, häiriintynyt kortiko-striataalinen kytkeytyvyys.
Synaptinen karsinta
Kehitysbiologinen prosessi, jossa ylimääräiset synapsit eliminoidaan. Välittyy mikroglian ja komplementtijärjestelmän kautta. Autismin kirjon häiriöissä (ASD) "karsiminen" voi olla häiriintynyt (liikaa tai liian vähän), mikä johtaa muuttuneeseen synaptiseen tiheyteen ja kytkeytyvyyteen.
Terpeeni
Luonnonaineiden monipuolinen luokka, joka koostuu isopreeniyksiköistä (C5H8); eteeristen öljyjen pääkomponentteja; monoterpeenit (C10): linalooli, 1,8-sineoli, α-pineeni; seskviterpeenit (C15): β-karyofylleeni, setdroli; triterpeenit (C30): boswellihapot.
TNF-α (kasvannaisnekroositekijä-α)
Tulehdusta edistävä sytokiini; ASD:ssä kohonneet TNF-α-tasot plasmassa, aivo-selkäydinnesteessä, postmortaalissa aivokudoksessa; äidin immunaktivointi kohonneella TNF-α:lla tuottaa ASD:n kaltaisia fenotyyppejä; TNF-α moduloi synaptista transmissiota, vähentää GABAergistä inhibitiota.
Translokatoriproteiini (TSPO)
Mitochondriaalinen proteiini, jota säädelty ylöspäin aktivoituneissa mikroglioissa; PET-ligandit (esim. [11C]-PBR28) sitoutuvat TSPO:hon ja mahdollistavat aktivoituneiden mikroglioiden in-vivo-kuvantamisen; ASD:ssä lisääntynyt TSPO-sitoutuminen useilla aivoalueilla.
Tryptofaani
Välttämätön aminohappo, serotoniinin ja melatoniinin esiaste; tryptofaanin metabolia voi olla häiriintynyt ASD:ssä; suolistomikrobiota vaikuttaa tryptofaanin saatavuuteen ja metaboliaan kynureniini- ja serotoniinireittien kautta.
Valproiinihappo (VPA)
Epilepsialääke; prenataalinen VPA-altistus on riskitekijä ihmisen autismikirjon häiriölle; VPA-indusoidut ASD-hiirimallit: tiineitä hiiriä käsitellään VPA:lla, jälkeläiset osoittavat ASD:n kaltaisia käyttäytymispiirteitä, neuroinflammaatiota, oksidatiivista stressiä; laajalti käytetty prekliininen malli.
Venturi-periaate
Fysikaalinen periaate (Bernoulli'n ilmiö): Nesteen paineen aleneminen sen virratessa ahtauman läpi; Organik Aromas Nebulizer 3.0 -laitteessa paineilma synnyttää suuttimen kautta alipaineen, joka imee eteerisen öljyn ja hajottaa sen hienoksi pisaroiksi (kylmäsumutus).
Vetiver (Vetiveria zizanioides)
Trooppinen ruoho, eteerinen öljy sisältää vetiverolia, khusimolia, α-vetivonia; anekdoottisia raportteja vaikutuksista tarkkaavaisuuteen ja hyperaktiivisuuteen, mutta kontrolloituja tutkimuksia ASD:ssä puuttuu; tieteellinen näyttö mekanismeista riittämätöntä.
Frankincense (Boswellia)
Boswellia-lajien pihka; eteerinen öljy ja uutteet sisältävät boswelliahappoja; prekliinistä näyttöä neuroinflammaatiota ehkäisevistä, antioksidatiivisista (Nrf2/HO-1) ja neuroprotektiivisista vaikutuksista; ASD-tutkimuksia ei tunnistettu.
Setripuu
Eteerinen öljy sisältää sedrolia, α-cedreeniä ja tujopsenia; sitä on perinteisesti käytetty rauhoittavana ja ahdistusta lievittävänä aineena, mutta tieteellistä näyttöä GABAergisista mekanismeista tai kliinisestä tehokkuudesta ASD:n hoidossa puuttuu.
Sirkadinen rytmi
Endogeeninen ~24-tunnin rytmi, säätelee uni-valverytmiä, hormonieritystä, ruumiinlämpöä; ASD:ssä usein häiriintyneitä vuorokausirytmejä, unihäiriöitä; melatoniini säätelee vuorokausirytmiä ja parantaa unta ASD:ssä.