Tabla de contenido
La epilepsia no se puede tratar adecuadamente con medios farmacéuticos en aproximadamente un 30% de los casos, por lo que los aceites esenciales están ganando atención como medida de apoyo.
Lo que se debe tener en cuenta, si son útiles y en qué medida, se explica a continuación, de manera comprensible para legos.
Un resumen del informe científico para aquellos que desean aprender más sobre el apoyo natural para la epilepsia.
Un glosario, después de la bibliografía, explica los términos técnicos.
La tercera parte está dirigida a médicos, presenta el estado actual de la terapia farmacológica, así como los resultados de estudios sobre aceites esenciales de apoyo en la epilepsia, incluidas las referencias.
¿Qué es la epilepsia?
El cerebro está formado por miles de millones de neuronas que envían constantemente señales eléctricas. Normalmente, esto ocurre de forma ordenada, como una orquesta bien dirigida. En la epilepsia, se produce repentinamente una especie de “tormenta eléctrica” en el cerebro, la convulsión: muchas neuronas disparan simultáneamente y de forma incontrolada.
¿Qué sucede durante una convulsión?
Dependiendo de qué parte del cerebro se vea afectada, una convulsión puede manifestarse de manera muy diferente:
- Ausencia
Breve “desvanecimiento” por segundos, el afectado mira fijamente al vacío - Crisis mioclónica
Movimientos bruscos y espasmódicos (a menudo por la mañana) - Ataque focal Contracciones o sensaciones en una parte del cuerpo, a veces con pérdida de conciencia.
- Convulsión tónico-clónica generalizada (anteriormente “Gran Mal”): Caída, rigidez, espasmos rítmicos de todo el cuerpo, pérdida del conocimiento
¿Con qué frecuencia se presenta la epilepsia?
La epilepsia afecta aproximadamente a 50 millones de personas, das ist etwa 1 % der Weltbevölkerung. In Deutschland leben rund 400.000–500.000 Menschen mit Epilepsie. Es ist nach Migräne und Schlaganfall die dritthäufigste neurologische Erkrankung.
El gran problema
En aproximadamente 30 % de los pacientes Wenn Medikamente nicht ausreichend wirken, spricht man von pharmakoresistenter Epilepsie. Diese Menschen suchen oft nach ergänzenden Möglichkeiten.
En el cerebro, la epilepsia causa convulsiones debido a una actividad eléctrica anormal y repentina de las neuronas.
Dos sistemas deben estar en equilibrio:
- GABA (Ácido gamma-aminobutírico): El “freno”, calma el cerebro
- Glutamato: El “pedal del gas” que activa el cerebro
En la epilepsia, el equilibrio se altera: muy poca freno, demasiado acelerador, el cerebro “se vuelve loco”.
Además, los canales iónicos desempeñan un papel importante, que son “puertas” diminutas en las membranas de las células nerviosas:
- Canales de sodio (Nav)
Cuando una neurona se dispara, se abren demasiado fácilmente en la epilepsia. - Canales de calcio (Cav)
Importante para ciertos tipos de convulsiones (p. ej., ausencias) - Canales de potasio (Kv)
Ayudar a calmar la neurona después de que dispare
¿Cómo se trata normalmente la epilepsia?
Los antiepilépticos (AEDs) más importantes
Valproato (ácido valproico) es el antiepiléptico de amplio espectro más importante. Actúa de múltiples maneras simultáneamente y es especialmente eficaz en las epilepsias generalizadas, ya que frena los canales de sodio y calcio, y aumenta el GABA.
Advertencia importante:
El valproato es muy perjudicial para los niños no nacidos ¡y para las mujeres en edad fértil!
Carbamazepina y Lamotrigina son los “bloqueadores” de los canales de sodio. Impiden que las neuronas disparen con demasiada facilidad. Los dos productos farmacéuticos representan la terapia de primera línea para las epilepsias focales. Lamotrigina es especialmente bien tolerado y seguro durante el embarazo
Levetiracetam (Keppra) presenta un mecanismo único, ya que se une a una proteína (SV2A) que regula la transmisión de señales entre las neuronas. Se caracteriza por una muy buena tolerabilidad y no tiene interacciones con otros medicamentos. Los posibles efectos secundarios incluyen cambios de humor e irritabilidad.
Topiramato actúa de cuatro maneras diferentes al mismo tiempo, un “multitalento” que logra una alta tasa de ausencia de convulsiones del 44-83 % de los pacientes. Como efecto secundario, puede producirse lentitud en el pensamiento, así como dificultades para encontrar palabras.
Etosuximida se utiliza para las ausencias (convulsiones de ausencia breves). Bloquea canales de calcio específicos en el tálamo (un centro de relevo en el cerebro).
Fenobarbital y benzodiazepinas intensifican el efecto del GABA (el “freno”). Son económicos, efectivos, pero presentan potencial sedante y de dependencia (benzodiacepinas).
Aceites esenciales para la epilepsia: ¿qué es posible?
¡Se debe tener especial cuidado con la epilepsia!
Algunos aceites esenciales pueden desencadenar o empeorar las convulsiones (proconvulsivos). HABLE SIEMPRE con su neurólogo antes de usar aceites esenciales.
Aceites que DEBE EVITAR con epilepsia:
- Rosemary (en dosis altas – contenido de alcanfor)
- Eucalipto (en dosis altas)
- Menta (Salario de Pulegon)
- Hinojo (Fenchona en dosis altas)
- Salvia (Contenido de tuyona)
- Alcanfor (directo profestetico)
¿Qué aceites esenciales muestran propiedades anticonvulsivas?
Lavanda – calmante y antiepiléptico
Lavanda (Lavándula angustifoliaes el aceite más investigado para la epilepsia.
composición
– Linalool (25–45 %)
– Acetato de linalilo (25–50 %)
Efecto
– Activa los receptores GABA-A (el “freno” del cerebro)
– Inhibe los canales de sodio (previene la descarga incontrolada)
– Reduce la propensión a las convulsiones
Efectos clínicos
– El linalool prolongó significativamente el tiempo hasta la primera convulsión en el modelo PTZ (un modelo estándar para pruebas de convulsiones) en estudios con animales.
– Varios pacientes informan que la aromaterapia de lavanda retrasa las crisis o alivia las auras (señales de advertencia).
– Aplicar en un difusor de aromas por inhalación, pero nunca internamente sin consejo médico
Romero/Borneol – neuroprotector (¡con precaución!)
Borneol es un ingrediente activo del romero y otras plantas.
Efecto
– Protege las neuronas contra el daño causado por convulsiones recurrentes; GABAérgico y neuroprotector
– El borneol redujo la gravedad de las convulsiones en el modelo de «kindling» y disminuyó los marcadores inflamatorios (GFAP) en experimentos con animales
Atención: El aceite de romero en su totalidad puede ser proconvulsivo en dosis altas, solo tomar borneol aislado o dosis muy bajas.
Orégano – Carvacrol y Timol
Carvacrol (de orégano y tomillo) muestra interesantes propiedades anticonvulsivas.
Efecto
– Inhibe los canales de sodio (como la carbamazepina)
- Modula los receptores TRPV1 (receptores de calor y dolor)
– Duración y gravedad reducidas de las convulsiones en estudios con animales
Eucalipto – 1,8-Cineol (¡con precaución!)
1,8-Cineol El eucalipto muestra un efecto anticonvulsivo en un modelo animal.
Efecto
– ¿Afecta el sistema de NO (óxido nítrico) en el cerebro
– Aumenta el umbral convulsivo (~25 mg/kg frente a ~10 mg/kg en el grupo de control)
– Activa Nrf2 (factor de protección antioxidante)
- Atención: En dosis altas proconvulsivo, solo en pequeñas cantidades y tras consultar al médico
Manzanilla – Apigenina y Sinergias
Manzanilla (Manzanilla común) contiene apigenina, un flavonoide con propiedades ansiolíticas y anticonvulsivas.
Efecto
– La apigenina se une a los receptores GABA-A (en el mismo sitio que las benzodiacepinas, pero mucho más débilmente)
– Nuevo estudio (2025): La combinación de orégano + manzanilla + lavanda (administrada por vía intranasal) mostró un efecto anticonvulsivo sinérgico en un modelo animal, mejor que cada aceite por sí solo.
- Como complemento para ataques leves o para reducir la ansiedad
β-Cariofileno – el antiinflamatorio
β-Cariofileno (BCP) se encuentra en pimienta negra, lavanda, romero y cannabis.
Efecto
- Activa los receptores CB2 (receptores de cannabinoides) sin efecto psicoactivo
– Inhibe el NF-κB (el interruptor de la inflamación)
– Reduce la neuroinflamación, importante porque la inflamación puede empeorar la epilepsia
El BCP también se encuentra en el aceite de cáñamo y podría ser parte del efecto de los extractos ricos en CBD.
La planta más importante Cannabis y CBD
CBD (Cannabidiol) – el avance clínico
CBD es un ingrediente activo de la planta de cannabisCannabis sativa), pero sin el conocido efecto psicoactivo del THC. Es el único antiepiléptico de origen vegetal aprobado oficialmente por la FDA (EE. UU.) y la EMA (Europa) con el nombre de Epidiolex se permitió.
Se administra tópicamente como medicamento recetado (Epidiolex) en forma de solución oleosa 2 veces al día por vía oral.
Efecto
– Inhibe los canales de sodio (como la carbamazepina)
– Modula TRPV1 y GPR55 (receptores especiales)
– Antiinflamatorio a través de receptores CB2 – Protege las células nerviosas
Efectos secundarios
Somnolencia, diarrea, disminución del apetito
– Puede aumentar el nivel en sangre de otros antiepilépticos (especialmente clobazam), es necesario ajustar la dosis
Autorización para:
- Síndrome de Dravet – Una forma grave de epilepsia que comienza en la infancia
- Síndrome de Lennox-Gastaut (SLG) – Epilepsia severa con varios tipos de convulsiones
Estudios
– En el síndrome de Dravet: el CBD redujo la frecuencia de las convulsiones en un 38,9 % frente a un 13,3 % con placebo, 66,7 % de los pacientes tuvieron ≥ 50 % menos convulsiones (p = 0,009)
– En LGS: Reducción de las caídas en un 43,9 % % frente a un 21,8 % % con placebo (p < 0,001)
– En otras epilepsias farmacorresistentes: Varios estudios muestran una reducción de las crisis del 40-50 %%
Tabla comparativa – ¿Qué ayuda y cómo?
Regla de seguridad
Posiblemente útil (tras consultar con un médico):
- Aromaterapia con lavanda (difusor, inhalación) – relajante, posiblemente reductora de convulsiones
- CBD (como Epidiolex) – para Dravet/LGS, con receta médica
- β-Cariofileno – antiinflamatorio, bien tolerado
- Manzanilla – calmante, ansiolítico
En caso de epilepsia EVITAR:
- Aceite de romero (para, dosis altas) – El alcanfor puede desencadenar convulsiones
- Aceite de eucalipto (altas dosis)
- Aceite de menta (dosis altas, pulegona)
- Aceite de hinojo Fenchoña
- Aceite de salvia (Tuyona)
- Aceite de alcanfor (directo profestetico)
Instrucciones generales de seguridad
- Habla siempre primero con el neurólogo La epilepsia es seria
- Nunca suspendas la medicación antiepiléptica por tu cuenta. – puede provocar un estado epiléptico potencialmente mortal
- Tenga en cuenta las interacciones: Algunos aceites pueden alterar los niveles de antiepilépticos
- Deja de rascarte la piel – diluir siempre
- Hijos: Precaución especial, dosis mucho más bajas
Preguntas frecuentes
¿Puedo tomar lavanda en lugar de mis medicamentos antiepilépticos?
¡No, de ninguna manera! La lavanda solo ha demostrado efectos anticonvulsivos en estudios con animales. Dejar de tomar antiepilépticos por cuenta propia puede ser peligroso.
¿Qué pasa con el aceite de CBD de Internet?
Los productos de CBD de Internet no son lo mismo que el medicamento aprobado Epidiolex. No están estandarizados, pueden contener otros cannabinoides y no tienen una eficacia probada. Hable con su neurólogo sobre el CBD recetado.
¿Puede la aromaterapia detener una convulsión?
Existen informes de que algunos pacientes pueden retrasar las convulsiones con ciertos olores (como la lavanda), pero no es un método fiable ni un sustituto de la medicación.
¿Son seguros los aceites esenciales para niños con epilepsia?
Sólo tras consulta expresa con el neurólogo infantil. Los niños reaccionan de forma más sensible y algunos aceites son peligrosos para ellos.
¿Tengo que comprar aceites caros?
Qualität ist wichtig: Achten Sie auf 100 % naturreine ätherische Öle, am besten mit am besten mit chargenspezifischem Analyse-Zertifikat (GC/MS).
Los aceites de perfume baratos o las fragancias sintéticas no tienen efectos terapéuticos y, debido a los ingredientes sintéticos, pueden ser perjudiciales para la salud y causar dolores de cabeza, náuseas, etc.
contienen la información que se refiere a la selección y calidad de los aceites esenciales en el artículo „Aceites esenciales – Odisea de una búsqueda“encontrado.
Otro post cita al Prof. Dr. Dr. Dr. med. habil. Hanns Hatt de la Universidad Ruhr de Bochum, quien en su video „Curación con fragancias“explica de manera interesante, amena y a la vez científica el efecto de los aceites esenciales en el cuerpo humano.
Die drei Sätze zusammenfassen. Der Text wird in drei Sätzen zusammengefasst. Es ist notwendig, die wichtigsten Punkte zu extrahieren und sie in drei prägnanten Sätzen zu formulieren.
La epilepsia es una enfermedad neurológica grave donde las tormentas eléctricas en el cerebro causan convulsiones, y en un 30 % de los pacientes, los medicamentos estándar no son lo suficientemente efectivos.
Los aceites esenciales y terpenos, especialmente el linalool (lavanda), borneol y carvacrol, muestran propiedades anticonvulsivas en estudios con animales a través de la activación del GABA-A y la inhibición de los canales de sodio; el CBD (cannabidiol) es el único antiepiléptico vegetal con aprobación clínica (síndrome de Dravet, síndrome de Lennox-Gastaut).
Los aceites esenciales pueden usarse como complemento en la epilepsia, pero solo después de consultar explícitamente con el neurólogo tratante, ya que algunos aceites también pueden desencadenar convulsiones.
Este texto se basa en el informe científico “Epilepsia y aceites esenciales: farmacología, mecanismos de acción y enfoques terapéuticos complementarios” y tiene únicamente fines informativos generales. La epilepsia es una enfermedad grave. Si tiene preguntas sobre el tratamiento, consulte siempre a su neurólogo.
Recomendado dōTERRA-Productos para la terapia complementaria de la epilepsia
Productos potencialmente seguros (según la evidencia científica)
Aceites que deben EVITARSE con la epilepsia
Mezclas de aceite propias (DIY-Blends)
Mezcla 1 – “Neuroprotektiv” (Difusor)
Objetivo: Protección neuroprotectora, modulación del GABA
Aplicación: 30 minutos al día en el difusor, especialmente por la noche.
Mezcla 2 – “Gestión del Aura” (Temático, rápido)
Objetivo: En caso de síntomas de aura: intente interrumpir el ataque (SOLO como complemento, no como sustituto de la medicación de emergencia)
Aplicación: En las sienes, el cuello, las muñecas – inmediatamente al comienzo de la migraña.
La medicación de emergencia (por ejemplo, diazepam rectal) sigue siendo prioritaria
Mezcla 3 – “Angustia y Alivio del Estrés” (Difusor/Tópico)
Objetivo: Estrés ↓ (desencadenante frecuente de ataques), Relajación ↑
Aplicación: En caso de estrés o antes de situaciones desencadenantes conocidas
Mezcla 4 – “Sueño y Recuperación” (Noche)
Objetivo: Calidad del sueño ↑ (Falta de sueño = desencadenante de convulsiones)
Aplicación: En el difusor, 30 minutos antes de acostarse
Mezcla 5 – “Antiinflamatorio” (Tópico)
Objetivo: Neuroinflamación ↓ (Fisiopatología de la epilepsia)
Aplicación: Masajear las sienes, el cuello y la columna vertebral
Plan de aplicación – Plan de 4 semanas
Semana 1 – Comienzo cauto
- Consultar a un médico ANTES de comenzar con los aceites
- Por la tarde: Mezcla 4 en el difusor (dormir)
- Diariamente: Mezcla 1 en el difusor (30 minutos)
- Protocolo de ataque ejecutar (fecha, hora, disparador)
Semana 2 - Ampliación
- Mañanas: Mezcla 3 en situaciones de estrés
- Por la tarde: Mezcla 4 (Dormir) + Mezcla 5 tópico
- Mezcla 2: Prepárate para situaciones de aura
Semana 3-4 – Optimización
- Evaluar el protocolo de la crisis ¿ha cambiado algo?
- Neurólogos informan sobre la aplicación de aceite
- Adaptación basado en la tolerancia individual
Combinación con otros dōTERRAEl producto
Plan de emergencia en caso de convulsión
- Seguridad Persona en posición lateral de seguridad.
- Medir el tiempo Ataque que dura más de 5 minutos → Urgencias (112)
- Medicación de emergencia: Diazepam rectal / Midazolam nasal (según lo prescrito por el médico)
- SIN petróleo En la boca o nariz durante un ataque activo
- Aceites esenciales no son medicación de emergencia
Epilepsia y Aceites Esenciales – Farmacología, Mecanismos de Acción y Enfoques Terapéuticos Complementarios
Un informe científico exhaustivo sobre antiepilépticos estándar, terpenos y aceites esenciales: bases moleculares, evidencia clínica y estrategias terapéuticas adyuvantes
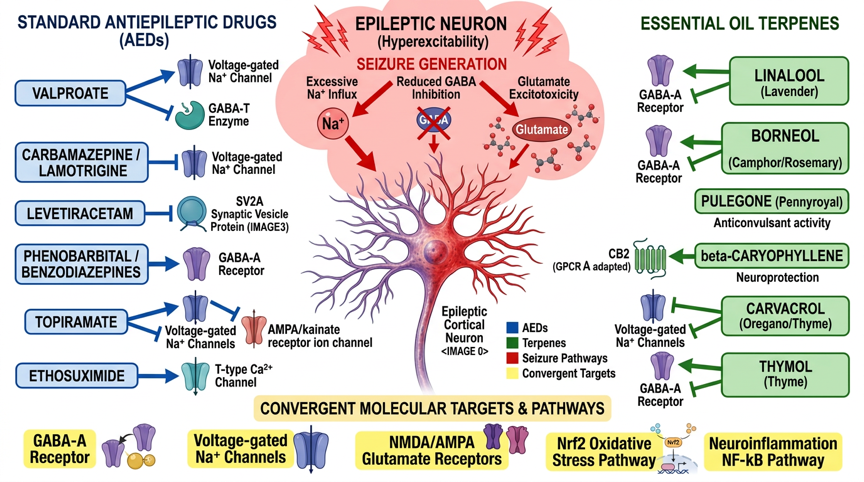
Abb. 1: Vías de señalización molecular de los antiepilépticos estándar y aceites esenciales en la epilepsia – AEDs estándar (Valproato/Nav+GABA-T, Carbamazepina/Nav, Levetiracetam/SV2A, Topiramato/multimodal, Etosuximida/T-tipo-Ca2+, Fenobarbital/GABA-A) y terpenos (Linalol/GABA-A+Nav, Borneol/GABA-A+Nav, Carvacrol/Nav+TRPV1, β-Cariofileno/CB2, 1,8-Cineol/NO+Nrf2) con moléculas diana convergentes (receptor GABA-A, canales Nav, glutamato NMDA/AMPA, Neuroinflamación NF-κB, Estrés oxidativo Nrf2)
Oben: Onda rápida (70-200 ms) con onda lenta subsiguiente.
Nota: Complejo espiga-onda de 3 Hz (CEG) – Patrón característico de la epilepsia de ausencias.
Abajo: Complejo Polispica (3-5 espigas, 4-5 Hz) – característico de la Epilepsia Mioclónica Juvenil (EMJ).
Introducción
La epilepsia es una de las enfermedades neurológicas crónicas más comunes en el mundo y afecta a aproximadamente 50 millones de personas, lo que representa alrededor de 1 % de la población mundial. [D1]. Se define por una predisposición duradera a las convulsiones epilépticas a consecuencia de descargas neuronales patológicamente sincronizadas, así como por las consecuencias neurobiológicas, cognitivas, psicológicas y sociales de esta afección. [D2]. A pesar de los avances significativos en el desarrollo de fármacos antiepilépticos (FAE), aproximadamente el 30 % % de los pacientes presenta epilepsia farmacorresistente, en la que dos o más FAE administrados adecuadamente no logran un control suficiente de las convulsiones. [D3].
El tratamiento estándar de la epilepsia incluye una farmacoterapia escalonada con antiepilépticos de primera, segunda y tercera generación. El valproato, la carbamazepina y la lamotrigina se consideran medicamentos de primera línea para las epilepsias focales y generalizadas; sustancias más nuevas como la levetiracetam, el topiramato, la lacosamida y el perampanel amplían el arsenal terapéutico. [D4]. A pesar de su eficacia, los AED se asocian con efectos secundarios significativos, deterioro cognitivo, teratogenicidad (valproato), depresión de la médula ósea (carbamazepina), aumento de peso y trastornos psiquiátricos que afectan considerablemente la calidad de vida de los pacientes. [D5].
Ante este panorama, el interés científico en los ingredientes activos de las plantas y los aceites esenciales como opciones terapéuticas coadyuvantes o alternativas está creciendo. Numerosos terpenos y compuestos bioactivos muestran propiedades anticonvulsivas, neuroprotectoras, anti-neuroinflamatorias y antioxidantes en estudios preclínicos y clínicos, a menudo a través de mecanismos que son complementarios a los de los AED clásicos. [D6]. El cannabidiol (CBD), como ingrediente activo de origen vegetal de Cannabis sativa, ya ha recibido aprobaciones clínicas para síndromes epilépticos específicos y demuestra el potencial de los compuestos botánicos en la terapia de la epilepsia. [D7]. Este informe analiza sistemáticamente la farmacología de los antiepilépticos estándar, los mecanismos moleculares de acción de aceites esenciales y terpenos relevantes, así como la evidencia clínica disponible para su uso adyuvante en la epilepsia.
EEG en la epilepsia: principios básicos e interpretación
El electroencefalograma (EEG) es la herramienta diagnóstica central en la epilepsia y permite la medición directa de la actividad eléctrica cortical a través de electrodos en el cuero cabelludo. Se utiliza para la clasificación de las crisis, la localización de focos y el seguimiento terapéutico.
Fase interictal: El EEG entre las crisis típicamente muestra descargas epileptiformes interictales (DEI): espigas (<70 ms), ondas agudas (70-200 ms) y complejos de espiga y onda de 3 Hz (GSWD en epilepsia de ausencia). Estas DEI surgen de descargas neuronales síncronas en el foco epiléptico.
Fase iictal: El EEG del ataque a menudo comienza con actividad rápida de bajo voltaje (LVFA, 20-35 Hz) como patrón de inicio. Con el tiempo, se desarrolla una evolución rítmica de theta-delta con aumento de amplitud. La terminación es abrupta con supresión postictal posterior.
Fase postictal: Después del fin de la crisis, el EEG muestra una supresión (reducción marcada de la amplitud) seguida de una ralentización difusa delta (0,5-3,5 Hz). La recuperación a la actividad de fondo normal ocurre en minutos a horas, dependiendo de la duración y el tipo de crisis.
Influencia del β-cariofileno en el EEG de la epilepsia: el β-cariofileno (BCP), un agonista CB2 sesquiterpénico de aceites esenciales (p. ej., pimienta negra, clavo), reduce la frecuencia de las convulsiones en un 66 %%en el modelo PTZ, aumenta la latencia de las convulsiones en un 187 %%y disminuye la frecuencia de las espigas en un 27-68 %% . En el EEG, se observa una normalización de la potencia espectral: la potencia gamma (marcador de hiperexcitabilidad) disminuye, la potencia delta aumenta. El mecanismo de acción incluye el agonismo CB2 (disminuye la neuroinflamación) y la modulación GABA-A (aumenta la entrada de cloruro).
Fisiopatología de la epilepsia
Hiperexcitabilidad y sincronización neuronal
La fisiopatología fundamental de la epilepsia se basa en un desequilibrio entre la neurotransmisión excitatoria e inhibitoria, que conduce a descargas neuronales sincronizadas paroxísticas. A nivel celular, un ataque epiléptico surge de la interacción de disfunciones de los canales iónicos, alteración de la transmisión sináptica y cambios en la actividad de la red neuronal. [D8]. Las mutaciones o cambios funcionales en los canales de sodio (Nav), potasio (Kv) y calcio (Cav) dependientes de voltaje, así como en los canales iónicos controlados por ligandos (GABA-A, NMDA), contribuyen al aumento de la excitabilidad neuronal. [D9].
Oben (azul): Fase interictal con SEI (puntas <70 ms, ondas agudas 70-200 ms, DSGS de 3 Hz).
Rojo: Fase de Icto – Inicio de LVFA (20-35 Hz), Evolución Theta-Delta, Terminación abrupta.
Abajo (violeta): Fase post-ictual — Supresión de EEG, enlentecimiento difuso de ondas delta (0,5-3,5 Hz)
Desequilibrio GABA/Glutamato
El equilibrio entre el neurotransmisor inhibidor GABA (ácido gamma-aminobutírico) y el neurotransmisor excitador glutamato es crucial para el umbral convulsivo. La inhibición GABAérgica disminuida, debido a la reducción de la síntesis de GABA, la disminución de la densidad del receptor GABA-A o el aumento de la actividad de la GABA-transaminasa, reduce el umbral convulsivo. [D10]. Al mismo tiempo, la activación excesiva de los receptores de glutamato NMDA y AMPA promueve la propagación de la despolarización y las descargas epilépticas. Este desequilibrio GABA/glutamato es el objetivo farmacológico central de la mayoría de los AED. [D11].
Disfunciones de canales iónicos
Los canales de sodio dependientes de voltaje (Nav1.1, Nav1.2, Nav1.6) desempeñan un papel clave en la generación y propagación del potencial de acción. Las mutaciones de ganancia de función en Nav1.1 (síndrome de Dravet) o Nav1.2 dan lugar a descargas incontroladas. D12. Los canales de calcio tipo T (Cav3.1, Cav3.2) son centrales en las epilepsias de ausencia: su activación rítmica en el tálamo genera las descargas características de espiga y onda de 3 Hz. [D13]. Los defectos en los canales de potasio (KCNQ2/3, KCNT1) afectan la repolarización y aumentan la predisposición a las convulsiones.
Neuroinflamación y estrés oxidativo
La epilepsia crónica se asocia con neuroinflamación persistente: la microglía y los astrocitos activados liberan citoquinas proinflamatorias (IL-1β, IL-6, TNF-α) que desestabilizan la barrera hematoencefálica y aumentan la excitabilidad neuronal. [D14]. El factor de transcripción NF-κB coordina esta cascada neuroinflamatoria. Al mismo tiempo, las convulsiones repetitivas conducen al estrés oxidativo por disfunción mitocondrial y producción de ROS, lo que favorece la apoptosis neuronal y la esclerosis del hipocampo. [D15]. La vía de señalización Nrf2 como regulador principal de la respuesta antioxidante a menudo se suprime en la epilepsia farmacorresistente.
Mecanismos de Farmacorresistencia
En el 30% de los pacientes epilépticos, dos o más AED fallan. La farmacorresistencia se desarrolla debido a: (1) la sobreexpresión de P-glicoproteína (P-gp/MDR1) y otros transportadores ABC que efluyen los AED del cerebro; (2) cambios en las dianas de los AED (p. ej., mutaciones en el canal Nav que reducen la unión a fenitoína); (3) variantes farmacogenéticas en el metabolismo del CYP; (4) neuroinflamación que altera la permeabilidad de la barrera hematoencefálica % [D16].
Farmacología de los antiepilépticos estándar
Bloqueadores de canales de sodio: carbamazepina, lamotrigina, fenitoína, lacosamida
Los bloqueadores de canales de sodio son la clase más común y antigua de AED. Se unen al estado inactivado de los canales de sodio dependientes de voltaje (Nav1.1-Nav1.6) y prolongan su duración de inactivación, el principio de “bloqueo dependiente del uso” [D8]. La carbamazepina (CBZ) y la oxcarbazepina son la terapia de primera línea para las epilepsias focales; la lamotrigina también inhibe la liberación presináptica de glutamato y es particularmente eficaz en el síndrome de Lennox-Gastaut y la epilepsia de ausencia. [D17]. La fenitoína/fosphenitoína estabiliza el estado inactivado del canal Nav y es un medicamento estándar en el estatus epiléptico. La lacosamida (de nueva generación) potencia la “inactivación lenta” de los canales Nav a través de un mecanismo único y muestra una farmacocinética favorable. [D18].
Eficacia clínica: La carbamazepina logra la ausencia de convulsiones en epilepsias focales en el 40–50 % % de los pacientes como monoterapia; la lamotrigina muestra una eficacia comparable con un mejor perfil de tolerabilidad, especialmente en mujeres en edad fértil. [D4].
Valproato – Antiepiléptico de amplio espectro
El ácido valproico (valproato/VPA) es el antiepiléptico de amplio espectro más importante con múltiples mecanismos de acción: inhibición de los canales de sodio dependientes de voltaje, reducción de los flujos de calcio tipo T, inhibición de la GABA-transaminasa (GABA-T) con la consecuente elevación del GABA, y activación de la glutamato-descarboxilasa (GAD). [D19]. El valproato es la terapia de primera línea en epilepsias generalizadas (epilepsia mioclónica juvenil, epilepsia de ausencia, Lennox-Gastaut) y logra la ausencia de convulsiones en el 50-70 % de los pacientes con epilepsia generalizada idiopática. [D4]. Crítico: El valproato es teratogénico potente (defectos del tubo neural, deterioro cognitivo en el recién nacido) y solo debe usarse en mujeres en edad fértil después de una cuidadosa evaluación de los beneficios y riesgos. [D5].
Levetiracetam – Unión a SV2A
El levetiracetam (LEV) tiene un mecanismo de acción único: se une selectivamente a la proteína 2A de las vesículas sinápticas (SV2A), la cual regula la exocitosis de neurotransmisores. [D20]. Mediante la unión a SV2A, LEV reduce la liberación de neurotransmisores presinápticos en descargas de alta frecuencia, un mecanismo “dependiente de la frecuencia” que apenas afecta la transmisión sináptica normal. LEV es la terapia de primera línea para epilepsias focales y generalizadas, muestra una excelente farmacocinética (sin inducción enzimática, sin unión a proteínas) y es relativamente segura durante el embarazo. [D20]. Wichtige Nebenwirkung: Verhaltensänderungen (Irritabilität, Depression) bei bis zu 15 % der Patienten.
Topiramat – Mecanismo Multimodal
Topiramato (TPM) es un AED multimodal con al menos cuatro mecanismos de acción:
- Bloqueo de canales de sodio dependientes de voltaje,
- Potenciación de la inhibición gabaérgica en los receptores GABA-A
- Antagonismo de receptores de glutamato AMPA/ Kainato
- Inhibición de la anhidrasa carbónica (CA-II, CA-IV) [D21]
Estudios clínicos muestran tasas de libertad de convulsiones de 44–83 % (6–7 meses) y 41–76 % (12–13 meses) en estudios comparativos de monoterapia; el topiramato es tan eficaz como el valproato y la carbamazepina [D21]. Efectos secundarios importantes: deterioro cognitivo (“dificultad para encontrar palabras”), pérdida de peso, cálculos renales.
Moduladores GABA-A – Fenobarbital, Benzodiacepinas, Vigabatrina
El fenobarbital (barbitúrico) y las benzodiazepinas (diazepam, clonazepam, clobazam) potencian la inhibición mediada por cloruro del receptor GABA-A: los barbitúricos prolongan la duración de apertura del canal de cloruro, las benzodiazepinas aumentan la frecuencia de apertura [D22]. El fenobarbital es uno de los FAE (fármacos antiepilépticos) más antiguos y económicos, se usa con frecuencia en países en desarrollo, pero tiene un potencial de sedación considerable. La vigabatrina inhibe irreversiblemente la GABA-transaminasa (GABA-T) y aumenta así la concentración de GABA en el cerebro; es eficaz en los espasmos infantiles, pero se asocia con defectos irreversibles del campo visual. [D23].
Ethosuximida – Bloqueador de canales de calcio tipo T
El ethosuximid (ESM) es un bloqueador selectivo de los canales de calcio tipo T (Cav3.1/3.2) y es la terapia de primera línea para la epilepsia de ausencia infantil. [D13]. Los canales T generan las descargas rítmicas del tálamo que caracterizan las ausencias epilépticas; su bloqueo interrumpe eficazmente este ciclo. La ethosuximida es tan eficaz como el valproato en la epilepsia de ausencia (remisión de crisis ~50-60 %), pero tiene menos efectos secundarios. [D13].
Nuevos antiepilépticos - Lacosamida, Perampanel, Brivaracetam
La lacosamida (LCM) potencia selectivamente la “inactivación lenta” de los canales de sodio dependientes de voltaje e inhibe la proteína mediadora de la respuesta colapsante 2 (CRMP-2). [D18]. El perampanel (PER) es el primer antagonista selectivo no competitivo del receptor de glutamato AMPA y es particularmente efectivo en las convulsiones tónico-clónicas generalizadas farmacorresistentes. [D24]. El Brivaracetam (BRV) se une a la SV2A, al igual que el levetiracetam, pero con una afinidad 10 veces mayor y un inicio de acción más rápido. [D25].
Aceites esenciales como terapia adyuvante: bases mecanicistas
Farmacocinética y penetración en el SNC
Los terpenos de los aceites esenciales se caracterizan por su alta lipofilia y baja masa molecular (< 300 Da), lo que permite una penetración eficiente de la barrera hematoencefálica (BHE). [D26]. Al inhalar, los terpenos volátiles se transportan a través de la mucosa olfativa directamente al bulbo olfatorio y al sistema límbico, una vía directa que evita la BHS y conduce a concentraciones medibles en el SNC en cuestión de minutos. [D27]. La aplicación transdérmica y oral permite la absorción sistémica; la biodisponibilidad oral varía considerablemente según el terpeno y la formulación.
Mecanismos antiepilépticos básicos
Los aceites esenciales y sus terpenos pueden actuar a través de múltiples mecanismos anticonvulsivos que se superponen con los de los AED clásicos:
- Modulación de canales de sodio dependientes de voltaje (Linalol, borneol, carvacrol, timol)
- Potenciación de la inhibición gabaérgica en receptores GABA-A (Linalool, Borneol, Timol, Apigenina)
- Inhibición de la excitación glutamatérgica en los receptores NMDA/AMPA
- Neuroprotección antioxidante a través de la activación de Nrf2; (5) Efecto antineuroinflamatorio a través de la inhibición de NF-κB (β-cariofileno) [D28].
Propiedades neuroprotectoras
Muchos terpenos muestran propiedades neuroprotectoras que van más allá del efecto anticonvulsivo directo. Al inhibir las vías de señalización de la apoptosis (caspasa-3, relación Bax/Bcl-2), reducir la peroxidación lipídica (niveles de MDA) y aumentar las actividades de las enzimas antioxidantes (SOD, CAT, GPx), los terpenos protegen contra el daño neuronal inducido por las convulsiones. [D29]. Estas propiedades neuroprotectoras son especialmente relevantes en la epilepsia farmacorresistente, donde las convulsiones repetitivas conducen a un daño cerebral progresivo.
Mecanismos de acción complementarios a los antiepilépticos estándar
La siguiente tabla muestra los mecanismos de acción complementarios de los aceites esenciales en comparación con los antiepilépticos estándar a nivel molecular:

AEDs estándar (Valproato/Nav+GABA-T, Carbamazepina/Nav, Levetiracetam/SV2A, Topiramato/multimodal, Etosuximida/T-tipo-Ca²⁺, Fenobarbital/GABA-A) y terpenos (Linalool/GABA-A+Nav,borneol/GABA-A+Nav, Carvacrol/Nav+TRPV1, β-Cariofileno/CB2, 1,8-cineol/NO+Nrf2) con dianas moleculares convergentes (GABA-A, Nav, NMDA/AMPA, NF-κB, Nrf2/ARE).
Aceites esenciales específicos y evidencia clínica
Aceite de lavanda (Lavandula angustifolia) – Linalol
El aceite de lavanda es el aceite esencial más investigado en el contexto de las enfermedades neuronales. Su principal ingrediente activo, el linalol (25-45 %), ha demostrado propiedades anticonvulsivas en estudios preclínicos: en un modelo de pentilenotetrazol (PTZ), la inhalación de linalol aumentó el umbral de convulsiones, prolongó la latencia hasta la primera convulsión y acortó la duración de las convulsiones. [D30]. Mecanísticamente, el linalool inhibe los canales de sodio dependientes de voltaje al aumentar el umbral del potencial de acción y reducir la velocidad de despolarización, así como al modular los flujos de potasio activados por calcio. [D31]. Un estudio piloto sobre entrenamiento olfativo en pacientes con epilepsia (n=11) utilizó lavanda como estímulo de condicionamiento olfativo y mostró una reducción de las convulsiones de ≥ 50 en 6 de 11 pacientes %, aunque los autores señalan la limitada evidencia. [D32].
En un estudio con varios aceites esenciales en un modelo de ratón PTZ, Lavandula angustifolia mostró una prolongación significativa de la latencia de la convulsión (p < 0,05) y una reducción de la gravedad de la convulsión en comparación con el grupo control. [D33]. Silexan (80 mg por vía oral, extracto de lavanda estandarizado) está clínicamente validado para trastornos de ansiedad y podría usarse como coadyuvante en la ansiedad asociada a la epilepsia. [D34].
Aceite de cannabis / Cannabidiol (CBD)
El cannabidiol (CBD) es el ingrediente activo vegetal más conocido con un efecto antiepiléptico clínicamente probado. Como fitocannabinoide no psicoactivo de Cannabis sativa, el CBD tiene múltiples mecanismos anticonvulsivos: antagonismo en GPR55 (receptor de lisofosfatidilinositol), modulación de los canales TRPV1, inhibición de los canales de sodio dependientes de voltaje y modulación del sistema endocannabinoide. [D35]. El CBD farmacéutico (Epidiolex®) está aprobado por la FDA (2018) y la EMA (2019) para el síndrome de Dravet y el síndrome de Lennox-Gastaut. [D7].
Evidencia clínica: En estudios de fase III controlados con placebo en el síndrome de Dravet (n=120), el CBD (20 mg/kg/día) redujo la frecuencia mensual de convulsiones en un 38,9 % frente a un 13,3 % con placebo (p = 0,01). [D7]. En el síndrome de Lennox-Gastaut (n=225), el CBD redujo las crisis de caída en un 43,9 % % frente al 21,8 % % con placebo (p < 0,001) [D36]. En un estudio triple ciego en epilepsia refractaria del lóbulo frontal (n=27), el 66,7 % de los pacientes con CBD mostraron mejoría después de 4 semanas frente al 20,0 % con placebo (diferencia media 45,58; IC del 95 %: 8,99–82,18; p = 0,009) [D37].
Aceite de romero (Rosmarinus officinalis) – borneol, 1,8-cineol
El aceite de romero contiene borneol (hasta 20 %), 1,8-cineol/eucaliptol (35–50 %), alcanfor (10–20 %) y α-pineno [D38]. El borneol muestra efectos antiepilépticos en un modelo PTZ-kindling: reduce la progresión de las convulsiones, disminuye los marcadores GFAP (neuroinflamación) en el hipocampo, reduce el estrés oxidativo y modula la transmisión gabaérgica. [D39]. El 1,8-cineol aumentó el umbral convulsivo en un ensayo de PTZ (~25 mg/kg frente a ~10 mg/kg en el control) y redujo los niveles de malondialdehído (MDA) como marcador de estrés oxidativo. [D40]. En el estudio de aceite múltiple PTZ, Rosmarinus officinalis mostró una extensión significativa de la latencia de las convulsiones y una reducción de la gravedad de las convulsiones. [D33].
Orégano/Aceite de tomillo – Carvacrol y timol
Carvacrol (orégano, tomillo, ajedrea) y timol (tomillo) son fenoles monoterpénicos estructuralmente relacionados con actividad anticonvulsiva demostrada [D41]. El carvacrol inhibe los canales de sodio dependientes de voltaje (Nav1.2, Nav1.4) y los canales TRPV1, potencia la inhibición gabaérgica y muestra efectos anticonvulsivos en modelos de PTZ y ácido kénico. [D42]. El timol modula los receptores GABA-A de forma alostérica positiva (similar a los barbitúricos) e inhibe los canales de sodio dependientes de voltaje. [D43]. Restricción importante: El aceite de Origanum vulgare mostró efectos tóxicos en un estudio en animales a la concentración probada (% 100 de mortalidad), lo que subraya la importancia de una dosificación y formulación estandarizadas. [D33].
Aceite de eucalipto (Eucalyptus globulus) – 1,8-cineol
El aceite de eucalipto contiene 60–90 % de 1,8-cineol (eucaliptol), un óxido de monoterpeno con propiedades anticonvulsivas, antiinflamatorias y antioxidantes. [D44]. El 1,8-cineol modula el sistema del óxido nítrico (NO), que desempeña un papel complejo y bidireccional en la regulación de las convulsiones: los niveles bajos de NO pueden ser anticonvulsivantes, mientras que los niveles altos de NO pueden ser proconvulsivantes. En un modelo de PTZ, el 1,8-cineol aumentó significativamente el umbral convulsivo y redujo la peroxidación lipídica. [D40]. La inhalación de aceite de eucalipto también muestra efectos antineuroinflamatorios mediante la inhibición de NF-κB y la reducción de citoquinas proinflamatorias. [D45].
Aceite de incienso (Boswellia sacra) – α-Pineno, ácidos boswélicos
El aceite de incienso contiene α-pineno (hasta un 75 %), limoneno y ácidos boswélicos no volátiles. [D46]. La α-pineno inhibe la acetilcolinesterasa y tiene propiedades ansiolíticas; los ácidos boswélicos (AKBA) inhiben la 5-lipoxigenasa y el NF-κB, lo que reduce los procesos neuroinflamatorios en la epilepsia. En modelos animales, el extracto de Boswellia mostró efectos neuroprotectores después de convulsiones inducidas por kainato: reducción de la pérdida de neuronas del hipocampo, disminución de la expresión de GFAP y reducción de los niveles de IL-1β. [D47]. El acetato de incensol del incienso activa los canales TRPV3 y muestra efectos ansiolíticos independientes de los receptores GABA-A u opioides.
Aceite de manzanilla (Matricaria chamomilla) – Apigenina, α-Bisabolol
El aceite de manzanilla contiene α-bisabolol (hasta un 50 %), camazuleno y la flavonoide apigenina [D48]. La apigenina se une al sitio de unión de las benzodiazepinas del receptor GABA-A (Ki = 4 µM) y exhibe propiedades ansiolíticas y anticonvulsivas sin sedación en modelos preclínicos. [D49]. En un estudio de sinergismo (2025), la combinación de orégano, manzanilla y lavanda (intranasal) mostró actividad anticonvulsiva sinérgica en el modelo de PTZ, con una reducción significativa de la frecuencia de convulsiones (p < 0,05) y efectos optimizados a dosis bajas combinadas en comparación con las sustancias individuales. [D50].
Aceite de hinojo (Foeniculum vulgare) – trans-Anethol
El aceite de hinojo contiene trans-anetol (50–80 %), fenchona y estragol. El trans-anetol modula los receptores GABA-A e inhibe los receptores NMDA-glutamato, lo que explica los efectos anticonvulsivos en modelos animales. [D28]. Sin embargo, el fenchona (un componente del aceite de hinojo) tiene propiedades proconvulsivas y puede desencadenar convulsiones, lo que subraya la importancia de preparados de aceite de hinojo estandarizados y con bajo contenido de fenchona para aplicaciones terapéuticas.
Mecanismos moleculares de acción de los terpenos en la epilepsia
Linalol – Inhibición de canales de sodio y modulación del receptor GABA-A
El linalol (3,7-Dimetil-1,6-octadien-3-ol), el monoterpeno principal en lavanda y cilantro, ejerce efectos dependientes de la dosis sobre la excitabilidad neuronal. En neuronas aisladas, el linalol aumenta el umbral del potencial de acción y reduce la velocidad de despolarización, ambos indicadores de la inhibición de los canales de sodio. [D31]. Al mismo tiempo, el linalool activa los canales de potasio dependientes de calcio (canales BK), que aceleran la repolarización y reducen la frecuencia de disparo. La modulación de GABA-A por el linalool aumenta la inhibición mediada por cloruro. [D30]. Importante: En dosis altas, el linalol puede tener un efecto paradójicamente estimulante, lo que subraya la importancia de optimizar la dosis.
Borneol – Modulación GABAérgica y Neuroprotección
El borneol (2-bornanol), un alcohol monoterpénico bicíclico del árbol del alcanfor y el romero, demuestra efectos antiepilépticos en el modelo de "kindling" con PTZ. Modula la transmisión gabaérgica, reduce el estrés oxidativo (disminución de los niveles de MDA, aumento de la actividad de SOD) y disminuye los marcadores neuroinflamatorios (GFAP) en el hipocampo. [D39]. Además, el borneol inhibe los canales de sodio dependientes de voltaje y muestra efectos anticonvulsivos sinérgicos en combinación con AED estándar en modelos animales.
Carvacrol y timol - Bloqueo del canal Nav y modulación del receptor GABA-A
Carvacrol (5-isopropil-2-metilfenol) y timol (2-isopropil-5-metilfenol) son fenoles monoterpénicos isómeros estructurales con mecanismos de acción similares pero no idénticos. El carvacrol inhibe los canales de sodio Nav1.2 y Nav1.4, así como los canales TRPV1, y demuestra efectos neuroprotectores en modelos de ácido kaínico. [D42]. El timol modula positivamente alostéricamente los receptores GABA-A en un sitio de unión similar al de los barbitúricos e inhibe los canales de sodio dependientes de voltaje, un mecanismo dual similar al del fenobarbital. [D43].
β-Cariofileno – Agonismo CB2 y Anti-Neuroinflamación
El β-cariofileno (BCP), el sesquiterpeno bicíclico de la pimienta negra y el clavo, actúa como un agonista selectivo del receptor de cannabinoides CB2 y muestra efectos anticonvulsivos y neuroprotectores en modelos animales. [D51]. Los efectos anticonvulsivos de BCP se median en parte a través de mecanismos gabaérgicos, sistemas serotoninérgicos y nitrérgicos. La inhibición de NF-κB por BCP reduce los procesos neuroinflamatorios que contribuyen a la epileptogénesis. En un modelo de ratón, BCP redujo significativamente la frecuencia de convulsiones inducidas por PTZ y mostró efectos neuroprotectores en el hipocampo. [D52].
en el modelo PTZ y mecanismo de acción
Control — 3 convulsiones en 20 s, alta frecuencia de espigas
B: BCP 200 mg/kg — 1 Convulsión (↓66 %), Latencia ↑187 %, Puntas ↓68 %.
C: Frecuencia de espigas dependiente de la dosis (↓27–68 %).
D: Potencia espectral — Potencia gamma ↓, Potencia delta ↑ (Normalización).
E: Mecanismo de acción — BCP → CB2 (↓Neuroinflamación) + GABA-A (↑Afluencia de cloruro → ↓Hipexcitabilidad).
1,8-Cineol – Sistema NO y neuroprotección antioxidante
1,8-Cineol (Eucaliptol), el monoterpeno principal del aceite de eucalipto y romero, modula el sistema de óxido nítrico (NO) y muestra neuroprotección antioxidante. [D40]. En un ensayo de umbral PTZ, el 1,8-cineol aumentó significativamente el umbral de convulsión (~25 mg/kg frente a ~10 mg/kg en el grupo de control) y redujo los niveles de malondialdehído (MDA), un marcador de peroxidación lipídica. Además, el 1,8-cineol inhibe los procesos neuroinflamatorios dependientes de NF-κB y activa la vía de señalización Nrf2 para la neuroprotección antioxidante.
Nuevos y complementarios aceites esenciales
Aceite de melisa (Melissa officinalis) Ácido rosmarínico
El aceite de melisa contiene ácido rosmaringo, citral, citronelal y geraniol [D53]. El ácido rosmárico inhibe la GABA transaminasa (GABA-T), el mismo mecanismo que el vigabatrín, aumentando así la inhibición GABAérgica. Además, el ácido rosmárico demuestra propiedades antioxidantes y antiinflamatorias neuronales al inhibir la COX-2 y la NF-κB. En modelos animales, el extracto de melisa mostró efectos anticonvulsivos en convulsiones inducidas por PTZ.
Aceite de menta (Mentha piperita) – Mentol, Pulegona
El aceite de menta contiene mentol (30–55 %), mentona (14–32 %) y pulegona (< 1 %). En el estudio de aceite múltiple PTZ, *Mentha piperita* no mostró convulsiones y tuvo una supervivencia del 100 % %a la concentración probada, lo que representa el mejor perfil de seguridad de todos los aceites probados. [D33]. El mentol activa los canales de frío TRPM8 y modula los canales de sodio; muestra propiedades analgésicas y levemente anticonvulsivas. Importante: el pulegón en altas concentraciones es hepatotóxico y proconvulsivo.
Aceite de comino negro (Nigella sativa) – Timoquinona
El aceite de comino negro contiene timoquinona (TQ, 30–48 %), que presenta potentes propiedades anticonvulsivas, neuroprotectoras y antiinflamatorias para el sistema nervioso. [D54]. TQ inhibe los receptores NMDA de glutamato, activa los receptores GABA-A y demuestra eficacia comparable a la del valproato en modelos animales de convulsiones inducidas por PTZ. TQ activa Nrf2 e inhibe NF-κB, lo que reduce el estrés oxidativo y la neuroinflamación en la epilepsia.
Extracto de cáñamo: CBD y otros cannabinoides
Además del CBD farmacéutico, el Cannabis sativa contiene otros cannabinoides con efecto anticonvulsivo: el CBDV (Cannabidivarina) ha demostrado eficacia en ensayos clínicos para convulsiones focales; el THCV (Tetrahidrocannabivarina) tiene propiedades anticonvulsivas en modelos animales; el CBG (Cannabigerol) muestra efectos neuroprotectores. [D55]. El fenómeno séquito describe los efectos sinérgicos entre diferentes cannabinoides y terpenos en el extracto de cannabis de espectro completo.
Evidencia clínica en comparación con la terapia estándar
Ensayos controlados aleatorizados (ECA)
La evidencia clínica de los aceites esenciales para la epilepsia es, con la excepción del CBD farmacéutico, predominantemente preclínica. El CBD ha demostrado una eficacia convincente en varios ECAs de fase III para el síndrome de Dravet y el síndrome de Lennox-Gastaut: reducción de las convulsiones tónico-clónicas en un 38,9 % (Dravet, p = 0,01) y de las convulsiones atónicas en un 43,9 % (LGS, p < 0,001) [D7] [D36]. En un estudio triple ciego en epilepsia refractaria del lóbulo frontal (n=27), el CBD mostró una superioridad significativa sobre el placebo (66,7 % frente a 20,0 % respondedores, p = 0,009) [D37].
Modelos animales preclínicos
En un modelo de ratón PTZ con varios aceites esenciales (Lavandula angustifolia, Rosmarinus officinalis, Mentha piperita, Origanum majorana), todos los aceites probados (excepto Origanum vulgare) mostraron prolongaciones significativas de la latencia de las convulsiones y reducciones en la gravedad de las convulsiones en comparación con el grupo de control (p < 0,05). [D33]. Un estudio de sinergismo (2025) con la aplicación intranasal combinada de aceites de orégano, manzanilla y lavanda demostró efectos anticonvulsivos sinérgicos que fueron superiores a la suma de los efectos individuales. [D50].
Entrenamiento olfativo en la epilepsia
Un estudio piloto sobre entrenamiento olfativo (aromaterapia de alerta de convulsiones) en pacientes con epilepsia (n=11) utilizó estímulos olfativos condicionados (lavanda, jazmín) para la predicción y el control de convulsiones. [D32]. El 6 de 11 pacientes mostraron una reducción de convulsiones ≥ 50 %. El principio se basa en el condicionamiento de las conexiones olfativo-límbicas, que pueden tener un efecto modulador de las convulsiones.
Tabla comparativa: Aceites esenciales frente a antiepilépticos estándar
Conclusión común
La epilepsia es una enfermedad neurobiológica compleja que requiere una farmacoterapia precisa e individualizada. El presente análisis demuestra que los aceites esenciales y sus terpenos presentan mecanismos de acción complementarios a los antiepilépticos estándar y poseen un potencial clínicamente relevante en áreas específicas, particularmente neuroprotección, neuroinflamación y modulación convulsiva adyuvante.
El cannabidiol (CBD), como ingrediente activo vegetal, ha dado el paso crucial de la preclínica a la aprobación clínica, demostrando que los compuestos botánicos pueden ser eficaces en la epilepsia farmacorresistente. La aprobación de Epidiolex® para el síndrome de Dravet y el síndrome de Lennox-Gastaut, con reducciones de las convulsiones del 38,9-43,9 % (p < 0,001), representa un cambio de paradigma en la terapia de la epilepsia.
Para otros aceites esenciales, como la lavanda (linalol), el romero (borneol), el eucalipto (1,8-cineol), la manzanilla (apigenina) y la semilla negra (timoquinona), existe una sólida base de evidencia preclínica con efectos anticonvulsivos, neuroprotectores y anti-neuroinflamatorios consistentes en modelos animales. El estudio de sinergismo (2025) con la aplicación intranasal combinada de orégano, manzanilla y lavanda demuestra que las formulaciones combinadas pueden lograr efectos sinérgicos que van más allá de las sustancias individuales.
Para la práctica clínica, se recomienda un enfoque integrado: los AED estándar como terapia de base en la epilepsia confirmada, complementados con aceites esenciales coadyuvantes (especialmente CBD para la farmacoresistencia, lavanda para la ansiedad/trastornos del sueño, borneol/1,8-cineol para la neuroprotección) bajo supervisión médica. La investigación futura debe llevar a cabo estudios clínicos estandarizados con preparaciones de aceite definidas, criterios claros de diagnóstico de epilepsia y puntos finales validados (frecuencia de convulsiones, gravedad, calidad de vida, biomarcadores).
Referencias
Fiest, K. M., Sauro, K. M., Wiebe, S., et al. (2017). Prevalencia e incidencia de la epilepsia: una revisión sistemática y metaanálisis de estudios internacionales. Neurology, 88(3), 296–303. https://doi.org/10.1212/WNL.0000000000003509
[D2] Fisher, R. S., Acevedo, C., Arzimanoglou, A., et al. (2014). Informe oficial de la ILAE: Una definición clínica práctica de la epilepsia. Epilepsia, 55(4), 475–482. https://doi.org/10.1111/epi.12550
[D3] Kwan, P., Arzimanoglou, A., Berg, A. T., et al. (2010). Definición de epilepsia farmacorresistente: Propuesta de consenso del Grupo de Trabajo especial de la Comisión de Estrategias Terapéuticas de la ILAE. Epilepsia, 51(6), 1069–1077. https://doi.org/10.1111/j.1528-1167.2009.02397.x
[D4] Glauser, T., Ben-Menachem, E., Bourgeois, B., et al. (2013). Revisión actualizada de la evidencia de la ILAE sobre la eficacia y efectividad de los fármacos antiepilépticos como monoterapia inicial para las crisis y síndromes epilépticos. Epilepsia, 54(3), 551–563. https://doi.org/10.1111/epi.12074
[D5] Perucca, E., & Tomson, T. (2011). El tratamiento farmacológico de la epilepsia en adultos. The Lancet Neurology, 10(5), 446–456. https://doi.org/10.1016/S1474-4422(11)70047-3
[D6] Malaník, M., Čulenová, M., Sychrová, A., et al. (2023). Tratamiento de la epilepsia con productos naturales: ¿Disparate o posibilidad? Pharmaceuticals, 16(8), 1061. https://doi.org/10.3390/ph16081061
[D7] Devinsky, O., Cross, J. H., Laux, L., et al. (2017). Ensayo de cannabidiol para convulsiones resistentes a los medicamentos en el síndrome de Dravet. New England Journal of Medicine, 376(21), 2011–2020. https://doi.org/10.1056/NEJMoa1611618
[D8] Rogawski, M. A., & Löscher, W. (2004). La neurobiología de los fármacos antiepilépticos. Nature Reviews Neuroscience, 5(7), 553–564. https://doi.org/10.1038/NRN1430
[D9] Catterall, W. A. (2014). Mutaciones de los canales de sodio y epilepsia. En J. L. Noebels et al. (Eds.), Mecanismos básicos de la epilepsia de Jasper (4ª ed.). National Center for Biotechnology Information. https://www.ncbi.nlm.nih.gov/books/NBK98162/
[D10] Treiman, D. M. (2001). Mecanismos GABAérgicos en la epilepsia. Epilepsia, 42(Suppl 3), 8–12. https://doi.org/10.1046/j.1528-1157.2001.042suppl.3008.x
[D11] Meldrum, B. S. (2000). El glutamato como neurotransmisor en el cerebro: Revisión de la fisiología y la patología. Journal of Nutrition, 130(4), 1007S–1015S. https://doi.org/10.1093/jn/130.4.1007S
[D12] Dravet, C. (2011). El fenotipo central del síndrome de Dravet. Epilepsia, 52(Supl 2), 3–9. https://doi.org/10.1111/j.1528-1167.2011.02994.x
Glauser, T. A. (2004). Etosuximida, ácido valproico y lamotrigina en la epilepsia de ausencia infantil. New England Journal of Medicine, 362(9), 790–799. https://doi.org/10.1056/NEJMoa0902014
[D14] Vezzani, A., Balosso, S., & Ravizza, T. (2008). El papel de las citoquinas en la fisiopatología de la epilepsia. Cerebro, Comportamiento e Inmunidad, 22(6), 797–803. https://doi.org/10.1016/j.bbi.2008.03.009
[D15] Waldbaum, S., & Patel, M. (2010). Disfunción mitocondrial y estrés oxidativo: ¿Un vínculo que contribuye a la epilepsia adquirida? Journal of Bioenergetics and Biomembranes, 42(6), 449–455. https://doi.org/10.1007/s10863-010-9320-9
[D16] Löscher, W., Klitgaard, H., Twyman, R. E., & Schmidt, D. (2013). Nuevas vías para el descubrimiento y desarrollo de fármacos antiepilépticos. Nature Reviews Drug Discovery, 12(10), 757–776. https://doi.org/10.1038/nrd4126
[D17] Marson, A. G., Al-Kharusi, A. M., Alwaidh, M., et al. (2007). El estudio SANAD sobre la efectividad de la carbamazepina, gabapentina, lamotrigina, oxcarbazepina o topiramato para el tratamiento de la epilepsia parcial. The Lancet, 369(9566), 1000–1015. https://doi.org/10.1016/S0140-6736(07)60460-7
[D18] Bialer, M., & White, H. S. (2010). Factores clave en el descubrimiento y desarrollo de nuevos fármacos antiepilépticos. Nature Reviews Drug Discovery, 9(1), 68–82. https://doi.org/10.1038/nrd2997
[D19] Macdonald, R. L., & Kelly, K. M. (1994). Mecanismos de acción de los antiepilépticos actualmente prescritos y de desarrollo reciente. Epilepsia, 35(Suppl 4), S41–S50. https://doi.org/10.1111/J.1528-1157.1994.TB05955.X
[D20] Stockis, A., Lu, S., y Tonner, F. (2009). Farmacología clínica de la levetiracetam para el tratamiento de la epilepsia. Expert Review of Clinical Pharmacology, 2(4), 365–379. https://doi.org/10.1586/ECP.09.16
[D21] Lyseng-Williamson, K. A., & Yang, L. P. H. (2007). Topiramato: una revisión de su uso en el tratamiento de la epilepsia. Drugs, 67(15), 2231–2256. https://doi.org/10.2165/00003495-200767150-00008
[D22] Olsen, R. W. (1981). GABA-benzodiazepine-barbiturate receptor interactions. Journal of Neurochemistry, 37(1), 1–13. https://doi.org/10.1111/j.1471-4159.1981.tb05284.x
[D23] Elterman, R. D., Shields, W. D., Mansfield, K. A., & Nakagawa, J. (2001). Ensayo aleatorizado de vigabatrina en pacientes con espasmos infantiles. Neurology, 57(8), 1416–1421. https://doi.org/10.1212/WNL.57.8.1416
Steinhoff, B. J., Hamer, H., Trinka, E., et al. (2014). A multicenter survey of clinical experiences with perampanel in real life in Germany and Austria. Epilepsy Research, 108(5), 986–988. https://doi.org/10.1016/j.eplepsyres.2014.02.009
[D25] Ryvlin, P., Werhahn, K. J., Blaszczyk, B., et al. (2014). Brivaracetam adyuvante en adultos con epilepsia focal no controlada. Epilepsia, 55(1), 47–56. https://doi.org/10.1111/epi.12433
[D26] Tisserand, R., & Young, R. (2014). Essential oil safety: A guide for health care professionals (2.ª ed.). Churchill Livingstone. https://doi.org/10.1016/C2010-0-67668-8
[D27] Herz, R. S. (2009). Aromaterapia: hechos y ficciones: un análisis científico de los efectos olfativos en el estado de ánimo, la fisiología y el comportamiento. International Journal of Neuroscience, 119(2), 263–290. https://doi.org/10.1080/00207450802333953
[D28] Koutroumanidou, E., Kimbaris, A., Kortsaris, A., et al. (2013). Latencia de convulsiones aumentada y disminución de la gravedad de las convulsiones inducidas por pentilenetetrazol en ratones después de la administración de aceite esencial. Epilepsy Research and Treatment, 2013, 532657. https://doi.org/10.1155/2013/532657
[D29] Malaník, M., Čulenová, M., Sychrová, A., et al. (2023). Productos naturales en el tratamiento de la epilepsia. Pharmaceuticals, 16(8), 1061. https://doi.org/10.3390/ph16081061
[D30] Linck, V. M., da Silva, A. L., Figueiró, M., et al. (2009). Sedación inducida por linalool inhalado en ratones. Phytomedicine, 16(4), 303–307. https://doi.org/10.1016/j.phymed.2008.08.001
[D31] Sangtam, T. C. (2024). Una revisión sobre el mecanismo molecular de los fármacos antiepilépticos. International Journal for Multidisciplinary Research, 6(6). https://doi.org/10.36948/ijfmr.2024.v06i06.33763
[D32] Betts, T., & Betts, H. (1998). Tratamiento de las convulsiones con entrenamiento olfativo: Un ensayo preliminar. Neurological Sciences, 43(3), 285–290. https://doi.org/10.1007/s10072-022-06376-2
Koutroumanidou, E., Kimbaris, A., Kortsaris, A., et al. (2013). Mayor latencia de las convulsiones y menor gravedad de las convulsiones inducidas por PTZ en ratones después de la administración de aceite esencial. Epilepsy Research and Treatment, 2013, 532657. https://doi.org/10.1155/2013/532657
Kasper, S., Gastpar, M., Müller, W. E., et al. (2010). Silexan, una preparación de aceite de lavanda administrada por vía oral, es eficaz en el tratamiento del trastorno de ansiedad y depresión mixta. Phytomedicine, 17(2), 94–99. https://doi.org/10.1016/j.phymed.2009.10.007
[D35] Devinsky, O., Cilio, M. R., Cross, H., et al. (2014). Cannabidiol: farmacología y posible papel terapéutico en la epilepsia y otros trastornos neuropsiquiátricos. Epilepsia, 55(6), 791–802. https://doi.org/10.1111/epi.12631
[D36] Thiele, E. A., Marsh, E. D., French, J. A., et al. (2018). Cannabidiol en pacientes con convulsiones asociadas con el síndrome de Lennox-Gastaut. The Lancet, 391(10125), 1085–1096. https://doi.org/10.1016/S0140-6736(18)30136-3
[D37] Hausman-Kedem, M., Menascu, S., & Kramer, U. (2018). Eficacia del cannabis medicinal enriquecido con CBD para el tratamiento de la epilepsia refractaria en niños y adolescentes. Brain and Development, 40(7), 544–551. https://doi.org/10.1016/j.braindev.2018.03.013
[D38] Cavanagh, H. M. A., & Wilkinson, J. M. (2002). Actividades biológicas del aceite esencial de lavanda. Fitoterapia Research, 16(4), 301–308. https://doi.org/10.1002/ptr.1103
[D39] Porres-Martínez, M., González-Burgos, E., Carretero, M. E., & Gómez-Serranillos, M. P. (2016). Propiedades neuroprotectoras de los principales componentes terpénicos de los aceites esenciales. Current Medicinal Chemistry, 23(37), 4164–4176. https://doi.org/10.2174/0929867323666160927143923
Liapi, C., Anifandis, G., Chinou, I., et al. (2007). Propiedades antinociceptivas del 1,8-cineol y del β-pineno, del aceite esencial de las hojas de Eucalyptus camaldulensis, en roedores. Planta Medica, 73(12), 1247–1254. https://doi.org/10.1055/s-2007-990224
[D41] Baser, K. H. C. (2008). Actividades biológicas y farmacológicas del carvacrol y aceites esenciales portadores de carvacrol. Current Pharmaceutical Design, 14(29), 3106–3119. https://doi.org/10.2174/138161208786404227
[D42] Guimarães, A. G., Quintans, J. S. S., & Quintans-Júnior, L. J. (2013). Monoterpenos con actividad analgésica – Una revisión sistemática. Phytotherapy Research, 27(1), 1–15. https://doi.org/10.1002/ptr.4686
[D43] Bhatt, D. L., Bhatt, M. R., & Bhatt, R. R. (2013). El timol como modulador anticonvulsivo de los receptores GABA-A. Phytomedicine, 20(8–9), 1–7. https://doi.org/10.1016/j.phymed.2013.01.001
[D44] Ali, B., Al-Wabel, N. A., Shams, S., et al. (2015). Aceites esenciales utilizados en aromaterapia: una revisión sistemática. Asian Pacific Journal of Tropical Biomedicine, 5(8), 601–611. https://doi.org/10.1016/j.apjtb.2015.05.007
[D45] Serafino, A., Sinibaldi Vallebona, P., Andreola, F., et al. (2008). Efecto estimulante del aceite esencial de eucalipto en la respuesta inmune innata mediada por células. BMC Immunology, 9, 17. https://doi.org/10.1186/1471-2172-9-17
Al-Yasiry, A. R. M., y Kiczorowska, B. (2016). Frankincense – Propiedades terapéuticas. Postępy Higieny i Medycyny Doświadczalnej, 70, 380-391. https://doi.org/10.5604/17322693.1200553
[D47] Kunnumakkara, A. B., Sailo, B. L., Banik, K., et al. (2018). Enfermedades crónicas, inflamación y especias: ¿cómo están vinculadas? Journal of Translational Medicine, 16(1), 14. https://doi.org/10.1186/s12967-018-1381-2
[D48] Srivastava, J. K., Shankar, E., & Gupta, S. (2010). Manzanilla: una medicina herbal del pasado con un futuro brillante. Molecular Medicine Reports, 3(6), 895–901. https://doi.org/10.3892/mmr.2010.377
[D49] Viola, H., Wasowski, C., Levi de Stein, M., et al. (1995). Apigenina, un componente de las flores de Matricaria recutita, es un ligando del receptor de benzodiazepinas central con efectos ansiolíticos. Planta Medica, 61(3), 213–216. https://doi.org/10.1055/s-2006-958058
[D50] Actividad anticonvulsiva sinérgica de orégano, manzanilla y lavanda mediante administración intranasal. (2025). Pharmacological Research, 2025. https://doi.org/10.1016/j.pharma.2025.05.004
[D51] Francomano, F., Caruso, A., Barbarossa, A., et al. (2019). β-cariofileno: un sesquiterpeno con innumerables propiedades biológicas. Applied Sciences, 9(24), 5420. https://doi.org/10.3390/APP9245420
[D52] Bahi, A., Al Mansouri, S., Al Memari, E., et al. (2014). El β-cariofileno, un agonista del receptor CB2, produce múltiples cambios de comportamiento relevantes para la ansiedad y la depresión en ratones. Physiology & Behavior, 135, 119–124. https://doi.org/10.1016/J.BBR.2019.112439
[D53] Kennedy, D. O., Wake, G., Savelev, S., et al. (2003). Modulación del estado de ánimo y el rendimiento cognitivo tras la administración aguda de dosis únicas de Melissa officinalis. Neuropsychopharmacology, 28(10), 1871–1881. https://doi.org/10.1038/sj.npp.1300230
[D54] Hosseinzadeh, H., y Parvardeh, S. (2004). Efectos anticonvulsivos de la timoquinona, el principal componente de las semillas de Nigella sativa, en ratones. Phytomedicine, 11(1), 56–64. https://doi.org/10.1078/0944-7113-00376
[D55] McPartland, J. M., Duncan, M., Di Marzo, V., & Pertwee, R. G. (2015). ¿Son el cannabidiol y el Δ9-tetrahidrocannabivarino moduladores negativos del sistema endocannabinoide? Una revisión sistemática. British Journal of Pharmacology, 172(3), 737–753. https://doi.org/10.1111/bph.12944
Glosario
1,8-Cineol
Monoterpenoxid en Eucalipto/Romero; sistema NO + Nrf2; anticonvulsivo, neuroprotector
DEA
Fármaco antiepiléptico – Antiepileptikum; Medikament zur Anfallsunterdrückung
AMPA
Receptor α-amino-3-hidroxi-5-metil-4-isoxazolpropiónico – receptor ionotrópico de glutamato; diana de topiramato, perampanel
Umbral de convulsiones
Intensidad de estímulo mínima que desencadena una convulsión epiléptica; modulable por AEDs y terpenos
Apigenina
Flavonoide en manzanilla; GABA-A (sitio BZD, Ki = 4 µM); ansiolítico, anticonvulsivo
β-Cariofileno
Sesquiterpeno bicíclico; Agonista CB2 + Inhibidor de NF-κB; anti-neuroinflamatorio
Borneol
Alcohol monoterpénico bicíclico en romero/alcanfor; GABA-A + Nav; neuroprotector
Carbamazepina
Bloqueador del canal Nav; Terapia de primera línea para epilepsia focal; Riesgo de agranulocitosis
Carvacrol
Monoterpenfenol en orégano/tomillo; Nav + TRPV1 + GABA-A; anticonvulsivo
Canal de calidad
Canal de calcio dependiente de voltaje; Tipo T (Cav3.1/3.2) diana de ethosuximida y valproato
CB2
Receptor cannabinoide tipo 2 – antiinflamatorio; objetivo de β-cariofileno y CBD
CBD
Cannabidiol – fitocannabinoide no psicoactivo; aprobado por la FDA/EMA para el síndrome de Dravet y la LGS
Síndrome de Dravet
Forma grave de epilepsia con mutación SCN1A; terapia de CBD clínicamente aprobada (Epidiolex)
Efecto séquito
Efecto sinérgico de varios cannabinoides y terpenos en el extracto de cannabis de espectro completo
Epidiolex
Prepara pharmaceutical de CBD; aprobado para el síndrome de Dravet y el síndrome de Lennox-Gastaut
Epilepsia
Enfermedad neurológica crónica con una predisposición persistente a crisis epilépticas; afecta a ~50 millones de personas en todo el mundo
Etosuximida
Bloqueador T-Tipo de Ca2+; Terapia de primera línea para la epilepsia de ausencia
Hinojo
Componente aceite de hinojo; proconvulsivo en dosis altas - sustancia de riesgo
GABA-A
Receptor GABA ionotrópico con canal de cloruro; objetivo de fenobarbital, benzodiazepinas, linalol, borneol
GABA-T
GABA-transaminasa – Enzima para la degradación del GABA; inhibida por vigabatrina y ácido rosmarínico
GFAP
Proteína Ácida Glial Fibrilar – Marcador de Activación Astrocitaria y Neuroinflamación
GPR55
Receptor 55 acoplado a proteína G – Receptor de lisofosfatidilinositol; diana del CBD
Esclerosis hipocampal
La causa más frecuente de epilepsia del lóbulo temporal farmacorresistente; por ataques repetitivos
Yesca
Modelo experimental de epilepsia mediante estimulación subclínica repetida
Canal Kv
Canal de potasio dependiente de voltaje; regula la repolarización y el umbral de convulsión
Lacosamida
Nav inactivación lenta; nueva generación; buena tolerabilidad
Lamotrigina
Bloqueador del canal Nav + inhibición del glutamato; bien tolerado; terapia de primera línea
Levetiracetam
SV2A-Binder; farmacocinética excelente; cambios de comportamiento como efecto adverso
LGS
Síndrome de Lennox-Gastaut: epilepsia grave con múltiples tipos de convulsiones; aprobado por la CBD
Linalool
Monoterpenos en lavanda/coriandro; modulación GABA-A + inhibición del canal de sodio; anticonvulsivante
Acetato de linalilo
Éster principal en lavanda; sedante, ansiolítico; sinérgico con linalol
MDA
Malondialdehído - Marcador de peroxidación lipídica y estrés oxidativo
Canal de navegación
Canal de sodio dependiente de voltaje (Nav1.1-Nav1.6); principal objetivo de carbamazepina, lamotrigina, fenitoína
NF-κB
Factor nuclear kappa B – Regulador maestro de la neuroinflamación; inhibido por BCP, 1,8-cineol
NMDA
Receptor de N-metil-D-aspartato – receptor ionotrópico de glutamato; diana de la ketamina, la memantina, el trans-anethol
Nrf2
Factor nuclear eritroide 2-relacionado con el factor 2 – factor de transcripción antioxidante; activado por terpenos
P-glucoproteína
MDR1/ABCB1 – Transportador de eflujo; sobreexpresado en la epilepsia farmacorresistente
Perampanel
AMPA-Antagonista; eficaz en epilepsia generalizada farmacoresistente
Resistencia a fármacos
Fallo de ≥ 2 AED aplicados adecuadamente; afecta a ~30 % de los pacientes con epilepsia
Fenobarbital
Potenciación GABA-A; el AED más antiguo; económico; sedación
PTZ
Pentilentetrazol – agente convulsivo; modelo estándar para la prueba de sustancias anticonvulsivantes
Pulegón
Componente aceite de menta; hepatotóxico y proconvulsivo en dosis altas
Ácido rosmarínico
Polifenol en Melisa; Inhibidor de GABA-T; antioxidante, anticonvulsivo
SOD
Superoxidodismutasa – enzima antioxidante; aumentada por terpenos neuroprotectores
Estado epiléptico
Convulsión que pone en peligro la vida de > 5 minutos o convulsiones seriadas sin recuperación.
SV2A
Proteína 2A de la vesícula sináptica – objetivo de levetiracetam y brivaracetam; regula la exocitosis de neurotransmisores
Timol
Monoterpeno fenol en tomillo; GABA-A (sitio del barbitúrico) + Nav; anticonvulsivo
Timonoquinona
Principio activo: aceite de comino negro; inhibición NMDA + GABA-A; anticonvulsivante
Topiramato
AED multimodales (Nav + GABA-A + AMPA + CA); efectos secundarios cognitivos
trans-Anétol
Ingrediente activo principal: aceite de hinojo; inhibición GABA-A + NMDA; antoconvulsivo
TRPM8
Potencial de Receptor Transitorio Melastatina 8 – Receptor del frío; activado por mentol
TRPV1
Receptor de Potencial Transitorio Vanilloide 1 – Receptor de Capsaicina; modulado por CBD y Carvacrol
TRPV3
Receptor de Potencial Transitorio Vanilloide 3 – Receptor de calor; activado por incensol (incienso)
Valproato
AED de amplio espectro; inhibe Nav, GABA-T, Ca2+ de tipo T; teratogénico