Innehållsförteckning
Epilepsi kan i cirka 30% av fallen inte tillräckligt behandlas med farmaceutiska medel, varför eteriska oljor riktar uppmärksamheten mot som en stödjande åtgärd.
Vad som bör beaktas här, huruvida och i vilken utsträckning de är till hjälp, förklaras nedan – begripligt för lekmän.
En kort sammanfattning av den vetenskapliga rapporten för alla som vill veta mer om naturligt stöd vid epilepsi.
En ordlista, efter källförteckningen, förklarar facktermer.
Den tredje delen riktar sig till läkare, presenterar det aktuella läget för farmakologisk behandling, samt studieresultat gällande stödjande eteriska oljor vid epilepsi inklusive källhänvisning.
Vad är epilepsi?
Hjärnan består av miljarder nervceller som ständigt sänder elektriska signaler. Normalt sker detta på ett organiserat sätt, som en väl dirigerad orkester. Vid epilepsi uppstår plötsligt en sorts “elektrisk storm” i hjärnan, anfallet: Många nervceller avfyrar samtidigt och okontrollerat.
Vad händer under ett anfall?
Beroende på vilken del av hjärnan som drabbas kan ett anfall se mycket olika ut:
- Frånvaro
Kort “stå still” i sekunder, den drabbade stirrar in i tomheten - Myoklonisk anfall
Korta ryckningar (ofta på morgonen) - Fokala anfall Ryckningar eller känslor i en kroppsdel, ibland med medvetandeförlust
- Generaliserat tonisk-kloniskt anfall (tidigare “Grand Mal”): Fall, Steifheit, rhythmiskt ryckande av hela kroppen, medvetslöshet
Hur vanligt är epilepsi?
Epilepsi drabbar globalt cirka 50 miljoner människor, det är ungefär 1 % av världens befolkning. I Tyskland lever cirka 400 000–500 000 människor med epilepsi. Det är den tredje vanligaste neurologiska sjukdomen efter migrän och stroke.
Det stora problemet
Vid ungefär 30 % av patienterna Om medicinerna inte ger tillräcklig effekt talar man om läkemedelsresistent epilepsi. Dessa människor söker ofta efter kompletterande möjligheter.
Vid epilepsi sker onormala, synkroniserade elektriska urladdningar i hjärnan. Dessa urladdningar kan påverka olika delar av hjärnan, vilket leder till anfall. Symptomen på ett anfall beror på var i hjärnan urladdningarna sker och hur utbredda de är.
Två system måste vara i jämvikt:
- GABA (GABA): “Bromsmedlet”, lugnar hjärnan
- Glutamat: “Gaspedalen”, som aktiverar hjärnan
Vid epilepsi är balansen störd: för lite broms, för mycket gas, hjärnan “får spel”.
Dessutom spelar jonkanaler en viktig roll, det är små “grindar” i nervcellernas membran:
- Natriumkanaler (Nav)
De öppnar sig, när en nervcell avfyrar, vid epilepsi öppnar de sig för lätt - Kalciumkanaler (Cav)
Viktigt för vissa anfallstyper (t.ex. absenser) - Kaliumkanaler (Kv)
Hjälp att lugna nervcellen efter avfyrning
Hur behandlas epilepsi vanligtvis?
De viktigaste antiepileptika (AEDs)
Valproat (Valproinsyra) är det viktigaste bredspektrum-antiepileptikum. Det verkar på flera sätt samtidigt och är särskilt effektivt mot generaliserade epilepsier genom att bromsa natrium- och kalciumkanaler samt öka GABA.
Viktig varning:
Valproat är starkt skadligt för ofödda barn, kvinnor i fertil ålder!
KarIn Swedish, "Carbamazepin und Lamotrigin" translates to "karbamazepin och lamotrigin". är “dörrstoppare” för natriumkanaler. De förhindrar att nervcellerna avfyrar för lätt. De båda läkemedlen utgör förstahandsbehandlingen vid fokala epilepsier. Lamotrigin är särskilt bra tolererat och säkert under graviditet
Levetiracetam (Keppra) har en unik mekanism eftersom den binder till ett protein (SV2A) som reglerar signalöverföringen mellan nervceller. Den kännetecknas av en mycket god tolerabilitet och har inga interaktioner med andra läkemedel. Möjliga biverkningar är humörsvängningar och irritabilitet.
Topiramat verkar på fyra olika sätt samtidigt, en “multitalang” som man kan säga, som uppnår en hög andel anfallsfrihet på 44–83 % av patienterna. Som biverkning kan nedsatt tankeförmåga, liksom svårigheter att hitta ord, förekomma.
Etosuximid används vid absenser (korta “drömperioder”). Den blockerar specifika kalciumkanaler i thalamus (ett reläcenter i hjärnan).
Fenobarbital och bensodiazepiner förstärker GABA-effekten (“bromsen”). De är billiga, effektiva, men har sederande och beroendeframkallande potential (bensodiazepiner).
Eteriska oljor vid epilepsi – vad är möjligt?
Vid epilepsi ska särskild försiktighet iakttas!
Vissa eteriska oljor kan utlösa eller förvärra anfall (prokonvulsiva). Tala ALLTID med din neurolog innan du använder eteriska oljor.
Oljor du bör UNDVIKA vid epilepsi:
- Rosmarin (i höga doser – kamferinnehåll)
- Eukalyptus (i höga doser)
- Pepparmint (Pulegonhalt)
- Fänkål (Fänkål i höga doser)
- Salvia (Tujonhalt)
- Kamfer (direkt kramputlösande)
Vilka eteriska oljor visar antikonvulsiva egenskaper?
Lavendel – lugnande och krampförhindrande
Lavendel (Lavendel) är den mest studerade oljan vid epilepsi.
Sammansättning
– Linalool (25–45 %)
– Linalylacetat (25–50 %)
Effekt
– Aktiverar GABA-A-receptorer (hjärnans “broms”)
– Hämmar natriumkanaler (förhindrar okontrollerad avfyrning)
– Sänk anfallsberedskapen
Kliniska effekter
– Linalool förlängde signifikant tiden till första anfallet i PTZ-modellen (standardmodell för anfallstester) i djurförsök
– Vissa patienter rapporterar att aromaterapi med lavendel fördröjer anfall eller lindrar auror (varningssignaler).
– Använd i aromadiffusor via inandning, men aldrig invärtes utan läkarrådgivning
Rosmarin/Borneol – neuroprotektiv (med försiktighet!)
Borneol är ett aktivt ämne från rosmarin och andra växter.
Effekt
– Skyddar nervceller från skada orsakad av upprepade anfall; GABAerg och neuroprotektiv
– Borneol minskade svårighetsgraden av anfall i en kindling-modell och sänkte inflammationsmarkörer (GFAP) i djurförsök
Lystring! Rosmarinolja som helhet kan vara krampanfallsprovocerande i höga doser, inta endast isolerad borneol eller mycket låga doser
Oregano – Karvakrol och tymol
Karvakrol (från oregano och timjan) visar intressanta antikonvulsiva egenskaper.
Effekt
– Hämmar natriumkanaler (som karbamazepin)
– Modulerar TRPV1-receptorer (värme- och smärtreceptorer)
– Reducerad anfalls varaktighet och svårighetsgrad i djurförsök
Eukalyptus – 1,8-Cineol (med försiktighet!)
1,8-kineol eukalyptus uppvisar antikonvulsiv effekt i djurmodell.
Effekt
Påverkar NO-systemet (kvävemonoxid) i hjärnan
– Ökar anfallströskeln (~25 mg/kg jämfört med ~10 mg/kg i kontrollgruppen)
– Aktiverar Nrf2 (antioxidativ skyddsfaktor)
- Lystring! I höga doser prokonvulsivt, endast i små mängder och efter samråd med läkare
Kamomill – Apigenin och synergier
Kamomill (Matricaria chamomilla) innehåller apigenin, en flavonoid med ångestdämpande och kramplösande egenskaper.
Effekt
– Apigenin binder till GABA-A-receptorn (på samma ställe som bensodiazepiner, men mycket svagare)
– Ny studie (2025): Kombination av oregano + kamomill + lavendel (administrerat intranasalt) visade synergistisk antikonvulsiv effekt i djurmodell – bättre än någon olja ensam
- Som ett komplement vid milda anfall eller för att minska ångest
β-Karyofyllen – antiinflammatorisk
β-karyofyllen (BCP) finns i svartpeppar, lavendel, rosmarin och cannabis.
Effekt
– Aktiverar CB2-receptorer (cannabinoidreceptorer) utan psykoaktiv effekt
– Hämma NF-κB (inflammationsomkopplaren)
– Minskar neuroinflammation, viktigt eftersom inflammation kan förvärra epilepsi
– BCP finns också i hampaolja och kan vara en del av effekten av CBD-rika extrakt
Den viktigaste växten Cannabis och CBD
CBD (Cannabidiol) – det kliniska genombrottet
CBD är en aktiv substans från cannabisväxten (Cannabis sativa), men utan den kända psykoaktiva effekten av THC. Det är det enda växtbaserade epilepsiläkemedlet som officiellt godkändes av FDA (USA) och EMA (Europa) under namnet Epidiolex godkänts.
Det administreras som receptbelagt läkemedel (Epidiolex) i form av en olje-lösning oralt 2 gånger dagligen.
Effekt
– Hämmar natriumkanaler (som karbamazepin)
– Modulerar TRPV1 och GPR55 (speciella receptorer)
– Antiinflammatorisk via CB2-receptorer – Skyddar nervceller
Biverkningar
– Sömnighet, diarré, minskad aptit
– Kan spegeln av andra antiepileptika (särskilt klobazam) öka, dosjustering nödvändig
Auktorisation för:
- Dravets syndrom – En svår form av epilepsi som börjar i spädbarnsåldern
- Lennox-Gastaut-syndrom (LGS) – Svår epilepsi med flera anfallstyper
Studier
– Vid Dravet syndrom: CBD minskade anfallsfrekvensen med 38,9 % jämfört med 13,3 % med placebo, 66,7 % av patienterna hatten ≥ 50 % färre anfall (p = 0,009)
– Vid LGS: Minskning av fall med 43,9 % jämfört med 21,8 % med placebo (p < 0,001)
– Vid andra läkemedelsresistenta epilepsier: Olika studier visar 40–50 % anfallsreduktion
Jämförelsetabell – Vad hjälper hur?
Säkerhetsregel
Potentiellt hjälpsamt (efter samråd med läkare):
- Lavendel Aromaterapi (Diffusor, Inhalation) – avkopplande, möjligtvis anfallsreducerande
- CBD (som Epidiolex) – vid Dravet/LGS, receptbelagt
- β-Caryophyllen – antiinflammatoriskt, lätt att tolerera
- Kamomill – lugnande, ångestdämpande
Vid epilepsi UNDVIK:
- Rosmarinolja (ren, höga doser) – Kamfer kan utlösa anfall
- Eukalyptusolja (höga doser)
- Pepparmyntsolja (höga doser, pulegon)
- Fänkålsolja Fänkål
- Salviaolja (Thujon)
- Kampferolja (direkt kramputlösande)
Allmänna säkerhetsanvisningar
- TALKA ALLTID med neurologen först Epilepsi är allvarligt
- Sluta aldrig att ta antiepileptika på egen hand – kan leda till livshotande status epilepticus
- Beakta växelverkan: Vissa oljor kan förändra nivån av antiepileptika
- Aldrig gnugga direkt på huden – alltid späd
- Barn: Särskild försiktighet, doserna mycket lägre
Vanliga frågor
Kan jag ta lavendel istället för mina epilepsimediciner?
Nej, absolut inte! Lavendel har endast visat antikonvulsiva effekter i djurförsök. Att egenmäktigt avsluta antiepileptika kan vara livsfarligt.
Vad är det med CBD-olja från internet?
CBD-produkter från internet är inte samma sak som det godkända läkemedlet Epidiolex. De är inte standardiserade, kan innehålla andra cannabinoider och har ingen bevisad effekt. Tala med din neurolog om receptbelagt CBD.
Kan aromaterapi stoppa ett anfall?
Det finns rapporter om att vissa patienter kan fördröja anfall med hjälp av specifika dofter (som lavendel), men detta är inte en tillförlitlig metod och ingen ersättning för medicinering.
Är eteriska oljor säkra för barn med epilepsi?
Endast efter uttrycklig konsultation med barnneurologen. Barn reagerar känsligare, och vissa oljor är farliga för barn.
Måste jag köpa dyra oljor?
Kvalitet är viktigt: Se upp för 100 % 100 % rena eteriska oljor, helst med ett laddningsspecifikt analyscertifikat (GC/MS).
Billiga parfymoljor eller syntetiska doftämnen har ingen terapeutisk effekt och kan, på grund av de syntetiska ingredienserna, vara skadliga för hälsan och orsaka huvudvärk, illamående etc.
Den som vill veta mer om valet och kvaliteten på eteriska oljor hittar information i inlägget „Eteriska oljor – Sökandets odyssé“funnit.
Ett annat inlägg citerar professor Dr. med. habil. Hanns Hatt från Ruhr-Universität Bochum, som i en video säger:„Healing med dofter“förklarar på ett intressant, underhållande och ändå vetenskapligt sätt eteriska oljors verkan på människokroppen.
Här är en sammanfattning på tre meningar. Den ger en kort överblick över det viktigaste innehållet. Texten är koncis och lätt att förstå.
Epilepsi är en allvarlig neurologisk sjukdom där elektriska stormar i hjärnan orsakar anfall, och hos 30 % av patienterna hjälper standardmediciner inte tillräckligt.
Eteriska oljor och terpener, särskilt linalool (lavendel), borneol och karvakrol, visar antikonvulsiva egenskaper i djurförsök via GABA-A-aktivering och hämning av natriumkanaler; CBD (cannabidiol) är den enda växtbaserade antiepileptikan med kliniskt godkännande (Dravets syndrom, Lennox-Gastaut-syndrom).
Eteriska oljor kan användas som ett komplement vid epilepsi, men endast efter uttrycklig konsultation med den behandlande neurologen, eftersom vissa oljor också kan utlösa anfall.
Denna text baseras på den vetenskapliga rapporten “Epilepsi och eteriska oljor: Farmakologi, verkningsmekanismer och komplementära terapier” och är endast avsedd för allmän information. Epilepsi är en allvarlig sjukdom, vänd dig alltid till din neurolog med frågor om behandling.
Rekommenderade dōTERRA-Produkter för komplementärbehandling av epilepsi
Potentiellt säkra produkter (enligt forskningsläget)
Oljor som bör undvikas vid epilepsi
Egna oljeblandningar (Gör-det-själv-blandningar)
Blandning 1 – “Neuroprotektiv” (Diffuser)
Mål: Neuroprotektivt skydd, GABA-modulering
Ansökan: 30 minuter dagligen i diffusorn, särskilt på kvällen
Blandning 2 – “Aura-hantering” (Topisk, snabb)
Mål: Vid aurastadier: Försök att avbryta anfallet (ENDAST som ett komplement, inte som ersättning för akutmedicinering)
Ansökan: Vid tinningarna, nacken, handlederna – omedelbart vid migrationsbegynnelse
Nödmedicinering (t.ex. Diazepam rektalt) är fortfarande en prioritet
Blandning 3 – “Ångest & Stresslindring” (Diffusor/Topisk)
Mål: Stress ↓ (oftare anfallsutlösande), Avslappning ↑
Ansökan: Vid stress eller inför kända triggersituationer
Blandning 4 – “Sömn & Återhämtning” (Kväll)
Mål: Sömnkvalitet ↑ (Sömnbrist = anfallstrigger)
Ansökan: I diffusorn, 30 minuter innan sänggåendet
Blandning 5 – “Antiinflammatorisk” (Topisk)
Mål: Neuroinflammation ↓ (Epilepsipatofysiologi)
Ansökan: Massera tinningar, nacke och ryggrad.
Applikationsprotokoll – 4-veckorsplan
Vecka 1 – Försiktig start
- Konsultera läkare INNAN oljorna påbörjas
- Kvällsmat Blanda 4 i diffusorn (sömn)
- Dagligen Blanda 1 i diffusorn (30 min)
- Attackprotokoll köra (Datum, Tid, Utlösare)
Vecka 2 – Utökning
- Morgonen: Blanda 3 vid stressade situationer
- Kvällsmat Blanda 4 (Sömn) + Blanda 5 topiskt
- Blandning 2: Beredskap för aurastörningar
Vecka 3-4 – Optimering
- Analysera anfallsprotokoll – har något förändrats?
- Informera neurologen om oljeanvändning
- Anpassning baserat på individuell tolerans
Kombination med andra dōTERRAProdukten
Nödplan vid anfall
- Säkerhet Person in stabil sidoläge
- Mäta tid: Anfall som varar längre än 5 minuter → Ring 112
- Nödmedicin Diazepam-Rektal / Midazolam-Nasal (enligt läkares ordination)
- INGEN olja i mun eller näsa vid aktiv anfall
- Eteriska oljor är INTE akutmedicin
Epilepsi och eteriska oljor – farmakologi, verkningsmekanismer och komplementära terapier
En omfattande vetenskaplig rapport om vanliga antiepileptika, terpener och eteriska oljor – molekylära grunder, klinisk evidens och adjuvanta terapistrategier
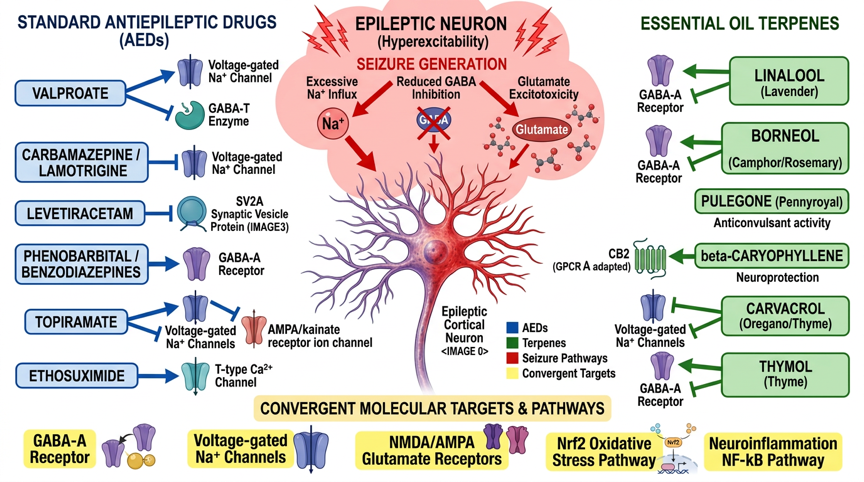
Fig. 1: Molekylära signalvägar för standard-antiepileptika och eteriska oljor vid epilepsi – Standard-AEDs (Valproat/Nav+GABA-T, Karbamazepin/Nav, Levetiracetam/SV2A, Topiramat/multimodal, Etosuximid/T-typ-Ca2+, Fenobarbital/GABA-A) och terpener (Linalool/GABA-A+Nav, Borneol/GABA-A+Nav, Karvakrol/Nav+TRPV1, β-Karyofyllen/CB2, 1,8-Cineol/NO+Nrf2) med konvergenta målölekyler (GABA-A-receptorn, Nav-kanaler, NMDA/AMPA-glutamat, NF-κB-neuroinflammation, Nrf2-oxidativ stress)
Ovan: Sharp Wave (70-200 ms) med efterföljande Slow Wave.
Mitte: 3-Hz spik-våg-komplex (GSWD) – Ett kännetecknande mönster vid absensepilepsi.
Nedan: Polyspikar (3–5 spikar, 4–5 Hz) – karakteristiskt för juvenil myoklonisk epilepsi (JME).
Inledning
Epilepsi är en av de vanligaste kroniska neurologiska sjukdomarna globalt och drabbar uppskattningsvis 50 miljoner människor, cirka 1 % av världens befolkning [D1]. Den definieras av en ihållande predisposition för epileptiska anfall till följd av patologiskt synkroniserade neurala urladdningar samt av de neurobiologiska, kognitiva, psykologiska och sociala konsekvenserna av denna sjukdom [D2]. Trots betydande framsteg i utvecklingen av antiepileptika (AEDs) kvarstår farmakoresistent epilepsi hos ungefär 30 % av patienterna, där två eller flera adekvat använda AEDs inte uppnår tillräcklig anfallskontroll [D3].
Standardbehandlingen av epilepsi innefattar en stegvis farmakoterapi med antiepileptika av första, andra och tredje generationen. Valproat, karbamazepin och lamotrigin anses vara förstahandsmedel vid fokala och generaliserade epilepsier; nyare substanser som levetiracetam, topiramat, lakosamid och perampanel utökar det terapeutiska arsenalet. [D4]. Trots sin effektivitet är AEDs förknippade med betydande biverkningar, kognitiva störningar, teratogenitet (valproat), benmärgsdepression (karbamazepin), viktökning och psykiska störningar som avsevärt påverkar patienternas livskvalitet. [D5].
Mot denna bakgrund växer det vetenskapliga intresset för växtbaserade ämnen och eteriska oljor som adjuvanta eller alternativa behandlingsalternativ. Talrika terpener och bioaktiva föreningar visar antikonvulsiva, neuroprotektiva, anti-neuroinflammatoriska och antioxidativa egenskaper i prekliniska och kliniska studier, ofta via mekanismer som beter sig komplementärt till klassiska AEDs. [D6]. Cannabidiol (CBD) har som aktiv substans från Cannabis sativa redan erhållit kliniskt godkännande för specifika epilepsisyndrom och visar potentialen hos botaniska föreningar i epilepsibehandling. [D7]. Denna rapport analyserar systematiskt farmakologin för standardantiepileptika, de molekylära verkningsmekanismerna för relevanta eteriska oljor och terpener, samt tillgängliga kliniska bevis för deras adjuvanta användning vid epilepsi.
EEG vid epilepsi – grunder och tolkningsprinciper
Elektroencefalografi (EEG) är det centrala diagnostiska instrumentet vid epilepsi och möjliggör direkt mätning av kortikal elektrisk aktivitet via elektroder på skalpen. Det används för anfallsklassificering, lokaliseringsdiagnostik och terapiövervakning.
Interiktal fas: EEG-svaret mellan anfallen visar typiskt interiktala epileptiforma urladdningar (IEDs): Spikar (<70 ms), vassa vågor (70-200 ms) och 3 Hz spike-wave-komplex (GSWDs vid absens epilepsi). Dessa IEDs uppstår från synkroniserade neuronala urladdningar i den epileptiska fokus.
Iktal fas: Anfallsektroencefalogrammet börjar ofta med lågspännings snabb aktivitet (LVFA, 20–35 Hz) som startmönster. Med tiden utvecklas en rytmisk theta-delta-utveckling med ökande amplitud. Avslutningen sker abrupt med efterföljande postiktal dämpning.
Postiktal fas: Efter att anfallet har upphört visar EEG en suppression (markant minskning av amplituden) följt av diffus delta-uppbromsning (0,5-3,5 Hz). Återhämtningen till normal bakgrundsaktivitet sker inom minuter till timmar, beroende på anfallslängd och typ.
Inverkan av β-karyofyllen på epilepsi-EEG: β-karyofyllen (BCP), en seskviterpenoid CB2-agonist från eteriska oljor (t.ex. svartpeppar, nejlika), reducerar vid PTZ-modellen anfallfrekvensen med 66%, ökar anfallslatenstiden med 187%och sänker spikfrekvensen med 27-68% . I EEG ses en normalisering av spektraleffekten: gammavågor (hyperexcitabilitetsmarkör) sjunker, deltasvågor ökar. Verkningsmekanismen omfattar CB2-agonism (neuroinflammation sjunker) och GABA-A-modulering (kloridinflöde ökar).
Epilepsins patofysiologi
Neuronala hyperkollaps och synkronisering
Epilepsins grundläggande patofysiologi bygger på en obalans mellan excitatorisk och inhibitorisk neurotransmission, vilket leder till anfallsartad synkroniserad neuronal urladdning. På cellnivå uppstår en epileptisk anfall genom samverkan mellan jonkanaldysfunktioner, störd synaptisk transmission och förändrad nätverksaktivitet. D8. Mutationer eller funktionella förändringar i spänningsberoende natrium- (Nav), kalium- (Kv) och kalciumkanaler (Cav) samt i ligandstyrda jonkanaler (GABA-A, NMDA) bidrar till ökad neuronal retbarhet. [D9].
Ovan (blå): Interiktal fas med IEDs (spikar <70 ms, skarpa vågor 70-200 ms, 3 Hz GSWDs).
Mitte (röd): Iktal fas – LVFA-inslag (20-35 Hz), theta-delta-utveckling, abrupt avslut.
Nedan (violett): Postiktal fas – EEG-suppression, diffus delta-saktning (0,5-3,5 Hz)
GABA/Glutamat-obalans
Balansen mellan den hämmande signalsubstansen GABA (gamma-aminosmörsyra) och den stimulerande signalsubstansen glutamat är avgörande för kramptröskeln. Minskad GABAerg hämning, orsakad av minskad GABA-syntes, minskad densitet av GABA-A-receptorer eller ökad aktivitet av GABA-transaminas, sänker kramptröskeln. [D10]. Samtidigt främjar överdriven aktivering av NMDA- och AMPA-glutamatreceptorer spridningen av depolarisering och epileptiska urladdningar. Denna GABA/glutamat-obalans är den centrala farmakologiska måltavlan för de flesta AEDs. [D11].
Jonkanalsdysfunktion
Spänningsberoende natriumkanaler (Nav1.1, Nav1.2, Nav1.6) spelar en central roll i genereringen och spridningen av aktionspotentialer. Gain-of-function-mutationer i Nav1.1 (Dravets syndrom) eller Nav1.2 leder till okontrollerade urladdningar. [D12]. T-typ-kalciumkanaler (Cav3.1, Cav3.2) är centrala vid absensanfall: Deras rytmiska aktivering i thalamus genererar de karakteristiska 3 Hz spik-våg-urladdningarna [D13]. Kaliumkanaldeffekter (KCNQ2/3, KCNT1) påverkar repolariseringen och ökar anlagsdispositionen.
Neuroinflammation och oxidativ stress
Kronisk epilepsi är associerad med ihållande neuroinflammation: Aktiverade mikroglia och astrocyter frisätter proinflammatoriska cytokiner (IL-1β, IL-6, TNF-α) som destabiliserar blod-hjärnbarriären och ökar neuronal retbarhet [D14]. Transkriptionsfaktorn NF-κB samordnar denna neuroinflammatoriska kaskad. Samtidigt leder repetitiva attacker till oxidativ stress genom mitokondriell dysfunktion och ROS-produktion, vilket gynnar neuronal apoptos och hippocampus-skleros. [D15]. Nrf2-signalvägen, som är den huvudsakliga regulatorn av det antioxidativa svaret, är ofta undertryckt vid läkemedelsresistent epilepsi.
Farmakoresistensmekanismer
Hos 30 % av epilepsipatienterna misslyckas två eller fler AED. Läkemedelsresistens beror på: (1) överuttryck av P-glykoprotein (P-gp/MDR1) och andra ABC-transportörer som pumpar ut AED från hjärnan; (2) förändringar i AED-måltavlor (t.ex. Nav-kanalmutationer som minskar fenytoinbindningen); (3) farmakogenetiska varianter i CYP-metabolismen; (4) neuroinflammation som förändrar blod-hjärnbarriärens permeabilitet [D16].
Farmakologi för standard-antiepileptika
Natriumkanalblockerare – Karbamazepin, Lamotrigin, Fenytoin, Lakosamid
Natriumkanalblocker är den vanligaste och äldsta klassen av AED. De binder till det inaktiverade tillståndet hos spänningsberoende natriumkanaler (Nav1.1–Nav1.6) och förlänger deras inaktiveringstid, principen för “användningsberoende blockad”.” D8. KarBamazepin (CBZ) och oxkarbazepin är förstahandsbehandling vid fokala epilepsier; lamotrigin hämmar dessutom presynaptisk frisättning av glutamat och är särskilt effektivt vid Lennox-Gastauts syndrom och absensenepilepsi [D17]. Fenytoin/Fosfenytoin stabiliserar det inaktiverade tillståndet hos Nav-kanaler och är ett standardläkemedel vid status epilepticus. Lakosamid (nyare generation) förstärker den “långsamma inaktiveringen” av Nav-kanaler via en unik mekanism och uppvisar gynnsam farmakokinetik. [D18].
Klinisk effekt: Karbamazepin uppnår anfallsfrihet hos 40–50 % av patienterna med fokala epilepsier som monoterapi; lamotrigin visar jämförbar effekt med bättre tolerabilitetsprofil, särskilt hos kvinnor i fertil ålder [D4].
Valproat – bredspektrum-antiepileptikum
Valproinsyra (valproat/VPA) är det viktigaste bredspektrum-antiepileptiska läkemedlet med multipla verkningsmekanismer: hämning av spänningskänsliga natriumkanaler, minskning av T-typ kalciumflöden, hämning av GABA-transaminas (GABA-T) med efterföljande ökning av GABA samt aktivering av glutamatdekarboxylas (GAD). [D19]. Valproat är förstahandsval vid behandling av generaliserade epilepsier (juvenil myoklonisk epilepsi, absens-epilepsi, Lennox-Gastaut) och uppnår anfallsfrihet hos 50–70 % av patienterna med idiopatisk generaliserad epilepsi [D4]. Kritiskt: Valproat är starkt teratogent (neuralrörsdefekter, kognitiva störningar hos nyfödda) och bör endast användas till kvinnor i fertil ålder efter en noggrann nytta-risk-bedömning [D5].
Levetiracetam – SV2A-bindning
Levetiracetam (LEV) har en unik verkningsmekanism: det binder selektivt till det synaptiska vesikelproteinet 2A (SV2A), som reglerar neurotransmittorexocytosen [D20]. Genom SV2A-bindning minskar LEV den presynaptiska frisättningen av neurotransmittorer vid högfrekventa urladdningar, en “frekvensberoende” mekanism som knappast påverkar normal synaptisk transmission. LEV är förstahandsbehandling vid fokala och generaliserade epilepsier, uppvisar utmärkt farmakokinetik (ingen enzyminduktion, ingen proteinbindning) och är relativt säker under graviditet. [D20]. Viktig biverkning: Beteendeförändringar (irritabilitet, depression) hos upp till 15 % av patienterna.
Topiramat – Multimodal mekanism
Topiramat (TPM) är en multimodal AED med minst fyra verkningsmekanismer:
- Blockering av spänningskänsliga natriumkanaler,
- Förstärkning av GABAerg hämning via GABA-A-receptorer
- Antagonism vid AMPA/kainat glutamatreceptorer
- Hämning av karbanhydras (CA-II, CA-IV) [D21]
Kliniska studier visar anfallsfria frekvenser på 44–83 % (6–7 månader) och 41–76 % (12–13 månader) i monoterapi-jämförelsestudier; topiramat är jämförbart effektivt med valproat och karbamazepin [D21]. Viktiga biverkningar: kognitiva funktionsnedsättningar (“svårigheter att hitta ord”), viktnedgång, njursten.
GABA-A-modulatorer – Fenobarbital, bensodiazepiner, vigabatrin
Fenobarbital (Barbiturat) och bensodiazepiner (diazepam, klonazepam, klobazam) förstärker GABA-A-receptormedierad kloridhämning: Barbiturater förlänger kloridkanalens öppningstid, bensodiazepiner ökar öppningsfrekvensen [D22]. Fenobarbital är en av de äldsta och billigaste AED:erna, används ofta i utvecklingsländer men har en betydande sederande potential. Vigabatrin hämmar irreversibelt GABA-transaminaset (GABA-T) och ökar därmed GABA-koncentrationen i hjärnan; det är effektivt vid spädbarnsspasmer, men förknippat med irreversibla synfältsdefekter [D23].
Ethosuximid – T-typ kalciumkanalblockerare
Ethosuximid (ESM) är en selektiv blockare av T-typ-kalciumkanaler (Cav3.1/3.2) och förstahandsbehandling vid fokal epilepsi hos barn [D13]. T-typkanaler genererar de rytmiska thalamiska urladdningarna som kännetecknar absenser; deras blockering bryter effektivt denna cykel. Etosuximid är lika effektivt som valproat vid absensepilepsi (anfallsfrihet ~50–60 %), men har färre biverkningar [D13].
Nyare AED – Lamotrigin, Perampanel, Brivaracetam
Lacosamid (LCM) förstärker selektiv den “långsamma inaktiveringen” av spänningsberoende natriumkanaler och hämmar Collapsin-Response-Mediator-Protein 2 (CRMP-2). [D18]. Perampanel (PER) är den första selektiva, icke-kompetitiva AMPA-glutamatreceptorantagonisten och är särskilt effektiv vid farmakoresistenta generaliserade tonisk-kloniska anfall. [D24]. Brivaracetam (BRV) binder likt levetiracetam till SV2A, men med 10 gånger högre affinitet och snabbare insättande effekt [D25].
Eteriska oljor som stödbehandling – Mekanistiska grunder
Farmakokinetik och CNS-penetration
Terpener från eteriska oljor kännetecknas av hög lipofilicitet och låg molekylvikt (< 300 Da), vilket möjliggör effektiv penetration av blod-hjärnbarriären (BBB). [D26]. Vid inhalation transporteras flyktiga terpener via luktslemhinnan direkt till luktbulben och det limbiska systemet, en direkt väg som kringgår blod-hjärnbarriären och leder till mätbara CNS-koncentrationer inom några minuter. [D27]. Transdermal och oral applicering möjliggör systemisk absorption; oral biotillgänglighet varierar kraftigt beroende på terpen och formulering.
Antikonvulsiva grundmekanismer
Eteriska oljor och deras terpener kan verka via flera antikonvulsiva mekanismer som överlappar med klassiska AEDs:
- Modulation av spänningsberoende natriumkanaler (Linalool, Borneol, Carvacrol, Thymol)
- Förstärkning av GABAerg hämning vid GABA-A-receptorer (Linalool, Borneol, Tymol, Apigenin)
- Hämning av glutamaterg excitering vid NMDA/AMPA-receptorer
- Antioxidativ neuroprotektion via Nrf2-aktivering; (5) Anti-neuroinflammatorisk verkan via NF-κB-hämning (β-karyofyllen) [D28].
Neuroprotektiva egenskaper
Många terpener uppvisar neuroprotektiva egenskaper som sträcker sig bortom direkt antikonvulsiv verkan. Genom att hämma apoptotiska signalvägar (kaspas-3, Bax/Bcl-2-förhållande), minska lipidperoxidation (MDA-nivåer) och öka antioxidativ enzymaktivitet (SOD, CAT, GPx) skyddar terpener mot anfallsinducerad nervskada. [D29]. Dessa neuroprotektiva egenskaper är särskilt relevanta vid farmakoresistent epilepsi, där upprepade anfall leder till progressiva hjärnskador.
Komplementära verkningsmekanismer till standardantiepileptika
Följande tabell visar eteriska oljors kompletterande verkningsmekanismer jämfört med standard-antiepileptika på molekylär nivå:

Standard-AEDs (Valproat/Nav+GABA-T, Karbamazepin/Nav, Levetiracetam/SV2A, Topiramat/multimodal, Etosuximid/T-typ-Ca²⁺, Fenobarbital/GABA-A) och terpener (Linalool/GABA-A+Nav, Bornylol/GABA-A+Nav, Karvakrol/Nav+TRPV1, β-karyofyllen/CB2, 1,8-cineol/NO+Nrf2) med konvergenta målspecifika molekyler (GABA-A, Nav, NMDA/AMPA, NF-κB, Nrf2/ARE).
Specifika eteriska oljor och kliniska bevis
Lavendelolja (Lavandula angustifolia) – Linalool
Lavendelolja är den mest undersökta eteriska oljan i samband med neurologiska sjukdomar. Den huvudsakliga aktiva substansen linalool (25–45 %) uppvisar antikonvulsiva egenskaper i prekliniska studier: I en pentylentetrazol-(PTZ)-modell ökade inhalation av linalool anfallströskeln, förlängde latensen till det första anfallet och minskade anfallsvaraktigheten [D30]. Linalool hämmar mekanistiskt spänningsberoende natriumkanaler genom att höja tröskeln för aktionspotentialen och minska uppåtgående hastighet, samt genom att modulera kalciumaktiverade kaliumströmmar. [D31]. En pilotstudie för luktträning vid epilepsipatienter (n=11) använde lavendel som en olfaktorisk betingningsstimuli och visade en ≥ 50 % minskning av anfallsfrekvensen hos 6 av 11 patienter %, medan författarna noterade den begränsade datamängden. [D32].
I en studie med flera eteriska oljor i en musmodell för PTZ visade Lavandula angustifolia en signifikant förlängning av anfallslatenstiden (p < 0,05) och en minskning av anfallssvårighetsgraden jämfört med kontrollgruppen. [D33]. Silexan (80 mg oralt, standardiserat lavendelextrakt) är kliniskt validerat för ångestsyndrom och skulle kunna användas som tilläggsbehandling vid epilepsi-relaterad ångest [D34].
Cannabisolja / Cannabidiol (CBD)
Kannabidiol (CBD) är den mest kända växtbaserade substansen med kliniskt bevisad antikonvulsiv effekt. Som en icke-psykoaktiv fytocannabinoid från Cannabis sativa har CBD flera antikonvulsiva mekanismer: antagonism vid GPR55 (lyso-fosfatidylinositol-receptorn), modulering av TRPV1-kanaler, hämning av spänningsberoende natriumkanaler och modulering av endocannabinoidsystemet. [D35]. Farmaceutisk CBD (Epidiolex®) är godkänd av FDA (2018) och EMA (2019) för Dravet syndrom och Lennox-Gastaut syndrom [D7].
Kliniska bevis: I placebokontrollerade fas III-studier av Dravets syndrom (n=120) reducerade CBD (20 mg/kg/dag) den månatliga konvulsiva anfallfrekvensen med 38,9 % jämfört med 13,3 % med placebo (p = 0,01) [D7]. Vid Lennox-Gastaut syndrom (n=225) reducerade CBD drop-anfallen med 43,9 % jämfört med 21,8 % under placebo (p < 0,001) [D36]. I en trippelblindstudie med refraktär epilepsi i frontalloben (n=27) visade 66,7 % av CBD-patienterna förbättring efter 4 veckor jämfört med 20,0 % med placebo (genomsnittlig skillnad 45,58; 95 % KI: 8,99–82,18; p = 0,009) [D37].
Rosmarinolja (Rosmarinus officinalis) – borneol, 1,8-cineol
Rosmarinolja innehåller borneol (upp till 20 %), 1,8-cineol/eukalyptol (35–50 %), kamfer (10–20 %) och α-pinen [D38]. Borneol uppvisar antiepileptogena effekter i en PTZ-kindling-modell: Det minskar anfallsutvecklingen, sänker GFAP-markörer (neuroinflammation) i hippocampus, minskar oxidativ stress och modulerar GABAerg transmission. [D39]. 1,8-Cineol höjde kramptröskeln i ett PTZ-tröskelförsök (~25 mg/kg vs. ~10 mg/kg i kontroll) och reducerade malondialdehyd-(MDA)-nivåer som en markör för oxidativ stress [D40]. I PTZ-multipeloljestudien visade Rosmarinus officinalis en signifikant förlängning av anfalls-latensen och en minskning av anfallens svårighetsgrad [D33].
Oregano-/Timjanolja – Karvakrol och tymol
Carvacrol (oregano, timjan, bondeör) och tymol (timjan) är strukturellt besläktade monoterpenfenoler med påvisad antikonvulsiv aktivitet [D41]. Karvakrol hämmar spänningskänsliga natriumkanaler (Nav1.2, Nav1.4) och TRPV1-kanaler, förstärker GABAergisk inhibition och uppvisar antikonvulsiva effekter i PTZ- och kaininsyramodeller. [D42]. Tymol modulerar GABA-A-receptorer positivt allosteriskt (liknande barbiturater) och hämmar spänningsberoende natriumkanaler [D43]. Viktig begränsning: Origanum vulgare-olja visade sig i en djurstudie vid den testade koncentrationen ha toxiska effekter (% 100 % dödlighet), vilket understryker vikten av standardiserad dosering och formulering [D33].
Eukalyptusolja (Eucalyptus globulus) – 1,8-Cineol
Eukalyptusolja innehåller 60–90 % 1,8-Cineol (Eukalyptol), ett monoterpenoxid med antikonvulsiva, antiinflammatoriska och antioxidativa egenskaper [D44]. 1,8-Cineol modulerar kväveoxid-(NO)-systemet, som har en komplex, dubbelriktad roll i anfallsregleringen: låga NO-nivåer kan verka antikonvulsivt medan höga NO-nivåer kan vara prokonvulsiva. I en PTZ-modell ökade 1,8-cineol anfallströskeln signifikant och minskade lipidperoxidation. [D40]. Inhalation av eukalyptusolja visar också anti-neuroinflammatoriska effekter genom NF-κB-hämning och minskning av proinflammatoriska cytokiner [D45].
Rökelseolja (Boswellia sacra) – α-pinen, boswelliasyror
Rökelseolja innehåller α-pinen (upp till 75 %), limonen och icke-flyktiga boswelliasyror [D46]. α-Pinen hämmar acetylkolinesteras och har ångestdämpande egenskaper; boswelliasyror (AKBA) hämmar 5-lipoxygenas och NF-κB, vilket minskar neuroinflammatoriska processer vid epilepsi. I djurmodeller visade boswelliaextrakt neuroprotektiva effekter efter kaininsyreinducerade anfall: minskad förlust av hippocampus-neuroner, minskad GFAP-expression och reducerade IL-1β-nivåer. [D47]. Incensolacetat från rökelse aktiverar TRPV3-kanaler och uppvisar ångestdämpande effekter oberoende av GABA-A- eller opioidreceptorer.
Kamomillolja (Matricaria chamomilla) – Apigenin, α-Bisabolol
Kamomillolja innehåller α-bisabolol (upp till 50 %), chamazulen och flavonen apigenin [D48]. Apigenin binder till bensodiazepinbindningsstället på GABA-A-receptorn (Ki=4 µM) och uppvisar ångestdämpande och antikonvulsiva egenskaper utan sedering i prekliniska modeller. [D49]. I en synergistudien (2025) visade kombinationen av oregano, kamomill och lavendel (intranasalt) synergistisk antikonvulsiv aktivitet i PTZ-modellen, med signifikant minskning av anfallsfrekvensen (p < 0,05) och optimerade effekter vid kombinerade lägre doser jämfört med enskilda substanser [D50].
Fänkålsolja (Foeniculum vulgare) – trans-Anetol
Fänkålsolja innehåller trans-anetol (50–80 %), fankon och estragol. Trans-anetol modulerar GABA-A-receptorer och hämmar NMDA-glutamatreceptorer, vilket förklarar antikonvulsiva effekter i djurmodeller [D28]. Däremot har fenkon (en beståndsdel i fänkålsolja) prokonvulsiva egenskaper och kan utlösa anfall, vilket understryker vikten av standardiserade, fenkonfattiga fänkålsoljepreparat för terapeutiska ändamål.
Molekylära verkningsmekanismer för terpener vid epilepsi
Linalool – Natriumkanalsinhibering och GABA-A-modulering
Linalool (3,7-Dimetyl-1,6-oktadien-3-ol), den huvudsakliga monoterpenen i lavendel och koriander, uppvisar dosberoende effekter på neuronal retbarhet. I isolerade neuroner ökar linalool tröskelvärdet för aktionspotentialer och minskar stegringen, vilka båda är indikatorer på natriumkanaldämpning. [D31]. Samtidigt aktiverar linalool kalciumberoende kaliumkanaler (BK-kanaler) som accelererar repolarisationen och minskar avfyrningsfrekvensen. GABA-A-modulering av linalool ökar kloridförmedlad inhibition. [D30]. Viktigt: Vid höga doser kan linalool verka paradoxalt stimulerande, vilket understryker vikten av dosoptimering.
Borneol – GABAerg modulering och neuroprotektion
Borneol (2-Bornanol), en bicyklisk monoterpenalkohol från kamferträd och rosmarin, uppvisar antiepileptogena effekter i PTZ-kindling-modellen. Den modulerar GABAerg transmission, minskar oxidativ stress (sänkta MDA-nivåer, ökad SOD-aktivitet) och sänker neuroinflammatoriska markörer (GFAP) i hippocampus. [D39]. Borneol hämmar också spänningskänsliga natriumkanaler och uppvisar synergistiska antikonvulsiva effekter i kombination med standard-AEDs i djurmodeller.
Karvakrol och tymol – Nav-kanalsblockad och GABA-A-modulering
Karvakrol (5-Isopropyl-2-metylfenol) och tymol (2-Isopropyl-5-metylfenol) är strukturisomeriska monoterpenfenoler med liknande men inte identiska verkningsmekanismer. Karvakrol hämmar Nav1.2- och Nav1.4-natriumkanaler samt TRPV1-kanaler och uppvisar neuroprotektiva effekter i kaininsyramodeller. [D42]. Tymol modulerar positivt GABA-A-receptorer allosteriskt på en bindningsplats liknande den för barbiturater och hämmar spänningsberoende natriumkanaler, en dubbelmekanism som liknar den för fenobarbital [D43].
β-Caryophyllen – CB2-agonism och anti-neuroinflammation
β-Caryophyllen (BCP), den tvåcykliska seskviterpenen från svartpeppar och kryddnejlika, verkar som en selektiv CB2-cannabinoidreceptoagonist och visar antikonvulsiva och neuroprotektiva effekter i djurmodeller [D51]. BCP:s antikonvulsiva effekter medieras delvis via GABAerga mekanismer samt serotonerga och nitrerga system. NF-κB-hämning av BCP reducerar neuroinflammatoriska processer som bidrar till epileptogenes. I en musmodell reducerade BCP signifikant krampanfallen inducerade av PTZ och visade neuroprotektiva effekter i hippocampus. [D52].
PTZ-modellens effekter och verkningsmekanism
A: Kontroll — 3 anfall på 20 s, hög spikfrekvens
B: BCP 200 mg/kg — 1 Anfall (↓66 %), Latenstid ↑187 %, Spikar ↓68 %.
C: Spikfrekvens dosberoende (↓27–68 %).
D: Spektraleffekten — Gamma-Power ↓, Delta-Power ↑ (Normalisering).
E: Verkningsmekanism — BCP → CB2 (↓Neuroinflammation) + GABA-A (↑Kloridinflöde → ↓Hyperexcitabilitet).
1,8-Cineol – NO-systemet och antioxidativ neuroprotektion
1,8-Cineol (Eukalyptol), den huvudsakliga monoterpenen i eukalyptus- och rosmarinolja, modulerar kvävemonoxid-(NO)-systemet och visar antioxidativ neuroprotektion [D40]. I ett PTZ-krampanfallstest ökade 1,8-cineol signifikant kramptröskeln (~25 mg/kg jämfört med ~10 mg/kg kontrollgrupp) och minskade nivåerna av malondialdehyd (MDA) som en markör för lipidperoxidation. Dessutom hämmar 1,8-cineol NF-κB-beroende neuroinflammatoriska processer och aktiverar Nrf2-signalvägen för antioxidativ neuroprotektion.
Nya och kompletterande eteriska oljor
Citronmelissolja (Melissa officinalis) Rosmarinsyra
Melissolja innehåller rosmarinsyra, citral, citronellal och geraniol [D53]. Rosmarinsyra hämmar GABA-transaminas (GABA-T), samma mekanism som vigabatrin, och ökar därmed GABAerg hämning. Dessutom visar rosmarinsyra antioxidativa och anti-neuroinflammatoriska egenskaper genom hämning av COX-2 och NF-κB. I djurmodeller har citronmelissextrakt visat antikonvulsiva effekter vid PTZ-inducerade anfall.
Pepparmyntsolja (Mentha piperita) – Mentol, Pulégon
Pepparmyntsolja innehåller mentol (30–55 %), menton (14–32 %) och pulegon (< 1 %). I PTZ-multiolje-studien visade Mentha piperita, vid den testade koncentrationen, inga anfall och 100 % överlevnad, den bästa säkerhetsprofilen av alla oljor som testades [D33]. Mentol aktiverar TRPM8-köldreceptorer och modulerar natriumkanaler; det uppvisar analgetiska och svagt antikonvulsiva egenskaper. Viktigt: Pulegon i höga koncentrationer är hepatotoxiskt och prokonvulsivt.
Svartkumminolja (Nigella sativa) – Tymokinon
Svartkumminolja innehåller tymokinon (TQ, 30–48 %), som uppvisar starka antikonvulsiva, neuroprotektiva och anti-neuroinflammatoriska egenskaper [D54]. TQ hämmar NMDA-glutamatreceptorn, aktiverar GABA-A-receptorn och uppvisar i djurmodeller effekt jämförbar med valproat vid PTZ-inducerade anfall. TQ aktiverar Nrf2 och hämmar NF-κB, vilket minskar oxidativ stress och neuroinflammation vid epilepsi.
Hampaextrakt – CBD och andra cannabinoider
Förutom farmaceutisk CBD innehåller Cannabis sativa ytterligare kramplösande cannabinoider: CBDV (Cannabidivarin) visar effekt vid fokala anfall i kliniska studier; THCV (Tetrahydrocannabivarin) har kramplösande egenskaper i djurmodeller; CBG (Cannabigerol) visar neuroprotektiva effekter [D55]. Entourageeffekten beskriver synergistiska effekter mellan olika cannabinoider och terpener i ett fullspektrum cannabisextrakt.
Kliniska bevis i jämförelse med standardbehandling
Randomiserade kontrollerade studier (RCTs)
Den kliniska evidensen för eteriska oljor vid epilepsi är, med undantag för farmaceutisk CBD, huvudsakligen preklinisk. CBD har visat övertygande effekt i flera fas III RCTs för Dravet syndrom och Lennox-Gastaut syndrom: Minskning av konvulsiva anfall med 38,9 % (Dravet, p = 0,01) och droppanfall med 43,9 % (LGS, p < 0,001) [D7] [D36]. I en trippelblindstudie med refraktär frontallapsepilepsi (n=27) visade CBD signifikant överlägsenhet jämfört med placebo (66,7 % vs. 20,0 % svarande, p = 0,009) [D37].
Prekliniska djurmodeller
I en PTZ-musemodell med flera eteriska oljor (Lavandula angustifolia, Rosmarinus officinalis, Mentha piperita, Origanum majorana) visade alla testade oljor (utom Origanum vulgare) signifikanta förlängningar av anfallslatenstiden och minskningar av anfallens svårighetsgrad jämfört med kontrollgruppen (p < 0,05). [D33]. En synergistisk studie (2025) med kombinerad intranasal applicering av oregano-, kamomill- och lavendeloljor visade synergistiska antikonvulsiva effekter som översteg summan av de enskilda effekterna. [D50].
Olfaktorisk träning vid epilepsi
En pilotstudie av luktträning (seizure alert aromaterapi) hos epilepsipatienter (n=11) använde konditionerade doftstimuli (lavendel, jasmin) för anfallsprognos och kontroll [D32]. 6 av 11 patienter visade en ≥ 50 %% anfallsreduktion. Principen bygger på konditionering av lukt-limbisk koppling, som kan ha anfallsmodulerande effekt.
Jämförelsetabell – Eteriska oljor vs. Standardläkemedel mot epilepsi
Gemensam slutsats
Epilepsi är en komplex neurobiologisk sjukdom som kräver en precis, individualiserad farmakoterapi. Denna analys visar att eteriska oljor och deras terpener uppvisar kompletterande verkningsmekanismer till standardantiepileptika och har kliniskt relevanta potentialer inom specifika områden, särskilt neuroprotektion, neuroinflammation och adjuvant anfallsmodulering.
Cannabidiol (CBD) har som växtbaserad aktiv substans tagit det avgörande steget från preklinisk till klinisk godkännande och visar att botaniska föreningar kan vara effektiva vid läkemedelsresistent epilepsi. Godkännandet av Epidiolex® för Dravet-syndrom och Lennox-Gastaut-syndrom med anfallsreduktioner på 38,9–43,9 % (p < 0,001) representerar ett paradigmskifte i behandling av epilepsi.
För andra eteriska oljor, som lavendel (linalool), rosmarin (borneol), eukalyptus (1,8-cineol), kamomill (apigenin) och svartkummin (tymokinon), finns det en gedigen preklinisk evidensgrund med konsekventa antikonvulsiva, neuroprotektiva och anti-neuroinflammatoriska effekter i djurmodeller. Synergistudien (2025) med kombinerad intranasal administrering av oregano, kamomill och lavendel visar att kombinerade formuleringar kan uppnå synergistiska effekter som överstiger enskilda substanser.
För klinisk praxis rekommenderas ett integrerat angreppssätt: standard-AED:er som basbehandling vid påvisad epilepsi, kompletterat med adjuvanta eteriska oljor (särskilt CBD vid farmakoresistens, lavendel vid ångest/sömnstörningar, borneol/1,8-cineol för neuroprotektion) under läkarövervakning. Framtida forskning måste genomföra standardiserade kliniska studier med definierade oljepreparat, tydliga epilepsidiagnoskriterier och validerade slutpunkter (anfallshastighet, -svårighetsgrad, livskvalitet, biomarkörer).
Referenser
Fiest, K. M., Sauro, K. M., Wiebe, S., et al. (2017). Prevalence and incidence of epilepsy: A systematic review and meta-analysis of international studies. Neurology, 88(3), 296–303. https://doi.org/10.1212/WNL.0000000000003509
[D2] Fisher, R. S., Acevedo, C., Arzimanoglou, A., m.fl. (2014). ILAE officiell rapport: En praktisk klinisk definition av epilepsi. Epilepsia, 55(4), 475–482. https://doi.org/10.1111/epi.12550
[D3] Kwan, P., Arzimanoglou, A., Berg, A. T., et al. (2010). Definition of drug resistant epilepsy: Consensus proposal by the ad hoc Task Force of the ILAE Commission on Therapeutic Strategies. Epilepsia, 51(6), 1069–1077. https://doi.org/10.1111/j.1528-1167.2009.02397.x
[D4] Glauser, T., Ben-Menachem, E., Bourgeois, B., et al. (2013). Uppdaterad ILAE-översikt av evidens för antiepileptikaeffekt och -effektivitet som initial monoterapi för epileptiska anfall och syndrom. Epilepsia, 54(3), 551–563. https://doi.org/10.1111/epi.12074
[D5] Perucca, E., & Tomson, T. (2011). The pharmacological treatment of epilepsy in adults. The Lancet Neurology, 10(5), 446–456. https://doi.org/10.1016/S1474-4422(11)70047-3
[D6] Malaník, M., Čulenová, M., Sychrová, A., et al. (2023). Behandling av epilepsi med naturliga produkter: Nonsens eller möjlighet? Pharmaceuticals, 16(8), 1061. https://doi.org/10.3390/ph16081061
[D7] Devinsky, O., Cross, J. H., Laux, L., et al. (2017). Rättegång med cannabidiol för läkemedelsresistent krampanfall vid Dravets syndrom. New England Journal of Medicine, 376(21), 2011–2020. https://doi.org/10.1056/NEJMoa1611618
[D8] Rogawski, M. A., & Löscher, W. (2004). Neurobiologin hos antiepileptiska läkemedel. Nature Reviews Neuroscience, 5(7), 553–564. https://doi.org/10.1038/NRN1430
[D9] Catterall, W. A. (2014). Sodium channel mutations and epilepsy. I J. L. Noebels et al. (red.), Jasper’s Basic Mechanisms of the Epilepsies (4:e uppl.). National Center for Biotechnology Information. https://www.ncbi.nlm.nih.gov/books/NBK98162/
[D10] Treiman, D. M. (2001). GABAerga mekanismer vid epilepsi. Epilepsia, 42(Suppl 3), 8–12. https://doi.org/10.1046/j.1528-1157.2001.042suppl.3008.x
[D11] Meldrum, B. S. (2000). Glutamat som signalsubstans i hjärnan: Översikt av fysiologi och patologi. Journal of Nutrition, 130(4), 1007S–1015S. https://doi.org/10.1093/jn/130.4.1007S
[D12] Dravet, C. (2011). The core Dravet syndrome phenotype. Epilepsia, 52(Suppl 2), 3–9. https://doi.org/10.1111/j.1528-1167.2011.02994.x
[D13] Glauser, T. A. (2004). Etosuximid, valproinsyra och lamotrigin vid absensenepilepsi hos barn. New England Journal of Medicine, 362(9), 790–799. https://doi.org/10.1056/NEJMoa0902014
[D14] Vezzani, A., Balosso, S., & Ravizza, T. (2008). Cytokinernas roll i epilepsins patofysiologi. Brain, Behavior, and Immunity, 22(6), 797–803. https://doi.org/10.1016/j.bbi.2008.03.009
[D15] Waldbaum, S., & Patel, M. (2010). Mitochondrial dysfunction and oxidative stress: A contributing link to acquired epilepsy? Journal of Bioenergetics and Biomembranes, 42(6), 449–455. https://doi.org/10.1007/s10863-010-9320-9
[D16] Löscher, W., Klitgaard, H., Twyman, R. E., & Schmidt, D. (2013). New avenues for anti-epileptic drug discovery and development. Nature Reviews Drug Discovery, 12(10), 757–776. https://doi.org/10.1038/nrd4126
[D17] Marson, A. G., Al-Kharusi, A. M., Alwaidh, M., et al. (2007). SANAD-studien om effektiviteten av karbamazepin, gabapentin, lamotrigin, oxkarbazepin eller topiramat för behandling av partiell epilepsi. The Lancet, 369(9566), 1000–1015. https://doi.org/10.1016/S0140-6736(07)60460-7
[D18] Bialer, M., & White, H. S. (2010). Key factors in the discovery and development of new antiepileptic drugs. Nature Reviews Drug Discovery, 9(1), 68–82. https://doi.org/10.1038/nrd2997
[D19] Macdonald, R. L., & Kelly, K. M. (1994). Verkansmekanismer för nuvarande och nyutvecklade antiepileptiska läkemedel. Epilepsia, 35(Suppl 4), S41–S50. https://doi.org/10.1111/J.1528-1157.1994.TB05955.X
Stockis, A., Lu, S., & Tonner, F. (2009). Clinical pharmacology of levetiracetam for the treatment of epilepsy. Expert Review of Clinical Pharmacology, 2(4), 365–379. https://doi.org/10.1586/ECP.09.16
[D21] Lyseng-Williamson, K. A., & Yang, L. P. H. (2007). Topiramat: En översikt över dess användning vid behandling av epilepsi. Drugs, 67(15), 2231–2256. https://doi.org/10.2165/00003495-200767150-00008
[D22] Olsen, R. W. (1981). GABA-benzodiazepine-barbiturate receptor interactions. Journal of Neurochemistry, 37(1), 1–13. https://doi.org/10.1111/j.1471-4159.1981.tb05284.x
[D23] Elterman, R. D., Shields, W. D., Mansfield, K. A., & Nakagawa, J. (2001). Randomiserad studie av vigabatrin hos patienter med infantil spasm. Neurology, 57(8), 1416–1421. https://doi.org/10.1212/WNL.57.8.1416
[D24] Steinhoff, B. J., Hamer, H., Trinka, E., et al. (2014). En multicenterundersökning av kliniska erfarenheter av perampanel i verkliga livet i Tyskland och Österrike. Epilepsy Research, 108(5), 986–988. https://doi.org/10.1016/j.eplepsyres.2014.02.009
[D25] Ryvlin, P., Werhahn, K. J., Blaszczyk, B., m.fl. (2014). Tilläggsbehandling med brivaracetam hos vuxna med okontrollerad fokal epilepsi. Epilepsia, 55(1), 47–56. https://doi.org/10.1111/epi.12433
[D26] Tisserand, R., & Young, R. (2014). Essential oil safety: A guide for health care professionals (2nd ed.). Churchill Livingstone. https://doi.org/10.1016/C2010-0-67668-8
[D27] Herz, R. S. (2009). Aromaterapins fakta och fiktion: En vetenskaplig analys av luktens effekter på humör, fysiologi och beteende. International Journal of Neuroscience, 119(2), 263–290. https://doi.org/10.1080/00207450802333953
[D28] Koutroumanidou, E., Kimbaris, A., Kortsaris, A., et al. (2013). Ökad anfallslatens och minskad svårighetsgrad av pentylentetrazol-inducerade anfall hos möss efter administrering av eterisk olja. Epilepsy Research and Treatment, 2013, 532657. https://doi.org/10.1155/2013/532657
[D29] Malaník, M., Čulenová, M., Sychrová, A., et al. (2023). Naturliga produkter vid behandling av epilepsi. Pharmaceuticals, 16(8), 1061. https://doi.org/10.3390/ph16081061
[D30] Linck, V. M., da Silva, A. L., Figueiró, M., et al. (2009). Inhalerad linalool-inducerad sedering hos möss. Phytomedicine, 16(4), 303–307. https://doi.org/10.1016/j.phymed.2008.08.001
[D31] Sangtam, T. C. (2024). En översikt av den molekylära mekanismen för antiepileptiska läkemedel. International Journal for Multidisciplinary Research, 6(6). https://doi.org/10.36948/ijfmr.2024.v06i06.33763
[D32] Betts, T., & Betts, H. (1998). Anfallskontroll med luktträning: En preliminär studie. Neurological Sciences, 43(3), 285–290. https://doi.org/10.1007/s10072-022-06376-2
[D33] Koutroumanidou, E., Kimbaris, A., Kortsaris, A., et al. (2013). Ökad anfallslatens och minskad svårighetsgrad av PTZ-inducerade anfall hos möss efter administrering av eterisk olja. Epilepsy Research and Treatment, 2013, 532657. https://doi.org/10.1155/2013/532657
[D34] Kasper, S., Gastpar, M., Müller, W. E., et al. (2010). Silexan, en oralt administrerad lavendelolja-beredning, är effektiv vid behandling av en blandad ångest- och depressionssjukdom. Phytomedicine, 17(2), 94–99. https://doi.org/10.1016/j.phymed.2009.10.007
[D35] Devinsky, O., Cilio, M. R., Cross, H., et al. (2014). Cannabidiol: Farmakologi och potentiell terapeutisk roll vid epilepsi och andra neuropsykiatriska störningar. Epilepsia, 55(6), 791–802. https://doi.org/10.1111/epi.12631
Thiele, E. A., Marsh, E. D., French, J. A., et al. (2018). Cannabidiol hos patienter med krampanfall associerade med Lennox-Gastaut syndrom. The Lancet, 391(10125), 1085–1096. https://doi.org/10.1016/S0140-6736(18)30136-3
[D37] Hausman-Kedem, M., Menascu, S., & Kramer, U. (2018). Efficacy of CBD-enriched medical cannabis for treatment of refractory epilepsy in children and adolescents. Brain and Development, 40(7), 544–551. https://doi.org/10.1016/j.braindev.2018.03.013
[D38] Cavanagh, H. M. A., & Wilkinson, J. M. (2002). Biologiska aktiviteter hos lavendel eterisk olja. Phytotherapy Research, 16(4), 301–308. https://doi.org/10.1002/ptr.1103
[D39] Porres-Martínez, M., González-Burgos, E., Carretero, M. E., & Gómez-Serranillos, M. P. (2016). Neuroprotektiva egenskaper hos större terpenkomponenter i eteriska oljor. Current Medicinal Chemistry, 23(37), 4164–4176. https://doi.org/10.2174/0929867323666160927143923
[D40] Liapi, C., Anifandis, G., Chinou, I., et al. (2007). Antinociceptiva egenskaper hos 1,8-cineol och β-pinen, från eterisk olja från Eucalyptus camaldulensis-blad, hos gnagare. Planta Medica, 73(12), 1247–1254. https://doi.org/10.1055/s-2007-990224
[D41] Baser, K. H. C. (2008). Biological and pharmacological activities of carvacrol and carvacrol bearing essential oils. Current Pharmaceutical Design, 14(29), 3106–3119. https://doi.org/10.2174/138161208786404227
[D42] Guimarães, A. G., Quintans, J. S. S., & Quintans-Júnior, L. J. (2013). Monoterpener med smärtstillande aktivitet – en systematisk översikt. Phytotherapy Research, 27(1), 1–15. https://doi.org/10.1002/ptr.4686
[D43] Bhatt, D. L., Bhatt, M. R., & Bhatt, R. R. (2013). Tymol som en antikonvulsiv modulator av GABA-A-receptorer. Phytomedicine, 20(8–9), 1–7. https://doi.org/10.1016/j.phymed.2013.01.001
[D44] Ali, B., Al-Wabel, N. A., Shams, S., et al. (2015). Essential oils used in aromatherapy: A systematic review. Asian Pacific Journal of Tropical Biomedicine, 5(8), 601–611. https://doi.org/10.1016/j.apjtb.2015.05.007
[D45] Serafino, A., Sinibaldi Vallebona, P., Andreola, F., et al. (2008). Stimulatory effect of eucalyptus essential oil on innate cell-mediated immune response. BMC Immunology, 9, 17. https://doi.org/10.1186/1471-2172-9-17
[D46] Al-Yasiry, A. R. M., & Kiczorowska, B. (2016). Frankincense – Therapeutic properties. Postępy Higieny i Medycyny Doświadczalnej, 70, 380–391. https://doi.org/10.5604/17322693.1200553
[D47] Kunnumakkara, A. B., Sailo, B. L., Banik, K., et al. (2018). Kroniska sjukdomar, inflammation och kryddor: Hur är de kopplade? Journal of Translational Medicine, 16(1), 14. https://doi.org/10.1186/s12967-018-1381-2
[D48] Srivastava, J. K., Shankar, E., & Gupta, S. (2010). Kamomill: En örtmedicin från förr med en ljus framtid. Molecular Medicine Reports, 3(6), 895–901. https://doi.org/10.3892/mmr.2010.377
[D49] Viola, H., Wasowski, C., Levi de Stein, M., et al. (1995). Apigenin, en komponent i blommor från Matricaria recutita, är en central bensodiazepinreceptorligand med anxiolytiska effekter. Planta Medica, 61(3), 213–216. https://doi.org/10.1055/s-2006-958058
[D50] Synergistisk antikonvulsiv aktivitet av oregano, kamomill och lavendel via intranasal administrering. (2025). Pharmacological Research, 2025. https://doi.org/10.1016/j.pharma.2025.05.004
[D51] Francomano, F., Caruso, A., Barbarossa, A., et al. (2019). β-caryofyllen: en sesquiterpen med otaliga biologiska egenskaper. Applied Sciences, 9(24), 5420. https://doi.org/10.3390/APP9245420
[D52] Bahi, A., Al Mansouri, S., Al Memari, E., et al. (2014). β-Caryophyllene, en CB2-receptoragonist, producerar flera beteendeförändringar relevanta för ångest och depression hos möss. Physiology & Behavior, 135, 119–124. https://doi.org/10.1016/J.BBR.2019.112439
[D53] Kennedy, D. O., Wake, G., Savelev, S., et al. (2003). Modulation av humör och kognitiv prestation efter akut administrering av enstaka doser av Melissa officinalis. Neuropsychopharmacology, 28(10), 1871–1881. https://doi.org/10.1038/sj.npp.1300230
[D54] Hosseinzadeh, H., & Parvardeh, S. (2004). Anticonvulsiva effekter av tymokinon, den huvudsakliga beståndsdelen i Nigella sativa-frön, hos möss. Phytomedicine, 11(1), 56–64. https://doi.org/10.1078/0944-7113-00376
[D55] McPartland, J. M., Duncan, M., Di Marzo, V., & Pertwee, R. G. (2015). Är cannabidiol och Δ9-tetrahydrocannivarin negativa modulatorer av endocannabinoidsystemet? En systematisk översikt. British Journal of Pharmacology, 172(3), 737–753. https://doi.org/10.1111/bph.12944
Glossar
1,8-kineol
Monoterpenoxid i Eukalyptus/Rosmarin; NO-system + Nrf2; antikonvulsiv, neuroprotektiv
AED
Antiepileptiskt läkemedel – Antiepileptikum; Medikament för anfallsupptryckning
AMPA
Alfa-amino-3-hydroxi-5-metyl-4-isoxazolpropionsyra-receptor – jonotrop glutamatreceptor; mål för topiramat, perampanel
Anfallströskel
Minimal reaktionsintensitet som utlöser ett epileptiskt anfall; modulerbar genom AED och terpener
Apigenin
Flavonoider i kamomill; GABA-A (BZD-site, Ki = 4 µM); ångestdämpande, kramplösande
β-karyofyllen
Bicyklisk sesquiterpen; CB2-agonist + NF-κB-hämmare; anti-neuroinflammatorisk
Borneol
Bicyklisk monoterpenalkohol i rosmarin/kamfer; GABA-A + Nav; neuroprotektiv
Karbamazepin
Nav-kanal-blockerare; förstahandsbehandling vid fokal epilepsi; risk för agranulocytos
Karvakrol
Monoterpenfenol i oregano/timjan; Nav + TRPV1 + GABA-A; antikonvulsiv
Cav-kanal
Spänningsberoende kalciumkanal; T-typ (Cav3.1/3.2) mål för etosuximid och valproat
CB2
Cannabinoidreceptor typ 2 – anti-neuroinflammatorisk; mål för β-karyofyllen och CBD
CBD
Kannabidiol – icke-psykoaktivt fytocannabinoid; FDA/EMA-godkänt för Dravet och LGS
Dravets syndrom
Svår epilepsi med SCN1A-mutation; kliniskt godkänd CBD-behandling (Epidiolex)
Omgivningseffekt
Synergistisk effekt av flera cannabinoider och terpener i helspektrum cannabisextrakt
Epidiolex
Farmaceutiskt CBD-preparat; godkänt för Dravets syndrom och Lennox-Gastauts syndrom
Epilepsi
Kronisk neurologisk sjukdom med bestående benägenhet att drabbas av epileptiska anfall; drabbar cirka 50 miljoner människor globalt
Etosuximid
T-typ-kalciumkanalblockerare; förstahandsbehandling absensenepilepsi
Fänkål
Beståndsdel fänkålsolja; prokonvulsiv i höga doser – riskämne
GABA-A
Jonotroper GABA-receptor med kloridkanal; mål för fenobarbital, bensodiazepiner, linalool, borneol
GABA-T
GABA-transaminas – Enzym för nedbrytning av GABA; hämmas av vigabatrin och rosmarinsyra
GFAP
Glial Fibrillary Acidic Protein – Markör för astrocytaaktivering och neuroinflammation
GPR55
G-proteinkopplad receptor 55 – Lyso-fosfatidylinositol-receptor; mål för CBD
Hippocampusskleros
Vanligaste orsaken till farmakoresistent temporal lobsepilepsi; genom upprepade anfall
Tändved
Experimentell epilepsimodell genom upprepad subtröskelstimulering
Kv-Kanal
Spänningsberoende kaliumkanal; reglerar repolarisering och anfallströskel
Lacosamid
Nav långsam inaktivering; ny generation; god tolerabilitet
Lamotrigin
Nav-kanalblocker + glutamathämning; väl tolererad; förstahandsbehandling
Levetiracetam
SV2A-bindare; utmärkt farmakokinetik; beteendeförändringar som biverkning
LGS
Lennox-Gastaut-syndrom – svår epilepsi med flera anfallstyper; CBD-godkänd
Linalool
Monoterpen i lavendel/koriander; GABA-A-modulering + Nav-hämning; antikonvulsiv
Linalylacetat
Huvudterpen i lavendel; sedativ, ångestdämpande; synergistisk med linalool
MDA
Malondialdehyd – Markörer för lipidperoxidation och oxidativ stress
Nav-kanal
Spänningsberoende natriumkanaler (Nav1.1-Nav1.6); Huvudmål för karbamazepin, lamotrigin, fenytoin
NF-κB
Kärnfaktor kappa B – Masterregulator av neuroinflammation; hämmad av BCP, 1,8-Cineol
NMDA
N-metyl-D-aspartatreceptor – jonotropisk glutamatreceptor; mål för ketamin, memantin, trans-anetol
Nrf2
Kärnfaktor erytroid 2-relaterad faktor 2 – antioxidant transkriptionsfaktor; aktiverad av terpener
P-glykoprotein
MDR1/ABCB1 – Efflux-transportör; överuttryckt vid farmakoresistent epilepsi
Perampanel
AMPA-antagonist; effektivt vid farmakoresistent generaliserad epilepsi
Läkemedelsresistens
Misslyckande av ≥ 2 adekvat använda AED; drabbar ca 30 % av epilepsipatienterna
Fenobarbital
GABA-A-potensiering; äldsta AED; billigt; sedering
PTZ
Pentylentetrazol – krampfutlösande medel; standardmodell för testning av antikonvulsiva substanser
Pulegon
Beståndsdel pepparmyntsolja; hepatotoxiskt och krampframkallande i höga doser
Rosmarinsyra
Polyfenol i meliss; GABA-T-hämmare; antioxidativt, antikonvulsivt
SOD
Superoxiddismutas – ett antioxidativt enzym; ökat av neuroprotektiva terpener
Status epilepticus
Livshotande anfall > 5 minuter eller seriella anfall utan återhämtning
SV2A
Synaptisk vesikelprotein 2A – mål för levetiracetam och brivaracetam; reglerar neurotransmittorexocytos
Thymol
Monoterpenfenol i timjan; GABA-A (barbituratbindningsställe) + Nav; antikonvulsiv
Tymokinon
Aktiva ingredienser svartkumminolja; NMDA-hämning + GABA-A; antikonvulsiv
Topiramat
Multimodalt AED (Nav + GABA-A + AMPA + CA); kognitiv NV
trans-Anetol
Huvudsaklig aktiv ingrediens fänkålsolja; GABA-A + NMDA-hämning; antikonvulsiv
TRPM8
Transient Receptor Potential Melastatin 8 – köldreceptor; aktiverad av mentol
TRPV1
Transient Receptor Potential Vanilloid 1 – Kapsaicinreceptor; modulerad av CBD och karvakrol
TRPV3
Transient Receptor Potential Vanilloid 3 – Värmereceptor; aktiverad av Incensol (rökelse)
Valproat
Bredspektrum-AED; hämmar Nav, GABA-T, T-typ-Ca2+; teratogen