Innholdsfortegnelse
Epilepsi kan i omtrent 30% av tilfellene ikke behandles tilstrekkelig med farmasøytiske midler, noe som gjør at eteriske oljer får økt oppmerksomhet som en støttende tiltak.
Hva som er viktig å merke seg her, om og i hvilken grad de er nyttige, blir nedenfor – forståelig for folk uten fagkunnskap – forklart.
En kortfattet oppsummering av den vitenskapelige rapporten for alle som ønsker å lære mer om naturlig støtte ved epilepsi.
Et ordliste, etter litteraturlisten, forklarer faguttrykk.
Den tredje delen retter seg mot leger, presenterer dagens status for farmakologisk behandling, samt studieresultater med hensyn til støttende eteriske oljer ved epilepsi inklusive kildereferanser.
Hva er epilepsi?
Hjernen består av milliarder av nerveceller som sender elektriske signaler hele tiden. Vanligvis skjer dette på en organisert måte, som et velsmurt orkester. Ved epilepsi oppstår det plutselig en slags “elektrisk storm” i hjernen, anfallet: Mange nerveceller fyrer samtidig og ukontrollert.
Hva skjer under et anfall?
Avhengig av hvilken del av hjernen som er rammet, kan et anfall se veldig forskjellig ut:
- Fravær
Kort “tilbaketrekking” i sekunder, den berørte stirrer tomt ut i luften - Myoklonusanfall
Korte, rykkvise bevegelser (ofte om morgenen) - Fokale anfall: Rykkninger eller prikking i en kroppsdel, noen ganger med sviktende bevissthet –
- Generalisert tonisk-klonisk anfall (tidligere “Grand Mal”): Fall, stivhet, rytmisk rykning i hele kroppen, bevisstløshet
Hvor vanlig er epilepsi?
Epilepsi rammer globalt omtrent 50 millioner mennesker, det er omtrent 1 % av verdens befolkning. I Tyskland lever rundt 400 000–500 000 mennesker med epilepsi. Det er den tredje vanligste nevrologiske sykdommen, etter migrene og hjerneslag.
Det store problemet
Ved omtrent 30 % der pasienten Hvis medisinene ikke virker tilstrekkelig, snakker man om medikamentresistent epilepsi. Disse menneskene ser ofte etter supplerende muligheter.
Det som skjer i hjernen ved epilepsi er plutselige, ukontrollerte elektriske utladninger i en gruppe hjerneceller. Disse utladningene kan spre seg til andre deler av hjernen og forstyrre normal hjerneaktivitet. Dette kan føre til anfall, som kan variere fra kortvarige forstyrrelser i bevissthet eller atferd til kraftige muskelsammentrekninger.
To systemer må være i balanse:
- GABA (Gamma-aminosmørsyre): “Bremseren”, beroliger hjernen
- Glutamat: “Gasspedalen” som aktiverer hjernen
Ved epilepsi er balansen forstyrret: for lite brems, for mye gass, hjernen “går i spinn”.
Dessuten spiller ionekanaler en viktig rolle, det er små “porter” i nervecellemembranene:
- Natriumkanaler (Nav)
Åpner seg, når en nervecelle fyrer, ved epilepsi åpner de seg for lett - Kalsiumkanaler (Cav)
Viktig for spesifikke anfallstyper (f.eks. absensanfall) - Kaliumkanaler (Kv)
Hjelp til å roe ned nevronet etter avfyring
Hvordan epilepsi vanligvis behandles
De viktigste antiepileptika (AEDs)
Valproat (Valproinsyre) er det viktigste bredspektrum-antiepileptikum. Det virker på flere måter samtidig og virker spesielt godt ved generaliserte epilepsier ved å bremse natrium- og kalsiumkanaler, og øke GABA.
Viktig advarsel:
Valproat er sterkt skadelig for ufødte barn, kvinner i fertil alder!
Karbamazepin og lamotrigin er “dørstoppere” for natriumkanaler. De hindrer nervecellene i å avfyre for lett. De to legemidlene utgjør førstelinjebehandlingen for fokale anfall. Lamotrigin er spesielt godt tolerert og trygt under graviditet
Levetiracetam (Keppra) har en unik virkningsmekanisme, da den binder seg til et protein (SV2A) som regulerer signaloverføringen mellom nerveceller. Den kjennetegnes ved svært god toleranse og har ingen interaksjoner med andre medisiner. Mulige bivirkninger er humørsvingninger og irritabilitet.
Topiramat virker på fire forskjellige måter samtidig, liksom et “multitalent”, som oppnår en høy prosentandel av anfallsfrihet på 44–83 % av pasientene. Som bivirkning kan nedsatt tenkning, samt ordsøkevansker, forekomme.
Ethosuksimid brukes ved absenser (korte “bortfall”). Det blokkerer spesifikke kalsiumkanaler i thalamus (et relésenter i hjernen).
Fenobarbital og benzodiazepiner forsterker GABA-effekten (“bremsen”). De er rimelige, effektive, men har sedativ- og avhengighetspotensial (benzodiazepiner).
Eteriske oljer ved epilepsi – hva er mulig?
Ved epilepsi må det utvises spesiell forsiktighet!
Noen eteriske oljer kan utløse eller forverre anfall (prokonvulsive). Snakk ALLTID med nevrologen din før du bruker eteriske oljer.
Oljer du bør UNNGÅ ved epilepsi:
- Rosmarin (i høye doser – kamferinnhold)
- Eukalyptus (i høye doser)
- Peppermynte (Pulegoninnhold)
- Fennikel (Fennikel i høye doser)
- Salvie (Tujon-innhold)
- Kamfer (direkte krampeutløsende)
Hvilke eteriske oljer viser antikonvulsive egenskaper?
Lavendel – beroligende og anfallshemmende
Lavendel (Lavandula angustifolia) er den best studerte oljen for epilepsi.
Sammensetning
– Linalool (25–45 %)
– Linalylacetat (25–50 %)
Effekt
– Aktiverer GABA-A-reseptoren (hjernens “bremse”)
– Hemmer natriumkanaler (forhindrer ukontrollert avfyring)
– Reduser anfallsterskelen
Kliniske effekter
– Linalool forlenget i dyreforsøk tiden til det første anfallet i PTZ-modellen (standardmodell for anfallstester) signifikant
– Noen pasienter rapporterer at lavendel-aromaterapi forsinker anfall eller lindrer auraer (forvarsler).
– Brukes i aromadiffusor via inhalering, men aldri internt uten legehjelp
Rosmarin/Borneol – nevrobeskyttende (med forsiktighet!)
Borneol er et virkestoff fra rosmarin og andre planter.
Effekt
Beskytter nerveceller mot skader fra gjentatte anfall; GABAerg og nevrobeskyttende
– Borneol reduserte anfallssjansen i «kindling»-modellen og senket inflammatoriske markører (GFAP) i dyreforsøk
Hør etter! Rosmarinolje som helhet kan være prokonvulsiv i høye doser, bare innta isolert borneol eller svært lave doser
Oregano – karvakrol og tymol
Karbakrol (fra Oregano og Timian) viser interessante antikonvulsive egenskaper.
Effekt
– Hemmer natriumkanaler (som karbamazepin)
– Modulerer TRPV1-reseptoren (varme- og smertereseptorer)
– Redusert anfallsvarighet og alvorlighetsgrad i dyreforsøk
Eukalyptus – 1,8-Cineol (med forsiktighet!)
1,8-kinol ekstrakt fra eukalyptus har antikonvulsiv effekt i dyremodeller.
Effekt
– Påvirker NO-systemet (nitrogenoksid) i hjernen
– Øker anfallsterskelen (~25 mg/kg vs. ~10 mg/kg i kontrollgruppen)
– Aktiverer Nrf2 (antioksidant beskyttelsesfaktor)
- Hør etter! I høye doser prokonvulsivt, kun i små mengder og etter samråd med lege
Kamille – Apigenin og synergier
Kamille (Matricaria chamomilla) inneholder apigenin, et flavonoid med angstdempende og krampestillende egenskaper.
Effekt
– Apigenin binder seg til GABA-A-reseptoren (på samme sted som benzodiazepiner, men mye svakere)
– Ny studie (2025): Kombinasjon av oregano + kamille + lavendel (administrert intranasalt) viste synergistisk antikonvulsiv effekt i dyremodell – bedre enn hver enkelt olje alene
- Som tillegg ved lette anfall eller for angstreduksjon
β-Caryophyllen – betennelsesdemperen
β-karyofyllen (BCP) finnes i svart pepper, lavendel, rosmarin og cannabis.
Effekt
– Aktiverer CB2-reseptorene (cannabinoid-reseptorene) uten psykoaktiv virkning
– Hemmer NF-κB (inflammasjonsbryteren)
– Reduserer nevroinflammasjon, viktig fordi betennelse kan forverre epilepsi
– BCP er også i hampolje og kan være en del av effekten av CBD-rike ekstrakter
Den viktigste planten Cannabis og CBD
CBD (Cannabidiol) – det kliniske gjennombruddet
CBD er et virkestoff fra cannabisplanten (Cannabis sativa), men uten den kjente psykoaktive effekten av THC. Det er det eneste plantebaserte antiepileptiske middelet som offisielt er godkjent av FDA (USA) og EMA (Europa) under navnet Epidiolex ble godkjent.
Det gis som et reseptbelagt legemiddel (Epidiolex) i form av en oljeoppløsning 2 ganger daglig oralt.
Effekt
– Hemmer natriumkanaler (som karbamazepin)
– Modulerer TRPV1 og GPR55 (spesifikke reseptorer)
- Betennelsesdempende via CB2-reseptorer - Beskytter nerveceller
Bivirkninger
– Søvnighet, diaré, redusert matlyst
– Kan speil av andre antiepileptika (spesielt klobazam) øke, dosejustering nødvendig
Autorisasjon for:
- Dravet syndrom – En alvorlig epilepsi form som starter i spedbarnsalderen
- Lennox-Gastaut syndrom (LGS) – Alvorlig epilepsi med flere anfallstyper
Studier
– Ved Dravet syndrom: CBD reduserte anfallsfrekvensen med 38,9 % vs. 13,3 % med placebo, 66,7 % der pasienten hatten ≥ 50 % færre anfall (p = 0,009)
– Ved LGS: Reduksjon av falltilfeller med 43,9 % vs. 21,8 % med placebo (p < 0,001)
– Ved annen farmakoresistent epilepsi: Ulike studier viser 40–50 % anfallsreduksjon
Sammenligningstabell – Hva hjelper hvordan?
Sikkerhetsregel
Muligens nyttig (etter samråd med lege):
- Lavendel-aromaterapi (diffusor, inhalasjon) – avslappende, muligens anfallsreduserende
- CBD (som Epidiolex) – for Dravet/LGS, reseptbelagt
- β-Karyofyllen – betennelsesdempende, godt tolerert
- Kamille – beroligende, angstdempende
Ved epilepsi UNNGÅ:
- Rosmarinolje (pur, høye doser) – Kamfer kan utløse kramper
- Eukalyptusolje (høye doser)
- Peppermynteolje (høye doser, pulegon)
- Fennikelolje Fennikel
- Salvieolje (Thujon)
- Kamferolje (direkte krampeutløsende)
Generelle sikkerhetsinstruksjoner
- Snakk ALLTID først med nevrologen – Epilepsi er alvorlig
- Antiepileptika må aldri seponeres på eget initiativ – kan føre til livstruende status epilepticus
- Vær oppmerksom på interaksjoner: Noen oljer kan endre nivået av antiepileptika.
- Bare ikke mot huden – alltid fortynne
- Barn: Spesiell forsiktighet, doser mye lavere
Ofte stilte spørsmål
Kan jeg ta lavendel i stedet for medisinene mine mot epilepsi?
Nei, absolutt ikke! Lavendel har kun vist krampestillende effekt i dyreforsøk. Å kutte ut antiepileptika på eget initiativ kan være livsfarlig.
Hva med CBD-olje fra Internett?
CBD-produkter fra internett er ikke det samme som det godkjente legemiddelet Epidiolex. De er ikke standardiserte, kan inneholde andre cannabinoider og har ingen påvist effekt. Snakk med nevrologen din om reseptpliktig CBD.
Kan aromaterapi stoppe et anfall?
Det finnes rapporter om at noen pasienter kan forsinke anfall med visse lukter (som lavendel), men det er ingen pålitelig metode og ingen erstatning for medisiner.
Er eteriske oljer trygge for barn med epilepsi?
Bare etter uttrykkelig konsultasjon med barne nevrolog. Barn reagerer mer følsomt, og noen oljer kan være farlige for barn.
Må jeg kjøpe dyre oljer?
Kvalitet er viktig: Se etter 100 % naturrene eteriske oljer, helst med analysebevis for hvert parti (GC/MS).
Billige parfymeoljer eller syntetiske duftstoffer har ingen terapeutisk virkning og kan på grunn av de syntetiske ingrediensene være helsefarlige og forårsake hodepine, kvalme osv.
De som ønsker å lære mer om utvalget og kvaliteten på eteriske oljer, vil finne det i innlegget „Eteriske oljer – En søkenodyssé“funnet.
Et ytterligere bidrag siterer Prof. Dr. Dr. Dr. med. habil. Hanns Hatt fra Ruhr-Universität Bochum, som i sin video „Helbredelse med dufter“på en interessant, underholdende og likevel vitenskapelig måte forklarer effekten av eteriske oljer på menneskekroppen.
Her er en oppsummering i tre setninger. Sammenfatningen er en kortfattet presentasjon av hovedpunktene i en lengre tekst. Den lar leseren raskt få oversikt over innholdet uten å måtte lese hele originalen. Formålet er å gi en konsis og informativ gjengivelse av kjerneargumentene.
Epilepsi er en alvorlig nevrologisk sykdom der elektriske stormer i hjernen forårsaker anfall, og hos 30 % av pasientene hjelper standardmedisiner ikke tilstrekkelig.
Eteriske oljer og terpener, spesielt linalool (lavendel), borneol og karvakrol, viser antikonvulsive egenskaper i dyreforsøk via GABA-A-aktivering og natriumkanalblokkering; CBD (cannabidiol) er det eneste plantebaserte antiepileptikumet med klinisk godkjenning (Dravet-syndrom, Lennox-Gastaut-syndrom).
Eteriske oljer kan brukes som et supplement til epilepsi, men bare etter uttrykkelig samråd med den behandlende nevrologen, da noen oljer også kan utløse anfall.
Denne teksten er basert på den vitenskapelige rapporten “Epilepsy and Essential Oils: Pharmacology, Mechanisms of Action and Complementary Therapeutic Approaches” og er kun ment som generell informasjon. Epilepsi er en alvorlig tilstand, og du bør alltid rådføre deg med nevrologen din hvis du har spørsmål om behandling.
Anbefalte dōTERRA-Produkter for tilleggsbehandling av epilepsi
Potensielt trygge produkter (basert på forskning)
Olje som bør unngås ved epilepsi
Egne oljeblandinger (DIY-blandinger)
Blanding 1 – “Nevrobeskyttende” (Diffusor)
Målet: Nevrobeskyttende beskyttelse, GABA-modulering
Søknad: 30 minutter daglig i diffusoren, spesielt om kvelden
Blend 2 – “Aura-Management” (Topisk, raskt)
Målet: Ved auru-symptomer: forsøk å stanse anfallet (KUN som tillegg, ikke som erstatning for nødmedisinering)
Søknad: På tinningene, nakken, håndleddene – umiddelbart ved begynnende aura
Nødmedisin (f.eks. diazepam rektal) forblir prioritert
Blend 3 – “Angst & Stressreduksjon” (Diffusor/Topisk)
Målet: Stress ↓ (hyppigere anfallstrigger), avspenning ↑
Søknad: Ved stress eller før kjente triggersituasjoner
Blend 4 – “Søvn og hvile” (Kveld)
Målet: Søvnkvalitet ↑ (Søvnmangel = anfallstrigger)
Søknad: I diffusoren, 30 minutter før sengetid
Blanding 5 – “Betennelsesdemping” (lokal)
Målet: Nevroinflammasjon ↓ (Epilepsipatofysiologi)
Søknad: Massasje på tinning, nakke og ryggrad
Applikasjonsprotokoll – 4-ukers plan
Uke 1 – Forsiktig start
- Konsultere lege FØR man starter med oljer
- Om kvelden Bland 4 i diffusoren (sove)
- Daglig Bland 1 i diffusoren (30 min
- Anfallsprotokoll kjøre (Dato, Tid, Utløser)
Uke 2 – Utvidelse
- Morgen: Bland 3 ved stressituasjoner
- Om kvelden Blanding 4 (Søvn) + Blanding 5 topisk
- Blanding 2: Være forberedt på Aura-situasjoner
Uke 3-4 – Optimalisering
- Vurder anfallsprotokoll – har noe endret seg?
- Legen informerer nevrologen om oljebruk
- Tilpasning basert på individuell toleranse
Kombinasjon med andre dōTERRA-Produktene
Nødplan ved anfall
- Sikkerhet Person i sideleie
- Måle tid: Anfall lenger enn 5 minutter → Legebil (112)
- Nødsituasjonsmedisinering Diazepam-rektal / Midazolam-nesespray (som forskrevet av lege)
- INGEN olje i munn eller nese under et aktivt anfall
- Eteriske oljer er IKKE nødmedisin
Epilepsi og eteriske oljer – farmakologi, virkningsmekanismer og komplementære terapeutiske tilnærminger
En omfattende vitenskapelig rapport om standard antiepileptika, terpener og eteriske oljer – molekylære grunnlag, klinisk evidens og adjuverende terapistrategier
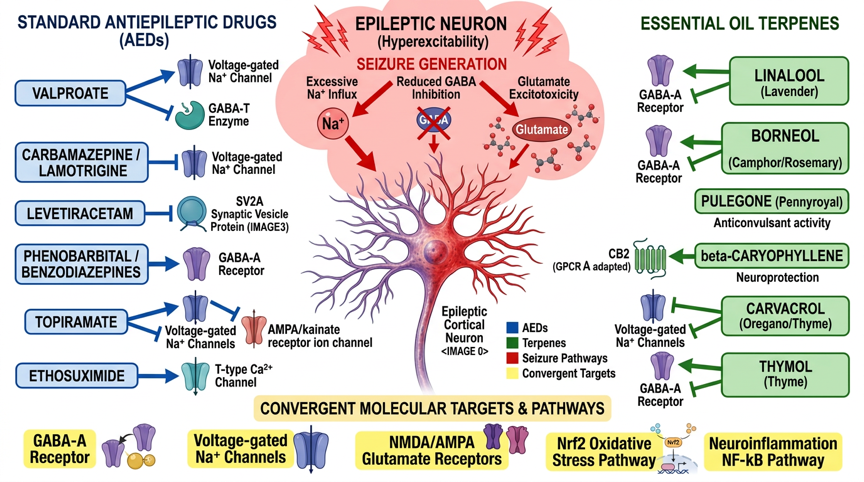
Abb. 1: Molekylære signalveier for standard antiepileptika og eteriske oljer ved epilepsi – Standard-AEDs (Valproat/Nav+GABA-T, Karbamazepin/Nav, Levetiracetam/SV2A, Topiramat/multimodal, Etosukksimid/T-type-Ca2+, Fenobarbital/GABA-A) og terpener (Linalool/GABA-A+Nav, Borneol/GABA-A+Nav, Karvakrol/Nav+TRPV1, β-Caryophyllen/CB2, 1,8-Cineol/NO+Nrf2) med konvergente målmmolekyyler (GABA-A-reseptor, Nav-kanaler, NMDA/AMPA-glutamat, NF-κB-nevroinflammasjon, Nrf2-oksidativt stress)
Overst: Sharp Wave (70-200 ms) med påfølgende Slow Wave.
3-Hz spike-wave-kompleks (GSWD) – Kardinaltegn på absensepilepsi.
Nedenfor: Polyspike-kompleks (3-5 pigger, 4-5 Hz) – karakteristisk for juvenil myoklonisk epilepsi (JME).
Innledning
Epilepsi er en av de vanligste kroniske nevrologiske lidelsene på verdensbasis og rammer anslagsvis 50 millioner mennesker, omtrent 1 % av verdens befolkning [D1]. Den er definert ved en vedvarende predisposisjon for epileptiske anfall som følge av patologisk synkroniserte nevrale utladninger, samt de nevrobiologiske, kognitive, psykologiske og sosiale konsekvensene av denne sykdommen. [D2]. Til tross for betydelige fremskritt i utviklingen av antiepileptika (AEDs) forblir farmakoresistent epilepsi hos omtrent 30 % av pasientene, der to eller flere adekvat brukte AEDs ikke gir tilstrekkelig anfallskontroll [D3].
Standardbehandlingen av epilepsi inkluderer en trinnvis farmakoterapi med antiepileptika av første, andre og tredje generasjon. Valproat, karbamazepin og lamotrigin regnes som førstelinjemidler ved fokale og generaliserte epilepsier; nyere substanser som levetiracetam, topiramat, lakosamid og perampanel utvider det terapeutiske arsenalet [D4]. Til tross for sin effektivitet er AEDer forbundet med betydelige bivirkninger, kognitive svekkelser, teratogenitet (valproat), benmargsdepresjon (karbamazepin), vektøkning og psykiske lidelser, som betydelig påvirker pasientenes livskvalitet. [D5].
I lys av dette øker den vitenskapelige interessen for plantevirkningsstoffer og eteriske oljer som komplementære eller alternative behandlingsmuligheter. Tallrike terpener og bioaktive forbindelser viser antikonvulsive, nevrobeskyttende, anti-nevroinflammatoriske og antioksidative egenskaper i prekliniske og kliniske studier, ofte via mekanismer som komplementerer klassiske antiepileptika. [D6]. Kannabidiol (CBD) har som en plantebasert aktiv ingrediens fra Cannabis sativa allerede oppnådd kliniske godkjenninger for spesifikke epilepsisyndromer og demonstrerer potensialet til botaniske forbindelser i epilepsibehandling. [D7]. Denne rapporten analyserer systematisk farmakologien til standard antiepileptika, de molekylære virkningsmekanismene til relevante eteriske oljer og terpener, samt tilgjengelig klinisk evidens for deres bruk som tilleggsbehandling ved epilepsi.
EEG ved epilepsi – grunnlag og tolkningsprinsipper
Elektroencefalogram (EEG) er det sentrale diagnostiske verktøyet ved epilepsi og muliggjør direkte måling av kortikal elektrisk aktivitet via elektrodder på hodet. Det brukes til klassifisering av anfall, lokalisering av ursprung og monitorering av behandling.
Interiktal fase: EEG mellom anfallene viser typisk interiktale epileptiforme utladninger (IEDs): spikes (<70 ms), skarpe bølger (70-200 ms) og 3-Hz spike-wave-komplekser (GSWDs ved absens-epilepsi). Disse IEDs oppstår fra synkrone nevronale utladninger i den epileptiske fokusen.
Iktal fase: Anfalls-EEG begynner ofte med lavvolts rask aktivitet (LVFA, 20-35 Hz) som startmønster. Over tid utvikles en rytmisk theta-delta-evolusjon med økende amplitude. Avslutningen skjer brått med påfølgende postiktal undertrykkelse.
Postiktal fase: Etter at anfallet er avsluttet, viser EEG-en en supprimering (markert reduksjon i amplitude) etterfulgt av diffus delta-sakning (0,5-3,5 Hz). Gjenoppretting til normal bakgrunnsaktivitet skjer i løpet av minutter til timer, avhengig av anfallslengde og -type.
Effekten av β-Caryophyllen på epilepsi-EEG: β-Caryophyllen (BCP), en sesquiterpenoid CB2-agonist fra eteriske oljer (f.eks. svart pepper, nellik), reduserer anfallshyppigheten med 66%i PTZ-modellen, øker anfallslatensen med 187%og senker spike-frekvensen med 27-68% . I EEG vises en normalisering av spektral effekt: Gammastyrke (hypereritabillitetsmarkør) synker, deltastyrke øker. Virkningsmekanismen inkluderer CB2-agonisme (nevroinflammasjon synker) og GABA-A-modulering (kloridinnstrømning øker).
Patofysiologi for epilepsi
Nevral hyper eksitabilitet og synkronisering
Den fundamentale patofysiologien ved epilepsi hviler på en ubalanse mellom eksitatorisk og inhibitorisk nevrotransmisjon, som fører til paroksysmal synkronisert nevronal utladning. På cellenivå oppstår et epileptisk anfall gjennom samspillet mellom ionekanal-dysfunksjoner, svekket synaptisk transmisjon og endret nettverksaktivitet. [D8]. Mutasjoner eller funksjonelle endringer i spenningsstyrte natrium- (Nav), kalium- (Kv) og kalsiumkanaler (Cav), samt i ligandstyrte ionekanaler (GABA-A, NMDA), bidrar til økt nevronal eksitabilitet. [D9].
Ovenfor (blå): Interiktal fase med IED-er (spikes <70 ms, skarpe bølger 70-200 ms, 3-Hz GSWD-er).
Midt (rot): Ikral fase – LVFA-onset (20-35 Hz), theta-delta-evolusjon, brå avslutning.
Nedenfor (lilla): Postiktal fase – EEG-suppresjon, diffus deltaseinkelse (0,5–3,5 Hz)
GABA/Glutamat-ubalanse
Balansen mellom den hemmende nevrotransmitteren GABA (gamma-aminosmørsyre) og den eksitatoriske nevrotransmitteren glutamat er avgjørende for krampetærskelen. Redusert GABAerg inhibisjon, forårsaket av redusert GABA-syntese, redusert tetthet av GABA-A-reseptorer eller økt aktivitet av GABA-transaminase, senker krampetærskelen. [D10]. Samtidig fremmer overdreven aktivering av NMDA- og AMPA-glutamatreseptorer depolarisasjonsspredning og epileptiske utladninger. Denne GABA/glutamat-ubalansen er det sentrale farmakologiske angrepsmålet for de fleste AED-er. [D11].
Ionekanal-dysfunksjon
Spenningsstyrte natriumkanaler (Nav1.1, Nav1.2, Nav1.6) spiller en nøkkelrolle i generering og spredning av aksjonspotensialer. Gain-of-function-mutasjoner i Nav1.1 (Dravet-syndrom) eller Nav1.2 fører til ukontrollerte utladninger [D12]. T-type kalsiumkanaler (Cav3.1, Cav3.2) er sentrale ved absensepilepsier: Deres rytmiske aktivering i thalamus genererer de karakteristiske 3-Hz spike-wave-utladningene [D13]. Kaliumkanaldefekter (KCNQ2/3, KCNT1) påvirker repolariseringen og øker disposisjonen for anfall.
Nevroinflammasjon og oksidativt stress
Kronisk epilepsi er assosiert med vedvarende nevroinflammasjon: Aktiverte mikroglia og astrocyter frigjør proinflammatoriske cytokiner (IL-1β, IL-6, TNF-α), som destabiliserer blod-hjerne-barrieren og øker nevronal eksitabilitet [D14]. Transkripsjonsfaktoren som NF-κB koordinerer denne nevroinflammatoriske kaskaden. Samtidig fører repetitive anfall til oksidativt stress gjennom mitokondriell dysfunksjon og ROS-produksjon, noe som fremmer nevronal apoptose og hippocampussklerose. [D15]. Nrf2-signalveien, som er hovedregulatoren av den antioksidative responsen, er ofte undertrykt ved farmakoresistent epilepsi.
Farmakoresistensmekanismer
Bei 30 % der Epilepsiepatienten versagen zwei oder mehr AEDs. Pharmakoresistenz entsteht durch: (1) Überexpression von P-Glykoprotein (P-gp/MDR1) und anderen ABC-Transportern, die AEDs aus dem Gehirn effluxieren; (2) Veränderungen der AED-Zielstrukturen (z. B. Nav-Kanal-Mutationen, die die Phenytoin-Bindung verringern); (3) pharmakogenetische Varianten im CYP-Metabolismus; (4) Neuroinflammation, die die Blut-Hirn-Schranken-Permeabilität verändert [D16].
Farmakologi av standard antiepileptika
Natriumkanalblokkere – Karbamazepin, Lamotrigin, Fenytoin, Lakosamid
Natriumkanalblokkere er den vanligste og eldste klassen av AEDer. De binder seg til den inaktiverte tilstanden til spenningsstyrte natriumkanaler (Nav1.1–Nav1.6) og forlenger deres inaktiveringstid, prinsippet om “use-dependent blockade”.” [D8]. KarBamazepin (CBZ) og okskarbazepin er førstelinjebehandling ved fokale epilepsier; lamotrigin hemmer i tillegg den presynaptiske frigjøringen av glutamat og er spesielt effektivt ved Lennox-Gastaut syndrom og absens-epilepsi [D17]. Fenytoin/Fosfenytoin stabiliserer den inaktiverte tilstanden til Nav-kanalen og er et standardmedikament ved status epilepticus. Lakosamid (nyere generasjon) forsterker den “langsomme inaktiveringen” av Nav-kanaler via en unik mekanisme og viser gunstig farmakokinetikk. [D18].
Klinisk effekt: Karbamazepin oppnår anfallsfrihet hos 40–50 % av pasientene som monoterapi for fokale epilepsier; lamotrigin viser sammenlignbar effekt med en bedre toleranseprofil, spesielt hos kvinner i fertil alder. [D4].
Valproat – Bredspektret antiepileptikum
Valproinsyre (valproat/VPA) er det viktigste bredspektrede antiepileptikumet med multiple virkningsmekanismer: hemming av spenningsstyrte natriumkanaler, reduksjon av T-type kalsiumstrømmer, hemming av GABA-transaminase (GABA-T) med påfølgende økning av GABA, samt aktivering av glutamat-dekarboksylase (GAD) [D19]. Valproat er førstelinjebehandling ved generaliserte epilepsier (juvenil myoklonisk epilepsi, absensepilepsi, Lennox-Gastaut) og oppnår anfallsfrihet hos 50–70 % av pasientene med idiopatisk generalisert epilepsi [D4]. Kritisk: Valproat er sterkt teratogent (nevralrørsdefekter, kognitive svekkelser hos nyfødte) og bør kun brukes hos kvinner i fertil alder etter en nøye nytte-risiko-vurdering. [D5].
Levetiracetam – SV2A-binding
Levetiracetam (LEV) har en unik virkningsmekanisme: Det binder selektivt til det synaptiske vesikkelproteinet 2A (SV2A), som regulerer nevrotransmitter-eksocytose [D20]. Gjennom SV2A-binding reduserer LEV den presynaptiske nevrotransmitterfrisettingen ved høyfrekvente utladninger, en “frekvensavhengig” mekanisme som knapt påvirker normal synaptisk transmisjon. LEV er førstelinjebehandling for fokale og generaliserte epilepsier, viser utmerket farmakokinetikk (ingen enzyminduksjon, ingen proteinbinding) og er relativt trygg under graviditet. [D20]. Viktig bivirkning: Atferdsendringer (irritabilitet, depresjon) hos opptil 15 % av pasientene.
Topiramat – Multimodal mekanisme
Topiramat (TPM) er et multivalens medikament for epileptiske anfall med minst fire virkningsmekanismer:
- Blokkering av spenningsavhengige natriumkanaler,
- Forsterkning av GABAerg hemming ved GABA-A-reseptorer
- Antagonisme ved AMPA/kainat-glutamatreseptorer
- Hemming av karboanhydrase (CA-II, CA-IV) [D21]
Kliniske studier viser anfallsfrihetsrater på 44–83 % (6–7 måneder) og 41–76 % (12–13 måneder) i monoterapi-sammenligningsstudier; topiramat er tilsvarende effektivt som valproat og karbamazepin [D21]. Viktige bivirkninger: kognitive svekkelser (“ord-finne vansker”), vekttap, nyrestein.
GABA-A-modulatoren – Fenobarbital, Benzodiazepin, Vigabatrin
Fenobarbital (barbiturat) og benzodiazepiner (diazepam, klonazepam, klobazam) forsterker GABA-A-reseptor-mediert kloridhemming: barbiturater forlenger åpningstiden til kloridkanalen, benzodiazepiner øker åpningsfrekvensen [D22]. Fenbobarbital er et av de eldste og billigste antiepileptika, brukes ofte i utviklingsland, men har betydelig sederende potensial. Vigabatrin hemmer irreversibelt GABA-transaminase (GABA-T) og øker dermed GABA-konsentrasjonen i hjernen; det er effektivt mot infantile spasmer, men er forbundet med irreversible synsfeltutfall. [D23].
Etosuksimid – T-type kalsiumkanalblokker
Ethosuximid (ESM) er en selektiv blokker av T-type kalsiumkanaler (Cav3.1/3.2) og førstelinjebehandling for absensanfall hos barn. [D13]. T-type-kanaler genererer de rytmiske thalamiske utladningene som kjennetegner absensanfall; deres blokkering avbryter denne syklusen effektivt. Etosuksimid er sammenlignbart effektivt med valproat ved absensepilepsi (beslagsfrihet ~50–60 %), men har færre bivirkninger [D13].
Nyere AE-midler – Lacosamid, Perampanel, Brivaracetam
Lacosamid (LCM) forsterker selektiv den “langsomme inaktiveringen” av spenningsstyrte natriumkanaler og hemmer Collapsin-Response-Mediator-Protein 2 (CRMP-2). [D18]. Perampanel (PER) er den første selektive, ikke-kompetitive AMPA-glutamatreseptorantagonisten og er spesielt effektiv ved farmakoresistente generaliserte tonisk-kloniske anfall. [D24]. Brivaracetam (BRV) binder seg, i likhet med levetiracetam, til SV2A, men med 10 ganger høyere affinitet og raskere innsettende effekt [D25].
Eteriske oljer som adjuvant terapi – Mekanistiske grunnlag
Farmakokinetikk og CNS-penetrering
Terpener fra eteriske oljer kjennetegnes ved høy lipofilitet og lav molekylmasse (< 300 Da), noe som muliggjør effektiv penetrasjon av blod-hjerne-barrieren (BBB). [D26]. Ved inhalasjon transporteres flyktige terpener via lukteslimhinnen direkte til luktelappen og det limbiske system, en direkte vei som omgår blod-hjerne-barrieren og fører til målbare CNS-konsentrasjoner innen minutter. [D27]. Transdermal og oral administrasjon muliggjør systemisk absorpsjon; oral biotilgjengelighet varierer sterkt avhengig av terpen og formulering.
Antikonvulsive grunnmekanismer
Eteriske oljer og deres terpener kan virke gjennom flere antikonvulsive mekanismer som overlapper med de til klassiske AED-er:
- Modulering av spenningsstyrte natriumkanaler (Linalool, Borneol, Carvacrol, Thymol)
- Forsterkning av GABAerg hemming på GABA-A-reseptorer (Linalool, Borneol, Tymol, Apigenin)
- Hemming av glutamaterg eksitasjon ved NMDA/AMPA-reseptorer
- Antioksidativ nevrobeskyttelse via Nrf2-aktivering; (5) Anti-nevroinflammatorisk effekt via NF-κB-hemming (β-karyofyllen) [D28].
Nevrobeskyttende egenskaper
Mange terpener viser nevrobeskyttende egenskaper som går utover den direkte antikonvulsive effekten. Ved å hemme apoptose-signalveier (caspase-3, Bax/Bcl-2-forhold), redusere lipidperoksidasjon (MDA-nivå) og øke antioksidante enzymaktiviteter (SOD, CAT, GPx) beskytter terpener mot anfallsrelatert nevronal skade. [D29]. Disse nevrobeskyttende egenskapene er spesielt relevante ved farmakoresistent epilepsi, der repeterende anfall fører til progressiv hjerneskade.
Komplementære virkningsmekanismer til standard antiepileptika
Den følgende tabellen viser de komplementære virkningsmekanismene til eteriske oljer sammenlignet med standard antiepileptiske legemidler på molekylært nivå:

Standard-AEDer (Valproat/Nav+GABA-T, Karbamazepin/Nav, Levetiracetam/SV2A, Topiramat/multimodal, Etosuksimid/T-type-Ca²⁺, Fenobarbital/GABA-A) og terpener (Linalool/GABA-A+Nav, Borneol/GABA-A+Nav, Karvakrol/Nav+TRPV1, β-Caryofyllen/CB2, 1,8-Cineol/NO+Nrf2) med konvergente målmolekyler (GABA-A, Nav, NMDA/AMPA, NF-κB, Nrf2/ARE).
Spesifikke eteriske oljer og kliniske bevis
Lavendelolje (Lavandula angustifolia) – Linalool
Lavendelolje er den mest undersøkte eteriske oljen i forbindelse med nevrologiske sykdommer. Hovedbestanddelen linalool (25–45 %) viser antikonvulsive egenskaper i prekliniske studier: I en pentylentetrazolmodell (PTZ) økte inhalering av linalool anfallsterskelen, forlenget latenstiden til det første anfallet og reduserte anfallstiden [D30]. Mekanistisk hemmer linalool spenningsstyrte natriumkanaler ved å øke terskelverdien for aksjonspotensialet og redusere hastigheten på oppadgående fase, samt ved å modulere kalsiumaktiverte kaliumstrømmer [D31]. En pilotstudie om lukttrening hos epilepsipasienter (n=11) brukte lavendel som luktkondisjoneringsstimulus og viste anfallsreduksjon på ≥ 50 %hos 6 av 11 pasienter, der forfatterne pekte på det begrensede datagrunnlaget [D32].
I en studie med flere eteriske oljer i en PTZ-musemodell viste Lavandula angustifolia en signifikant forlengelse av anfallslatenstiden (p < 0,05) og reduksjon av anfallsskylden sammenlignet med kontrollgruppen [D33]. Silexan (80 mg oral, standardisert lavendelextrakt) er klinisk validert for angstlidelser og kan brukes som et tilleggsmiddel ved epilepsirelatert angst. [D34].
Cannabisolje / Cannabidiol (CBD)
Cannabidiol (CBD) er den mest kjente planteaktive substansen med klinisk dokumentert antikonvulsiv effekt. Som et ikke-psykoaktivt fytocannabinoid fra Cannabis sativa har CBD flere antikonvulsive mekanismer: Antagonisme ved GPR55 (lyso-fosfatidylinositol-reseptor), modulering av TRPV1-kanaler, hemming av spenningsstyrte natriumkanaler og modulering av endocannabinoid-systemet. [D35]. Farmasøytisk CBD (Epidiolex®) er godkjent av FDA (2018) og EMA (2019) for Dravet syndrom og Lennox-Gastaut syndrom [D7].
Kliniske bevis: I placebokontrollerte fase III-studier ved Dravet syndrom (n=120) reduserte CBD (20 mg/kg/dag) den månedlige forekomsten av konvulsive anfall med 38,9 % mot 13,3 % med placebo (p = 0,01) [D7]. Ved Lennox-Gastaut syndrom (n=225) reduserte CBD stupanfall med 43,9 % vs. 21,8 % under placebo (p < 0,001) [D36]. I en trippelblindstudie på refraktær frontallappsepilepsi (n=27) viste 66,7 % av CBD-pasientene bedring etter 4 uker vs. 20,0 % under placebo (gjennomsnittlig forskjell 45,58; 95 % KI: 8,99–82,18; p = 0,009) [D37].
Rosmarinolje (Rosmarinus officinalis) – Borneol, 1,8-Cineol
Rosmarinolje inneholder borneol (opptil 20 %), 1,8-cineol/eukalyptol (35–50 %), kamfer (10–20 %) og α-pinen [D38]. Borneol viser antiepileptogene effekter i en PTZ-kvippemodell: Det reduserer anfallsprogresjon, senker GFAP-markører (nevroinflammasjon) i hippocampus, reduserer oksidativt stress og modulerer GABAerg transmisjon. [D39]. 1,8-cineol økte anfallsterskelen i en PTZ-terskeltest (~25 mg/kg vs. ~10 mg/kg i kontroll) og reduserte malondialdehyd-(MDA)-nivåer som en markør for oksidativt stress [D40]. I PTZ poly-olje-studien viste Rosmarinus officinalis en signifikant forlengelse av anfallslatenstiden og reduksjon av anfallsskylden [D33].
Oregano-/timianolje – Karvakrol og tymol
Karvakrol (oregano, timian, bønneurt) og tymol (timian) er strukturelt beslektede monoterpenfenoler med påvist antikonvulsiv aktivitet. [D41]. Carvacrol hemmer spenningsensitive natriumkanaler (Nav1.2, Nav1.4) og TRPV1-kanaler, forsterker GABAergisk hemming og viser antikonvulsive effekter i PTZ- og kaininsyremodeller. [D42]. Tymol modulerer GABA-A-reseptoren positivt allosterisk (likt barbiturater) og hemmer spenningsstyrte natriumkanaler [D43]. Viktig begrensning: Origanum vulgare-olje viste toksiske effekter (100 % dødelighet) i en dyrestudie ved den testede konsentrasjonen, noe som understreker viktigheten av standardisert dosering og formulering [D33].
Eukalyptusolje (Eucalyptus globulus) – 1,8-Cineol
Eukalyptusolje inneholder 60–90 % 1,8-Cineol (eukalyptol), et monoterpenoksid med antikonvulsive, antiinflammatoriske og antioksidative egenskaper [D44]. 1,8-Cineol modulerer nitrogenoksid-(NO)-systemet, som spiller en kompleks, toveis rolle i anfallsregulering: Lave NO-nivåer kan være antikonvulsive, mens høye NO-nivåer kan være prokonvulsive. I en PTZ-modell økte 1,8-Cineol anfallsterskelen signifikant og reduserte lipidperoksidasjon [D40]. Eukalyptusoljeinhalasjon viser også anti-neuroinflammatoriske effekter gjennom NF-κB-hemming og reduksjon av proinflammatoriske cytokiner. [D45].
Røkelseolje (Boswellia sacra) – α-Pinen, Boswelliasyrer
Røkelsesolje inneholder α-pinen (opptil 75 %), limonen og ikke-flyktige boswelliasyrer [D46]. α-Pinen hemmer acetylkolinesterase og har angstdempende egenskaper; boswelliasyrer (AKBA) hemmer 5-lipoksygenase og NF-κB, noe som reduserer nevroinflammatoriske prosesser ved epilepsi. I dyremodeller viste Boswellia-ekstrakt nevrobeskyttende effekter etter kaininsyre-induserte anfall: reduksjon i tap av hippocampus-nevroner, nedsatt GFAP-ekspresjon og reduserte IL-1β-nivåer. [D47]. Incensolacetat fra frankincense aktiverer TRPV3-kanaler og viser angstdempende effekter uavhengig av GABA-A- eller opioidreseptorer.
Kamilleolje (Matricaria chamomilla) – Apigenin, α-Bisabolol
Kamilleolje inneholder α-Bisabolol (opptil 50 %), Chamazulen og flavonoïdet Apigenin [D48]. Apigenin binder seg til benzodiazepinbindingssetet på GABA-A-reseptoren (Ki = 4 µM) og viser anxiolytiske og krampestillende egenskaper uten sedasjon i prekliniske modeller. [D49]. I en synergistudium (2025) viste kombinasjonen av oregano, kamille og lavendel (intranasalt) signifikant antikonvulsiv aktivitet i PTZ-modellen, med markant reduksjon av anfallshyppighet (p < 0,05) og optimaliserte effekter med kombinerte lavere doser sammenlignet med enkeltstoffer [D50].
Fennikelolje (Foeniculum vulgare) – trans-Anetol
Fennikelolje inneholder trans-anethol (50–80 %), fenkon og estragol. Trans-anethol modulerer GABA-A-reseptorer og hemmer NMDA-glutamatreseptorer, noe som forklarer antikonvulsive effekter i dyremodeller [D28]. Imidlertid har fenkon (en bestanddel av fennikelolje) prokonvulsive egenskaper og kan utløse anfall, noe som understreker viktigheten av standardiserte, fenkon-fattige fennikeloljepreparater for terapeutiske anvendelser.
Molekylære virkningsmekanismer for terpener ved epilepsi
Linalool – Natriumkanalhemming og GABA-A-modulering
Linalool (3,7-dimetyl-1,6-oktadien-3-ol), hovedmonoterpenet i lavendel og koriander, viser doseavhengige effekter på nevronal eksitabilitet. I isolerte nevroner øker linalool terskelen for aksjonspotensialet og reduserer stigningshastigheten, begge indikatorer på natriumkanalhemming. [D31]. Samtidig aktiverer linalool kalsiumavhengige kaliumkanaler (BK-kanaler), som akselererer repolarisering og reduserer avfyringsfrekvensen. GABA-A-modulering av linalool øker kloridmediert inhibisjon [D30]. Viktig: Ved høye doser kan linalool virke paradoksalt stimulerende, noe som understreker viktigheten av optimal dosering.
Borneol – GABAerg modulering og nevrobeskyttelse
Borneol (2-Bornanol), en bisyklisk monoterpenalkohol fra kamfertre og rosmarin, viser antiepileptogene effekter i PTZ-kindling-modellen. Det modulerer GABAerg transmisjon, reduserer oksidativt stress (reduserte MDA-nivåer, økt SOD-aktivitet) og senker nevroinflammatoriske markører (GFAP) i hippocampus. [D39]. Borneol hemmet også spenningsavhengige natriumkanaler og viste synergistiske antikonvulsive effekter i kombinasjon med standard-AED-er i dyremodeller.
Carvacrol og tymol – Nav-kanal-blokade og GABA-A-modulering
Karvakrol (5-isopropyl-2-metylfenol) og tymol (2-isopropyl-5-metylfenol) er strukturisomere monoterpenfenoler med lignende, men ikke identiske virkningsmekanismer. Karvakrol hemmer Nav1.2- og Nav1.4-natriumkanaler samt TRPV1-kanaler og viser nevrobeskyttende effekter i kaininsyremodeller. [D42]. Tymol modulerer GABA-A-reseptoren positiv allosterisk ved et bindingssete som ligner på barbiturater, og hemmer spenningsstyrte natriumkanaler, en dobbel mekanisme som ligner på fenobarbital. [D43].
β-Caryophyllen – CB2-agonisme og anti-nevroinflammasjon
β-Caryophyllen (BCP), et syklisk sesquiterpen fra svart pepper og nellik, fungerer som en selektiv CB2-cannabinoidreseptoragonist og viser antikonvulsive og nevrobeskyttende effekter i dyremodeller. [D51]. De antikonvulsive effektene av BCP medieres delvis via GABAerge mekanismer, serotonerge og nitrergiske systemer. NF-κB-hemming av BCP reduserer nevroinflammatoriske prosesser som bidrar til epilepsi. I en musemodell reduserte BCP signifikant PTZ-indusert anfallshyppighet og viste nevrobeskyttende effekter i hippocampus. [D52].
e Effekter i PTZ-modellen og virkningsmekanisme
A: Kontroll – 3 anfall i 20 sek, høy spikereisefrekvens
B: BCP 200 mg/kg — 1 anfall (↓66 %), latens ↑187 %, spikes ↓68 %.
C: Spike-frekvensen dosavhengig (↓27–68 %).
Spektral effekt — Gammakraft ↓, Deltakraft ↑ (normalisering).
E: Virkningsmekanisme — BCP → CB2 (↓Nevroinflammasjon) + GABA-A (↑Chlorid-inntak → ↓Hypereksitabilitet).
1,8-Cineol – NO-system og antioksidativ nevrobeskyttelse
1,8-Cineol (Eukalyptol), det viktigste monoterpenet i eukalyptus- og rosmarinolje, modulerer nitrogenmonoksid-(NO)-systemet og viser antioksidant nevrobeskyttelse [D40]. I et PTZ-anfallforsøk økte 1,8-cineol signifikant anfallsterskelen (~25 mg/kg vs. ~10 mg/kg kontrollgruppe) og reduserte malondialdehyd (MDA)-nivåer som en markør for lipidperoksidasjon. I tillegg hemmer 1,8-cineol NF-κB-avhengige nevroinflammatoriske prosesser og aktiverer Nrf2-signalveien for antioksidativ nevrobeskyttelse.
Nye og supplementære eteriske oljer
Sitronmelisseolje (Melissa officinalis) Rosmarinsyre
Melisseolje inneholder rosmarinsyre, citral, citronellal og geraniol [D53]. Rosmarinsyre hemmer GABA-transaminase (GABA-T), den samme mekanismen som vigabatrin, og øker derved GABAerg hemming. I tillegg viser rosmarinsyre antioksidante og anti-neuroinflammatoriske egenskaper ved å hemme COX-2 og NF-κB. I dyremodeller viste sitronmelisseekstrakt antikonvulsive effekter ved PTZ-induserte anfall.
Peppermynteolje (Mentha piperita) – Mentol, Pulegon
Peppermynteolje inneholder mentol (30–55 %), menton (14–32 %) og pulegon (< 1 %). I PTZ-studien med flere oljer viste Mentha piperita ingen anfall og 100 %overlevelse ved den testede konsentrasjonen, med den beste sikkerhetsprofilen av alle de testede oljene [D33]. Mentol aktiverer TRPM8-kuldekanaler og modulerer natriumkanaler; det viser smertestillende og svakt krampestillende egenskaper. Viktig: Pulegon i høye konsentrasjoner er hepatotoksisk og prokonvulsivt.
Svartfrøolje (Nigella sativa) – Tymokinon
Svartfrøolje inneholder tymokinon (TQ, 30–48 %), som viser sterke antikonvulsive, nevrobeskyttende og anti-nevroinflammatoriske egenskaper [D54]. TQ hemmer NMDA-glutamatreseptoren, aktiverer GABA-A-reseptorer og viser i dyremodeller en effekt sammenlignbar med valproat mot PTZ-induserte anfall. TQ aktiverer Nrf2 og hemmer NF-κB, noe som reduserer oksidativt stress og nevroinflammasjon ved epilepsi.
Hampekstrakt – CBD og andre cannabinoider
I tillegg til farmasøytisk CBD inneholder Cannabis sativa andre krampeløsende cannabinoider: CBDV (Cannabidivarin) viser effekt i kliniske studier ved fokale anfall; THCV (Tetrahydrocannabivarin) har krampeløsende egenskaper i dyremodeller; CBG (Cannabigerol) viser nevrobeskyttende effekter [D55]. Entourage-effekten beskriver synergistiske virkninger mellom ulike cannabinoider og terpener i fullspektrum cannabis ekstrakt.
Kliniske bevis sammenlignet med standardbehandling
Randomiserte kontrollerte studier (RCT-er)
Den kliniske evidensen for eteriske oljer ved epilepsi er, med unntak av farmasøytisk CBD, overveiende preklinisk. CBD har demonstrert overbevisende effekt i flere fase III RCT-er ved Dravet syndrom og Lennox-Gastaut syndrom: reduksjon av konvulsive anfall med 38,9 % (Dravet, p = 0,01) og dropsanfall med 43,9 % (LGS, p < 0,001) [D7] [D36]. I en trippelblindstudie med refraktær epilepsi i frontallappen (n=27) viste CBD signifikant overlegenhet sammenlignet med placebo (66,7 % vs. 20,0 % respondere, p = 0,009) [D37].
Prekliniske dyremodeller
I en PTZ-musemodell med flere eteriske oljer (Lavandula angustifolia, Rosmarinus officinalis, Mentha piperita, Origanum majorana), viste alle de testede oljene (unntatt Origanum vulgare) en signifikant økning i anfallslatens og reduksjon i anfallets alvorlighetsgrad sammenlignet med kontrollgruppen (p < 0,05). [D33]. En synergistudie (2025) med kombinert intranasal påføring av oregano-, kamille- og lavendelolje viste synergistiske antikonvulsive effekter som oversteg summen av de individuelle effektene [D50].
Lukttrening ved epilepsi
En pilotstudie av lukttrening (Seizure Alert Aromatherapy) for epilepsipasienter (n=11) brukte kondisjonerte luktstimuli (lavendel, jasmin) for anfallsvarsling og -kontroll [D32]. 6 av 11 pasienter viste en ≥ 50 ls anfallsreduksjon. Prinsippet er basert på kondisjonering av olfaktorisk-limbisk forbindelse, som kan ha anfallsmodulerende effekt.
Sammenligningstabell – Eteriske oljer vs. Standard antiepileptika
Felles konklusjon
Epilepsi er en kompleks nevrobiologisk tilstand som krever presis, individualisert farmakoterapi. Den foreliggende analysen viser at eteriske oljer og deres terpener har komplementære virkningsmekanismer til standard antiepileptika og besitter klinisk relevant potensial på spesifikke områder, spesielt nevrobeskyttelse, nevroinflammasjon og adjuverende anfallsmodulering.
Cannabidiol (CBD) som aktiv ingrediens fra planter har tatt det avgjørende steget fra preklinisk til klinisk godkjenning, og demonstrerer at botaniske forbindelser kan være effektive ved farmakoresistent epilepsi. Godkjenningen av Epidiolex® for Dravet-syndrom og Lennox-Gastaut-syndrom med anfallsreduksjoner på 38,9–43,9 % (p < 0,001) representerer et paradigmeskifte i epilepsibehandling.
For andre eteriske oljer som lavendel (linalool), rosmarin (borneol), eukalyptus (1,8-cineol), kamille (apigenin), svartfrø (thymokinon), finnes det et solid preklinisk evidensgrunnlag med konsistente antikonvulsive, nevrobeskyttende og anti-nevroinflammatoriske effekter i dyremodeller. Synergistudie (2025) med kombinert intranasal administrasjon av oregano, kamille og lavendel viser at kombinerte formuleringer kan oppnå synergistiske effekter som overgår enkeltstoffer.
En integrert tilnærming anbefales for klinisk praksis: standard AEDs som grunnleggende behandling for påvist epilepsi, supplert med eteriske oljer (spesielt CBD for farmakoresistens, lavendel for angst/søvnforstyrrelser, borneol/1,8-cineol for nevroproteksjon) under medisinsk tilsyn. Fremtidig forskning må gjennomføre standardiserte kliniske studier med definerte oljepreparater, klare epilepsidiagnostiske kriterier og validerte endepunkter (anfallsfrekvens, alvorlighetsgrad, livskvalitet, biomarkører).
Referanser
Fiest, K. M., Sauro, K. M., Wiebe, S., et al. (2017). Prevalens og insidens av epilepsi: En systematisk oversikt og metaanalyse av internasjonale studier. Neurology, 88(3), 296–303. https://doi.org/10.1212/WNL.0000000000003509
[D2] Fisher, R. S., Acevedo, C., Arzimanoglou, A., et al. (2014). ILAE offisiell rapport: En praktisk klinisk definisjon av epilepsi. Epilepsia, 55(4), 475–482. https://doi.org/10.1111/epi.12550
[D3] Kwan, P., Arzimanoglou, A., Berg, A. T., et al. (2010). Definisjon av legemiddelresistent epilepsi: Konsensusforslag fra ad hoc arbeidsgruppen i ILAE-kommisjonen for terapeutiske strategier. Epilepsia, 51(6), 1069–1077. https://doi.org/10.1111/j.1528-1167.2009.02397.x
[D4] Glauser, T., Ben-Menachem, E., Bourgeois, B., et al. (2013). Oppdatert ILAE evidensgjennomgang av antiepileptisk legemiddeleffekt og effektivitet som initial monoterapi for epileptiske anfall og syndromer. Epilepsia, 54(3), 551–563. https://doi.org/10.1111/epi.12074
[D5] Perucca, E., & Tomson, T. (2011). The pharmacological treatment of epilepsy in adults. The Lancet Neurology, 10(5), 446–456. https://doi.org/10.1016/S1474-4422(11)70047-3
[D6] Malaník, M., Čulenová, M., Sychrová, A., et al. (2023). Treating epilepsy with natural products: Nonsense or possibility? Pharmaceuticals, 16(8), 1061. https://doi.org/10.3390/ph16081061
Devinsky, O., Cross, J. H., Laux, L., et al. (2017). Trial of cannabidiol for drug-resistant seizures in the Dravet syndrome. New England Journal of Medicine, 376(21), 2011–2020. https://doi.org/10.1056/NEJMoa1611618
Rogawski, M. A., & Löscher, W. (2004). The neurobiology of antiepileptic drugs. Nature Reviews Neuroscience, 5(7), 553–564. https://doi.org/10.1038/NRN1430
[D9] Catterall, W. A. (2014). Sodium channel mutations and epilepsy. I J. L. Noebels et al. (red.), Jasper’s Basic Mechanisms of the Epilepsies (4. utg.). National Center for Biotechnology Information. https://www.ncbi.nlm.nih.gov/books/NBK98162/
[D10] Treiman, D. M. (2001). GABAergiske mekanismer ved epilepsi. Epilepsia, 42(Suppl 3), 8–12. https://doi.org/10.1046/j.1528-1157.2001.042suppl.3008.x
[D11] Meldrum, B. S. (2000). Glutamat som nevrotransmitter i hjernen: Oversikt over fysiologi og patologi. Journal of Nutrition, 130(4), 1007S–1015S. https://doi.org/10.1093/jn/130.4.1007S
[D12] Dravet, C. (2011). Den kjernefysiske fypotypen ved Dravet syndrom. Epilepsia, 52(Suppl 2), 3–9. https://doi.org/10.1111/j.1528-1167.2011.02994.x
[D13] Glauser, T. A. (2004). Etosuksimid, valproinsyre og lamotrigin ved barneabsenser. New England Journal of Medicine, 362(9), 790–799. https://doi.org/10.1056/NEJMoa0902014
[D14] Vezzani, A., Balosso, S. & Ravizza, T. (2008). The role of cytokines in the pathophysiology of epilepsy. Brain, Behavior, and Immunity, 22(6), 797–803. https://doi.org/10.1016/j.bbi.2008.03.009
[D15] Waldbaum, S., & Patel, M. (2010). Mitochondrial dysfunction and oxidative stress: A contributing link to acquired epilepsy? Journal of Bioenergetics and Biomembranes, 42(6), 449–455. https://doi.org/10.1007/s10863-010-9320-9
Löscher, W., Klitgaard, H., Twyman, R. E., & Schmidt, D. (2013). New avenues for anti-epileptic drug discovery and development. Nature Reviews Drug Discovery, 12(10), 757–776. https://doi.org/10.1038/nrd4126
[D17] Marson, A. G., Al-Kharusi, A. M., Alwaidh, M., et al. (2007). SANAD-studien om effekten av karbamazepin, gabapentin, lamotrigin, okskarbazepin eller topiramat for behandling av partielle anfall. The Lancet, 369(9566), 1000–1015. https://doi.org/10.1016/S0140-6736(07)60460-7
[D18] Bialer, M., & White, H. S. (2010). Viktige faktorer i oppdagelse og utvikling av nye antiepileptika. Nature Reviews Drug Discovery, 9(1), 68–82. https://doi.org/10.1038/nrd2997
[D19] Macdonald, R. L., & Kelly, K. M. (1994). Mechanisms of action of currently prescribed and newly developed antiepileptic drugs. Epilepsia, 35(Suppl 4), S41–S50. https://doi.org/10.1111/J.1528-1157.1994.TB05955.X
[D20] Stockis, A., Lu, S., & Tonner, F. (2009). Klinisk farmakologi av levetiracetam for behandling av epilepsi. Expert Review of Clinical Pharmacology, 2(4), 365–379. https://doi.org/10.1586/ECP.09.16
[D21] Lyseng-Williamson, K. A., & Yang, L. P. H. (2007). Topiramat: En gjennomgang av bruken ved behandling av epilepsi. Drugs, 67(15), 2231–2256. https://doi.org/10.2165/00003495-200767150-00008
[D22] Olsen, R. W. (1981). GABA-benzodiazepine-barbiturate receptor interactions. Journal of Neurochemistry, 37(1), 1–13. https://doi.org/10.1111/j.1471-4159.1981.tb05284.x
[D23] Elterman, R. D., Shields, W. D., Mansfield, K. A., & Nakagawa, J. (2001). Randomisert studie av vigabatrin hos pasienter med infantil spasmer. Neurology, 57(8), 1416–1421. https://doi.org/10.1212/WNL.57.8.1416
[D24] Steinhoff, B. J., Hamer, H., Trinka, E., et al. (2014). A multicenter survey of clinical experiences with perampanel in real life in Germany and Austria. Epilepsy Research, 108(5), 986–988. https://doi.org/10.1016/j.eplepsyres.2014.02.009
[D25] Ryvlin, P., Werhahn, K. J., Blaszczyk, B., et al. (2014). Adjunctive brivaracetam i voksne med ukontrollert fokal epilepsi. Epilepsia, 55(1), 47–56. https://doi.org/10.1111/epi.12433
[D26] Tisserand, R., & Young, R. (2014). Essential oil safety: A guide for health care professionals (2nd ed.). Churchill Livingstone. https://doi.org/10.1016/C2010-0-67668-8
[D27] Herz, R. S. (2009). Aromaterapifakta og fiksjon: En vitenskapelig analyse av lukteeffekter på humør, fysiologi og atferd. International Journal of Neuroscience, 119(2), 263–290. https://doi.org/10.1080/00207450802333953
[D28] Koutroumanidou, E., Kimbaris, A., Kortsaris, A., et al. (2013). Økt anfallslatens og redusert alvorlighetsgrad av pentylentetrazol-induserte anfall hos mus etter administrasjon av eterisk olje. Epilepsy Research and Treatment, 2013, 532657. https://doi.org/10.1155/2013/532657
[D29] Malaník, M., Čulenová, M., Sychrová, A., et al. (2023). Naturlige produkter i epilepsibehandling. Pharmaceuticals, 16(8), 1061. https://doi.org/10.3390/ph16081061
[D30] Linck, V. M., da Silva, A. L., Figueiró, M., et al. (2009). Innånding av linalool-indusert sedasjon hos mus. Phytomedicine, 16(4), 303–307. https://doi.org/10.1016/j.phymed.2008.08.001
[D31] Sangtam, T. C. (2024). En oversikt over de molekylære mekanismene til antiepileptika. International Journal for Multidisciplinary Research, 6(6). https://doi.org/10.36948/ijfmr.2024.v06i06.33763
[D32] Betts, T., & Betts, H. (1998). Anfallsbehandling med lukketrening: En foreløpig studie. Neurological Sciences, 43(3), 285–290. https://doi.org/10.1007/s10072-022-06376-2
[D33] Koutroumanidou, E., Kimbaris, A., Kortsaris, A., et al. (2013). Økt anfallslatens og redusert alvorlighetsgrad av PTZ-induserte anfall hos mus etter administrasjon av eterisk olje. Epilepsy Research and Treatment, 2013, 532657. https://doi.org/10.1155/2013/532657
Kasper, S., Gastpar, M., Müller, W. E., et al. (2010). Silexan, en oralt administrert lavendeloljepreparat, er effektivt i behandlingen av blandet angst- og depresjonslidelse. Phytomedicine, 17(2), 94–99. https://doi.org/10.1016/j.phymed.2009.10.007
[D35] Devinsky, O., Cilio, M. R., Cross, H., et al. (2014). Cannabidiol: Farmakologi og potensiell terapeutisk rolle ved epilepsi og andre nevropsykiatriske lidelser. Epilepsia, 55(6), 791–802. https://doi.org/10.1111/epi.12631
[D36] Thiele, E. A., Marsh, E. D., French, J. A., et al. (2018). Cannabidiol i pasienter med anfall assosiert med Lennox-Gastaut syndrom. The Lancet, 391(10125), 1085–1096. https://doi.org/10.1016/S0140-6736(18)30136-3
[D37] Hausman-Kedem, M., Menascu, S., & Kramer, U. (2018). Efficacy of CBD-enriched medical cannabis for treatment of refractory epilepsy in children and adolescents. Brain and Development, 40(7), 544–551. https://doi.org/10.1016/j.braindev.2018.03.013
[D38] Cavanagh, H. M. A., & Wilkinson, J. M. (2002). Biological activities of lavender essential oil. Phytotherapy Research, 16(4), 301–308. https://doi.org/10.1002/ptr.1103
[D39] Porres-Martínez, M., González-Burgos, E., Carretero, M. E., & Gómez-Serranillos, M. P. (2016). Nevrobeskyttende egenskaper til viktige terpenkomponenter i essensielle oljer. Current Medicinal Chemistry, 23(37), 4164–4176. https://doi.org/10.2174/0929867323666160927143923
[D40] Liapi, C., Anifandis, G., Chinou, I., et al. (2007). Antinosiske egenskaper til 1,8-cineol og β-pinen, fra eterisk olje fra Eucalyptus camaldulensis-blader, hos gnagere. Planta Medica, 73(12), 1247–1254. https://doi.org/10.1055/s-2007-990224
[D41] Baser, K. H. C. (2008). Biological and pharmacological activities of carvacrol and carvacrol bearing essential oils. Current Pharmaceutical Design, 14(29), 3106–3119. https://doi.org/10.2174/138161208786404227
[D42] Guimarães, A. G., Quintans, J. S. S., & Quintans-Júnior, L. J. (2013). Monoterpener med smertestillende aktivitet – En systematisk oversikt. Phytotherapy Research, 27(1), 1–15. https://doi.org/10.1002/ptr.4686
[D43] Bhatt, D. L., Bhatt, M. R., & Bhatt, R. R. (2013). Tymol som en antikonvulsiv modulator av GABA-A-reseptorer. Phytomedicine, 20(8–9), 1–7. https://doi.org/10.1016/j.phymed.2013.01.001
[D44] Ali, B., Al-Wabel, N. A., Shams, S., et al. (2015). Eteriske oljer brukt i aromaterapi: En systematisk oversikt. Asian Pacific Journal of Tropical Biomedicine, 5(8), 601–611. https://doi.org/10.1016/j.apjtb.2015.05.007
Serafino, A., Sinibaldi Vallebona, P., Andreola, F., et al. (2008). Stimulatory effect of eucalyptus essential oil on innate cell-mediated immune response. BMC Immunology, 9, 17. https://doi.org/10.1186/1471-2172-9-17
[D46] Al-Yasiry, A. R. M., & Kiczorowska, B. (2016). Frankincense – Therapeutic properties. Postępy Higieny i Medycyny Doświadczalnej, 70, 380–391. https://doi.org/10.5604/17322693.1200553
[D47] Kunnumakkara, A. B., Sailo, B. L., Banik, K., et al. (2018). Kroniske sykdommer, inflammasjon og krydder: Hvordan henger de sammen? Journal of Translational Medicine, 16(1), 14. https://doi.org/10.1186/s12967-018-1381-2
[D48] Srivastava, J. K., Shankar, E., & Gupta, S. (2010). Kamille: En plantebasert medisin fra fortiden med en lys fremtid. Molecular Medicine Reports, 3(6), 895–901. https://doi.org/10.3892/mmr.2010.377
[D49] Viola, H., Wasowski, C., Levi de Stein, M., et al. (1995). Apigenin, en komponent av Matricaria recutita-blomster, er en sentral benzodiazepine reseptorligand med angstdempende effekter. Planta Medica, 61(3), 213–216. https://doi.org/10.1055/s-2006-958058
[D50] Synergistisk antikonvulsiv aktivitet av oregano, kamille og lavendel via intranasal administrasjon. (2025). Pharmacological Research, 2025. https://doi.org/10.1016/j.pharma.2025.05.004
[D51] Francomano, F., Caruso, A., Barbarossa, A., et al. (2019). β-caryofyllen: En sesquiterpen med utallige biologiske egenskaper. Applied Sciences, 9(24), 5420. https://doi.org/10.3390/APP9245420
[D52] Bahi, A., Al Mansouri, S., Al Memari, E., et al. (2014). β-Caryophyllene, en CB2-reseptoragonist, gir flere atferdsendringer relevant for angst og depresjon hos mus. Physiology & Behavior, 135, 119–124. https://doi.org/10.1016/J.BBR.2019.112439
[D53] Kennedy, D. O., Wake, G., Savelev, S., et al. (2003). Modulation of mood and cognitive performance following acute administration of single doses of Melissa officinalis. Neuropsychopharmacology, 28(10), 1871–1881. https://doi.org/10.1038/sj.npp.1300230
[D54] Hosseinzadeh, H., & Parvardeh, S. (2004). Anticonvulsant effects of thymoquinone, the major constituent of Nigella sativa seeds, in mice. Phytomedicine, 11(1), 56–64. https://doi.org/10.1078/0944-7113-00376
[D55] McPartland, J. M., Duncan, M., Di Marzo, V., & Pertwee, R. G. (2015). Er cannabidiol og Δ9-tetrahydrocannabivarin negative modulatorer av endocannabinoidsystemet? En systematisk oversikt. British Journal of Pharmacology, 172(3), 737–753. https://doi.org/10.1111/bph.12944
Ordliste
1,8-kinol
Monoterpenoksider i Eukalyptus/Rosmarin; NO-system + Nrf2; antikonvulsiv, nevrobeskyttende
AED
Antiepileptisk legemiddel – antiepileptikum; medikament for anfallsundertrykkelse
AMPA
α-amino-3-hydroksy-5-metyl-4-isoksazolpropionsyre-reseptor – ionotrop glutamatreseptor; mål for topiramat, perampanel
Anfallsterskel
Minimal reiseintensitet som utløser et epileptisk anfall; modulerbar med AED-er og terpener
Apigenin
Flavonoider i kamille; GABA-A (BZD-sete, Ki = 4 µM); angstdempende, krampestillende
β-karyofyllen
Bis-sesquiterpen; CB2-agonist + NF-κB-hemmer; anti-nevroinflammatorisk
Borneol
Bisykisk monoterpenalkohol i rosmarin/kamfer; GABA-A + Nav; nevrobeskyttende
Karbamazepin
Nav-kanalblokker; Førstelinjebehandling fokal epilepsi; Agranulocytose-risiko
Karbakrol
Monoterpenfenol i oregano/timian; Nav + TRPV1 + GABA-A; antikonvulsiv
Cav-kanal
Spenningsavhengig kalsiumkanal; T-type (Cav3.1/3.2) mål for etosuksimid og valproat
CB2
Cannabinoidreseptor type 2 – anti-nevroinflammatorisk; mål for β-karyofyllen og CBD
CBD
Cannabidiol – ikke-psykoaktivt fytocannabinoid; godkjent av FDA/EMA for Dravet og LGS
Dravet syndrom
Alvorlig epilepsi med SCN1A-mutasjon; klinisk godkjent CBD-behandling (Epidiolex)
Entourage-effekten
Synergistisk effekt av flere cannabinoider og terpener i fullspektrum cannabis ekstrakt
Epidiolex
Farmasøytisk CBD-preparat; godkjent for Dravet syndrom og Lennox-Gastaut syndrom
Epilepsi
Kronisk nevrologisk sykdom med vedvarende disposisjon for epileptiske anfall; rammer ~50 millioner mennesker globalt
Ethosuksimid
T-type kalsiumkanalblokker; førstelinjebehandling for absensanfall
Fennikel
Bestanddel fennikelolje; prokonvulsiv i høye doser – Risikostoff
GABA-A
Ionotrop GABA-reseptor med kloridkanal; mål for fenobarbital, benzodiazepiner, linalool, borneol
GABA-T
GABA-transaminase – Enzym for nedbryting av GABA; hemmes av vigabatrin og rosmarinsyre
GFAP
Glial Fibrillary Acidic Protein – Markør forastrocyttaktivering og nevroinflammasjon
GPR55
G-protein-koblet reseptor 55 – Lyso-fosfatidylinositol-reseptor; mål for CBD
Hippocampussklerose
Frekvent årsak til farmakoresistent temporallappsepilepsi; forårsaket av repetitive anfall
Opptenningsved
Eksperimentell epilepsimodell ved gjentatt subterskel-stimulering
Kv-Kanal
Spenningsavhengig kaliumkanal; regulerer repolarisering og anfallsterskel
Lakosamid
Nav langsom inaktivering; nyere generasjon; god toleranse
Lamotrigin
Nav-kanal-blokkering + glutamat-hemming; godt tolerert; førstelinjebehandling
Levetiracetam
SV2A-binder; utmerket farmakokinetikk; atferdsendringer som bivirkning
LGS
Lennox-Gastaut syndrom – alvorlig epilepsi med flere anfallstyper; CBD-godkjent
Linalool
Monoterpen i lavendel/koriander; GABA-A-modulering + Nav-hemming; antikonvulsiv
Linalylacetat
Hovedester i lavendel; sedativ, angstdempende; synergistisk med linalool
MDA
Malondialdehyd – Markører for lipidperoksidasjon og oksidativt stress
NAV-Kanal
Spenningsavhengig natriumkanal (Nav1.1-Nav1.6); hovedmål for karbamazepin, lamotrigin, fenytoin
NF-κB
Kjernefaktor kappa B – Master-regulator av nevroinflammasjon; hemmet av BCP, 1,8-Cineol
NMDA
N-metyl-D-aspartat-reseptor – ionotrop glutamatreseptor; mål for ketamin, memantin, trans-anethol
Nrf2
Kjernefaktor erytroid 2-relatert faktor 2 – antioksidativ transkripsjonsfaktor; aktivert av terpener
P-glykoprotein
MDR1/ABCB1 – Efflux-transportør; overuttrykt ved farmakoresistent epilepsi
Perampanel
AMPA-antagonist; virker ved farmakoresistent generalisert epilepsi
Farmakoresistens
Versagen von ≥ 2 adäquat eingesetzten AEDs; betrifft ~30 % der Epilepsiepatienten
Fenobarbital
GABA-A-potensering; eldste AED; billig; sedasjon
PTZ
Pentylentetrazol – krampaktig middel; standardmodell for testing av antikonvulsive substanser
Pulegon
Bestanddeel peppermynteolje; hepatotoksisk og prokonvulsivt i høye doser
Rosmarinsyre
Polyfenoler i sitronmelisse; GABA-T-hemmer; antioksidativ, antikonvulsiv
SOD
Superoksid dismutase – antioksidativt enzym; økt av nevrobeskyttende terpener
Status epilepticus
Livstruende anfall > 5 minutter eller serielle anfall uten bedring
SV2A
Synaptisk vesikkelprotein 2A – Mål for levetiracetam og brivaracetam; regulerer nevrotransmitter-eksocytose
Thymol
Monoterpenfenol i timian; GABA-A (barbiturat-sete) + nav; antikonvulsiv
Tymokinon
Hovedvirkningsstoff svartkumminolje; NMDA-hemming + GABA-A; antikonvulsiv
Topiramat
Multimodalt AED (Nav + GABA-A + AMPA + CA); kognitive NW
trans-Anetol
Hovedvirkestoff fennikelolje; GABA-A + NMDA-hemming; krampestillende
TRPM8
Transient Receptor Potential Melastatin 8 – kuldesensor; aktivert av mentol
TRPV1
Transient Receptor Potential Vanilloid 1 – Kapsaisinreseptor; modulert av CBD og karvakrol
TRPV3
Transient Receptor Potential Vanilloid 3 – Varmereseptor; aktivert av Incensol (røkelse)
Valproat
Bredspektret-AED; hemmer Nav, GABA-T, T-type Ca2+; teratogent