Inhaltsverzeichnis
Epilepsie kann in etwa 30% der Fälle nicht ausreichend mit pharmazeutischen Mitteln behandelt werden, weshalb ätherische Öle als unterstützende Maßnahme in den Fokus rücken.
Was es hierbei zu beachten gilt, ob und in welchem Umfang sie hilfreich sind, wird nachfolgend – für Laien verständlich – erläutert.
Eine Kurzfassung des wissenschaftlichen Berichts für alle, die mehr über natürliche Unterstützung bei Epilepsie erfahren möchten.
Ein Glossar, nach dem Quellenverzeichnis, erklärt Fachbegriffe.
Der dritte Teil richtet sich an Mediziner, präsentiert den aktuellen Stand der pharmakologischen Therapie, sowie Studienergebnisse hinsichtlich supportiver ätherischer Öle bei Eplilepsie samt Quellennachweis.
Was ist Epilepsie?
Das Gehirn besteht aus Milliarden von Nervenzellen, die ständig elektrische Signale senden. Normalerweise geschieht das geordnet, wie ein gut dirigiertes Orchester. Bei Epilepsie kommt es plötzlich zu einer Art “elektrischem Sturm” im Gehirn, dem Anfall: Viele Nervenzellen feuern gleichzeitig und unkontrolliert.
Was passiert während eines Anfalls?
Je nachdem, welcher Teil des Gehirns betroffen ist, kann ein Anfall sehr unterschiedlich aussehen:
- Absence
Kurzes “Wegtreten” für Sekunden, der Betroffene starrt ins Leere - Myoklonischer Anfall
Kurze, zuckende Bewegungen (oft morgens) - Fokaler Anfall: Zuckungen oder Empfindungen in einem Körperteil, manchmal mit Bewusstseinstrübung –
- Generalisierter tonisch-klonischer Anfall (früher “Grand Mal”): Sturz, Versteifung, rhythmisches Zucken des ganzen Körpers, Bewusstlosigkeit
Wie häufig ist Epilepsie?
Epilepsie betrifft weltweit etwa 50 Millionen Menschen, das ist etwa 1 % der Weltbevölkerung. In Deutschland leben rund 400.000–500.000 Menschen mit Epilepsie. Es ist nach Migräne und Schlaganfall die dritthäufigste neurologische Erkrankung.
Das große Problem
Bei etwa 30 % der Patienten schlagen Medikamente nicht ausreichend an, man spricht von pharmakoresistenter Epilepsie. Diese Menschen suchen oft nach ergänzenden Möglichkeiten.
Was passiert im Gehirn bei Epilepsie?
Zwei Systeme müssen im Gleichgewicht sein:
- GABA (Gamma-Aminobuttersäure): Der “Bremser”, beruhigt das Gehirn
- Glutamat: Der “Gaspedal”, aktiviert das Gehirn
Bei Epilepsie ist das Gleichgewicht gestört: Zu wenig Bremse, zu viel Gas, das Gehirn “dreht durch”.
Außerdem spielen Ionenkanäle eine wichtige Rolle, das sind winzige “Tore” in den Nervenzellmembranen:
- Natriumkanäle (Nav)
Öffnen sich, wenn eine Nervenzelle feuer, bei Epilepsie öffnen sie sich zu leicht - Calciumkanäle (Cav)
Wichtig für bestimmte Anfallstypen (z. B. Absencen) - Kaliumkanäle (Kv)
Helfen, die Nervenzelle nach dem Feuern zu beruhigen
Wie wird Epilepsie normalerweise behandelt?
Die wichtigsten Antiepileptika (AEDs)
Valproat (Valproinsäure) ist das wichtigste Breitspektrum-Antiepileptikum. Es wirkt auf mehreren Wegen gleichzeitig und wirkt besonders gut bei generalisierten Epilepsien, indem es Natrium- und Calciumkanäle bremst, und GABA erhöht.
Wichtige Warnung:
Valproat ist stark schädigend für ungeborene Kinder, Frauen im gebärfähigen Alter!
Carbamazepin und Lamotrigin sind die “Türstopper” für Natriumkanäle. Sie verhindern, dass die Nervenzellen zu leicht feuern. Die beiden Pharmazeutika stellen die Erstlinientherapie bei fokalen Epilepsien dar. Lamotrigin ist besonders gut verträglich und sicher in der Schwangerschaft
Levetiracetam (Keppra) weist einen einzigartigen Mechanismus auf, denn es bindet an ein Protein (SV2A), das die Signalübertragung zwischen Nervenzellen reguliert. Es zeichnet sich durch sehr gute Verträglichkeit aus und hat keine Wechselwirkungen mit anderen Medikamenten. Mögliche Nebenwirkung sind Stimmungsschwankungen und Reizbarkeit
Topiramat wirkt auf vier verschiedene Wege gleichzeitig, sozusagen ein “Multitalent”, das eine hohe Anfallsfreiheitsrate von 44–83 % der Patienten erreicht. Als Nebenwirkung kann verlangsamtes Denken, wie auch Wörter-Findungs-Störungen auftreten.
Ethosuximid wird bei Absencen (kurze “Wegtreter”) eingesetzt. Es blockiert spezifische Calciumkanäle im Thalamus (einem Relais-Zentrum im Gehirn).
Phenobarbital und Benzodiazepine verstärken die GABA-Wirkung (die “Bremse”). Sie sind kostengünstig, wirksam, weisen aber Sedierungs- und Suchtpotenzial (Benzodiazepine) auf.
Ätherische Öle bei Epilepsie – was ist möglich?
Bei Epilepsie ist besondere Vorsicht geboten!
Einige ätherische Öle können Anfälle auslösen oder verstärken (prokonvulsiv). Sprechen Sie IMMER mit Ihrem Neurologen, bevor Sie ätherische Öle verwenden.
Öle, die Sie bei Epilepsie MEIDEN sollten:
– Rosmarin (in hohen Dosen – Kampfer-Gehalt)
– Eukalyptus (in hohen Dosen)
– Pfefferminze (Pulegon-Gehalt)
– Fenchel (Fenchon in hohen Dosen)
– Salbei (Thujon-Gehalt)
– Kampfer (direkt prokonvulsiv)
Welche ätherischen Öle zeigen antikonvulsive Eigenschaften?
Lavendel – beruhigend und anfallshemmend
Lavendel (Lavandula angustifolia) ist das am besten erforschte Öl bei Epilepsie.
Zusammensetzung
– Linalool (25–45 %)
– Linalylacetat (25–50 %)
Wirkung
– Aktiviert GABA-A-Rezeptoren (die “Bremse” des Gehirns)
– Hemmt Natriumkanäle (verhindert unkontrolliertes Feuern)
– Senkt die Anfallsbereitschaft
Klinische Effekte
– Linalool verlängerte in Tierversuchen die Zeit bis zum ersten Anfall im PTZ-Modell (Standardmodell für Anfallstests) signifikant
– Manche Patienten berichten, dass Lavendel-Aromatherapie Anfälle verzögert oder Auren (Vorwarnzeichen) lindert
– Im Aromadiffusor via Inhalation anwenden, aber niemals innerlich ohne ärztliche Beratung
Rosmarin/Borneol – neuroprotektiv (mit Vorsicht!)
Borneol ist ein Wirkstoff aus Rosmarin und anderen Pflanzen.
Wirkung
– Schützt Nervenzellen vor Schäden durch wiederholte Anfälle; GABAerg und neuroprotektiv
– Borneol reduzierte Anfallsschwere im Kindling-Modell und senkte Entzündungsmarker (GFAP) in Tierversuchen
Achtung: Rosmarin-Öl als Ganzes kann in hohen Dosen prokonvulsiv sein, nur isoliertes Borneol oder sehr niedrige Dosen einnehmen
Oregano – Carvacrol und Thymol
Carvacrol (aus Oregano und Thymian) zeigt interessante antikonvulsive Eigenschaften.
Wirkung
– Hemmt Natriumkanäle (wie Carbamazepin)
– Moduliert TRPV1-Rezeptoren (Wärme- und Schmerzrezeptoren)
– Reduzierte Anfallsdauer und -schwere in Tierversuchen
Eukalyptus – 1,8-Cineol (mit Vorsicht!)
1,8-Cineol aus Eukalyptus zeigt im Tiermodell antikonvulsive Wirkung.
Wirkung
– Beeinflusst das NO-System (Stickstoffmonoxid) im Gehirn
– Erhöht die Anfallsschwelle (~25 mg/kg vs. ~10 mg/kg in Kontrollgruppe)
– Aktiviert Nrf2 (antioxidativer Schutzfaktor)
- Achtung: In hohen Dosen prokonvulsiv, nur in geringen Mengen und nach Rücksprache mit Arzt
Kamille – Apigenin und Synergien
Kamille (Matricaria chamomilla) enthält Apigenin, ein Flavonoid mit anxiolytischen und antikonvulsiven Eigenschaften.
Wirkung
– Apigenin bindet an GABA-A-Rezeptoren (an derselben Stelle wie Benzodiazepine, aber viel schwächer)
– Neue Studie (2025): Kombination aus Oregano + Kamille + Lavendel (intranasal verabreicht) zeigte synergistische antikonvulsive Wirkung im Tiermodell – besser als jedes Öl alleine
- Als Ergänzung bei leichten Anfällen oder zur Angstreduktion
β-Caryophyllen – der Entzündungshemmer
β-Caryophyllen (BCP) kommt in schwarzem Pfeffer, Lavendel, Rosmarin und Cannabis vor.
Wirkung
– Aktiviert CB2-Rezeptoren (Cannabinoid-Rezeptoren) ohne psychoaktive Wirkung
– Hemmt NF-κB (den Entzündungs-Schalter)
– Reduziert Neuroinflammation, wichtig, weil Entzündungen Epilepsie verschlimmern können
– BCP ist auch in Hanföl enthalten und könnte Teil der Wirkung von CBD-reichen Extrakten sein
Die wichtigste Pflanze Cannabis und CBD
CBD (Cannabidiol) – der klinische Durchbruch
CBD ist ein Wirkstoff aus der Cannabispflanze (Cannabis sativa), aber ohne die bekannte psychoaktive Wirkung von THC. Es ist das einzige pflanzliche Antiepileptikum, das offiziell von der FDA (USA) und EMA (Europa) unter dem Namen Epidiolex zugelassen wurde.
Es wird als verschreibungspflichtiges Medikament (Epidiolex) in Form einer Öllösung 2× täglich oral verabreicht.
Wirkung
– Hemmt Natriumkanäle (wie Carbamazepin)
– Moduliert TRPV1 und GPR55 (spezielle Rezeptoren)
– Entzündungshemmend über CB2-Rezeptoren – Schützt Nervenzellen
Nebenwirkungen
– Schläfrigkeit, Durchfall, verminderter Appetit
– Kann den Spiegel anderer Antiepileptika (besonders Clobazam) erhöhen, Dosisanpassung nötig
Zulassung für:
– Dravet-Syndrom – Eine schwere Epilepsieform, die im Säuglingsalter beginnt
– Lennox-Gastaut-Syndrom (LGS) – Schwere Epilepsie mit mehreren Anfallstypen
Studien
– Beim Dravet-Syndrom: CBD reduzierte die Anfallshäufigkeit um 38,9 % vs. 13,3 % mit Placebo, 66,7 % der Patienten hatten ≥ 50 % weniger Anfälle (p = 0,009)
– Beim LGS: Reduktion der Sturzanfälle um 43,9 % vs. 21,8 % mit Placebo (p < 0,001)
– Bei anderen pharmakoresistenten Epilepsien: Verschiedene Studien zeigen 40–50 % Anfallsreduktion
Vergleichstabelle – Was hilft wie?
Sicherheitsregel
Möglicherweise hilfreich (nach Rücksprache mit Arzt):
- Lavendel-Aromatherapie (Diffusor, Inhalation) – entspannend, möglicherweise anfallsreduzierend
- CBD (als Epidiolex) – bei Dravet/LGS, verschreibungspflichtig
- β-Caryophyllen – entzündungshemmend, gut verträglich
- Kamille – beruhigend, anxiolytisch
Bei Epilepsie MEIDEN:
- Rosmarin-Öl (pur, hohe Dosen) – Kampfer kann Anfälle auslösen
- Eukalyptus-Öl (hohe Dosen)
- Pfefferminz-Öl (hohe Dosen, Pulegon)
- Fenchelöl (Fenchon)
- Salbeiöl (Thujon)
- Kampferöl (direkt prokonvulsiv)
Allgemeine Sicherheitshinweise
- IMMER zuerst mit dem Neurologen sprechen – Epilepsie ist ernst
- Antiepileptika niemals eigenmächtig absetzen – kann zu lebensbedrohlichem Status epilepticus führen
- Wechselwirkungen beachten: Manche Öle können den Spiegel von Antiepileptika verändern
- Nie pur auf die Haut – immer verdünnen
- Kinder: Besondere Vorsicht, Dosen viel niedriger
Häufig gestellte Fragen
Kann ich Lavendel statt meiner Antiepileptika nehmen?
Nein, auf keinen Fall! Lavendel hat nur in Tierversuchen antikonvulsive Wirkung gezeigt. Antiepileptika eigenmächtig abzusetzen kann lebensgefährlich sein.
Was ist mit CBD-Öl aus dem Internet?
CBD-Produkte aus dem Internet sind nicht das gleiche wie das zugelassene Medikament Epidiolex. Sie sind nicht standardisiert, können andere Cannabinoide enthalten und haben keine nachgewiesene Wirksamkeit. Sprechen Sie mit Ihrem Neurologen über verschreibungspflichtiges CBD.
Kann Aromatherapie einen Anfall stoppen?
Es gibt Berichte, dass manche Patienten durch bestimmte Gerüche (wie Lavendel) Anfälle verzögern können, aber das ist keine zuverlässige Methode und kein Ersatz für Medikamente.
Sind ätherische Öle bei Kindern mit Epilepsie sicher?
Nur nach ausdrücklicher Rücksprache mit dem Kinderneurologen. Kinder reagieren empfindlicher, und manche Öle sind für Kinder gefährlich.
Muss ich teure Öle kaufen?
Qualität ist wichtig: Achten Sie auf 100 % naturreine ätherische Öle, am besten mit am besten mit chargenspezifischem Analyse-Zertifikat (GC/MS).
Günstige Parfümöle oder synthetische Duftstoffe haben keine therapeutische Wirkung und sind auf Grund der synthetischen Inhaltsstoffe u.U. gesundheitlich schädlich und verursachen Kopfschmerzen, Übelkeit, etc..
Wer mehr über die Auswahl und Qualität ätherischer Öle erfahren möchte, der wird in dem Beitrag „Ätherische Öle – Odysse einer Suche“ fündig.
Ein weiterer Beitrag zitiert Prof. Dr. Dr. Dr. med. habil. Hanns Hatt von der Ruhr-Universität Bochum, der in seinem Video „Heilen mit Düften“ auf interessante, kurzweilige und dennoch wissenschaftliche Weise die Wirkung ätherischer Öle auf den menschlichen Körper erklärt.
Zusammenfassung in drei Sätzen
Epilepsie ist eine ernste neurologische Erkrankung, bei der elektrische Stürme im Gehirn zu Anfällen führen, und bei 30 % der Patienten helfen Standard-Medikamente nicht ausreichend.
Ätherische Öle und Terpene, besonders Linalool (Lavendel), Borneol und Carvacrol, zeigen in Tierversuchen antikonvulsive Eigenschaften über GABA-A-Aktivierung und Natriumkanal-Hemmung; CBD (Cannabidiol) ist das einzige pflanzliche Antiepileptikum mit klinischer Zulassung (Dravet-Syndrom, Lennox-Gastaut-Syndrom).
Ätherische Öle können bei Epilepsie ergänzend eingesetzt werden, aber nur nach ausdrücklicher Rücksprache mit dem behandelnden Neurologen, da einige Öle Anfälle auch auslösen können.
Dieser Text basiert auf dem wissenschaftlichen Bericht “Epilepsie und Ätherische Öle: Pharmakologie, Wirkmechanismen und komplementäre Therapieansätze” und dient ausschließlich der allgemeinen Information. Epilepsie ist eine ernste Erkrankung, wenden Sie sich bei Fragen zur Behandlung immer an Ihren Neurologen.
Empfohlene dōTERRA-Produkte für Epilepsie-Begleittherapie
Potenziell sichere Produkte (nach Studienlage)
Öle, die bei Epilepsie GEMIEDEN werden sollten
Eigene Ölmischungen (DIY-Blends)
Blend 1 – “Neuroprotektiv” (Diffusor)
Ziel: Neuroprotektiver Schutz, GABA-Modulation
Anwendung: Täglich 30 Minuten im Diffusor, besonders abends
Blend 2 – “Aura-Management” (Topisch, schnell)
Ziel: Bei Aura-Symptomen: Anfallsunterbrechung versuchen (NUR als Ergänzung, nicht als Ersatz für Notfallmedikation)
Anwendung: Auf Schläfen, Nacken, Handgelenke – sofort bei Aura-Beginn
Notfallmedikation (z.B. Diazepam-Rectal) bleibt Priorität
Blend 3 – “Angst & Stressabbau” (Diffusor/Topisch)
Ziel: Stress ↓ (häufiger Anfallstrigger), Entspannung ↑
Anwendung: Bei Stress oder vor bekannten Trigger-Situationen
Blend 4 – “Schlaf & Erholung” (Abend)
Ziel: Schlafqualität ↑ (Schlafmangel = Anfallstrigger)
Anwendung: Im Diffusor, 30 Minuten vor dem Schlafen
Blend 5 – “Entzündungshemmung” (Topisch)
Ziel: Neuroinflammation ↓ (Epilepsie-Pathophysiologie)
Anwendung: Auf Schläfen, Nacken und Wirbelsäule massieren
Anwendungsprotokoll – 4-Wochen-Plan
Woche 1 – Vorsichtiger Einstieg
- Arzt konsultieren BEVOR mit Ölen begonnen wird
- Abends: Blend 4 im Diffusor (Schlaf)
- Täglich: Blend 1 im Diffusor (30 Min)
- Anfallsprotokoll führen (Datum, Uhrzeit, Trigger)
Woche 2 – Erweiterung
- Morgens: Blend 3 bei Stresssituationen
- Abends: Blend 4 (Schlaf) + Blend 5 topisch
- Blend 2: Bereithalten für Aura-Situationen
Woche 3-4 – Optimierung
- Anfallsprotokoll auswerten – hat sich etwas verändert?
- Neurologen informieren über Öl-Anwendung
- Anpassung basierend auf individueller Verträglichkeit
Kombination mit anderen dōTERRA-Produkten
Notfallplan bei Anfall
- Sicherheit: Person in stabile Seitenlage
- Zeit messen: Anfall länger als 5 Minuten → Notarzt (112)
- Notfallmedikation: Diazepam-Rectal / Midazolam-Nasal (wie vom Arzt verordnet)
- KEIN Öl in Mund oder Nase bei aktivem Anfall
- Ätherische Öle sind KEINE Notfallmedikation
Epilepsie und Ätherische Öle – Pharmakologie, Wirkmechanismen und komplementäre Therapieansätze
Ein umfassender wissenschaftlicher Bericht zu Standard-Antiepileptika, Terpenen und ätherischen Ölen – molekulare Grundlagen, klinische Evidenz und adjuvante Therapiestrategien
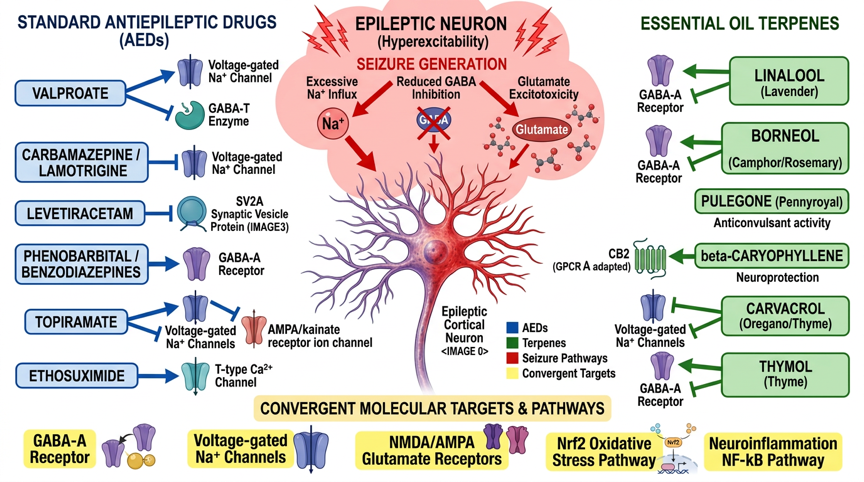
Abb. 1: Molekulare Signalwege der Standard-Antiepileptika und ätherischen Öle bei Epilepsie – Standard-AEDs (Valproat/Nav+GABA-T, Carbamazepin/Nav, Levetiracetam/SV2A, Topiramat/multimodal, Ethosuximid/T-Typ-Ca2+, Phenobarbital/GABA-A) und Terpene (Linalool/GABA-A+Nav, Borneol/GABA-A+Nav, Carvacrol/Nav+TRPV1, β-Caryophyllen/CB2, 1,8-Cineol/NO+Nrf2) mit konvergenten Zielmolekülen (GABA-A-Rezeptor, Nav-Kanäle, NMDA/AMPA-Glutamat, NF-κB-Neuroinflammation, Nrf2-Oxidativer Stress)
Oben: Sharp Wave (70-200 ms) mit nachfolgender Slow Wave.
Mitte: 3-Hz Spike-Wave-Komplex (GSWD) – Hallmark-Muster der Absenz-Epilepsie.
Unten: Polyspike-Komplex (3-5 Spikes, 4-5 Hz) – charakteristisch für Juvenile Myoklonische Epilepsie (JME).
Einleitung
Epilepsie ist eine der häufigsten chronischen neurologischen Erkrankungen weltweit und betrifft schätzungsweise 50 Millionen Menschen, etwa 1 % der Weltbevölkerung [D1]. Sie ist definiert durch eine anhaltende Prädisposition zu epileptischen Anfällen infolge pathologisch synchronisierter neuronaler Entladungen sowie durch die neurobiologischen, kognitiven, psychologischen und sozialen Konsequenzen dieser Erkrankung [D2]. Trotz bedeutender Fortschritte in der Entwicklung von Antiepileptika (AEDs) bleibt bei etwa 30 % der Patienten eine pharmakoresistente Epilepsie bestehen, bei der zwei oder mehr adäquat eingesetzte AEDs keine ausreichende Anfallskontrolle erzielen [D3].
Die Standardbehandlung der Epilepsie umfasst eine stufenweise Pharmakotherapie mit Antiepileptika der ersten, zweiten und dritten Generation. Valproat, Carbamazepin und Lamotrigin gelten als Erstlinienmedikamente bei fokalen und generalisierten Epilepsien; neuere Substanzen wie Levetiracetam, Topiramat, Lacosamid und Perampanel erweitern das therapeutische Arsenal [D4]. Trotz ihrer Wirksamkeit sind AEDs mit erheblichen Nebenwirkungen verbunden, kognitive Beeinträchtigungen, Teratogenität (Valproat), Knochenmarkdepression (Carbamazepin), Gewichtszunahme und psychische Störungen, die die Lebensqualität der Patienten erheblich beeinflussen [D5].
Vor diesem Hintergrund wächst das wissenschaftliche Interesse an pflanzlichen Wirkstoffen und ätherischen Ölen als adjuvante oder alternative Therapieoptionen. Zahlreiche Terpene und bioaktive Verbindungen zeigen in präklinischen und klinischen Studien antikonvulsive, neuroprotektive, anti-neuroinflammatorische und antioxidative Eigenschaften, oft über Mechanismen, die sich komplementär zu klassischen AEDs verhalten [D6]. Cannabidiol (CBD) hat als pflanzlicher Wirkstoff aus Cannabis sativa bereits klinische Zulassungen für spezifische Epilepsiesyndrome erhalten und demonstriert das Potenzial botanischer Verbindungen in der Epilepsietherapie [D7]. Dieser Bericht analysiert systematisch die Pharmakologie der Standard-Antiepileptika, die molekularen Wirkmechanismen relevanter ätherischer Öle und Terpene sowie die verfügbare klinische Evidenz für deren adjuvanten Einsatz bei Epilepsie.
EEG bei Epilepsie – Grundlagen und Interpretationsprinzipien
Das Elektroenzephalogramm (EEG) ist das zentrale diagnostische Instrument bei Epilepsie und erlaubt die direkte Messung kortikaler elektrischer Aktivität über Skalp-Elektroden. Es dient der Anfallsklassifikation, Herdlokalisation und Therapiemonitoring.
Interiktale Phase: Das EEG zwischen den Anfällen zeigt typischerweise interiktale epileptiforme Entladungen (IEDs): Spikes (<70 ms), Sharp Waves (70-200 ms) und 3-Hz Spike-Wave-Komplexe (GSWDs bei Absenz-Epilepsie). Diese IEDs entstehen durch synchrone neuronale Entladungen im epileptischen Fokus.
Iktale Phase: Das Anfalls-EEG beginnt häufig mit Low-Voltage Fast Activity (LVFA, 20-35 Hz) als Onset-Muster. Im Verlauf entwickelt sich eine rhythmische Theta-Delta-Evolution mit Amplitudenzunahme. Die Termination erfolgt abrupt mit nachfolgender postiktaler Suppression.
Postiktale Phase: Nach Anfallsende zeigt das EEG eine Suppression (markierte Amplitudenreduktion) gefolgt von diffuser Delta-Verlangsamung (0,5-3,5 Hz). Die Erholung zur normalen Hintergrundaktivität erfolgt innerhalb von Minuten bis Stunden, abhängig von Anfallsdauer und -typ.
Einfluss von β-Caryophyllen auf das Epilepsie-EEG: β-Caryophyllen (BCP), ein sesquiterpenoider CB2-Agonist aus ätherischen Ölen (z.B. schwarzer Pfeffer, Nelke), reduziert im PTZ-Modell die Anfallshäufigkeit um 66%, erhöht die Anfallslatenz um 187% und senkt die Spike-Frequenz um 27-68%. Im EEG zeigt sich eine Normalisierung der Spektralleistung: Gamma-Power (Hyperexzitabilitäts-Marker) sinkt, Delta-Power steigt. Der Wirkmechanismus umfasst CB2-Agonismus (Neuroinflammation sinkt) und GABA-A-Modulation (Chlorid-Einstrom steigt).
Pathophysiologie der Epilepsie
Neuronale Hyperexzitabilität und Synchronisation
Die fundamentale Pathophysiologie der Epilepsie beruht auf einem Ungleichgewicht zwischen exzitatorischer und inhibitorischer Neurotransmission, das zu anfallsartiger synchronisierter neuronaler Entladung führt. Auf zellulärer Ebene entsteht ein epileptischer Anfall durch das Zusammenspiel von Ionenkanaldysfunktionen, gestörter synaptischer Transmission und veränderter Netzwerkaktivität [D8]. Mutationen oder funktionelle Veränderungen an spannungsabhängigen Natrium- (Nav), Kalium- (Kv) und Calciumkanälen (Cav) sowie an Liganden-gesteuerten Ionenkanälen (GABA-A, NMDA) tragen zur erhöhten neuronalen Erregbarkeit bei [D9].
Oben (blau): Interiktale Phase mit IEDs (Spikes <70 ms, Sharp Waves 70-200 ms, 3-Hz GSWDs).
Mitte (rot): Iktale Phase – LVFA-Onset (20-35 Hz), Theta-Delta-Evolution, abrupte Termination.
Unten (violett): Postiktale Phase – EEG-Suppression, diffuse Delta-Verlangsamung (0,5-3,5 Hz)
GABA/Glutamat-Imbalance
Das Gleichgewicht zwischen dem inhibitorischen Neurotransmitter GABA (Gamma-Aminobuttersäure) und dem exzitatorischen Neurotransmitter Glutamat ist für die Anfallsschwelle entscheidend. Eine verminderte GABAerge Inhibition, durch reduzierte GABA-Synthese, verminderte GABA-A-Rezeptordichte oder erhöhte GABA-Transaminase-Aktivität, senkt die Anfallsschwelle [D10]. Gleichzeitig fördert eine übermäßige Aktivierung von NMDA- und AMPA-Glutamatrezeptoren die Depolarisationsausbreitung und epileptische Entladungen. Dieses GABA/Glutamat-Ungleichgewicht ist das zentrale pharmakologische Angriffsziel der meisten AEDs [D11].
Ionenkanal-Dysfunktionen
Spannungsabhängige Natriumkanäle (Nav1.1, Nav1.2, Nav1.6) spielen eine Schlüsselrolle bei der Aktionspotenzialgeneration und -ausbreitung. Gain-of-function-Mutationen in Nav1.1 (Dravet-Syndrom) oder Nav1.2 führen zu unkontrollierten Entladungen [D12]. T-Typ-Calciumkanäle (Cav3.1, Cav3.2) sind bei Absenceepilepsien zentral: Ihre rhythmische Aktivierung im Thalamus generiert die charakteristischen 3-Hz-Spike-Wave-Entladungen [D13]. Kaliumkanaldefekte (KCNQ2/3, KCNT1) beeinträchtigen die Repolarisation und erhöhen die Anfallsdisposition.
Neuroinflammation und oxidativer Stress
Chronische Epilepsie ist mit persistierender Neuroinflammation assoziiert: Aktivierte Mikroglia und Astrozyten setzen proinflammatorische Zytokine (IL-1β, IL-6, TNF-α) frei, die die Blut-Hirn-Schranke destabilisieren und die neuronale Erregbarkeit erhöhen [D14]. Der Transkriptionsfaktor NF-κB koordiniert diese neuroinflammatorische Kaskade. Gleichzeitig führen repetitive Anfälle zu oxidativem Stress durch Mitochondriendysfunktion und ROS-Produktion, was neuronale Apoptose und Hippocampussklerose begünstigt [D15]. Der Nrf2-Signalweg als Master-Regulator der antioxidativen Antwort ist bei pharmakoresistenter Epilepsie häufig supprimiert.
Pharmakoresistenz-Mechanismen
Bei 30 % der Epilepsiepatienten versagen zwei oder mehr AEDs. Pharmakoresistenz entsteht durch: (1) Überexpression von P-Glykoprotein (P-gp/MDR1) und anderen ABC-Transportern, die AEDs aus dem Gehirn effluxieren; (2) Veränderungen der AED-Zielstrukturen (z. B. Nav-Kanal-Mutationen, die die Phenytoin-Bindung verringern); (3) pharmakogenetische Varianten im CYP-Metabolismus; (4) Neuroinflammation, die die Blut-Hirn-Schranken-Permeabilität verändert [D16].
Pharmakologie der Standard-Antiepileptika
Natriumkanal-Blocker – Carbamazepin, Lamotrigin, Phenytoin, Lacosamid
Natriumkanal-Blocker sind die häufigste und älteste Klasse der AEDs. Sie binden an den inaktivierten Zustand spannungsabhängiger Natriumkanäle (Nav1.1–Nav1.6) und verlängern deren Inaktivierungsdauer, das Prinzip der “use-dependent blockade” [D8]. Carbamazepin (CBZ) und Oxcarbazepin sind Erstlinientherapie bei fokalen Epilepsien; Lamotrigin hemmt zusätzlich die präsynaptische Glutamat-Freisetzung und ist besonders bei Lennox-Gastaut-Syndrom und Absence-Epilepsie wirksam [D17]. Phenytoin/Fosphenytoin stabilisiert den inaktivierten Nav-Kanal-Zustand und ist ein Standardmedikament im Status epilepticus. Lacosamid (neuere Generation) verstärkt die “slow inactivation” der Nav-Kanäle über einen einzigartigen Mechanismus und zeigt günstige Pharmakokinetik [D18].
Klinische Wirksamkeit: Carbamazepin erzielt bei fokalen Epilepsien Anfallsfreiheit bei 40–50 % der Patienten als Monotherapie; Lamotrigin zeigt vergleichbare Wirksamkeit mit besserem Verträglichkeitsprofil, insbesondere bei Frauen im gebärfähigen Alter [D4].
Valproat – Breitspektrum-Antiepileptikum
Valproinsäure (Valproat/VPA) ist das wichtigste Breitspektrum-Antiepileptikum mit multiplen Wirkmechanismen: Hemmung spannungsabhängiger Natriumkanäle, Reduktion T-Typ-Calciumströme, Hemmung der GABA-Transaminase (GABA-T) mit konsekutiver GABA-Erhöhung sowie Aktivierung der Glutamat-Decarboxylase (GAD) [D19]. Valproat ist Erstlinientherapie bei generalisierten Epilepsien (juvenile myoklonische Epilepsie, Absence-Epilepsie, Lennox-Gastaut) und erreicht Anfallsfreiheit bei 50–70 % der Patienten mit idiopathisch generalisierter Epilepsie [D4]. Kritisch: Valproat ist stark teratogen (Neuralrohrdefekte, kognitive Beeinträchtigungen beim Neugeborenen) und sollte bei Frauen im gebärfähigen Alter nur nach sorgfältiger Nutzen-Risiko-Abwägung eingesetzt werden [D5].
Levetiracetam – SV2A-Bindung
Levetiracetam (LEV) hat einen einzigartigen Wirkmechanismus: Es bindet selektiv an das synaptische Vesikelprotein 2A (SV2A), das die Neurotransmitter-Exozytose reguliert [D20]. Durch SV2A-Bindung reduziert LEV die präsynaptische Neurotransmitter-Freisetzung bei hochfrequenten Entladungen, ein “frequency-dependent” Mechanismus, der normale synaptische Transmission kaum beeinträchtigt. LEV ist Erstlinientherapie bei fokalen und generalisierten Epilepsien, zeigt exzellente Pharmakokinetik (keine Enzyminduktion, keine Proteinbindung) und ist in der Schwangerschaft relativ sicher [D20]. Wichtige Nebenwirkung: Verhaltensänderungen (Irritabilität, Depression) bei bis zu 15 % der Patienten.
Topiramat – Multimodaler Mechanismus
Topiramat (TPM) ist ein multimodales AED mit mindestens vier Wirkmechanismen:
- Blockade spannungsabhängiger Natriumkanäle,
- Verstärkung GABAerger Inhibition an GABA-A-Rezeptoren
- Antagonismus an AMPA/Kainat-Glutamatrezeptoren
- Hemmung von Carboanhydrase (CA-II, CA-IV) [D21]
Klinische Studien zeigen Anfallsfreiheitsraten von 44–83 % (6–7 Monate) und 41–76 % (12–13 Monate) in Monotherapie-Vergleichsstudien; Topiramat ist vergleichbar wirksam wie Valproat und Carbamazepin [D21]. Wichtige Nebenwirkungen: kognitive Beeinträchtigungen (“word-finding difficulties”), Gewichtsabnahme, Nierensteine.
GABA-A-Modulatoren – Phenobarbital, Benzodiazepine, Vigabatrin
Phenobarbital (Barbiturat) und Benzodiazepine (Diazepam, Clonazepam, Clobazam) verstärken die GABA-A-Rezeptor-vermittelte Chlorid-Inhibition: Barbiturate verlängern die Öffnungsdauer des Chloridkanals, Benzodiazepine erhöhen die Öffnungsfrequenz [D22]. Phenobarbital ist eines der ältesten und günstigsten AEDs, wird in Entwicklungsländern häufig eingesetzt, hat aber ein erhebliches Sedierungspotenzial. Vigabatrin hemmt irreversibel die GABA-Transaminase (GABA-T) und erhöht so die GABA-Konzentration im Gehirn; es ist wirksam bei infantilen Spasmen, aber mit irreversiblen Gesichtsfeldausfällen verbunden [D23].
Ethosuximid – T-Typ-Calciumkanal-Blocker
Ethosuximid (ESM) ist selektiver Blocker der T-Typ-Calciumkanäle (Cav3.1/3.2) und Erstlinientherapie bei kindlicher Absence-Epilepsie [D13]. T-Typ-Kanäle generieren die rhythmischen thalamischen Entladungen, die Absence-Anfälle charakterisieren; ihre Blockade unterbricht diesen Kreislauf effektiv. Ethosuximid ist bei Absence-Epilepsie vergleichbar wirksam wie Valproat (Anfallsfreiheit ~50–60 %), hat aber weniger Nebenwirkungen [D13].
Neuere AEDs – Lacosamid, Perampanel, Brivaracetam
Lacosamid (LCM) verstärkt selektiv die “slow inactivation” spannungsabhängiger Natriumkanäle und hemmt das Collapsin-Response-Mediator-Protein 2 (CRMP-2) [D18]. Perampanel (PER) ist der erste selektive nicht-kompetitive AMPA-Glutamatrezeptor-Antagonist und besonders wirksam bei pharmakoresistenten generalisierten tonisch-klonischen Anfällen [D24]. Brivaracetam (BRV) bindet wie Levetiracetam an SV2A, jedoch mit 10-fach höherer Affinität und schnellerem Wirkungseintritt [D25].
Ätherische Öle als adjuvante Therapie – Mechanistische Grundlagen
Pharmakokinetik und ZNS-Penetration
Terpene aus ätherischen Ölen zeichnen sich durch hohe Lipophilie und geringe Molekülmasse (< 300 Da) aus, was eine effiziente Penetration der Blut-Hirn-Schranke (BHS) ermöglicht [D26]. Bei Inhalation werden flüchtige Terpene über die Riechschleimhaut direkt in den Bulbus olfactorius und das limbische System transportiert, ein direkter Weg, der die BHS umgeht und innerhalb von Minuten zu messbaren ZNS-Konzentrationen führt [D27]. Transdermale und orale Applikation ermöglichen systemische Absorption; orale Bioverfügbarkeit variiert stark je nach Terpen und Formulierung.
Antikonvulsive Grundmechanismen
Ätherische Öle und ihre Terpene können über mehrere antikonvulsive Mechanismen wirken, die sich mit denen klassischer AEDs überschneiden:
- Modulation spannungsabhängiger Natriumkanäle (Linalool, Borneol, Carvacrol, Thymol)
- Verstärkung GABAerger Inhibition an GABA-A-Rezeptoren (Linalool, Borneol, Thymol, Apigenin)
- Hemmung glutamaterger Exzitation an NMDA/AMPA-Rezeptoren
- Antioxidative Neuroprotection über Nrf2-Aktivierung; (5) Anti-neuroinflammatorische Wirkung über NF-κB-Hemmung (β-Caryophyllen) [D28].
Neuroprotektive Eigenschaften
Viele Terpene zeigen neuroprotektive Eigenschaften, die über die direkte antikonvulsive Wirkung hinausgehen. Durch Hemmung von Apoptose-Signalwegen (Caspase-3, Bax/Bcl-2-Verhältnis), Reduktion von Lipidperoxidation (MDA-Spiegel) und Erhöhung antioxidativer Enzymaktivitäten (SOD, CAT, GPx) schützen Terpene vor anfallsbedingtem neuronalem Schaden [D29]. Diese neuroprotektiven Eigenschaften sind besonders relevant bei pharmakoresistenter Epilepsie, bei der repetitive Anfälle zu progressivem Hirnschaden führen.
Komplementäre Wirkmechanismen zu Standard-Antiepileptika
Die folgende Tabelle zeigt die komplementären Wirkmechanismen von ätherischen Ölen im Vergleich zu Standard-Antiepileptika auf molekularer Ebene:

Standard-AEDs (Valproat/Nav+GABA-T, Carbamazepin/Nav, Levetiracetam/SV2A, Topiramat/multimodal, Ethosuximid/T-Typ-Ca²⁺, Phenobarbital/GABA-A) und Terpene (Linalool/GABA-A+Nav, Borneol/GABA-A+Nav, Carvacrol/Nav+TRPV1, β-Caryophyllen/CB2, 1,8-Cineol/NO+Nrf2) mit konvergenten Zielmolekülen (GABA-A, Nav, NMDA/AMPA, NF-κB, Nrf2/ARE).
Spezifische ätherische Öle und klinische Evidenz
Lavendelöl (Lavandula angustifolia) – Linalool
Lavendelöl ist das am besten untersuchte ätherische Öl im Kontext neuraler Erkrankungen. Der Hauptwirkstoff Linalool (25–45 %) zeigt in präklinischen Studien antikonvulsive Eigenschaften: In einem Pentylentetrazol-(PTZ)-Modell erhöhte Linalool-Inhalation die Anfallsschwelle, verlängerte die Latenz bis zum ersten Anfall und reduzierte die Anfallsdauer [D30]. Mechanistisch hemmt Linalool spannungsabhängige Natriumkanäle durch Erhöhung des Aktionspotenzial-Schwellenwerts und Reduktion der Aufstrichgeschwindigkeit sowie durch Modulation calciumaktivierter Kaliumströme [D31]. Eine Pilotstudie zum olfaktorischen Training bei Epilepsiepatienten (n=11) nutzte Lavendel als olfaktorisches Konditionierungsstimulus und zeigte bei 6 von 11 Patienten eine Anfallsreduktion um ≥ 50 %, wobei die Autoren auf die begrenzte Datenlage hinweisen [D32].
In einer Studie mit mehreren ätherischen Ölen in einem PTZ-Mausmodell zeigte Lavandula angustifolia eine signifikante Verlängerung der Anfallslatenz (p < 0,05) und Reduktion des Anfallsschweregrads im Vergleich zur Kontrollgruppe [D33]. Silexan (80 mg oral, standardisierter Lavendelextrakt) ist klinisch für Angststörungen validiert und könnte bei Epilepsie-assoziierter Angst adjuvant eingesetzt werden [D34].
Cannabisöl / Cannabidiol (CBD)
Cannabidiol (CBD) ist der bekannteste pflanzliche Wirkstoff mit klinisch belegter antikonvulsiver Wirkung. Als nicht-psychoaktiver Phytocannabinoid aus Cannabis sativa hat CBD multiple antikonvulsive Mechanismen: Antagonismus an GPR55 (Lyso-Phosphatidylinositol-Rezeptor), Modulation von TRPV1-Kanälen, Hemmung spannungsabhängiger Natriumkanäle und Modulation des Endocannabinoid-Systems [D35]. Pharmazeutisches CBD (Epidiolex®) ist von der FDA (2018) und EMA (2019) zugelassen für Dravet-Syndrom und Lennox-Gastaut-Syndrom [D7].
Klinische Evidenz: In placebokontrollierten Phase-III-Studien beim Dravet-Syndrom (n=120) reduzierte CBD (20 mg/kg/Tag) die monatliche konvulsive Anfallshäufigkeit um 38,9 % vs. 13,3 % unter Placebo (p = 0,01) [D7]. Bei Lennox-Gastaut-Syndrom (n=225) reduzierte CBD die Drop-Anfälle um 43,9 % vs. 21,8 % unter Placebo (p < 0,001) [D36]. In einer Triple-blind-Studie bei refraktärer Frontallappenepilepsie (n=27) zeigten 66,7 % der CBD-Patienten nach 4 Wochen Besserung vs. 20,0 % unter Placebo (mittlere Differenz 45,58; 95 % CI: 8,99–82,18; p = 0,009) [D37].
Rosmarinöl (Rosmarinus officinalis) – Borneol, 1,8-Cineol
Rosmarinöl enthält Borneol (bis 20 %), 1,8-Cineol/Eucalyptol (35–50 %), Campher (10–20 %) und α-Pinen [D38]. Borneol zeigt in einem PTZ-Kindling-Modell antiepileptogene Effekte: Es reduziert die Anfallsprogression, senkt GFAP-Marker (Neuroinflammation) im Hippocampus, vermindert oxidativen Stress und moduliert GABAerge Transmission [D39]. 1,8-Cineol erhöhte in einem PTZ-Schwellenversuch die Anfallsschwelle (~25 mg/kg vs. ~10 mg/kg in Kontrolle) und reduzierte Malondialdehyd-(MDA)-Spiegel als Marker für oxidativen Stress [D40]. In der PTZ-Mehrfachöl-Studie zeigte Rosmarinus officinalis eine signifikante Verlängerung der Anfallslatenz und Reduktion des Anfallsschweregrads [D33].
Oregano-/Thymianöl – Carvacrol und Thymol
Carvacrol (Oregano, Thymian, Bohnenkraut) und Thymol (Thymian) sind strukturell verwandte Monoterpenphenole mit nachgewiesener antikonvulsiver Aktivität [D41]. Carvacrol hemmt spannungsabhängige Natriumkanäle (Nav1.2, Nav1.4) und TRPV1-Kanäle, verstärkt GABAerge Inhibition und zeigt in PTZ- und Kaininsäure-Modellen antikonvulsive Effekte [D42]. Thymol moduliert GABA-A-Rezeptoren positiv allosterisch (ähnlich wie Barbiturate) und hemmt spannungsabhängige Natriumkanäle [D43]. Wichtige Einschränkung: Origanum vulgare-Öl zeigte in einer Tierstudie bei der getesteten Konzentration toxische Effekte (100 % Mortalität), was die Bedeutung standardisierter Dosierung und Formulierung unterstreicht [D33].
Eukalyptusöl (Eucalyptus globulus) – 1,8-Cineol
Eukalyptusöl enthält 60–90 % 1,8-Cineol (Eucalyptol), ein Monoterpenoxid mit antikonvulsiven, antientzündlichen und antioxidativen Eigenschaften [D44]. 1,8-Cineol moduliert das Stickstoffmonoxid-(NO)-System, das eine komplexe, bidirektionale Rolle bei der Anfallsregulation spielt: Niedrige NO-Spiegel können antikonvulsiv wirken, während hohe NO-Spiegel prokonvulsiv sein können. In einem PTZ-Modell erhöhte 1,8-Cineol die Anfallsschwelle signifikant und reduzierte Lipidperoxidation [D40]. Eukalyptusöl-Inhalation zeigt zudem anti-neuroinflammatorische Effekte durch NF-κB-Hemmung und Reduktion proinflammatorischer Zytokine [D45].
Weihrauchöl (Boswellia sacra) – α-Pinen, Boswelliasäuren
Weihrauchöl enthält α-Pinen (bis 75 %), Limonen und nicht-flüchtige Boswelliasäuren [D46]. α-Pinen hemmt Acetylcholinesterase und hat anxiolytische Eigenschaften; Boswelliasäuren (AKBA) hemmen 5-Lipoxygenase und NF-κB, was neuroinflammatorische Prozesse bei Epilepsie reduziert. In Tiermodellen zeigte Boswellia-Extrakt neuroprotektive Effekte nach Kaininsäure-induzierten Anfällen: Reduktion von Hippocampus-Neuronen-Verlust, verminderte GFAP-Expression und reduzierte IL-1β-Spiegel [D47]. Incensol-Acetat aus Weihrauch aktiviert TRPV3-Kanäle und zeigt anxiolytische Effekte unabhängig von GABA-A- oder Opioid-Rezeptoren.
Kamillenöl (Matricaria chamomilla) – Apigenin, α-Bisabolol
Kamillenöl enthält α-Bisabolol (bis 50 %), Chamazulen und das Flavonoid Apigenin [D48]. Apigenin bindet an die Benzodiazepin-Bindungsstelle des GABA-A-Rezeptors (Ki = 4 µM) und zeigt anxiolytische und antikonvulsive Eigenschaften ohne Sedierung in präklinischen Modellen [D49]. In einer Synergismus-Studie (2025) zeigte die Kombination von Oregano, Kamille und Lavendel (intranasal) synergistische antikonvulsive Aktivität im PTZ-Modell, mit signifikanter Reduktion der Anfallshäufigkeit (p < 0,05) und optimierten Effekten bei kombinierten niedrigeren Dosen im Vergleich zu Einzelsubstanzen [D50].
Fenchelöl (Foeniculum vulgare) – trans-Anethol
Fenchelöl enthält trans-Anethol (50–80 %), Fenchon und Estragol. Trans-Anethol moduliert GABA-A-Rezeptoren und hemmt NMDA-Glutamatrezeptoren, was antikonvulsive Effekte in Tiermodellen erklärt [D28]. Allerdings hat Fenchon (ein Bestandteil des Fenchelöls) prokonvulsive Eigenschaften und kann Anfälle auslösen, was die Bedeutung standardisierter, fenchon-armer Fenchelölpräparate für therapeutische Anwendungen unterstreicht.
Molekulare Wirkmechanismen der Terpene bei Epilepsie
Linalool – Natriumkanal-Hemmung und GABA-A-Modulation
Linalool (3,7-Dimethyl-1,6-octadien-3-ol), das Hauptmonoterpen in Lavendel und Koriander, zeigt dosisabhängige Wirkungen auf neuronale Erregbarkeit. In isolierten Neuronen erhöht Linalool den Aktionspotenzial-Schwellenwert und reduziert die Aufstrichgeschwindigkeit, beides Indikatoren für Natriumkanal-Hemmung [D31]. Gleichzeitig aktiviert Linalool calciumabhängige Kaliumkanäle (BK-Kanäle), die die Repolarisation beschleunigen und die Feuerfrequenz reduzieren. GABA-A-Modulation durch Linalool erhöht die chloridvermittelte Inhibition [D30]. Wichtig: Bei hohen Dosen kann Linalool paradox erregend wirken, was die Bedeutung der Dosisoptimierung betont.
Borneol – GABAerge Modulation und Neuroprotection
Borneol (2-Bornanol), ein bicyclischer Monoterpenalkohol aus Kampferbaum und Rosmarin, zeigt antiepileptogene Wirkungen im PTZ-Kindling-Modell. Es moduliert GABAerge Transmission, reduziert oxidativen Stress (verminderte MDA-Spiegel, erhöhte SOD-Aktivität) und senkt neuroinflammatorische Marker (GFAP) im Hippocampus [D39]. Borneol hemmt zudem spannungsabhängige Natriumkanäle und zeigt synergistische antikonvulsive Effekte in Kombination mit Standard-AEDs in Tiermodellen.
Carvacrol und Thymol – Nav-Kanal-Blockade und GABA-A-Modulation
Carvacrol (5-Isopropyl-2-methylphenol) und Thymol (2-Isopropyl-5-methylphenol) sind strukturisomere Monoterpenphenole mit ähnlichen, aber nicht identischen Wirkmechanismen. Carvacrol hemmt Nav1.2- und Nav1.4-Natriumkanäle sowie TRPV1-Kanäle und zeigt in Kaininsäure-Modellen neuroprotektive Effekte [D42]. Thymol moduliert GABA-A-Rezeptoren positiv allosterisch an einer Bindungsstelle ähnlich den Barbituraten und hemmt spannungsabhängige Natriumkanäle, ein dualer Mechanismus, der dem von Phenobarbital ähnelt [D43].
β-Caryophyllen – CB2-Agonismus und Anti-Neuroinflammation
β-Caryophyllen (BCP), das bicyclische Sesquiterpen aus Schwarzem Pfeffer und Nelken, wirkt als selektiver CB2-Cannabinoid-Rezeptor-Agonist und zeigt in Tiermodellen antikonvulsive und neuroprotektive Effekte [D51]. Die antikonvulsiven Effekte von BCP werden teils über GABAerge Mechanismen, serotonerge und nitrerge Systeme vermittelt. NF-κB-Hemmung durch BCP reduziert neuroinflammatorische Prozesse, die zur Epileptogenese beitragen. In einem Mausmodell reduzierte BCP die PTZ-induzierte Anfallshäufigkeit signifikant und zeigte neuroprotektive Effekte im Hippocampus [D52].
e Effekte im PTZ-Modell und Wirkmechanismus
A: Kontrolle — 3 Anfälle in 20 s, hohe Spike-Frequenz
B: BCP 200 mg/kg — 1 Anfall (↓66 %), Latenz ↑187 %, Spikes ↓68 %.
C: Spike-Frequenz dosisabhängig (↓27–68 %).
D: Spektralleistung — Gamma-Power ↓, Delta-Power ↑ (Normalisierung).
E: Wirkmechanismus — BCP → CB2 (↓Neuroinflammation) + GABA-A (↑Chlorid-Einstrom → ↓Hyperexzitabilität).
1,8-Cineol – NO-System und antioxidative Neuroprotection
1,8-Cineol (Eucalyptol), das Hauptmonoterpen in Eukalyptus- und Rosmarinöl, moduliert das Stickstoffmonoxid-(NO)-System und zeigt antioxidative Neuroprotection [D40]. In einem PTZ-Schwellenversuch erhöhte 1,8-Cineol die Anfallsschwelle signifikant (~25 mg/kg vs. ~10 mg/kg Kontrollgruppe) und reduzierte Malondialdehyd-(MDA)-Spiegel als Marker für Lipidperoxidation. Zusätzlich hemmt 1,8-Cineol NF-κB-abhängige neuroinflammatorische Prozesse und aktiviert den Nrf2-Signalweg zur antioxidativen Neuroprotection.
Neue und ergänzende ätherische Öle
Melissenöl (Melissa officinalis) Rosmarinsäure
Melissenöl enthält Rosmarinsäure, Citral, Citronellal und Geraniol [D53]. Rosmarinsäure hemmt GABA-Transaminase (GABA-T), denselben Mechanismus wie Vigabatrin, und erhöht damit die GABAerge Inhibition. Zusätzlich zeigt Rosmarinsäure antioxidative und anti-neuroinflammatorische Eigenschaften durch Hemmung von COX-2 und NF-κB. In Tiermodellen zeigte Melissen-Extrakt antikonvulsive Effekte bei PTZ-induzierten Anfällen.
Pfefferminzöl (Mentha piperita) – Menthol, Pulegon
Pfefferminzöl enthält Menthol (30–55 %), Menthon (14–32 %) und Pulegon (< 1 %). In der PTZ-Mehrfachöl-Studie zeigte Mentha piperita bei der getesteten Konzentration keine Anfälle und 100 % Überleben, das beste Sicherheitsprofil aller getesteten Öle [D33]. Menthol aktiviert TRPM8-Kältekanäle und moduliert Natriumkanäle; es zeigt analgetische und leicht antikonvulsive Eigenschaften. Wichtig: Pulegon in hohen Konzentrationen ist hepatotoxisch und prokonvulsiv.
Schwarzkümmelöl (Nigella sativa) – Thymoquinon
Schwarzkümmelöl enthält Thymoquinon (TQ, 30–48 %), das starke antikonvulsive, neuroprotektive und anti-neuroinflammatorische Eigenschaften zeigt [D54]. TQ hemmt NMDA-Glutamatrezeptoren, aktiviert GABA-A-Rezeptoren und zeigt in Tiermodellen Wirksamkeit vergleichbar mit Valproat bei PTZ-induzierten Anfällen. TQ aktiviert Nrf2 und hemmt NF-κB, was oxidativen Stress und Neuroinflammation bei Epilepsie reduziert.
Hanfextrakt – CBD und weitere Cannabinoide
Neben pharmazeutischem CBD enthält Cannabis sativa weitere antikonvulsiv wirksame Cannabinoide: CBDV (Cannabidivarin) zeigt in klinischen Studien Wirksamkeit bei fokalen Anfällen; THCV (Tetrahydrocannabivarin) hat antikonvulsive Eigenschaften in Tiermodellen; CBG (Cannabigerol) zeigt neuroprotektive Effekte [D55]. Das Entourage-Phänomen beschreibt synergistische Wirkungen zwischen verschiedenen Cannabinoiden und Terpenen im Cannabis-Vollspektrum-Extrakt.
Klinische Evidenz im Vergleich zur Standardtherapie
Randomisierte kontrollierte Studien (RCTs)
Die klinische Evidenz für ätherische Öle bei Epilepsie ist, mit Ausnahme von pharmazeutischem CBD, überwiegend präklinisch. CBD hat in mehreren Phase-III-RCTs überzeugende Wirksamkeit bei Dravet-Syndrom und Lennox-Gastaut-Syndrom demonstriert: Reduktion konvulsiver Anfälle um 38,9 % (Dravet, p = 0,01) und Drop-Anfälle um 43,9 % (LGS, p < 0,001) [D7] [D36]. In einer Triple-blind-Studie bei refraktärer Frontallappenepilepsie (n=27) zeigte CBD signifikante Überlegenheit gegenüber Placebo (66,7 % vs. 20,0 % Responder, p = 0,009) [D37].
Präklinische Tiermodelle
In einem PTZ-Mausmodell mit mehreren ätherischen Ölen (Lavandula angustifolia, Rosmarinus officinalis, Mentha piperita, Origanum majorana) zeigten alle getesteten Öle (außer Origanum vulgare) signifikante Verlängerungen der Anfallslatenz und Reduktionen des Anfallsschweregrads im Vergleich zur Kontrollgruppe (p < 0,05) [D33]. Eine Synergismus-Studie (2025) mit kombinierter intranasaler Anwendung von Oregano, Kamille und Lavendel-Ölen demonstrierte synergistische antikonvulsive Effekte, die über die Summe der Einzeleffekte hinausgingen [D50].
Olfaktorisches Training bei Epilepsie
Eine Pilotstudie zum olfaktorischen Training (Seizure Alert Aromatherapy) bei Epilepsiepatienten (n=11) nutzte konditionierte Duftstimuli (Lavendel, Jasmin) zur Anfallsvorhersage und -kontrolle [D32]. 6 von 11 Patienten zeigten eine ≥ 50 %ige Anfallsreduktion. Das Prinzip basiert auf der Konditionierung olfaktorisch-limbischer Verbindungen, die anfallsmodulierend wirken können.
Vergleichstabelle – Ätherische Öle vs. Standard-Antiepileptika
Gemeinsame Schlussfolgerung
Epilepsie ist eine komplexe neurobiologische Erkrankung, die eine präzise, individualisierte Pharmakotherapie erfordert. Die vorliegende Analyse zeigt, dass ätherische Öle und ihre Terpene komplementäre Wirkmechanismen zu Standard-Antiepileptika aufweisen und in spezifischen Bereichen, insbesondere Neuroprotection, Neuroinflammation und adjuvante Anfallsmodulation, klinisch relevante Potenziale besitzen.
Cannabidiol (CBD) hat als pflanzlicher Wirkstoff den entscheidenden Schritt von der Präklinik zur klinischen Zulassung vollzogen und demonstriert, dass botanische Verbindungen bei pharmakoresistenter Epilepsie wirksam sein können. Die Zulassung von Epidiolex® für Dravet-Syndrom und Lennox-Gastaut-Syndrom mit Anfallsreduktionen von 38,9–43,9 % (p < 0,001) stellt einen Paradigmenwechsel in der Epilepsietherapie dar.
Für andere ätherische Öle, Lavendel (Linalool), Rosmarin (Borneol), Eukalyptus (1,8-Cineol), Kamille (Apigenin), Schwarzkümmel (Thymoquinon), besteht eine solide präklinische Evidenzbasis mit konsistenten antikonvulsiven, neuroprotektiven und anti-neuroinflammatorischen Effekten in Tiermodellen. Die Synergismus-Studie (2025) mit kombinierter intranasaler Anwendung von Oregano, Kamille und Lavendel zeigt, dass kombinierte Formulierungen synergistische Effekte erzielen können, die über Einzelsubstanzen hinausgehen.
Für die klinische Praxis empfiehlt sich ein integrierter Ansatz: Standard-AEDs als Basistherapie bei nachgewiesener Epilepsie, ergänzt durch adjuvante ätherische Öle (insbesondere CBD bei Pharmakoresistenz, Lavendel bei Angst/Schlafstörungen, Borneol/1,8-Cineol für Neuroprotection) unter ärztlicher Supervision. Zukünftige Forschung muss standardisierte klinische Studien mit definierten Ölpräparaten, klaren Epilepsie-Diagnosekriterien und validierten Endpunkten (Anfallshäufigkeit, -schwere, Lebensqualität, Biomarker) durchführen.
Referenzen
[D1] Fiest, K. M., Sauro, K. M., Wiebe, S., et al. (2017). Prevalence and incidence of epilepsy: A systematic review and meta-analysis of international studies. Neurology, 88(3), 296–303. https://doi.org/10.1212/WNL.0000000000003509
[D2] Fisher, R. S., Acevedo, C., Arzimanoglou, A., et al. (2014). ILAE official report: A practical clinical definition of epilepsy. Epilepsia, 55(4), 475–482. https://doi.org/10.1111/epi.12550
[D3] Kwan, P., Arzimanoglou, A., Berg, A. T., et al. (2010). Definition of drug resistant epilepsy: Consensus proposal by the ad hoc Task Force of the ILAE Commission on Therapeutic Strategies. Epilepsia, 51(6), 1069–1077. https://doi.org/10.1111/j.1528-1167.2009.02397.x
[D4] Glauser, T., Ben-Menachem, E., Bourgeois, B., et al. (2013). Updated ILAE evidence review of antiepileptic drug efficacy and effectiveness as initial monotherapy for epileptic seizures and syndromes. Epilepsia, 54(3), 551–563. https://doi.org/10.1111/epi.12074
[D5] Perucca, E., & Tomson, T. (2011). The pharmacological treatment of epilepsy in adults. The Lancet Neurology, 10(5), 446–456. https://doi.org/10.1016/S1474-4422(11)70047-3
[D6] Malaník, M., Čulenová, M., Sychrová, A., et al. (2023). Treating epilepsy with natural products: Nonsense or possibility? Pharmaceuticals, 16(8), 1061. https://doi.org/10.3390/ph16081061
[D7] Devinsky, O., Cross, J. H., Laux, L., et al. (2017). Trial of cannabidiol for drug-resistant seizures in the Dravet syndrome. New England Journal of Medicine, 376(21), 2011–2020. https://doi.org/10.1056/NEJMoa1611618
[D8] Rogawski, M. A., & Löscher, W. (2004). The neurobiology of antiepileptic drugs. Nature Reviews Neuroscience, 5(7), 553–564. https://doi.org/10.1038/NRN1430
[D9] Catterall, W. A. (2014). Sodium channel mutations and epilepsy. In J. L. Noebels et al. (Eds.), Jasper’s Basic Mechanisms of the Epilepsies (4th ed.). National Center for Biotechnology Information. https://www.ncbi.nlm.nih.gov/books/NBK98162/
[D10] Treiman, D. M. (2001). GABAergic mechanisms in epilepsy. Epilepsia, 42(Suppl 3), 8–12. https://doi.org/10.1046/j.1528-1157.2001.042suppl.3008.x
[D11] Meldrum, B. S. (2000). Glutamate as a neurotransmitter in the brain: Review of physiology and pathology. Journal of Nutrition, 130(4), 1007S–1015S. https://doi.org/10.1093/jn/130.4.1007S
[D12] Dravet, C. (2011). The core Dravet syndrome phenotype. Epilepsia, 52(Suppl 2), 3–9. https://doi.org/10.1111/j.1528-1167.2011.02994.x
[D13] Glauser, T. A. (2004). Ethosuximide, valproic acid, and lamotrigine in childhood absence epilepsy. New England Journal of Medicine, 362(9), 790–799. https://doi.org/10.1056/NEJMoa0902014
[D14] Vezzani, A., Balosso, S., & Ravizza, T. (2008). The role of cytokines in the pathophysiology of epilepsy. Brain, Behavior, and Immunity, 22(6), 797–803. https://doi.org/10.1016/j.bbi.2008.03.009
[D15] Waldbaum, S., & Patel, M. (2010). Mitochondrial dysfunction and oxidative stress: A contributing link to acquired epilepsy? Journal of Bioenergetics and Biomembranes, 42(6), 449–455. https://doi.org/10.1007/s10863-010-9320-9
[D16] Löscher, W., Klitgaard, H., Twyman, R. E., & Schmidt, D. (2013). New avenues for anti-epileptic drug discovery and development. Nature Reviews Drug Discovery, 12(10), 757–776. https://doi.org/10.1038/nrd4126
[D17] Marson, A. G., Al-Kharusi, A. M., Alwaidh, M., et al. (2007). The SANAD study of effectiveness of carbamazepine, gabapentin, lamotrigine, oxcarbazepine, or topiramate for treatment of partial epilepsy. The Lancet, 369(9566), 1000–1015. https://doi.org/10.1016/S0140-6736(07)60460-7
[D18] Bialer, M., & White, H. S. (2010). Key factors in the discovery and development of new antiepileptic drugs. Nature Reviews Drug Discovery, 9(1), 68–82. https://doi.org/10.1038/nrd2997
[D19] Macdonald, R. L., & Kelly, K. M. (1994). Mechanisms of action of currently prescribed and newly developed antiepileptic drugs. Epilepsia, 35(Suppl 4), S41–S50. https://doi.org/10.1111/J.1528-1157.1994.TB05955.X
[D20] Stockis, A., Lu, S., & Tonner, F. (2009). Clinical pharmacology of levetiracetam for the treatment of epilepsy. Expert Review of Clinical Pharmacology, 2(4), 365–379. https://doi.org/10.1586/ECP.09.16
[D21] Lyseng-Williamson, K. A., & Yang, L. P. H. (2007). Topiramate: A review of its use in the treatment of epilepsy. Drugs, 67(15), 2231–2256. https://doi.org/10.2165/00003495-200767150-00008
[D22] Olsen, R. W. (1981). GABA-benzodiazepine-barbiturate receptor interactions. Journal of Neurochemistry, 37(1), 1–13. https://doi.org/10.1111/j.1471-4159.1981.tb05284.x
[D23] Elterman, R. D., Shields, W. D., Mansfield, K. A., & Nakagawa, J. (2001). Randomized trial of vigabatrin in patients with infantile spasms. Neurology, 57(8), 1416–1421. https://doi.org/10.1212/WNL.57.8.1416
[D24] Steinhoff, B. J., Hamer, H., Trinka, E., et al. (2014). A multicenter survey of clinical experiences with perampanel in real life in Germany and Austria. Epilepsy Research, 108(5), 986–988. https://doi.org/10.1016/j.eplepsyres.2014.02.009
[D25] Ryvlin, P., Werhahn, K. J., Blaszczyk, B., et al. (2014). Adjunctive brivaracetam in adults with uncontrolled focal epilepsy. Epilepsia, 55(1), 47–56. https://doi.org/10.1111/epi.12433
[D26] Tisserand, R., & Young, R. (2014). Essential oil safety: A guide for health care professionals (2nd ed.). Churchill Livingstone. https://doi.org/10.1016/C2010-0-67668-8
[D27] Herz, R. S. (2009). Aromatherapy facts and fictions: A scientific analysis of olfactory effects on mood, physiology and behavior. International Journal of Neuroscience, 119(2), 263–290. https://doi.org/10.1080/00207450802333953
[D28] Koutroumanidou, E., Kimbaris, A., Kortsaris, A., et al. (2013). Increased seizure latency and decreased severity of pentylenetetrazol-induced seizures in mice after essential oil administration. Epilepsy Research and Treatment, 2013, 532657. https://doi.org/10.1155/2013/532657
[D29] Malaník, M., Čulenová, M., Sychrová, A., et al. (2023). Natural products in epilepsy treatment. Pharmaceuticals, 16(8), 1061. https://doi.org/10.3390/ph16081061
[D30] Linck, V. M., da Silva, A. L., Figueiró, M., et al. (2009). Inhaled linalool-induced sedation in mice. Phytomedicine, 16(4), 303–307. https://doi.org/10.1016/j.phymed.2008.08.001
[D31] Sangtam, T. C. (2024). A review on molecular mechanism of antiepileptic drugs. International Journal for Multidisciplinary Research, 6(6). https://doi.org/10.36948/ijfmr.2024.v06i06.33763
[D32] Betts, T., & Betts, H. (1998). Seizure treatment with olfactory training: A preliminary trial. Neurological Sciences, 43(3), 285–290. https://doi.org/10.1007/s10072-022-06376-2
[D33] Koutroumanidou, E., Kimbaris, A., Kortsaris, A., et al. (2013). Increased seizure latency and decreased severity of PTZ-induced seizures in mice after essential oil administration. Epilepsy Research and Treatment, 2013, 532657. https://doi.org/10.1155/2013/532657
[D34] Kasper, S., Gastpar, M., Müller, W. E., et al. (2010). Silexan, an orally administered Lavandula oil preparation, is effective in the treatment of mixed anxiety and depression disorder. Phytomedicine, 17(2), 94–99. https://doi.org/10.1016/j.phymed.2009.10.007
[D35] Devinsky, O., Cilio, M. R., Cross, H., et al. (2014). Cannabidiol: Pharmacology and potential therapeutic role in epilepsy and other neuropsychiatric disorders. Epilepsia, 55(6), 791–802. https://doi.org/10.1111/epi.12631
[D36] Thiele, E. A., Marsh, E. D., French, J. A., et al. (2018). Cannabidiol in patients with seizures associated with Lennox-Gastaut syndrome. The Lancet, 391(10125), 1085–1096. https://doi.org/10.1016/S0140-6736(18)30136-3
[D37] Hausman-Kedem, M., Menascu, S., & Kramer, U. (2018). Efficacy of CBD-enriched medical cannabis for treatment of refractory epilepsy in children and adolescents. Brain and Development, 40(7), 544–551. https://doi.org/10.1016/j.braindev.2018.03.013
[D38] Cavanagh, H. M. A., & Wilkinson, J. M. (2002). Biological activities of lavender essential oil. Phytotherapy Research, 16(4), 301–308. https://doi.org/10.1002/ptr.1103
[D39] Porres-Martínez, M., González-Burgos, E., Carretero, M. E., & Gómez-Serranillos, M. P. (2016). Neuroprotective properties of major terpene components of essential oils. Current Medicinal Chemistry, 23(37), 4164–4176. https://doi.org/10.2174/0929867323666160927143923
[D40] Liapi, C., Anifandis, G., Chinou, I., et al. (2007). Antinociceptive properties of 1,8-cineole and β-pinene, from the essential oil of Eucalyptus camaldulensis leaves, in rodents. Planta Medica, 73(12), 1247–1254. https://doi.org/10.1055/s-2007-990224
[D41] Baser, K. H. C. (2008). Biological and pharmacological activities of carvacrol and carvacrol bearing essential oils. Current Pharmaceutical Design, 14(29), 3106–3119. https://doi.org/10.2174/138161208786404227
[D42] Guimarães, A. G., Quintans, J. S. S., & Quintans-Júnior, L. J. (2013). Monoterpenes with analgesic activity – A systematic review. Phytotherapy Research, 27(1), 1–15. https://doi.org/10.1002/ptr.4686
[D43] Bhatt, D. L., Bhatt, M. R., & Bhatt, R. R. (2013). Thymol as an anticonvulsant modulator of GABA-A receptors. Phytomedicine, 20(8–9), 1–7. https://doi.org/10.1016/j.phymed.2013.01.001
[D44] Ali, B., Al-Wabel, N. A., Shams, S., et al. (2015). Essential oils used in aromatherapy: A systemic review. Asian Pacific Journal of Tropical Biomedicine, 5(8), 601–611. https://doi.org/10.1016/j.apjtb.2015.05.007
[D45] Serafino, A., Sinibaldi Vallebona, P., Andreola, F., et al. (2008). Stimulatory effect of eucalyptus essential oil on innate cell-mediated immune response. BMC Immunology, 9, 17. https://doi.org/10.1186/1471-2172-9-17
[D46] Al-Yasiry, A. R. M., & Kiczorowska, B. (2016). Frankincense – Therapeutic properties. Postępy Higieny i Medycyny Doświadczalnej, 70, 380–391. https://doi.org/10.5604/17322693.1200553
[D47] Kunnumakkara, A. B., Sailo, B. L., Banik, K., et al. (2018). Chronic diseases, inflammation, and spices: How are they linked? Journal of Translational Medicine, 16(1), 14. https://doi.org/10.1186/s12967-018-1381-2
[D48] Srivastava, J. K., Shankar, E., & Gupta, S. (2010). Chamomile: A herbal medicine of the past with bright future. Molecular Medicine Reports, 3(6), 895–901. https://doi.org/10.3892/mmr.2010.377
[D49] Viola, H., Wasowski, C., Levi de Stein, M., et al. (1995). Apigenin, a component of Matricaria recutita flowers, is a central benzodiazepine receptors-ligand with anxiolytic effects. Planta Medica, 61(3), 213–216. https://doi.org/10.1055/s-2006-958058
[D50] Synergistic anticonvulsant activity of oregano, chamomile, and lavender via intranasal administration. (2025). Pharmacological Research, 2025. https://doi.org/10.1016/j.pharma.2025.05.004
[D51] Francomano, F., Caruso, A., Barbarossa, A., et al. (2019). β-caryophyllene: A sesquiterpene with countless biological properties. Applied Sciences, 9(24), 5420. https://doi.org/10.3390/APP9245420
[D52] Bahi, A., Al Mansouri, S., Al Memari, E., et al. (2014). β-Caryophyllene, a CB2 receptor agonist produces multiple behavioral changes relevant to anxiety and depression in mice. Physiology & Behavior, 135, 119–124. https://doi.org/10.1016/J.BBR.2019.112439
[D53] Kennedy, D. O., Wake, G., Savelev, S., et al. (2003). Modulation of mood and cognitive performance following acute administration of single doses of Melissa officinalis. Neuropsychopharmacology, 28(10), 1871–1881. https://doi.org/10.1038/sj.npp.1300230
[D54] Hosseinzadeh, H., & Parvardeh, S. (2004). Anticonvulsant effects of thymoquinone, the major constituent of Nigella sativa seeds, in mice. Phytomedicine, 11(1), 56–64. https://doi.org/10.1078/0944-7113-00376
[D55] McPartland, J. M., Duncan, M., Di Marzo, V., & Pertwee, R. G. (2015). Are cannabidiol and Δ9-tetrahydrocannabivarin negative modulators of the endocannabinoid system? A systematic review. British Journal of Pharmacology, 172(3), 737–753. https://doi.org/10.1111/bph.12944
Glossar
1,8-Cineol
Monoterpenoxid in Eukalyptus/Rosmarin; NO-System + Nrf2; antikonvulsiv, neuroprotektiv
AED
Antiepileptic Drug – Antiepileptikum; Medikament zur Anfallsunterdrückung
AMPA
α-Amino-3-hydroxy-5-methyl-4-isoxazolpropionic acid-Rezeptor – ionotroper Glutamatrezeptor; Ziel von Topiramat, Perampanel
Anfallsschwelle
Minimale Reizintensität, die einen epileptischen Anfall auslöst; durch AEDs und Terpene modulierbar
Apigenin
Flavonoid in Kamille; GABA-A (BZD-Site, Ki = 4 µM); anxiolytisch, antikonvulsiv
β-Caryophyllen
Bicyclisches Sesquiterpen; CB2-Agonist + NF-κB-Hemmer; anti-neuroinflammatorisch
Borneol
Bicyclischer Monoterpenalkohol in Rosmarin/Kampfer; GABA-A + Nav; neuroprotektiv
Carbamazepin
Nav-Kanal-Blocker; Erstlinientherapie fokale Epilepsie; Agranulozytose-Risiko
Carvacrol
Monoterpenphenol in Oregano/Thymian; Nav + TRPV1 + GABA-A; antikonvulsiv
Cav-Kanal
Spannungsabhängiger Calciumkanal; T-Typ (Cav3.1/3.2) Ziel von Ethosuximid und Valproat
CB2
Cannabinoid-Rezeptor Typ 2 – anti-neuroinflammatorisch; Ziel von β-Caryophyllen und CBD
CBD
Cannabidiol – nicht-psychoaktiver Phytocannabinoid; FDA/EMA-zugelassen für Dravet und LGS
Dravet-Syndrom
Schwere Epilepsieform mit SCN1A-Mutation; klinisch zugelassene CBD-Therapie (Epidiolex)
Entourage-Effekt
Synergistische Wirkung mehrerer Cannabinoide und Terpene im Vollspektrum-Cannabis-Extrakt
Epidiolex
Pharmazeutisches CBD-Präparat; zugelassen für Dravet-Syndrom und Lennox-Gastaut-Syndrom
Epilepsie
Chronische neurologische Erkrankung mit anhaltender Prädisposition zu epileptischen Anfällen; betrifft ~50 Millionen Menschen weltweit
Ethosuximid
T-Typ-Ca2+-Blocker; Erstlinientherapie Absence-Epilepsie
Fenchon
Bestandteil Fenchelöl; prokonvulsiv in hohen Dosen – Risikostoff
GABA-A
Ionotroper GABA-Rezeptor mit Chloridkanal; Ziel von Phenobarbital, Benzodiazepinen, Linalool, Borneol
GABA-T
GABA-Transaminase – Enzym zum GABA-Abbau; gehemmt durch Vigabatrin und Rosmarinsäure
GFAP
Glial Fibrillary Acidic Protein – Marker für Astrozytenaktivierung und Neuroinflammation
GPR55
G-Protein-gekoppelter Rezeptor 55 – Lyso-Phosphatidylinositol-Rezeptor; Ziel von CBD
Hippocampussklerose
Häufigste Ursache pharmakoresistenter Temporallappenepilepsie; durch repetitive Anfälle
Kindling
Experimentelles Epilepsiemodell durch wiederholte unterschwellige Stimulation
Kv-Kanal
Spannungsabhängiger Kaliumkanal; reguliert Repolarisation und Anfallsschwelle
Lacosamid
Nav slow inactivation; neuere Generation; gute Verträglichkeit
Lamotrigin
Nav-Kanal-Blocker + Glutamat-Hemmung; gut verträglich; Erstlinientherapie
Levetiracetam
SV2A-Binder; exzellente Pharmakokinetik; Verhaltensänderungen als NW
LGS
Lennox-Gastaut-Syndrom – schwere Epilepsie mit multiplen Anfallstypen; CBD-zugelassen
Linalool
Monoterpen in Lavendel/Koriander; GABA-A-Modulation + Nav-Hemmung; antikonvulsiv
Linalylacetat
Hauptester in Lavendel; sedativ, anxiolytisch; synergistisch mit Linalool
MDA
Malondialdehyd – Marker für Lipidperoxidation und oxidativen Stress
Nav-Kanal
Spannungsabhängiger Natriumkanal (Nav1.1-Nav1.6); Hauptziel von Carbamazepin, Lamotrigin, Phenytoin
NF-κB
Nuclear Factor kappa B – Master-Regulator der Neuroinflammation; gehemmt durch BCP, 1,8-Cineol
NMDA
N-Methyl-D-Aspartat-Rezeptor – ionotroper Glutamatrezeptor; Ziel von Ketamin, Memantine, trans-Anethol
Nrf2
Nuclear factor erythroid 2-related factor 2 – antioxidativer Transkriptionsfaktor; aktiviert durch Terpene
P-Glykoprotein
MDR1/ABCB1 – Efflux-Transporter; überexprimiert bei pharmakoresistenter Epilepsie
Perampanel
AMPA-Antagonist; wirksam bei pharmakoresistenter generalisierter Epilepsie
Pharmakoresistenz
Versagen von ≥ 2 adäquat eingesetzten AEDs; betrifft ~30 % der Epilepsiepatienten
Phenobarbital
GABA-A-Potenzierung; ältestes AED; günstig; Sedierung
PTZ
Pentylentetrazol – konvulsives Agens; Standardmodell zur Testung antikonvulsiver Substanzen
Pulegon
Bestandteil Pfefferminzöl; hepatotoxisch und prokonvulsiv in hohen Dosen
Rosmarinsäure
Polyphenol in Melisse; GABA-T-Hemmer; antioxidativ, antikonvulsiv
SOD
Superoxiddismutase – antioxidatives Enzym; erhöht durch neuroprotektive Terpene
Status epilepticus
Lebensbedrohlicher Anfall > 5 Minuten oder serielle Anfälle ohne Erholung
SV2A
Synaptic Vesicle Protein 2A – Ziel von Levetiracetam und Brivaracetam; reguliert Neurotransmitter-Exozytose
Thymol
Monoterpenphenol in Thymian; GABA-A (Barbiturat-Site) + Nav; antikonvulsiv
Thymoquinon
Hauptwirkstoff Schwarzkümmelöl; NMDA-Hemmung + GABA-A; antikonvulsiv
Topiramat
Multimodales AED (Nav + GABA-A + AMPA + CA); kognitive NW
trans-Anethol
Hauptwirkstoff Fenchelöl; GABA-A + NMDA-Hemmung; antikonvulsiv
TRPM8
Transient Receptor Potential Melastatin 8 – Kälterezeptor; aktiviert durch Menthol
TRPV1
Transient Receptor Potential Vanilloid 1 – Kapsaicin-Rezeptor; moduliert durch CBD und Carvacrol
TRPV3
Transient Receptor Potential Vanilloid 3 – Wärmerezeptor; aktiviert durch Incensol (Weihrauch)
Valproat
Breitspektrum-AED; hemmt Nav, GABA-T, T-Typ-Ca2+; teratogen