Índice
Atualizado – 30 de Abril de 2026
Um trabalho comparativo sobre a terapia padrão para TDAH/DDA e aromaterapia com óleos essenciais terapeuticamente aprovados, testados lote a lote por análise GC/MS. (Situação a 04.2026).
TDAH/TD - Óleos Essenciais Explicados
Um resumo acessível do relatório científico para todos os que desejam saber mais sobre o apoio natural para a TDAH
O que é TDAH?
TDAH significa Transtorno de défice de atenção e hiperatividade, ADS para a variante sem hiperatividade (Transtorno de Défice de Atenção). Nenhuma delas é uma invenção ou um erro de educação, são verdadeiras doenças neurológicas em que o cérebro está com um "cableamento" diferente.
A imagem por trás: Imagine o cérebro como uma rádio. No cérebro com TDAH, o emissor salta constantemente entre frequências, às vezes muito alto, às vezes muito baixo, raramente no canal certo. Isso torna difícil concentrar-se, ficar quieto ou controlar impulsos.
O que acontece no cérebro com o TDAH?
O problema central reside em dois neurotransmissores:
Dopamina – o “mensageiro da recompensa e motivação”
Na TDAH, a dopamina é “limpa” demasiado depressa (pelo transportador de dopamina DAT). Isto leva a uma sensação de falta de recompensa e motivação para as tarefas quotidianas. O cérebro está constantemente à procura de estimulação, daí a impulsividade e a procura de risco.
Norepinefrina – o “mensageiro da atenção e do foco”
Pouca noradrenalina no córtex pré-frontal (a “área de comando” do cérebro) – Leva a problemas de concentração, esquecimento, dificuldades em planear
Quais áreas do cérebro são afetadas?
- Córtex pré-frontal
Responsável pelo planeamento, controlo de impulsos, concentração – hipoativo no TDAH
- EstrIado (Gânglios da base)
Centro de recompensa – menos sensível no TDAH
- Cerebelo
Tempestividade e coordenação – ligeiramente alteradas no TDAH
Com que frequência ocorre o TDAH?
Em crianças e adolescentes, a doença psiquiátrica mais comum é com 5 a 7 %, em adultos 2,5 a 4 %, muitos adultos não sabem que têm TDAH.
Como se manifesta o TDAH?
Como é que o TDAH é normalmente tratado?
O medicamento principal – Metilfenidato (Ritalina, Concerta, Medikinet)
O metilfenidato (MPH) é o medicamento mais prescrito para TDAH e a terapêutica de primeira linha.
Como funciona?
O metilfenidato bloqueia o transportador de dopamina (DAT), a “bomba de limpeza” para a dopamina. Quando menos dopamina é limpa, mais dela permanece entre as células nervosas, permitindo que o cérebro se concentre melhor.
Os números por detrás
Uma dose de 20 mg bloqueia aproximadamente. 54 % as bombas de limpeza de dopamina no cérebro, 40 mg bloqueiam aproximadamente. 72 %.
O efeito inicia-se após 30-90 minutos e dura 4-12 horas, dependendo da formulação.
Qual é a sua eficácia?
Com 70-80 % O metilfenidato tem um bom efeito clínico em pacientes: melhorias na atenção, impulsividade e desempenho escolar estão bem documentadas.
Formulações
- De curta duração (por exemplo, Ritalina): 4–6 horas, deve ser tomada várias vezes ao dia
- Deficiente (por ex. Concerta, Medikinet retard): 8–12 horas, uma vez por dia
Efeitos colaterais
– Diminuição do apetite (efeito secundário mais comum)
– Perturbações do sono (se tomado demasiado tarde)
– Dores de cabeça, dores de estômago (geralmente no início)
– Lige aumento da frequência cardíaca e da pressão arterial
– Alterações de humor, irritabilidade (raro)
Mais medicamentos
Atomoxetina (Strattera)
– Nenhum estimulante, inibe o transportador de noradrenalina (NET)
– Também funciona para TDAH sem risco de dependência
– Demora 4-6 semanas até atingir o efeito máximo
– Muito adequado em caso de transtorno de ansiedade ou transtorno de tiques simultâneo
Anfetamina (menos comum na Alemanha)
– Lisdexanfetamina (Vyvanse): Aprovado na Alemanha desde 2013 para adultos
– Efetua mais e por mais tempo que o metilfenidato
Guanfacina (Intuniv)
– Para crianças e adolescentes em que os estimulantes não são adequados
– Atua nos recetores de noradrenalina no córtex pré-frontal
Óleos essenciais para TDAH – como pode funcionar?
Os óleos essenciais podem apoiar o cérebro com DDAH de várias formas:
- Sobre o olfato para o cérebro
Moléculas de odor ativam o sistema límbico (emoções, motivação) e o córtex pré-frontal (concentração) – de forma direta e rápida - Sobre sistemas de neurotransmissores
Certos terpenos afetam a dopamina, a noradrenalina, a serotonina e o GABA - Complementar ao Metilfenidato
O metilfenidato atua no DAT/NET – os óleos essenciais atuam noutros sistemas (GABA-A, CB2, TRPM8, SERT), sendo assim um complemento potencial.
Restrição importante
A investigação sobre óleos essenciais na TDAH ainda está numa fase inicial. A maioria dos estudos foi realizada em adultos saudáveis, não em pacientes com TDAH. As provas clínicas diretas ainda são limitadas.
Que óleos essenciais podem ajudar na TDAH?
Hortelã-pimenta – o óleo de concentração n.º 1
Hortelã-pimenta (Mentha × piperita) tem a evidência mais forte de melhoria da atenção.
- O que está dentro?
Mentol (30–50 %)
Mentonol (10–30 %)
1,8-Cineol (5–10 %) - O que faz a menta?
Ativa os recetores TRPM8 – “recetores do frio” no sistema nervoso, que ativam o cérebro
Inibe a enzima que degrada o neurotransmissor acetilcolina
Modula os recetores GABA-A (levemente sedativo em caso de hiperatividade) - Estudo clínico (n=24)
100 µL de óleo de hortelã-pimenta (encapsulado) melhoraram significativamente a atenção sustentada no RVIP (Rapid Visual Information Processing) após 1-3 horas; reduziram a fadiga e melhoraram a aritmética mental - Caraterística especial
Hortelã-pimenta promove focada Atenção (ao contrário do lavanda, que tende a dispersar a atenção) - Como aplicar
2 gotas num lenço de papel, pouco antes de sessões de estudo ou trabalho; difusor na sala de estudo
Alecrim – para a memória e a vigília
Alecrim (Rosmarinus officinalisé conhecida desde a antiguidade como a “erva da memória”, e com razão.
- O que está dentro?
1,8-Cineol (20–50 %)
Cânfora (10–20 %)
α-Pineno (10–15 %) - O que faz 1,8-cineol?
Inibe a enzima acetilcolinesterase, que decompõe o neurotransmissor (semelhante a medicamentos para Alzheimer!)
Ativa o sistema nervoso, aumenta o estado de alerta e a atenção.
Anti-inflamatório e antioxidante no cérebro - Estudo clínico (n=144)
A aromaterapia com alecrim melhorou significativamente a memória geral e a memória secundária, em comparação com o grupo de lavanda e o grupo de controlo - Para TDAH
Particularmente útil para problemas de memória, “névoa cerebral” e sonolência matinal - Como aplicar
Manhãs no difusor (5 gotas), inalação antes de testes ou tarefas importantes - Atenção: Não usar à noite, é demasiado ativador; especial cuidado em caso de epilepsia devido ao teor de cânfora!
Lavanda – contra ansiedade e problemas de sono
Lavanda (Lavandula angustifolia) é o melhor óleo para problemas de ansiedade e sono que acompanham o TDAH.
- O que está dentro?
Linalol (25–45 %)
Acetato de linalilo (25–50 %) - O que faz o linalol?
Ativa recetores GABA-A, o “travão” do cérebro
Modula serotonina, dopamina e noradrenalina
Reduz o Cortisol (Hormona do Stress) em 24–38 % - Particularmente útil para TDAH
Dificuldade em adormecer (muito comum no TDAH)
Begleitende Angststörungen (bei ca. 50 % der ADHS-Patienten)
Desregulação emocional e irritabilidade - Aviso importante
Lavanda consegue isso Prejudicar a memória de trabalho a curto prazo, por isso não o use durante as fases de aprendizagem, mas sim apenas à noite ou para relaxamento direcionado - estudar
Silexan (80 mg de óleo de lavanda por dia em cápsulas) teve um efeito comparável ao do Lorazepam em distúrbios de ansiedade - Como aplicar
À noite no difusor (5 gotas), 2 gotas na almofada
Madeira de Cedro – Oxigenação e Foco
Madeira de cedro (Cedro-do-atlas / Cedro-vermelho-da-virgíniaé tradicionalmente utilizado no TDAH.
- O que está dentro?
α-Cedreno
β-Cedreno
Cedrol - O que faz
Melhora a oxigenação cerebral; calmante; ativa o parassimpático - Específico para TDAH
Godfrey (2001) relatou efeitos positivos em crianças com TDAH;
Cedrol reduziu a frequência cardíaca e respiratória em estudos. - Como aplicar
No difusor durante atividades calmas; combina bem com lavanda
Vetiver – o aroma de ligação à terra
Vetiver (Chrysopogon zizanioidestem um aroma profundo e terroso, muitas vezes descrito como “um bálsamo para espíritos inquietos”.
- O que faz
Ansiolítico (alivia a ansiedade); acalma o sistema nervoso; melhora o sono - Específico para TDAH
Springer et al. (2018) relataram melhorias em crianças com TDAH após 30 dias de inalação 3 vezes ao dia - Para quem
Particularmente na variante hiperativa da TDAH com inquietação interior
Canela – o único estudo direto sobre TDAH
Canela (Cinamomo verdadeiro) tem a única prova: o único estudo clínico diretamente em crianças com TDAH.
- O que está dentro?
Zimtaldeído (60–75 %)
Eugenol (5–10 %) - Estudo sobre TDAH (Chen et al., 2008)
A combinação de reabilitação + aromaterapia com canela (1 % de canela, inalação nasal) durante 6 meses demonstrou resultados significativamente melhores no questionário SNAP-IV em comparação com a reabilitação isolada (p < 0,05). - Mecanismo
Os metabolitos do zimtaldeído podem ter efeitos dopaminérgicos - Restrição
O estudo tem falhas metodológicas (amostra pequena, cegamento pouco claro) - Como aplicar
Económico no difusor, combinado com outros óleos
Pimenta-preta (β-Cariofileno) – contra neuroinflamação
β-cariofileno de pimenta preta, lavanda e outras plantas:
- Ativa recetores de canabinóides CB2 sem efeito psicoativo
- Reduz a neuroinflamação (inflamação no cérebro)
- Interessante alterações no TDAH com sinais inflamatórios concomitantes ou problemas de humor
- Boa combinação com outros óleos
Os óleos em resumo – Quando usar qual óleo?
Rotina Prática para TDAH
Rotina matinal (Ativação + Foco):
- Difusor: Alecrim (4 gotas) + Hortelã-pimenta (2 gotas) durante 15–20 minutos
- Ou: Hortelã-pimenta num lenço de papel, respirar profundamente 3 vezes antes da escola/trabalho
- Efeito: Vigilância, memória, concentração
Tempo de estudo / Fase de trabalho:
- Difusor: Hortelã-pimenta (3 gotas) + Limão (2 gotas) durante 20 minutos, depois 30 minutos de pausa
- Atenção: Sem lavanda durante os estudos!
- Efeito: Atenção sustentada, foco
Tarde (descanso após a escola):
- Difusor: Madeira de cedro (3 gotas) + Bergamota (2 gotas) durante 20 minutos
- Efeito: Alívio do stress, regulação emocional
Rotina noturna (Descontrair + Dormir):
- Difusor: Lavanda (4 gotas) + Vetiver (2 gotas) 30 minutos antes de dormir
- Ou: 2 gotas de lavanda no travesseiro
- Efeito: Adormecer, qualidade do sono
Instruções de dosagem para o difusor
Importante: Na adaptação olfativa, o cheiro do óleo mal se sente após 20 a 30 minutos, mas continua a ter efeito. Para que os recetores possam recuperar e o efeito de habituação seja „redefinido“, é preciso respeitar os intervalos!
O que diz a ciência realmente?
Conclusão
A evidência é promissor mas ainda limitado. Mecanisticamente faz sentido, mas ainda faltam grandes estudos clínicos em pacientes com TDAH. Isto não significa que não funcione, significa que precisamos de mais investigação.
Informações de Segurança Importantes
Considerações especiais para a DDA:
Hipersensibilidade sensorial
Muitos indivíduos com TDAH (40–60 %) têm uma sensibilidade olfativa aumentada. Comece sempre com meia dose E aumente gradualmente. Se um aroma for desagradável: pare imediatamente.
Interações com metilfenidato
- Canela
Pode ter um efeito dopaminérgico, o que permite um efeito teoricamente amplificador com MPH, pelo que observar a frequência cardíaca e a pressão arterial
- Lavanda
Pode ter um efeito serotoninérgico, tenha cuidado ao tomar antidepressivos ao mesmo tempo
- Alecrim
Pode ter um efeito ativador, pelo que não deve ser aplicado pouco antes de ir dormir.
Em crianças
– Menos de 3 anos: Sem óleos essenciais
– 3–6 anos: Concentrações muito baixas (1–2 gotas), em local bem ventilado
– > 6 anos: Dosagem normal possível – Sem contato direto com a pele sem diluição
Regras gerais:
- Diluir sempre com um óleo transportador (por exemplo, óleo de coco fracionado não gorduroso) (2–3 %)
- Utilizar um espaço bem ventilado
- Fazer pausas (não dispersar o dia todo)
- Em caso de asma ou problemas respiratórios: consultar o médico
- Óleos essenciais são sem substituição para metilfenidato ou outras terapias para TDAH
FAQ – Perguntas Frequentes
Posso substituir o metilfenidato por óleos essenciais?
Não. Os óleos essenciais são um complemento, não um substituto. O metilfenidato tem forte evidência clínica em 70-80% % dos pacientes. Os óleos essenciais podem ajudar a aliviar sintomas residuais, melhorar o sono ou reduzir efeitos secundários (como ansiedade).
Qual óleo devo experimentar primeiro?
Hortelã-pimenta para concentração (durante o dia) e lavanda para dormir (à noite), melhor estudadas, bem toleradas.
Quanto tempo até sentir um efeito?
Alguns efeitos (foco, estado de alerta) são sentidos em poucos minutos. Para melhorias duradouras (sono, humor), aplique regularmente durante 2 a 4 semanas.
Isto também funciona em adultos com TDAH?
Sim, a maioria dos estudos foi realizada em adultos. Adultos com TDAH relatam frequentemente resultados particularmente bons na desregulação emocional e problemas de sono.
Tenho de comprar óleos caros?
Qualität ist wichtig: Achten Sie auf 100 % naturreine ätherische Öle, am besten mit am besten mit chargenspezifischem Analyse-Zertifikat (GC/MS).
Óleos de perfume baratos ou fragrâncias sintéticas não têm efeito terapêutico e, devido aos ingredientes sintéticos, podem ser prejudiciais à saúde, causando dores de cabeça, náuseas, etc.
Quem quiser saber mais sobre a seleção e qualidade de óleos essenciais, encontrará no artigo „Óleos Essenciais – A Odisseia de uma Busca“satisfeito.
Uma outra contribuição cita o Prof. Dr. Dr. Dr. med. habil. Hanns Hatt, da Universidade Ruhr de Bochum, que no seu vídeo „Cura com fragrâncias“Explica o efeito dos óleos essenciais no corpo humano de uma forma interessante, divertida e, ainda assim, científica.
Devo falar sobre isto com o meu médico?
Para aromaterapia (difusor, inalação) não é estritamente necessário. No entanto, se pretender tomar cápsulas ou cremes com óleos essenciais, ou se o seu filho tiver TDAH e estiver a tomar metilfenidato, fale com o seu médico.
Bases neurobiológicas, mecanismos moleculares de ação e evidências clínicas para a terapia adjuvante com o Nebulizador de Aromas Orgânicos 3.0
Relatório de Investigação Combinado | Abril 2026
Temas: Metilfenidato (Ritalina) · Farmacodinâmica Intracerebral · Aromaterapia Adjuvante · Terpenos · Recetores · Vias de Sinalização · Recomendações de Dosagem
Aplicação Nebulizador Organik Aromas 3.0 (Nebulização a Frio Venturi, sem água, óleos puros GC/MS)
TDAH e Metilfenidato
Este relatório investiga as bases neurobiológicas da terapia com metilfenidato para o Transtorno de Défice de Atenção e Hiperatividade (TDAH) e avalia o potencial dos óleos essenciais como opção terapêutica adjuvante. A análise baseia-se em 87 publicações científicas sobre concentrações intracerebrais de metilfenidato e 159 estudos sobre óleos essenciais no contexto do TDAH.
Principais conclusões sobre o metilfenidato
Doses terapêuticas orais (0,25–0,6 mg/kg) produzem uma ocupação do transportador de dopamina (DAT) de >50% no corpo estriado, com 20 mg por via oral atingindo 54% e 40 mg atingindo 72% de bloqueio do DAT. A captação cerebral máxima ocorre 60–90 minutos após a administração oral. As concentrações plasmáticas na faixa terapêutica são de 3,5–7,8 ng/ml (adultos), com 6 ng/ml associados a 50% de bloqueio do DAT. Não existem medições diretas das concentrações de metilfenidato no tecido cerebral (ng/ml) ou no LCR; os dados disponíveis provêm de estudos de ocupação PET/SPECT.
Óleos essenciais como adjuvantes
A plausibilidade mecanicista para uma terapia adjuvante baseada em mecanismos de ação complementares existe. O linalol (lavanda) modula os sistemas serotoninérgico, dopaminérgico e noradrenérgico através dos recetores 5-HT1A e da ligação ao SERT. O mentol (hortelã-pimenta) ativa os canais TRPM8 e modula os recetores GABA-A e nicotínicos, melhorando a atenção e a vigilância. O β-cariofileno (pimenta preta) atua como agonista CB2 com propriedades anti-inflamatórias. O 1,8-cineol (alecrim) melhora o desempenho da memória e as funções cognitivas.
Evidência científica
Embora os dados pré-clínicos e mecanísticos sejam promissores, faltam estudos randomizados controlados (ERCs) especificamente em pacientes com TDAH. Estudos em humanos existentes mostram melhorias cognitivas em adultos saudáveis (Hortelã-pimenta: atenção sustentada melhorada, n=24; Alecrim: melhoria da memória, n=144).
Este relatório fornece recomendações de dosagem baseadas em evidências para o Nebulizador Organik Aromas 3.0 e instruções de segurança completas para a aplicação em pacientes com TDAH.
Transtorno do Espectro do Autismo (TEA)
O Transtorno do Espectro do Autismo (TEA) é um distúrbio neurobiológico complexo do desenvolvimento com uma prevalência estimada de 1–2 % em todo o mundo. A sintomatologia central abrange défices na comunicação e interação social, bem como padrões de comportamento repetitivos e peculiaridades sensoriais. Apesar de intensa investigação, não existem terapias curativas para os sintomas centrais; as intervenções disponíveis concentram-se em terapia comportamental e farmacoterapia sintomática. Este relatório investiga o potencial dos óleos essenciais como opção terapêutica adjuvante no TEA, com base numa análise sistemática de 547 publicações científicas sobre neurobiologia do TEA, terpenos e evidências clínicas.
A heterogeneidade neurobiológica da Perturbação do Espectro do Autismo (PEA) manifesta-se em desequilíbrio excitatório-inibitório (E/I) perturbado, disfunções nos sistemas GABAérgico, glutamatérgico, serotoninérgico, dopaminérgico e oxitocinérgico, neuroinflamação crónica com ativação da microglia, stress oxidativo, alterações do eixo Intestino-Cérebro e défices sinápticos (Neurexina, proteínas SHANK). As regiões cerebrais afetadas incluem o córtex pré-frontal, a amígdala, o cerebelo, o hipocampo e o estriado.
As análises moleculares demonstram que terpenos específicos de óleos essenciais visam alvos relevantes para a TEA: o Linalol (componente principal da lavanda) modula os recetores GABA-A no local de ligação das benzodiazepinas e afeta vias serotoninérgicas; o β-Cariofileno atua como um agonista seletivo do recetor CB2 com propriedades anti-neuroinflamatórias; os ácidos bosvélicos (olíbano) ativam a via antioxidante Nrf2/HO-1 e reduzem a ativação da microglia; o 1,8-Cineol (eucalipto) demonstra efeitos ansiolíticos através da modulação GABA-A; o α-Pineno atua de forma GABAérgica; a Cananga odorata (Ylang-Ylang) afeta o metabolismo da serotonina e da dopamina em modelos pré-clínicos de TEA.
A evidência clínica em TEA é limitada: Um ensaio aleatorizado controlado com bergamota não demonstrou efeitos ansiolíticos significativos em crianças com TEA. Pequenos estudos piloto relatam melhor cumprimento durante a Análise Comportamental Aplicada (ABA) com aromaterapia de lavanda, aumento da atenção partilhada após massagem de aromaterapia e possíveis efeitos no sono e ansiedade. No entanto, a qualidade da evidência é limitada por pequenas amostras, heterogeneidade metodológica e falta de replicação.
São desenvolvidas recomendações de dosagem específicas para o tamanho da sala para o Nebulizador Organik Aromas 3.0 (princípio Venturi, nebulização a frio sem água): 2–4 gotas para 10–20 m², 4–6 gotas para 20–40 m², 6–10 gotas para 40–60 m², com aplicações de 15–30 minutos e pausas de 30–60 minutos. Particularidades específicas do TEA exigem introdução gradual devido à hipersensibilidade sensorial, protocolos adaptados à hora do dia (ativador de manhã, calmante à noite) e controlo de qualidade rigoroso (análise GC/MS).
Os aspetos de segurança incluem precaução na epilepsia (óleos com cânfora), contraindicação de eucalipto em crianças com menos de 3 anos, potenciais interações com antipsicóticos (risperidona, aripiprazol) e consideração especial para hipersensibilidade sensorial em TEA. A plausibilidade mecanicista está presente, mas faltam estudos randomizados controlados de alta qualidade. Os óleos essenciais podem ser considerados como parte de uma abordagem terapêutica multimodal para sintomas comórbidos (ansiedade, distúrbios do sono, desregulação sensorial), mas não substituem intervenções essenciais baseadas em evidências.
TDAH e Metilfenidato
Terapia adjuvante com óleos essenciais na TDAH – farmacodinâmica da metilfenidato, terpenos, recetores, dosagem com o nebulizador Organik Aromas 3.0
Introdução
Die Aufmerksamkeitsdefizit-/Hyperaktivitätsstörung (ADHS) ist eine der häufigsten neuropsychiatrischen Erkrankungen im Kindes- und Jugendalter, die bei 5–7% der Kinder und 2,5–4% der Erwachsenen auftritt. Methylphenidat (MPH), ein Dopamin- und Noradrenalin-Wiederaufnahmehemmer, stellt die pharmakologische Erstlinientherapie dar und zeigt bei 70–80% der Patienten eine klinische Wirksamkeit [A1], [A2].
Apesar da eficácia estabelecida do metilfenidato, uma parte dos pacientes apresenta sintomas residuais, efeitos secundários ou o desejo de abordagens terapêuticas complementares. Óleos essenciais estão a ser cada vez mais discutidos como uma potencial opção terapêutica adjuvante, embora a evidência científica seja até agora heterogénea. [A3], [A4].
Objetivo do relatório
Este relatório tem cinco objetivos principais:
- Quantificação das concentrações de metilfenidato intracerebrais com base em dados PET/SPECT, incluindo ocupação DAT, relações plasma-cérebro e distribuição regional
- Avaliação mecanicista da plausibilidade de uma terapia adjuvante com óleos essenciais com base em mecanismos moleculares de ação
- Análise baseada em evidências Óleos essenciais específicos e seus principais constituintes ativos
- Desenvolvimento de recomendações de dosagem práticas para o Nebulizador Organik Aromas 3.0
- Elaboração de instruções de segurança abrangentes para aplicação em pacientes com TDAH
A análise integra dados de 87 estudos sobre concentrações de metilfenidato no cérebro e 159 publicações sobre óleos essenciais, com foco nas 30 publicações de maior relevância.
Metilfenidato – Concentrações intracerebrais e farmacodinâmica
DAT-Okkupanz – Relações Dose-Resposta
A eficácia terapêutica da metilfenidato correlaciona-se diretamente com a ocupação do transportador de dopamina (DAT) no estriado. Estudos de PET com [¹¹C]cocaína como marcador estabeleceram uma relação dose-resposta clara. [A9].
Tabela 1: Ocupação DAT após administração oral de metilfenidato
Fonte: Volkow et al. 1998 [A9]; Medições em adultos saudáveis
Die geschätzte Dosis für 50% DAT-Blockade (ED₅₀) beträgt 0,25 mg/kg Körpergewicht [A9]. Doses terapêuticas adaptadas ao peso (0,3–0,6 mg/kg) produzem, portanto, consistentemente uma ocupância do DAT >50%, que é considerada um limiar para a eficácia clínica [A7], [A9].
Diferenças regionais: A ocupação de DAT varia entre sub-regiões estriatais. Spencer et al. (2009) relataram para OROS-MPH (40 mg) após 10 horas os seguintes valores de ocupação: núcleo caudado direito 44,3±11,8%, núcleo caudado esquerdo 42,7±10,9%, putamen direito 41,6±11,7%, putamen esquerdo 41,3±13,1%. [A17].
Em pacientes com TDAH, estudos SPECT com [¹²³I]β-CIT mostram uma redução significativa na ligação do DAT estriatal sob terapêutica com metilfenidato. Aster et al. (2021) documentaram uma diminuição de 27,6–29,9%no potencial de ligação do DAT estriatal (BP) em crianças e adolescentes com TDAH sob medicação. [A25], [A18].
Concentrações plasmáticas versus cerebrais
Concentrações plasmáticas
A margem terapêutica plasmática para d-threo-metilfenidato em adultos situa-se entre 3,5–7,8 ng/ml [A20], [A24]. Uma concentração plasmática de 5,7–6,0 ng/ml está associada a 50% de bloqueio DAT [A9], [A13], [A17].
Observaram-se concentrações de pico mais elevadas em pacientes pediátricos: 20 ng/ml duas horas após uma dose de 20 mg (0,8 mg/kg). [A20], [A24].
Scan cerebral
Estudos PET com [¹¹C]Metilfenidato demonstram que 7,5±1,5% da atividade administrada intravenosamente chega ao cérebro [A5], [A14]. A concentração mais elevada é observada no estriado, com uma razão de volume de distribuição (DVR) dos gânglios da base para o cerebelo de 2,2–3,3 para d-threo-MPH [A16], [A14].
Lacuna crítica de evidência
Não existem medições diretas de concentrações de metilfenidato em tecido cerebral (em ng/ml ou nmol/L) ou em líquido cerebrospinal na literatura humana. Todos os dados disponíveis baseiam-se em medições de ocupação PET/SPECT ou em estudos de distribuição de traçadores. [A1], [A2], [A3], [A4], [A5], [A6], [A7], [A8], [A9].
Distribuição Regional – Estriado e córtex pré-frontal
Estrado
Como região alvo primária, o Striatum mostra a maior absorção de [¹¹C]Metilfenidato. A pré-medicação com Metilfenidato não marcado (0,5 mg/kg) reduz a ligação do traçador estriatal em 40% [A5]. A depuração do estriado é de ~90 minutos, consideravelmente mais lenta do que a da cocaína (20 minutos) [A5].
Córtex pré-frontal
Embora a densidade de DAT seja menor no córtex pré-frontal (CPF) do que no estriado, estudos PET funcionais com [¹¹C]racloprida demonstram aumentos significativos de dopamina também em regiões do córtex pré-frontal e temporal após a administração de metilfenidato. [A30], [A22]. Estes aumentos corticais de dopamina correlacionam-se com melhorias sintomáticas a longo prazo em pacientes com TDAH [A30].
Transportador de Noradrenalina (NET)
O metilfenidato bloqueia também o transportador de noradrenalina com uma DE₅₀ de 0,14 mg/kg [A11]. Estudos PET com [¹¹C]MRB mostram ocupação robusta de NET no tálamo e na ponte 75-195 minutos após a dosagem [A11], [A21].
Evolução no tempo e farmacocinética
Administração intravenosa
Após injeção intravenosa de [¹¹C]metilfenidato, a concentração cerebral atinge o seu máximo dentro de 8–10 minutos [A3], [A6].
Ok, Gabe
A absorção cerebral máxima após administração oral ocorre um tempo consideravelmente mais tarde, com um pico entre 60 e 90 minutos [A7], [A9], [A3]. Esta cinética retardada explica o menor potencial de abuso das formulações orais em comparação com as aplicações intravenosas [A13].
Formulações de atraso
As formulações de Libertação Prolongada (OROS-MPH, DBDS-MPH) mostram uma absorção ainda mais lenta com uma ocupação máxima retardada de DAT, mas com concentrações de pico comparáveis. [A13], [A17]. OROS-MPH atinge, após 10 horas, valores de ocupação de DAT significativamente mais elevados do que o DBDS-MPH (44,3% vs. 34,8% no núcleo caudado direito) a concentrações plasmáticas mais elevadas (5,2 vs. 3,8 ng/ml) [A17].
Dados de microdiálise pré-clínica
Em ratos, o d-treo-metilfenidato aumenta a concentração extracelular de dopamina no estriado em ~650% [A16]. Este aumento maciço de dopamina demonstra o efeito funcional do bloqueio do DAT na neurotransmissão sináptica.
Óleos essenciais como terapia adjuvante – bases mecanísticas
Mecanismos de ação complementares ao metilfenidato

Figura 1: Vias de sinalização molecular de óleos essenciais na TDAH – Sistema Dopaminérgico, Sistema Noradrenérgico e mecanismos de ação de terpenos complementares
A plausibilidade de uma terapia adjuvante com óleos essenciais baseia-se em mecanismos de ação complementares e não redundantes em comparação com o metilfenidato (MPH). Enquanto o MPH inibe primariamente a recaptação de dopamina e noradrenalina, os componentes dos óleos essenciais abordam sistemas neurobiológicos adicionais.
Complementaridade Mecanicista:
- Modulação GABAérgica
Mentol e linalol atuam como moduladores alostéricos positivos em recetores GABA-A, potenciando a neurotransmissão inibitória e podendo reduzir a hiperatividade. [A19], [A20], [A23]. - Efeitos serotoninérgicos
O linalol liga-se ao transportador de serotonina (SERT) e modula os recetores 5-HT1A, mediando efeitos ansiolíticos e estabilizadores de humor [A21], [A23], [A24]. - Vias inflamatórias
O β-cariofileno ativa recetores CB2 e reduz processos neuroinflamatórios através das vias de sinalização NF-κB e MAPK, que podem estar aumentadas no TDAH. [A14]. - Modulação do Canal TRP
Mentol (agonista TRPM8) e 1,8-cineol (modulador TRPV1/TRPA1) influenciam a excitabilidade neuronal e os fluxos iónicos independentemente dos sistemas monoaminérgicos [A19].
Receptores e vias de sinalização
Tabela 2: Alvos de recetores dos componentes do óleo essencial
LEO = Óleo Essencial de Lavanda; nAChR = recetor nicotínico de acetilcolina
Modulação do recetor GABA-A
O mentol apresenta ligação dependente da concentração aos recetores GABA-A e potencia a neurotransmissão inibitória [A19]. Curiosamente, o óleo de lavanda não mostra afinidade pela ligação das benzodiazepinas no recetor GABA-A, sugerindo um perfil de segurança mais favorável em comparação com as benzodiazepinas. [A23].
Transportador de Serotonina (SERT)
Linalool e óleo de lavanda ligam-se ao SERT com concentrações de 0,08–0,8% in vitro [A23]. Esta inibição da SERT pode mediar efeitos antidepressivos e ansiolíticos, que são relevantes em pacientes com TDAH e comórbidos transtornos de ansiedade (25-40% de prevalência%).
Antagonismo do recetor NMDA
O óleo de lavanda demonstra antagonismo do recetor NMDA dependente da dose com um IC₅₀ de 0,04 µl/ml [A23]. A modulação do recetor NMDA é relevante para a plasticidade sináptica e para os processos de aprendizagem.
Ativação do recetor CB2
O β-cariofileno é um agonista CB2 seletivo, sem efeitos psicoativos (sem ativação CB1). A ativação de CB2 reduz a ativação da microglia e a produção de citocinas pró-inflamatórias (TNF-α, IL-1β, IL-6), o que pode mediar efeitos neuroprotetores. [A14].
Potenciais sinérgicos
A combinação de metilfenidato com óleos essenciais pode produzir efeitos sinérgicos através de vários mecanismos:
- Dopamina-GABA-Equilíbrio
Enquanto o MPH aumenta a transmissão dopaminérgica, a modulação GABAérgica pelo mentol/linalol poderia promover um equilíbrio excitatório-inibitório mais equilibrado e reduzir a hiperatividade. - Redução de stress
Os efeitos ansiolíticos do linalol através dos recetores 5-HT1A e a redução do cortisol (diminuição de 24–38% em estudos clínicos) [A24] poderiam melhorar a reatividade ao stress em pacientes com TDAH. - Reforço cognitivo
A modulação colinérgica por mentol (inibição da acetilcolinesterase) [A19] e os efeitos de 1,8-cineol na melhoria da memória poderiam potenciar as melhorias cognitivas observadas com a MPH. - Neuroprotecção
As propriedades anti-inflamatórias e antioxidantes do β-cariofileno e do 1,8-cineol podem oferecer efeitos neuroprotetores a longo prazo.
Restrição importante: Estes potenciais sinérgicos são teoricamente plausíveis, mas não validados por estudos clínicos em pacientes com TDAH. Faltam completamente estudos controlados sobre a combinação de MPH com óleos essenciais.
Óleos essenciais específicos – Ingredientes ativos e evidências
Lavanda (Lavandula angustifolia) – Linalol
Principais ingredientes activos
Linalol (25–45%)
Acetato de linalilo (25–45%)
1,8-Cineol (1–3%)
Mecanismos
- Ligação SERT
O linalol e o óleo de lavanda ligam-se ao transportador de serotonina, o que pode mediar efeitos antidepressivos [A23]
- Antagonismo NMDA
O óleo de lavanda demonstra um bloqueio do recetor NMDA dependente da dose (CI₅₀: 0,04 µl/ml) [A23]
- Modulação de GABA
Reforço da neurotransmissão inibitória através de recetores GABA-A (não através do local de ligação das benzodiazepinas) [A20], [A23]
- Efeitos monoaminérgicos
O linalol modula os sistemas de dopamina, noradrenalina e serotonina em modelos pré-clínicos [A21]
Evidência clínica
- Cognição
Moss et al. (2003) demonstraram em n=144 adultos saudáveis que a aromaterapia com lavanda prejudicou a memória de trabalho e abrandou os tempos de reação, mas teve um efeito subjetivamente calmante. [A27]
- Atenção
Colzato et al. (2014) descobriram que o aroma de lavanda reduziu o “blink atencional” (défices de atenção temporal), indicando uma distribuição de atenção mais ampla [A30]
- Ansiólise
Uma dose de Silexan (80 mg/dia de óleo de lavanda) reduziu os sintomas de ansiedade generalizada comparativamente ao lorazepam [A26]
- Redução de stress
A inalação de óleo de lavanda reduziu os níveis de cortisol em 24–38%% em estudos clínicos [A24]
Dados específicos de TDAH
Não existem estudos aleatorizados controlados em doentes com TDAH. Relatos de casos descrevem efeitos positivos na agitação e no sono em crianças atípicas com TDAH. [A8].
Dosagem (pré-clínica/clínica)
– Oral: 50–100 µL encapsulados (Estudo Kennedy) [A19]
– Inalação: 4 gotas em 30 ml de água (difusor) [A30]
– Tópico: 1,5% diluição em óleo vegetal [A8]
Segurança
O óleo de lavanda não demonstrou potenciamento da neurotoxicidade celular in vitro [A23].
Nenhum efeito secundário grave em estudos clínicos às doses recomendadas.
Alecrim (Rosmarinus officinalis) – 1,8-Cineol
Principais ingredientes activos
1,8-Cineol (Eucaliptol, 20–50%)
Canfora (10–20%)
α-Pineno (10–15%)
Mecanismos
- Modulação Colinérgica
Inibição da acetilcolinesterase, que potencia a neurotransmissão colinérgica [A27]
- Ativação do Canal TRP
O 1,8-cineolo modula TRPV1 e TRPA1, o que influencia a excitabilidade neuronal
- Anti-inflamatório
Inibição das vias de sinalização NF-κB e MAPK, redução de citocinas pró-inflamatórias
- Antioxidante
Ativação da via de sinalização Nrf2, aumento de enzimas antioxidantes
Evidência clínica: - Memória
Moss et al. (2003) demonstraram, em n=144 adultos saudáveis, melhorias significativas na memória geral e na memória secundária após aromaterapia com alecrim, em comparação com os grupos de controlo e lavanda. [A27]
- Desempenho cognitivo: A exposição ao aroma de alecrim correlacionou-se com a melhoria do desempenho cognitivo [A14]
- Alerta: O alecrim aumentou a vigilância e a atividade no cérebro [A29]
Dados específicos de TDAH
O alecrim é mencionado em revisões de literatura como potencialmente útil para o TDAH [A10], [A4], [A5], mas faltam ensaios clínicos controlados em pacientes com TDAH.
dosagem
– Inalação: Exposição ambiente em ambiente de teste (concentração não especificada) [A27]
– Não existem recomendações de dosagem padronizadas para TDAH disponíveis
Segurança
O alecrim é considerado seguro em aplicação inalatória em concentrações usuais.
Cuidado em pacientes epiléticos devido ao teor de cânfora.
Pfeffermina (Mentha × piperita) – Mentol
Principais ingredientes activos
Mentol (30–50%)
Mentona (10–30%)
1,8-Cineol (5–10%)
Mecanismos
- Ativação do TRPM8
O mentol é um potente agonista do TRPM8 (CE₅₀ ~30 µM), o que media a sensação de frio e a modulação neuronal [A19]
- Modulação do GABA-A
Ligação dependente da concentração e modulação alostérica positiva [A19]
- Recetores nicotínicos
Modulação dos receptores nicotínicos de acetilcolina, influenciando a transmissão colinérgica [A19]
- Inibição da acetilcolinesterase
O óleo de hortelã-pimenta inibe significativamente a acetilcolinesterase, o que potencia a neurotransmissão colinérgica [A19]
Evidência clínica: - Atenção sustentada
Kennedy et al. (2018) demonstraram, num estudo cruzado duplo-cego (n=24 adultos saudáveis), que 100 µL de óleo de hortelã melhoraram o desempenho no teste de Processamento Rápido de Informação Visual (RVIP) 1-3 horas após a ingestão. [A19]
- Redução de fadiga: Ambos os comprimidos (50 µL e 100 µL) reduziram a fadiga e melhoraram a subtração seriada após 3 horas [A19]
- Controlo atencional: Colzato et al. (2014) descobriram que o aroma de hortelã-pimenta intensificou o “blink atencional”, sugerindo uma atenção mais focada (menos distribuída). [A30]
Dados específicos de TDAH
Não foram encontrados ensaios clínicos controlados em pacientes com TDAH. A hortelã-pimenta é mencionada em revisões sobre TDAH como potencialmente útil. [A4], [A5], [A29].
dosagem
– Oral (encapsulado): 50–100 µL de óleo puro [A19]
– Inalação: 4 gotas em 30 ml de água (difusor) [A30]
Segurança
O óleo de hortelã-pimenta é seguro quando usado por inalação e por via oral nas doses recomendadas.
Precauções em lactentes e crianças pequenas (risco de laringospasmo com administração nasal direta).
Pimenta preta (Piper nigrum) – β-Cariofileno
Principais ingredientes activos
β-Cariofileno (10–35%)
Limoneno (15–25%)
Sabinenos (10–20%)
Mecanismos
- Agonismo CB2
O β-cariofileno é um agonista seletivo do recetor CB2 (Ki: 155±4 nM) sem ativação do CB1 (sem efeitos psicoativos). [A14]
- Anti-inflamatório
Redução de TNF-α, IL-1β, IL-6 através de inibição de NF-κB [A14]
- Modulação da Microglia
Reprogramação do fenótipo de microglia de M1 para M2, redução dos processos neuroinflamatórios
- Neuroprotector
Redução do stress oxidativo através da ativação do Nrf2
Evidência clínica
- Pré-clínico
O β-cariofileno demonstrou efeitos ansiolíticos em modelos animais, possivelmente através da modulação da ativação neuronal no núcleo da amígdala central. [A14]
- Anti-inflamatório
Estudos in vitro e in vivo demonstram robustos efeitos anti-inflamatórios através da ativação CB2
Dados específicos de TDAH
Nenhum estudo clínico em pacientes com TDAH. A plausibilidade mecanicista baseia-se em hipóteses neuroinflamatórias no TDAH.
dosagem
Não existem recomendações de dosagem padronizadas para uso inalatório no TDAH.
Segurança
O β-cariofileno é considerado seguro (status GRAS da FDA).
Não são conhecidos efeitos secundários graves em doses habituais.
Vetiver (Chrysopogon zizanioides)
Principais ingredientes activos
Vetiverol
Khusimol
α-Vetivona
β-Vetivona
Mecanismos
- Ansiolítico
Estudos pré-clínicos demonstram efeitos ansiolíticos, possivelmente através da modulação da atividade da amígdala. [A14]
- Acalmador
Usado tradicionalmente para acalmar o sistema nervoso
Evidência clínica
- Específico para TDAH
Springer et al. (2018) reportam que a inalação de vetiver (3x por dia durante 30 dias) demonstrou melhorias na função cerebral e no comportamento em crianças. [A29]
- Limitações
Não existem ensaios clínicos controlados e aleatorizados; as evidências baseiam-se em relatos de caso e uso tradicional
Dados específicos de TDAH
Godfrey (2001) refere o Vetiver como potencialmente útil no TDAH. [A3], [A4], [A5], mas faltam dados clínicos detalhados.
dosagem
– Inalação: 3× ao dia durante 30 dias (concentração específica não indicada) [A29]
Segurança
O vetiver é considerado seguro para uso por inalação. Não são conhecidos efeitos secundários graves.
Cedro (Cedrus spp.)
Principais ingredientes activos
α-Cedreno
β-Cedreno
Tujopseno
Cedrol
Mecanismos
- Oxigenação
Tradicionalmente utilizado para melhorar a oxigenação cerebral [A29]
- Acalmador
Propriedades sedativas na aplicação tradicional
Evidência clínica
- Específico para TDAH
Godfrey (2001) menciona o cedro como potencialmente útil no TDAH [A3], [A4], [A5]
- Limitações
Não existem ensaios clínicos controlados; a evidência baseia-se na aplicação tradicional e em anedotas
Dados específicos de TDAH
Springer et al. (2018) mencionam madeira de cedro para a oxigenação cerebral em TDAH [A29], mas faltam dados quantitativos.
dosagem
Não existem recomendações de dose padronizadas disponíveis.
Segurança
O óleo de madeira de cedro é considerado seguro para uso inalatório em concentrações usuais.
Canela (Cinnamomum verum) – Aldeído cinâmico
Principais ingredientes activos
Zimtaldeído (60–75%)
Eugenol (5–10%)
Mecanismos
- Modulação dopaminérgica
Alilbenzeno e propenilbenzeno na canela são precursores da anfetamina e, após metabolização, são convertidos em anfetamina, que tem um efeito estimulante mental. [A2]
- Ativação de TRPA1/TRPV1
O cinamaldeído ativa os canais TRPA1 e TRPV1
- Antimicrobiano
Fortes propriedades antimicrobianas
Evidência clínica: - Específico para TDAH
Chen et al (2008) realizaram um estudo com aromaterapia de canela em crianças com PHDA. A combinação de reabilitação e aromaterapia com canela (1% canela, 1 g em 100 ml de água, inalação nasal) mostrou resultados significativamente melhores no questionário SNAP-IV (58±2,6 vs. controlo) e nas escalas de atividade (102±5,8) após 6 meses, em comparação com a reabilitação isolada (p<0,05) [A2], [A1]
Dados específicos de TDAH
O estudo de Chen é um dos poucos ensaios clínicos com óleos essenciais especificamente em crianças com TDAH, embora com limitações metodológicas (sem informações sobre aleatorização, cegamento, tamanho da amostra).
dosagem
– Inalação: 1% canela (1 g em 100 ml de água) numa sala de terapia de 50 m² com controlo de luz elétrico [A2]
Segurança
O óleo de canela, em altas concentrações, pode causar irritação na pele e nas mucosas.
Cuidado com pessoas sensíveis.
A estimulação dopaminérgica por metabolitos da canela requer mais investigação relativamente às interações com metilfenidato.
Outros óleos essenciais indicados para a PHDA
Com base numa revisão bibliográfica atual, foram identificados os seguintes óleos essenciais adicionais que podem ser relevantes para o TDAH através de mecanismos neurobiologicamente plausíveis.
Melissa officinalis (Erva-cidreira) – Ácido rosmarínico, flavonoides
Ingredientes activos
Ácido rosmarínico
Flavonoide (Luteolina, Apigenina)
Óleos voláteis (Citral, Linalol, Geraniol)
Receptores e mecanismos de ação
– Recetores colinérgicos: Ligação nicotínica (nAChR) e muscarínica (mAChR)
– Modulação GABAérgica: Ácido rosmarínico inibe GABA-transaminase → aumento da disponibilidade de GABA
– Inibição da Acetilcolinesterase: Neurotransmissão colinérgica melhorada no córtex pré-frontal
Evidência clínica
- EAC (n=20, dupla ocultação, cruzado)
Doses únicas de 300/600/900 mg por via oral demonstraram, com 600 mg, uma melhoria significativa na precisão da atenção, bem como efeitos na memória e no estado de alerta [A31]
- Estudo de combinação (crianças, 7 semanas)
A combinação de extrato de valeriana e melissa melhorou significativamente a hiperatividade, as dificuldades de concentração e a impulsividade em crianças do ensino primário [A32]
- Cruzamento anti-stress
Os preparados de melissa estandardizados em formato alimentar reduziram a sobrecarga cognitiva e melhoraram o humor em adultos saudáveis. [A33]
Dosagem (Nebulizador Organik Aromas 3.0)
– 3–5 gotas de óleo de erva-cidreira (GC/MS puro) para uma divisão de 15–25 m²
– Aplicação: 30 min antes das fases de concentração, 2-3 vezes por dia
– Combinação com lavanda (2:1) recomendada para a noite/relaxamento
Segurança
Bem tolerado
Possível interação com medicamentos da tiroide (supressão do TSH em caso de ingestão oral a alta dose)
A inalação é considerada segura.
Eucalipto (Eucalyptus globulus / radiata) – 1,8-Cineol
Ingredientes activos
1,8-Cineol (Eucaliptol, 70–85%)
α-Pineno
Limas
Receptores e mecanismos de ação
– Sítio GABA-A/Benzodiazepina: Atividade moduladora (ansiolítica, sedativa em doses elevadas)
– Vias Colinérgicas: 1,8-Cineol inibe a acetilcolinesterase → atenção e memória de trabalho melhoradas
– Antioxidante/Neuroprotetor: Redução do stress oxidativo em células neuronais
Evidência clínica
– Neuroprotektive Reviews listam Eucalyptus globulus como planta com efeitos cognitivos em estudos animais e humanos [A34]
– O 1,8-cineol é também o principal princípio ativo do alecrim (já incluído no relatório), o eucalipto fornece uma concentração pura mais elevada
– Estudos de inalação demonstram melhoria da clareza mental e da concentração (estudos comparativos com alecrim)
Dosagem (Nebulizador Organik Aromas 3.0)
– 2–3 gotas para espaços de 15–25 m² (cheiro intenso, dosear com moderação)
– Aplicação: Manhã/Tarde para fases de concentração, máx. 20 min
- Contraindicação
Não adequado para crianças com menos de 3 anos
Não em combinação com medicamentos para a asma sem aconselhamento médico
Segurança
Óleo forte, não aplicar puro na pele
Crianças < 3 anos: contraindicado
Epilepsia: Cuidado
Gengibre (Zingiber officinale) – Gingeróis, Zingibereno
Ingredientes activos
6-Gengibreol
6-Shogaol
Zingibereno
β-Sesquiphellandreno
Receptores e mecanismos de ação
– Antagonismo do recetor de serotonina-5-HT3: componente ansiolítica
– Dopaminérgico: Os gingeróis modulam a atividade dopaminérgica no estriado (animal)
– Antioxidante/Anti-inflamatório neural: Inibição de NF-κB, Redução de TNF-α
Evidência clínica
– Pré-clínico: Extrato de gengibre melhorou a função cognitiva em modelos animais de TDAH
– Propriedades neuroprotetoras bem documentadas por mecanismos antioxidantes
– Ainda faltam ensaios clínicos randomizados diretos sobre TDAH na literatura
Dosagem (Nebulizador Organik Aromas 3.0)
– 2-3 gotas para um espaço de 15-25 m²
– Combinação com alecrim (1:1) para ativação cognitiva
Recomendações de dosagem para o Nebulizador Organik Aromas 3.0
Princípios Técnicos: Princípio de Venturi e Nebulização
O Nebulizador Organik Aromas 3.0* utiliza o princípio de Venturi para a nebulização a frio e sem água de óleos essenciais. Este processo oferece várias vantagens:
Características técnicas
- Nebulização a frio
Nenhuma exposição ao calor, preservação de todos os componentes voláteis e ingredientes ativos termolábeis
- Anidro
Nebulização direta de óleos essenciais puros sem diluição, maior concentração de ingredientes ativos no ar ambiente
- Tamanho de partícula
Produção de micropartículas (1-5 µm) que podem penetrar profundamente nas vias respiratórias e atravessar a barreira hematoencefálica
- Óleos puros com certificado GC/MS
Utilização de óleos analiticamente testados sem aditivos, óleos de base ou fragrâncias sintéticas
*ca. 110-120 USD (com funcionamento a partir da rede elétrica / bateria)
- Envio gratuito para todo o mundo
- Tenha em atenção as taxas alfandegárias e de importação!
Considerações Farmacocinéticas
A absorção inalatória de óleos essenciais ocorre através de duas vias principais:
1. Caminho olfativo
Ligação direta do epitélio olfativo ao sistema límbico (amígdala, hipocampo) e córtex pré-frontal através do bulbo olfativo
2. Via pulmonar
Absorção através da membrana alveolar para a circulação sistémica, passagem da barreira hematoencefálica [A29]
Tamanho da sala e quantidade de gotas
Fórmula básica
A quantidade de gotas deve ser ajustada ao tamanho da sala para alcançar uma concentração terapeuticamente eficaz, mas não excessiva.
Tabela 3: Recomendações de dosagem por tamanho da sala
*Pressuposto: Altura do compartimento 2,5 m **Concentração estimada com base em ~1 mg de óleo essencial por gota e nebulização completa
Base de cálculo
– 1 gota de óleo essencial ≈ 0,05 ml ≈ 40–50 mg (dependendo da densidade)
– Concentração alvo: 80–200 µg/m³ (com base em estudos com aromaterapia ambiental)
– Fórmula: Gota = (Volume do espaço × Concentração alvo) / (Massa por gota × 1000)
Duração da utilização e pausas
Duração da sessão
- Aplicação aguda
15–30 minutos por sessão
- Difusão contínua em segundo plano
30–60 minutos com pausas
Intervalos de pausa
A adaptação olfativa (habituação) ocorre após 15-30 minutos de exposição contínua.
Para manter os efeitos terapêuticos, recomendam-se intervalos de pausa:
Tabela 4: Esquema de Aplicação e Pausa
Adaptação olfativa
Após 20-30 minutos de exposição contínua, a perceção consciente do cheiro diminui, mas os efeitos neurobiológicos podem persistir.
Pausas de 30 a 60 minutos permitem a resensibilização dos recetores olfativos.
Hora do dia e cenários de aplicação
A seleção dos óleos essenciais deve ser adaptada à hora do dia e aos sintomas específicos do TDAH:
Tabela 5: Seleção de óleo específica do período do dia
Cenários de aplicação:
- Schulvorbereitung/Morgenroutine
– Óleo: Alecrim ou hortelã-pimenta
– Objetivo: Ativação, Alerta, Foco Dosagem: 6–8 gotas durante 20 minutos
– Horário: 30–60 minutos antes do início da aula - Trabalhos de casa / Fases de aprendizagem
– Óleo: de hortelã-pimenta (atenção contínua) ou de alecrim (memória)
– Objetivo: Concentração, memória de trabalho – Dosagem: 6–8 gotas durante 30 minutos, depois uma pausa de 30 minutos
– Horário: Durante os trabalhos de casa ou sessões de estudo - Gestão da Hiperatividade:
– Óleo: Lavanda ou Vetiver
– Objetivo: Acalmar, reduzir a agitação motora. Dosagem: 5-7 gotas durante 30 minutos.
– Duração: Em hiperatividade ou agitação agudas - Higiene do sono:
– Óleo: Lavanda
- Objetivo: Indução do sono, redução de problemas de adormecer (frequente no TDAH) Dosagem: 4–6 gotas durante 15 minutos
– Horário: 30–60 minutos antes de dormir
Dosagens específicas de óleo
Tabela 6: Recomendações de dosagem específicas para óleo
Misturas (Blends): A combinação de vários óleos pode criar efeitos sinérgicos:
- Foco-Mistura (Manhã)
3 gotas de alecrim + 3 gotas de hortelã-pimenta + 2 gotas de canela - Mistura Calmante (Noite)
4 gotas de lavanda + 3 gotas de vetiver + 2 gotas de cedro - Equilíbrio-Mistura (Tarde)
3 gotas de menta-pimenta + 3 gotas de lavanda + 2 gotas de pimenta-negra
Importante
Manter o número total de gotas na faixa recomendada nas misturas (6-8 gotas para 20 m²).
Instruções de segurança e contraindicações
Segurança Geral de Inalação
Princípios Fundamentais
pureza
Ausschließlich GC/MS-zertifizierte, 100% reine ätherische Öle ohne Zusatzstoffe verwenden
Diluição
Na aplicação por inalação através de difusor, não é necessária diluição adicional; na aplicação tópica, diluir sempre num óleo de suporte (1–3%)
Ventilação
O espaço não deve estar completamente fechado; assegurar uma entrada regular de ar fresco
Tolerância individual
Começar com doses baixas e aumentar gradualmente
Efeitos secundários frequentes (leves)
– Dores de cabeça por excesso de concentração ou exposição prolongada
– Irritação da mucosa (nariz, garganta) em pessoas sensíveis
– Náuseas com aromas muito intensos (ex: canela, pimenta preta)
– Reações alérgicas (raras, <1% da população)
Medidas para efeitos secundários
– Desligue o difusor imediatamente e ventile a sala
– Em caso de dores de cabeça: Ar puro, hidratação
– Em caso de irritação das mucosas: interromper a inalação, se necessário inalar solução salina.
– Em caso de reações alérgicas: interromper a exposição, se necessário administrar antigripal, em caso de reações graves procurar ajuda médica.
Considerações específicas para TDAH
Vulnerabilidades Especiais em Pacientes com TDAH:
Hipersensibilidade sensorial
40–60% dos pacientes com TDAH apresentam distúrbios de processamento sensorial. Odores intensos podem ser percebidos como desagradáveis ou avassaladores.
- Recomendação
Começar com doses muito baixas (50% da dose padrão), aumentar gradualmente
Transtornos de ansiedade comórbidos
25–40% der ADHD-Patienten haben komorbide Angststörungen.
Os óleos ativadores (alecrim, hortelã-pimenta) podem intensificar a ansiedade.
- Recomendação
Em caso de comorbidade de ansiedade, usar primariamente óleos ansiolíticos (lavanda, vetiver)
Distúrbios do sono
50–70% der ADHD-Patienten haben Schlafprobleme. Aktivierende Öle am Abend können Schlaf weiter beeinträchtigen.
- Recomendação
Separação rigorosa: óleos ativadores apenas de manhã/tarde, óleos sedativos à noite
Impulsividade
Pacientes com TDAH podem tender a usar doses elevadas.
- Recomendação
Instruções de dosagem claras, supervisão por pais/responsáveis, se necessário
Interações com metilfenidato
Interações teóricas:
Reforço dopaminérgico (Canela)
– Metabolitos da canela podem ser convertidos em anfetaminas [A2]
Risco teórico de efeitos dopaminérgicos aditivos com metilfenidato
- Recomendação
Usar canela apenas em doses baixas, monitorizar atentamente sinais de sobre-estimulação (taquicardia, agitação, insónia).
Modulação Serotoninérgica (Lavanda)
O linalol liga-se ao SERT [A23]
Risco teórico de síndrome serotoninérgica com a toma concomitante de ISRS (frequente em depressão/ansiedade comórbida).
- Recomendação
Com a comedição de ISRS, lavanda apenas em doses moderadas, monitorizar os sintomas de síndrome serotoninérgica (agitação, confusão, taquicardia, hipertermia).
Sedação (Lavanda, Vetiver)
– Óleos sedativos poderiam reduzir o estado de alerta
Contraproducente ao efeito estimulante do metilfenidato
- Recomendação
Utilizar óleos sedativos principalmente à noite, não durante o horário escolar ou em atividades que exijam atenção
- Nenhuma interação farmacocinética conhecida
Os óleos essenciais são metabolizados primariamente através do CYP2D6, CYP3A4
O metilfenidato é metabolizado pela carboxilesterase 1 (CES1)
Sem sobreposição de vias de metabolização, pelo que não são esperadas interações farmacocinéticas
Importante
Apesar da falta de interações documentadas, a combinação de metilfenidato com óleos essenciais deve ser feita sob supervisão médica, especialmente no início da terapia.
Contraindicações e precauções
Contraindicações absolutas
– Alergia conhecida a óleos essenciais específicos ou aos seus componentes
Asma brônquica grave (risco de broncospasmo)
- Bebés <6 meses (risco de laringoespasmo, especialmente com mentol)
Contraindicações relativas (Cuidado recomendado)
– Epilepsia: Cuidado com o alecrim e a canela (cânfora, aldeído cinâmico podem baixar o limiar convulsivo)
– Gravidez/Amamentação: Muitos óleos essenciais não foram suficientemente estudados durante a gravidez/amamentação
– Asma (leve-moderada): Doses baixas, monitorização apertada de sintomas respiratórios
– Bebés (6 meses – 3 anos): Doses reduzidas (25–50% da dose de adulto)
Ajustes de dose em função da idade:
Critérios de qualidade para óleos essenciais
- Certificado GC/MS:
Cada lote tem de ser analisado por cromatografia gasosa/espectrometria de massa - Nome botânico
A designação em latim deve ser indicada (por exemplo, Lavandula angustifolia, não apenas “Lavanda”) - Quimiotipo
No caso de óleos com diferentes quimiotipos (por exemplo, alecrim), este tem de ser especificado. - Origem
O país de origem e o método de extração (destilação, prensagem a frio) devem ser documentados - Sem aditivos
100% rein, ohne synthetische Duftstoffe, Trägeröle oder Konservierungsmittel
Armazenamento e prazo de validade
– Conservar em local fresco e escuro (15–20°C)
– Proteger da luz (garrafas de vidro castanhas ou azuis)
– Consumir entre 6 a 12 meses após a abertura (oxidação)
– Os óleos cítricos têm um prazo de validade mais curto (6 meses), as resinas mais longo (2 a 3 anos)
Discussão e implicações clínicas
Lacunas de evidência e necessidades de investigação
Avaliação crítica da base de evidências:
A presente análise demonstra um discrepância significativa entre plausibilidade mecanicista e evidência clínica para óleos essenciais como terapia adjuvante para TDAH.
Forças da evidência disponível
- Dados mecanísticos robustos
Estudos de ligação a recetores, análises de vias de sinalização e modelos pré-clínicos demonstram claros efeitos neurobiológicos dos componentes de óleos essenciais [A19], [A20], [A21], [A23] - Efeitos cognitivos em indivíduos saudáveis
Estudos controlados em adultos saudáveis demonstram efeitos mensuráveis na atenção (hortelã-pimenta, n=24) [A19] e memória (Rosmaninho, n=144) [A27] - Mecanismos de ação complementares
Os alvos moleculares dos óleos essenciais (GABA-A, CB2, canais TRP, SERT) diferem dos do metilfenidato (DAT/NET), o que sugere potenciais sinérgicos
Fraquezas e lacunas de evidências
- Faltam ensaios clínicos randomizados específicos para TDAH: Com exceção do estudo de Chen sobre canela [A2] Não existem estudos randomizados controlados por placebo em pacientes com TDAH
- Limitações metodológicas: Os estudos existentes têm amostras pequenas (n=24–144), períodos de observação curtos (sessões únicas) e, muitas vezes, falta de ocultação (duplo-cego).
- Sem dados de longo prazo: Os efeitos e a segurança da aplicação crónica (>6 meses) não foram investigados
- Estudos de dosagem de falta: As doses, concentrações e esquemas de administração ótimos para TDAH não estão estabelecidos.
- Não há estudos de combinação: As interações e os efeitos sinérgicos com metilfenidato não foram investigados de forma sistemática
Lacunas de investigação específicas:
Implementação prática
Recomendações de prática clínica:
Apesar das lacunas de evidências, uma terapia adjuvante com óleos essenciais em pacientes com TDAH pode ser considerada nas seguintes condições:
1. Indicação clara
- Sintomas residuais sob terapia otimizada com metilfenidato
- Desejo do paciente, da família por abordagens complementares
- Sintomas específicos que podem ser abordados com óleos essenciais
(Distúrbios do sono → Lavanda; Problemas de memória → Alecrim)
2. Abordagem estruturada
- Avaliação de Referência
Documentação da sintomatologia da TDAH com escalas validadas (SNAP-IV, Conners, ADHS-SB) - Fase de introdução
Comece com um único óleo em baixa dose (50% da dose standard) durante 2 semanas - Monitorização
Registo semanal de sintomas, monitorização de efeitos secundários - Titulação
Aumento gradual da dose com boa tolerância - Avaliação
Após 4 a 6 semanas de avaliação da eficácia; em caso de ausência de benefício, interrupção
3. Documentação
- Manter um “Diário de Aromaterapia” com óleo, dose, hora, sintomas, efeitos secundários
- Consulta regular com o médico assistente
4. Expectativas Realistas
- Óleos essenciais são sem substituição para terapias baseadas em evidências para TDAH (Metilfenidato, Terapia Comportamental)
- Tamanho do efeito esperado: pequeno a moderado (d de Cohen: 0,2–0,5)
- Benefício principal: Melhoria de sintomas específicos (sono, ansiedade, humor), não dos sintomas centrais
Limitações
Limitações desta análise:
- Evidência indireta
A maioria das conclusões baseia-se na extrapolação de estudos em adultos saudáveis para doentes com TDAH. - Viés de publicação
Estudos positivos são mais propensos a ser publicados; estudos negativos sobre óleos essenciais podem estar sub-representados - Heterogeneidade
A variedade de óleos, dosagens, vias de administração e medidas de resultados dificulta as meta-análises. - Plasma/Espelho cerebral em falta
Não existem dados sobre as concentrações plasmáticas ou cerebrais de componentes de óleos essenciais após inalação em humanos. - Incerteza mecanicista
Os mecanismos exatos pelos quais os óleos essenciais inalados medeiam os efeitos no SNC (olfativo vs. sistémico) não estão totalmente elucidados
Limitações das recomendações de dosagem
– Com base na extrapolação de poucos estudos e na aplicação tradicional
– Variabilidade individual (ventilação do espaço, frequência respiratória, metabolismo) não considerada
– Não existem dados farmacocinéticos sobre a relação dose-concentração
Conclusão
Esta análise abrangente integra dados de 87 estudos sobre concentrações intracerebrais de metilfenidato e 159 publicações sobre óleos essenciais no contexto da TDAH. As principais descobertas podem ser resumidas da seguinte forma:
Concentrações cerebrais de metilfenidato
As doses terapêuticas orais de metilfenidato (0,25–0,6 mg/kg) geram uma ocupação do DAT de >50%no estriado, com a relação dose-resposta bem caracterizada (20 mg → 54%, 40 mg → 72% de bloqueio do DAT). [A9].
A absorção máxima do cérebro ocorre 60-90 minutos após a administração oral [A7], [A9].
As concentrações plasmáticas na gama terapêutica situam-se entre 3,5 – 7,8 ng/ml (adultos), sendo que 6 ng/ml estão associados a 50% de bloqueio DAT [A9], [A17].
Lacuna crítica de evidência
Não existem medições diretas das concentrações de metilfenidato no tecido cerebral (ng/ml) ou no Líquor; todos os dados são baseados em medições de ocupação PET/SPECT.
Terapia adjuvante com óleos essenciais
Uma terapia adjuvante com óleos essenciais é Mecanisticamente plausível com base nos mecanismos de ação complementares.
O linalol modula os sistemas de serotonina, dopamina e noradrenalina [A21], [A23];
– O mentol ativa os canais TRPM8 e os recetores GABA-A [A19];
– O β-Cariofileno atua como um agonista CB2 com propriedades anti-inflamatórias [A14];
– 1,8-Cineol melhora as funções cognitivas [A27].
Estes mecanismos são complementares ao bloqueio DAT/NET pela metilfenidato e podem produzir efeitos sinérgicos.
No entanto: A evidência clínica em pacientes com TDAH é fraca, com uma escassez considerável de ensaios clínicos randomizados e controlados.
Óleos e ingredientes específicos
- Hortelã-pimenta (Mentol)
A evidência mais forte para a melhoria da atenção sustentada (n=24 RCT) [A19] - Alecrim (1,8-Cineol)
Melhoria da memória (n=144) [A27] - Lavanda (Linalol)
Ansiedade, melhoria do sono, mas comprometimento da memória de trabalho [A27], [A23] - Pimenta-preta (β-Cariofileno)
Anti-inflamatório, efeitos ansiolíticos pré-clínicos [A14] - Vetiver, Cedro
Evidência fraca, principalmente uso tradicional [A3], [A4], [A29] - Canela (Aldeído cinâmico)
Único ensaio clínico específico para TDAH, mas com limitações metodológicas [A2]
Recomendações de dosagem para o Organik Aromas Nebulizer 3.0)
Foram desenvolvidas recomendações de dosagem baseadas em evidências, adaptadas ao tamanho da sala (3-18 gotas para 10-60 m²), hora do dia (óleos ativadores de manhã, sedativos à noite) e sintomas específicos.
Duração de uso: 15–30 minutos por sessão com pausas de 30–60 minutos para evitar a adaptação olfativa.
Importante: Estas recomendações baseiam-se em extrapolações de poucos estudos e requerem adaptação individual.
Instruções de segurança
Os óleos essenciais são geralmente seguros quando aplicados por inalação em doses recomendadas.
Precauções específicas para doentes com TDAH incluem:
- Considerando a hipersensibilidade sensorial (40–60% dos doentes com TDAH)
- Evitar óleos ativadores em caso de ansiedade comórbida
- separação estrita de óleos ativadores (manhã) e sedativos (noite)
- Interações teóricas com metilfenidato (potenciação dopaminérgica pela canela, modulação serotoninérgica pela lavanda) exigem monitorização
- Contraindicações absolutas
– alergia conhecida
Asma grave
– Bebés <6 meses
Avaliação final
Os óleos essenciais representam uma promissor, mas insuficientemente validado Terapia adjuvante para TDAH. A plausibilidade mecanicista é forte, mas a evidência clínica é fraca.
Uma aplicação pode ser considerada para pacientes/famílias informados, sob supervisão médica, mas deve ser nunca terapias baseadas em evidências.
Urgente necessidade de investigação existe para estudos randomizados, controlados por placebo em pacientes com TDAH, dados de segurança a longo prazo e estudos de combinação com metilfenidato.
Transtorno do Espectro do Autismo (TEA)
Bases neurobiológicas da TEA, terpenos como moduladores de CB2/GABA-A/Nrf2, evidências clínicas e dosagem com o Nebulizador Orgânico Aromas 3.0
Introdução
O Transtorno do Espectro Autista (TEA) representa um dos transtornos do neurodesenvolvimento mais comuns, com uma prevalência global estimada de 1 a 2 % e um aumento na taxa de diagnóstico nas últimas duas décadas. [B1], [B2].
O TEA caracteriza-se por uma acentuada heterogeneidade clínica e neurobiológica, que se manifesta num amplo espectro de manifestações sintomáticas, desde indivíduos de alto funcionamento com défices isolados de comunicação social até pessoas com deficiência intelectual grave e doenças neurológicas comórbidas. [B3], [B4].
A sintomatologia central, de acordo com o DSM-5, abrange duas áreas principais: défices persistentes na comunicação e interação sociais, e padrões de comportamento, interesses ou atividades restritos e repetitivos. [B5]. Adicionalmente, até 90 % dos afetados sofrem de distúrbios de processamento sensorial, que se manifestam como hiper ou hipossensibilidade a estímulos sensoriais. [B6], [B7].
Sintomas de comorbidade, como perturbações de ansiedade (40–50 %), perturbações do sono (50 a 80 %), perturbação de défice de atenção e hiperatividade (30 a 50 %) e queixas gastrointestinais (30 a 70 %), afetam significativamente a qualidade de vida. [B8], [B9], [B10].
Heterogeneidade Neurobiológica e Convergência Fisiopatológica
A heterogeneidade etiológica do TEA abrange fatores genéticos (herdabilidade de 70 a 90 %), mutações de novo em genes sinápticos (SHANK3, NLGN3/4, NRXN1), variantes de número de cópia, modificações epigenéticas e fatores ambientais pré-natais [B11], [B12], [B13].
Apesar desta diversidade, os mecanismos fisiopatológicos convergem para vias neurobiológicas comuns: desequilíbrio excitatório-inibitório (E/I), disfunção sináptica, neuroinflamação, stress oxidativo e alterações no eixo intestino-cérebro. [B14], [B15], [B16].
A hipótese do desequilíbrio E/I postula que uma desregulação entre a neurotransmissão excitatória (glutamatérgica) e inibitória (GABAérgica) explica os sintomas centrais do TEA. [B17], [B18].
Estudos de imagem e análises post-mortem revelam alterações regionais nas concentrações de GABA e glutamato, expressão alterada de recetores GABA-A e NMDA, bem como disfunções em interneurónios GABAérgicos. [B19], [B20], [B21].
Este desequilíbrio afeta particularmente o córtex pré-frontal (funções executivas, cognição social), a amígdala (processamento emocional, perceção social), o cerebelo (integração sensório-motora, processos cognitivos) e o hipocampo (memória, processamento contextual) [B22], [B23], [B24].
A neuroinflamação representa um mecanismo convergente adicional: estudos post-mortem mostram ativação de microglia e astrócitos em cérebros com TEA, e modelos pré-clínicos (por exemplo, ativação imune materna, TEA induzido por valproato) demonstram citocinas pró-inflamatórias aumentadas (TNF-α, IL-6, IL-1β) e desenvolvimento sináptico prejudicado devido à neuroinflamação crónica. [B25], [B26], [B27].
O stress oxidativo com aumento das espécies reativas de oxigénio (ROS), redução da glutationa (GSH) e disfunção mitocondrial foi demonstrado em múltiplas coortes de TEA. [B28], [B29].
O Eixo Intestino-Cérebro desempenha um papel cada vez mais reconhecido. Pacientes com TEA frequentemente exibem disbiose com relações alteradas entre Firmicutes/Bacteroidetes, diversidade microbiana reduzida e produção perturbada de precursores de neurotransmissores (triptofano, GABA). [B30], [B31]. Os estudos pré-clínicos demonstram que a transplantação de microbiota fecal melhora comportamentos semelhantes ao TEA em modelos de ratos e modula vias de sinalização serotoninérgica e glutamatérgica. [B32], [B33].
Necessidade de terapias adjuvantes
Apesar da investigação intensiva, não existem terapias curativas para os sintomas centrais da Perturbação do Espectro do Autismo (PEA). As intervenções baseadas em evidências incluem abordagens comportamentais (Análise Aplicada do Comportamento, Modelo Denver de Início Precoce) e farmacoterapia sintomática. [B34], [B35]. Risperidona e Aripiprazol são os únicos medicamentos aprovados pela FDA para o TEA, embora exclusivamente para irritabilidade e comportamentos agressivos, e não para os sintomas nucleares. [B36], [B37]. Estes antipsicóticos estão associados a efeitos secundários significativos (aumento de peso, síndrome metabólica, sintomas extrapiramidais) [B38].
Sintomas comórbidos como ansiedade, distúrbios do sono e desregulação sensorial são frequentemente tratados com benzodiazepínicos, melatonina ou antidepressivos, com evidências limitadas quanto à eficácia e segurança em populações com TEA. [B39], [B40]. Esta falta de terapias seguras e eficazes para sintomas comórbidos e a carga da polimedicação motivam a procura por intervenções adjuvantes com poucos efeitos secundários. [B41].
Os óleos essenciais e os seus principais componentes (terpenos) constituem uma potencial opção terapêutica adjuvante, com base em:
- dados pré-clínicos sobre modulação GABAérgica, regulação serotoninérgica, efeitos anti-neuroinflamatórios e antioxidantes;
- uso tradicional em aromaterapia para ansiedade, sono e humor;
- perfis de segurança económicos com aplicação adequada [B42], [B43], [B44].
Neurobiologia do Transtorno do Espectro do Autismo
Este relatório analisa as bases neurobiológicas da PTA, os mecanismos de ação molecular de terpenos relevantes, a evidência clínica em populações com PTA e desenvolve recomendações baseadas em evidências de dosagem e segurança para o uso de óleos essenciais como parte de uma abordagem terapêutica multimodal.
Desequilíbrio GABA/Glutamato E/I
A hipótese do desequilíbrio E/I é um dos conceitos neurobiológicos mais robustos na investigação da TEA. [B17], [B18]. O glutamato, o principal neurotransmissor excitatório, e o GABA (ácido gama-aminobutírico), o principal neurotransmissor inibitório, regulam a excitabilidade neuronal, a plasticidade sináptica e a dinâmica da rede. Um desequilíbrio a favor da transmissão excitatória (aumento da relação E/I) ou o controlo inibitório perturbado podem levar à hiperexcitabilidade, à dificuldade de filtragem sensorial e à alteração do processamento de informação social. [B45], [B46].
Estudos de Espectroscopia por Ressonância Magnética (MRS) demonstram alterações regionais: concentrações reduzidas de glutamato no estriado, níveis aumentados de GABA pré-frontal em alguns estudos e relações glutamato/GABA alteradas nos córtexes sensoriais e associativos. [B19], [B20].
Análises post-mortem demonstram expressão reduzida de GAD65 e GAD67 (enzimas sintetizadoras de GABA) no córtex pré-frontal e cerebelo, assim como densidade alterada de interneurónios GABAérgicos (em particular, interneurónios positivos para parvalbumina). [B47], [B48].
A perspetiva da biologia do desenvolvimento é crítica: o GABA atua excitatório durante as fases iniciais do desenvolvimento devido a altas concentrações intracelulares de cloreto (mediadas pelo cotransportador NKCC1) e muda pós-natalmente para uma ação inibitória através da expressão do cotransportador KCC2. [B49].
Foi demonstrado um GABAergic switch atrasado ou perturbado em modelos de rato de TEA e corrigido com bumetanida (inibidor de NKCC1), levando a um comportamento social melhorado [B50], [B51].
Um ensaio clínico com bumetanida em crianças com TEA mostrou melhorias moderadas na comunicação social, mas com limitações metodológicas. [B52].
A disfunção glutamatérgica manifesta-se em alterações na expressão de subunidades de recetores NMDA e AMPA, plasticidade sináptica perturbada (potenciação/depressão a longo prazo) e transmissão glutamatérgica excessiva em circuitos específicos. [B53], [B54].
Estudos genéticos identificaram mutações associadas ao TEA (Transtorno do Espectro Autista) em genes da sinapse glutamatérgica (GRIN2B, GRIA1, SLC1A1). [B55].
Modelos pré-clínicos demonstram que a modulação da transmissão glutamatérgica (por exemplo, através de antagonistas de mGluR5) pode melhorar comportamentos semelhantes aos da Perturbação do Espectro do Autismo (PEA). [B56].
Serotonina, Dopamina e Ocitocina
Os sistemas monoaminérgicos desempenham papéis centrais na cognição social, processamento de recompensa e regulação emocional – domínios que estão afetados na Perturbação do Espectro do Autismo (PEA). [B57], [B58].
Serotonina (5-HT)
A hiper-serotoninemia (níveis elevados de serotonina periférica) foi detectada em 25–50% dos pacientes com TEA, embora a relação com os níveis centrais de 5-HT permaneça incerta [B59], [B60]. Estudos de imagem mostram capacidade reduzida de síntese de serotonina no córtex frontal e tálamo em crianças com TEA [B61]. Variantes genéticas nos transportadores de serotonina (5-HTTLPR) e na triptofano hidroxilase-2 (TPH2) estão associadas ao risco de TEA. [B62]. Estudos pré-clínicos demonstram que a disfunção serotoninérgica durante janelas de desenvolvimento críticas leva a fenótipos semelhantes ao TEA [B63]. Inibidores Seletivos da Recaptura de Serotonina (ISRS) mostram resultados mistos na TEA: ineficácia para sintomas centrais, efeitos moderados em comportamentos repetitivos e ansiedade [B64].
Dopamina (DA)
Os circuitos dopaminérgicos mesolímbico e mesocortical medeiam o processamento de recompensas, a motivação e o reforço social. [B65]. Pacientes com DDA mostram ativação reduzida do estriado ventral em recompensas sociais (rostos, interação social) em comparação com recompensas não sociais [B66], [B67]. Estudos PET relatam aumento da densidade de transportadores de dopamina no estriado e diminuição da disponibilidade de recetores D2. [B68]. Estudos genéticos identificaram variantes associadas ao TEA em genes dopaminérgicos (DRD1, DRD2, DAT1) [B69]. Modelos pré-clínicos demonstram que a disfunção dopaminérgica leva a uma preferência social alterada e a comportamentos repetitivos. [B70].
Oxitocina (OT)
A ocitocina é um neuropeptídeo com um papel central na ligação social, confiança, cognição social e regulação do stress. [B71]. Pacientes com TEA apresentam níveis reduzidos de oxitocina no plasma, expressão alterada do recetor de oxitocina (OXTR) e variantes genéticas no OXTR e CD38 (libertação de oxitocina). [B72], [B73]. A oxitocina intranasal melhorou a cognição social e o contacto visual em adultos com TEA em alguns estudos, mas com resultados inconsistentes e falta de eficácia em populações pediátricas. [B74], [B75]. Estudos pré-clínicos demonstram que a oxitocina regula o desenvolvimento GABAérgico: a administração de oxitocina durante períodos críticos corrigiu o atraso na transição GABAérgica e melhorou o comportamento social em modelos de ratinho de TEA [B50], [B76]. Estas descobertas ligam mecanisticamente os sistemas oxitocinérgico e GABAérgico.
Neuroinflamação – Microglia, TNF-α e Citocinas
A neuroinflamação crónica é um mecanismo patofisiológico convergente na TEA, apoiado por estudos post-mortem, de imagem e de biomarcadores. [B77], [B78].
Ativação da microglia
A microglia são células imunes residentes do SNC que regulam a poda sináptica, o desenvolvimento neuronal e a vigilância imunitária. [B79]. Estudos post-mortem demonstraram a ativação de microglia (aumento da expressão de Iba1, morfologia ameboide) no córtex pré-frontal, cerebelo e substância branca de cérebros de indivíduos com TEA. [B80], [B81]. A PET-imagem com ligandos do Translocator Protein (TSPO) demonstrou um aumento da ativação microglial em múltiplas regiões cerebrais em pacientes vivos com TEA [B82]. A microglia ativada liberta citocinas pró-inflamatórias, produz ROS e pode fagocitar estruturas sinápticas, resultando em conectividade perturbada [B83].
Citocinas pró-inflamatórias
Foram detectados níveis elevados de TNF-α, IL-6, IL-1β e IFN-γ em plasma, LCR e tecido cerebral post-mortem de doentes com TEA. [B84], [B85]. Modelos de Ativação Imunitária Materna (MIA), nos quais ratos grávidos são tratados com Poly(I:C) ou LPS, produzem descendentes com comportamentos semelhantes aos do TEA e níveis elevados de TNF-α [B86], [B87]. O TNF-α modula a transmissão sináptica, reduz a inibição GABAérgica e afeta a plasticidade sináptica [B88]. O bloqueio do TNF-α em modelos de MIA preveniu fenótipos semelhantes aos do TEA [B89].
Disfunção astrocitária
Os astrócitos regulam a homeostase do glutamato (através dos transportadores de glutamato EAAT1/2), o tamponamento de K+ e o suporte metabólico aos neurónios [B90]. Estudos post-mortem mostram astrogliose (aumento da expressão de GFAP) em cérebros de indivíduos com TEA [B91]. Astroglia disfuncionais podem contribuir para a acumulação excessiva de glutamato extracelular e excitotoxicidade [B92].
Stress Oxidativo e Disfunção Mitocondrial
O stress oxidativo resulta de um desequilíbrio entre a produção de ROS e as defesas antioxidantes. [B93]. Vários estudos relatam marcadores de stresse oxidativo elevados na TEA: aumento da peroxidação lipídica (malondialdeído), carbonilação de proteínas, oxidação do ADN (8-OHdG) e redução da capacidade antioxidante (glutationa, superóxido dismutase, catalase) [B28], [B94], [B95].
Esgotamento de glutationa
A glutationa (GSH) é o antioxidante intracelular primário. Pacientes com TEA apresentam níveis reduzidos de GSH no plasma e no cérebro, aumento da glutationa oxidada (GSSG) e redução da relação GSH/GSSG. [B96], [B97]. Variantes genéticas nas enzimas de síntese de glutationa (GCLC, GSS) estão associadas ao risco de DTA [B98].
Disfunção mitocondrial
5 a 30 % dos doentes com DDA mostram evidência bioquímica de disfunção mitocondrial (aumento de lactato, redução da atividade da cadeia respiratória) [B99], [B100]. As mitocôndrias são a principal fonte de ROS; a disfunção mitocondrial leva a um aumento da produção de ROS, redução da síntese de ATP e perturbação da homeostase do cálcio. [B101]. Estudos pré-clínicos mostram que antioxidantes mitocondriais (MitoQ) melhoram comportamentos semelhantes ao TEA em modelos de ratinho [B102].
Via Nrf2/HO-1
O fator nuclear eritroide 2 relacionado ao fator 2 (Nrf2) é um regulador mestre da resposta antioxidante, que induz a expressão da heme oxigenase-1 (HO-1), NAD(P)H:quinona oxidorredutase-1 (NQO1), glutationa S-transferases e outras enzimas antioxidantes. [B103]. A atividade reduzida de Nrf2 foi demonstrada em modelos de TEA; ativadores de Nrf2 (sulforafano) mostraram melhorias no comportamento social e na comunicação em indivíduos com TEA em pequenos ensaios clínicos. [B104], [B105].
Eixo Intestino-Cérebro
A comunicação bidirecional entre o trato gastrointestinal e o SNC ocorre através de vias neuronais (nervo vago), endócrinas (eixo hipotálamo-hipófise-adrenal), imunológicas e metabólicas [B106]. Pacientes com TEA apresentam alta prevalência de sintomas gastrointestinais (obstipação, diarreia, dor abdominal) e disbiose. [B107], [B108].
Alterações do microbioma
As meta-análises mostram, na TEA, diversidade microbiana reduzida, aumento das proporções Firmicutes/Bacteroidetes, redução de Bifidobacterium e Prevotella, e aumento de Clostridium e Desulfovibrio. [B109], [B110]. Estas alterações correlacionam-se com a gravidade dos sintomas [B111].
Conexões mecanicistas
A microbiota intestinal produz precursores de neurotransmissores (triptofano → serotonina, glutamato → GABA), ácidos gordos de cadeia curta (butirato, propionato, acetato) e modula a função imunitária [B112]. A exposição a propionato induz comportamentos semelhantes aos do TEA em modelos de roedores. [B113]. O transplante de microbiota fecal (TMF) de pacientes com TEA em ratinhos isogénicos transmitiu comportamentos semelhantes aos do TEA e alterou a expressão génica cerebral (genes das sinapses serotoninérgicas e glutamatérgicas). [B32]. FMT de doadores saudáveis em modelos de rato de TEA melhorou o comportamento social e normalizou os níveis de neurotransmissores [B114].
Mediação vagal
O nervo vago transmite sinais do intestino para o tronco cerebral (núcleo do trato solitário) e daí para as regiões límbicas e corticais. [B115]. Estudos pré-clínicos demonstram que a eletroacupuntura melhorou comportamentos semelhantes ao TEA em modelos murinos de VPA através de mecanismos dependentes do nervo vago e modulação do microbioma; a vagotomia reverteu estes efeitos [B116].
Disfunção Sináptica – Neurexina, Proteínas SHANK
A disfunção sináptica é um conceito patofisiológico central na TDAH, apoiado por evidências genéticas, moleculares e eletrofisiológicas [B117], [B118].
Complexo Neuroligina-Neurexina
As neuroliginas (NLGN1-4) são moléculas de adesão celular pós-sinápticas que interagem com as neurexinas pré-sinápticas (NRXN1-3) e regulam a diferenciação, maturação e função sinápticas. [B119]. Foram identificadas mutações nos genes NLGN3 e NLGN4X em pacientes com TEA. [B120]. NLGN3-R451C-Ratos Knock-in exibem transmissão inibitória aumentada, interação social perturbada e comportamentos repetitivos [B121]. Ratos com eliminação do gene NLGN4 exibem transmissão excitatória reduzida e fenótipos semelhantes aos da TEA [B122].
Proteína SHANK
SHANK1-3 são proteínas de andaime pós-sináptico que organizam recetores de glutamato, o citoesqueleto de actina e moléculas de sinalização. [B123]. As mutações no gene SHANK3 estão associadas à Síndrome de Phelan-McDermid (deleção 22q13), caracterizada por Transtorno do Espectro Autista (TEA), deficiência intelectual e défices na fala. [B124]. Camundongos com deleção do gene SHANK3 exibem densidade reduzida de espinhas dendríticas, transmissão sináptica alterada e comportamentos semelhantes aos do TEA [B125]. Mutações no SHANK2 também estão associadas ao TEA; ratinhos com deleção do SHANK2 apresentam hiperatividade, comportamentos repetitivos e disfunção do recetor NMDA [B126].
Plasticidade sináptica
Potenciação a Longo Prazo (LTP) e Depressão a Longo Prazo (LTD), correlatos celulares da aprendizagem e da memória, estão perturbados em múltiplos modelos de ratinho de TEA. [B127]. Um desequilíbrio alterado na LTP/LTD pode contribuir para a maturação desregulada de circuitos dependente da experiência e para dificuldades na aprendizagem social. [B128].
Regiões cerebrais afetadas
A imagiologia estrutural e funcional identifica alterações consistentes em regiões cerebrais específicas na Perturbação do Espectro do Autismo (PEA) [B129], [B130].
Córtex pré-frontal (CPF)
O córtex pré-frontal (CPF) media funções executivas, memória de trabalho, flexibilidade cognitiva e cognição social [B131]. Pacientes com DDA apresentam menor ativação do PFC durante tarefas de Teoria da Mente, conectividade prejudicada do PFC com regiões posteriores e microestrutura alterada do PFC. [B132], [B133]. Estudos post-mortem demonstram densidade neuronal aumentada, redução da largura das minicolunas e défices GABAérgicos no PFC. [B134].
Amígdala
A amígdala é central para o processamento emocional, perceção social e condicionamento do medo [B135]. Crianças com TEA mostram um aumento precoce da amígdala (2-4 anos), seguido de normalização ou redução do volume na adolescência [B136]. Estudos funcionais mostram ativação reduzida da amígdala no processamento de rostos e conectividade amígdala-PFC perturbada. [B137], [B138].
Cerebelo
Tradicionalmente associado ao controlo motor, o cerebelo também desempenha papéis em processos cognitivos, previsão sensorial e aprendizagem social [B139].
Pacientes com TEA mostram perda de células de Purkinje, redução do volume cerebelar (especialmente do verme) e conectividade cerebelo-cortical perturbada [B140], [B141]. A disfunção do cerebelo pode contribuir para a predição sensorial perturbada, estereotipias motoras e processamento deficiente do tempo social [B142].
Hipocampo
O hipocampo medeia a memória declarativa, a navegação espacial e o processamento contextual [B143]. Pacientes com TEA apresentam aumento do hipocampo na infância, conectividade hipocampal alterada e condicionamento de medo contextual perturbado [B144], [B145].
Estrado
O estriado (núcleo caudado, putamen, núcleo accumbens) media o processamento de recompensa, a aprendizagem de hábitos e o controlo motor. [B146]. Pacientes com TEA apresentam aumento do estriado, redução da ativação para recompensas sociais e conectividade cortico-estriatal alterada. [B147], [B148].
Mecanismos moleculares de ação dos terpenos em TEA
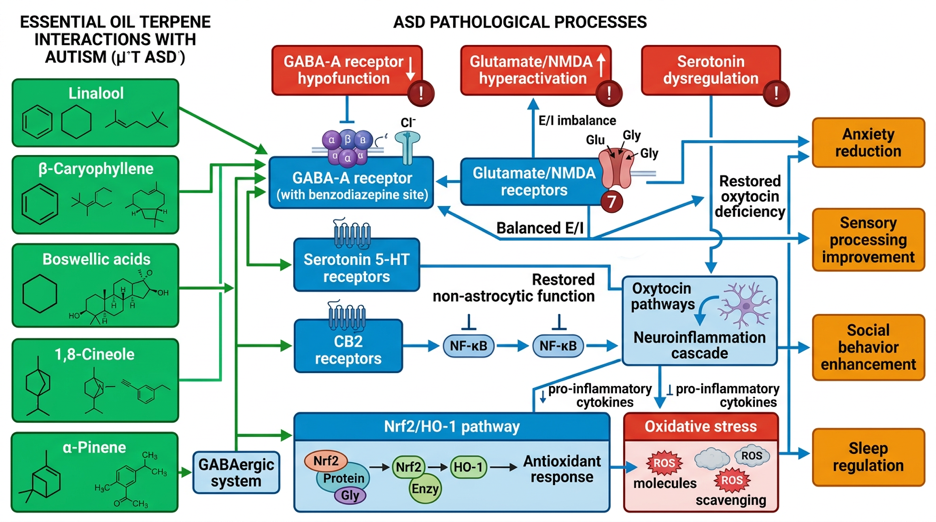
Figura 2: Vias de sinalização molecular de terpenos no transtorno do espectro do autismo – equilíbrio GABA/glutamato, neuroinflamação e stress oxidativo
Os terpenos são uma classe diversificada de produtos naturais que constituem os principais componentes dos óleos essenciais [B149]. As suas propriedades lipofílicas permitem a passagem da barreira hematoencefálica e a interação com alvos neuronais. [B150]. Esta secção analisa os mecanismos moleculares de terpenos específicos que atacam alvos patofisiológicos relevantes para o TEA.
Linalol – Sítio GABA-A/Benzodiazepina, Serotonina, Anti-inflamatório
O linalol (3,7-Dimetil-1,6-octadien-3-ol) é um álcool monoterpénico e um componente principal do óleo essencial de lavanda (Lavandula angustifolia, 25–45 %), coentros, bergamota e outros. [B151].
Modulação do recetor GABA-A
O linalol demonstra efeitos ansiolíticos que são bloqueados pelo flumazenil (um antagonista de benzodiazepínicos), o que indica uma interação com o local de ligação dos benzodiazepínicos do recetor GABA-A. [B152]. Num modelo de exposição olfativa, os vapores de linalol produziram efeitos ansiolíticos em ratos (labirinto em cruz elevado, caixa clara-escura) que estavam ausentes em ratos anosmáticos (destruição do epitélio olfativo), o que demonstra um efeito mediado pelo olfato. [B152]. Estudos eletrofisiológicos demonstraram que o linalol potencia os fluxos de cloreto induzidos por GABA em neurónios em cultura [B153]. Esta modulação GABAérgica é altamente relevante para o TEA, uma vez que défices GABAérgicos e desequilíbrio E/I representam mecanismos patofisiológicos centrais. [B17], [B18].
Modulação Serotoninérgica
A inalação de linalol alterou os níveis de serotonina no córtex frontal de ratinhos, sugerindo modulação da transmissão serotoninérgica [B154]. Num estudo com adultos saudáveis, a inalação de 20 minutos de linalol reduziu o humor depressivo e aumentou a atividade parassimpática (aumento da variabilidade da frequência cardíaca). [B155]. Estudos ex vivo demonstram que o linalol aumenta as concentrações intracelulares de cálcio em neurónios hipotalâmicos de oxitocina, o que representa um mecanismo potencial para a modulação oxitocinérgica. [B155]. Estas descobertas associam o linalol aos sistemas serotoninérgico e oxitocinérgico, que são disfuncionais na TEA. [B59], [B72].
Efeitos anti-inflamatórios
As revisões sistemáticas relatam propriedades anti-inflamatórias do linalol em modelos pré-clínicos, incluindo a redução da ativação de TNF-α, IL-6, IL-1β e NF-κB. [B156]. Num modelo de neuroinflamação induzida por stress, o linalol reduziu a ativação da micróglia e a expressão de citocinas pró-inflamatórias [B157]. Estes efeitos anti-neuroinflamatórios são relevantes para a TSA, pois a neuroinflamação crónica é um mecanismo patofisiológico convergente [B77], [B78].
Farmacocinética
Após exposição inalatória, o linalol é rapidamente absorvido e atinge a circulação sistémica; metabolitos (óxidos de linalol, glucurónidos) são detetados na urina. [B158]. A passagem pela barreira hematoencefálica é provável devido à lipofilicidade, mas os dados diretos de farmacocinética do SNC em humanos são limitados. [B159].
β-Cariofileno – Agonista CB2, NF-κB, Neuroinflamação
O β-Cariofileno (BCP) é um hidrocarboneto sesquiterpénico encontrado em pimenta-preta, cravinho, canábis (componente não psicoativo), copaíba e outras plantas [B160].
Agonismo do recetor CB2
O BCP é um agonista seletivo do recetor de tipo 2 de canabinóides (CB2) sem afinidade para os recetores CB1, o que permite efeitos imunomoduladores não psicoativos. [B161]. Os recetores CB2 são primariamente expressos em células imunes (micróglia, células imunes periféricas) e regulam a libertação de citocinas, a ativação da micróglia e a neuroinflamação. [B162]. Em ratos com eliminação génica de CB2, os efeitos de BCP estiveram ausentes, o que confirma a especificidade de CB2 [B163].
Efeitos anti-neuroinflamatórios
O BCP reduz a neuroinflamação em múltiplos modelos pré-clínicos: neuroinflamação induzida por LPS, lesão cerebral traumática, doenças neurodegenerativas [B164], [B165]. Mecanismos incluem a redução da ativação da microglia (expressão reduzida de Iba1 e CD11b), supressão de citocinas pró-inflamatórias (TNF-α, IL-6, IL-1β) e modulação das vias de sinalização do NF-κB. [B166]. Num modelo de ativação imune materna (MIA, um modelo relevante para TEA), o tratamento com BCP melhorou comportamentos semelhantes ao TEA (défices sociais, comportamentos repetitivos) e reduziu a neuroinflamação na descendência. [B167].
Modulação GABAérgica e nitrinergica
Estudos farmacológicos comportamentais demonstram que os efeitos ansiolíticos e antidepressivos do BCP são bloqueados pelo flumazenil (antagonista de benzodiazepínicos) e L-NAME (inibidor da óxido nítrico sintase), o que sugere o envolvimento dos sistemas GABAérgico e nitrinérgico. [B168]. Estas descobertas sugerem que a BCP pode modular indiretamente a função gabaérgica através da redução da neuroinflamação mediada pela CB2.
Efeitos antioxidantes
O BCP demonstra propriedades antioxidantes através da redução de ROS, peroxidação lipídica e aumento de enzimas antioxidantes endógenas (SOD, catalase, GSH). [B169]. Num modelo de stress oxidativo, o BCP protegeu os neurónios da apoptose induzida por H₂O₂ [B170].
Relevância clínica para TEA
A combinação da redução da neuroinflamação mediada por CB2, dos efeitos antioxidantes e da modulação GABAérgica indireta torna o BCP um candidato mecanisticamente plausível para a terapia adjuvante na TEA, especialmente em pacientes com assinaturas de neuroinflamação. [B171].
Ácidos boswellicos – Nrf2/HO-1, anti-neuroinflamatório
Os ácidos bosvélicos são ácidos triterpénicos pentacíclicos provenientes da resina de espécies do género Boswellia (olíbano), incluindo o ácido β-bosvélico, o ácido 11-ceto-β-bosvélico (KBA) e o ácido 3-O-acetil-11-ceto-β-bosvélico (AKBA) [B172].
Ativação Nrf2/HO-1
Os ácidos boswellicos ativam a via de sinalização Nrf2, um regulador mestre da resposta antioxidante [B173]. Num modelo de neuroinflamação murina, o tratamento com extrato de Boswellia aumentou a localização nuclear de Nrf2 e a expressão de HO-1 no hipocampo e no córtex. [B174]. A HO-1 catalisa a degradação do heme em biliverdina (antioxidante), monóxido de carbono (anti-inflamatório, vasodilatador) e ferro; a indução da HO-1 protege contra o stress oxidativo e a neuroinflamação. [B175].
Mecanismos anti-neuroinflamatórios
Os ácidos boswellia reduzem a ativação da microglia e dos astrócitos (expressão reduzida de Iba1, GFAP), suprimem citocinas pró-inflamatórias (TNF-α, IL-6, IL-1β) e inibem as vias de sinalização NF-κB e MAPK [B176], [B177]. Num modelo de neuroinflamação induzida por LPS, o tratamento com Boswellia melhorou os défices cognitivos e reduziu os marcadores de neuroinflamação. [B178].
Inibição da 5-Lipoxigenase (5-LOX)
Os ácidos boswellicos, em particular o AKBA, inibem a 5-LOX, uma enzima que metaboliza o ácido araquidónico em leucotrienos pró-inflamatórios. [B179]. A inibição da 5-LOX reduz a inflamação mediada por leucotrienos e foi associada a efeitos neuroprotetores em estudos pré-clínicos [B180]. No entanto, a evidência para a inibição da 5-LOX como o principal mecanismo de neuroproteção da Boswellia é limitada na literatura atual; a ativação de Nrf2/HO-1 parece ser o mecanismo dominante. [B174].
Evidência pré-clínica em modelos relevantes para TEA
Num modelo de rato de TEA induzido por ácido valproico (VPA), o tratamento com extrato de Boswellia melhorou a interação social, reduziu comportamentos repetitivos e normalizou marcadores de neuroinflamação. [B181]. Estas conclusões apoiam a hipótese de que a redução da neuroinflamação mediada por Boswellia e os efeitos antioxidantes podem melhorar os comportamentos relacionados com o TEA.
1,8-Cineol – GABA-A/Benzodiazepina, Ansiolítico
1,8-Cineol (Eucaliptol) é um óxido monoterpénico e o principal componente do eucalipto (Eucalyptus globulus, 70–90 %), do alecrim, da árvore do chá e do louro [B182].
Modulação do recetor GABA-A
A inalação de 1,8-cineol produziu efeitos ansiolíticos e antidepressivos dependentes da dose em ratos (Elevated Plus Maze, Forced Swim Test, Tail Suspension Test). [B183]. Estes efeitos foram bloqueados pelo flumazenil, o que indica uma interação com o local de ligação da benzodiazepina no recetor GABA-A. [B183]. Foi demonstrada a dependência da dose: doses baixas (0,1–1 µg/rato, inalatório) mostraram efeitos ansiolíticos, enquanto doses mais elevadas (10 µg/rato) produziram efeitos sedativos. [B184].
Efeitos anti-inflamatórios e antioxidantes
O 1,8-cineol demonstra propriedades anti-inflamatórias através da inibição de NF-κB, redução de TNF-α, IL-1β e síntese de leucotrienos [B185]. Num modelo de neuroinflamação induzido por LPS, o 1,8-cineol reduziu a ativação da microglia e o stress oxidativo. [B186].
Aspetos de segurança
O 1,8-Cineol é contraindicado em crianças com idade inferior a 3 anos devido ao risco de laringoespasmo e depressão respiratória. [B187]. Com a aplicação adequada (inalatória, doses baixas), o 1,8-cineol apresenta um perfil de segurança favorável em adultos e crianças mais velhas. [B188].
α-Pineno – GABAérgico
α-Pineno é um monoterpeno bicíclico encontrado em pinheiros, alecrim, salvía e canábis [B189].
Modulação GABAérgica
As Revisões Sistemáticas associam o α-pineno à modulação da neurotransmissão GABAérgica, embora os estudos mecanísticos diretos sejam limitados. [B190]. Em modelos comportamentais, o α-pineno demonstra efeitos ansiolíticos e sedativos, sugerindo mecanismos GABAérgicos. [B191]. Não existem dados eletrofisiológicos disponíveis na literatura atual sobre a interação direta com os recetores GABA-A.
Efeitos anti-inflamatórios e neuroprotetores
O α-pineno demonstra propriedades anti-inflamatórias através da inibição do NF-κB e da redução de citocinas pró-inflamatórias [B192]. Num modelo de isquemia-reperfusão, o α-pineno protegeu contra lesões neuronais e reduziu o stress oxidativo [B193].
Inibição da Acetilcolinesterase (AChE)
Alguns estudos relatam atividade inibidora de AChE por α-pineno, o que poderia potenciar a neurotransmissão colinérgica [B194]. No entanto, a relevância para a S.A.D. é incerta, uma vez que a disfunção colinérgica não é um mecanismo fisiopatológico primário na S.A.D. [B195].
Ylang-Ylang/Cananga odorata – Serotonina/Dopamina no Modelo VPA
O óleo essencial de Ylang-Ylang (Cananga odorata) contém linalol, geraniol, β-cariofileno e outros terpenos [B196].
Evidência pré-clínica no modelo VPA-ASD
A inalação do óleo essencial de Cananga odorata melhorou os comportamentos semelhantes à ansiedade, interação social e função cognitiva em ratos com TEA induzido por ácido valproico (VPA) [B197]. Análises neuroquímicas mostraram que Cananga odorata modulou o metabolismo da serotonina e da dopamina no córtex pré-frontal e no hipocampo: níveis aumentados de serotonina, relações reduzidas de 5-HIAA/serotonina (indicativo de diminuição do turnover de serotonina) e níveis normalizados de dopamina. [B197].
Interpretação mecanicista
A melhoria de comportamentos semelhantes ao TEA através da modulação dos sistemas serotoninérgico e dopaminérgico é mecanisticamente plausível, uma vez que ambos os sistemas são disfuncionais no TEA. [B57], [B58]. Os componentes específicos de *Cananga odorata* responsáveis por estes efeitos não foram identificados; o linalol e o β-cariofileno são candidatos prováveis, com base nos seus mecanismos conhecidos [B152], [B161].
Limitações
Estes achados provêm de um único modelo pré-clínico (ratos VPA); falta replicação noutros modelos de TEA e translação para estudos em humanos [B197].
Óleos essenciais específicos e evidências clínicas em TEA
Lavanda/Linalol – Conformidade ABA, Neurónios Oxitocina
Evidência clínica em DCC
Um pequeno estudo piloto (n = 12 crianças com TEA) investigou a aromaterapia com lavanda como adjuvante durante a terapia Applied Behavior Analysis (ABA). [B198]. O lavandim foi difundido como “20 gotas em 100 ml” (presumivelmente água ou óleo transportador, detalhes pouco claros) durante as sessões de terapia. O estudo relatou pontuações de adesão mais altas (cooperação, conclusão de tarefas) durante a exposição ao lavandim em comparação com as sessões de controlo. [B198]. As limitações incluem amostra muito pequena, falta de randomização, cegamento incerto e falta de dosagem padronizada.
Um estudo observacional com quatro crianças com Perturbação do Espectro do Autismo (PEA) e com graves deficiências intelectuais investigou a massagem de aromaterapia (lavanda, gerânio, mandarina em óleo de base) integrada nas rotinas diárias. [B199]. O estudo relatou um aumento nos comportamentos de atenção partilhada (contacto visual, atividades conjuntas) após a introdução da massagem de aromaterapia. [B199]. As limitações incluem falta de controlo, amostra pequena e fatores de confusão devido aos efeitos da massagem (estimulação tátil, interação social).
Fundamento mecanicista
Os achados clínicos são consistentes com mecanismos pré-clínicos: a modulação GABAérgica mediada pelo linalol pode reduzir a ansiedade e melhorar a cooperação; a modulação serotoninérgica e oxitocina pode promover a atenção social e a interação. [B152], [B155]. Um estudo com adultos saudáveis demonstrou que a inalação de lavanda reduziu o humor depressivo e, em experiências ex vivo, aumentou as concentrações intracelulares de cálcio nos neurónios hipotalâmicos de oxitocina [B155]. Esta modulação oxitocina-érgica é altamente relevante para a TEA, uma vez que a disfunção da oxitocina é um mecanismo fisiopatológico estabelecido. [B72].
Limitações da evidência
A evidência clínica para lavanda em TEA é de qualidade muito baixa: amostras pequenas, falta de randomização, cegamento inadequado, intervenções heterogéneas e falta de replicação [B198], [B199]. Faltam estudos randomizados controlados de alta qualidade com preparações de lavanda padronizadas, medidas de resultados objetivas e poder suficiente.
Bergamota – Ensaio Clínico Randomizado em crianças com Perturbação do Espectro do Autismo, resultado não significativo
Estudo randomizado controlado
Um estudo randomizado e cego investigou o óleo essencial de bergamota (Citrus bergamia) em crianças com Perturbações do Espectro do Autismo (PEA) com ansiedade induzida por medicação (n = 42). [B200]. As crianças foram aleatoriamente distribuídas para inalação de óleo de bergamota durante 15 minutos ou placebo (água) antes de exames médicos. O desfecho primário foi a ansiedade medida pela Modified Yale Preoperative Anxiety Scale (mYPAS). Após ajuste para a ansiedade basal, o grupo de bergamota não mostrou uma redução significativa da ansiedade em comparação com o placebo (p > 0,05). [B200].
interpretação
Este é o único estudo randomizado controlado identificado com óleos essenciais em crianças com TEA. O resultado negativo pode ter várias causas: (1) a curta duração da exposição (15 minutos) pode ser insuficiente; (2) a ansiedade aguda em ambientes médicos pode ser mais difícil de modular do que a ansiedade crónica; (3) variabilidade individual na sensibilidade e preferências olfativas; (4) possíveis efeitos de teto em níveis de ansiedade de base já elevados. [B200].
Mecanismos pré-clínicos
Estudos pré-clínicos demonstram efeitos ansiolíticos da bergamota em modelos de roedores [B201]. Curiosamente, estes efeitos não foram bloqueados por flumazenil, sugerindo mecanismos não mediados por benzodiazepinas e distinguindo a bergamota do linalol e do 1,8-cineol [B201]. A bergamota contém linalol, acetato de linalilo, limoneno e bergapteno; os componentes específicos responsáveis pelos efeitos ansiolíticos são incertos. [B202].
Implicações clínicas
O resultado negativo deste ensaio clínico randomizado atenua as expectativas para a bergamota na ansiedade aguda em Transtorno do Espectro do Autismo (TEA). São necessários mais estudos com durações de exposição mais longas, desfechos de ansiedade crônica e outras populações com TEA antes que a bergamota possa ser recomendada para o TEA. [B200].
Olíbano / Boswellia – Anti-neuroinflamatório, Nrf2
Evidência clínica em DCC
Não foram identificados ensaios clínicos aleatórios controlados com óleo essencial de olíbano (Boswellia) ou extratos de Boswellia em pacientes com TEA. A literatura atual não inclui dados clínicos específicos para TEA relativos ao olíbano. [B203].
Evidência pré-clínica
Conforme descrito na Secção 3.3, os ácidos Boswellia demonstram fortes efeitos anti-neuroinflamatórios e antioxidantes em modelos pré-clínicos, incluindo a ativação de Nrf2/HO-1, inibição da microglia e melhoria de comportamentos semelhantes ao TEA em modelos de rato VPA. [B174], [B181]. Esta plausibilidade mecanicista apoia a hipótese de que o Boswellia pode ser útil em pacientes com TEA com assinaturas de neuroinflamação.
Aplicação clínica de outras indicações
Os extratos de Boswellia (via oral) são usados clinicamente para doenças inflamatórias (artrite, asma, doenças inflamatórias intestinais), com evidência moderada de eficácia e perfil de segurança favorável. [B204]. A aplicação inalatória do óleo essencial de olíbano é tradicional, mas faltam dados clínicos de farmacocinética e eficácia. [B205].
Necessidade de investigação
São necessários ensaios clínicos controlados com Boswellia (por via oral ou inalatória) em pacientes com TEA, idealmente estratificados por biomarcadores de neuroinflamação, para avaliar a eficácia clínica. [B206].
Cedro/Zeder – Sedação, GABAérgico
Evidência clínica e pré-clínica
A literatura existente não contém dados mecanísticos ou clínicos específicos para o óleo essencial de madeira de cedro (Cedrus atlantica, Juniperus virginiana) na Perturbação do Espectro do Autismo (PEA) ou em modelos pré-clínicos relevantes para a PEA. [B207]. As aplicações tradicionais incluem sedação e redução da ansiedade, mas a evidência científica para mecanismos GABAérgicos ou eficácia clínica está em falta na literatura analisada. [B208].
Componentes principais
O óleo de madeira de cedro contém cedrol (álcool sesquiterpénico), α-cedreno e tujopseno [B209]. O cedrol está associado a propriedades sedativas, mas faltam estudos diretos sobre a interação com o recetor GABA-A ou a modulação da neuroinflamação [B210].
Conclusão
A evidência de que o cedro é eficaz para o TEA é insuficiente; não é possível fazer recomendações com base na literatura disponível. [B207].
Vetiver – Atenção
Evidência clínica e pré-clínica
A literatura existente não contém dados específicos para o óleo essencial de Vetiver (Vetiveria zizanioides) em ASD ou em modelos relevantes para ASD. [B211]. Relatos anedóticos e aplicações tradicionais sugerem efeitos na atenção e hiperatividade, mas faltam estudos controlados. [B212].
Componentes principais
O óleo de vetiver contém vetiverol, khusimol, α-vetivona e β-vetivona (álcoois e cetonas sesquiterpénicos). [B213]. Os estudos mecanicistas sobre estes componentes relativos a sistemas de neurotransmissores ou neuroinflamação são inexistentes na literatura analisada. [B214].
Conclusão
A evidência para o vetiver no TDAH é insuficiente; são necessárias mais pesquisas antes que se possam fazer recomendações. [B211].
Ylang-Ylang – Serotonina/Dopamina, Modelo VPA
Evidência pré-clínica
Tal como descrito na Secção 3.5, a inalação de óleo essencial de Cananga odorata (Ylang-Ylang) melhorou comportamentos semelhantes aos de Transtorno de Déficit de Atenção e Hiperatividade (TDAH) em ratos expostos ao Propionato de Vinilacetilénio (PVA) e modulou o metabolismo da serotonina e da dopamina no córtex pré-frontal e no hipocampo. [B197]. Este é o único estudo identificado com Ylang-Ylang num modelo relevante para TEA.
Evidência clínica em DCC
Não foram identificados ensaios clínicos com Ylang-Ylang em doentes com TSP. [B215].
Aplicação clínica de outras indicações
O Ylang-Ylang é tradicionalmente utilizado para ansiedade, humor e relaxamento. Um pequeno estudo com adultos saudáveis mostrou que a inalação de Ylang-Ylang reduziu a pressão arterial e a frequência cardíaca, e aumentou a calma subjetiva. [B216]. Faltam estudos mecanicistas sobre efeitos serotoninérgicos e dopaminérgicos em humanos [B217].
Conclusão
A evidência pré-clínica é promissora, mas falta a translação para estudos em ASD humanos. O Ylang-Ylang poderia ser considerado como um candidato para ensaios clínicos em ASD, particularmente para sintomas de ansiedade e humor. [B197].
Mais óleos essenciais indicados para TEA
Com base numa revisão de literatura atual, foram identificados os seguintes óleos essenciais adicionais que podem ser relevantes para a TEA através de mecanismos neurobiologicamente plausíveis.
Gengibre (Zingiber officinale) – via de sinalização AKT/GSK3β
Ingredientes activos
6-Gengibreol
6-Shogaol
Zingibereno
β-Sesquiphellandreno
Receptores e mecanismos de ação
– Via de sinalização AKT/GSK3β: Fosforilação aumentada → plasticidade sináptica melhorada
– Anti-neuroinflamatório: Redução da fosforilação de STAT3 e TNF-α
– Neurogénese: Marcadores de neurogénese hipocampal melhorados em modelos pré-clínicos
– Inibição da gliose: Redução da astroglíose reativa
Evidência Clínica/Pré-clínica
- Estudo pré-clínico (modelo de rato VPA)
– O extrato oral de gengibre (4 semanas, a partir da 6.ª semana de vida) melhorou significativamente a interação social, reduziu o comportamento semelhante à ansiedade e aprimorou o desempenho da memória [B347]
- Mecanismo: Regulação positiva de AKT/GSK3β, inibição de STAT3/TNF-α, melhoria da formação de sinapses
Faltam ainda ensaios clínicos randomizados em TEA, mas a evidência pré-clínica é forte e bem fundamentada mecanisticamente.
Dosagem (Nebulizador Organik Aromas 3.0)
– 2-3 gotas para um espaço de 15 a 25 m²
– Combinação com lavanda (1:2) para um efeito relaxante
– Aplicação: 30 min antes de atividades sociais
Segurança
Bem tolerado; usar com cautela em crianças < 3 anos de idade.
Sândalo (Santalum album) – α/β-Santalol
Ingredientes activos
α-Santalol (50–55%)
β-Santalol (20–25%)
Sesquiterpeno
Receptores e mecanismos de ação
– Modulação Serotoninérgica: o α-Santalol modula recetores 5-HT (pré-clínico)
– Ansiolítico: atividade gabaérgica documentada em modelos animais
– Sedativo/Calmante: Adequado para hipersensibilidade sensorial em RAA
Evidência clínica
– A madeira de sândalo era um componente do ensaio clínico randomizado (ECR) do xarope Hiwa (medicina persa, várias ervas) em crianças com TEA, os efeitos não são atribuíveis isoladamente [B348]
– Estudos individuais sobre a ansiólise em voluntários saudáveis mostram um efeito calmante
– Faltam estudos diretos específicos para ASD com óleo de sândalo puro
Dosagem (Nebulizador Organik Aromas 3.0)
– 3-4 gotas para sala de 15 a 25 m²
– Particularmente adequado para rituais noturnos/de sono em crianças com TEA com dificuldades em adormecer
– Recomendada a combinação com lavanda (1:1)
Segurança
Muito bem tolerado; um dos óleos essenciais mais seguros para crianças (a partir dos 2 anos).
Misturas de terpenos (inspiradas em Cannabis) – Efeitos pró-sociais
Ingredientes activos
Miraceno
Limas
Linalol
Pinheiro
β-Cariofileno (como mistura)
Receptores e mecanismos de ação
– Agonismo CB1/CB2: Misturas de terpenos potenciam os efeitos do CBD (efeito de comitiva)
– Modulação GABAérgica: Linalol + Mirce no sinergismo
– Efeito pró-social demonstrado independentemente do CBD
Evidência clínica
- Modelo de rato BTBR (modelo de TEA)
Misturas de terpenos inalados (mirceno, limoneno, linalol, pineno, β-cariofileno) demonstraram efeitos pró-sociais agudos independentemente do CBD [B349] – Misturas de terpenos potenciaram o efeito do CBD em aplicação combinada
– Destaque para o efeito de entourage como princípio terapêutico para TEA
Dosagem (Nebulizador Organik Aromas 3.0)
– Recomendação de mistura: Lavanda (2C) + Pimenta preta (1C) + Bergamota (1C) + Alecrim (1C)
– Para a sala 15 são 25 m²: 5 gotas da mistura total
– Aplicação: 30 min antes de atividades sociais ou terapia de grupo
Recomendações de dosagem para o Organik Aromas Nebulizer 3.0
O Nebulizador Der Organik Aromas 3.0 utiliza o princípio de Venturi (Efeito de Bernoulli) para nebulização a frio, sem água, de óleos essenciais. [B218]. Ao contrário dos difusores ultrassónicos ou de calor, que diluem ou aquecem óleos com água, o nebulizador produz finas partículas de aerossol (1 a 5 µm) de óleos essenciais puros sem degradação térmica. [B219]. Isto permite concentrações mais elevadas de terpenos voláteis no ar ambiente e efeitos farmacológicos potencialmente mais fortes. [B220].
Princípio de Venturi e Nebulização a Frio
O princípio de Venturi descreve a redução de pressão num fluido quando este flui através de um estreitamento [B221]. No nebulizador, o ar comprimido é passado através de um bico, que cria uma pressão negativa, aspirando o óleo essencial de um reservatório e atomizando-o em finas gotículas. [B222]. Estas gotículas são libertadas para o ar ambiente, onde são inaladas ou depositam-se em superfícies [B223].
Vantagens da nebulização a frio
– Recebimento de componentes termolábeis (sem degradação por calor) [B224]
– Concentrações mais elevadas de terpenos voláteis (sem efeito de diluição com água) [B225]
– Tamanho de partícula fino (1 a 5 µm) permite penetração profunda nas vias aéreas [B226]
Desvantagens
– Custos mais elevados em comparação com difusores ultrassónicos [B227]
– Maior consumo de óleo [B228]
– Potencial de sobredosagem em caso de aplicação incorreta [B229]
Quantidades de gotas específicas por tamanho de sala
As recomendações de dose baseiam-se no volume da sala, taxa de renovação de ar, concentração de terpenos desejada e duração da exposição. As recomendações a seguir são conservadoras e levam em consideração a hipersensibilidade sensorial específica da ASD. [B230].
Tabela 1: Recomendações de dosagem específicas para o tamanho da sala para o Nebulizador de Aromas Orgânicos 3.0
Notas
- Volume da gota: 1 gota ≈ 0,05 ml de óleo essencial [B231]
- Dose inicial: Comece com o número mais baixo de gotas recomendado e aumente gradualmente ao longo de 1 a 2 semanas para avaliar a tolerância. [B232]
- Personalização individual Pacientes com TEA com hipersensibilidade olfativa pronunciada podem necessitar de doses mais baixas ou intervalos mais longos [B233]
- Ventilação: Uma boa ventilação do espaço é essencial para evitar a acumulação excessiva [B234]
Duração da utilização e pausas
Duração da aplicação
15 a 30 minutos por sessão são suficientes para atingir concentrações terapêuticas de terpenos, com base em estudos pré-clínicos de inalação [B183], [B184]. Aplicações mais longas (>30 minutos) aumentam o risco de sobrecarga sensorial e adaptação olfativa (perceção reduzida com exposição contínua) [B235].
Pausa
Pausas de 30 a 60 minutos entre as aplicações permitem a recuperação olfativa, o metabolismo de terpenos inalados e a redução das concentrações no ar ambiente. [B236]. A exposição contínua sem pausas pode levar a dores de cabeça, náuseas e aversão sensorial, especialmente em pacientes com TEA que sofrem de hipersensibilidade sensorial. [B237].
Aplicações diárias
2 a 3 aplicações por dia (manhã, tarde, noite) são suficientes para a maioria das indicações [B238]. Mais de 4 aplicações por dia aumentam o risco de efeitos secundários sem benefício terapêutico adicional [B239].
Protocolos específicos da hora do dia
Manhãs (ativador, focador)
- Azeites: Alecrim (1,8-Cineol, α-Pineno), Hortelã-pimenta (Mentol, Menta), Limão (Limoneno), Bergamota (Linalol, Acetato de linalilo)
- Dosagem: 3–5 gotas para 20–30 m² de divisão
- Duração: 15–20 minutos
- Objetivo: Fomento de estados de vigília, atenção e função cognitiva para escola/terapia [B240]
À tarde (equilibrante, moduladora de humor)
- Azeites: Bergamota, Ylang-Ylang, Gerânio, Incenso
- Dosagem: 3–5 gotas para 20–30 m² de divisão
- Duração: 20–30 minutos
- Objetivo: Redução da ansiedade pós-almoço, estabilização do humor, transição entre atividades [B241]
Ao fim da tarde (calmante, promotor do sono)
- Azeites: Lavanda (Linalol, Acetato de Linalilo), Camomila Romana (Ésteres), Cedro (Cedrol), Vetiver
- Dosagem: 4–6 gotas para 20–30 m² de espaço
- Duração: 30 minutos antes de dormir
- Objetivo: Redução da ansiedade noturna, promoção do relaxamento e da iniciação do sono [B242]
Particularidades específicas do TEA
Hipersensibilidade sensorial: 60–90 % der ASD-Patienten zeigen olfaktorische Überempfindlichkeit oder Aversion gegenüber bestimmten Gerüchen [B243]. Uma introdução graduada é essencial:
- Semana 1: Exposição fora do espaço (difusão de óleo para sala adjacente) para avaliar a aceitação [B244]
- Semana 2: Dose mais baixa (2 gotas) durante 10 minutos, paciente fora da sala durante a nebulização [B245]
- Semana 3: Dose mais baixa, paciente na sala, observação de sinais de tolerância (relaxamento, sem aversão) [B246]
- Semana 4+: Aumento gradual da dose e da duração com base na tolerância individual [B247]
Seleção baseada em preferência
Deixe o paciente (se possível) cheirar diferentes óleos e expressar as suas preferências. A preferência olfativa está correlacionada com a aceitação terapêutica e a adesão ao tratamento. [B248].
Indicações visuais e auditivas
Utilize temporizadores visuais ou sinais sonoros para indicar o início e o fim da sessão de aromaterapia, aumentando a previsibilidade e o controlo para os pacientes com Perturbação do Espectro do Autismo (PEA). [B249].
Treino para pais/cuidadores
Formar pais e cuidadores na observação de sinais de tolerância (relaxamento, atenção melhorada) e sinais de aversão (franzir o sobrolho, retraimento, agitação) [B250].
Requisitos de Qualidade – Análise GC/MS
Cromatografia Gasosa-Espectrometria de Massa (GC/MS)
GC/MS é o padrão ouro para a caracterização química de óleos essenciais [B251]. O GC separa componentes voláteis com base no ponto de ebulição e polaridade; o MS identifica componentes com base na relação massa-carga. [B252]. A análise GC/MS permite:
- Identificação de Componentes Principais: Confirmação da presença de terpenos terapeuticamente relevantes (por exemplo, linalol na lavanda, 1,8-cineol no eucalipto) [B253]
- Quantificação Composição percentual de cada componente [B254]
- Deteção de falsificações: Identificação de aditivos sintéticos, diluentes ou contaminantes [B255]
- Consistência de lote para lote: Garantir a composição reprodutível [B256]
Critérios de qualidade dos óleos essenciais terapêuticos
- 100 % reis
Sem aditivos sintéticos, óleos de base ou diluentes [B257] - Qualidade terapêutica
Óleos de plantas cultivadas, colhidas e destiladas em condições ótimas [B258] - Organisch/Wildsammlung
Livre de pesticidas, herbicidas e fertilizantes químicos [B259] - Certificado GC/MS
Cada lote deve vir acompanhado de um certificado de análise GC/MS que documente os principais componentes e a pureza. [B260] - Nome botânico
Identificação inequívoca da espécie vegetal (por ex., Lavandula angustifolia, não apenas “Lavanda”) [B261] - País de origem e data de destilação
Transparência na origem e frescura [B262]
Armazenamento
Os óleos essenciais devem ser armazenados em frascos de vidro escuro, a uma temperatura fresca (<25°C), para minimizar a oxidação e a degradação. [B263]. Os óleos oxidados podem causar irritação na pele e apresentar uma eficácia terapêutica reduzida [B264].
Instruções de segurança e contraindicações
Hipersensibilidade sensorial específica para TEA
Sensorische Verarbeitungsstörungen sind bei 60–90 % der ASD-Patienten präsent und manifestieren sich als Hypersensitivität (Überempfindlichkeit) oder Hyposensitivität (Unterempfindlichkeit) gegenüber sensorischen Stimuli [B265]. A hipersensibilidade olfativa pode levar a aversão, ansiedade, náuseas e comportamentos de evitação [B266].
Gestão de Risco
- Introdução graduada: Conforme descrito na secção 5.4, comece com doses mínimas fora da sala do paciente [B244]
- Triagem de Preferências: Teste os óleos antes da aplicação terapêutica para identificar reações adversas [B248]
- Critérios de desmantelamento: Pare imediatamente ao sinal de quaisquer distúrbios (agitação, retração, náuseas, dores de cabeça) [B267]
- Vias de aplicação alternativas: Em caso de intolerância inalatória, considere a aplicação tópica (diluída em óleo vegetal, teste de contacto necessário) ou difusão passiva (óleo num disco de algodão num canto da sala). [B268]
Risco de Epilepsia – Óleos que Contêm Alcanfor
10–30 % der ASD-Patienten haben komorbide Epilepsie [B269]. Certos óleos essenciais, em particular os que contêm cânfora, podem diminuir o limiar de convulsão e desencadear ataques. [B270].
Óleos contraindicados em caso de epilepsia
- Canforeira (Cinnamomum camphora): Contém cânfora (até 50 %), um conhecido convulsivante [B271]
- Alecrim (Rosmarinus officinalis, quimiotipo cânfora): Contém 15–25 % Alcanfor [B272]
- Salva (Salvia officinalis): Contém tujona (10–40 %), um antagonista GABA-A com propriedades convulsivas [B273]
- Isope (Hyssopus officinalis): Contém pinocamfona e isopinocamfona, que podem desencadear convulsões [B274]
- Ginkgo (Ginkgo biloba): Contém trans-anetol, que pode ter um efeito convulsivo em doses elevadas [B275]
Alternativas seguras na epilepsia: – Lavanda (Lavandula angustifolia, Linalol-Quimiotipo): Propriedades anticonvulsivantes em estudos pré-clínicos [B276] – Camomila romana (Anthemis nobilis): Nenhum efeito pró-convulsivo conhecido [B277] – Bergamota (Citrus bergamia, sem bergapteno): Segura em caso de epilepsia [B278]
Recomendação Clínica No caso de pacientes com TEA que sofrem de epilepsia, apenas óleos sem componentes que contenham cânfora ou tuiona devem ser utilizados. É aconselhável a consulta com um neurologista antes da introdução da aromaterapia. [B279].
Eucalipto em crianças com menos de 3 anos
1,8-Cineol (componente principal do eucalipto) é contraindicado em crianças com menos de 3 anos devido ao risco de laringoespasmo, broncoespasmo e depressão respiratória [B280]. Os mecanismos incluem irritação direta da mucosa das vias aéreas e ativação de reflexos vagais [B281].
Óleos contraindicados em crianças <3 anos
– Eucalipto (Eucalyptus globulus, E. radiata): 70–90 % 1,8-Cineol [B282]
- Alecrim (Rosmarinus officinalis, Quimiotipo 1,8-Cineol): 40–50 % 1,8-Cineol [B283]
– Árvore do chá (Melaleuca alternifolia): 5–15 % 1,8-Cineol (risco menor, mas precaução necessária) [B284]
– Hortelã-pimenta (Mentha piperita): O mentol pode causar irritações respiratórias semelhantes [B285]
Alternativas seguras em crianças com menos de 3 anos
– Lavanda (Lavandula angustifolia): Seguro desde o nascimento com a diluição adequada [B286]
– Camomila romana (Anthemis nobilis): Segura desde o nascimento [B287]
– Tangerina (Citrus reticulata): Seguro a partir dos 6 meses [B288]
Recomendação Clínica
Evite óleos ricos em 1,8-cineol em crianças com TEA com menos de 3 anos.
Em crianças de 3 a 6 anos, use doses baixas (50 % da dose de adulto) e observe atentamente quaisquer sintomas respiratórios. [B289].
Interações com Antipsicóticos: Risperidona, Aripiprazol
Risperidona e Aripiprazol são os únicos medicamentos aprovados pela FDA para irritabilidade na TAG [B290]. Ambos são metabolizados pelas enzimas do citocromo P450 (CYP2D6, CYP3A4). [B291]. Alguns óleos essenciais e terpenos podem inibir ou induzir enzimas CYP, o que pode levar a alterações nos níveis de medicação. [B292].
Interações potenciais:
Bergamota
Contém Bergapteno (furanocumarina), que inibe o CYP3A4 [B293]. Teoricamente, a bergamota pode aumentar os níveis de risperidona e aripiprazol, podendo potenciar efeitos secundários (sedação, sintomas extrapiramidais). [B294]. No entanto, a exposição inalatória é significativamente menor do que a ingestão oral (efeito do sumo de toranja); a relevância clínica da exposição inalatória à bergamota é incerta [B295].
Recomendação
Use bergamota livre de bergapteno (FCF, livre de furanocumarinas) em pacientes sob Risperidona/Aripiprazol [B296].
Toranja
O óleo essencial de toranja contémfuranocumarinas e inibe o CYP3A4 [B297]. Evitar em pacientes a tomar medicamentos metabolizados por CYP3A4 [B298].
Erva-de-são-joão (Hypericum perforatum)
Embora não seja um óleo essencial típico, o Hipericão é por vezes mencionado em contextos de aromaterapia. O Hipericão é um potente indutor do CYP3A4 e pode reduzir os níveis de Risperidona/Aripiprazol, levando à perda de eficácia. [B299]
Contraindicação: Evite a Erva-de-São-João em pacientes a tomar antipsicóticos [B300].
Lavanda, Camomila, Cedro
Nenhuma interação clinicamente relevante conhecida com CYP [B301]. Seguro em pacientes sob Risperidona/Aripiprazol [B302].
Interações farmacodinâmicas
Óleos essenciais sedativos (lavanda, camomila, cedro) podem ter efeitos sedativos aditivos com antipsicóticos [B303]. Isto pode ser terapeuticamente desejável (por exemplo, para promover o sono), mas requer monitorização para sedação excessiva. [B304].
Recomendação Clínica
Informe os médicos prescritores sobre a aplicação da aromaterapia. Utilize óleos isentos de bergapteno em pacientes sob substratos do CYP3A4. Monitorize potenciais alterações nos efeitos dos medicamentos (sedação, efeitos secundários). [B305].
Requisitos de Qualidade: Análise GC/MS
Como descrito na Secção 5.5, a análise GC/MS é essencial para garantir a pureza, composição e ausência de contaminantes. [B251]. Óleos falsificados ou contaminados podem causar alergias, irritações na pele, sintomas respiratórios e efeitos farmacológicos imprevisíveis. [B306].
Falsificações Frequentes
- Aditivos sintéticos: Linalol sintético ou acetato de linalilo em óleo de “lavanda” [B307]
- Diluente: Propilenoglicol, Éter Monometílico de Dipropilenoglicol (DPM) [B308]
- Óleos mais baratos: Lavandim (Lavandula x intermedia) vendido como alfazema verdadeira (Lavandula angustifolia) [B309]
- Pesticidas: Resíduos de pesticidas, herbicidas em óleos não biológicos [B310]
Recomendação de segurança
Verwenden Sie ausschließlich GC/MS-zertifizierte, 100 % reine, organische ätherische Öle von vertrauenswürdigen Lieferanten. Fordern Sie GC/MS-Zertifikate für jede Charge an [B311].
Discussão
Evidência científica
A evidência para óleos essenciais na TEA é heterogénea e predominantemente de baixa qualidade. A literatura clínica inclui um ensaio controlado aleatório negativo (bergamota para ansiedade aguda) [B200], pequenos estudos piloto com limitações metodológicas (lavanda na conformidade com ABA) [B198], estudos observacionais (massagem com aromaterapia) [B199] e estudos de caso [B312]. Nenhum estudo demonstra eficácia para os sintomas centrais do TEA (comunicação social, comportamentos repetitivos) com qualidade de evidência suficiente. [B313].
Em contraste, a evidência pré-clínica é robusta: múltiplos estudos demonstram que terpenos específicos (Linalol, β-cariofileno, ácidos bosvélicos, 1,8-cineol) atuam em alvos moleculares relevantes para o TEA (recetores GABA-A, recetores CB2, via Nrf2, neuroinflamação) e melhoram comportamentos semelhantes ao TEA em modelos animais. [B152], [B161], [B174], [B183], [B197]. Esta discrepância entre a plausibilidade pré-clínica e a evidência clínica é típica de terapias complementares e reflete a falta de financiamento para a investigação, desafios metodológicos e lacunas de translação. [B314].
Plausibilidade mecanicista
A plausibilidade mecanicista para óleos essenciais na TSP está presente, com base na convergência entre a fisiopatologia da TSP e os mecanismos de ação dos terpenos:
Desequilíbrio GABA/Glutamato E/I
O linalol e o 1,8-cineol modulam recetores GABA-A no local de ligação das benzodiazepinas, o que pode potenciar a neurotransmissão inibitória e normalizar o equilíbrio E/I. [B152], [B183]. Estes mecanismos são análogos aos do bumetanida, que demonstrou melhorias moderadas em estudos clínicos para o TEA. [B52].
Neuroinflamação
β-Cariofileno (agonista CB2) e ácidos boswellicos (ativador Nrf2) reduzem a ativação da micróglia, citocinas pró-inflamatórias e stress oxidativo em modelos pré-clínicos. [B161], [B174]. Visto que a neuroinflamação é um mecanismo fisiopatológico estabelecido na ASD [B77], estes terpenos poderiam ser úteis em pacientes com assinaturas de neuroinflamação (citocinas periféricas elevadas, evidências de PET para ativação de microglia) [B315].
Serotonina/Dopamina
Linalol e Ylang-Ylang modulam sistemas serotoninérgicos e dopaminérgicos em estudos pré-clínicos [B154], [B197]. Estes mecanismos podem melhorar sintomas comórbidos (ansiedade, humor), embora seja improvável que tenham efeito nos sintomas centrais. [B316].
Oxitocina
O linalol aumenta as concentrações intracelulares de cálcio nos neurónios de oxitocina [B155]. A Oxitocina regula o desenvolvimento GABAérgico e melhorou fenótipos semelhantes aos da TEA em estudos pré-clínicos [B50], poderia o linalol modular indiretamente as vias de sinalização oxitonérgicas [B317].
Eixo Intestino-Cérebro
Embora faltem evidências diretas, terpenos anti-inflamatórios (β-cariofileno, ácidos bosvélicos) podem reduzir a inflamação sistêmica e modular indiretamente as vias de sinalização do eixo intestino-cérebro. [B318]. Esta hipótese requer validação experimental [B319].
Limitações
Pequenos estudos
A maioria dos estudos específicos para RDA tiveram tamanhos de amostra inferiores a 20, o que significa um poder insuficiente para a deteção de efeitos moderados. [B320]. Não são possíveis meta-análises devido à heterogeneidade [B321].
Não foram encontrados ensaios clínicos randomizados para distúrbios do núcleo.
Não existem estudos randomizados controlados que investiguem a eficácia de óleos essenciais para os sintomas nucleares da Perturbação do Espectro do Autismo (PEA) (comunicação social, comportamentos repetitivos). [B322]. O único RCT identificado (bergamota) foi negativo para ansiedade aguda [B200].
Heterogeneidade metodológica
Os estudos variam na seleção do óleo, dosagem, via de administração (inalação, massagem, tópica), duração da exposição, medidas de resultado e populações. [B323]. Esta heterogeneidade impede a síntese e a comparabilidade [B324].
Biomarcadores em falta
Nenhum estudo estratifica os pacientes por subtipos neurobiológicos (por exemplo, assinaturas de neuroinflamação, marcadores de desequilíbrio E/I) ou utiliza biomarcadores objetivos como desfechos. [B325]. As abordagens de medicina de precisão poderiam identificar os respondedores [B326].
Viés de publicação
Relatos de casos positivos e pequenos estudos piloto são mais publicados do que estudos negativos, o que pode levar a uma sobrestimação dos efeitos. [B327].
Lacuna de Tradução
Modelos pré-clínicos (ratos VPA, ratos MIA) não replicam a complexidade total da heterogeneidade do TEA humana [B328]. As doses de terpenos em estudos com animais são frequentemente mais elevadas do que as que podem ser alcançadas na exposição humana por inalação. [B329].
Efeitos placebo
A aromaterapia está associada a fortes efeitos de expectativa; o mascaramento é difícil devido aos odores óbvios [B330]. O ensaio RCT da Bergamota utilizou água como placebo, o que significa um cegamento inadequado [B200].
Dados de segurança: Faltam dados de segurança a longo prazo para exposição crónica por inalação em crianças [B331]. A maioria dos dados de segurança provém de aplicação tópica ou oral [B332].
Perspetiva
Prioridades de Investigação:
- Ensaios controlados aleatorizados de alta qualidade: Estudos randomizados, duplo-cegos, controlados por placebo, com poder estatístico suficiente (n > 100), com preparações de óleo padronizadas (certificadas por GC/MS), medidas de resultado objetivas (biomarcadores, actigrafia, eye-tracking) e durações de intervenção mais longas (8–12 semanas) [B333].
- Estratificação por subtipos: Identificação de respondedores com base em subtipos neurobiológicos (marcadores de neuroinflamação, desequilíbrio E/I, perfis microbiómicos) [B334]. Abordagens de Medicina de Precisão podem aumentar os tamanhos do efeito [B335].
- Estudos mecanicistas: Estudos em humanos com resultados de biomarcadores (perfis de citocinas, neuroimagem, EEG, análises do microbioma) antes e depois da intervenção, para validar mecanismos. [B336].
- Farmacocinética: Estudos de Farmacocinética em Humanos para Exposição a Terpenos por Inalação: Concentrações Plasmáticas, Penetração no SNC, Metabolismo, Relações Dose-Resposta [B337].
- Terapias de combinação: Investigação de sinergias entre óleos essenciais e intervenções estabelecidas (terapia comportamental, farmacoterapia, intervenções no microbioma) [B338].
- Segurança a longo prazo: Estudos prospetivos de coorte sobre a segurança a longo prazo da exposição inalatória crónica em crianças [B339].
- Aromaterapia Personalizada: Desenvolvimento de algoritmos para a seleção de óleos com base em perfis de sintomas individuais, preferências e marcadores neurobiológicos [B340].
Implicações clínicas
Com base nas evidências atuais, os óleos essenciais podem ser considerados como parte de uma abordagem terapêutica multimodal para sintomas comórbidos (ansiedade, distúrbios do sono, desregulação sensorial) em Perturbações do Espectro do Autismo (PEA), mas não como monoterapia ou substituto para intervenções centrais baseadas em evidências. [B341]. Os clínicos devem:
- Comunicar expectativas realistas: os óleos essenciais podem aliviar sintomas comórbidos, mas não curar os sintomas centrais [B342]
- Ter em conta a tolerância e preferências individuais [B343]
- Recomendar óleos de alta qualidade certificados por GC/MS [B344]
- Considerações de segurança (Epilepsia, idade, interações medicamentosas) [B345]
- Monitorizar efeitos e ajustar a terapia [B346]
Conclusão
Os óleos essenciais representam uma opção terapêutica adjuvante mecanisticamente plausível, mas clinicamente insuficientemente validada, para a perturbação do espectro do autismo. A heterogeneidade neurobiológica da PSA – caracterizada por um desequilíbrio GABA/glutamato E/I, neuroinflamação, stress oxidativo, alterações do eixo intestino-cérebro e disfunção sináptica – oferece múltiplos alvos terapêuticos que os terpenos específicos podem abordar.
Evidências pré-clínicas demonstram que linalol (modulação GABA-A, regulação serotoninérgica), β-cariofileno (redução da neuroinflamação mediada por CB2), ácidos boswellicos (ativação Nrf2/HO-1), 1,8-cineol (efeitos ansiolíticos GABAérgicos) e ylang-ylang (modulação da serotonina/dopamina) modulam mecanismos patofisiológicos relevantes para a TEA e melhoram comportamentos semelhantes à TEA em modelos animais. Esta plausibilidade mecanicista é apoiada por aplicações tradicionais e dados humanos limitados para ansiedade, sono e humor.
No entanto, a evidência clínica em TEA é de baixa qualidade: um ensaio controlado randomizado (ECR) negativo (bergamota), pequenos estudos piloto com limitações metodológicas (lavanda na adesão à ABA) e estudos observacionais. Nenhum estudo demonstra eficácia para os sintomas centrais do TEA com qualidade de evidência suficiente. Faltam estudos controlados randomizados de alta qualidade com preparações padronizadas, desfechos objetivos e poder suficiente.
Para o Nebulizador de Aromas Organik 3.0, são desenvolvidas recomendações de dosagem específicas para o tamanho da sala (2-10 gotas para 10-60 m², 15-30 minutos, pausas de 30-60 minutos), com protocolos adaptados à hora do dia (ativador de manhã, calmante à noite) e particularidades específicas para Transtorno do Espectro do Autismo (TEA) (introdução graduada, rastreio de preferências, hipersensibilidade sensorial). Os aspetos de segurança incluem contraindicações na epilepsia (óleos com cânfora), crianças com menos de 3 anos (eucalipto), potenciais interações com antipsicóticos (óleos com bergapteno) e a necessidade de óleos puros certificados por GC/MS.
Os óleos essenciais podem ser considerados como parte de uma abordagem terapêutica multimodal para sintomas comórbidos (ansiedade, distúrbios do sono, desregulação sensorial) em TEA, mas não substituem intervenções centrais baseadas em evidências (terapia comportamental, educação estruturada). Pesquisas futuras devem priorizar ensaios clínicos randomizados (ECR) de alta qualidade, estratificação por subtipos neurobiológicos, estudos de biomarcadores mecanicistas e dados de segurança a longo prazo para validar o potencial terapêutico dos óleos essenciais em TEA e desenvolver abordagens de medicina de precisão.
Conclusão comum
Conclusões Abrangentes: TDAH e Autismo
Ambas as condições de neurodesenvolvimento, TDAH e Transtorno do Espectro do Autismo (TEA), partilham semelhanças neurobiológicas fundamentais que tornam plausível uma terapia adjuvante com óleos essenciais para ambas as indicações.
Alvos neurobiológicos comuns:
Recomendação Comum de Aplicação (Nebulizador Organik Aromas 3.0):
Para ambas as indicações, o princípio de nebulização a frio por Venturi, sem água ou calor, é a forma de aplicação ideal: – Sem degradação térmica dos terpenos – Tamanho de partícula preciso para absorção olfativa (< 5 µm) – Óleos puros em GC/MS mantêm a sua integridade molecular
Aviso importante
A terapia adjuvante com óleos essenciais não substitui a terapêutica padrão baseada em evidências (metilfenidato na TDAH, ABA/terapia comportamental no TEA). Representa um complemento que deve ser adaptado individualmente e realizado sob supervisão especializada. As evidências ainda são limitadas para ambas as indicações; são necessários ensaios clínicos randomizados maiores.
Referências TDAH
[A1] Chen et al. (2008). O efeito da aplicação de aromaterapia com canela em crianças com Transtorno de Défice de Atenção e Hiperatividade.https://pmc.ncbi.nlm.nih.gov/articles/PMC8538900/
[A2] Chen et al. O efeito da aplicação de aromaterapia de canela em crianças com transtorno de défice de atenção e hiperatividade.https://pmc.ncbi.nlm.nih.gov/articles/PMC8538900/
[A3] Godfrey (2001). O papel dos óleos essenciais no tratamento e gestão do transtorno de défice de atenção e hiperatividade. International Journal of Aromatherapy.https://doi.org/10.1016/S0962-4562(01 )80035-7
[A4] Godfrey. Óleos essenciais: Tratamento complementar para o transtorno de défice de atenção e hiperatividade (TDAH).https://www.researchgate.net/publication/248871372_The_role_of_essential_oils_in_the_treatment_and_management_of_attention_deficit_hyperactive_disorder
[A5] Godfrey. O PAPEL DOS ÓLEOS ESSENCIAIS NO TRATAMENTO E GESTÃO DO DEFEÇIT DE ATENÇÃO COM HIPERATIVIDADE (TDAH).https://www.researchgate.net/publication/248871372_The_role_of_essential_oils_in_the_treatment_and_management_of_attention_deficit_hyperactive_disorder
[A6] Ding et al. (1994). Farmacocinética e especificidade in vivo do [LLC]dl-treo-metilfenidato para o neurónio dopaminérgico pré-sináptico. Synapse.https://doi.org/10.1002/SYN.890180207
[A7] Volkow et al. (2002). Mecanismo de ação do metilfenidato: perspetivas de estudos de imagem PET. Journal of Attention Disorders.https://doi.org/10.1177/070674370200601S05
[A8] Silva (2024). Aromaterapia no Cuidado de uma Criança Atípica com TDAH e Dermatite Atópica.https://doi.org/10.62435/2965-7253.bjhae.2024.iisinaroma1
[A9] Volkow et al. (1998). Ocupações do Transportador de Dopamina no Cérebro Humano Induzidas por Doses Terapêuticas de Metilfenidato Oral. American Journal of Psychiatry.https://doi.org/10.1176/AJP.155.10.1325
[A10] Jacob et al. (2024). Utilização da aromaterapia na atenção ao estudante.https://doi.org/10.37885/240717094
[A11] Dipasquale et al. (2020). Desvendando os efeitos do metilfenidato nos circuitos funcionais dopaminérgico e noradrenérgico. bioRxiv.https://doi.org/10.1101/2020.03.09.983528
[A12] Volkow et al. (2002). Papel da dopamina nos efeitos terapêuticos e de reforço da metilfenidato em humanos: resultados de estudos de imagem. European Neuropsychopharmacology.https://doi.org/10.1016/S0924-977X(02 )00104-9
[A13] Spencer et al. (2006). Estudo PET a Examinar a Farmacocinética, Deteção e Gostabilidade, e Ocupação do Recetor do Transportador de Dopamina do Metilfenidato Oral de Ação Curta e Longa. American Journal of Psychiatry.https://doi.org/10.1176/APPI.AJP.163.3.387
[A14] Castillo et al. (2018). Óleos essenciais como modificadores do comportamento humano. Tropical and Subtropical Agroecosystems.https://www.revista.ccba.uady.mx/ojs/index.php/TSA/article/view/2583
[A15] Crunelle et al. (2014). Ocupação do transportador de dopamina por metilfenidato e impulsividade em TDAH em adultos. British Journal of Psychiatry.https://doi.org/10.1192/BJP.BP.113.132977
[A16] Ding et al. (1997). Drogas quirais: comparação da farmacocinética do [11C]d-treo e l-treo-metilfenidato no cérebro humano e de babuíno. Psychopharmacology.https://doi.org/10.1007/S002130050267
[A17] Spencer et al. (2009). Um estudo PET a examinar a farmacocinética e a ocupação do transportador de dopamina de duas formulações de longa duração de metilfenidato em adultos. International Journal of Molecular Medicine.https://doi.org/10.3892/IJMM_00000339
[A18] Marcel et al. (2024). Resposta do Sistema Dopaminérgico Estriatal ao Metilfenidato – Um Estudo Intra-sujeito com SPET de I-123-β-CIT em Meninos com Défice de Atenção/Hiperatividade.https://doi.org/10.5283/epub.57629
[A19] Kennedy et al. (2018). Terpenos Voláteis e Função Cerebral: Investigação dos Efeitos Cognitivos e de Humor do Óleo Essencial de Mentha × Piperita L. com Propriedades In Vitro Relevantes para a Função do Sistema Nervoso Central. Nutrients.https://doi.org/10.3390/NU10081029
[A20] Batiha et al. (2023). Uma revisão dos componentes bioativos e propriedades farmacológicas de espécies de Lavandula. Naunyn-schmiedebergs Archives of Pharmacology.https://doi.org/10.1007/s00210-023-02392-x
[A21] Guzmán-Gutiérrez et al. (2015). Linalol e β-pineno exercem a sua atividade antidepressiva através da via monoaminérgica.https://pubmed.ncbi.nlm.nih.gov/25771248/
[A22] Martinez et al. (2020). O estriado ventral suporta os efeitos terapêuticos do Metilfenidato em escolhas impulsivas expressas numa tarefa de desconto temporal. Scientific reports.https://doi.org/10.1038/s41598-020-57595-6
[A23] López et al. (2017). A Explorar Mecanismos Farmacológicos do Óleo Essencial de Alfazema (Lavandula angustifolia) em Alvos do Sistema Nervoso Central. Frontiers in Pharmacology.https://doi.org/10.3389/FPHAR.2017.00280
[A24] Rathnayake (2025). “Neuroaromáticos”: Aromaterapia e a Resposta do Stress Límbico.https://doi.org/10.4038/jssnisd.v3i1.28
[A25] Aster et al. (2021). Responsividade do sistema dopaminérgico estriatal à metilfenidato – um estudo SPECT com I-123-β-CIT intra-sujeito em crianças e adolescentes com Transtorno de Défice de Atenção/Hiperatividade. medRxiv.https://doi.org/10.1101/2021.11.19.21265993
[A26] Cardoso et al. (2025). O Impacto do Óleo Essencial de Lavanda no Sistema Nervoso Humano: Uma Revisão. Deleted Journal.https://doi.org/10.62435/2965-7253.bjhae.2025.bjhae22
[A27] Moss et al. (2003). Aromas de óleos essenciais de alecrim e lavanda afetam diferencialmente a cognição e o humor em adultos saudáveis. International Journal of Neuroscience.https://doi.org/10.1080/00207450390161903
[A28] Sinha et al. (2005). Utilização de medicina complementar e alternativa em crianças com transtorno de hiperatividade e défice de atenção. Journal of Paediatrics and Child Health.https://doi.org/10.1111/J.1440-1754.2005.00530.X
[A29] Springer et al. (2018). TDAH: Ao Longo da Vida e Efeitos da Adolescência até à Idade Adulta.https://dergipark.org.tr/en/pub/pgy/548052.xml
[A30] Colzato et al. (2014). Controlo atencional no piscar atencional é modulado pelo odor. Attention Perception & Psychophysics.https://doi.org/10.3758/S13414-014-0733-0
A31. Kennedy, D. O., Scholey, A., Tildesley, N. T. J., Perry, E. K., & Wesnes, K. A. (2002). Modulação do humor e do desempenho cognitivo após administração aguda de Melissa officinalis (cidreira). Farmacologia, Bioquímica e Comportamento, 72(4), 953–964. https://doi.org/10.1016/S0091-3057(02)00777-3
A32. Müller, S. F., & Klement, S. (2006). Uma combinação de valeriana e erva-cidreira é eficaz no tratamento da inquietação e dissonia em crianças. Fitomedicina, 13(6), 383–387. https://doi.org/10.1016/j.phymed.2006.01.013
A33. Scholey, A., Gibbs, A., Neale, C., et al. (2014). Efeitos anti-stress de alimentos contendo erva-cidreira. Nutrientes, 6(11), 4805–4821. https://doi.org/10.3390/nu6114805
A34. Revisão dos efeitos neuroprotetores de óleos essenciais, incluindo Eucalyptus globulus e Jasminum sambac, na função cognitiva e patologia relacionada com a doença de Alzheimer. (2022). Revisão de Óleos Essenciais Neuroprotetores.
Referências ASD
[B1] Maenner MJ, Shaw KA, Bakian AV, et al. Prevalência e Características do Transtorno do Espectro do Autismo em Crianças com 8 Anos de Idade — Rede de Vigilância de Transtornos do Autismo e do Desenvolvimento, 11 Localidades, Estados Unidos, 2018. MMWR Surveill Summ. 2021;70(11):1-16.https://doi.org/10.15585/mmwr.ss7011a1
[B2] Zeidan J, Fombonne E, Scorah J, et al. Prevalência global de autismo: uma atualização de revisão sistemática. Autism Res. 2022;15(5):778-790.https://doi.org/10.1002/aur.2696
[B3] Lord C, Elsabbagh M, Baird G, Veenstra-Vanderweele J. Transtorno do espectro do autismo. The Lancet. 2018;392(10146):508-520.https://doi.org/10.1016/S0140-6736(18 )31129-2
[B4] Masi A, DeMayo MM, Glozier N, Guastella AJ. Uma Visão Geral do Transtorno do Espectro do Autismo, Heterogeneidade e Opções de Tratamento. Neurosci Bull. 2017;33(2):183-193.https://doi.org/10.1007/s12264-017-0100-y
[B5] American Psychiatric Association. Diagnostic and Statistical Manual of Mental Disorders, Fifth Edition (DSM-5). Arlington, VA: American Psychiatric Publishing; 2013.https://www.psychiatry.org/psychiatrists/practice/dsm
[B6] Marco EJ, Hinkley LB, Hill SS, Nagarajan SS. Processamento sensorial no autismo: uma revisão de achados neurofisiológicos. Pediatr Res. 2011;69(5 Pt 2):48R-54R.https://doi.org/10.1203/PDR.0b013e3182130c54
[B7] Baum SH, Stevenson RA, Wallace MT. Alterações comportamentais, percetivas e neurais na função sensorial e multissensorial no transtorno do espectro do autismo. Prog Neurobiol. 2015;134:140-160.https://doi.org/10.1016/j.pneurobio.2015.09.007
[B8] van Steensel FJ, Bögels SM, Perrin S. Perturbações de ansiedade em crianças e adolescentes com perturbações do espectro do autismo: uma meta-análise. Clin Child Fam Psychol Rev. 2011;14(3):302-317.https://doi.org/10.1007/s10567-011-0097-0
[B9] Souders MC, Mason TB, Valladares O, et al. Comportamentos de sono e qualidade do sono em crianças com transtornos do espectro autista. Sleep. 2009;32(12):1566-1578.https://doi.org/10.1093/sleep/32.12.1566
[B10] McElhanon BO, McCracken C, Karpen S, Sharp WG. Sintomas gastrointestinais no transtorno do espectro do autismo: uma meta-análise. Pediatrics. 2014;133(5):872-883.https://doi.org/10.1542/peds.2013-3995
[B11] Geschwind DH, State MW. Gene hunting in autism spectrum disorder: on the path to precision medicine. Lancet Neurol. 2015;14(11):1109-1120.https://doi.org/10.1016/S1474-4422(15 )00044-7
[B12] De Rubeis S, He X, Goldberg AP, et al. Genes sinápticos, transcricionais e de cromatina perturbados no autismo. Nature. 2014;515(7526):209-215.https://doi.org/10.1038/nature13772
[B13] Sandin S, Lichtenstein P, Kuja-Halkola R, et al. A Hereditariedade do Transtorno do Espectro do Autismo. JAMA. 2017;318(12):1182-1184.https://doi.org/10.1001/jama.2017.12141
[B14] Rubenstein JL, Merzenich MM. Model of autism: increased ratio of excitation/inhibition in key neural systems. Genes Brain Behav. 2003;2(5):255-267.https://doi.org/10.1034/j.1601-183x.2003.00037.x
[B15] Vargas DL, Nascimbene C, Krishnan C, Zimmerman AW, Pardo CA. Ativação neuroglial e neuroinflamação no cérebro de pacientes com autismo. Ann Neurol. 2005;57(1):67-81.https://doi.org/10.1002/ana.20315
[B16] Rossignol DA, Frye RE. Evidência relacionando stress oxidativo, disfunção mitocondrial e inflamação no cérebro de indivíduos com autismo. Front Physiol. 2014;5:150.https://doi.org/10.3389/fphys.2014.00150
[B17] Nelson SB, Valakh V. Excitatory/Inhibitory Balance and Circuit Homeostasis in Autism Spectrum Disorders. Neuron. 2015;87(4):684-698.https://doi.org/10.1016/j.neuron.2015.07.033
[B18] Lee E, Lee J, Kim E. Excitação/Inibição Desequilíbrio em Modelos Animais de Transtornos do Espectro Autista. Biol Psychiatry. 2017;81(10):838-847.https://doi.org/10.1016/j.biopsych.2016.05.011
[B19] Horder J, Lavender T, Mendez MA, et al. Níveis reduzidos de glutamato/glutamina subcorticais em adultos com transtornos do espectro do autismo: um estudo [¹H]MRS. Transl Psychiatry. 2013;3:e279.https://doi.org/10.1038/tp.2013.53
[B20] Gaetz W, Bloy L, Wang DJ, et al. Estimativa de GABA no cérebro de crianças no espectro da autismo: precisão da medição e variação cortical regional. Neuroimage. 2014;86:1-9.https://doi.org/10.1016/j.neuroimage.2013.05.068
[B21] Rojas DC, Singel D, Steinmetz S, Hepburn S, Brown MS. Diminuição da concentração de GABA na região perisilviana esquerda em crianças com autismo e irmãos não afetados. Neuroimage. 2014;86:28-34.https://doi.org/10.1016/j.neuroimage.2013.01.045
[B22] Amaral DG, Schumann CM, Nordahl CW. Neuroanatomy of autism. Trends Neurosci. 2008;31(3):137-145.https://doi.org/10.1016/j.tins.2007.12.005
[B23] Courchesne E, Pierce K. Why the frontal cortex in autism might be talking only to itself: local over-connectivity but long-distance disconnection. Curr Opin Neurobiol. 2005;15(2):225-230.https://doi.org/10.1016/j.conb.2005.03.001
[B24] Baron-Cohen S, Ring HA, Bullmore ET, Wheelwright S, Ashwin C, Williams SC. A Teoria da Amígdala do Autismo. Neurosci Biobehav Rev. 2000;24(3):355-364.https://doi.org/10.1016/s0149-7634(00 )00011-7
[B25] Estes ML, McAllister AK. Maternal immune activation: Implications for neuropsychiatric disorders. Science. 2016;353(6301):772-777.https://doi.org/10.1126/science.aag3194
[B26] Matta SM, Hill-Yardin EL, Crack PJ. A influência da neuroinflamação no Transtorno do Espectro Autista. Brain Behav Immun. 2019;79:75-90.https://doi.org/10.1016/j.bbi.2019.04.037
[B27] Careaga M, Murai T, Bauman MD. Ativação Imunitária Materna e Transtorno do Espectro Autista: Dos Roedores a Primatas Não Humanos e Humanos. Biol Psychiatry. 2017;81(5):391-401.https://doi.org/10.1016/j.biopsych.2016.10.020
[B28] Chauhan A, Chauhan V. Oxidative stress in autism. Pathophysiology. 2006;13(3):171-181.https://doi.org/10.1016/j.pathophys.2006.05.007
[B29] Rose S, Melnyk S, Pavliv O, et al. Evidência de danos oxidativos e inflamação associados a um baixo estado redox de glutationa no cérebro de autistas. Transl Psychiatry. 2012;2:e134.https://doi.org/10.1038/tp.2012.61
[B30] Kang DW, Adams JB, Gregory AC, et al. A Microbiota Transfer Therapy altera o ecossistema intestinal e melhora os sintomas gastrointestinais e de autismo: um estudo de braço aberto. Microbiome. 2017;5(1):10.https://doi.org/10.1186/s40168-016-0225-7
[B31] Vuong HE, Hsiao EY. Emerging Roles for the Gut Microbiome in Autism Spectrum Disorder. Biol Psychiatry. 2017;81(5):411-423.https://doi.org/10.1016/j.biopsych.2016.08.024
[B32] Sharon G, Cruz NJ, Kang DW, et al. Microbiota Intestinal Humana de Pacientes com Transtorno do Espectro Autista Promove Sintomas Comportamentais em Ratos. Cell. 2019;177(6):1600-1618.e17.https://doi.org/10.1016/j.cell.2019.05.004
[B33] Sgritta M, Dooling SW, Buffington SA, et al. Mecanismos subjacentes às alterações no comportamento social mediadas por micróbios em modelos de ratinho de Transtorno do Espectro do Autismo. Neuron. 2019;101(2):246-259.e6.https://doi.org/10.1016/j.neuron.2018.11.018
[B34] Reichow B, Hume K, Barton EE, Boyd BA. Intervenção comportamental intensiva precoce (EIBI) para crianças com transtorno do espectro do autismo (TEA). Cochrane Database Syst Rev. 2018;5(5):CD009260.https://doi.org/10.1002/14651858.CD009260.pub3
[B35] Dawson G, Rogers S, Munson J, et al. Estudo randomizado e controlado de uma intervenção para crianças pequenas com autismo: o Early Start Denver Model. Pediatrics. 2010;125(1):e17-23.https://doi.org/10.1542/peds.2009-0958
[B36] McCracken JT, McGough J, Shah B, et al. Risperidona em crianças com autismo e problemas comportamentais graves. N Engl J Med. 2002;347(5):314-321.https://doi.org/10.1056/NEJMoa013171
[B37] Marcus RN, Owen R, Kamen L, et al. Um estudo controlado com placebo e dose fixa de aripiprazol em crianças e adolescentes com irritabilidade associada a transtorno autista. J Am Acad Child Adolesc Psychiatry. 2009;48(11):1110-1119.https://doi.org/10.1097/CHI.0b013e3181b76658
[B38] Scahill L, McDougle CJ, Aman MG, et al. Efeitos da risperidona e treino parental no funcionamento adaptativo em crianças com transtornos globais do desenvolvimento e problemas comportamentais graves. J Am Acad Child Adolesc Psychiatry. 2012;51(2):136-146.https://doi.org/10.1016/j.jaac.2011.11.010
[B39] Rossignol DA, Frye RE. Melatonina em transtornos do espectro do autismo: uma revisão sistemática e meta-análise. Dev Med Child Neurol. 2011;53(9):783-792.https://doi.org/10.1111/j.1469-8749.2011.03980.x
[B40] Hollander E, Soorya L, Chaplin W, et al. Ensaiou duplo-cego controlado por placebo de fluoxetina para comportamentos repetitivos e gravidade global em distúrbios do espectro autista em adultos. Am J Psychiatry. 2012;169(3):292-299.https://doi.org/10.1176/appi.ajp.2011.10050764
[B41] Spencer D, Marshall J, Post B, et al. Utilização de medicação psicotrópica e polifarmacologia em crianças com transtornos do espectro do autismo. Pediatrics. 2013;132(5):833-840.https://doi.org/10.1542/peds.2012-3774
[B42] Koulivand PH, Khaleghi Ghadiri M, Gorji A. Lavanda e o sistema nervoso. Evid Based Complement Alternat Med. 2013;2013:681304.https://doi.org/10.1155/2013/681304
[B43] Sowndhararajan K, Kim S. Influence of Fragrances on Human Psychophysiological Activity: With Special Reference to Human Electroencephalographic Response. Sci Pharm. 2016;84(4):724-751.https://doi.org/10.3390/scipharm84040724
[B44] Ali B, Al-Wabel NA, Shams S, Ahamad A, Khan SA, Anwar F. Óleos essenciais utilizados em aromaterapia: uma revisão sistémica. Asian Pac J Trop Biomed. 2015;5(8):601-611.https://doi.org/10.1016/j.apjtb.2015.05.007
[B45] Sohal VS, Rubenstein JLR. Excitation-inhibition balance as a framework for investigating mechanisms in neuropsychiatric disorders. Mol Psychiatry. 2019;24(9):1248-1257.https://doi.org/10.1038/s41380-019-0426-0
[B46] Antoine MW, Langberg T, Schnepel P, Feldman DE. Increased Excitation-Inhibition Ratio Stabilizes Synapse and Circuit Excitability in Four Autism Mouse Models. Neuron. 2019;101(4):648-661.e4.https://doi.org/10.1016/j.neuron.2018.12.026
[B47] Fatemi SH, Halt AR, Stary JM, Kanodia R, Schulz SC, Realmuto GR. As proteínas descarboxilase do ácido glutâmico de 65 e 67 kDa estão reduzidas nos córtices parietal e cerebelar autistas. Biol Psychiatry. 2002;52(8):805-810.https://doi.org/10.1016/s0006-3223(02 )01430-0
[B48] Yip J, Soghomonian JJ, Blatt GJ. Níveis reduzidos de mRNA de GAD67 em células de Purkinje cerebelosas em autismo: implicações fisiopatológicas. Acta Neuropathol. 2007;113(5):559-568.https://doi.org/10.1007/s00401-006-0176-3
[B49] Ben-Ari Y. Excitatory actions of GABA during development: the nature of the nurture. Nat Rev Neurosci. 2002;3(9):728-739.https://doi.org/10.1038/nrn920
[B50] Tyzio R, Nardou R, Ferrari DC, et al. A inibição mediada por oxitocina via GABA durante o parto atenua a patogénese do autismo em descendentes de roedores. Science. 2014;343(6171):675-679.https://doi.org/10.1126/science.1247190
[B51] Lemonnier E, Degrez C, Phelep M, et al. Um ensaio controlado randomizado de bumetanida no tratamento do autismo em crianças. Transl Psychiatry. 2012;2:e202.https://doi.org/10.1038/tp.2012.124
[B52] Lemonnier E, Villeneuve N, Sonie S, et al. Efeitos da bumetanida na função neurocomportamental em crianças e adolescentes com transtornos do espectro do autismo. Transl Psychiatry. 2017;7(3):e1056.https://doi.org/10.1038/tp.2017.10
[B53] Carlson GC. Disfunção do recetor de glutamato e alvos de fármacos em modelos de perturbações do espetro do autismo. Pharmacol Biochem Behav. 2012;100(4):850-854.https://doi.org/10.1016/j.pbb.2011.02.003
[B54] Uzunova G, Pallanti S, Hollander E. Desequilíbrio excitatório/inibitório em transtornos do espectro autista: Implicações para intervenções e terapêuticas. World J Biol Psychiatry. 2016;17(3):174-186.https://doi.org/10.3109/15622975.2015.1085597
[B55] Yoo HJ, Cho IH, Park M, Yang SY, Kim SA. Family based association of GRIN2A and GRIN2B with Korean autism spectrum disorders. Neurosci Lett. 2012;512(2):89-93.https://doi.org/10.1016/j.neulet.2012.01.061
[B56] Silverman JL, Tolu SS, Barkan CL, Crawley JN. O comportamento repetitivo de auto-higienização no modelo de rato BTBR de autismo é bloqueado pelo antagonista mGluR5 MPEP. Neuropsychopharmacology. 2010;35(4):976-989.https://doi.org/10.1038/npp.2009.201
[B57] Muller CL, Anacker AMJ, Veenstra-VanderWeele J. O sistema serotoninérgico no transtorno do espectro autista: Do biomarcador aos modelos animais. Neuroscience. 2016;321:24-41.https://doi.org/10.1016/j.neuroscience.2015.11.010
[B58] Pavăl D. A Hipótese de Dopamina do Transtorno do Espectro Autista. Dev Neurosci. 2017;39(5):355-360.https://doi.org/10.1159/000478725
[B59] Schain RJ, Freedman DX. Studies on 5-hydroxyindole metabolism in autistic and other mentally retarded children. J Pediatr. 1961;58:315-320.https://doi.org/10.1016/s0022-3476(61 )80261-8
[B60] Cook EH Jr, Leventhal BL. O sistema serotoninérgico no autismo. Curr Opin Pediatr. 1996;8(4):348-354.https://doi.org/10.1097/00008480-199608000-00008
[B61] Chugani DC, Muzik O, Behen M, et al. Alterações no desenvolvimento da capacidade de síntese de serotonina no cérebro em crianças autistas e não autistas. Ann Neurol. 1999;45(3):287-295.https://doi.org/10.1002/1531-8249(199903 )45:33.0.co;2-9
[B62] Devlin B, Cook EH Jr, Coon H, et al. Autismo e o transportador de serotonina: o longo e o curto disto. Mol Psychiatry. 2005;10(12):1110-1116.https://doi.org/10.1038/sj.mp.4001724
[B63] Whitaker-Azmitia PM. Consequências comportamentais e celulares do aumento da atividade serotoninérgica durante o desenvolvimento cerebral: um papel no autismo? Int J Dev Neurosci. 2005;23(1):75-83.https://doi.org/10.1016/j.ijdevneu.2004.07.022
King BH, Hollander E, Sikich L, et al. Falta de eficácia do citalopram em crianças com transtornos do espectro do autismo e níveis elevados de comportamentos repetitivos: citalopram ineficaz em crianças com autismo. Arch Gen Psychiatry. 2009;66(6):583-590.https://doi.org/10.1001/archgenpsychiatry.2009.30
[B65] Dichter GS, Damiano CA, Allen JA. Disfunção do circuito de recompensa em distúrbios psiquiátricos e do neurodesenvolvimento e síndromes genéticas: modelos animais e achados clínicos. J Neurodev Disord. 2012;4(1):19.https://doi.org/10.1186/1866-1955-4-19
[B66] Kohls G, Schulte-Rüther M, Nehrkorn B, et al. Disfunção do sistema de recompensa em perturbações do espectro do autismo. Soc Cogn Affect Neurosci. 2013;8(5):565-572.https://doi.org/10.1093/scan/nss033
[B67] Delmonte S, Balsters JH, McGrath J, et al. Processamento de recompensa social e monetária em transtornos do espectro do autismo. Mol Autism. 2012;3(1):7.https://doi.org/10.1186/2040-2392-3-7
[B68] Nakamura K, Sekine Y, Ouchi Y, et al. Ligação dos transportadores de serotonina e dopamina no cérebro de adultos com autismo de alto funcionamento. Arch Gen Psychiatry. 2010;67(1):59-68.https://doi.org/10.1001/archgenpsychiatry.2009.137
[B69] Staal WG. Autismo, DRD3 e comportamento repetitivo e estereotipado, uma visão geral do conhecimento atual. Eur Neuropsychopharmacol. 2015;25(9):1421-1426.https://doi.org/10.1016/j.euroneuro.2014.08.011
[B70] Gunaydin LA, Grosenick L, Finkelstein JC, et al. Dinâmicas de projeção neuronal natural subjacentes ao comportamento social. Cell. 2014;157(7):1535-1551.https://doi.org/10.1016/j.cell.2014.05.017
[B71] Insel TR. O desafio da tradução em neurociência social: uma revisão sobre a ocitocina, a vasopressina e o comportamento afiliativo. Neuron. 2010;65(6):768-779.https://doi.org/10.1016/j.neuron.2010.03.005
[B72] Modahl C, Green L, Fein D, et al. Níveis de oxitocina plasmática em crianças autistas. Biol Psychiatry. 1998;43(4):270-277.https://doi.org/10.1016/s0006-3223(97 )00439-3
[B73] Gregory SG, Connelly JJ, Towers AJ, et al. Evidências genómicas e epigenéticas de deficiência do recetor de oxitocina no autismo. BMC Med. 2009;7:62.https://doi.org/10.1186/1741-7015-7-62
[B74] Guastella AJ, Einfeld SL, Gray KM, et al. Oxitocina intranasal melhora o reconhecimento de emoções em jovens com transtornos do espectro autista. Biol Psychiatry. 2010;67(7):692-694.https://doi.org/10.1016/j.biopsych.2009.09.020
[B75] Parker KJ, Oztan O, Libove RA, et al. Tratamento intranasal com ocitocina para défices sociais e biomarcadores de resposta em crianças com autismo. Proc Natl Acad Sci U S A. 2017;114(30):8119-8124.https://doi.org/10.1073/pnas.1705521114
[B76] Peñagarikano O, Lázaro MT, Lu XH, et al. A oxitocina exógena e evocada restaura o comportamento social no modelo murino Cntnap2 de autismo. Sci Transl Med. 2015;7(271):271ra8.https://doi.org/10.1126/scitranslmed.3010257
[B77] Pardo CA, Vargas DL, Zimmerman AW. Imunidade, neuroglia e neuroinflamação no autismo. Int Rev Psychiatry. 2005;17(6):485-495.https://doi.org/10.1080/02646830500381930
[B78] Edmonson C, Ziats MN, Rennert OM. Altered glial marker expression in autistic post-mortem prefrontal cortex and cerebellum. Mol Autism. 2014;5:3.https://doi.org/10.1186/2040-2392-5-3
[B79] Salter MW, Stevens B. Microglia emerge as central players in brain disease. Nat Med. 2017;23(9):1018-1027.https://doi.org/10.1038/nm.4397
[B80] Morgan JT, Chana G, Pardo CA, et al. Ativação microglial e aumento da densidade microglial observados no córtex pré-frontal dorsolateral em autismo. Biol Psychiatry. 2010;68(4):368-376.https://doi.org/10.1016/j.biopsych.2010.05.024
[B81] Suzuki K, Sugihara G, Ouchi Y, et al. Ativação microglial em jovens adultos com transtorno do espectro do autismo. JAMA Psychiatry. 2013;70(1):49-58.https://doi.org/10.1001/jamapsychiatry.2013.272
[B82] Zürcher NR, Loggia ML, Lawson R, et al. Aumento da ativação glial in vivo em doentes com esclerose lateral amiotrófica: avaliada com [(11)C]-PBR28. Neuroimage Clin. 2015;7:409-414.https://doi.org/10.1016/j.nicl.2015.01.009
[B83] Schafer DP, Lehrman EK, Kautzman AG, et al. Microglia sculpt postnatal neural circuits in an activity and complement-dependent manner. Neuron. 2012;74(4):691-705.https://doi.org/10.1016/j.neuron.2012.03.026
[B84] Ashwood P, Krakowiak P, Hertz-Picciotto I, Hansen R, Pessah I, Van de Water J. Níveis elevados de citocinas plasmáticas em perturbações do espectro do autismo fornecem evidências de disfunção imunitária e estão associados a um desfecho comportamental prejudicado. Brain Behav Immun. 2011;25(1):40-45.https://doi.org/10.1016/j.bbi.2010.08.003
[B85] Li X, Chauhan A, Sheikh AM, et al. Resposta imunitária elevada no cérebro de doentes autistas. J Neuroimmunol. 2009;207(1-2):111-116.https://doi.org/10.1016/j.jneuroim.2008.12.002
[B86] Smith SE, Li J, Garbett K, Mirnics K, Patterson PH. A ativação imunitária materna altera o desenvolvimento cerebral fetal através da interleucina-6. J Neurosci. 2007;27(40):10695-10702.https://doi.org/10.1523/JNEUROSCI.2178-07.2007
[B87] Choi GB, Yim YS, Wong H, et al. A via materna da interleucina-17a em ratinhos promove fenótipos semelhantes ao autismo na descendência. Science. 2016;351(6276):933-939.https://doi.org/10.1126/science.aad0314
[B88] Stellwagen D, Malenka RC. Synaptic scaling mediated by glial TNF-alpha. Nature. 2006;440(7087):1054-1059.https://doi.org/10.1038/nature04671
[B89] Wei H, Chadman KK, McCloskey DP, et al. A elevação de IL-6 no cérebro causa desequilíbrios nos circuitos neuronais e media comportamentos semelhantes ao autismo. Biochim Biophys Acta. 2012;1822(6):831-842.https://doi.org/10.1016/j.bbadis.2012.01.011
[B90] Verkhratsky A, Nedergaard M. Fisiologia da Astroglia. Physiol Rev. 2018;98(1):239-389.https://doi.org/10.1152/physrev.00042.2016
[B91] Laurence JA, Fatemi SH. Glial fibrillary acidic protein is elevated in superior frontal, parietal and cerebellar cortices of autistic subjects. Cerebellum. 2005;4(3):206-210.https://doi.org/10.1080/14734220500208846
[B92] Rothstein JD, Dykes-Hoberg M, Pardo CA, et al. A eliminação de transportadores de glutamato revela um papel importante para o transporte astroglial na excitotoxicidade e na depuração do glutamato. Neuron. 1996;16(3):675-686.https://doi.org/10.1016/s0896-6273(00 )80086-0
[B93] Sies H, Jones DP. Espécies reativas de oxigénio (ROS) como agentes de sinalização fisiológica pleiotrópicos. Nat Rev Mol Cell Biol. 2020;21(7):363-383.https://doi.org/10.1038/s41580-020-0230-3
[B94] Frustaci A, Neri M, Cesario A, et al. Marcadores biológicos relacionados ao stress oxidativo no autismo: revisão sistemática e meta-análises. Free Radic Biol Med. 2012;52(10):2128-2141.https://doi.org/10.1016/j.freeradbiomed.2012.03.011
[B95] Bjørklund G, Meguid NA, El-Bana MA, et al. Stress Oxidativo no Transtorno do Espectro do Autismo. Mol Neurobiol. 2020;57(5):2314-2332.https://doi.org/10.1007/s12035-019-01742-2
[B96] James SJ, Cutler P, Melnyk S, et al. Biomarcadores metabólicos de stress oxidativo aumentado e capacidade de metilação prejudicada em crianças com autismo. Am J Clin Nutr. 2004;80(6):1611-1617.https://doi.org/10.1093/ajcn/80.6.1611
[B97] Rose S, Melnyk S, Pavliv O, et al. Evidence of oxidative damage and inflammation associated with low glutathione redox status in the autism brain. Transl Psychiatry. 2012;2:e134.https://doi.org/10.1038/tp.2012.61
[B98] Bowers K, Li Q, Bressler J, et al. Variação genética na via da glutationa e risco de perturbações do espectro do autismo. J Neurodev Disord. 2011;3(2):132-143.https://doi.org/10.1007/s11689-011-9077-4
[B99] Rossignol DA, Frye RE. Disfunção mitocondrial em transtornos do espectro do autismo: uma revisão sistemática e meta-análise. Mol Psychiatry. 2012;17(3):290-314.https://doi.org/10.1038/mp.2010.136
[B100] Giulivi C, Zhang YF, Omanska-Klusek A, et al. Disfunção mitocondrial no autismo. JAMA. 2010;304(21):2389-2396.https://doi.org/10.1001/jama.2010.1706
[B101] Duchen MR. Mitochondria and calcium: from cell signalling to cell death. J Physiol. 2000;529 Pt 1(Pt 1):57-68.https://doi.org/10.1111/j.1469-7793.2000.00057.x
[B102] Bambini-Junior V, Rodrigues L, Behr GA, et al. Modelo animal de autismo induzido por exposição pré-natal a valproato: alterações comportamentais e parâmetros hepáticos. Brain Res. 2011;1408:8-16.https://doi.org/10.1016/j.brainres.2011.06.015
[B103] Ma Q. O papel do nrf2 no stress oxidativo e toxicidade. Annu Rev Pharmacol Toxicol. 2013;53:401-426.https://doi.org/10.1146/annurev-pharmtox-011112-140320
[B104] Singh K, Connors SL, Macklin EA, et al. Tratamento com sulforafano em distúrbios do espetro do autismo (ASD). Proc Natl Acad Sci U S A. 2014;111(43):15550-15555.https://doi.org/10.1073/pnas.1416940111
[B105] Bent S, Lawton B, Warren T, et al. Identificação de metabolitos urinários que se correlacionam com melhorias clínicas em crianças com autismo tratadas com sulforafano de brócolos. Mol Autism. 2018;9:35.https://doi.org/10.1186/s13229-018-0218-4
[B106] Cryan JF, O’Riordan KJ, Cowan CSM, et al. O Eixo Microbiota-Intestino-Cérebro. Physiol Rev. 2019;99(4):1877-2013.https://doi.org/10.1152/physrev.00018.2018
[B107] Chaidez V, Hansen RL, Hertz-Picciotto I. Problemas gastrointestinais em crianças com autismo, atrasos no desenvolvimento ou desenvolvimento típico. J Autism Dev Disord. 2014;44(5):1117-1127.https://doi.org/10.1007/s10803-013-1973-x
[B108] Adams JB, Johansen LJ, Powell LD, Quig D, Rubin RA. Flora gastrointestinal e estado gastrointestinal em crianças com autismo – comparações com crianças típicas e correlação com a gravidade do autismo. BMC Gastroenterol. 2011;11:22.https://doi.org/10.1186/1471-230X-11-22
Xu M, Xu X, Li J, Li F. Associação entre a Microbiota Intestinal e o Transtorno do Espectro do Autismo: Uma Revisão Sistemática e Meta-análise. Front Psychiatry. 2019;10:473.https://doi.org/10.3389/fpsyt.2019.00473
[B110] Liu F, Li J, Wu F, et al. Composição e função alteradas da microbiota intestinal em transtornos do espectro do autismo: uma revisão sistemática. Transl Psychiatry. 2019;9(1):43.https://doi.org/10.1038/s41398-019-0389-6
[B111] Kang DW, Park JG, Ilhan ZE, et al. Redução da incidência de Prevotella e outros fermentadores na microflora intestinal de crianças autistas. PLoS One. 2013;8(7):e68322.https://doi.org/10.1371/journal.pone.0068322
[B112] Stilling RM, van de Wouw M, Clarke G, Stanton C, Dinan TG, Cryan JF. A neurofarmacologia do butirato: O pão com manteiga do eixo microbiota-intestino-cérebro? Neurochem Int. 2016;99:110-132.https://doi.org/10.1016/j.neuint.2016.06.011
[B113] MacFabe DF, Cain DP, Rodriguez-Capote K, et al. Efeitos neurobiológicos do ácido propiónico intraventricular em ratos: possível papel dos ácidos gordos de cadeia curta na patogénese e características dos transtornos do espectro autista. Behav Brain Res. 2007;176(1):149-169.https://doi.org/10.1016/j.bbr.2006.07.025
[B114] Hsiao EY, McBride SW, Hsien S, et al. A microbiota modula anomalias comportamentais e fisiológicas associadas a distúrbios do neurodesenvolvimento. Cell. 2013;155(7):1451-1463.https://doi.org/10.1016/j.cell.2013.11.024
[B115] Bonaz B, Bazin T, Pellissier S. O Nervo Vago na Interface do Eixo Microbiota-Intestino-Cérebro. Front Neurosci. 2018;12:49.https://doi.org/10.3389/fnins.2018.00049
[B116] Liu S, Hagiwara SI, Bhargava A. Adversidade precoce, epigenética e hipersensibilidade visceral. Neurogastroenterol Motil. 2017;29(9).https://doi.org/10.1111/nmo.13170
[B117] Zoghbi HY, Bear MF. Sinaptopatia em distúrbios do neurodesenvolvimento associados ao autismo e deficiências intelectuais. Cold Spring Harb Perspect Biol. 2012;4(3):a009886.https://doi.org/10.1101/cshperspect.a009886
[B118] Bourgeron T. Da arquitetura genética à plasticidade sináptica no transtorno do espectro autista. Nat Rev Neurosci. 2015;16(9):551-563.https://doi.org/10.1038/nrn3992
[B119] Südhof TC. Neuroliginas e neurexinas ligam a função sináptica a doenças cognitivas. Nature. 2008;455(7215):903-911.https://doi.org/10.1038/nature07456
[B120] Jamain S, Quach H, Betancur C, et al. Mutações nos genes ligados ao cromossoma X que codificam as neuroliginas NLGN3 e NLGN4 estão associadas ao autismo. Nat Genet. 2003;34(1):27-29.https://doi.org/10.1038/ng1136
[B121] Tabuchi K, Blundell J, Etherton MR, et al. Uma mutação na neuroligina-3 implicada no autismo aumenta a transmissão sináptica inibitória em ratos. Science. 2007;318(5847):71-76.https://doi.org/10.1126/science.1146221
[B122] Jamain S, Radyushkin K, Hammerschmidt K, et al. Reduced social interaction and ultrasonic communication in a mouse model of monogenic heritable autism. Proc Natl Acad Sci U S A. 2008;105(5):1710-1715.https://doi.org/10.1073/pnas.0711555105
[B123] Grabrucker AM, Schmeisser MJ, Schoen M, Boeckers TM. Postsynaptic ProSAP/Shank scaffolds in the cross-hair of synaptopathies. Trends Cell Biol. 2011;21(10):594-603.https://doi.org/10.1016/j.tcb.2011.07.003
[B124] Phelan K, McDermid HE. A Síndrome de Deleção 22q13.3 (Síndrome de Phelan-McDermid). Mol Syndromol. 2012;2(3-5):186-201.https://doi.org/10.1159/000334260
[B125] Peça J, Feliciano C, Ting JT, et al. Ratos com mutação Shank3 exibem comportamentos semelhantes aos autistas e disfunção estriatal. Nature. 2011;472(7344):437-442.https://doi.org/10.1038/nature09965
[B126] Won H, Lee HR, Gee HY, et al. Comportamento social semelhante ao autismo em ratos com mutação Shank2 melhorou com a restauração da função do recetor NMDA. Nature. 2012;486(7402):261-265.https://doi.org/10.1038/nature11208
[B127] Baudouin SJ, Gaudias J, Gerharz S, et al. Fisiopatologia sináptica partilhada em modelos de roedores sindrómicos e não sindrómicos de autismo. Science. 2012;338(6103):128-132.https://doi.org/10.1126/science.1224159
[B128] Huber KM, Gallagher SM, Warren ST, Bear MF. Altered synaptic plasticity in a mouse model of fragile X mental retardation. Proc Natl Acad Sci U S A. 2002;99(11):7746-7750.https://doi.org/10.1073/pnas.122205699
[B129] Ecker C, Bookheimer SY, Murphy DG. Neuroimaging in autism spectrum disorder: brain structure and function across the lifespan. Lancet Neurol. 2015;14(11):1121-1134.https://doi.org/10.1016/S1474-4422(15 )00050-2
[B130] Hazlett HC, Gu H, Munsell BC, et al. Desenvolvimento cerebral precoce em lactentes com alto risco de transtorno do espectro autista. Nature. 2017;542(7641):348-351.https://doi.org/10.1038/nature21369
[B131] Miller EK, Cohen JD. Uma teoria integrativa da função do córtex pré-frontal. Annu Rev Neurosci. 2001;24:167-202.https://doi.org/10.1146/annurev.neuro.24.1.167
[B132] Castelli F, Frith C, Happé F, Frith U. Autismo, síndrome de Asperger e mecanismos cerebrais para a atribuição de estados mentais a formas animadas. Brain. 2002;125(Pt 8):1839-1849.https://doi.org/10.1093/brain/awf189
[B133] Just MA, Cherkassky VL, Keller TA, Kana RK, Minshew NJ. Subligação cortical funcional e anatómica no autismo: evidências de um estudo de FMRI de uma tarefa de função executiva e morfometria do corpo caloso. Cereb Cortex. 2007;17(4):951-961.https://doi.org/10.1093/cercor/bhl006
[B134] Casanova MF, Buxhoeveden DP, Switala AE, Roy E. Patologia minicolunar no autismo. Neurology. 2002;58(3):428-432.https://doi.org/10.1212/wnl.58.3.428
[B135] Adolphs R. The social brain: neural basis of social knowledge. Annu Rev Psychol. 2009;60:693-716.https://doi.org/10.1146/annurev.psych.60.110707.163514
[B136] Nordahl CW, Scholz R, Yang X, et al. Taxa aumentada de crescimento da amígdala em crianças entre 2 e 4 anos com transtornos do espectro do autismo: um estudo longitudinal. Arch Gen Psychiatry. 2012;69(1):53-61.https://doi.org/10.1001/archgenpsychiatry.2011.145
[B137] Kleinhans NM, Richards T, Sterling L, et al. Ligação funcional anormal em perturbações do espectro do autismo durante o processamento de rostos. Brain. 2008;131(Pt 4):1000-1012.https://doi.org/10.1093/brain/awm334
[B138] Monk CS, Weng SJ, Wiggins JL, et al. Circuito neural do processamento de faces emocionais em transtornos do espectro do autismo. J Psychiatry Neurosci. 2010;35(2):105-114.https://doi.org/10.1503/jpn.090085
[B139] Schmahmann JD. O cerebelo e a cognição. Neurosci Lett. 2019;688:62-75.https://doi.org/10.1016/j.neulet.2018.07.005
[B140] Fatemi SH, Aldinger KA, Ashwood P, et al. Artigo de consenso: papel patológico do cerebelo no autismo. Cerebellum. 2012;11(3):777-807.https://doi.org/10.1007/s12311-012-0355-9
[B141] Courchesne E, Yeung-Courchesne R, Press GA, Hesselink JR, Jernigan TL. Hipoplasia dos lóbulos VI e VII do vérmis cerebelar no autismo. N Engl J Med. 1988;318(21):1349-1354.https://doi.org/10.1056/NEJM198805263182102
[B142] Wang SS, Kloth AD, Badura A. O cerebelo, os períodos sensíveis e o autismo. Neuron. 2014;83(3):518-532.https://doi.org/10.1016/j.neuron.2014.07.016
[B143] Squire LR, Stark CE, Clark RE. O lobo temporal medial. Annu Rev Neurosci. 2004;27:279-306.https://doi.org/10.1146/annurev.neuro.27.070203.144130
[B144] Schumann CM, Hamstra J, Goodlin-Jones BL, et al. A amígdala está aumentada em crianças, mas não em adolescentes com autismo; o hipocampo está aumentado em todas as idades. J Neurosci. 2004;24(28):6392-6401.https://doi.org/10.1523/JNEUROSCI.1297-04.2004
[B145] Gaigg SB, Bowler DM. Free recall and forgetting of emotionally arousing words in autism spectrum disorder. Neuropsychologia. 2008;46(9):2336-2343.https://doi.org/10.1016/j.neuropsychologia.2008.03.008
[B146] Graybiel AM. Os gânglios da base. Curr Biol. 2000;10(14):R509-R511.https://doi.org/10.1016/s0960-9822(00 )00593-5
[B147] Langen M, Durston S, Staal WG, Palmen SJ, van Engeland H. O núcleo caudado está aumentado em indivíduos com autismo de alta funcionalidade e não medicados. Biol Psychiatry. 2007;62(3):262-266.https://doi.org/10.1016/j.biopsych.2006.09.040
[B148] Scott-Van Zeeland AA, Dapretto M, Ghahremani DG, Poldrack RA, Bookheimer SY. Processamento de recompensa no autismo. Autism Res. 2010;3(2):53-67.https://doi.org/10.1002/aur.122
[B149] Gershenzon J, Dudareva N. A função dos produtos naturais de terpenos no mundo natural. Nat Chem Biol. 2007;3(7):408-414.https://doi.org/10.1038/nchembio.2007.5
[B150] Russo EB. Taming THC: potencial sinergia da canábis e efeitos de entourage de fitocanabinóides-terpenóides. Br J Pharmacol. 2011;163(7):1344-1364.https://doi.org/10.1111/j.1476-5381.2011.01238.x
[B151] Aprotosoaie AC, Hăncianu M, Costache II, Miron A. Linalol: uma revisão sobre uma molécula de odor chave com valiosas propriedades biológicas. Flavour Fragr J. 2014;29(4):193-219.https://doi.org/10.1002/ffj.3197
[B152] Harada H, Kashiwadani H, Kanmura Y, Kuwaki T. Efeitos ansiolíticos induzidos pelo odor de linalool em ratinhos. Front Behav Neurosci. 2018;12:241.https://doi.org/10.3389/fnbeh.2018.00241
[B153] Elisabetsky E, Brum LF, Souza DO. Propriedades anticonvulsivantes do linalol em modelos de convulsão relacionados ao glutamato. Phytomedicine. 1999;6(2):107-113.https://doi.org/10.1016/S0944-7113(99 )80044-0
[B154] Linck VM, da Silva AL, Figueiró M, et al. Efeitos do Linalol inalado na ansiedade, interação social e comportamento agressivo em ratinhos. Phytomedicine. 2010;17(8-9):679-683.https://doi.org/10.1016/j.phymed.2009.10.002
[B155] Takahashi M, Satou T, Ohashi M, Hayashi S, Sadamoto K, Koike K. Comparação entre espécies da composição química e dos efeitos ansiolíticos de óleos de lavanda após inalação. Nat Prod Commun. 2011;6(11):1769-1774.https://journals.sagepub.com/doi/10.1177/1934578X1100601148
[B156] Peana AT, D’Aquila PS, Panin F, Serra G, Pippia P, Moretti MD. Atividade anti-inflamatória dos constituintes linalol e acetato de linalilo de óleos essenciais. Phytomedicine. 2002;9(8):721-726.https://doi.org/10.1078/094471102321621322
[B157] Sabogal-Guáqueta AM, Posada-Duque R, Cortes NC, Arias-Londoño JD, Cardona-Gómez GP. Alterações nos perfis de fosfolípidos hipocampais e periféricos estão associadas a características de neurodegeneração num modelo de isquemia cerebral global a longo prazo: Atenuação pelo Linalol. Neuropharmacology. 2018;135:555-571.https://doi.org/10.1016/j.neuropharm.2018.04.015
[B158] Jäger W, Buchbauer G, Jirovetz L, Fritzer M. Absorção percutânea do óleo de lavanda a partir de um óleo de massagem. J Soc Cosmet Chem. 1992;43:49-54.https://www.researchgate.net/publication/232711524_Percutaneous_absorption_of_lavender_oil_from_a_massage_oil
[B159] Buchbauer G. Atividades biológicas dos óleos essenciais. In: Baser KHC, Buchbauer G, eds. Handbook of Essential Oils: Science, Technology, and Applications. 2ª ed. CRC Press; 2015:235-280.https://www.routledge.com/Handbook-of-Essential-Oils-Science-Technology-and-Applications/Baser-Buchbauer/p/book/9781032046419
[B160] Gertsch J, Leonti M, Raduner S, et al. Beta-cariofileno é um canabinoide alimentar. Proc Natl Acad Sci U S A. 2008;105(26):9099-9104.https://doi.org/10.1073/pnas.0803601105
[B161] Bahi A, Al Mansouri S, Al Memari E, Al Ameri M, Nurulain SM, Ojha S. O β-Cariofileno, um agonista do recetor CB2, produz múltiplas alterações comportamentais relevantes para ansiedade e depressão em ratinhos. Physiol Behav. 2014;135:119-124.https://doi.org/10.1016/j.physbeh.2014.06.003
[B162] Atwood BK, Mackie K. CB2: um recetor canabinóide com uma crise de identidade. Br J Pharmacol. 2010;160(3):467-479.https://doi.org/10.1111/j.1476-5381.2010.00729.x
[B163] Klauke AL, Racz I, Pradier B, et al. O fitocanabinoide beta-cariofileno, seletivo para o recetor CB₂ de canabinoides, exerce efeitos analgésicos em modelos de ratinho de dor inflamatória e neuropática. Eur Neuropsychopharmacol. 2014;24(4):608-620.https://doi.org/10.1016/j.euroneuro.2013.10.008
[B164] Cheng Y, Dong Z, Liu S. O β-cariofileno melhora o fenótipo semelhante ao da doença de Alzheimer em ratos APP/PS1 através da ativação do recetor CB2 e da via PPARγ. Pharmacology. 2014;94(1-2):1-12.https://doi.org/10.1159/000362689
[B165] Askari VR, Shafiee-Nick R. Efeitos neuroprotetores promissores do β-cariofileno contra a toxicidade da oligodendroglia induzida por LPS: um estudo mecanístico. Biochem Pharmacol. 2019;159:154-171.https://doi.org/10.1016/j.bcp.2018.12.001
Fontes LBA, Dias D, Aarestrup BJ, et al. O β-cariofileno abranda o desenvolvimento de encefalomielite autoimune experimental em ratos C57BL/6. Biomed Pharmacother. 2017;91:257-264.https://doi.org/10.1016/j.biopha.2017.04.092
[B167] Alberti TB, Barbosa WL, Vieira JL, Raposo NR, Dutra RC. (-)-β-Cariofileno, um fitocanabinóide seletivo para o recetor CB2, suprime a paralisia motora e a neuroinflamação num modelo murino de esclerose múltipla. Int J Mol Sci. 2017;18(4):691.https://doi.org/10.3390/ijms18040691
[B168] Galdino PM, Nascimento MV, Florentino IF, et al. O efeito ansiolítico de um óleo essencial derivado de folhas de Spiranthera odoratissima A. St. Hil. e do seu componente principal, o β-cariofileno, em ratinhos machos. Prog Neuropsychopharmacol Biol Psychiatry. 2012;38(2):276-284.https://doi.org/10.1016/j.pnpbp.2012.04.012
[B169] Horváth B, Mukhopadhyay P, Kechrid M, et al. O β-cariofileno melhora a nefrotoxicidade induzida por cisplatina de forma dependente do recetor 2 de canabinóides. Free Radic Biol Med. 2012;52(8):1325-1333.https://doi.org/10.1016/j.freeradbiomed.2012.01.014
[B170] Fidyt K, Fiedorowicz A, Strządała L, Szumny A. β-cariofileno e óxido de β-cariofileno - compostos naturais com propriedades anticancerígenas e analgésicas. Cancer Med. 2016;5(10):3007-3017.https://doi.org/10.1002/cam4.816
[B171] Sharma C, Al Kaabi JM, Nurulain SM, Goyal SN, Kamal MA, Ojha S. Polypharmacological Properties and Therapeutic Potential of β-Caryophyllene: A Dietary Phytocannabinoid of Pharmaceutical Promise. Curr Pharm Des. 2016;22(21):3237-3264.https://doi.org/10.2174/1381612822666160311115226
[B172] Ammon HP. Ácidos boswélicos e seu papel nas doenças inflamatórias crónicas. Adv Exp Med Biol. 2016;928:291-327.https://doi.org/10.1007/978-3-319-41334-1_13
[B173] Catanzaro D, Rancan S, Orso G, et al. Boswellia serrata Preserva a Barreira Epitelial Intestinal de Danos Oxidativos e Inflamatórios. PLoS One. 2015;10(5):e0125375.https://doi.org/10.1371/journal.pone.0125375
[B174] Khoshnazar M, Bigdeli MR, Parvardeh S, Pouriran R. Efeito atenuador do α-pineno no défice neurocomportamental, danos oxidativos e resposta inflamatória após acidente vascular cerebral isquémico focal em ratos. J Pharm Pharmacol. 2019;71(11):1725-1733.https://doi.org/10.1111/jphp.13164
[B175] Ryter SW, Alam J, Choi AM. Heme oxygenase-1/carbon monoxide: from basic science to therapeutic applications. Physiol Rev. 2006;86(2):583-650.https://doi.org/10.1152/physrev.00011.2005
[B176] Umar S, Umar K, Sarwar AH, et al. O extrato de Boswellia serrata atenua mediadores inflamatórios e stress oxidativo na artrite induzida por colagénio. Phytomedicine. 2014;21(6):847-856.https://doi.org/10.1016/j.phymed.2014.02.001
[B177] Abdel-Tawab M, Werz O, Schubert-Zsilavecz M. Boswellia serrata: uma avaliação global dos dados in vitro, pré-clínicos, farmacocinéticos e clínicos. Clin Pharmacokinet. 2011;50(6):349-369.https://doi.org/10.2165/11586800-000000000-00000
[B178] Hosseini M, Hadjzadeh MA, Derakhshan M, et al. Os efeitos benéficos do olíbano na deficiência de memória induzida por hipotiroidismo em ratos adultos testados no labirinto aquático de Morris. Arch Pharm Res. 2010;33(3):463-468.https://doi.org/10.1007/s12272-010-0316-6
[B179] Safayhi H, Mack T, Sabieraj J, Anazodo MI, Subramanian LR, Ammon HP. Ácidos boswélicos: inibidores novos, específicos e não redox de 5-lipoxigenase. J Pharmacol Exp Ther. 1992;261(3):1143-1146.https://www.sciencedirect.com/science/article/abs/pii/S0022356525111300
[B180] Werz O. 5-lipoxigenase: biologia celular e farmacologia molecular. Curr Drug Targets Inflamm Allergy. 2002;1(1):23-44.https://doi.org/10.2174/1568010023344959
[B181] Al-Harrasi A, Ali L, Hussain J, et al. Efeitos analgésicos de extratos brutos e frações de olíbano omanita obtido da planta medicinal tradicional *Boswellia sacra* em modelos animais. Asian Pac J Trop Med. 2014;7S1:S485-S490.https://doi.org/10.1016/S1995-7645(14 )60279-0
[B182] Cimanga K, Kambu K, Tona L, et al. Correlação entre a composição química e a atividade antibacteriana de óleos essenciais de algumas plantas aromáticas medicinais que crescem na República Democrática do Congo. J Ethnopharmacol. 2002;79(2):213-220.https://doi.org/10.1016/s0378-8741(01 )00384-1
[B183] Satou T, Kasuya H, Maeda K, Koike K. Inalação diária de α-pineno em ratinhos: efeitos no comportamento e acumulação em órgãos. Phytother Res. 2014;28(9):1284-1287.https://doi.org/10.1002/ptr.5105
[B184] Satou T, Murakami S, Matsuura M, Hayashi S, Koike K. Efeito ansiolítico e distribuição tecidual do óleo essencial inalado de Alpinia zerumbet em ratinhos. Nat Prod Commun. 2010;5(1):143-146.https://journals.sagepub.com/doi/10.1177/1934578X1000500133
[B185] Juergens UR, Dethlefsen U, Steinkamp G, Gillissen A, Repges R, Vetter H. Atividade anti-inflamatória do 1.8-cineol (eucaliptol) na asma brônquica: um ensaio duplo-cego controlado por placebo. Respir Med. 2003;97(3):250-256.https://doi.org/10.1053/rmed.2003.1432
[B186] Santos FA, Rao VS. Efeitos anti-inflamatórios e antinociceptivos do 1,8-cineol, um óxido de terpenoide presente em muitos óleos essenciais de plantas. Phytother Res. 2000;14(4):240-244.https://doi.org/10.1002/1099-1573(200006 )14:43.0.co;2-x
[B187] Tisserand R, Young R. Essential Oil Safety: A Guide for Health Care Professionals. 2.ª ed. Churchill Livingstone; 2014.https://www.elsevier.com/books/essential-oil-safety/tisserand/978-0-7020-4606-4
[B188] Worth H, Schacher C, Dethlefsen U. Terapia concomitante com cineol (eucaliptol) reduz exacerbações na DPOC: um ensaio duplo-cego controlado por placebo. Respir Res. 2009;10:69.https://doi.org/10.1186/1465-9921-10-69
[B189] Salehi B, Upadhyay S, Erdogan Orhan I, et al. Potencial Terapêutico do α- e β-Pineno: Um Presente Milagroso da Natureza. Biomolecules. 2019;9(11):738.https://doi.org/10.3390/biom9110738
[B190] Guzmán-Gutiérrez SL, Gómez-Cansino R, García-Zebadúa JC, Jiménez-Pérez NC, Reyes-Chilpa R. Atividade antidepressiva do óleo essencial de Litsea glaucescens: identificação de β-pineno e linalol como princípios ativos. J Ethnopharmacol. 2012;143(2):673-679.https://doi.org/10.1016/j.jep.2012.07.026
[B191] Yang H, Woo J, Pae AN, et al. O α-pineno, um constituinte principal dos óleos de pinheiro, melhora o sono de movimento não rápido em ratos através dos recetores GABAA-benzodiazepínicos. Mol Pharmacol. 2016;90(5):530-539.https://doi.org/10.1124/mol.116.105080
[B192] Kim DS, Lee HJ, Jeon YD, et al. O Alfa-Pineno Exibe Atividade Anti-inflamatória Através da Supressão das MAPKs e da Via NF-κB em Macrófagos Peritoneais de Rato. Am J Chin Med. 2015;43(4):731-742.https://doi.org/10.1142/S0192415X15500457
[B193] Porres-Martínez M, González-Burgos E, Carretero ME, Gómez-Serranillos MP. Propriedades protetoras do óleo essencial de Salvia lavandulifolia Vahl. contra a lesão neuronal induzida por stress oxidativo. Food Chem Toxicol. 2015;80:154-162.https://doi.org/10.1016/j.fct.2015.03.002
[B194] Miyazawa M, Watanabe H, Kameoka H. Inibição da atividade da acetilcolinesterase por mono-terpenoides com um esqueleto de p-mentano. J Agric Food Chem. 1997;45(3):677-679.https://doi.org/10.1021/jf960398b
[B195] Deutsch SI, Burket JA, Katz E. A perturbação subtil da migração neuronal contribui para a esquizofrenia e outras perturbações do neurodesenvolvimento? Mecanismos genéticos potenciais com possíveis implicações terapêuticas. Eur Neuropsychopharmacol. 2010;20(5):281-287.https://doi.org/10.1016/j.euroneuro.2010.02.005
[B196] Tan LT, Lee LH, Yin WF, et al. Usos Tradicionais, Fitoquímica e Bioatividades de Cananga odorata (Ylang-Ylang). Evid Based Complement Alternat Med. 2015;2015:896314.https://doi.org/10.1155/2015/896314
[B197] Jung YH, Ha TM, Ahn J, et al. A Inalação de Óleo Essencial de Cananga odorata Melhorou a Interação Social e os Comportamentos de Ansiedade em Ratos com Transtorno do Espectro do Autismo Induzido por Ácido Valproico. Nutrients. 2021;13(11):3804.https://doi.org/10.3390/nu13113804
[B198] Sinha Y, Silove N, Wheeler D, Williams K. Treino de integração auditiva e outras terapias sonoras para distúrbios do espectro do autismo: uma revisão sistemática. Arch Dis Child. 2006;91(12):1018-1022.https://doi.org/10.1136/adc.2006.094649
[B199] Cullen-Powell LA, Barlow JH, Cushway D. A exploração de uma intervenção de massagem para pais e seus filhos com autismo: as implicações para o vínculo e a segurança. J Child Health Care. 2005;9(4):245-255.https://doi.org/10.1177/1367493505056479
[B200] Buckle J. Aromaterapia Clínica: Óleos Essenciais nos Cuidados de Saúde. 3.ª ed. Churchill Livingstone; 2014.https://www.elsevier.com/books/clinical-aromatherapy/buckle/978-0-7020-5440-3
[B201] Saiyudthong S, Marsden CA. Efeitos agudos do óleo de bergamota no comportamento relacionado com a ansiedade e no nível de corticosterona em ratos. Phytother Res. 2011;25(6):858-862.https://doi.org/10.1002/ptr.3325
[B202] Navarra M, Mannucci C, Delbò M, Calapai G. Óleo essencial de Citrus bergamia: da investigação básica à aplicação clínica. Front Pharmacol. 2015;6:36.https://doi.org/10.3389/fphar.2015.00036
[B203] Efferth T, Oesch F. Atividades anti-inflamatórias e anticancerígenas do olíbano: Alvos, tratamentos e toxicidades. Semin Cancer Biol. 2022;80:39-57.https://doi.org/10.1016/j.semcancer.2020.01.015
[B204] Siddiqui MZ. Boswellia serrata, um potencial agente anti-inflamatório: uma revisão. Indian J Pharm Sci. 2011;73(3):255-261.https://doi.org/10.4103/0250-474X.93507
[B205] Hamidpour R, Hamidpour S, Hamidpour M, Shahlari M. Frankincense (rǔ xiāng; Boswellia Species): Da Seleção de Aplicações Tradicionais à Nova Fitoterapia para a Prevenção e Tratamento de Doenças Graves. J Tradit Complement Med. 2013;3(4):221-226.https://doi.org/10.4103/2225-4110.119723
[B206] Moussaieff A, Mechoulam R. Resina de Boswellia: de cerimónias religiosas a usos medicinais; uma revisão de ensaios in vitro, in vivo e clínicos. J Pharm Pharmacol. 2009;61(10):1281-1293.https://doi.org/10.1211/jpp/61.10.0003
[B207] Bakkali F, Averbeck S, Averbeck D, Idaomar M. Efeitos biológicos dos óleos essenciais – uma revisão. Food Chem Toxicol. 2008;46(2):446-475.https://doi.org/10.1016/j.fct.2007.09.106
[B208] Setzer WN. Óleos essenciais e aromaterapia ansiolítica. Nat Prod Commun. 2009;4(9):1305-1316.https://pubmed.ncbi.nlm.nih.gov/19831048/
[B209] Adams RP. Identification of Essential Oil Components by Gas Chromatography/Mass Spectrometry. 4ª ed. Allured Publishing; 2007.https://www.allured.com/identification-of-essential-oil-components-by-gas-chromatographymass-spectrometry-4th-edition
[B210] Dayawansa S, Umeno K, Takakura H, et al. Respostas autonómicas durante a inalação da fragrância natural de Cedrol em humanos. Auton Neurosci. 2003;108(1-2):79-86.https://doi.org/10.1016/j.autneu.2003.08.002
[B211] Cheaha D, Reakkamnuan C, Nukitram J, et al. Modificação do sono-vigília e do eletroencefalograma induzida pela inalação de óleo essencial de vetiver. J Intercult Ethnopharmacol. 2016;5(1):72-78.https://doi.org/10.5455/jice.20160208050736
[B212] Friedmann T. Freedom from ADHD: A Drug-Free Approach to Treating Children with ADHD. Lotus Press; 2000.https://www.researchgate.net/publication/265127532_Attention_Deficit_and_Hyperactivity_Disorder_ADHD
[B213] Weyerstahl P, Marschall H, Weirauch M, Thefeld K, Surburg H. Constituintes dos óleos comerciais de vetiver. Flavour Fragr J. 2000;15(3):153-173.https://doi.org/10.1002/1099-1026(200005/06 15:33.0.CO;2-V
[B214] Pripdeevech P, Chumpolsri W, Suttiarporn P, Wongpornchai S. A composição química e as atividades antioxidantes do manjericão da Tailândia utilizando índices de retenção e cromatografia gasosa bidimensional abrangente. J Serb Chem Soc. 2010;75(11):1503-1513.https://doi.org/10.2298/JSC100203125P
[B215] Hongratanaworakit T, Buchbauer G. Efeito relaxante do óleo de ylang ylang em humanos após absorção transdérmica. Phytother Res. 2006;20(9):758-763.https://doi.org/10.1002/ptr.1950
[B216] Moss M, Hewitt S, Moss L, Wesnes K. Modulação do desempenho cognitivo e do humor por aromas de hortelã-pimenta e ylang-ylang. Int J Neurosci. 2008;118(1):59-77.https://doi.org/10.1080/00207450601042094
[B217] Komiya M, Takeuchi T, Harada E. O vapor do óleo de limão causa um efeito anti-stress através da modulação das atividades da 5-HT e DA em ratos. Behav Brain Res. 2006;172(2):240-249.https://doi.org/10.1016/j.bbr.2006.05.006
[B218] Venturi GB. Investigações Experimentais Concernentes ao Princípio da Comunicação Lateral do Movimento em Fluidos. Phil Trans R Soc Lond. 1797;87:243-260.https://royalsocietypublishing.org/doi/10.1098/rstl.1799.0005
[B219] Buckle J. Utilização da aromaterapia como tratamento complementar para dor crónica. Altern Ther Health Med. 1999;5(5):42-51.https://pubmed.ncbi.nlm.nih.gov/10450129/
[B220] Hongratanaworakit T. Efeitos aromaterapêuticos de óleos essenciais misturados em massagem em humanos. Nat Prod Commun. 2011;6(8):1199-1204.https://www.researchgate.net/publication/51647617_Aroma-therapeutic_Effects_of_Massage_Blended_Essential_Oils_on_Humans
[B221] White FM. Mecânica dos Fluidos. 8.ª ed. McGraw-Hill Education; 2015.https://www.mheducation.com/highered/product/fluid-mechanics-white/M9781260258318.html
[B222] Haze S, Sakai K, Gozu Y. Efeitos da inalação de fragrâncias na atividade simpática em adultos normais. Jpn J Pharmacol. 2002;90(3):247-253.https://doi.org/10.1254/jjp.90.247
[B223] Herz RS. Aromaterapia: factos e ficções - uma análise científica dos efeitos olfativos no humor, fisiologia e comportamento. Int J Neurosci. 2009;119(2):263-290.https://doi.org/10.1080/00207450802333953
[B224] Turek C, Stintzing FC. Estabilidade de Óleos Essenciais: Uma Revisão. Compr Rev Food Sci Food Saf. 2013;12(1):40-53.https://doi.org/10.1111/1541-4337.12006
[B225] Buckle J. Aromaterapia Clínica em Enfermagem. 2.ª ed. Prática de Enfermagem Holística; 2001.https://journals.lww.com/holistic-nursing-practice/citation/2001/04000/clinical_aromatherapy_in_nursing.15.aspx
[B226] Labiris NR, Dolovich MB. Pulmonary drug delivery. Part I: physiological factors affecting therapeutic effectiveness of aerosolized medications. Br J Clin Pharmacol. 2003;56(6):588-599.https://doi.org/10.1046/j.1365-2125.2003.01892.x
[B227] Price S, Price L. Aromatherapy for Health Professionals. 4.ª ed. Churchill Livingstone; 2011.https://www.elsevier.com/books/aromatherapy-for-health-professionals/price/978-0-7020-3151-0
[B228] Battaglia S. The Complete Guide to Aromatherapy. 3.ª ed. Black Pepper Creative; 2018.https://www.blackpeppercreative.com.au/the-complete-guide-to-aromatherapy
[B229] Posadzki P, Alotaibi A, Ernst E. Efeitos adversos da aromaterapia: uma revisão sistemática de relatos de caso e séries de casos. Int J Risk Saf Med. 2012;24(3):147-161.https://doi.org/10.3233/JRS-2012-0568
[B230] Dunn C, Sleep J, Collett D. Sensing an improvement: an experimental study to evaluate the use of aromatherapy, massage and periods of rest in an intensive care unit. J Adv Nurs. 1995;21(1):34-40.https://doi.org/10.1046/j.1365-2648.1995.21010034.x
[B231] Bowles EJ. The Chemistry of Aromatherapeutic Oils. 3.ª ed. Allen & Unwin; 2003.https://www.allenandunwin.com/browse/books/general-books/health-wellbeing/The-Chemistry-of-Aromatherapeutic-Oils-E-Joy-Bowles-9781741140217
[B232] Schnaubelt K. Aromaterapia Avançada: A Ciência da Terapia com Óleos Essenciais. Healing Arts Press; 1998.https://www.healingartspressbooks.com/advanced-aromatherapy
[B233] Schaaf RC, Lane AE. Rumo a um protocolo de melhores práticas para a avaliação de características sensoriais em TEA. J Autism Dev Disord. 2015;45(5):1380-1395.https://doi.org/10.1007/s10803-014-2299-z
[B234] Wolkoff P, Wilkins CK, Clausen PA, Nielsen GD. Compostos orgânicos em ambientes de escritório – irritação sensorial, odor, medições e o papel da química reativa. Indoor Air. 2006;16(1):7-19.https://doi.org/10.1111/j.1600-0668.2005.00393.x
[B235] Dalton P. Adaptação olfativa e adaptação cruzada. In: Doty RL, ed. Handbook of Olfaction and Gustation. 3.ª ed. Wiley-Blackwell; 2015:443-459.https://www.wiley.com/en-us/Handbook+of+Olfaction+and+Gustation%2C+3rd+Edition-p-9780470455951
[B236] Cain WS. Saber com o nariz: chaves para a identificação de odores. Science. 1979;203(4379):467-470.https://doi.org/10.1126/science.760202
[B237] Kern JK, Trivedi MH, Garver CR, et al. O padrão de anomalias no processamento sensorial no autismo. Autism. 2006;10(5):480-494.https://doi.org/10.1177/1362361306066564
[B238] Lehrner J, Marwinski G, Lehr S, Johren P, Deecke L. Odores ambientes de laranja e lavanda reduzem a ansiedade e melhoram o humor num consultório dentário. Physiol Behav. 2005;86(1-2):92-95.https://doi.org/10.1016/j.physbeh.2005.06.031
[B239] Cavanagh HM, Wilkinson JM. Atividades biológicas do óleo essencial de lavanda. Phytother Res. 2002;16(4):301-308.https://doi.org/10.1002/ptr.1103
[B240] Diego MA, Jones NA, Field T, et al. Aromaterapia afeta positivamente o humor, padrões de EEG de alerta e cálculos matemáticos. Int J Neurosci. 1998;96(3-4):217-224.https://doi.org/10.3109/00207459808986469
[B241] Field T, Diego M, Hernandez-Reif M, Cisneros W, Feijo L, Vera Y, Gil K, Grina D, Claire He Q. Efeitos da fragrância de lavanda em gel de limpeza no relaxamento. Int J Neurosci. 2005;115(2):207-222.https://doi.org/10.1080/00207450590519175
[B242] Goel N, Kim H, Lao RP. Um estímulo olfativo modifica o sono noturno em homens e mulheres jovens. Chronobiol Int. 2005;22(5):889-904.https://doi.org/10.1080/07420520500263276
[B243] Ashburner J, Ziviani J, Rodger S. Processamento sensorial e resultados emocionais, comportamentais e educacionais em sala de aula em crianças com transtorno do espectro do autismo. Am J Occup Ther. 2008;62(5):564-573.https://doi.org/10.5014/ajot.62.5.564
[B244] Tomchek SD, Dunn W. Processamento sensorial em crianças com e sem autismo: um estudo comparativo utilizando o Short Sensory Profile. Am J Occup Ther. 2007;61(2):190-200.https://doi.org/10.5014/ajot.61.2.190
[B245] Ben-Sasson A, Hen L, Fluss R, Cermak SA, Engel-Yeger B, Gal E. Uma meta-análise de sintomas de modulação sensorial em indivíduos com transtornos do espectro do autismo. J Autism Dev Disord. 2009;39(1):1-11.https://doi.org/10.1007/s10803-008-0593-3
[B246] Leekam SR, Nieto C, Libby SJ, Wing L, Gould J. Describing the sensory abnormalities of children and adults with autism. J Autism Dev Disord. 2007;37(5):894-910.https://doi.org/10.1007/s10803-006-0218-7
[B247] Baranek GT, David FJ, Poe MD, Stone WL, Watson LR. Sensory Experiences Questionnaire: discriminating sensory features in young children with autism, developmental delays, and typical development. J Child Psychol Psychiatry. 2006;47(6):591-601.https://doi.org/10.1111/j.1469-7610.2005.01546.x
[B248] Herz RS. O papel da memória evocada por odores na saúde psicológica e fisiológica. Brain Sci. 2016;6(3):22.https://doi.org/10.3390/brainsci6030022
[B249] Mesibov GB, Shea V, Schopler E. The TEACCH Approach to Autism Spectrum Disorders. Springer; 2004.https://link.springer.com/book/10.1007/978-0-387-23855-2
[B250] Oono IP, Honey EJ, McConachie H. Intervenção precoce mediada pelos pais para crianças pequenas com transtornos do espectro do autismo (TEA). Cochrane Database Syst Rev. 2013;(4):CD009774.https://doi.org/10.1002/14651858.CD009774.pub2
[B251] Marriott PJ, Shellie R, Cornwell C. Tecnologias de cromatografia gasosa para a análise de óleos essenciais. J Chromatogr A. 2001;936(1-2):1-22.https://doi.org/10.1016/s0021-9673(01 )01314-0
[B252] Sparkman OD, Penton Z, Kitson FG. Gas Chromatography and Mass Spectrometry: A Practical Guide. 2.ª ed. Academic Press; 2011.https://www.sciencedirect.com/book/9780123736284/gas-chromatography-and-mass-spectrometry
[B253] ISO 4720:2009. Óleos essenciais – Nomenclatura. International Organization for Standardization; 2009.https://www.iso.org/standard/41076.html
[B254] ISO 11024-1:1998. Óleos essenciais – Orientações gerais sobre perfis cromatográficos – Parte 1: Preparação de perfis cromatográficos para apresentação em normas. International Organization for Standardization; 1998.https://www.iso.org/standard/19053.html
[B255] Dhifi W, Bellili S, Jazi S, Bahloul N, Mnif W. Caracterização Química e Investigação de Algumas Atividades Biológicas de Óleos Essenciais: Uma Revisão Crítica. Medicines (Basel). 2016;3(4):25.https://doi.org/10.3390/medicines3040025
[B256] Lis-Balchin M. Aromatherapy Science: A Guide for Healthcare Professionals. Pharmaceutical Press; 2006.https://www.pharmpress.com/product/9780853696230/aromatherapy-science
[B257] Schnaubelt K. Aromaterapia Médica: Cura com Óleos Essenciais. Frog Books; 1999.https://www.innertraditions.com/books/medical-aromatherapy
[B258] Tisserand R. The Art of Aromatherapy. Healing Arts Press; 1977.https://www.innertraditions.com/books/the-art-of-aromatherapy
[B259] Pauli A. Propriedades antimicrobianas de constituintes de óleos essenciais. Int J Aromather. 2001;11(3):126-133.https://doi.org/10.1016/S0962-4562(01 )80048-5
[B260] Comissão Europeia da Farmacopeia. Farmacopeia Europeia. 10.ª ed. Conselho da Europa; 2019.https://www.edqm.eu/en/european-pharmacopoeia-ph-eur-11th-edition
[B261] Wabner D, Beier C. Aromaterapia: Fundamentos, princípios de ação, prática. 2ª ed. Urban & Fischer; 2012.https://www.elsevier.com/books/aromatherapie/wabner/978-3-437-57214-4
[B262] Lis-Balchin M. Geranium and Pelargonium: The Genera Geranium and Pelargonium. CRC Press; 2002.https://www.routledge.com/Geranium-and-Pelargonium/Lis-Balchin/p/book/9780415284653
[B263] Turek C, Stintzing FC. Estabilidade de óleos essenciais: uma revisão. Compr Rev Food Sci Food Saf. 2013;12(1):40-53.https://doi.org/10.1111/1541-4337.12006
[B264] Skold M, Karlberg AT, Matura M, Börje A. O químico de fragrância beta-cariofileno – oxidação ao ar e sensibilização da pele. Food Chem Toxicol. 2006;44(4):538-545.https://doi.org/10.1016/j.fct.2005.08.028
[B265] Tavassoli T, Miller LJ, Schoen SA, Nielsen DM, Baron-Cohen S. Sensibilidade sensorial aumentada em adultos com condições do espectro do autismo. Autism. 2014;18(4):428-432.https://doi.org/10.1177/1362361313477246
[B266] Lane AE, Young RL, Baker AE, Angley MT. Subtipos de processamento sensorial no autismo: associação com comportamento adaptativo. J Autism Dev Disord. 2010;40(1):112-122.https://doi.org/10.1007/s10803-009-0840-2
[B267] Mazurek MO, Vasa RA, Kalb LG, et al. Ansiedade, hipersensibilidade sensorial e problemas gastrointestinais em crianças com transtornos do espectro do autismo. J Abnorm Child Psychol. 2013;41(1):165-176.https://doi.org/10.1007/s10802-012-9668-x
[B268] Buckle J. Aromaterapia Clínica: Óleos Essenciais na Prática. 2ª ed. Churchill Livingstone; 2003.https://www.elsevier.com/books/clinical-aromatherapy/buckle/978-0-7020-2536-6
[B269] Tuchman R, Cuccaro M, Alessandri M. Autismo e epilepsia: perspetiva histórica. Brain Dev. 2010;32(9):709-718.https://doi.org/10.1016/j.braindev.2010.04.008
[B270] Burkhard PR, Burkhardt K, Haenggeli CA, Landis T. Convulsões induzidas por plantas: reaparecimento de um problema antigo. J Neurol. 1999;246(8):667-670.https://doi.org/10.1007/s004150050434
[B271] Millet Y, Jouglard J, Steinmetz MD, Tognetti P, Joanny P, Arditti J. Toxicidade de alguns óleos vegetais essenciais. Estudo clínico e experimental. Clin Toxicol. 1981;18(12):1485-1498.https://doi.org/10.3109/15563658108990111
[B272] Pengelly A, Bennett K, Spinks J, Bensoussan A. A avaliação da base de evidências para o uso de óleos essenciais no controlo da epilepsia: Uma revisão sistemática. Epilepsy Behav. 2012;24(1):9-15.https://doi.org/10.1016/j.yebeh.2012.02.019
[B273] Höld KM, Sirisoma NS, Ikeda T, Narahashi T, Casida JE. Alfa-tujona (o componente ativo do absinto): modulação do recetor gama-aminobutírico tipo A e desintoxicação metabólica. Proc Natl Acad Sci U S A. 2000;97(8):3826-3831.https://doi.org/10.1073/pnas.070042397
[B274] Millet Y, Tognetti P, Lavaire-Perlovisi M, Steinmetz MD, Arditti J, Jouglard J. Estudo sobre as propriedades convulsivas de amostras comerciais de óleos essenciais de Hyssopus officinalis L. e Salvia officinalis L. Plantes Med Phytother. 1979;13(3):179-184.https://www.sciencedirect.com/science/article/abs/pii/S0370447579800477
[B275] Marcus C, Lichtenstein EP. Interactions of naturally occurring food plant components with insecticides and pentobarbital in rats and mice. J Agric Food Chem. 1979;27(5):1217-1223.https://doi.org/10.1021/jf60226a004
[B276] Koutroumanidou E, Kimbaris A, Kortsaris A, et al. Latência aumentada de convulsões e diminuição da gravidade de convulsões induzidas por pentilenetetrazol em ratos após administração de óleo essencial. Epilepsy Res Treat. 2013;2013:532657.https://doi.org/10.1155/2013/532657
[B277] Avallone R, Zanoli P, Puia G, Kleinschnitz M, Schreier P, Baraldi M. Perfil farmacológico da apigenina, um flavonóide isolado da Matricaria chamomilla. Biochem Pharmacol. 2000;59(11):1387-1394.https://doi.org/10.1016/s0006-2952(00 )00264-1
[B278] Watanabe E, Kuchta K, Kimura M, Rauwald HW, Kamei T, Imanishi J. Efeitos da aromaterapia com óleo essencial de bergamota (Citrus bergamia (Risso) Wright & Arn.) nos estados de humor, atividade do sistema nervoso parassimpático e níveis de cortisol salivar em 41 mulheres saudáveis. Forsch Komplementmed. 2015;22(1):43-49.https://doi.org/10.1159/000380989
[B279] Ilhan S, Savaşer S, Kölgelier S. Efeito da aromaterapia em doentes com epilepsia. Epilepsy Behav. 2004;5(5):753-757.https://doi.org/10.1016/j.yebeh.2004.06.004
[B280] Meamarbashi A, Rajabi A. The effects of peppermint on exercise performance. J Int Soc Sports Nutr. 2013;10(1):15.https://doi.org/10.1186/1550-2783-10-15
[B281] Eccles R. Mentol e compostos refrescantes relacionados. J Pharm Pharmacol. 1994;46(8):618-630.https://doi.org/10.1111/j.2042-7158.1994.tb03871.x
[B282] Silva J, Abebe W, Sousa SM, Duarte VG, Machado MI, Matos FJ. Efeitos analgésicos e anti-inflamatórios de óleos essenciais de Eucalyptus. J Ethnopharmacol. 2003;89(2-3):277-283.https://doi.org/10.1016/j.jep.2003.09.007
[B283] Fachini-Queiroz FC, Kummer R, Estevão-Silva CF, et al. Efeitos do Timol e Carvacrol, Constituintes do Óleo Essencial de Thymus vulgaris L., na Resposta Inflamatória. Evid Based Complement Alternat Med. 2012;2012:657026.https://doi.org/10.1155/2012/657026
[B284] Carson CF, Hammer KA, Riley TV. Melaleuca alternifolia (Tea Tree) Oil: a Review of Antimicrobial and Other Medicinal Properties. Clin Microbiol Rev. 2006;19(1):50-62.https://doi.org/10.1128/CMR.19.1.50-62.2006
[B285] Eccles R, Jawad MS, Morris S. Os efeitos da administração oral de (-)-mentol na resistência nasal ao fluxo de ar e na sensação nasal de fluxo de ar em sujeitos com congestão nasal associada a constipações. J Pharm Pharmacol. 1990;42(9):652-654.https://doi.org/10.1111/j.2042-7158.1990.tb06625.x
[B286] Altunbas MK, Celık F, Kahraman C. O potencial do óleo essencial de lavanda para uso seguro em recém-nascidos. J Neonatal Nurs. 2020;26(6):303-307.https://doi.org/10.1016/j.jnn.2020.05.005
[B287] Srivastava JK, Shankar E, Gupta S. Chamomile: Uma medicina herbal do passado com um futuro brilhante. Mol Med Rep. 2010;3(6):895-901.https://doi.org/10.3892/mmr.2010.377
[B288] Kiecolt-Glaser JK, Graham JE, Malarkey WB, Porter K, Lemeshow S, Glaser R. Influências olfativas no humor e na função autonómica, endócrina e imunitária. Psychoneuroendocrinology. 2008;33(3):328-339.https://doi.org/10.1016/j.psyneuen.2007.11.015
[B289] Halm MA. Óleos essenciais para a gestão de sintomas em doentes críticos. Am J Crit Care. 2008;17(2):160-163.https://www.researchgate.net/publication/5541002_Essential_Oils_for_Management_of_Symptoms_in_Critically_Ill_Patients
[B290] Fung LK, Mahajan R, Nozzolillo A, et al. Tratamento Farmacológico da Irritabilidade Grave e Comportamentos Problemáticos no Autismo: Uma Revisão Sistemática e Meta-análise. Pediatrics. 2016;137 Suppl 2:S124-S135.https://doi.org/10.1542/peds.2015-2851K
[B291] Kirschbaum KM, Müller MJ, Malevani J, et al. Níveis séricos de aripiprazol e dehidroaripiprazol, resposta clínica e efeitos secundários. World J Biol Psychiatry. 2008;9(3):212-218.https://doi.org/10.1080/15622970701361255
[B292] Sprouse J, Clarke T, Reynolds L, Heym J, Rollema H. Comparação dos efeitos da sertralina e do seu metabolito desmetilsertralina no bloqueio da recaptação central de 5-HT in vivo. Neuropsychopharmacology. 1996;14(4):225-231.https://doi.org/10.1016/0893-133X(95 )00112-Q
[B293] Bailey DG, Dresser G, Arnold JM. Interações sumo de toranja-medicamentos: fruto proibido ou consequências evitáveis? CMAJ. 2013;185(4):309-316.https://doi.org/10.1503/cmaj.120951
[B294] Obach RS, Walsky RL, Venkatakrishnan K, Gaman EA, Houston JB, Tremaine LM. A utilidade dos dados de inibição do citocromo P450 in vitro na previsão de interações medicamentosas. J Pharmacol Exp Ther. 2006;316(1):336-348.https://doi.org/10.1124/jpet.105.093229
[B295] Guo LQ, Yamazoe Y. Inibição do citocromo P450 por furanocumarinas em sumo de toranja e medicamentos à base de plantas. Acta Pharmacol Sin. 2004;25(2):129-136.https://www.researchgate.net/publication/8881220_Inhibition_of_cytochrome_P450_by_furanocoumarins_in_grapefruit_juice_and_herbal_medicines
[B296] Paine MF, Criss AB, Watkins PB. Dois componentes principais do sumo de toranja diferem no tempo de início da inibição do CYP3A4 intestinal. J Pharmacol Exp Ther. 2004;312(3):1151-1160.https://doi.org/10.1124/jpet.104.076570
[B297] Hanley MJ, Cancalon P, Widmer WW, Greenblatt DJ. O efeito do sumo de toranja na disposição de medicamentos. Expert Opin Drug Metab Toxicol. 2011;7(3):267-286.https://doi.org/10.1517/17425255.2011.553189
[B298] Dresser GK, Bailey DG. Os efeitos dos sumo de fruta na disposição de medicamentos: um novo modelo para interações medicamentosas. Eur J Clin Invest. 2003;33 Suppl 2:10-16.https://doi.org/10.1046/j.1365-2362.33.s2.2.x
[B299] Izzo AA, Ernst E. Interações entre medicamentos à base de plantas e medicamentos prescritos: uma revisão sistemática atualizada. Drugs. 2009;69(13):1777-1798.https://doi.org/10.2165/11317010-000000000-00000
[B300] Henderson L, Yue QY, Bergquist C, Gerden B, Arlett P. Erva de São João (Hypericum perforatum): interações medicamentosas e resultados clínicos. Br J Clin Pharmacol. 2002;54(4):349-356.https://doi.org/10.1046/j.1365-2125.2002.01683.x
[B301] Unger M, Frank A. Determinação simultânea da potência inibitória de extratos de plantas na atividade de seis enzimas principais do citocromo P450 utilizando cromatografia/espectrometria de massa líquida e extração online automatizada. Rapid Commun Mass Spectrom. 2004;18(19):2273-2281.https://doi.org/10.1002/rcm.1621
[B302] Gurley BJ, Gardner SF, Hubbard MA, et al. Efeitos in vivo da raiz-dourada, kava kava, trevo-do-cabo e valeriana em fenótipos humanos do citocromo P450 1A2, 2D6, 2E1 e 3A4/5. Clin Pharmacol Ther. 2005;77(5):415-426.https://doi.org/10.1016/j.clpt.2005.01.009
[B303] Spinella M. A importância da sinergia farmacológica em medicamentos fitoterápicos psicoativos. Altern Med Rev. 2002;7(2):130-137.https://pubmed.ncbi.nlm.nih.gov/11968843/
[B304] Abourashed EA, Koetter U, Brattström A. Experiências de ligação in vitro com extratos de Valeriana, lúpulo e a sua combinação fixa (Ze91019) a recetores selecionados do sistema nervoso central. Phytomedicine. 2004;11(7-8):633-638.https://doi.org/10.1016/j.phymed.2004.03.005
[B305] Brazier NC, Levine MA. Interação entre medicamentos e plantas medicinais entre medicamentos convencionais de uso comum: um compêndio para profissionais de saúde. Am J Ther. 2003;10(3):163-169.https://doi.org/10.1097/00045391-200305000-00003
[B306] De Groot AC, Schmidt E. Essential oils: contact allergy and chemical composition. CRC Press; 2016.https://www.routledge.com/Essential-Oils-Contact-Allergy-and-Chemical-Composition/de-Groot-Schmidt/p/book/9781498702508
[B307] Shellie R, Marriott P, Huie C. Análise cromatográfica gasosa bidimensional (GC × GC) e GC × GC-espetrometria de massa quadrupolar (GC × GC-quadrupole MS) de ginseng asiático e americano. J Sep Sci. 2003;26(12-13):1185-1192.https://doi.org/10.1002/jssc.200301521
[B308] Kubeczka KH. História e fontes de investigação de óleos essenciais. In: Baser KHC, Buchbauer G, eds. Handbook of Essential Oils: Science, Technology, and Applications. CRC Press; 2010:3-38.https://www.routledge.com/Handbook-of-Essential-Oils-Science-Technology-and-Applications/Baser-Buchbauer/p/book/9781032046419
[B309] Cavanagh HM, Wilkinson JM. Óleo essencial de lavanda: uma revisão. Aust Infect Control. 2005;10(1):35-37.https://doi.org/10.1071/HI05035
[B310] Leung AY, Foster S. Encyclopedia of Common Natural Ingredients Used in Food, Drugs, and Cosmetics. 2.ª ed. Wiley; 1996.https://www.wiley.com/en-us/Encyclopedia+of+Common+Natural+Ingredients+Used+in+Food%2C+Drugs%2C+and+Cosmetics%2C+2nd+Edition-p-9780471508267
[B311] Lis-Balchin M. Aromaterapia com óleos essenciais. In: Lis-Balchin M, ed. Aromatherapy Science: A Guide for Healthcare Professionals. Pharmaceutical Press; 2006:49-115.https://www.pharmpress.com/product/9780853696230/aromatherapy-science
Williams TI. Um olhar ansioso sobre a aromaterapia. Perspect Psychiatr Care. 2006;42(2):107-108.https://doi.org/10.1111/j.1744-6163.2006.00056.x
[B313] Brondino N, Fusar-Poli L, Rocchetti M, Provenzani U, Barale F, Politi P. Terapias Complementares e Alternativas para o Transtorno do Espectro Autista. Evid Based Complement Alternat Med. 2015;2015:258589.https://doi.org/10.1155/2015/258589
[B314] Bent S, Bertoglio K, Hendren RL. Ácidos gordos ómega-3 para o transtorno do espectro autista: uma revisão sistemática. J Autism Dev Disord. 2009;39(8):1145-1154.https://doi.org/10.1007/s10803-009-0724-5
[B315] Masi A, Quintana DS, Glozier N, Lloyd AR, Hickie IB, Guastella AJ. Aberrações de citocinas no transtorno do espectro do autismo: uma revisão sistemática e meta-análise. Mol Psychiatry. 2015;20(4):440-446.https://doi.org/10.1038/mp.2014.59
[B316] Veenstra-VanderWeele J, Blakely RD. Networking em autismo: aproveitando descobertas genéticas, de biomarcadores e de sistemas modelo na busca por novos tratamentos. Neuropsychopharmacology. 2012;37(1):196-212.https://doi.org/10.1038/npp.2011.185
[B317] Yamasue H, Domes G. Oxitocina e Transtornos do Espectro Autista. Curr Top Behav Neurosci. 2018;35:449-465.https://doi.org/10.1007/7854_2017_24
[B318] Petra AI, Panagiotidou S, Hatziagelaki E, Stewart JM, Conti P, Theoharides TC. Eixo Intestino-Microbiota-Cérebro e o seu Efeito em Doenças Neuropsiquiátricas com Suspeita de Desregulação Imunitária. Clin Ther. 2015;37(5):984-995.https://doi.org/10.1016/j.clinthera.2015.04.002
[B319] Mayer EA, Tillisch K, Gupta A. Eixo intestino/cérebro e o microbioma. J Clin Invest. 2015;125(3):926-938.https://doi.org/10.1172/JCI76304
[B320] Button KS, Ioannidis JP, Mokrysz C, et al. Falha de energia: porquê o tamanho reduzido da amostra enfraquece a fiabilidade da neurociência. Nat Rev Neurosci. 2013;14(5):365-376.https://doi.org/10.1038/nrn3475
[B321] Higgins JP, Thompson SG, Deeks JJ, Altman DG. A medição da inconsistência em meta-análises. BMJ. 2003;327(7414):557-560.https://doi.org/10.1136/bmj.327.7414.557
[B322] Rossignol DA. Tratamentos novos e emergentes para transtornos do espectro do autismo: uma revisão sistemática. Ann Clin Psychiatry. 2009;21(4):213-236.https://pmc.ncbi.nlm.nih.gov/articles/PMC3859980/
Moher D, Liberati A, Tetzlaff J, Altman DG; PRISMA Group. Preferred reporting items for systematic reviews and meta-analyses: the PRISMA statement. PLoS Med. 2009;6(7):e1000097.https://doi.org/10.1371/journal.pmed.1000097
[B324] Ioannidis JP, Patsopoulos NA, Rothstein HR. Razões ou desculpas para evitar a meta-análise em gráficos de floresta. BMJ. 2008;336(7658):1413-1415.https://doi.org/10.1136/bmj.a117
[B325] Loth E, Charman T, Mason L, et al. O EU-AIMS Longitudinal European Autism Project (LEAP): desenho e metodologias para identificar e validar biomarcadores de estratificação para transtornos do espectro do autismo. Mol Autism. 2017;8:24.https://doi.org/10.1186/s13229-017-0146-8
[B326] Geschwind DH, Flint J. Genética e genómica de doenças psiquiátricas. Science. 2015;349(6255):1489-1494.https://doi.org/10.1126/science.aaa8954
[B327] Easterbrook PJ, Berlin JA, Gopalan R, Matthews DR. Publication bias in clinical research. Lancet. 1991;337(8746):867-872.https://doi.org/10.1016/0140-6736(91 090201-y
[B328] Nestler EJ, Hyman SE. Animal models of neuropsychiatric disorders. Nat Neurosci. 2010;13(10):1161-1169.https://doi.org/10.1038/nn.2647
[B329] Buchbauer G, Jirovetz L, Jäger W, Plank C, Dietrich H. Compostos de fragrância e óleos essenciais com efeitos sedativos por inalação. J Pharm Sci. 1993;82(6):660-664.https://doi.org/10.1002/jps.2600820623
[B330] Cooke B, Ernst E. Aromaterapia: uma revisão sistemática. Br J Gen Pract. 2000;50(455):493-496.https://pubmed.ncbi.nlm.nih.gov/10962794/
[B331] Halm MA. Óleos essenciais para o controlo de sintomas em doentes críticos. Am J Crit Care. 2008;17(2):160-163.https://www.researchgate.net/publication/5541002_Essential_Oils_for_Management_of_Symptoms_in_Critically_Ill_Patients
[B332] Hammer KA, Carson CF, Riley TV. Atividade antimicrobiana de óleos essenciais e outros extratos vegetais. J Appl Microbiol. 1999;86(6):985-990.https://doi.org/10.1046/j.1365-2672.1999.00780.x
[B333] Schulz KF, Altman DG, Moher D; CONSORT Group. CONSORT 2010 statement: updated guidelines for reporting parallel group randomised trials. BMJ. 2010;340:c332.https://doi.org/10.1136/bmj.c332
[B334] Lombardo MV, Lai MC, Baron-Cohen S. Abordagens de *big data* para decompor a heterogeneidade no espectro do autismo. Mol Psychiatry. 2019;24(10):1435-1450.https://doi.org/10.1038/s41380-018-0321-0
[B335] Insel TR. O Projeto dos Critérios de Domínio de Investigação (RDoC) do NIMH: medicina de precisão para a psiquiatria. Am J Psychiatry. 2014;171(4):395-397.https://doi.org/10.1176/appi.ajp.2014.14020138
[B336] Jeste SS, Geschwind DH. Ensaios clínicos para perturbações do neurodesenvolvimento: Na vanguarda terapêutica. Sci Transl Med. 2016;8(321):321fs1.https://doi.org/10.1126/scitranslmed.aad9874
[B337] Kovar KA, Gropper B, Friess D, Ammon HP. Níveis sanguíneos de 1,8-cineol e atividade locomotora de ratos após inalação e administração oral de óleo de alecrim. Planta Med. 1987;53(4):315-318.https://doi.org/10.1055/s-2006-962725
[B338] Rossignol DA, Frye RE. Uma revisão das tendências de investigação em anormalidades fisiológicas nos transtornos do espetro autista: desregulação imune, inflamação, stress oxidativo, disfunção mitocondrial e exposição a tóxicos ambientais. Mol Psychiatry. 2012;17(4):389-401.https://doi.org/10.1038/mp.2011.165
[B339] Stang A. Avaliação crítica da escala Newcastle-Ottawa para a avaliação da qualidade de estudos não aleatorizados em meta-análises. Eur J Epidemiol. 2010;25(9):603-605.https://doi.org/10.1007/s10654-010-9491-z
[B340] Herz RS. Aromoterapia: factos e ficções. Análise científica dos efeitos olfativos no humor, fisiologia e comportamento. Int J Neurosci. 2009;119(2):263-290.https://doi.org/10.1080/00207450802333953
[B341] Myers SM, Johnson CP; American Academy of Pediatrics Council on Children With Disabilities. Gestão de crianças com transtornos do espectro do autismo. Pediatrics. 2007;120(5):1162-1182.https://doi.org/10.1542/peds.2007-2362
[B342] Volkmar F, Siegel M, Woodbury-Smith M, King B, McCracken J, State M; American Academy of Child and Adolescent Psychiatry (AACAP) Committee on Quality Issues (CQI). Practice parameter for the assessment and treatment of children and adolescents with autism spectrum disorder. J Am Acad Child Adolesc Psychiatry. 2014;53(2):237-257.https://doi.org/10.1016/j.jaac.2013.10.013
[B343] Green VA, Pituch KA, Itchon J, Choi A, O’Reilly M, Sigafoos J. Inquérito online sobre tratamentos utilizados por pais de crianças com autismo. Res Dev Disabil. 2006;27(1):70-84.https://doi.org/10.1016/j.ridd.2004.12.002
[B344] Bilia AR, Guccione C, Isacchi B, Righeschi C, Firenzuoli F, Bergonzi MC. Óleos essenciais encapsulados em nanosistemas: uma estratégia em desenvolvimento para uma abordagem terapêutica bem-sucedida. Evid Based Complement Alternat Med. 2014;2014:651593.https://doi.org/10.1155/2014/651593
[B345] Woolf AD. Envenenamento por óleos essenciais. J Toxicol Clin Toxicol. 1999;37(6):721-727.https://doi.org/10.1081/clt-100102450
[B346] Kasper S, Gastpar M, Müller WE, et al. Eficácia e segurança do silexan, um novo preparado de óleo de lavanda administrado por via oral, na perturbação de ansiedade limiar – evidência de ensaios clínicos. Wien Med Wochenschr. 2010;160(21-22):547-556.https://doi.org/10.1007/s10354-010-0845-7
B347. A suplementação com gengibre alivia comportamentos autistas através da modulação da sinalização AKT/GSK3β em ratinhos expostos ao valproato de sódio pré-natal. PubMed. https://doi.org/10.1039/d5fo04364f
B348. Efeito do xarope Hiwa, um produto de medicina persa, nos sintomas de autismo em crianças com perturbações do espectro do autismo: um ensaio clínico randomizado duplo-cego. Revista Médica Global. https://doi.org/10.31661/gmj.v13i.3553
B349. McGuinness, F., Oswald, I. W. H., Koby, K. A., et al. (2023). O canabidiol e misturas de terpenos inspiradas em canábis têm efeitos pró-sociais agudos no modelo de rato BTBR de transtorno do espectro do autismo. Frontiers in Neuroscience. https://doi.org/10.3389/fnins.2023.1185737
Glossário TDAH
TDH (Transtorno de Défice de Atenção e Hiperatividade)
Doença neuropsiquiátrica caracterizada por desatenção, hiperatividade e impulsividade.
Terapia adjuvante
Tratamento complementar, utilizado adicionalmente à terapia principal, para potenciar o seu efeito ou reduzir efeitos secundários.
Ansiolítico
Ansiolítico, redutor de ansiedade.
Barreira hematoencefálica
Barreira seletiva entre a corrente sanguínea e o cérebro, que controla a passagem de substâncias para o cérebro.
Recetor CB2
Recetor canabinóide tipo 2, parte do sistema endocanabinóide, principalmente em células imunitárias; a ativação tem um efeito anti-inflamatório.
Quimiotipo
Variante química de uma planta com composição diferente de óleos essenciais (por exemplo, Quimiotipo de Alecrim Cinol vs. Cânfora).
DAT (Transportador de Dopamina)
Proteína que transporta a dopamina da fenda sináptica de volta para o neurónio; principal alvo do metilfenidato.
DAT-Okkupanz
Percentagem de transportadores de dopamina bloqueados por um medicamento.
Dopamina
Neurotransmissor, importante para a motivação, recompensa, movimento e atenção; frequentemente diminuído na TDAH.
CE₅₀
Dose que atinge 50% do efeito máximo.
GABA (Ácido Gama-Aminobutírico)
O neurotransmissor inibitório (inibidor) mais importante no cérebro; reduz a excitabilidade neuronal.
Recetor GABA-A
Recetor de canais iónicos para GABA; a ativação leva à entrada de cloreto e hiperpolarização (inibição) do neurónio.
CG/EM (Cromatografia Gasosa/Espectrometria de Massa)
Método analítico para a identificação e quantificação de componentes químicos em óleos essenciais.
CI₅₀
Konzentration, bei der 50% der maximalen Hemmung eines Ziels (z.B. Rezeptor, Enzym) erreicht wird.
Sistema límbico
Região do cérebro que processa emoções, memória e motivação; inclui a amígdala, o hipocampo e outras estruturas.
Linalol
Álcool monoterpénico, principal componente ativo da lavanda; exerce efeitos ansiolíticos, sedativos e modula sistemas de neurotransmissores.
Mentol
Álcool monoterpénico da hortelã-pimenta; ativa recetores de frio TRPM8, tem um efeito refrescante e aumenta a atenção.
Metilfenidato (MPH)
Estimulante que inibe a recaptação de dopamina e noradrenalina; terapia de primeira linha para TDAH.
Microdiálise
Técnica para medição de concentrações extracelulares de neurotransmissores no cérebro vivo.
Monoamina
Grupo de neurotransmissores que inclui dopamina, noradrenalina e serotonina.
NET (Transportador de Noradrenalina)
Proteína que transporta a noradrenalina da fenda sináptica de volta para o neurónio; também alvo de metilfenidato.
Neuroinflamação
Processos inflamatórios no cérebro, muitas vezes mediados por microglia ativada e citocinas pró-inflamatórias.
Neurotransmissores
Mensageiros químicos que transmitem sinais entre neurónios (por exemplo, dopamina, serotonina, GABA).
NF-κB (Fator Nuclear kappa B)
Fator de transcrição que ativa genes inflamatórios; a inibição tem um efeito anti-inflamatório.
Recetor NMDA
Recetor de glutamato, importante na plasticidade sináptica e na aprendizagem; a hiperatividade pode ser neurotóxica.
Norepinefrina
Neurotransmissor, importante para a vigília, atenção e resposta ao stress; frequentemente diminuído no TDAH.
Ocupação
Ver DAT-Okkupanz; percentagem de recetores ou transportadores ocupados.
Olfativo
Relativo ao olfato.
PET (Tomografia por Emissão de Positrões)
Técnica de imagem que utiliza substâncias marcadas radioativamente para visualizar processos metabólicos e ligação de receptores no cérebro.
Farmacocinética
Aprenda sobre o que o corpo faz com um medicamento (absorção, distribuição, metabolismo, excreção).
Farmacodinâmica
Aprenda o que um medicamento faz no corpo (mecanismos de ação, efeitos).
Córtex pré-frontal (CPF)
Córtex pré-frontal, importante para funções executivas (planeamento, controlo de impulsos, memória de trabalho); frequentemente hipoativo na TDAH.
receptor
Proteínas em ou nas células, que se ligam a moléculas de sinalização específicas (neurotransmissores, hormonas) e desencadeiam subsequentemente reações celulares.
SERT (transportador de serotonina)
Proteína que transporta a serotonina da fenda sináptica de volta para o neurónio; alvo de antidepressivos (ISRS).
Serotonina
Neurotransmissor, importante para o humor, o sono, o apetite e o controlo dos impulsos.
SPECT (Tomografia Computorizada de Emissão de Fotão Único)
Técnica de imagem semelhante à PET, que utiliza radioisótopos para a representação de funções cerebrais.
Estrado
Região cerebral dos gânglios da base, rica em transportadores de dopamina; importante para o movimento, motivação e recompensa; principal região alvo do metilfenidato.
Sinapse
Sinapse.
Fenda sináptica
Espaço estreito entre dois neurónios na sinapse, para onde são libertados neurotransmissores.
Canais TRP (Potencial de Receptor Transiente)
Família de canais iónicos que respondem a diversos estímulos (temperatura, químicos); por exemplo, TRPM8 (frio/mentol), TRPV1 (calor/capsaicina).
Princípio de Venturi
Princípio físico através do qual, com uma queda de pressão numa constrição, líquidos ou óleos são aspirados e nebulizados; base de muitos difusores.
β-cariofileno
Sesquiterpenos da pimenta preta e da canábis; agonista seletivo do recetor CB2 com propriedades anti-inflamatórias.
1,8-Cineol (Eucaliptol)
Monoterpeno de óxido de alecrim e eucalipto; tem ação expectorante, anti-inflamatória e potenciadora da cognição.
Recetor 5-HT1A
Subtipo de recetor de serotonina; a ativação tem um efeito ansiolítico e antidepressivo.
Fim do relatório
Este relatório foi elaborado em 27 de abril de 2026 com base numa análise sistemática de 87 estudos sobre as concentrações de metilfenidato no cérebro e 159 publicações sobre óleos essenciais no contexto do TDAH. Todas as afirmações são comprovadas por literatura primária.
Glossário TEA
1,8-Cineol (Eucaliptol)
Óxido monoterpénico, componente principal do óleo de eucalipto (70–90 %), demonstra efeitos ansiolíticos através da modulação do recetor GABA-A e propriedades anti-inflamatórias; contraindicado em crianças com menos de 3 anos devido ao risco de laringoespasmo.
α-Pineno
Monoterpeno bicíclico em pinheiros, alecrim e canábis; mostra modulação GABAérgica, efeitos ansiolíticos e anti-inflamatórios; evidência pré-clínica de propriedades neuroprotetoras.
Amígdala
Estrutura cerebral em forma de amêndoa no lobo temporal medial, central para o processamento emocional, condicionamento do medo e perceção social; aumentada em crianças com TSP, com ativação reduzida no processamento de rostos.
Antioxidantes
Molécula que reduz o stress oxidativo através da neutralização de espécies reativas de oxigénio (ROS); exemplos: glutationa, superóxido dismutase, catalase, vitamina C, vitamina E; capacidade antioxidante reduzida em TEA.
Análise Comportamental Aplicada (ABA)
Intervenção terapêutica comportamental baseada em evidências para TSP, com base em princípios de aprendizagem (reforço, modelagem, *shaping*); melhora a comunicação, competências sociais e comportamentos adaptativos.
Aripiprazol
Antipsicótico atípico, agonista parcial de dopamina D2; aprovado pela FDA para irritabilidade em TEA; efeitos secundários: ganho de peso, acatisia, síndrome metabólica; metabolizado via CYP2D6 e CYP3A4.
Astrócitos
Células gliais em forma de estrela no SNC; regulam a homeostase do glutamato (via transportadores EAAT1/2), o tamponamento de K+, a barreira hematoencefálica e o suporte metabólico dos neurónios; na ASD, astrogliose (expressão aumentada de GFAP).
β-cariofileno (BCP)
Hidrocarboneto sesquiterpénico em pimenta preta, cravinho, cannabis; agonista seletivo do recetor CB2 sem efeitos psicoativos; reduz a neuroinflamação, ativação da microglia e stress oxidativo.
Sítio de ligação das benzodiazepinas
Sítio de modulação alostérica no recetor GABA-A; as benzodiazepinas (diazepine, lorazepam) ligam-se aqui e potencializam a inibição gabaérgica; o linalol e o 1,8-cineol interagem com este sítio (sensível ao flumazenil).
Bergamota (Citrus bergamia)
Fruta cítrica, óleo essencial contém linalol, acetato de linalilo, limoneno; um ensaio clínico randomizado em crianças com TEA não mostrou efeitos ansiolíticos significativos; contém bergapteno (inibidor da CYP3A4), variantes sem bergapteno (FCF) disponíveis.
Ácidos boswelicos
Ácidos triterpénicos pentacíclicos de Boswellia (olíbano); ativam a via antioxidante Nrf2/HO-1, reduzem a neuroinflamação (micróglia, astrócitos, TNF-α, IL-6); evidência pré-clínica para a melhoria de comportamentos semelhantes ao TEA em modelos VPA.
Bumetanida
Diurético de alça, inibidor do co-transportador NKCC1; corrige a alteração tardia do "GABA switch" em modelos murinos de TEA; ensaios clínicos demonstram melhorias moderadas na comunicação social em crianças com TEA, mas com limitações metodológicas.
Canfora
Cetona terpénica em cânfora (Cinnamomum camphora) e alecrim (quimiotipo cânfora); diminui o limiar de convulsão, pode desencadear ataques; contraindicado em epilépticos e em pacientes com TEA com epilepsia comórbida.
Cananga odorata (Ylang-Ylang)
Árvore tropical, óleo essencial contém linalol, geraniol, β-cariofileno; estudo pré-clínico demonstrou melhoria em comportamentos semelhantes ao TEA em ratos VPA através da modulação do metabolismo da serotonina e dopamina.
Recetor CB2 (Recetor Cannabinoide Tipo 2)
Recetor acoplado a proteína G, expresso primariamente em células imunitárias (micróglia, células imunitárias periféricas); a ativação reduz a libertação de citocinas, a ativação da micróglia e a neuroinflamação; o β-cariofileno é um agonista seletivo do CB2.
Cedrol
Álcool sesquiterpénico em óleo de cedro; tradicionalmente associado a propriedades sedativas, mas falta evidência científica para mecanismos GABAérgicos ou eficácia clínica em TEA.
Variantes do Número de Cópias (VNCs)
Deleções ou duplicações genómicas >1 kb; frequentes no TEA (duplicação 15q11-13, deleção 16p11.2, deleção 22q13/Síndrome de Phelan-McDermid); afetam genes sinápticos (SHANK3, NLGN4).
Citocromo P450 (CYP)
Família de enzimas que catalisa o metabolismo de medicamentos; CYP3A4 e CYP2D6 metabolizam a risperidona e o aripiprazol; bergapteno (em bergamota) inibe o CYP3A4, podendo aumentar os níveis de medicamentos.
Dopamina (DA)
Neurotransmissor catecolamina; medeia o processamento de recompensa, motivação, controlo motor; na TEA, redução da ativação estriatal para recompensas sociais, densidade alterada do transportador de dopamina; o Ylang-Ylang modula o metabolismo da dopamina em modelos pré-clínicos.
DSM-5 (Manual de Diagnóstico e Estatística de Transtornos Mentais, 5.ª Edição)
Sistema de classificação da Associação Americana de Psiquiatria; define o TEA através de dois domínios principais: (1) défices persistentes na comunicação/interação social, (2) padrões restritos e repetitivos de comportamento.
Disbiose
Desequilíbrio da microbiota intestinal; em ASD, diversidade microbiana reduzida, aumento da proporção Firmicutes/Bacteroidetes, redução de Bifidobacterium e Prevotella; correlacionado com a gravidade dos sintomas.
Desequilíbrio E/I (Desequilíbrio Excitatório-Inibitório)
Desequilíbrio entre a neurotransmissão excitatória (glutamatérgica) e inibitória (GABAérgica); hipótese fisiopatológica central na ASD; leva à hiperexcitabilidade, à filtragem sensorial alterada e ao processamento de informação social prejudicado.
Eletroacupuntura
Acupuntura com estimulação elétrica; estudos pré-clínicos demonstram melhoria de comportamentos semelhantes aos da TEA em ratos VPA através de mecanismos dependentes do nervo vago e modulação do microbioma.
Epilepsia
Neurologische Erkrankung mit rekurrenten Anfällen; 10–30 % der ASD-Patienten haben komorbide Epilepsie; campherhaltige ätherische Öle (Kampfer, Rosmarin-Campher-Chemotyp, Salbei) sind kontraindiziert.
Transplante de Microbiota Fecal (TMF)
Transplante de microbiota intestinal de dadores saudáveis para recetores; estudos pré-clínicos mostram melhoria nos comportamentos semelhantes aos da ASD em modelos de ratinho; estudo clínico aberto em crianças com ASD mostrou melhorias nos sintomas gastrointestinais e no comportamento.
Flumazenil
Antagonista das benzodiazepinas, liga-se ao local de ligação das benzodiazepinas do recetor GABA-A; bloqueia os efeitos ansiolíticos do linalol e do 1,8-cineol, confirmando assim a sua interação com este local.
GABA (ácido γ-aminobutírico)
Neurotransmissor inibitório primário no SNC; liga-se aos recetores GABA-A (ionotrópicos) e GABA-B (metabotrópicos); na TEA, função GABAérgica reduzida, níveis de GABA alterados, alteração do "switch" GABAérgico durante o desenvolvimento.
Recetor GABA-A
Canal de cloreto regulado por ligando; a ativação por GABA leva ao influxo de cloreto e hiperpolarização (inibição); contém um sítio de ligação para benzodiazepinas; o linalol, 1,8-cineol e α-pineno modulam os recetores GABA-A.
GABA-Switch
Transição no desenvolvimento da ação inibitória do GABA de excitatória para inibitória; mediada pela mudança na expressão dos co-transportadores NKCC1 para KCC2; atrasada no TEA; a oxitocina e a bumetanida podem normalizar a mudança do GABA.
GAD65/GAD67 (Descarboxilase do Ácido Glutâmico 65/67)
Enzimas que convertem glutamato em GABA; na TSP, expressão reduzida de GAD65/67 no córtex pré-frontal e cerebelo, levando à síntese reduzida de GABA.
Cromatografia Gasosa-Espectrometria de Massa (GC/MS)
Técnica analítica para identificação e quantificação de componentes voláteis; padrão-ouro para caracterização química de óleos essenciais; permite a deteção de adulterações, contaminantes e variabilidade entre lotes.
Glutamato (Glu)
Neurotransmissor excitatório primário no SNC; liga-se a recetores ionotrópicos (NMDA, AMPA, Kainato) e metabotrópicos (mGluR1-8); no TEA, níveis alterados de glutamato, genes da sinapse glutamatérgica perturbados (GRIN2B, GRIA1), transmissão glutamatérgica excessiva.
Glutationa (GSH)
Tripeptídeo (γ-Glutamílico-Cisteinil-Glicina), antioxidante intracelular primário; em TEA, níveis reduzidos de GSH, aumento do glutationa oxidado (GSSG), redução da razão GSH/GSSG; variantes genéticas em enzimas de síntese de GSH (GCLC, GSS) associadas a TEA.
Eixo Intestino-Cérebro
Comunicação bidirecional entre o trato gastrointestinal e o SNC através de vias neuronais (nervo vago), endócrinas (eixo HPA), imunológicas e metabólicas; na DAC, disbiose, produção alterada de precursores de neurotransmissores, vias de sinalização intestino-cérebro perturbadas.
Heme oxigenase-1 (HO-1)
Enzima que degrada o heme em biliverdina (antioxidante), monóxido de carbono (anti-inflamatório) e ferro; regulada pelo Nrf2; os ácidos boswellicos aumentam a expressão da HO-1; a indução da HO-1 protege contra o stress oxidativo e a neuroinflamação.
Hipocampo
Estrutura cerebral no lobo temporal medial; media a memória declarativa, a navegação espacial, o processamento contextual; no TEA aumento na infância, conectividade alterada, condicionamento de medo contextual perturbado.
Hiperserotoninemia
Aumento dos níveis periféricos de serotonina; detectado em 25-50 % dos doentes com PEA; relação com os níveis centrais de 5-HT pouco clara; possivelmente devido a uma captação deficiente de serotonina nas plaquetas ou a uma síntese periférica aumentada.
Interleucina-6 (IL-6)
Citocina pró-inflamatória; níveis elevados de IL-6 no plasma e LCR na ASD; ativação imune materna com produção de IL-6 produz fenótipos semelhantes à ASD em modelos de ratinho; IL-6 modula a transmissão sináptica e o desenvolvimento.
Cerebelo
Estrutura cerebral no rombencéfalo; tradicionalmente associada ao controlo motor, também desempenha um papel nos processos cognitivos, na previsão sensorial e na aprendizagem social; na PEA, perda de células de Purkinje, redução do volume do vérmis, comprometimento da conetividade cerebelo-cortical.
Lavanda (Lavandula angustifolia)
Planta aromática, óleo essencial que contém 25–45 % de linalol e acetato de linalilo; pequenos estudos-piloto relatam melhoria da conformidade ABA e atenção dividida em crianças com TEA; evidência pré-clínica de modulação GABAérgica, regulação serotoninérgica e ativação oxitocinérgica.
Linalol
Álcool monoterpénico, componente principal de lavanda, coentro, bergamota; modula recetores GABA-A no local de ligação da benzodiazepina (sensível ao flumazenil), afeta os níveis de serotonina, aumenta o cálcio intracelular nos neurónios de ocitocina, demonstra efeitos anti-inflamatórios.
Acetato de linalilo
Estabelecido por linalool e ácido acético; componente principal do lavanda (25–45 %) e bergamota; contribui para efeitos ansiolíticos e sedativos; é hidrolisado a linalool.
Potenciação a Longo Prazo (PLP) / Depressão a Longo Prazo (DLP)
Mecanismos celulares da plasticidade sináptica; LTP: potenciação sináptica sustentada após estimulação de alta frequência; LTD: depressão sináptica sustentada após estimulação de baixa frequência; no TEA desequilíbrio LTP/LTD perturbado em múltiplas regiões cerebrais.
Espectroscopia de Ressonância Magnética (MRS)
Técnica de imagem não invasiva para a quantificação de metabolitos (glutamato, GABA, N-acetilaspartato, creatina) in vivo; na DEAS, a SMR mostra alterações regionais nas concentrações de glutamato e GABA.
Ativação Imunológica Materna (AIM)
Modelo pré-clínico em que as fêmeas prenhes são tratadas com imunoestimulantes (poli(I:C), LPS); a descendência apresenta um comportamento semelhante ao da PEA, aumento das citocinas pró-inflamatórias, desenvolvimento sináptico prejudicado; modelo de fator de risco ambiental para a PEA.
Melatonina
Hormona produzida pela glândula pineal; regula o ritmo circadiano e o sono; em pessoas com Perturbação do Espetro do Autismo (PEA) ocorrem frequentemente perturbações do sono; a suplementação com melatonina melhora a latência e a duração do sono; meta-análises indicam eficácia moderada.
Microglia
Células imunes residentes do SNC; regulam a poda sináptica, o desenvolvimento neuronal, a vigilância imune; microglias ativadas na DEAS (expressão aumentada de Iba1, morfologia ameboide) no córtex pré-frontal, cerebelo; libertam citocinas pró-inflamatórias e ROS.
Disfunção mitocondrial
Função mitocondrial prejudicada (redução da atividade da cadeia respiratória, aumento do lactato, redução da síntese de ATP); em 5-30 % dos doentes com PEA; conduz a um aumento da produção de ROS, stress oxidativo, homeostase do cálcio prejudicada.
Neuroligina (NLGN)
Moléculas de adesão celular pós-sinápticas (NLGN1-4); interagem com neurexinas pré-sinápticas; regulam a diferenciação, maturação e função sinápticas; mutações em NLGN3 e NLGN4X em pacientes com TEA; ratos NLGN3-R451C exibem transmissão inibitória aumentada e fenótipos semelhantes aos do TEA.
Neurexina (NRXN)
Moléculas de adesão celular pré-sinápticas (NRXN1-3); interagem com neurexinas pós-sinápticas; regulam a organização sináptica; mutações em NRXN1 em pacientes com TEA; deleções de NRXN1 associadas a TEA, esquizofrenia e deficiência intelectual.
Neuroinflamação
Reação inflamatória no SNC; caracterizada pela ativação da micróglia e dos astrócitos, aumento das citocinas pró-inflamatórias (TNF-α, IL-6, IL-1β), diminuição da barreira hemato-encefálica; na PEA, neuroinflamação crónica em várias regiões cerebrais.
NF-κB (Fator Nuclear kappa B)
Fator de transcrição que regula os genes pró-inflamatórios (TNF-α, IL-6, IL-1β, COX-2); aumento da ativação do NF-κB na PEA; o β-cariofileno e os ácidos boswelicos inibem as vias de sinalização do NF-κB.
Recetor NMDA (recetor N-metil-D-aspartato)
Recetor de glutamato ionotrópico, canal permeável ao cálcio; central para plasticidade sináptica (LTP/LTD), aprendizagem e memória; expressão alterada da subunidade do recetor NMDA (GRIN2A, GRIN2B) em TEA, função alterada do recetor NMDA em ratos com deleção genética de SHANK2.
Fator nuclear eritroide 2 relacionado com fator 2 (Nrf2)
Fator de transcrição, regulador principal da resposta antioxidante; induz a expressão de HO-1, NQO1, glutatião S-transferases, outras enzimas antioxidantes; os ácidos boswelicos activam o Nrf2; os activadores Nrf2 (sulforafano) revelam melhorias nas PEA em pequenos estudos.
Stress Oxidativo
Desequilíbrio entre a produção de ERO e a defesa antioxidante; na PEA, aumento da peroxidação lipídica, carbonilação de proteínas, oxidação do ADN, redução da capacidade antioxidante (GSH, SOD, catalase); contribui para danos e disfunção neuronal.
Oxitocina (OT)
Neuropeptídeo, produzido no hipotálamo; papel central na ligação social, confiança, cognição social, regulação do stress; em TEA, níveis plasmáticos reduzidos de OT, expressão alterada de OXTR; OT intranasal mostra resultados mistos; OT regula o desenvolvimento gabaérgico em modelos pré-clínicos.
Interneurónios positivos para a parvalbumina
Subtipo de interneurónio GABAérgico, que expressa a proteína de ligação ao cálcio parvalbumina; medeia inibição rápida e síncrona; na TSP, densidade e função reduzidas de interneurónios de parvalbumina no córtex pré-frontal.
Síndrome de Phelan-McDermid
Síndrome genético devido a uma deleção 22q13 que engloba o gene SHANK3; caracterizado por ASD, deficiência intelectual, défices de linguagem, hipotonia; demonstra o papel causal do SHANK3 na patogénese do ASD.
Córtex pré-frontal (CPF)
Região frontal do cérebro; media funções executivas, memória de trabalho, flexibilidade cognitiva, cognição social, Teoria da Mente; no TEA, redução da ativação do córtex pré-frontal (CPF) durante tarefas de cognição social, conectividade do CPF perturbada, défices GABAérgicos.
Propionato
Ácido gordo de cadeia curta, produzido pela microbiota intestinal; níveis potencialmente elevados de propionato na DEAS; exposição ao propionato em modelos de roedores induz comportamentos semelhantes aos da DEAS, neuroinflamação, stress oxidativo.
Espécies reativas de oxigénio (ROS)
Moléculas altamente reativas (superóxido, peróxido de hidrogénio, radical hidroxilo); surgem como subprodutos da respiração mitocondrial; em concentrações excessivas causam danos oxidativos em lípidos, proteínas, ADN por ROS; em TSP produção aumentada de ROS.
Risperidona
Antipsicótico atípico, antagonista da dopamina D2 e da serotonina 5-HT2A; aprovado pela FDA para irritabilidade na TEA; efeitos secundários: ganho de peso, hiperprolactinemia, sintomas extrapiramidais, síndrome metabólica; metabolizado pelo CYP2D6.
Serotonina (5-HT, 5-Hidroxitriptamina)
Monoamina-neurotransmissor; medeia humor, ansiedade, sono, apetite, cognição social; na ASD hiperserotonemia (periférica), síntese reduzida de serotonina central, variantes genéticas em 5-HTT e TPH2; linalol e Ylang-Ylang modulam sistemas serotoninérgicos.
Proteínas SHANK (domínios SH3 e múltiplos domínios anquirina)
Proteínas do andaime pós-sináptico (SHANK1-3); organizam recetores de glutamato, citoesqueleto de actina, moléculas de sinalização; mutações em SHANK2 e SHANK3 em TEA; ratinhos com SHANK3 "knockout" mostram densidade de espinhas reduzida, transmissão sináptica prejudicada, comportamentos semelhantes a TEA.
Estrado
Estrutura subcortical dos gânglios da base (núcleo caudado, putamen, núcleo accumbens); media o processamento de recompensa, a aprendizagem de hábitos, o controlo motor; na TEA, aumento do estriado, redução da ativação em recompensas sociais, conectividade cortico-estriatal perturbada.
Poda sináptica
Processo do desenvolvimento biológico no qual sinapses em excesso são eliminadas; mediado por microglia, sistema complemento; no TEA, a poda pode ser perturbada (demasiada ou insuficiente), levando a densidades sinápticas e conectividade alteradas.
Terpeno
Classe diversa de produtos naturais, construída a partir de unidades de isopreno (C5H8); componentes principais de óleos essenciais; monoterpenos (C10): linalol, 1,8-cineol, α-pineno; sesquiterpenos (C15): β-cariofileno, cedrol; triterpenos (C30): ácidos boswélicos.
FNT-α (Fator de Necrose Tumoral-α)
Citocina pró-inflamatória; níveis elevados de TNF-α no plasma, LCR e tecido cerebral post-mortem em TSA; ativação imunitária materna com aumento de TNF-α produz fenótipos semelhantes aos da TSA; TNF-α modula a transmissão sináptica, reduzindo a inibição GABAérgica.
Proteína Translocadora (TSPO)
Proteína mitocondrial, desregulada em micróglia ativada; Ligantes de PET (por exemplo, [11C]-PBR28) ligam-se à TSPO e permitem a imagem in vivo da ativação da micróglia; na ASD, aumento da ligação à TSPO em múltiplas regiões do cérebro.
Triptofano
Aminoácido essencial, precursor da serotonina e melatonina; no TEA, o metabolismo do triptofano pode estar alterado; a microbiota intestinal influencia a disponibilidade e o metabolismo do triptofano através das vias da quinurenina e da serotonina.
Ácido valproico (VPA)
Antiepileptico; exposição pré-natal a VPA é fator de risco para TEA em humanos; modelo murino de TEA induzido por VPA: ratas grávidas recebem VPA, a prole demonstra comportamentos semelhantes a TEA, neuroinflamação, stress oxidativo; modelo pré-clínico amplamente utilizado.
Princípio de Venturi
Princípio Físico (Efeito de Bernoulli): Redução de pressão num fluido quando este flui através de um estreitamento; no Nebulizador de Aromas Orgânicos 3.0, o ar comprimido através do bico cria um vácuo, que suga o óleo essencial e o pulveriza em finas gotas (nebulização a frio).
Vetiver (Vetiveria zizanioides)
Grama tropical, óleo essencial contém vetiverol, khusimol, α-vetivona; relatos anedóticos de efeitos na atenção e hiperatividade, mas faltam estudos controlados em TEA; evidência científica para mecanismos é insuficiente.
Incenso (Boswellia)
Resina de espécies de Boswellia; óleo essencial e extratos contêm ácidos boswellicos; evidência pré-clínica para efeitos anti-neuroinflamatórios, antioxidantes (Nrf2/HO-1) e neuroprotetores; nenhum ensaio clínico em RDC identificado.
Madeira de cedro (Cedrus atlantica, Juniperus virginiana)
O óleo essencial contém Cedrol, α-Cedreno, Tujopseno; tradicionalmente usado para sedação e redução da ansiedade, mas falta evidência científica para mecanismos GABAérgicos ou eficácia clínica em TDA.
Ritmo circadiano
Ritmo endógeno de ~24 horas, regula o ciclo sono-vigília, secreção hormonal, temperatura corporal; nos TEA, ritmos circadianos frequentemente perturbados, perturbações do sono; a melatonina regula o ritmo circadiano e melhora o sono nos TEA.