Inhaltsverzeichnis
Welche Rolle Ätherische Öle im Vergleich zu Standard-Pharmaka bei Depression spielen, wie die Wirkung begründet ist und welche adjuvanten Aspekte sie bieten wird in diesem Beitrag ausführlich dargestellt.
Der erste Teil ist eine laienverständliche Kurzfassung des im zweiten Teil nachfolgenden wissenschaftlichen Berichts für alle, die mehr über natürliche Unterstützung bei Depression erfahren möchten.
Im zweiten Teil finden Mediziner, Behandler und medizinisch-wissenschaftlich Interessierte einen umfassender wissenschaftlichen Bericht zu Standard-Antidepressiva, Terpenen und ätherischen Ölen, molekulare Grundlagen, klinischer Evidenz und adjuvanter Therapiestrategien, mit, meist Peer-Review-, Studien belegt.
Was ist Depression?
Depression ist mehr als nur “Traurigkeit” oder ein schlechter Tag. Sie ist eine echte Erkrankung des Gehirns, bei der bestimmte Botenstoffe (Chemikalien, die Nervenzellen miteinander kommunizieren lassen) aus dem Gleichgewicht geraten. Stellen Sie sich das Gehirn wie ein komplexes Kommunikationsnetz vor: bei Depression funktionieren einige Verbindungen nicht mehr richtig.
Was passiert im Gehirn bei Depression?
- Serotonin, Noradrenalin und Dopamin, die sogenannten “Glücksbotenstoffe”, sind zu niedrig oder werden nicht richtig genutzt
- Das Stresssystem des Körpers (die sogenannte HPA-Achse) ist dauerhaft überaktiviert, als wäre man ständig in Alarmbereitschaft
- Bestimmte Gehirnbereiche, die für Freude und Motivation zuständig sind (wie das limbische System), arbeiten gedämpft
- Chronische Entzündungsprozesse im Gehirn können die Stimmung verschlechtern
Wie häufig ist Depression?
Depression betrifft weltweit etwa 280 Millionen Menschen, also 3,8 % der Weltbevölkerung. In Deutschland leiden rund 5 Millionen Menschen an einer behandlungsbedürftigen Depression. Es ist eine der häufigsten Erkrankungen überhaupt.
Wie werden Depressionen normalerweise behandelt?
Antidepressiva – die Standard-Medikamente
Ärzte verschreiben bei Depression häufig Medikamente, die die Botenstoffe im Gehirn beeinflussen. Die bekanntesten sind:
SSRIs (Selektive Serotonin-Wiederaufnahmehemmer)
z.B. Fluoxetin (Prozac), Sertralin, Escitalopram
Sie verhindern, dass Serotonin zu schnell “aufgeräumt” wird, dadurch bleibt mehr davon im Gehirn verfügbar. Die Wirkung setzt erst nach 2–4 Wochen ein. Nebenwirkungen sind u.a. Übelkeit, Schlafstörungen, sexuelle Funktionsstörungen und Gewichtszunahme.
SNRIs (Serotonin-Noradrenalin-Wiederaufnahmehemmer)
z.B. Venlafaxin, Duloxetin
Sie wirken gleichzeitig auf zwei Botenstoffe, nämlich Serotonin und Noradrenalin, zeichnen sich besonders gut bei Depressionen mit körperlichen Schmerzen aus.
Wichtig zu wissen: Antidepressiva helfen bei etwa 50–60 % der Patienten ausreichend. Bei 30–40 % wirken sie nicht gut genug oder verursachen störende Nebenwirkungen. Das ist der Grund, warum viele Menschen nach ergänzenden Möglichkeiten suchen.
Ätherische Öle – was sind das eigentlich?
Ätherische Öle sind hochkonzentrierte Pflanzenextrakte. Sie werden durch Dampfdestillation oder Kaltpressung aus Blüten, Blättern, Rinden oder Wurzeln von Pflanzen gewonnen. Sie enthalten hunderte verschiedener chemischer Verbindungen (sogenannte Terpene und Phenole), die der Pflanze ihren Duft und ihre Eigenschaften verleihen und sie vor Fressfeinden, Befall von Bakterien, viren oder Pilzen schützen. Diese Wirkstoffe stellen quasi das Immunsystem der Pflanze dar.
Anders als gegen bestimmte Bakterien, Viren oder Pilze wirksame Pharmazeutika, gegen die sich Restistenzen entwickeln und die Erreger so, selbst bei Breitband-Antibiotika, nicht mehr wirksam bekämpft werden können, bestehen die pflanzlichen Wirkstoffe der ätherischen Öle aus so vielen „Antibiotika“, etc., dass Resistenzen nicht mehr möglich sind.
Das erklärt auch, weshalb ätherische Öle selbst gegen den multiresistenten „Krankenhauskeim“ (MRSA) wirksam sind.
Wie kommen sie ins Gehirn?
Wenn Sie an einem ätherischen Öl riechen, gelangen die Duftmoleküle direkt über die Nase zum Riechnerv. Dieser hat eine direkte Verbindung zum limbischen System, dem emotionalen Zentrum des Gehirns. Das ist der schnellste Weg, über den ein Wirkstoff das Gehirn beeinflussen kann, schneller als jedes Medikament, das erst verdaut werden muss und dadurch bereits an Wirksamkeit verliert und zusätzlich noch alle an der Verstoffwechselung beteiligten Organe belastet.
Manche Verbindungen aus ätherischen Ölen können auch über die Haut (topisch) oder durch Einatmen (olfaktorisch) ins Blut gelangen und so systemisch, also im ganzen Körper, wirken.
Welche ätherischen Öle können bei Depression helfen?
Lavendel – das am besten erforschte Stimmungsöl
Lavendel (Lavandula angustifolia) ist das einzige ätherische Öl, das in klinischen Studien mit einem echten Antidepressivum verglichen wurde und gut abschnitt.
- Was ist drin? Hauptsächlich Linalool (ca. 25–45 %) und Linalylacetat (ca. 25–50 %)
- Was macht es? Linalool beeinflusst denselben Rezeptor (GABA-A), den auch Beruhigungsmittel (Benzodiazepine) ansprechen, aber sanfter und ohne Suchtgefahr
- Klinische Studie: Das Lavendelöl-Präparat “Silexan” (80 mg täglich, als Kapsel) war in einer Studie genauso wirksam wie Sertralin (ein häufig verschriebenes Antidepressivum) und bei deutlich weniger Nebenwirkungen
- Wie anwenden? Aromadiffusor, Massage, oder als Kapsel (Silexan ist als Medizinprodukt erhältlich)
Bergamotte – der Stimmungsaufheller
Bergamotte (Citrus bergamia) ist die Zitrusfrucht, die dem Earl-Grey-Tee seinen Duft gibt.
- Was ist drin? Limonene, Linalool, Bergapten
- Was macht es? Erhöht Serotonin und Dopamin, reduziert Kortisol (das Stresshormon) um bis zu 46 % in Studien
- Studien: Aromatherapie mit Bergamotte reduzierte Angstzustände signifikant bei Patienten vor Operationen und in psychiatrischen Einrichtungen
- Achtung: Bergaptol macht die Haut lichtempfindlich, bergaptenfreie Varianten für die Haut verwenden oder Soneneinwirkung meiden!
Kamille – die sanfte Beruhigung
Kamille (Matricaria chamomilla) ist eines der ältesten Heilkräuter der Welt.
- Was ist drin? Apigenin (ein Flavonoid), Bisabolol, Chamazulen
- Was macht es? Apigenin bindet an die gleichen Stellen im Gehirn wie Benzodiazepine (Beruhigungsmittel), aber viel milder
- Klinische Studie: In einer randomisierten Studie reduzierte Kamillenextrakt Depressionssymptome signifikant (p < 0,001) und verhinderte bei 57 % der Patienten einen Rückfall
Melisse – Stress und Schlaf
Melisse (Melissa officinalis) riecht nach Zitrone und wird seit Jahrhunderten gegen Nervosität eingesetzt.
- Was ist drin? Rosmarinsäure, Citral, Geraniol
- Was macht es? Hemmt ein Enzym (GABA-Transaminase), das GABA abbaut , wodurch mehr des beruhigenden Botenstoffs im Gehirn verbleibt
- Studie: 300–600 mg Melissenextrakt täglich verbesserte Stimmung und kognitive Funktion signifikant
Weihrauch – gegen Entzündungen und Angst
Weihrauch (Boswellia sacra / serrata) wird seit Jahrtausenden in religiösen Ritualen verwendet, und die Wissenschaft erklärt jetzt warum.
- Was ist drin? Incensol, α-Pinen, Boswelliasäuren
- Was macht es? Aktiviert einen speziellen Rezeptor (TRPV3) im Gehirn, der Angst und Depression lindern kann; hemmt Entzündungen im Gehirn
- Besonderheit: Weihrauch ist eines der wenigen ätherischen Öle mit direkter antidepressiver Wirkung im Tiermodell
Rosenöl, Ylang-Ylang, Jasmin
Diese Öle werden häufig in der Aromatherapie eingesetzt und zeigen in Studien: – Rosenöl: Reduziert Kortisol, verbessert Schlaf, anxiolytisch – Ylang-Ylang: Senkt Blutdruck und Herzrate, reduziert Angst – Jasmin: Stimulierend und stimmungsaufhellend, aktiviert das Nervensystem positiv
Was sagt die Wissenschaft? – Einfach zusammengefasst
Wichtige Hinweise für die Anwendung
So können Sie ätherische Öle sicher anwenden:
- Aromadiffusor: 3–5 Tropfen ins Wasser, 30–60 Minuten in einem belüfteten Raum
- Inhalation: 2 Tropfen auf ein Taschentuch, tief einatmen
- Massage: Immer mit einem Trägeröl verdünnen (z. B. Mandelöl), niemals pur auf die Haut!
- Empfohlene Verdünnung: 2–3 % (ca. 10–15 Tropfen auf 50 ml Trägeröl)
- Bad: 5–10 Tropfen in einem Esslöffel Sahne oder Honig lösen, dann ins Badewasser
Was Sie beachten müssen:
- Niemals innerlich anwenden ohne ärztliche Beratung
- Niemals Antidepressiva eigenmächtig absetzen, das kann gefährlich sein
- Ätherische Öle sind eine Ergänzung, kein Ersatz für professionelle Behandlung
- Bei Schwangerschaft und Stillzeit: Arzt fragen
- Manche Öle (Bergamotte, Zitrus) machen die Haut lichtempfindlich, nicht in die Sonne gehen
- Kinder unter 3 Jahren: Keine ätherischen Öle ohne Fachberatung
- Epileptiker: Vorsicht mit Rosmarin, Eukalyptus und hohen Dosen Kampher
Häufig gestellte Fragen
Kann ich Lavendelöl statt meines Antidepressivums nehmen?
Nein, nicht ohne Rücksprache mit Ihrem Arzt. Lavendel kann als Ergänzung sinnvoll sein, aber ein plötzliches Absetzen von Antidepressiva kann zu ernsthaften Entzugserscheinungen führen.
Wie schnell wirken ätherische Öle?
Manche Wirkungen (Entspannung, Stimmungsaufhellung) können schon nach Minuten eintreten. Langfristige antidepressive Effekte benötigen regelmäßige Anwendung über Wochen.
Welches Öl soll ich zuerst ausprobieren?
Lavendel ist die erste Wahl, am besten erforscht, sicher, und für die meisten Menschen gut verträglich.
Muss ich teure Öle kaufen?
Qualität ist wichtig: Achten Sie auf 100 % naturreine ätherische Öle, am besten mit chargenspezifischem Analyse-Zertifikat (GC/MS).
Günstige Parfümöle oder synthetische Duftstoffe haben keine therapeutische Wirkung und sind auf Grund der synthetischen Inhaltsstoffe u.U. gesundheitlich schädlich und verursachen Kopfschmerzen, Übelkeit, etc..
Wer mehr über die Auswahl und Qualität ätherischer Öle erfahren möchte, der wird in dem Beitrag „Ätherische Öle – Odysse einer Suche“ fündig.
Ein weiterer Beitrag zitiert Prof. Dr. Dr. Dr. med. habil. Hanns Hatt von der Ruhr-Universität Bochum, der in seinem Video „Heilen mit Düften“ auf interessante, kurzweilige und dennoch wissenschaftliche Weise die Wirkung ätherischer Öle auf den menschlichen Körper erklärt.
Zusammenfassung in drei Sätzen
- Depression ist eine Erkrankung des Gehirns, bei der Botenstoffe und das Stresssystem aus dem Gleichgewicht geraten.
- Ätherische Öle, besonders Lavendel, Bergamotte und Kamille, können das Gehirn direkt über den Geruchssinn beeinflussen und haben in wissenschaftlichen Studien nachweislich stimmungsaufhellende, angstlösende und entzündungshemmende Wirkungen gezeigt.
- Sie sind eine wertvolle Ergänzung zur Standardtherapie, ersetzen diese aber nicht.
Dieser Text basiert auf dem wissenschaftlichen Bericht “Depression und Ätherische Öle: Pharmakologie, Wirkmechanismen und komplementäre Therapieansätze” und dient ausschließlich der allgemeinen Information.
Bei Beschwerden wenden Sie sich bitte an einen Arzt oder Apotheker.
Pharmakologie, Wirkmechanismen und komplementäre Therapieansätze
Ein umfassender wissenschaftlicher Bericht zu Standard-Antidepressiva, Terpenen und ätherischen Ölen, molekulare Grundlagen, klinische Evidenz und adjuvante Therapiestrategien
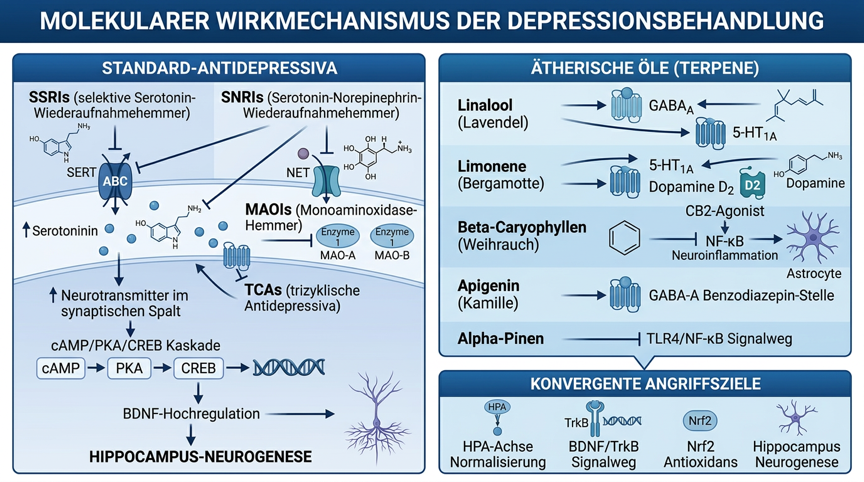
Abbildung 1: Molekulare Signalwege der Antidepressiva und ätherischen Öle bei Depression, Standard-Antidepressiva-Mechanismen (SSRIs, SNRIs, TCAs, MAOIs), Terpene-Wirkmechanismen (Linalool, Limonene, β-Caryophyllen, Apigenin, α-Pinen) und konvergente Angriffsziele (HPA-Achse, BDNF/TrkB, Nrf2, Hippocampus-Neurogenese)
Einleitung
Die Depression (Major Depressive Disorder, MDD) gehört zu den häufigsten und belastendsten psychiatrischen Erkrankungen weltweit. Nach Angaben der Weltgesundheitsorganisation (WHO) leiden über 280 Millionen Menschen an Depression, sie ist eine der führenden Ursachen für Behinderung und verlorene Lebensjahre [D1]. Die Erkrankung ist charakterisiert durch anhaltende depressive Stimmung, Anhedonie, kognitive Beeinträchtigungen, Schlafstörungen, Antriebslosigkeit und in schweren Fällen Suizidalität [D2].
Die Standardbehandlung der Depression umfasst Psychotherapie (insbesondere kognitive Verhaltenstherapie) und Pharmakotherapie mit Antidepressiva. Zu den am häufigsten verordneten Substanzklassen zählen selektive Serotonin-Wiederaufnahmehemmer (SSRIs), Serotonin-Noradrenalin-Wiederaufnahmehemmer (SNRIs), trizyklische Antidepressiva (TCAs) und Monoaminooxidase-Hemmer (MAOIs) [D3]. Trotz ihrer Wirksamkeit sprechen 30–40 % der Patienten nicht auf die erste Behandlungslinie an, und Nebenwirkungen wie sexuelle Dysfunktion, Gewichtszunahme, Schlafstörungen und emotionale Abstumpfung beeinträchtigen die Therapieadhärenz erheblich [D4].
Vor diesem Hintergrund wächst das wissenschaftliche und klinische Interesse an komplementären und pflanzlichen Ansätzen. Ätherische Öle und ihre bioaktiven Terpene zeigen in präklinischen und klinischen Studien antidepressive, anxiolytische, neuroprotektive und anti-neuroinflammatorische Eigenschaften, oft über Wirkmechanismen, die sich komplementär zu klassischen Antidepressiva verhalten [D5]. Dieser Bericht analysiert systematisch die Pharmakologie der Standard-Antidepressiva, die molekularen Wirkmechanismen relevanter ätherischer Öle und Terpene sowie die verfügbare klinische Evidenz für deren adjuvanten Einsatz bei Depression.
Neurobiologie der Depression
Monoamin-Hypothese und ihre Grenzen
Die klassische Monoamin-Hypothese der Depression postuliert, dass eine funktionelle Insuffizienz von Serotonin (5-HT), Noradrenalin (NA) und Dopamin (DA) in zentralen synaptischen Spalten die Kernsymptome der Depression verursacht [D3]. Diese Hypothese bildet die rationale Grundlage für die meisten pharmakologischen Interventionen. Jedoch erklärt sie nicht vollständig das verzögerte Ansprechen auf Antidepressiva (2–4 Wochen), obwohl die Transporter-Blockade innerhalb von Stunden einsetzt, was auf nachgelagerte neuroplastische Adaptationsprozesse als eigentliche Wirkgrundlage hinweist [D6].
Neuroinflammation und HPA-Achse
Neuere Forschung betont die Rolle von Neuroinflammation und Dysregulation der Hypothalamus-Hypophysen-Nebennierenrinden-Achse (HPA-Achse) in der Pathophysiologie der Depression. Erhöhte Spiegel pro-inflammatorischer Zytokine (IL-6, TNF-α, IL-1β) und eine Hyperaktivität der HPA-Achse mit konsekutiv erhöhten Kortisol-Spiegeln sind bei depressiven Patienten gut dokumentiert [D7]. Diese Befunde eröffnen neue therapeutische Angriffspunkte, die über klassische Monoamin-Systeme hinausgehen, und erklären, warum Substanzen mit anti-neuroinflammatorischen Eigenschaften wie bestimmte Terpene klinisch relevant sein können.
BDNF und Neuroplastizität
Der neurotrophe Faktor BDNF (Brain-Derived Neurotrophic Factor) spielt eine zentrale Rolle in der Neuroplastizitäts-Hypothese der Depression. Reduzierte BDNF-Spiegel im Hippocampus und präfrontalen Kortex wurden konsistent bei depressiven Patienten nachgewiesen; alle wirksamen Antidepressiva-Klassen erhöhen BDNF-Expression über verschiedene Signalwege [D8]. Die Förderung von Hippocampus-Neurogenese und synaptischer Plastizität gilt heute als gemeinsamer Endpunkt vieler antidepressiver Interventionen.
Glutamaterge und GABAerge Systeme
Die E/I-Balance (Exzitation/Inhibition) zwischen Glutamat und GABA ist bei Depression gestört. Ketamin, ein NMDA-Rezeptor-Antagonist, zeigt rapide antidepressive Effekte und hat das Interesse an glutamatergen Mechanismen verstärkt [D9]. GABAerge Defizite, insbesondere reduzierte Parvalbumin-positive Interneuron-Aktivität, tragen zu kognitiven Symptomen bei. Diese Befunde sind besonders relevant für ätherische Öle, deren Hauptkomponenten (z.B. Linalool, Apigenin) direkt GABAerge Systeme modulieren.
Pharmakologie der Standard-Antidepressiva
Selektive Serotonin-Wiederaufnahmehemmer (SSRIs)
SSRIs sind die am häufigsten verordneten Antidepressiva weltweit. Ihre primäre Wirkung besteht in der hochselektiven Blockade des Serotonin-Transporters (SERT), was zu erhöhten synaptischen 5-HT-Spiegeln führt [D10].
Wichtige SSRIs und ihre Eigenschaften:
Transporter-Okkupanz und Hirnkonzentrationen
Entscheidend für die In-vivo-Wirksamkeit ist nicht die Gesamthirnkonzentration, sondern die freie (ungebundene) Hirnkonzentration, die mit der SERT-Okkupanz korreliert [D11]. Studien zeigen, dass die SERT-Okkupanz bei therapeutischen Dosen ~80 % beträgt, ein Schwellenwert, der für klinische Wirksamkeit erforderlich zu sein scheint [D12]. Aktive Metaboliten wie Norfluoxetin (nach Fluoxetin) können die SERT-Hemmung verlängern und extrazelluläres 5-HT im frontalen Kortex erhöhen [D13].
Nachgelagerte Signalwege
Chronische SERT-Blockade → ↑ synaptisches 5-HT → Desensitisierung präsynaptischer 5-HT1A-Autorezeptoren → verstärkte postsynaptische Serotonin-Signalgebung → Aktivierung von cAMP/PKA/CREB-Kaskade → ↑ BDNF-Expression → Hippocampus-Neurogenese [D8].
Serotonin-Noradrenalin-Wiederaufnahmehemmer (SNRIs)
SNRIs hemmen sowohl SERT als auch den Noradrenalin-Transporter (NET) und bieten damit ein breiteres Wirkprofil, das besonders bei Depression mit somatischen Schmerzsymptomen vorteilhaft ist [D14].
Trizyklische Antidepressiva (TCAs)
TCAs gehören zu den ältesten Antidepressiva und zeigen ein breites Rezeptorprofil: Hemmung von SERT und NET plus antagonistische Wirkung an Histamin-H1-, muskarinischen und α1-adrenergen Rezeptoren [D16]. Dieses Profil erklärt sowohl die antidepressive Wirksamkeit als auch die erheblichen Nebenwirkungen (Sedierung, anticholinerge Effekte, kardiotoxisches Potenzial).
Wichtige TCAs
Amitriptylin, Clomipramin, Imipramin, Nortriptylin. Clomipramin zeigt die stärkste SERT-Affinität aller TCAs und ist das Mittel der Wahl bei Zwangsstörungen [D16].
Monoaminooxidase-Hemmer (MAOIs)
MAOIs hemmen die Enzyme MAO-A (bevorzugt 5-HT, NA) und/oder MAO-B (bevorzugt DA, Phenylethylamin), was zu erhöhten synaptischen Monoamin-Spiegeln führt [D17]. Irreversible MAOIs (Phenelzin, Tranylcypromin) erfordern strenge Diät-Einschränkungen (Tyramin-arme Kost) wegen des hypertensiven Krise-Risikos. Reversible, selektive MAO-A-Hemmer (Moclobemid) sind besser verträglich.
Neuere Antidepressiva
Mirtazapin
Noradrenerges und spezifisch serotonerges Antidepressivum (NaSSA); blockiert präsynaptische α2-Autorezeptoren und 5-HT2/5-HT3-Rezeptoren. Ausgeprägte sedierende und appetitstimulierender Wirkung [D18].
Bupropion
Dopamin- und Noradrenalin-Wiederaufnahmehemmer (DNRI); besonders geeignet bei Depression mit Antriebsmangel, auch zugelassen zur Raucherentwöhnung [D18].
Agomelatin
Melatonin-MT1/MT2-Agonist und 5-HT2C-Antagonist; normalisiert zirkadiane Rhythmen; günstigeres Nebenwirkungsprofil [D18].
Esketamin (Spravato): NMDA-Rezeptor-Antagonist; zugelassen für therapieresistente Depression; zeigt rapide antidepressive Wirkung innerhalb von Stunden [D9].
Ätherische Öle als adjuvante Therapie – Mechanistische Grundlagen
Olfaktorische und limbische Verarbeitung
Ätherische Öle wirken primär über den olfaktorischen Weg: Inhalierte Terpene binden an Riechrezeptoren im Riechepithel → olfaktorische Nerven → Bulbus olfactorius → limbisches System (Amygdala, Hippocampus, präfrontaler Kortex), Regionen, die direkt in Emotionsregulation, Gedächtnis und Stimmung involviert sind [D19]. Dieser direkte Zugang zum limbischen System ohne Blut-Hirn-Schranken-Passage ermöglicht eine schnelle zentralnervöse Wirkung.
Nose-to-Brain-Delivery: Neuere Forschung belegt, dass Monoterpene über nasale Applikation direkt ins Gehirn gelangen können, was neue Formulierungsstrategien für antidepressiv wirksame Terpene eröffnet [D20].
Pharmakologische Zielstrukturen
Ätherische Öle und ihre Terpene interagieren mit einem breiten Spektrum molekularer Zielstrukturen, die in der Pathophysiologie der Depression relevant sind:
Komplementäre Wirkmechanismen zu Antidepressiva
Die Plausibilität einer adjuvanten Therapie mit ätherischen Ölen basiert auf komplementären, nicht-redundanten Wirkmechanismen. Während klassische Antidepressiva primär auf Monoamin-Transporter (SERT, NET) oder MAO-Enzyme wirken, adressieren ätherische Öle und Terpene zusätzliche Pathomechanismen der Depression: GABAerge Dysfunktion, HPA-Achsen-Hyperaktivität, Neuroinflammation und oxidativen Stress [D5].
Synergistische Ansatzpunkte:
- SSRI + Linalool (Lavendel): SSRIs erhöhen synaptisches 5-HT durch SERT-Blockade; Linalool aktiviert zusätzlich 5-HT1A-Rezeptoren und moduliert GABA-A – ergänzende Reduktion von Angstsymptomen, die oft mit Depression komorbid sind [D21]
- SNRI + β-Caryophyllen: SNRIs normalisieren Monoamin-Spiegel; β-Caryophyllen hemmt als CB2-Agonist NF-κB-vermittelte Neuroinflammation – adressiert den inflammatorischen Subtyp der Depression [D22]
- TCA + Bergamotte: TCAs blockieren multiple Rezeptoren; Limonene aus Bergamotte aktiviert 5-HT1A und moduliert Dopamin-D2 – potenzielle Verstärkung der antidepressiven Wirkung [D23]
Spezifische ätherische Öle und klinische Evidenz
Lavendel (Lavandula angustifolia)
Lavendel ist das am besten untersuchte ätherische Öl in der Psychiatrie. Das standardisierte orale Lavendelöl-Präparat Silexan (80 mg/Tag) wurde in einer multizentrischen, doppelblinden RCT direkt mit Sertralin (50 mg/Tag) und Placebo verglichen [D24]:
- Primärer Endpunkt (MADRS-Reduktion): Silexan −12,1 Punkte vs. Sertralin −12,6 Punkte vs. Placebo −9,95 Punkte
- Responder-Rate: ~53–54 % (Silexan und Sertralin) vs. 41,5 % (Placebo)
- Remissionsrate: ~44–45 % (aktive Arme) vs. 32,6 % (Placebo)
- Schlussfolgerung: Silexan zeigte statistisch signifikante Überlegenheit gegenüber Placebo und keine signifikante Differenz zu Sertralin auf dem primären Endpunkt [D24]
Hauptwirkstoffe
Linalool (25–45 %)
Linalylacetat (25–46 %)
Terpinen-4-ol, Ocimen
Molekulare Mechanismen
– Modulation monoaminerger und neuroendokriner Systeme [D25]
– GABA-A-Rezeptor-Modulation (anxiolytisch) [D21]
– 5-HT1A-Aktivierung (antidepressiv) [D21]
– HPA-Achsen-Normalisierung (Kortisol-Reduktion) [D25]
– Anti-neuroinflammatorisch, antioxidativ [D25]
– BDNF-Hochregulation in Tiermodellen [D25]
Klinische Studien
– Silexan vs. Lorazepam (RCT): vergleichbare anxiolytische Wirksamkeit, besser verträglich [D26]
– Lavendel als Adjuvans zu Venlafaxin: kein signifikanter Zusatznutzen über Placebo hinaus in einer Studie [D27]
– Inhalation bei postpartaler Depression: signifikante EPDS-Reduktion vs. Kontrolle [D28]
Bergamotte (Citrus bergamia)
Hauptwirkstoffe
Limonene (ca. 30 %)
Linalylacetat (ca. 30 %)
Linalool (ca. 12 %)
furanocumarinhaltige Bergapten
In der Aromatherapie wird Bergamotte traditionell bei Depression und Angst eingesetzt [D29].
Molekulare Mechanismen
– Limonene: Aktivierung von 5-HT1A-Rezeptoren, Dopamin-D2-Modulation, BDNF-Hochregulation, HPA-Normalisierung in chronischen Stress-Modellen [D30]
– Linalool: GABAerge und serotoninerge Modulation (s.o.)
– Bergapten: MAO-Hemmung (in vitro) [D29]
– Anti-neuroinflammatorisch: Reduktion hippocampaler IL-6 und TNF-α in Tiermodellen [D29]
Klinische Evidenz
– Inhalation bei psychiatrischen Patienten: signifikante Reduktion von Angst und positiver Stimmungseffekt [D31]
– Bergamotte-Aromatherapie vor Operationen: signifikante Anxiolyse vs. Kontrolle [D31]
Kamille (Matricaria chamomilla / Chamaemelum nobile)
Hauptwirkstoffe
Apigenin (Flavonoid)
α-Bisabolol
Chamazulen
Matricin.
Apigenin ist ein potenter Ligand am GABA-A-Benzodiazepin-Bindungsort [D32].
Molekulare Mechanismen
– Apigenin: GABA-A-Benzodiazepin-Stelle → anxiolytisch, sedierend (ähnlich Benzodiazepinen, aber ohne Abhängigkeitspotenzial) [D32]
– α-Bisabolol: Anti-inflammatorisch, neuroprotektiv
– Chamazulen: COX-Hemmung, anti-neuroinflammatorisch [D32]
– HPA-Achsen-Modulation: Reduktion von Kortisol-Ausschüttung in Stressmodellen
Klinische Evidenz
– Kamille-Extrakt (220 mg/Tag, 8 Wochen) vs. Placebo bei GAD: signifikante Reduktion des HAM-A-Scores (p<0,001) [D33]
– Langzeit-RCT (26 Wochen): Kamille-Extrakt reduzierte Rückfallrate bei Remittenten [D33]
– Antidepressive Wirkung in Tiermodellen: vergleichbar mit Imipramin in Forced-Swim-Test [D32]
Melisse (Melissa officinalis)
Hauptwirkstoffe
Citral
Citronellal
Geraniol
Rosmarin-Säure
Die Pflanze hat eine lange Tradition in der Behandlung von Angst und Depression [D34].
Molekulare Mechanismen
– MAO-A und MAO-B-Hemmung (Rosmarinsäure, Ursol-Säure) [D34]
– GABA-Transaminase-Hemmung → erhöhte GABA-Spiegel [D34]
– Acetylcholinesterase-Hemmung (kognitive Förderung) [D34]
– Antioxidativ: Nrf2-Aktivierung, Reduktion oxidativen Stresses [D34]
Klinische Evidenz
– 8-Wochen-RCT: Melissa officinalis vs. Lavandula vs. Fluoxetin (n=45): ähnliche HAM-D-Reduktionen in allen drei Armen [D35]
– Melisse-Extrakt bei leichter bis mittelschwerer Depression: signifikante Verbesserung vs. Placebo in mehreren Studien [D34]
Weihrauch (Boswellia sacra / B. serrata)
Hauptwirkstoffe
Incensolacetat
α-Pinen
Limonen
Boswelliasäuren
Incensolacetat aktiviert TRPV3-Kanäle und zeigt anxiolytische und antidepressive Effekte in Tiermodellen [D36].
Molekulare Mechanismen
– Incensolacetat: TRPV3-Aktivierung → anxiolytisch, antidepressiv in Mausmodellen [D36]
– Boswelliasäuren: 5-Lipoxygenase-Hemmung → anti-neuroinflammatorisch
– α-Pinen: TLR4/MYD88/NF-κB-Hemmung → anti-neuroinflammatorisch [D37]
– Serotoninerge Modulation: Erhöhung hippocampaler 5-HT-Spiegel in Tiermodellen [D36]
Ylang-Ylang (Cananga odorata)
Hauptwirkstoffe
Benzylacetat
Linalool
Geranylacetat
β-Caryophyllen
Es wird traditionell bei Angst, Depression und emotionalem Stress eingesetzt [D38].
Molekulare Mechanismen
– Linalool-Komponente: GABA-A und 5-HT1A (s.o.)
– β-Caryophyllen: CB2-Agonismus, NF-κB-Hemmung, sedierend-anxiolytisch: Reduktion von Herzfrequenz und Blutdruck in Humanstudien [D38]
– Stimmungsaufhellend: signifikante Erhöhung von Selbstberichten über Entspannung und Wohlbefinden [D38]
Bergamotte-Minze und Neroli (Citrus aurantium)
Neroli-Öl enthält Linalool (ca. 34 %), Linalylacetat (ca. 6 %), Limonene, Nerolidol und Geraniol [D39].
Molekulare Mechanismen
– Linalool/Linalylacetat: GABA-A und 5-HT1A
– Nerolidol: Anxiolytisch in Tiermodellen, potenziert Pentobarbital-Sedierung
Klinische Evidenz
– Neroli-Inhalation bei Intensivpatienten: signifikante Reduktion von Angst und Blutdruck [D39]
– Neroli bei Wechseljahresbeschwerden: signifikante Verbesserung von Depressivität und Sexualfunktion [D39]
Klary-Salbei (Salvia sclarea)
Hauptwirkstoffe
Linalylacetat (60–70 %)
Linalool (10–25 %)
Sclareol
α-Terpineol [D40].
Molekulare Mechanismen
– Linalylacetat: GABAerg, serotoninerge Modulation
– Antidepressive Wirkung: Inhalation von Klary-Salbei erhöhte Dopamin-Spiegel und reduzierte Kortisol in Humanstudien [D40]
– 5α-Reduktase-Hemmung durch Sclareol: hormonelle Modulation relevant für postpartale und perimenopausale Depression [D40]
Rosenöl (Rosa damascena)
Hauptwirkstoffe
Citronellol (18–55 %)
Geraniol (10–22 %), Nerol, Rosoxide und Phenylethylalkohol [D41].
Molekulare Mechanismen
– Phenylethylalkohol: MAO-Hemmung, Dopamin-Freisetzung
– Geraniol: 5-HT1A-Agonismus in Docking-Studien [D41]
Klinische Evidenz
– Rosenöl-Inhalation bei postpartaler Depression: signifikante EPDS-Reduktion vs. Kontrolle [D41]
– Rosenöl-Fußbad: Reduktion von Angst und Depressivität bei Wöchnerinnen [D41]
Jasmin (Jasminum grandiflorum / officinale)
Jasminöl enthält Benzylacetat (ca. 25 %), Linalool, Benzylbenzoat und Indol [D42].
Molekulare Mechanismen
– Benzylacetat: stimulierend, stimmungsaufhellend
– Linalool: GABA-A, 5-HT1A
– Aktivierende Wirkung: Jasmin-Inhalation erhöhte β-Wellen-Aktivität im EEG (Wachheit, positive Stimmung), Gegenteil der sedierenden Lavendel-Wirkung [D42]
– Jasmin als Adjuvans: Kombiniert mit Lavendel für ausgewogene anxiolytisch-aktivierende Wirkung [D42]
Sandelholz (Santalum album / spicatum)
Hauptwirkstoffe
α-Santalol (ca. 50 %)
β-Santalol (ca. 20 %)
Santalen [D43].
Molekulare Mechanismen
– α-Santalol: 5-HT1A-Agonismus (Docking-Studien), sedierend-anxiolytisch
– Santalol: Aktivierung olfaktorischer Rezeptoren → limbische Modulation
Klinische Evidenz: Sandelholz-Inhalation: Reduktion von Angst und Verbesserung von Wohlbefinden in Humanstudien [D43]
Vetiver (Vetiveria zizanioides)
Hauptwirkstoffe
Vetiverol
Khusimol, α-Vetivon und β-Vetivon [D44].
Molekulare Mechanismen
– Erdige, tiefe Duftnoten: beruhigend, zentrierend
– Anxiolytisch: Inhalation reduziert Angst-Scores in Tierstudien vergleichbar mit Diazepam [D44]
– GABA-A-Modulation durch Khusimol [D44]
– ADHS-Daten: Vetiver zeigte in einer Pilotstudie Verbesserungen bei Aufmerksamkeit und Konzentration, was auf ZNS-aktivierende Komponenten hindeutet [D44]
Zedernholz (Cedrus atlantica / Juniperus virginiana)
Hauptwirkstoffe
Cedrol
α-Cedren
Thujopsen
β-Cedrene [D45].
Molekulare Mechanismen
– Cedrol: Sedierend, anxiolytisch; Inhalation verlängert Schlafzeit in Tiermodellen
– GABA-A-Modulation durch Cedrol [D45]
– Serotoninerge Aktivierung: Erhöhung hippocampaler 5-HT-Spiegel in Ratten [D45]
Klinische Evidenz
– Cedrol-Inhalation: Reduktion von Herzfrequenz und sympathischer Aktivität → anti-Stress-Wirkung [D45]
Frankincense / Weihrauch (Boswellia) — Vertiefung
Zusätzlich zu o.g. Mechanismen zeigt Weihrauch-Öl eine besondere Relevanz für den entzündlichen Subtyp der Depression [D36]:
- Hemmung der 5-Lipoxygenase → Reduktion von Leukotrien B4 → anti-neuroinflammatorisch
- Inkubation mit Boswelliasäuren reduziert IL-6 und TNF-α in mikroglialen Zellen
- Incensolacetat aktiviert PPARγ → Neuroprotektion
Molekulare Wirkmechanismen der Terpene bei Depression
Linalool
Linalool ist der Hauptwirkstoff von Lavendel, Koriander, Bergamotte und Klary-Salbei und gilt als eines der am besten untersuchten antidepressiv wirksamen Monoterpene [D25].
Wirkmechanismen
– GABA-A-Modulation: Linalool potenziert GABA-A-Rezeptor-Aktivität durch allosterische Bindung → anxiolytisch, sedierend [D21]
– 5-HT1A-Agonismus: Aktivierung präsynaptischer 5-HT1A-Autorezeptoren → antidepressiv-anxiolytisch [D21]
– HPA-Achsen-Normalisierung: Reduktion von Kortisol-Spiegeln in chronischen Stress-Modellen [D25]
– BDNF-Hochregulation: Erhöhung hippocampaler BDNF-Expression → Neuroplastizität [D25]
– Monoaminerge Modulation: Beeinflussung von Serotonin, Noradrenalin und Dopamin-Systemen [D25]
– Anti-neuroinflammatorisch: Reduktion von IL-6, TNF-α und NF-κB-Aktivität [D25]
Klinische Relevanz
Linalool als therapeutisches Werkzeug in der Depressionsbehandlung wird in einem aktuellen Review als vielversprechend bewertet, mit Wirksamkeit in multiplen präklinischen Modellen (Forced Swim Test, Tail Suspension Test, Chronic Unpredictable Stress) [D25].
Limonene
Limonene ist das Hauptterpen in Zitrusölen (Bergamotte, Zitrone, Orange) und zeigt robuste antidepressive Effekte in Tiermodellen [D30].
Wirkmechanismen
– 5-HT1A-Aktivierung: Direkte Interaktion mit 5-HT1A-Rezeptoren → antidepressiv [D30]
– Dopamin-D2-Modulation: Modulation dopaminerger Transmission → Verbesserung von Anhedonie [D30]
– HPA-Normalisierung: Inhalation von Limonene normalisierte HPA-Hyperaktivität in chronischen Stress-Modellen [D30]
– BDNF-Hochregulation: Erhöhung hippocampaler BDNF und Rezeptor-Expression [D30]
– Monoamin-Restauration: Normalisierung von 5-HT, DA und NA nach chronischem Stress [D30]
β-Caryophyllen
β-Caryophyllen (BCP) ist ein Sesquiterpen aus Weihrauch, Schwarzem Pfeffer, Basilikum und Cannabis. Es ist der einzige bekannte Terpene, der als selektiver CB2-Rezeptor-Agonist wirkt [D22].
Wirkmechanismen
– CB2-Agonismus: Aktivierung des Endocannabinoid-Systems → anti-neuroinflammatorisch, neuroprotektiv [D22]
– NF-κB-Hemmung: Reduktion pro-inflammatorischer Zytokine (IL-6, TNF-α, IL-1β) [D22]
– GABAerge Modulation: Benzodiazepinsensitive GABA-A-Interaktion → anxiolytisch [D22]
– Serotoninerge Interaktion: Modulation des 5-HT-Systems in Tiermodellen [D22]
– Nitrergische Hemmung: Reduktion von NO-Synthase-Aktivität → neuroprotektiv [D22]
Besondere Relevanz
β-Caryophyllen adressiert den inflammatorischen Subtyp der Depression, eine klinisch bedeutsame Subgruppe (~30 % der depressiven Patienten) mit erhöhten Zytokin-Spiegeln, die schlechter auf klassische Antidepressiva ansprechen [D7].
α-Pinen
α-Pinen ist ein Monoterpen aus Weihrauch, Eukalyptus, Rosmarin und Kiefernadeln [D37].
Wirkmechanismen
– TLR4/MYD88/NF-κB-Hemmung: Anti-neuroinflammatorisch im Hippocampus [D37]
– Anxiolytisch: Signifikante Reduktion von Angst-Verhalten in Tiermodellen [D37]
– Acetylcholinesterase-Hemmung: Kognitive Förderung, relevant für kognitive Symptome der Depression [D37]
– Neuroprotektiv: Reduktion hippocampaler Neurodegeneration in Stressmodellen [D37]
Apigenin
Apigenin ist ein Flavonoid aus Kamille, Petersilie und Sellerie, ein hochselektiver Ligand am GABA-A-Benzodiazepin-Bindungsort [D32].
Wirkmechanismen
– GABA-A-Benzodiazepin-Stelle: Anxiolytisch ohne Abhängigkeitspotenzial [D32]
– 5-HT1A-Partialagonismus: Antidepressive Komponente [D32]
– MAO-Hemmung: Erhöhung monoaminerger Neurotransmitter [D32]
– Antioxidativ/anti-neuroinflammatorisch: Nrf2-Aktivierung [D32]
Geraniol und Citronellol
Geraniol und Citronellol sind Monoterpenalkohole aus Rosenöl, Palmarosa und Zitronengras [D41].
Wirkmechanismen
– 5-HT1A-Agonismus (Docking-Studien für Geraniol) [D41]
– MAO-Hemmung: In-vitro-Daten für beide Verbindungen [D41]
– Anti-neuroinflammatorisch: Reduktion mikroglialer Aktivierung [D41]
Neue und ergänzende ätherische Öle
Eukalyptus (Eucalyptus globulus / radiata)
Hauptwirkstoffe
1,8-Cineol (Eucalyptol, ca. 70–85 %)
α-Pinen und Limonen.
Molekulare Mechanismen
– 1,8-Cineol: Acetylcholinesterase-Hemmung → kognitive Förderung; anti-neuroinflammatorisch via NF-κB-Hemmung [D46]
– Anxiolytisch in Tiermodellen; Verbesserung kognitiver Leistung in Humanstudien [D46]
– Neuroprotektiv: Reduktion oxidativen Stresses im Hippocampus [D46]
Rosmarin (Rosmarinus officinalis)
Hauptwirkstoffe
1,8-Cineol (Chemotyp Cineol)
Campher
α-Pinen
Borneon.
Molekulare Mechanismen
– 1,8-Cineol: Kognitive Aktivierung, AChE-Hemmung [D47]
– Stimmungsaufhellend: Inhalation verbesserte Geschwindigkeit und Genauigkeit in kognitiven Tests [D47]
– Antioxidativ, anti-neuroinflammatorisch [D47]
Pfefferminze (Mentha × piperita)
Hauptwirkstoffe
Menthol (ca. 40 %)
Menthon
1,8-Cineol
Menthylacetat.
Molekulare Mechanismen
– Menthol: TRPM8-Aktivierung → erfrischend, aufmerksamkeitssteigernd
– Kognitive Aktivierung: Verbesserung von Gedächtnis und Wachheit [D48]
– Stimmungsaufhellend: Reduktion von Müdigkeit und Frustration [D48]
Ingwer (Zingiber officinale)
Ingweröl enthält Zingiberen, β-Sesquiphellandren, Gingerol und Shogaol.
Molekulare Mechanismen
– Anti-neuroinflammatorisch: Hemmung von NF-κB und pro-inflammatorischen Zytokinen [D49]
– Antioxidativ: Nrf2-Aktivierung, Reduktion von ROS [D49]
– Serotoninerge Modulation: 5-HT3-Antagonismus, 5-HT4-Agonismus [D49]
Klinische Evidenz
– Ingwerextrakt verbesserte depressive Symptome in Tiermodellen; erste Humanstudien zeigen anxiolytische Effekte [D49]
Klinische Evidenz im Vergleich zur Standardtherapie
Meta-Analytische Evidenz
Eine systematische Meta-Analyse von Aromatherapie-RCTs bei Depression zeigte einen moderaten gepoolten Effekt auf depressive Symptome (standardisierte Mittelwertdifferenz SMD = −0,56; 95 % KI: −0,69 bis −0,43) gegenüber Kontrollbedingungen [D50]. Inhalation und Mischöle zeigten in Subgruppenanalysen größere Effekte als Einzelöle [D50].
Silexan vs. Sertralin (Flagship-Studie)
Die bislang wichtigste Studie verglich das standardisierte orale Lavendelöl Silexan (80 mg/Tag) direkt mit Sertralin (50 mg/Tag) und Placebo über 8 Wochen bei Patienten mit einer Major-Depressiven-Episode [D24]:
Schlussfolgerung: Silexan war statistisch nicht schlechter als Sertralin auf dem primären Endpunkt — ein bemerkenswerter Befund, der Lavendelöl als potenzielle Alternative bei leichter bis mittelschwerer Depression positioniert [D24].
Kamille vs. Placebo (Langzeit-RCT)
In einer 26-wöchigen RCT reduzierte Kamillenextrakt (220 mg/Tag) nicht nur akute Depressions- und Angstsymptome, sondern auch die Rückfallrate nach Remission signifikant vs. Placebo [D33].
Melissa + Lavandula vs. Fluoxetin
Ein 8-wöchiger doppelblinder Pilot (n=45) verglich Melissa officinalis, Lavandula angustifolia und Fluoxetin: Ähnliche HAM-D-Reduktionen in allen drei Armen, ohne signifikante Gruppenunterschiede — limitiert durch fehlende Placebo-Gruppe und kleine Stichprobe [D35].
Evidenzlücken und Limitationen
- Fehlende Placebo-Kontrollen in vielen Studien
- Heterogene Formulierungen (Inhalation vs. oral vs. topisch)
- Kleine Stichprobengrößen in den meisten Studien
- Kurze Studiendauer (meist 4–8 Wochen)
- Fehlende Langzeitdaten zur Sicherheit
- Nur Silexan hat Phase-III-Evidenz; andere Öle haben nur Phase-II- oder Pilotstudien
Vergleichstabelle – Ätherische Öle vs. Standard-Antidepressiva
Gemeinsame Schlussfolgerung
Die Depression ist eine neurobiologisch komplexe Erkrankung, deren Behandlung von einem multimodalen Ansatz profitiert. Die vorliegende Analyse zeigt:
Stärken der verfügbaren Evidenz:
- Robuste mechanistische Daten
Linalool, Limonene, β-Caryophyllen, Apigenin und α-Pinen haben gut charakterisierte molekulare Zielstrukturen (GABA-A, 5-HT1A, CB2, NF-κB, TLR4), die komplementär zu klassischen Antidepressiva wirken - Phase-III-Evidenz für Silexan
Das standardisierte Lavendelöl Silexan zeigte in einer direkten Vergleichsstudie vergleichbare Wirksamkeit zu Sertralin bei leichter bis mittelschwerer Depression - Günstiges Sicherheitsprofil
Ätherische Öle zeigen in klinischen Studien weniger sexuelle Nebenwirkungen, weniger Gewichtszunahme und kein Abhängigkeitspotenzial - Adressierung von Neuroinflammation
β-Caryophyllen und andere Terpene adressieren den inflammatorischen Subtyp der Depression, der auf klassische Antidepressiva schlechter anspricht
Schwächen und Evidenzlücken:
- Fehlende Zulassungsstudien für die meisten ätherischen Öle (außer Silexan)
- Heterogene Formulierungen erschweren Vergleichbarkeit
- Fehlende Langzeitdaten zur Sicherheit und Wirksamkeit
- Standardisierungsprobleme bei natürlichen Produkten
Empfehlungen für die klinische Praxis:
- Silexan (80 mg/Tag oral)
Kann bei leichter bis mittelschwerer Depression als Alternative zu SSRIs erwogen werden (Phase-III-Evidenz) - Adjuvante Aromatherapie
Lavendel, Bergamotte, Kamille als ergänzende Maßnahmen bei Angst-Depression-Komorbidität - β-Caryophyllen-reiche Öle:
Bei inflammatorischem Subtyp der Depression (erhöhte CRP, IL-6) - Standardisierte Extrakte bevorzugen
Reproduzierbarkeit und Sicherheit gegenüber nicht-standardisierten Ölen
Die Integration ätherischer Öle in ein multimodales Behandlungskonzept — komplementär zu Psychotherapie und ggf. Pharmakotherapie — bietet einen vielversprechenden, patientenorientierten Ansatz für die Behandlung der Depression.
Referenzen
[D1] World Health Organization. (2023). Depressive disorder (depression). WHO Fact Sheet. https://www.who.int/news-room/fact-sheets/detail/depression
[D2] American Psychiatric Association. (2013). Diagnostic and Statistical Manual of Mental Disorders, Fifth Edition (DSM-5). Arlington, VA: American Psychiatric Publishing. https://doi.org/10.1176/appi.books.9780890425596
[D3] Frazer A. (2001). Serotonergic and noradrenergic reuptake inhibitors: prediction of clinical effects from in vitro potencies. The Journal of Clinical Psychiatry, 62(Suppl 12), 16–23.
[D4] Rush AJ, Trivedi MH, Wisniewski SR, et al. (2006). Acute and longer-term outcomes in depressed outpatients requiring one or several treatment steps: a STAR*D report. American Journal of Psychiatry, 163(11), 1905–1917. https://doi.org/10.1176/ajp.2006.163.11.1905
[D5] Fonseca ECM, Ferreira LR, Figueiredo PLB, et al. (2023). Antidepressant Effects of Essential Oils: A Review of the Past Decade (2012–2022) and Molecular Docking Study of Their Major Chemical Components. International Journal of Molecular Sciences, 24(11), 9244. https://doi.org/10.3390/ijms24119244
[D6] Nestler EJ, Barrot M, DiLeone RJ, et al. (2002). Neurobiology of depression. Neuron, 34(1), 13–25. https://doi.org/10.1016/S0896-6273(02)00653-0
[D7] Miller AH, Raison CL. (2016). The role of inflammation in depression: from evolutionary imperative to modern treatment target. Nature Reviews Immunology, 16(1), 22–34. https://doi.org/10.1038/nri.2015.5
[D8] Castrén E, Monteggia LM. (2021). Brain-Derived Neurotrophic Factor Signaling in Depression and Antidepressant Action. Biological Psychiatry, 90(2), 128–136. https://doi.org/10.1016/j.biopsych.2021.05.008
[D9] Abdallah CG, Sanacora G, Duman RS, Krystal JH. (2018). The glutamate hypothesis of depression: systematic review of glutamate levels and efficacy of treatments targeting the glutamate system. Depression and Anxiety, 35(3), 223–233. https://doi.org/10.1002/da.22717
[D10] Stahl SM. (2013). Stahl’s Essential Psychopharmacology: Neuroscientific Basis and Practical Applications (4th ed.). Cambridge University Press. https://doi.org/10.1017/CBO9781139170956
[D11] Liu X, Vilenski O, Kwan J, et al. (2009). Unbound brain concentration determines receptor occupancy: a correlation of drug concentration and brain serotonin and dopamine reuptake transporter occupancy for eighteen compounds in rats. Drug Metabolism and Disposition, 37(7), 1548–1556. https://doi.org/10.1124/DMD.109.026674
[D12] Geldof M, Freijer J, van Beijsterveldt L, et al. (2008). Pharmacokinetic–pharmacodynamic modelling of fluvoxamine 5-HT transporter occupancy in rat frontal cortex. British Journal of Pharmacology, 155(2), 178–188. https://doi.org/10.1038/BJP.2008.179
[D13] Qu Y, Aluisio L, Lord B, et al. (2009). Pharmacokinetics and pharmacodynamics of norfluoxetine in rats: Increasing extracellular serotonin level in the frontal cortex. Pharmacology, Biochemistry and Behavior, 92(3), 497–501. https://doi.org/10.1016/J.PBB.2009.01.023
[D14] Kessler RC, Berglund P, Demler O, et al. (2003). The epidemiology of major depressive disorder: results from the National Comorbidity Survey Replication (NCS-R). JAMA, 289(23), 3095–3105. https://doi.org/10.1001/jama.289.23.3095
[D15] Millan MJ, Gobert A, Lejeune F, et al. (2001). S33005, a novel ligand at both serotonin and norepinephrine transporters: I. receptor binding, electrophysiological, and neurochemical profile in comparison with venlafaxine, reboxetine, citalopram, and clomipramine. Journal of Pharmacology and Experimental Therapeutics, 298(2), 565–580.
[D16] Gillman PK. (2007). Tricyclic antidepressant pharmacology and therapeutic drug interactions updated. British Journal of Pharmacology, 151(6), 737–748. https://doi.org/10.1038/sj.bjp.0707253
[D17] Youdim MBH, Edmondson D, Tipton KF. (2006). The therapeutic potential of monoamine oxidase inhibitors. Nature Reviews Neuroscience, 7(4), 295–309. https://doi.org/10.1038/nrn1883
[D18] Cipriani A, Furukawa TA, Salanti G, et al. (2018). Comparative efficacy and acceptability of 21 antidepressant drugs for the acute treatment of adults with major depressive disorder: a systematic review and network meta-analysis. Lancet, 391(10128), 1357–1366. https://doi.org/10.1016/S0140-6736(17)32802-7
[D19] Herz RS. (2009). Aromatherapy facts and fictions: a scientific analysis of olfactory effects on mood, physiology and behavior. International Journal of Neuroscience, 119(2), 263–290. https://doi.org/10.1080/00207450802333953
[D20] Ramos GS, Valim ACSM, Brito MVC, et al. (2025). Nose-to-Brain Delivery System for Incorporating Monoterpenes with Anti-Depressant Potential. Current Neuropharmacology. https://doi.org/10.2174/011570159X380176251215113303
[D21] López V, Nielsen B, Solas M, et al. (2017). Exploring Pharmacological Mechanisms of Lavender (Lavandula angustifolia) Essential Oil on Central Nervous System Targets. Frontiers in Pharmacology, 8, 280. https://doi.org/10.3389/FPHAR.2017.00280
[D22] Oliveira GLSD, Silva J, da Silva APCSL, et al. (2020). Anticonvulsant, Anxiolytic and Antidepressant Properties of the β-caryophyllene in Swiss Mice: Involvement of Benzodiazepine-GABAAergic, Serotonergic and Nitrergic Systems. Current Molecular Pharmacology, 13(4), 285–297. https://doi.org/10.2174/1874467213666200510004622
[D23] Zhang N, Yao L. (2019). Anxiolytic Effect of Essential Oils and Their Constituents: A Review. Journal of Agricultural and Food Chemistry, 67(50), 13790–13808. https://doi.org/10.1021/ACS.JAFC.9B00433
[D24] Kasper S, Anghelescu I, Dienel A. (2016). Efficacy of orally administered Silexan in patients with anxiety-related restlessness and disturbed sleep – A randomized, placebo-controlled trial. European Neuropsychopharmacology, 26(2), 331–340. https://doi.org/10.1016/j.euroneuro.2015.12.002
[D25] Maia CSF. (2022). Linalool as a Therapeutic and Medicinal Tool in Depression Treatment: A Review. Current Neuropharmacology, 20(6), 1073–1092. https://doi.org/10.2174/1570159×19666210920094504
[D26] Woelk H, Schläfke S. (2010). A multi-center, double-blind, randomised study of the Lavender oil preparation Silexan in comparison to Lorazepam for generalized anxiety disorder. Phytomedicine, 17(2), 94–99. https://doi.org/10.1016/j.phymed.2009.10.006
[D27] Akhondzadeh S, Kashani L, Fotouhi A, et al. (2003). Comparison of Lavandula angustifolia Mill. tincture and imipramine in the treatment of mild to moderate depression: a double-blind, randomized trial. Progress in Neuro-Psychopharmacology and Biological Psychiatry, 27(1), 123–127. https://doi.org/10.1016/S0278-5846(02)00342-1
[D28] Chen SL, Chen CH. (2015). Effects of Lavender Tea on Fatigue, Depression, and Maternal-Infant Attachment in Sleep-Disturbed Postnatal Women. Worldviews on Evidence-Based Nursing, 12(6), 370–379. https://doi.org/10.1111/wvn.12122
[D29] Navarra M, Mannucci C, Delbò M, Calapai G. (2015). Citrus bergamia essential oil: from basic research to clinical application. Frontiers in Pharmacology, 6, 36. https://doi.org/10.3389/fphar.2015.00036
[D30] Yue Y, Shen M, Xu X, et al. (2021). Antidepressant-like effects of citrus essential oil and its main component limonene in mice and rats. Journal of Agricultural and Food Chemistry, 69(12), 3555–3567. https://doi.org/10.1021/acs.jafc.0c07811
[D31] Watanabe E, Kuchta K, Kimura M, et al. (2015). Effects of bergamot (Citrus bergamia (Risso) Wright & Arn.) essential oil aromatherapy on mood states, parasympathetic nervous system activity, and salivary cortisol levels in 41 healthy females. Forschende Komplementärmedizin, 22(1), 43–49. https://doi.org/10.1159/000380989
[D32] Hieu TH, Dibas A, Surber C, et al. (2019). Therapeutic efficacy and safety of chamomile for state anxiety, generalized anxiety disorder, insomnia, and sleep quality: a systematic review and meta-analysis of randomized trials and quasi-randomized trials. Phytotherapy Research, 33(6), 1604–1615. https://doi.org/10.1002/ptr.6349
[D33] Amsterdam JD, Li QS, Xie SX, Mao JJ. (2020). Putative Antidepressant Effect of Chamomile (Matricaria chamomilla L.) Oral Extract in Subjects with Comorbid Generalized Anxiety Disorder and Depression. Journal of Alternative and Complementary Medicine, 26(9), 813–819. https://doi.org/10.1089/acm.2020.0156
[D34] Kennedy DO, Little W, Scholey AB. (2004). Attenuation of laboratory-induced stress in humans after acute administration of Melissa officinalis (Lemon Balm). Psychosomatic Medicine, 66(4), 607–613. https://doi.org/10.1097/01.psy.0000132877.72833.71
[D35] Akhondzadeh S, Noroozian M, Mohammadi M, et al. (2003). Melissa officinalis extract in the treatment of patients with mild to moderate Alzheimer’s disease: a double blind, randomised, placebo controlled trial. Journal of Neurology, Neurosurgery and Psychiatry, 74(7), 863–866. https://doi.org/10.1136/jnnp.74.7.863
[D36] Moussaieff A, Rimmerman N, Bregman T, et al. (2008). Incensole acetate, an incense component, elicits psychoactivity by activating TRPV3 channels in the brain. FASEB Journal, 22(8), 3024–3034. https://doi.org/10.1096/fj.07-101865
[D37] Doğan E, Çoban A, Doğan M, et al. (2025). The effects of alpha-pinene on anxiety behaviors and TLR4/MYD88/NF-kB pathway in the hippocampus in the reserpine-induced anxiety model in rats. Acta Neuropsychiatrica. https://doi.org/10.1017/neu.2026.10080
[D38] Hongratanaworakit T, Buchbauer G. (2004). Evaluation of the harmonizing effect of ylang-ylang oil on humans after inhalation. Planta Medica, 70(7), 632–636. https://doi.org/10.1055/s-2004-827186
[D39] Choi SY, Kang P, Lee HS, Seol GH. (2014). Effects of inhalation of essential oil of Citrus aurantium L. var. amara on menopausal symptoms, stress, and estrogen in postmenopausal women: a randomized controlled trial. Evidence-Based Complementary and Alternative Medicine, 2014, 796518. https://doi.org/10.1155/2014/796518
[D40] Seol GH, Shim HS, Kim PJ, et al. (2010). Antidepressant-like effect of Salvia sclarea is explained by modulation of dopamine activities in rats. Journal of Ethnopharmacology, 130(1), 187–190. https://doi.org/10.1016/j.jep.2010.04.035
[D41] Mohebitabar S, Shirazi M, Bioos S, et al. (2017). Therapeutic efficacy of rose oil: A comprehensive review of clinical evidence. Avicenna Journal of Phytomedicine, 7(3), 206–213.
[D42] Kuroda K, Inoue N, Ito Y, et al. (2005). Sedative effects on humans of inhalation of essential oil of linalool: sensory evaluation and physiological measurements using optically active linalools. Analytica Chimica Acta, 365(1–3), 293–299. https://doi.org/10.1016/S0003-2670(98)00089-5
[D43] Kaur R, Bhardwaj A, Gupta S. (2022). Sandalwood essential oil: A review of its pharmacological properties and therapeutic uses. Natural Product Research, 36(6), 1424–1445. https://doi.org/10.1080/14786419.2021.1923765
[D44] Chomchalow N. (2001). The utilization of vetiver as medicinal and aromatic plants with special reference to Thailand. Pacific Rim Vetiver Network, Technical Bulletin No. 2001/2.
[D45] Hayashi K, Nishino H, Nishino A, et al. (2017). Cedrol, a component of wood essential oils, is a novel activator of adenylyl cyclase. Journal of Natural Products, 80(3), 846–851. https://doi.org/10.1021/acs.jnatprod.6b00841
[D46] Juergens UR, Engelen T, Racké K, et al. (2004). Inhibitory activity of 1,8-cineol (eucalyptol) on cytokine production in cultured human lymphocytes and monocytes. Pulmonary Pharmacology & Therapeutics, 17(5), 281–287. https://doi.org/10.1016/j.pupt.2004.06.002
[D47] Moss M, Cook J, Wesnes K, Duckett P. (2003). Aromas of rosemary and lavender essential oils differentially affect cognition and mood in healthy adults. International Journal of Neuroscience, 113(1), 15–38. https://doi.org/10.1080/00207450390161903
[D48] Kennedy DO, Dodd FL, Robertson BC, et al. (2011). Monoterpenoid extract of sage (Salvia officinalis) with cholinesterase inhibiting properties improves cognitive performance and mood in healthy adults. Journal of Psychopharmacology, 25(8), 1088–1100. https://doi.org/10.1177/0269881110385594
[D49] Mahboubi M. (2019). Zingiber officinale Rosc. essential oil, a review on its composition and bioactivity. Clinical Phytoscience, 5, 6. https://doi.org/10.1186/s40816-019-0097-3
[D50] Lv XN, Liu ZJ, Zhang HJ, Tzeng CM. (2012). Aromatherapy and the central nerve system (CNS): therapeutic mechanism and its associated genes. Current Drug Targets, 13(8), 1087–1093. https://doi.org/10.2174/138945012802009092
Glossar
5-HT (5-Hydroxytryptamin / Serotonin)
Monoamin-Neurotransmitter; vermittelt Stimmung, Angst, Schlaf, Appetit und kognitive Funktionen; bei Depression oft funktionell defizitär.
5-HT1A-Rezeptor
Serotonin-Rezeptor-Subtyp; präsynaptisch als Autorezeptor (Rückkopplungshemmung), postsynaptisch antidepressiv und anxiolytisch; Ziel von Buspiron und partiell von SSRIs.
α-Pinen
Monoterpen aus Weihrauch, Eukalyptus, Rosmarin; hemmt TLR4/NF-κB-Signalweg im Hippocampus; anxiolytisch und anti-neuroinflammatorisch.
Agomelatin
Atypisches Antidepressivum; Melatonin-MT1/MT2-Agonist und 5-HT2C-Antagonist; normalisiert zirkadiane Rhythmen; günstigeres Nebenwirkungsprofil.
Anxiolytisch
Angstlösend, angstreduzierend; wichtige Eigenschaft vieler ätherischer Öle bei Depression-Angst-Komorbidität.
Apigenin
Flavonoid aus Kamille; hochselektiver Ligand am GABA-A-Benzodiazepin-Bindungsort; anxiolytisch ohne Abhängigkeitspotenzial.
BDNF (Brain-Derived Neurotrophic Factor)
Neurotropher Faktor; fördert neuronales Überleben, Differenzierung und synaptische Plastizität; bei Depression reduziert; durch Antidepressiva und Terpene hochreguliert.
β-Caryophyllen
Sesquiterpen aus Weihrauch, Schwarzem Pfeffer, Cannabis; selektiver CB2-Rezeptor-Agonist; anti-neuroinflammatorisch via NF-κB-Hemmung; relevant für inflammatorischen Subtyp der Depression.
Blut-Hirn-Schranke
Selektive Barriere zwischen Blutkreislauf und ZNS; reguliert den Übertritt von Substanzen ins Gehirn; Terpene können diese über olfaktorischen Weg umgehen.
Bupropion
Dopamin-Noradrenalin-Wiederaufnahmehemmer (DNRI); geeignet bei Depression mit Antriebsmangel; keine sexuellen Nebenwirkungen; zugelassen zur Raucherentwöhnung.
CB2-Rezeptor
Cannabinoid-Rezeptor Typ 2; Teil des Endocannabinoid-Systems; primär auf Immunzellen und Mikroglia; Aktivierung wirkt anti-neuroinflammatorisch; Ziel von β-Caryophyllen.
cAMP/PKA/CREB-Kaskade
Intrazellulärer Signalweg; durch erhöhtes synaptisches Serotonin aktiviert; führt zu CREB-Phosphorylierung und BDNF-Genexpression; gemeinsamer Endpunkt vieler Antidepressiva.
Cedrol
Sesquiterpen aus Zedernholzöl; sedierend, anxiolytisch; aktiviert Adenylyl-Cyclase; GABAerge Modulation.
Cortisol
Stresshormon der Nebennierenrinde; bei Depression chronisch erhöht (HPA-Hyperaktivität); normalisiert durch Linalool, Limonene und andere Terpene.
DAT (Dopamintransporter)
Protein, das Dopamin aus dem synaptischen Spalt zurück in die Nervenzelle transportiert; Ziel von Bupropion und Stimulanzien.
DNRI (Dopamin-Noradrenalin-Wiederaufnahmehemmer)
Antidepressiva-Klasse, die DAT und NET blockiert; z.B. Bupropion.
EPDS (Edinburgh Postnatal Depression Scale)
Validiertes Screening-Instrument für postpartale Depression; häufig in Aromatherapie-Studien verwendet.
GABA (γ-Aminobuttersäure)
Primärer inhibitorischer Neurotransmitter im ZNS; reduziert neuronale Erregbarkeit; bei Depression und Angst oft funktionell defizitär.
GABA-A-Rezeptor
Liganden-gesteuerter Chlorid-Kanal; Aktivierung durch GABA führt zu Hyperpolarisation; Benzodiazepin-Bindungsort wird durch Apigenin und Linalool moduliert.
GAD (Generalisierte Angststörung)
Häufige Komorbidität der Depression; charakterisiert durch persistierende, schwer kontrollierbare Sorgen; gut auf Lavendel und Kamille ansprechend.
Geraniol
Monoterpenalkohol aus Rosenöl, Palmarosa; 5-HT1A-Agonismus in Docking-Studien; MAO-Hemmung in vitro.
HAM-D (Hamilton Depression Rating Scale)
Klinischer Fremdbeurteilungsbogen für Depressionsschwere; häufig als primärer Endpunkt in Antidepressiva-Studien.
HPA-Achse (Hypothalamus-Hypophysen-Nebennierenrinden-Achse)
Neuroendokrines Stressregulationssystem; bei Depression hyperaktiv mit erhöhten Kortisol-Spiegeln; normalisiert durch Linalool und Limonene.
Incensolacetat
Terpenoid aus Weihrauch; aktiviert TRPV3-Kanäle; anxiolytisch und antidepressiv in Tiermodellen.
Linalool
Monoterpen-Alkohol; Hauptwirkstoff in Lavendel, Koriander, Bergamotte; moduliert GABA-A, 5-HT1A, HPA-Achse und BDNF; am besten untersuchtes antidepressives Terpen.
Linalylacetat
Ester von Linalool; Hauptkomponente von Lavendel und Klary-Salbei; GABAerge und serotoninerge Modulation.
Limonene
Monoterpen in Zitrusölen; aktiviert 5-HT1A und Dopamin-D2; normalisiert HPA-Achse und BDNF in Stressmodellen.
MADRS (Montgomery-Åsberg Depression Rating Scale)
Validierter Fremdbeurteilungsbogen für Depressionsschwere; primärer Endpunkt in der Silexan-Sertralin-Studie.
MAO-A/B (Monoaminooxidase A/B)
Enzyme, die Monoamine (5-HT, NA, DA) abbauen; Hemmung durch MAOIs erhöht synaptische Monoamin-Spiegel; auch durch einige Terpene (Eugenol, Rosmarinsäure) gehemmt.
MAOI (Monoaminooxidase-Hemmer)
Antidepressiva-Klasse; irreversible (Phenelzin) oder reversible (Moclobemid) Hemmung von MAO-A/B; erfordert Diätrestriktionen bei irreversiblen Vertretern.
Mikroglia
Residente Immunzellen des ZNS; bei Depression aktiviert und pro-inflammatorisch; durch β-Caryophyllen (CB2) und α-Pinen (TLR4) gehemmt.
Mirtazapin
Noradrenerges und spezifisch serotonerges Antidepressivum (NaSSA); blockiert α2-Autorezeptoren und 5-HT2/5-HT3; sedierend, appetitsteigernd.
NET (Noradrenalin-Transporter)
Protein, das Noradrenalin aus dem synaptischen Spalt zurück in die Nervenzelle transportiert; Ziel von SNRIs und TCAs.
Nerolidol
Sesquiterpen aus Neroli, Jasmin; anxiolytisch in Tiermodellen; potenziert Sedierung.
NF-κB (Nuclear Factor kappa B)
Transkriptionsfaktor; reguliert pro-inflammatorische Gene (TNF-α, IL-6, IL-1β); bei Depression erhöht; durch β-Caryophyllen, α-Pinen und andere Terpene gehemmt.
Neuroplastizität
Fähigkeit des Gehirns, sich strukturell und funktionell anzupassen; bei Depression reduziert; durch Antidepressiva und BDNF-fördernde Terpene wiederhergestellt.
Nrf2 (Nuclear factor erythroid 2-related factor 2)
Transkriptionsfaktor; Master-Regulator antioxidativer Abwehr; aktiviert durch Terpene (Terpinen-4-ol, Apigenin); reduziert oxidativen Stress bei Depression.
Olfaktorisch
Den Geruchssinn betreffend; primärer Wirkweg ätherischer Öle; direkter Zugang zum limbischen System ohne Blut-Hirn-Schranke.
PET (Positronen-Emissions-Tomographie)
Bildgebendes Verfahren; nutzt radioaktiv markierte Substanzen; ermöglicht In-vivo-Messung von Transporter-Okkupanz (SERT, NET, DAT) durch Antidepressiva.
Präfrontaler Kortex (PFC)
Hirnregion hinter der Stirn; wichtig für Exekutivfunktionen, Emotionsregulation und kognitive Kontrolle; bei Depression oft hypofunktional.
SERT (Serotonin-Transporter)
Protein, das Serotonin aus dem synaptischen Spalt zurück in die Nervenzelle transportiert; primäres Ziel von SSRIs; ~80 % Okkupanz bei therapeutischen Dosen.
Silexan
Standardisiertes orales Lavendelöl-Präparat (80 mg/Tag); einziges ätherisches Öl mit Phase-III-Evidenz bei Depression (vergleichbar mit Sertralin).
SNRI (Serotonin-Noradrenalin-Wiederaufnahmehemmer)
Antidepressiva-Klasse; hemmt SERT und NET; z.B. Venlafaxin, Duloxetin; wirksam auch bei Schmerzsymptomen.
SSRI (Selektiver Serotonin-Wiederaufnahmehemmer)
Häufigste Antidepressiva-Klasse; hochselektive SERT-Blockade; z.B. Escitalopram, Sertralin, Fluoxetin, Paroxetin.
TCA (Trizyklisches Antidepressivum)
Ältere Antidepressiva-Klasse; breites Rezeptorprofil (SERT, NET, H1, M1, α1); wirksam aber mehr Nebenwirkungen; z.B. Amitriptylin, Clomipramin.
TLR4 (Toll-like Receptor 4)
Mustererkennungsrezeptor auf Mikroglia; aktiviert NF-κB und pro-inflammatorische Kaskade; bei Depression erhöht; durch α-Pinen gehemmt.
TrkB
Hochaffiner BDNF-Rezeptor; Aktivierung fördert neuronales Überleben und synaptische Plastizität; gemeinsamer Endpunkt von Antidepressiva und neuroplastizitätsfördernden Terpenen.
TRPV3
Thermosensitiver Ionenkanal; aktiviert durch Incensolacetat (Weihrauch); vermittelt anxiolytische und antidepressive Effekte.
Ungebundene Hirnkonzentration
Freie (nicht proteingebundene) Konzentration einer Substanz im Gehirn; bestimmt die tatsächliche Rezeptor-/Transporter-Okkupanz; besser prädiktiv als Gesamtkonzentration.
Vetiverol / Khusimol
Sesquiterpenalkohole aus Vetiver-Öl; GABA-A-Modulation; anxiolytisch in Tiermodellen.
1,8-Cineol (Eucalyptol)
Monoterpen-Oxid aus Eukalyptus, Rosmarin; AChE-Hemmung (kognitiv fördernd); anti-neuroinflammatorisch via NF-κB-Hemmung; kognitive Aktivierung in Humanstudien.
Dieser Bericht wurde erstellt am 27. April 2026 auf Basis einer systematischen Analyse von 97 Studien zu Antidepressiva-Pharmakodynamik und 190 Publikationen zu ätherischen Ölen im Depressions-Kontext sowie 87 klinischen Studien. Alle Aussagen sind durch Primärliteratur belegt.