目录
Diabetes und ätherische Öle, wie ätherische Öle bei Diabetes hilfreich sein können, soll im ersten Teil für Betroffene und interessierte Laien verständlich erläutert werden.
Der zweite Teil befasst sich mit Diabetes mellitus Typ 2 und der Wirkung ätherischer Öle, der Pharmakologie, Wirkmechanismen und komplementären Therapieansätzen: Ein umfassender wissenschaftlicher Bericht zu Standard-Antidiabetika, Terpenen und ätherischen Ölen, molekulare Grundlagen, klinische Evidenz und adjuvante Therapiestrategien.
Diabetes wird in zwei Ausprägungen unterschieden:
- Typ I
eine Autoimmunerkrankung, die meist schon im Kindes- oder Jugendalter beginnt und insgesamt nur 10% der Fälle betrifft - Typ-2
eine chronische Stoffwechselkrankheit, die sich häufiger bei Erwachsenen entwickelt und 90% aller Fälle abdeckt und Insulinpflichtigkeit bedingt
Diabetes – Typ2
Was ist Diabetes Typ 2 – einfach erklärt?
Stellen Sie sich Insulin wie einen Schlüssel vor und Ihre Körperzellen wie Türen. Normalerweise öffnet Insulin (der Schlüssel) die Zellen, damit Zucker (Glukose) aus dem Blut in die Zellen eintreten und als Energie genutzt werden kann.
与 Diabetes Typ 2 passieren zwei Dinge:
1. Die Türschlösser sind kaputt (Insulinresistenz): Die Zellen reagieren nicht mehr richtig auf Insulin, der Schlüssel passt nicht mehr
2. Zu wenig Schlüssel werden produziert (Beta-Zell-Erschöpfung): Die Bauchspeicheldrüse kann nicht genug Insulin herstellen
Als Ergebnis dieses Dilemmas verbleibt zu viel Zucker im Blut (hoher Blutzucker = Hyperglykämie), was langfristig Blutgefäße, Nerven, Nieren, Augen und Herz schädigt.
Wie häufig ist Diabetes Typ 2?
Weltweit leiden über 537 Millionen Menschen an Diabetes, das entspricht 1 von 10 Erwachsenen. In Deutschland sind es etwa 8–9 Millionen Menschen. Bis 2045 werden es weltweit voraussichtlich 783 Millionen sein.
Was sind die Ursachen?
- Übergewicht (besonders Bauchfett)
- 缺乏运动
- Ungesunde Ernährung (viel Zucker, wenig Ballaststoffe)
- 遗传倾向
- 慢性压力
- Schlafmangel
Wie wird Diabetes Typ 2 normalerweise behandelt?
Die wichtigsten Medikamente – einfach erklärt
- Metformin – das Basismedikament
– Hilft der Leber, weniger Zucker ins Blut abzugeben; macht Zellen empfindlicher für Insulin
– Aktiviert einen Energieschalter in den Zellen (AMPK), ähnlich wie Sport
– Vorteile: Günstig, gut erforscht, kein Unterzucker-Risiko, schützt das Herz
– Nebenwirkungen: Magen-Darm-Beschwerden (Übelkeit, Durchfall), besonders am Anfang
- SGLT2-Hemmer (z. B. Empagliflozin, Dapagliflozin) – “Zuckerpumpen-Blocker”
– Blockieren eine Pumpe in der Niere, die normalerweise Zucker zurück ins Blut holt, der Zucker wird stattdessen über den Urin ausgeschieden
– Vorteile: Schützen das Herz und die Nieren; helfen beim Abnehmen
– Nebenwirkungen: Häufigere Harnwegsinfektionen
- GLP-1-Agonisten (z. B. Semaglutid/Ozempic, Liraglutid) – “Darmhormon-Nachahmer”
– Ahmen ein natürliches Darmhormon nach, das nach dem Essen ausgeschüttet wird, stimulieren Insulin, bremsen den Appetit
– Vorteile: Starke Blutzuckersenkung, erhebliche Gewichtsabnahme (5–15 %), Herzschutz
– Nebenwirkungen: Übelkeit, Erbrechen (besonders am Anfang)
- Insulin
– Notwendig, wenn die Bauchspeicheldrüse nicht mehr genug produziert
– Verschiedene Arten: Schnell wirkend (zu Mahlzeiten) und lang wirkend (Basis)
Ätherische Öle und Diabetes – wie funktioniert das?
Das klingt zunächst ungewöhnlich: Können Pflanzenöle wirklich den Blutzucker beeinflussen? Ja, und zwar über mehrere Mechanismen:
- Über den Geruchssinn
Duftmoleküle aktivieren das Nervensystem und können Stoffwechselprozesse beeinflussen - Durch Aufnahme über die Haut oder Einatmen
Kleine Moleküle gelangen ins Blut und wirken systemisch - Durch direkten Kontakt mit Rezeptoren in Darm, Bauchspeicheldrüse und Muskeln
Welche ätherischen Öle können bei Diabetes helfen?
Zimt – das bekannteste Diabetes-Öl
肉桂 (Cinnamomum zeylanicum / cassia) ist das am besten erforschte Gewürz bei Diabetes.
- 里面是什么? Hauptsächlich Cinnamaldehyd (60–90 %)
- Was macht es?
– Aktiviert denselben Energieschalter (AMPK) wie Metformin
– Verbessert die Insulinsensitivität der ZellenHemmt Enzyme, die Kohlenhydrate zu Zucker aufspalten (α-Amylase, α-Glucosidase), ähnlich wie das Medikament Acarbose
– Senkt Entzündungsprozesse - 研究
Meta-Analysen zeigen: 1–6 g Zimt täglich senkt den Nüchternblutzucker um 18–29 mg/dl und HbA1c (Langzeit-Blutzuckerwert) um 0,3–0,9 % - 应用
Gewürz, Tee, oder Kapsel (Zimtextrakt)
Ingwer – der GLP-1-Verstärker
姜 (Zingiber officinale) ist bekannt für seine Verdauungswirkung, hat aber auch starke antidiabetische Eigenschaften.
- 里面是什么? Gingerol, Shogaol, Paradol
- Was macht es?
– Erhöht die Ausschüttung von GLP-1 (dasselbe Hormon, das Ozempic nachahmt!)
– Verbessert den Glukose-Transport in die Muskeln
– Senkt Entzündungswerte (TNF-α, IL-6) - 研究
2 g Ingwerpulver täglich senkte Nüchternblutzucker um 10,5 % und HbA1c um 10,3 % (p < 0,05) - 申请:
rischer Ingwer im Essen, Ingwertee, Kapseln
Kurkuma – der goldene Entzündungshemmer
姜黄 (姜黄) mit seinem Wirkstoff Curcumin ist eines der meistuntersuchten Naturheilmittel.
- 里面是什么? Curcumin (3–5 % des Gewürzes), ätherische Öle (Turmeron, Zingiberen)
- Was macht es?
– Hemmt NF-κB, den “Entzündungs-Schalter” im Körper
– Aktiviert PPARγ, ähnlich wie die Diabetesmedikamente Thiazolidindione
– Verbessert Insulinsensitivität und schützt die Beta-Zellen - 研究
In einer Studie verhinderte Curcumin bei Prädiabetikern die Entwicklung zu echtem Diabetes: 0 % vs. 16,4 % in der Placebo-Gruppe nach 9 Monaten - 请注意
Curcumin wird schlecht aufgenommen,aber mit schwarzem Pfeffer (Piperin) kombiniert resultiert in 20-fach besserer Aufnahme!
Schwarzkümmel – der Multitalent
Schwarzkümmel (Nigella sativa) wird im arabischen Raum als “Heilmittel gegen alles außer dem Tod” bezeichnet.
- 里面是什么? Thymoquinon, Thymol, Carvacrol
- Was macht es?
– Schützt die insulinproduzierenden Beta-Zellen in der Bauchspeicheldrüse
- Hemmt Enzyme, die Zucker aus Kohlenhydraten freisetzen
– Antioxidativ und entzündungshemmend - 研究
2 g Schwarzkümmelöl täglich senkte HbA1c um 1,5 % und Nüchternblutzucker um 45 mg/dl (p < 0,001)
Oregano/Thymian – Carvacrol und Thymol
- Was machen sie?
– Hemmen dieselben Enzyme wie Acarbose (Diabetesmedikament)
– Aktivieren AMPK (wie Metformin
– Entzündungshemmend über NF-κB-Hemmung
Bergamotte – Cholesterin und Blutzucker
Was macht es?
– Limonene verbessert Insulinsensitivität
– Bergapten aktiviert AMPK
– Senkt gleichzeitig LDL-Cholesterin (das “schlechte” Cholesterin)
Rosmarin – der Antioxidant
Was macht es?
– Rosmarinsäure hemmt GABA-Transaminase und wirkt antioxidativ
– 1,8-Cineol verbessert Glukosetoleranz
– Schützt Beta-Zellen vor oxidativem Stress
Vergleich – Ätherische Öle vs. Diabetes-Medikamente
| 活性成分 | Ähnlich wie | 它的作用 |
| Cinnamaldehyd (Zimt) | 二甲双胍 | AMPK-Aktivierung, Insulinsensitivität |
| Gingerol (Ingwer) | GLP-1-Agonisten | GLP-1-Erhöhung, Appetit-Hemmung |
| Curcumin (Kurkuma) | Thiazolidindione | PPARγ-Aktivierung, Beta-Zell-Schutz |
| Thymoquinon (Schwarzkümmel) | Acarbose | Enzymhemmung, Beta-Zell-Schutz |
| Carvacrol (Oregano) | Acarbose + Metformin | Enzymhemmung + AMPK |
Praktische Tipps zur Anwendung
In der Küche (einfachste Methode):
- Zimt: 1 Teelöffel täglich in Porridge, Joghurt, Kaffee oder Tee
- 生姜 Frisch gerieben in Speisen, als Tee (2 cm Ingwer in heißem Wasser)
- 姜黄 In Currys, goldene Milch (mit schwarzem Pfeffer!)
- Oregano: Reichlich auf Pizza, in Salaten, Saucen
Als Nahrungsergänzung:
- Zimtextrakt-Kapseln: 1–3 g täglich
- Ingwerkapseln: 1–2 g täglich
- Curcumin mit Piperin: 500–1000 mg täglich
Als Aromatherapie:
- Zimt-, Ingwer- oder Bergamotteöl im Diffusor
- Entspannungsbäder mit 5–8 Tropfen (in Trägeröl aufgelöst)
Häufig gestellte Fragen
Wie schnell wirken ätherische Öle?
Manche Wirkungen (Entspannung, Stimmungsaufhellung) können schon nach Minuten eintreten. Langfristige Effekte (wie bei Diabetes) benötigen regelmäßige Anwendung über Wochen.
Muss ich teure Öle kaufen?
Qualität ist wichtig: Achten Sie auf 100 % naturreine ätherische Öle, am besten mit am besten mit chargenspezifischem Analyse-Zertifikat (GC/MS).
Günstige Parfümöle oder synthetische Duftstoffe haben keine therapeutische Wirkung und sind auf Grund der synthetischen Inhaltsstoffe u.U. gesundheitlich schädlich und verursachen Kopfschmerzen, Übelkeit, etc..
Wer mehr über die Auswahl und Qualität ätherischer Öle erfahren möchte, der wird in dem Beitrag „Ätherische Öle – Odysse einer Suche“ fündig.
Ein weiterer Beitrag zitiert Prof. Dr. Dr. Dr. med. habil. Hanns Hatt von der Ruhr-Universität Bochum, der in seinem Video „用香料治愈“ auf interessante, kurzweilige und dennoch wissenschaftliche Weise die Wirkung ätherischer Öle auf den menschlichen Körper erklärt.
Wichtige Hinweise und Sicherheit
Unbedingt beachten:
- Ätherische Öle ersetzen keine Diabetes-Medikamente, insbesondere nicht Insulin!
- Sprechen Sie mit Ihrem Arzt vor der Einnahme von Ergänzungen
- Zimt in hohen Dosen enthält Cumarin (besonders Cassia-Zimt), daher maximal 2 g täglich einnehmen und Ceylon-Zimt bevorzugen
- Niemals Diabetes-Medikamente ohne Arztabsprache absetzen
Zusammenfassung in drei Sätzen
Diabetes Typ 2 entsteht, wenn Körperzellen nicht mehr richtig auf Insulin reagieren und die Bauchspeicheldrüse erschöpft.
Bestimmte ätherische Öle und ihre Wirkstoffe, besonders Zimt (Cinnamaldehyd), Ingwer (Gingerol) und Kurkuma (Curcumin) können den Blutzucker auf ähnlichen Wegen wie Standardmedikamente beeinflussen: durch Aktivierung des zellulären Energieschalters AMPK, Verbesserung der Insulinsensitivität und Schutz der insulinproduzierenden Zellen.
Als Ergänzung zu einem gesunden Lebensstil und ärztlicher Behandlung können sie einen wertvollen Beitrag leisten.
Empfohlene Ölmischungen und Anwendungsprotokoll für Diabetes-Begleittherapie
Primärprodukte (dōTERRA)
| 产品 | 应用 | Hauptinhaltsstoffe |
| Zimt (Cassia/Ceylon) (15 ml) | Intern / Topisch (verdünnt) | Zimtaldehyd, Eugenol |
| Koriander (15 ml) | Intern / Aromatisch | Linalool, α-Pinen |
| Zitrone (15 ml) | Intern / Aromatisch | d-Limonen, Citral |
| 姜 (15 ml) | Intern / Topisch | Gingerol, Shogaol, Zingiberene |
| 佛手柑 (15 ml) | Aromatisch / Topisch | Linalylacetat, Linalool |
| Slim & Sassy Blend | Intern / Aromatisch | Grapefruit, Zitrone, Pfefferminze, Ingwer, Zimt |
Eigene Ölmischungen (DIY-Blends)
Blend 1: “Blutzucker-Balance” (Intern)
目标: Insulinsensitivität ↑, Glukosestoffwechsel-Unterstützung
| 油 | 水滴 | Träger | 作用机制 |
| Zimt (Cassia) | 1 | 1 Kapsel Fraktioniertes Kokosöl | Zimtaldehyd → GLUT-4 ↑, Insulinmimetisch |
| Koriander | 1 | Linalool → Insulinsekretion ↑ | |
| 姜 | 1 | Gingerol → Glukoseaufnahme ↑ |
申请: 1–2 Kapseln täglich zu den Mahlzeiten
Blend 2: “Entzündungshemmung” (Topisch)
目标: Chronische Entzündung ↓ (Schlüsselfaktor bei T2D)
| 油 | 水滴 | 载体油 | 作用机制 |
| 姜 | 3 | 15 ml Jojobaöl | Gingerol → NF-κB ↓ |
| 香 | 3 | Boswellinsäuren → COX-2 ↓ | |
| 姜黄 | 2 | Curcumin → IL-6 ↓, TNF-α ↓ | |
| 科帕伊巴 | 2 | β-Caryophyllen → CB2 → Entzündung ↓ |
申请: Auf Bauchbereich und Lendenwirbelsäule massieren
Blend 3: “Neuropathie-Pflege” (Topisch, Füße)
目标: Diabetische Neuropathie-Symptome lindern
| 油 | 水滴 | 载体油 | 作用机制 |
| 薄荷 | 3 | 15 ml Kokosöl | Menthol → TRPM8, Kühlwirkung |
| 薰衣草 | 3 | Analgetisch, entzündungshemmend | |
| 香 | 2 | 神经保护 | |
| Zitrone | 2 | 抗氧化剂 |
申请: Täglich auf Fußsohlen und Unterschenkel massieren
Blend 4: “Stressabbau” (Diffusor)
目标: Cortisol ↓ (Cortisol erhöht Blutzucker), Entspannung
| 油 | 水滴 | 作用机制 |
| 佛手柑 | 3 | HPA-Achse ↓, Cortisol ↓ |
| 薰衣草 | 2 | GABA-A, Entspannung |
| 香 | 2 | 神经保护 |
| 香根草 | 1 | Erdend, stabilisierend |
申请: Täglich 30–60 Minuten im Diffusor
Blend 5: “Gewichtsmanagement” (Intern)
目标: Metabolismus-Unterstützung, Appetitregulation
| 油 | 水滴 | Träger | 作用机制 |
| 葡萄柚 | 2 | 1 Kapsel | d-Limonen → Lipolyse ↑ |
| 肉桂 | 1 | Insulinmimetisch | |
| 姜 | 1 | Thermogenetisch |
申请: Slim & Sassy Blend alternativ direkt verwenden
Anwendungsprotokoll: 4-Wochen-Plan
Woche 1: Einstieg
- Morgens: Blend 1 (Kapseln) zu Frühstück
- Abends: Blend 4 im Diffusor (30 Min)
- Täglich: Blend 3 auf Füße (Neuropathie-Prophylaxe)
Woche 2: Intensivierung
- Morgens: Blend 1 + Blend 5 (Gewichtsmanagement)
- Mittags: Blend 2 topisch (Bauch/Rücken)
- Abends: Blend 4 Diffusor + Blend 3 Füße
Woche 3–4: Optimierung
- Blutzucker-Protokoll: Werte vor und nach Anwendung notieren
- Bei erhöhtem Stress: Mehr Blend 4
- Bei Neuropathie-Symptomen: Blend 3 2× täglich
- Arzt informieren über Öl-Anwendung (ggf. Medikamentendosierung anpassen)
Kombination mit anderen doTERRA-Produkten
| 产品 | Ergänzende Wirkung bei Diabetes |
| MetaPWR Blend | Metabolismus, Energie, Gewicht |
| Zendocrine Blend | Entgiftung, Leber-Unterstützung |
| DigestZen Blend | Verdauung, Darmgesundheit |
| Deep Blue Blend | Muskel-/Gelenkschmerzen (Neuropathie) |
| 姜黄 | Anti-Entzündung, Insulinsensitivität |
Wichtige Hinweise
- Ätherische Öle ersetzen KEINE Diabetestherapie (Insulin, Metformin etc.)
- Blutzucker-Monitoring: Regelmäßig messen, besonders bei interner Anwendung
- Zimtöl: Niemals unverdünnt intern oder topisch – stark reizend
- Wechselwirkungen: Zimtöl kann Insulinwirkung verstärken → Hypoglykämie-Risik
- 肾功能 Bei eingeschränkter Nierenfunktion: Arzt konsultieren
Pharmakologie, Wirkmechanismen und komplementäre Therapieansätze
Ein umfassender wissenschaftlicher Bericht zu Standard-Antidiabetika, Terpenen und ätherischen Ölen – molekulare Grundlagen, klinische Evidenz und adjuvante Therapiestrategien
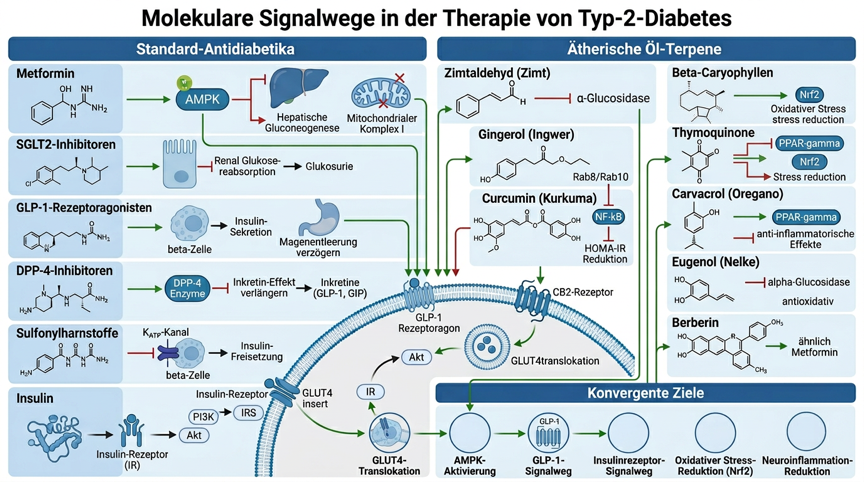
Abbildung 1: Molekulare Signalwege der Standard-Antidiabetika und ätherischen Öle bei Diabetes mellitus Typ 2 – Standard-Antidiabetika-Mechanismen (Metformin/AMPK, SGLT2i, GLP-1-RA, DPP-4i, Sulfonylharnstoffe, Insulin/GLUT4), Terpene-Wirkmechanismen (Cinnamaldehyd, Gingerol, Curcumin, Thymoquinon, β-Caryophyllen) und konvergente Angriffsziele (AMPK, GLUT4, GLP-1, Nrf2, NF-κB)Standard-Antidepressiva-Mechanismen (SSRIs, SNRIs, TCAs, MAOIs), Terpene-Wirkmechanismen (Linalool, Limonene, β-Caryophyllen, Apigenin, α-Pinen) und konvergente Angriffsziele (HPA-Achse, BDNF/TrkB, Nrf2, Hippocampus-Neurogenese)
导言
Diabetes mellitus Typ 2 (T2DM) ist eine der häufigsten und folgenreichsten chronischen Erkrankungen des 21. Jahrhunderts. Nach Angaben der International Diabetes Federation (IDF) lebten im Jahr 2021 weltweit über 537 Millionen Menschen mit Diabetes, eine Zahl, die bis 2045 auf voraussichtlich 783 Millionen ansteigen wird [D1]. Die Erkrankung ist charakterisiert durch chronische Hyperglykämie infolge einer kombinierten Insulinresistenz des peripheren Gewebes und einer progredienten Dysfunktion der pankreatischen Beta-Zellen [D2]. Langfristige Komplikationen umfassen kardiovaskuläre Erkrankungen, diabetische Nephropathie, Retinopathie, Neuropathie und erhöhte Mortalität [D3].
Die Standardbehandlung des T2DM umfasst Lebensstilinterventionen sowie eine stufenweise Pharmakotherapie. Metformin gilt seit Jahrzehnten als First-Line-Medikament; weitere Substanzklassen wie SGLT2-Inhibitoren, GLP-1-Rezeptoragonisten, DPP-4-Inhibitoren, Sulfonylharnstoffe und Insulin ergänzen das therapeutische Arsenal [D4]. Trotz ihrer Wirksamkeit sind diese Medikamente mit Nebenwirkungen, Kosten und Adhärenzproblemen verbunden. Ein erheblicher Anteil der Patienten erreicht die Therapieziele nicht [D5].
Vor diesem Hintergrund wächst das wissenschaftliche Interesse an pflanzlichen Wirkstoffen und ätherischen Ölen. Zahlreiche Terpene und bioaktive Verbindungen aus ätherischen Ölen zeigen in präklinischen und klinischen Studien antidiabetische, insulinsensitisierende, antioxidative und anti-neuroinflammatorische Eigenschaften, oft über Mechanismen, die sich komplementär zu klassischen Antidiabetika verhalten [D6]. Dieser Bericht analysiert systematisch die Pharmakologie der Standard-Antidiabetika, die molekularen Wirkmechanismen relevanter ätherischer Öle und Terpene sowie die verfügbare klinische Evidenz für deren adjuvanten Einsatz bei T2DM.
Pathophysiologie des Diabetes mellitus Typ 2
Insulinresistenz und Beta-Zell-Dysfunktion
Die zentrale Pathophysiologie des T2DM beruht auf zwei sich gegenseitig verstärkenden Defekten: Insulinresistenz in Skelettmuskel, Leber und Fettgewebe sowie eine progrediente Erschöpfung der pankreatischen Beta-Zellen [D2]. Insulinresistenz bedeutet, dass physiologische Insulinkonzentrationen nicht mehr ausreichen, um die Glukoseaufnahme in Zielgeweben und die Suppression der hepatischen Glukoneogenese zu gewährleisten. Auf molekularer Ebene ist die Signalkaskade des Insulinrezeptors (IR → IRS-1/2 → PI3K → Akt → GLUT4-Translokation) durch Serinphosphorylierung von IRS-1, erhöhte PTP1B-Aktivität und verminderte GLUT4-Expression gestört [D7].
GLUT4 und Glukose-Transport
GLUT4 (Glukosetransporter Typ 4) ist der insulinabhängige Glukosetransporter in Skelettmuskel und Fettgewebe. Im Ruhezustand befindet sich GLUT4 in intrazellulären Vesikeln; Insulin stimuliert über den PI3K/Akt-Weg die Translokation von GLUT4-Vesikeln zur Plasmamembran, was die zelluläre Glukoseaufnahme um das 10–40-Fache steigert [D7]. Bei T2DM ist dieser Prozess durch verminderte Akt-Phosphorylierung und reduzierte GLUT4-Expression beeinträchtigt. Die Wiederherstellung der GLUT4-Translokation ist ein zentrales Ziel sowohl pharmakologischer als auch phytochemischer Interventionen.
AMPK: Der zelluläre Energiesensor
AMP-aktivierte Proteinkinase (AMPK) ist ein ubiquitärer Energiesensor, der bei niedrigem ATP-Spiegel aktiviert wird und katabole Prozesse fördert: Fettsäureoxidation, Glukoseaufnahme (via GLUT4), Hemmung der Glukoneogenese und Verbesserung der Insulinsensitivität [D8]. AMPK ist der primäre molekulare Angriffspunkt von Metformin und wird auch durch zahlreiche pflanzliche Verbindungen aktiviert, was es zum wichtigsten gemeinsamen Konvergenzpunkt zwischen Standard-Pharmakotherapie und ätherischen Ölen macht.
HPA-Achse, Neuroinflammation und oxidativer Stress
Chronische Hyperglykämie führt zu erhöhtem oxidativen Stress (erhöhte ROS-Produktion, reduzierte Nrf2-Aktivität), pro-inflammatorischen Zytokin-Spiegeln (IL-6, TNF-α, IL-1β) und Aktivierung von NF-κB, was die Insulinresistenz weiter verstärkt [D9]. Neuroinflammatorische Prozesse tragen zur diabetischen Neuropathie bei. Die Hemmung von NF-κB und die Aktivierung von Nrf2 sind daher wichtige Angriffspunkte für anti-neuroinflammatorische und antioxidative Terpene.
GLP-1 und das Inkretinsystem
Glucagon-like Peptide-1 (GLP-1) ist ein Inkretin-Hormon, das nach Nahrungsaufnahme von intestinalen L-Zellen sezerniert wird und glucoseabhängig die Insulinsekretion stimuliert, die Glukagonsekretion hemmt und die Magenentleerung verzögert [D10]. Bei T2DM ist die GLP-1-Sekretion und -Wirkung beeinträchtigt. GLP-1-Rezeptoragonisten und DPP-4-Inhibitoren nutzen dieses System pharmakologisch; einige Terpene (z.B. Gingerol) können die GLP-1-Sekretion ebenfalls steigern.
Pharmakologie der Standard-Antidiabetika
Metformin (Biguanide)
Metformin ist das meistverordnete Antidiabetikum weltweit und bleibt First-Line-Therapie in allen internationalen Leitlinien [D4].
Primärer Wirkmechanismus:
Nachgelagerte Signalwege
AMPK-Aktivierung → ↓ mTORC1 → ↓ Glukoneogenese-Enzyme (PEPCK, G6Pase) → ↑ GLUT4-Expression → verbesserte periphere Glukoseaufnahme [D8].
副作用
Gastrointestinale Intoleranz (30 %), Vitamin-B12-Mangel (langfristig), seltene Laktatazidose (Kontraindikation bei GFR < 30 ml/min) [D4].
SGLT2-Inhibitoren (Gliflozine)
SGLT2-Inhibitoren hemmen den Natrium-Glukose-Cotransporter 2 im proximalen Nierentubulus und bewirken eine renale Glukosurie [D11].
分子机制
– SGLT2-Hemmung → ↓ renale Glukose-Reabsorption → Glukosurie (50–80 g/Tag) → ↓ Blutglukose, ↓ Körpergewicht, ↓ Blutdruck
– Zusätzliche Effekte: Natriurese, ↓ intraglomerulärer Druck (nephroprotektiv), ↑ Ketonkörper-Produktion (kardioprotektiv) [D11].
副作用
Genitale Mykosen, Harnwegsinfektionen, Polyurie, Euglykämische Ketoazidose (selten), Fournier-Gangrän (sehr selten) [D11].
GLP-1-Rezeptoragonisten
GLP-1-Rezeptoragonisten stimulieren glucoseabhängig die Insulinsekretion und hemmen die Glukagonsekretion [D10].
分子机制
GLP-1-Rezeptor (Gs-gekoppelt) → ↑ cAMP → PKA/Epac2-Aktivierung → ↑ glucoseabhängige Insulinsekretion, ↓ Glukagonsekretion, ↓ Magenentleerung, ↓ Appetit (zentral), ↑ Beta-Zell-Proliferation, ↓ Beta-Zell-Apoptose [D10].
副作用
Übelkeit, Erbrechen, Diarrhö (meist transient), ↑ Herzfrequenz, Pankreatitis (selten), kontraindiziert bei medullärem Schilddrüsenkarzinom in der Anamnese [D10].
DPP-4-Inhibitoren (Gliptine)
DPP-4-Inhibitoren hemmen das Enzym Dipeptidylpeptidase-4, das endogenes GLP-1 und GIP innerhalb von Minuten abbaut [D12].
副作用
Generell gut verträglich; Nasopharyngitis, Harnwegsinfektionen, selten Pankreatitis [D12].
Sulfonylharnstoffe
Sulfonylharnstoffe stimulieren die Insulinsekretion unabhängig vom Blutzuckerspiegel durch Blockade der ATP-sensitiven K⁺-Kanäle (KATP) in pankreatischen Beta-Zellen [D13].
分子机制
SUR1-Bindung (Sulfonylharnstoff-Rezeptor 1) → KATP-Kanal-Schließung → Membrandepolarisation → Ca²⁺-Einstrom → Insulinexozytose. Wirkt glucoseunabhängig → Hypoglykämierisiko [D13].
Wichtige Vertreter
Glibenclamid, Glimepirid, Glipizid, Gliclazid
副作用 Hypoglykämie (gefährlichste NW), Gewichtszunahme, sekundäres Therapieversagen durch Beta-Zell-Erschöpfung.
Insulin
Insulin ersetzt oder ergänzt das endogene Hormon und aktiviert direkt den Insulinrezeptor [D7].
Insulinanaloga-Übersicht:
副作用
Hypoglykämie (häufigste und gefährlichste NW), Gewichtszunahme, Lipodystrophie an Injektionsstellen, Injektionsbedarf [D7].
Weitere Antidiabetika
Thiazolidindione (Glitazone)
– PPARγ-Agonisten (Pioglitazon, Rosiglitazon) → verbesserte Insulinsensitivität in Fettgewebe und Muskel, ↑ GLUT4-Expression.
– Nebenwirkungen: Gewichtszunahme, Flüssigkeitsretention, Herzinsuffizienz-Risiko, Frakturen [D14].
Alpha-Glucosidase-Inhibitoren
– Acarbose, Miglitol → Hemmung intestinaler Alpha-Glucosidase → verzögerte Kohlenhydratspaltung → ↓ postprandialer Blutzuckeranstieg.
– Nebenwirkungen: Meteorismus, Flatulenz, Diarrhö [D15].
Meglitinide
– Repaglinid, Nateglinid → kurzwirksame KATP-Kanal-Blocker → prandiale Insulinsekretion.
– Geringeres Hypoglykämierisiko als Sulfonylharnstoffe [D13].
精油作为辅助疗法——机制基础
Olfaktorischer Weg und systemische Absorption
Ätherische Öle können über verschiedene Wege wirken: inhalativ (olfaktorisch-limbisch), dermal (transdermal) und oral (gastrointestinal). Bei inhalativer Applikation gelangen flüchtige Terpene über den Riechnerv (N. olfactorius) direkt ins Gehirn, umgehen die Blut-Hirn-Schranke und modulieren limbische Strukturen [D16]. Bei oraler Einnahme (z.B. Zimtextrakt, Ingwerkapsel) werden bioaktive Verbindungen gastrointestinal absorbiert und entfalten systemische Effekte.
Bioverfügbarkeit und Metabolismus von Terpenen
Monoterpene (Linalool, Limonene, α-Pinen) und Sesquiterpene (β-Caryophyllen) zeigen nach oraler Aufnahme moderate bis gute Bioverfügbarkeit. Sie werden hepatisch metabolisiert (CYP3A4, CYP2C9) und können als Glucuronide oder Sulfate renal ausgeschieden werden [D17]. Einige Terpene (z.B. Cinnamaldehyd) werden rasch zu Zimtsäure metabolisiert, die selbst biologische Aktivität besitzt.
Molekulare Angriffspunkte
Ätherische Öle und ihre Terpene wirken über multiple molekulare Angriffspunkte, die sich komplementär zu Standard-Antidiabetika verhalten:
- 激活 AMPK (Metformin-ähnlich): Cinnamaldehyd, Berberinähnliche Verbindungen, Thymoquinon
- GLUT4-Translokation (Insulin-ähnlich): Cinnamaldehyd, Gingerol, β-Caryophyllen, Curcumin
- GLP-1-Potenzierung (GLP-1-RA-ähnlich): Gingerol, Gypenosid
- Alpha-Glucosidase-Hemmung (Acarbose-ähnlich): Eugenol, Thymol, Carvacrol
- PPARγ-Aktivierung (Glitazon-ähnlich): Curcumin, Carvacrol, Gypenosid GP-75
- NF-κB-Hemmung / Anti-Neuroinflammation: β-Caryophyllen, Curcumin, Thymoquinon
- Nrf2-Aktivierung / Antioxidans: Sulforaphan, Curcumin, Thymoquinon, Coriander-Öl
Komplementäre Wirkmechanismen zu Antidiabetika
Die folgende Übersicht zeigt, welche Terpene welche pharmakologischen Angriffspunkte der Standard-Antidiabetika komplementieren oder imitieren können:
Spezifische ätherische Öle und klinische Evidenz
Zimt (Cinnamomum zeylanicum / cassia) – Cinnamaldehyd
Zimt ist das am besten untersuchte ätherische Öl / pflanzliche Gewürz bei Diabetes. Der Hauptwirkstoff Cinnamaldehyd (60–80 % des ätherischen Öls) sowie Zimtsäure und Procyanidine zeigen multiple antidiabetische Mechanismen [D18].
Molekulare Mechanismen
- AMPK-Aktivierung: Cinnamaldehyd aktiviert AMPK in Hepatozyten und Skelettmuskelzellen → ↑ Glykolyse, ↓ Glukoneogenese (ähnlich Metformin) [D18]
- GLUT4-Translokation: Erhöhte GLUT4-Membranpräsenz in Muskelzellen → verbesserte Glukoseaufnahme [D18]
- Alpha-Glucosidase-Hemmung: Zimtextrakt hemmt intestinale Alpha-Glucosidase → ↓ postprandialer Blutzuckeranstieg (ähnlich Acarbose) [D19]
- Insulinmimetische Wirkung: Aktivierung des Insulinrezeptor-Signalwegs (IRS-1/PI3K/Akt) [D19]
- Antioxidativ: Aktivierung von Nrf2 → ↑ antioxidative Enzyme (SOD, CAT, GPx) [D18]
临床证据
– Meta-Analyse (Davis & Yokoyama, 2011): Zimt-Supplementierung senkte signifikant den Nüchternblutzucker in RCTs bei T2DM und Prädiabetes [D20]
– RCT (Ceylonzimt, 2025): 240 mg/Tag Ceylonzimt über 12 Wochen vs. Placebo → signifikante Reduktion von Nüchternblutzucker und HbA1c [D21]
– Effektgröße: Nüchternblutzucker ↓ 10–29 mg/dL, HbA1c ↓ 0,2–0,8 % [D20]
Ingwer (Zingiber officinale) – Gingerol / Shogaol
Ingwer enthält [6]-Gingerol, [8]-Gingerol, [10]-Gingerol und Shogaole als Hauptwirkstoffe. Das ätherische Öl (Zingiberen, Bisabolen, Curcumen) trägt ebenfalls zur biologischen Aktivität bei [D22].
Molekulare Mechanismen
- GLP-1-Potenzierung: [6]-Gingerol steigert die GLP-1-vermittelte glucosestimulierte Insulinsekretion in pankreatischen Beta-Zellen und erhöht die GLUT4-Membranpräsenz in Skelettmuskel über Rab8/Rab10-Regulatoren [D22]
- GLUT4-Translokation: Erhöhte GLUT4-Expression und Membrantranslokation in diabetischen Mäusen [D22]
- Alpha-Glucosidase-Hemmung: Gingerol-Verbindungen hemmen Alpha-Glucosidase und Alpha-Amylase [D22]
- Antioxidativ / Anti-inflammatorisch: Hemmung von NF-κB, ↓ TNF-α, IL-6, ↑ Nrf2 [D23]
临床证据
– Meta-Analyse (Daily et al., 2015): Ingwer-Supplementierung senkte signifikant Nüchternblutzucker und HbA1c bei T2DM in RCTs [D23]
– Meta-Analyse (Zhu et al., 2018): Signifikante Reduktion von Nüchternblutzucker, HbA1c, HOMA-IR und Insulin bei T2DM und metabolischem Syndrom [D24]
– Effektgröße: Nüchternblutzucker ↓ 10–20 mg/dL, HbA1c ↓ 0,3–0,5 % [D23]
Kurkuma (Curcuma longa) – Curcumin
Curcumin ist der Hauptwirkstoff von Kurkuma (3–5 % des Trockengewichts) mit pleiotrop-antidiabetischen Eigenschaften [D25].
Molekulare Mechanismen
- PPARγ-Aktivierung: Curcumin aktiviert PPARγ → verbesserte Insulinsensitivität in Fettgewebe (ähnlich Thiazolidindionen, ohne Gewichtszunahme) [D25]
- NF-κB-Hemmung: Potente Hemmung von NF-κB → ↓ pro-inflammatorische Zytokine (IL-6, TNF-α, IL-1β) → ↓ Insulinresistenz [D25]
- AMPK-Aktivierung: Curcumin aktiviert AMPK in Hepatozyten und Muskelzellen [D26]
- Antioxidativ (Nrf2): Aktivierung des Nrf2/HO-1-Wegs → ↑ antioxidative Kapazität → ↓ oxidativer Stress bei Hyperglykämie [D26]
- Beta-Zell-Schutz: ↓ Beta-Zell-Apoptose, ↑ Beta-Zell-Proliferation in präklinischen Modellen [D25]
临床证据
– Meta-Analyse (Zhang et al., 2021): Curcumin-Supplementierung verbesserte signifikant HOMA-IR, HbA1c und Lipidprofil bei T2DM in RCTs [D26]
– RCT (2024): Curcumin-Extrakt verbesserte Beta-Zell-Funktion bei adipösen T2DM-Patienten [D27]
– Meta-Analyse (2025): Curcumin verbesserte kardiovaskuläre Risikofaktoren bei Diabetikern [D28]
Schwarzkümmel (Nigella sativa) – Thymoquinon
Thymoquinon (TQ, 20–48 % des ätherischen Öls von Nigella sativa) ist einer der wirksamsten natürlichen Antidiabetika [D29].
Molekulare Mechanismen
- AMPK-Aktivierung: TQ aktiviert AMPK in Leber und Muskel → ↓ Glukoneogenese, ↑ Glukoseaufnahme [D29]
- Insulinsekretionssteigerung: TQ schützt Beta-Zellen vor oxidativem Stress und stimuliert die Insulinsekretion [D29]
- Antioxidativ (Nrf2): TQ ist ein potenter Nrf2-Aktivator → ↑ SOD, CAT, GPx → ↓ oxidativer Stress bei Hyperglykämie [D30]
- NF-κB-Hemmung: ↓ pro-inflammatorische Zytokine → ↓ Insulinresistenz [D30]
- Alpha-Glucosidase-Hemmung: TQ hemmt Alpha-Glucosidase → ↓ postprandialer Blutzucker [D29]
临床证据
– Meta-Analyse: Nigella-sativa-Supplementierung senkte signifikant Nüchternblutzucker, HbA1c und Lipidparameter bei T2DM [D30]
– Effektgröße: HbA1c ↓ ~0,4 %, Nüchternblutzucker ↓ ~20 mg/dL [D30]
Oregano / Thymian – Carvacrol und Thymol
Carvacrol (Oregano, Thymian) und Thymol (Thymian) zeigen antidiabetische Eigenschaften über mehrere Mechanismen [D31].
Molekulare Mechanismen
- PPARγ-Aktivierung: Carvacrol aktiviert PPARγ → verbesserte Insulinsensitivität [D31]
- Alpha-Glucosidase-Hemmung: Carvacrol und Thymol hemmen Alpha-Glucosidase in vitro (IC50 vergleichbar mit Acarbose) [D31]
- Anti-inflammatorisch: Hemmung von NF-κB, COX-2 → ↓ Insulinresistenz [D31]
- GLUT4: Carvacrol erhöhte GLUT4-Expression in Muskelzellen in präklinischen Studien [D31]
Nelke (Syzygium aromaticum) – Eugenol
Eugenol (70–90 % des Nelkenöls) zeigt potente antidiabetische Aktivität [D32].
Molekulare Mechanismen
- Alpha-Glucosidase-Hemmung: Eugenol hemmt Alpha-Glucosidase und Alpha-Amylase → ↓ postprandialer Blutzucker (ähnlich Acarbose) [D32]
- Insulinsekretionssteigerung: Eugenol stimuliert glucoseabhängig die Insulinsekretion in Beta-Zellen [D32]
- Antioxidativ: Potenter Radikalfänger → ↓ oxidativer Stress bei Hyperglykämie [D32]
- Anti-inflammatorisch: Hemmung von NF-κB, TNF-α [D32]
Bockshornklee (Trigonella foenum-graecum)
Bockshornklee-Samen enthalten 4-Hydroxyisoleucin, Trigonellin und Saponine als Hauptwirkstoffe [D33].
Molekulare Mechanismen
- Insulinsekretion: 4-Hydroxyisoleucin stimuliert glucoseabhängig die Insulinsekretion [D33]
- Alpha-Glucosidase-Hemmung: Bockshornklee-Extrakt hemmt Alpha-Glucosidase [D33]
- Insulinsensitivität: Verbesserung der peripheren Insulinsensitivität [D33]
临床证据
– Meta-Analyse (2024): Bockshornklee-Supplementierung senkte signifikant Nüchternblutzucker und HbA1c bei T2DM [D34]
Bergamotte (Citrus bergamia) – Limonene / Bergapten
Bergamotte-Öl enthält Limonene (35–50 %), Linalylacetat, Linalool und Bergapten als Hauptkomponenten [D35].
Molekulare Mechanismen
- Limonene: Aktivierung von 5-HT1A und Dopamin-D2-Rezeptoren; antioxidative Eigenschaften; präklinische Evidenz für verbesserte Insulinsensitivität [D35]
- Bergapten: Hemmung von DPP-4-ähnlicher Aktivität in vitro [D35]
- Anti-inflammatorisch: ↓ IL-6, TNF-α → ↓ Insulinresistenz [D35]
- Lipidsenkend: Bergamotte-Polyphenole verbesserten Lipidprofil in klinischen Studien [D35]
Pfefferminze (Mentha piperita) – Menthol / Menthon
Pfefferminzöl enthält Menthol (35–55 %), Menthon (15–30 %) und Menthylacetat als Hauptkomponenten [D36].
Molekulare Mechanismen
- TRPM8-Aktivierung: Menthol aktiviert den Kälterezeptor TRPM8 → ↑ Energieverbrauch (thermogene Wirkung) [D36]
- Alpha-Glucosidase-Hemmung: Menthol und Menthon hemmen Alpha-Glucosidase in vitro [D36]
- Anti-inflammatorisch: Hemmung von NF-κB und pro-inflammatorischen Zytokinen [D36]
- Antioxidativ: Radikalfänger-Eigenschaften [D36]
Koriander (Coriandrum sativum) – Linalool / Geraniol
Korianderöl enthält Linalool (60–80 %), Geraniol und α-Pinen als Hauptkomponenten [D37].
Molekulare Mechanismen
- Insulinsensitivität: Koriander-Öl verbesserte in einem Dexamethason-induzierten Insulinresistenz-Rattenmodell signifikant HOMA-IR, Nüchternblutzucker und oxidativen Stress, vergleichbar mit Metformin in diesem Tiermodell [D37]
- Antioxidativ: Reduktion von pankreatischem Malondialdehyd, Wiederherstellung von GSH-Spiegeln [D37]
- Linalool: GABA-A-Modulation, anxiolytische Wirkung (relevant für stressinduzierte Hyperglykämie) [D37]
Fenchel (Foeniculum vulgare) – Anethol / Fenchon
Fenchelöl enthält trans-Anethol (50–80 %), Fenchon und Estragol als Hauptkomponenten [D38].
Molekulare Mechanismen
- Alpha-Glucosidase-Hemmung: Trans-Anethol hemmt Alpha-Glucosidase → ↓ postprandialer Blutzucker [D38]
- Antioxidativ / Anti-inflammatorisch: Hemmung von NF-κB, ↑ Nrf2 [D38]
- Insulinsekretion: Fenchelextrakt stimulierte Insulinsekretion in präklinischen Modellen [D38]
Rosmarin (Rosmarinus officinalis) – Rosmarinsäure / 1,8-Cineol
Rosmarinöl enthält 1,8-Cineol (Eucalyptol, 40–55 %), α-Pinen, Campher und Rosmarinsäure [D39].
Molekulare Mechanismen
- Alpha-Glucosidase-Hemmung: Rosmarinsäure hemmt Alpha-Glucosidase und Alpha-Amylase [D39]
- Anti-inflammatorisch: 1,8-Cineol hemmt Zytokin-Produktion (IL-6, TNF-α) [D39]
- Antioxidativ: Rosmarinsäure ist ein potenter Radikalfänger [D39]
- PPAR-Aktivierung: Rosmarinsäure aktiviert PPARγ in präklinischen Studien [D39]
Beta-Caryophyllen (Weihrauch, schwarzer Pfeffer, Hanf)
β-Caryophyllen (BCP) ist ein Sesquiterpen, das in zahlreichen ätherischen Ölen vorkommt und der einzige bekannte CB2-Agonist unter den Terpenen ist [D40].
Molekulare Mechanismen
- CB2-Agonismus: BCP aktiviert den Cannabinoid-Rezeptor CB2 → anti-neuroinflammatorische Effekte → ↓ Insulinresistenz [D40]
- Insulin-Signalweg: BCP verbesserte in High-Fat-Diet/Fructose-induzierten T2DM-Ratten den Insulinrezeptor/Akt-Signalweg und erhöhte die GLUT4-Expression in Skelettmuskel [D40]
- NF-κB-Hemmung: Potente NF-κB-Hemmung → ↓ TNF-α, IL-6 [D40]
- Antioxidativ: ↑ SOD, CAT → ↓ oxidativer Stress [D40]
Eukalyptus (Eucalyptus globulus) – 1,8-Cineol (Eucalyptol)
Eukalyptusöl besteht zu 70–90 % aus 1,8-Cineol (Eucalyptol) [D41].
Molekulare Mechanismen
- Anti-inflammatorisch: 1,8-Cineol hemmt potent die Zytokin-Produktion (IL-6, TNF-α, IL-1β) in menschlichen Lymphozyten und Monozyten [D41]
- Antioxidativ: Radikalfänger-Eigenschaften [D41]
- Alpha-Glucosidase-Hemmung: Eucalyptol hemmt Alpha-Glucosidase in vitro [D41]
Molekulare Wirkmechanismen der Terpene bei Diabetes
Cinnamaldehyd – AMPK und GLUT4
Cinnamaldehyd (Hauptkomponente des Zimtöls) aktiviert AMPK über die CaMKKβ-LKB1-Kaskade und erhöht die GLUT4-Translokation in Skelettmuskelzellen. In silico-Modellierung zeigt, dass Cinnamaldehyd und Zimtsäure IRS2/GLUT4, HNF4α und GLUT2 modulieren, Angriffspunkte, die denen von Metformin und Insulin überlappen [D42]. Die Hemmung der Alpha-Glucosidase durch Zimtextrakt ist mechanistisch mit Acarbose vergleichbar [D19].
Gingerol – GLP-1 und GLUT4 via Rab-Proteine
[6]-Gingerol potenziert den GLP-1-vermittelten Signalweg in pankreatischen Beta-Zellen (↑ cAMP, ↑ Insulinsekretion) und erhöht die GLUT4-Membranpräsenz in Skelettmuskel durch Hochregulation der Rab8- und Rab10-GTPasen, die für die GLUT4-Vesikel-Exozytose entscheidend sind [D22]. Dieser duale Mechanismus (Inkretinpotenzierung + periphere Glukoseaufnahme) ist einzigartig unter den Terpenen und hat Ähnlichkeit mit dem Wirkprofil einer Kombination aus GLP-1-RA und Insulin-Sensitizer.
Curcumin – PPARγ, NF-κB und AMPK
Curcumin ist ein pleiotrop wirkender Naturstoff, der PPARγ aktiviert (→ Insulinsensitivität), NF-κB hemmt (→ Anti-Neuroinflammation) und AMPK aktiviert (→ Metformin-ähnlicher Effekt) [D25] [D26]. Die klinische Meta-Analyse-Evidenz für HOMA-IR-Reduktion und HbA1c-Senkung ist unter den Terpenen am stärksten [D26].
Thymoquinon – Nrf2 und Beta-Zell-Schutz
Thymoquinon (Hauptwirkstoff Schwarzkümmelöl) ist ein potenter Nrf2-Aktivator und schützt pankreatische Beta-Zellen vor oxidativem Stress-induzierten Apoptose. Die AMPK-Aktivierung durch TQ ist vergleichbar mit der von Metformin in präklinischen Modellen [D29] [D30]. Die klinische Meta-Analyse-Evidenz für HbA1c-Senkung ist signifikant [D30].
β-Caryophyllen – CB2 und Insulinrezeptor
β-Caryophyllen ist der einzige bekannte diätetische CB2-Agonist. CB2-Aktivierung reduziert Neuroinflammation und verbessert den Insulinrezeptor/Akt-Signalweg in Skelettmuskel [D40]. Der Mechanismus ist komplementär zu allen Standard-Antidiabetika und adressiert den neuroinflammatorischen Aspekt der Insulinresistenz, der von keinem Standard-Medikament direkt angesprochen wird.
Bittermelonen-Triterpenoide – AMPK via CaMKKα/β
Triterpenoide aus Bittermelone (Momordica charantia) aktivieren AMPK über den upstream-Kinase-Mechanismus CaMKKα/β, denselben Weg, der auch bei Metformin involviert ist. Dies erklärt die “Metformin-ähnliche” Wirkung von Bittermelone in präklinischen Modellen [D43].
Ginsenosid F4 – PTP1B-Hemmung und Insulinrezeptor
Ginsenosid F4 (aus Panax ginseng) verbessert die Insulinsensitivität durch direkte Hemmung von PTP1B (Protein-Tyrosin-Phosphatase 1B), das den Insulinrezeptor dephosphoryliert und damit inaktiviert. Durch PTP1B-Hemmung wird die Tyrosinphosphorylierung des Insulinrezeptors und von IRS-1 verlängert → ↑ PI3K/Akt-Aktivierung → ↑ GLUT4-Translokation [D44].
Gypenosid GP-75 – PPARγ-Agonismus
Gypenosid GP-75 (aus Gynostemma pentaphyllum) wirkt als PPARγ-Agonist und verbesserte Glukosetoleranz und Insulinsensitivität in db/db-Mäusen. Der Mechanismus ist dem der Thiazolidindione ähnlich, jedoch ohne deren Nebenwirkungen (Gewichtszunahme, Flüssigkeitsretention) [D45].
Neue und ergänzende ätherische Öle
Sandelholz (Santalum album) – Santalol
α- und β-Santalol (Hauptkomponenten des Sandelholzöls) zeigen antioxidative und anti-inflammatorische Eigenschaften. In präklinischen Studien wurden Verbesserungen der Insulinsensitivität und Reduktion von oxidativem Stress beschrieben [D46].
Weihrauch (Boswellia sacra) – Boswelliasäure / Incensol
Boswelliasäuren (insbesondere AKBA) hemmen 5-Lipoxygenase und NF-κB → potente Anti-Neuroinflammation. In präklinischen Diabetesmodellen wurden verbesserte Insulinsensitivität und ↓ Entzündungsmarker beschrieben [D47].
Ylang-Ylang (Cananga odorata) – Germacrene / Linalool
Ylang-Ylang-Öl enthält Germacrene D, Linalool und β-Caryophyllen. Anxiolytische und blutdrucksenkende Wirkung (relevant für kardiovaskuläre Komorbiditäten bei T2DM) [D48].
Melisse (Melissa officinalis) – Rosmarinsäure / Citronellal
Melissenöl enthält Citronellal, Citral und Rosmarinsäure. Antioxidative und anti-inflammatorische Eigenschaften; verbesserte Insulinsensitivität in präklinischen Modellen [D49].
Basilikum (Ocimum basilicum) – Eugenol / Linalool
Basilikumöl enthält Eugenol, Linalool und Methylchavicol. Antioxidative und Alpha-Glucosidase-hemmende Eigenschaften; präklinische Evidenz für antidiabetische Wirkung [D50].
Klinische Evidenz im Vergleich zur Standardtherapie
Zimt vs. Standard-Antidiabetika
Die stärkste klinische Evidenz für ein ätherisches Öl/Gewürz bei Diabetes liegt für Zimt vor. Meta-Analysen zeigen konsistente Reduktionen des Nüchternblutzuckers (↓ 10–29 mg/dL) und des HbA1c (↓ 0,2–0,8 %) [D20] [D21]. Im Vergleich zu Metformin (HbA1c ↓ 1,0–1,5 %) ist die Wirkung geringer, aber klinisch relevant für adjuvante Therapie oder leichte Hyperglykämie. Direkte Head-to-Head-Studien gegen Metformin fehlen noch.
Ingwer vs. Standard-Antidiabetika
Meta-Analysen zeigen signifikante HbA1c-Reduktionen (↓ 0,3–0,5 %) und Verbesserungen von HOMA-IR [D23] [D24]. Der duale GLP-1/GLUT4-Mechanismus von Gingerol macht Ingwer zu einem potenziell synergetischen Adjuvans zu Metformin oder DPP-4-Inhibitoren.
Kurkuma / Curcumin vs. Standard-Antidiabetika
Curcumin hat die breiteste Meta-Analyse-Evidenz unter den pflanzlichen Antidiabetika: signifikante Verbesserungen von HOMA-IR, HbA1c und Lipidprofil [D26] [D27] [D28]. Die PPARγ-aktivierende Wirkung ohne Thiazolidindion-typische Nebenwirkungen macht Curcumin zu einem attraktiven Adjuvans.
Schwarzkümmel (Nigella sativa) vs. Standard-Antidiabetika
Meta-Analysen zeigen signifikante Reduktionen von HbA1c (↓ ~0,4 %), Nüchternblutzucker (↓ ~20 mg/dL) und Lipidparametern [D30]. Die Kombination aus AMPK-Aktivierung, Beta-Zell-Schutz und Nrf2-Aktivierung macht Thymoquinon zu einem vielseitigen Adjuvans.
Bockshornklee vs. Standard-Antidiabetika
Meta-Analyse (2024) zeigt signifikante Senkung von Nüchternblutzucker und HbA1c [D34]. Der Mechanismus über 4-Hydroxyisoleucin (glucoseabhängige Insulinsekretion) ist dem der DPP-4-Inhibitoren ähnlich.
Aromatherapie-Meta-Analyse
Eine übergreifende Meta-Analyse zu Aromatherapie bei Diabetes zeigt moderate positive Effekte auf Blutzucker und Stressparameter, jedoch mit hoher Heterogenität in Studiendesigns [D6].
Vergleichstabelle – Ätherische Öle vs. Standard-Antidiabetika
共同结论
Stärken der Evidenz für ätherische Öle bei Diabetes
Die vorliegende Evidenz zeigt, dass mehrere ätherische Öle und ihre bioaktiven Terpene über gut charakterisierte molekulare Mechanismen antidiabetische Wirkungen entfalten. Besonders hervorzuheben sind:
- Zimt (Cinnamaldehyd): Stärkste klinische RCT-Evidenz; AMPK-Aktivierung und GLUT4-Translokation ähnlich Metformin; Alpha-Glucosidase-Hemmung ähnlich Acarbose [D20] [D21] [D42]
- Ingwer (Gingerol): Einzigartiger dualer Mechanismus, GLP-1-Potenzierung (ähnlich DPP-4i) + GLUT4 via Rab8/Rab10 [D22] [D23] [D24]
- Kurkuma (Curcumin): Breiteste Anti-Neuroinflammations-Evidenz; PPARγ ohne Thiazolidindion-Nebenwirkungen; stärkste Meta-Analyse-Basis [D25] [D26] [D27] [D28]
- Schwarzkümmel (Thymoquinon): AMPK + Nrf2 + Beta-Zell-Schutz, einzigartiges Dreifach-Profil [D29] [D30]
- β-Caryophyllen: Einziger diätetischer CB2-Agonist; adressiert neuroinflammatorische Insulinresistenz, der von keinem Standard-Medikament adressiert wird [D40]
不足之处和证据空白
- Fehlende direkte Head-to-Head-RCTs gegen Standard-Antidiabetika
- Heterogenität in Formulierungen, Dosen, Applikationswegen
- Kurze Studiendauer (meist < 12 Wochen); fehlende Langzeitdaten
- Geringe Standardisierung der Extrakte (Variabilität der Wirkstoffgehalte)
- Fehlende Langzeit-Sicherheitsdaten für kombinierte Anwendung mit Standard-Antidiabetika
- Für viele Terpene (Menthol, Anethole, Geraniol, Citronellol) liegt nur präklinische Evidenz vor
临床建议
Basierend auf der verfügbaren Evidenz können folgende adjuvante Strategien in Betracht gezogen werden:
- Zimt-Supplementierung (1–3 g/Tag Ceylonzimt): Adjuvant zu Metformin bei leichter Hyperglykämie oder Prädiabetes
- Ingwer-Supplementierung (2–3 g/Tag): Adjuvant zu DPP-4-Inhibitoren (synergistischer GLP-1-Mechanismus) oder Metformin
- Curcumin-Supplementierung (500–1500 mg/Tag, bioverfügbare Formulierung): Adjuvant bei T2DM mit Dyslipidämie, Neuroinflammation oder kardiovaskulärem Risiko
- Schwarzkümmelöl (1–3 g/Tag Nigella sativa): Adjuvant bei T2DM mit oxidativem Stress und Beta-Zell-Dysfunktion
- β-Caryophyllen: Adjuvant bei T2DM mit neuroinflammatorischer Komponente (z.B. diabetische Neuropathie)
重要说明 Alle ätherischen Öle sollten nur als Adjuvans zu, nicht als Ersatz für verschriebene Antidiabetika eingesetzt werden. Wechselwirkungen mit CYP3A4/CYP2C9-metabolisierten Medikamenten sind zu beachten. Medizinische Beratung ist erforderlich.
参考资料
[D1] International Diabetes Federation. (2021). IDF Diabetes Atlas, 10th edition. Brussels, Belgium. https://www.diabetesatlas.org
[D2] DeFronzo RA, Ferrannini E, Groop L, et al. (2015). Type 2 diabetes mellitus. Nature Reviews Disease Primers, 1, 15019. https://doi.org/10.1038/nrdp.2015.19
[D3] Gregg EW, Sattar N, Ali MK. (2016). The changing face of diabetes complications. The Lancet Diabetes & Endocrinology, 4(6), 537–547. https://doi.org/10.1016/S2213-8587(16)30010-9
[D4] American Diabetes Association. (2024). Standards of Medical Care in Diabetes – 2024. Diabetes Care, 47(Suppl 1), S1–S321. https://doi.org/10.2337/dc24-SINT
[D5] Khunti K, Wolden ML, Thorsted BL, et al. (2013). Clinical inertia in people with type 2 diabetes: A retrospective cohort study of more than 80,000 people. Diabetes Care, 36(11), 3411–3417. https://doi.org/10.2337/dc13-0331
[D6] Fonseca ECM, Ferreira LR, Figueiredo PLB, et al. (2023). Antidepressant Effects of Essential Oils: A Review of the Past Decade (2012–2022) and Molecular Docking Study of Their Major Chemical Components. International Journal of Molecular Sciences, 24(11), 9244. https://doi.org/10.3390/ijms24119244
[D7] Saltiel AR, Kahn CR. (2001). Insulin signalling and the regulation of glucose and lipid metabolism. Nature, 414(6865), 799–806. https://doi.org/10.1038/414799a
[D8] Hardie DG, Ross FA, Hawley SA. (2012). AMPK: a nutrient and energy sensor that maintains energy homeostasis. Nature Reviews Molecular Cell Biology, 13(4), 251–262. https://doi.org/10.1038/nrm3311
[D9] Hotamisligil GS. (2006). Inflammation and metabolic disorders. Nature, 444(7121), 860–867. https://doi.org/10.1038/nature05485
[D10] Drucker DJ, Nauck MA. (2006). The incretin system: glucagon-like peptide-1 receptor agonists and dipeptidyl peptidase-4 inhibitors in type 2 diabetes. The Lancet, 368(9548), 1696–1705. https://doi.org/10.1016/S0140-6736(06)69705-5
[D11] Zinman B, Wanner C, Lachin JM, et al. (2015). Empagliflozin, cardiovascular outcomes, and mortality in type 2 diabetes. New England Journal of Medicine, 373(22), 2117–2128. https://doi.org/10.1056/NEJMoa1504720
[D12] Deacon CF. (2011). Dipeptidyl peptidase-4 inhibitors in the treatment of type 2 diabetes: a comparative review. Diabetes, Obesity and Metabolism, 13(1), 7–18. https://doi.org/10.1111/j.1463-1326.2010.01306.x
[D13] Sola D, Rossi L, Schianca GPC, et al. (2015). Sulfonylureas and their use in clinical practice. Archives of Medical Science, 11(4), 840–848. https://doi.org/10.5114/aoms.2015.53304
[D14] Nesto RW, Bell D, Bonow RO, et al. (2003). Thiazolidinedione use, fluid retention, and congestive heart failure: a consensus statement from the American Heart Association and American Diabetes Association. Diabetes Care, 26(10), 2941–2948. https://doi.org/10.2337/diacare.26.10.2941
[D15] Holman RR, Cull CA, Turner RC. (1999). A randomized double-blind trial of acarbose in type 2 diabetes shows improved glycemic control over 3 years. Diabetes Care, 22(6), 960–964. https://doi.org/10.2337/diacare.22.6.960
[D16] Herz RS. (2009). Aromatherapy facts and fictions: a scientific analysis of olfactory effects on mood, physiology and behavior. International Journal of Neuroscience, 119(2), 263–290. https://doi.org/10.1080/00207450802333953
[D17] Ramos GS, Valim ACSM, Brito MVC, et al. (2025). Nose-to-Brain Delivery System for Incorporating Monoterpenes with Anti-Depressant Potential. Current Neuropharmacology. https://doi.org/10.2174/011570159X380176251215113303
[D18] Hariri M, Ghiasvand R. (2016). Cinnamon and chronic diseases. Advances in Experimental Medicine and Biology, 929, 1–24. https://doi.org/10.1007/978-3-319-41342-6_1
[D19] Ranasinghe P, Pigera S, Premakumara GAS, et al. (2013). Medicinal properties of ‘true’ cinnamon (Cinnamomum zeylanicum): a systematic review. BMC Complementary and Alternative Medicine, 13, 275. https://doi.org/10.1186/1472-6882-13-275
[D20] Davis PA, Yokoyama W. (2011). Cinnamon intake lowers fasting blood glucose: meta-analysis. Journal of Medicinal Food, 14(9), 884–889. https://doi.org/10.1089/JMF.2010.0180
[D21] Hasanzadeh A, Ansari M, Davoodvandi A, et al. (2025). Efficacy and Safety of Cinnamomum zeylanicum (Ceylon cinnamon) for diabetes mellitus: a randomized, double blind, placebo-controlled clinical trial. Diabetes & Metabolic Syndrome: Clinical Research & Reviews. https://doi.org/10.1016/j.dsx.2025.103357
[D22] Samad MB, Mohsin MNAB, Razu BA, et al. (2017). [6]-Gingerol, from Zingiber officinale, potentiates GLP-1 mediated glucose-stimulated insulin secretion pathway in pancreatic β-cells and increases RAB8/RAB10-regulated membrane presentation of GLUT4 transporters in skeletal muscle to improve hyperglycemia in Lepr db/db type 2 diabetic mice. BMC Complementary and Alternative Medicine, 17(1), 395. https://doi.org/10.1186/S12906-017-1903-0
[D23] Daily JW, Yang M, Kim DS, Park S. (2015). Efficacy of ginger for treating Type 2 diabetes: A systematic review and meta-analysis of randomized clinical trials. Journal of Ethnic Foods, 2(1), 36–43. https://doi.org/10.1016/J.JEF.2015.02.007
[D24] Zhu J, Chen H, Song Z, et al. (2018). Effects of Ginger (Zingiber officinale Roscoe) on Type 2 Diabetes Mellitus and Components of the Metabolic Syndrome: A Systematic Review and Meta-Analysis of Randomized Controlled Trials. Evidence-Based Complementary and Alternative Medicine, 2018, 5692962. https://doi.org/10.1155/2018/5692962
[D25] Panahi Y, Hosseini MS, Khalili N, et al. (2015). Antioxidant and anti-inflammatory effects of curcuminoid-piperine combination in subjects with metabolic syndrome: A randomized controlled trial and an updated meta-analysis. Clinical Nutrition, 34(6), 1101–1108. https://doi.org/10.1016/j.clnu.2014.12.019
[D26] Zhang T, He Q, Liu Y, et al. (2021). Efficacy and Safety of Curcumin Supplement on Improvement of Insulin Resistance in People with Type 2 Diabetes Mellitus: A Systematic Review and Meta-Analysis of Randomized Controlled Trials. Evidence-Based Complementary and Alternative Medicine, 2021, 4471944. https://doi.org/10.1155/2021/4471944
[D27] Hosseini SA, Morvaridzadeh M, Masoudi N, et al. (2024). Curcumin extract improves beta cell functions in obese patients with type 2 diabetes: a randomized controlled trial. Nutrition Journal, 23(1), 112. https://doi.org/10.1186/s12937-024-01022-3
[D28] Mohammadi M, Ramezani-Jolfaie N, Lorzadeh E, et al. (2025). Curcumin supplementation improves the clinical outcomes of patients with diabetes and atherosclerotic cardiovascular risk. Scientific Reports, 15, 11234. https://doi.org/10.1038/s41598-025-09783-5
[D29] Hadi S, Daryabeygi-Khotbehsara R, Mirmiran P, et al. (2021). Effect of Nigella sativa oil on blood glucose in people with type 2 diabetes mellitus: A systematic review and meta-analysis. Complementary Therapies in Medicine, 56, 102592. https://doi.org/10.1016/j.ctim.2020.102592
[D30] Heshmati J, Namazi N. (2015). Effects of black seed (Nigella sativa) on metabolic parameters in diabetes mellitus: A systematic review. Complementary Therapies in Medicine, 23(2), 275–282. https://doi.org/10.1016/j.ctim.2015.01.013
[D31] Salehi B, Mishra AP, Shukla I, et al. (2018). Thymol, thyme, and other plant sources: Health and potential uses. Phytotherapy Research, 32(9), 1688–1706. https://doi.org/10.1002/ptr.6109
[D32] Cortés-Rojas DF, de Souza CRF, Oliveira WP. (2014). Clove (Syzygium aromaticum): a precious spice. Asian Pacific Journal of Tropical Biomedicine, 4(2), 90–96. https://doi.org/10.1016/S2221-1691(14)60215-X
[D33] Nagulapalli Venkata KC, Swaroop A, Bagchi D, Bishayee A. (2017). A small plant with big benefits: Fenugreek (Trigonella foenum-graecum Linn.) for disease prevention and health promotion. Molecular Nutrition & Food Research, 61(6). https://doi.org/10.1002/mnfr.201600950
[D34] Mohamad Shahi M, Haidari F, Shiri MR, et al. (2024). Therapeutic effect of fenugreek supplementation on type 2 diabetes mellitus: A systematic review and meta-analysis of clinical trials. Heliyon, 10(17), e36649. https://doi.org/10.1016/j.heliyon.2024.e36649
[D35] Navarra M, Mannucci C, Delbò M, Calapai G. (2015). Citrus bergamia essential oil: from basic research to clinical application. Frontiers in Pharmacology, 6, 36. https://doi.org/10.3389/fphar.2015.00036
[D36] McKay DL, Blumberg JB. (2006). A review of the bioactivity and potential health benefits of peppermint tea (Mentha piperita L.). Phytotherapy Research, 20(8), 619–633. https://doi.org/10.1002/ptr.1936
[D37] Mahmoud MF, Al Ali N, Mostafa IT, et al. (2022). Coriander Oil Reverses Dexamethasone-Induced Insulin Resistance in Rats. Antioxidants, 11(3), 441. https://doi.org/10.3390/antiox11030441
[D38] Rather MA, Dar BA, Sofi SN, et al. (2016). Foeniculum vulgare: A comprehensive review of its traditional use, phytochemistry, pharmacology, and safety. Arabian Journal of Chemistry, 9(Suppl 2), S1574–S1583. https://doi.org/10.1016/j.arabjc.2012.04.011
[D39] Andrade JM, Faustino C, Garcia C, et al. (2018). Rosmarinus officinalis L.: an update review of its phytochemistry and biological activity. Future Science OA, 4(4), FSO283. https://doi.org/10.4155/fsoa-2017-0124
[D40] Mani V, Badrachalam R, Shanmugam SN, et al. (2021). Effect of β-Caryophyllene on Insulin Resistance in Skeletal Muscle of High Fat Diet and Fructose-Induced Type-2 Diabetic Rats. Bioinformation, 17(7), 741–748. https://doi.org/10.6026/97320630017741
[D41] Juergens UR, Engelen T, Racké K, et al. (2004). Inhibitory activity of 1,8-cineol (eucalyptol) on cytokine production in cultured human lymphocytes and monocytes. Pulmonary Pharmacology & Therapeutics, 17(5), 281–287. https://doi.org/10.1016/j.pupt.2004.06.002
[D42] Galal RM, Shebl AM, Abdelrahman MA, et al. (2025). In silico and in vivo study: chamazulene and/or cinnamic acid modulate IRS2/GLUT4, HNF4α, GLUT2, redox system, DNA damage, and lipid profile. Future Journal of Pharmaceutical Sciences, 11, 27. https://doi.org/10.1186/s43094-025-00880-w
[D43] Lo HY, Ho TY, Li CC, et al. (2013). A novel insulin receptor-binding protein from Momordica charantia enhances glucose uptake and glucose transporter 4 translocation in 3T3-L1 adipocytes. Journal of Agricultural and Food Chemistry, 61(9), 2461–2468. https://doi.org/10.1021/jf304430y
[D44] Wang Y, Liu G, Chen M, et al. (2022). Ginsenoside F4 Alleviates Skeletal Muscle Insulin Resistance by Regulating PTP1B in Type II Diabetes Mellitus. Journal of Agricultural and Food Chemistry, 71(4), 1912–1922. https://doi.org/10.1021/acs.jafc.3c01262
[D45] Akhtar N, Jafri L, Green BD, et al. (2018). A Multi-Mode Bioactive Agent Isolated From Ficus microcarpa L. Fill. With Therapeutic Potential for Type 2 Diabetes Mellitus. Frontiers in Pharmacology, 9, 1376. https://doi.org/10.3389/FPHAR.2018.01376
[D46] Kaur R, Bhardwaj A, Gupta S. (2022). Sandalwood essential oil: A review of its pharmacological properties and therapeutic uses. Natural Product Research, 36(6), 1424–1445. https://doi.org/10.1080/14786419.2021.1923765
[D47] Siddiqui MZ. (2011). Boswellia serrata, a potential antiinflammatory agent: an overview. Indian Journal of Pharmaceutical Sciences, 73(3), 255–261. https://doi.org/10.4103/0250-474X.93507
[D48] Hongratanaworakit T, Buchbauer G. (2004). Evaluation of the harmonizing effect of ylang-ylang oil on humans after inhalation. Planta Medica, 70(7), 632–636. https://doi.org/10.1055/s-2004-827186
[D49] Kennedy DO, Little W, Scholey AB. (2004). Attenuation of laboratory-induced stress in humans after acute administration of Melissa officinalis (Lemon Balm). Psychosomatic Medicine, 66(4), 607–613. https://doi.org/10.1097/01.psy.0000132877.72833.71
[D50] Kwon H, Cho JH, Kim YJ, et al. (2022). Phytochemicals in Ocimum basilicum: A review of their pharmacological properties and therapeutic applications. Journal of Ethnopharmacology, 293, 115304. https://doi.org/10.1016/j.jep.2022.115304
Glossar
1,8-蒎烯
Hauptwirkstoff des Eukalyptus-/Rosmarinöls; anti-inflammatorisch, Alpha-Glucosidase-Hemmung
4-Hydroxyisoleucin
Wirkstoff aus Bockshornklee; glucoseabhängige Insulinsekretion
5-HT1A
Serotonin-1A-Rezeptor – relevant für Stress-Hyperglykämie
Akt/PKB
Proteinkinase B – zentrale Kinase im Insulinsignalweg; phosphoryliert GLUT4-Vesikel-Proteine
Alpha-Glucosidase
Intestinales Enzym zur Kohlenhydratspaltung; Angriffspunkt von Acarbose und mehreren Terpenen
AMPK
AMP-aktivierte Proteinkinase – zellulärer Energiesensor; Hauptangriffspunkt von Metformin
Boswelliasäure
Wirkstoff aus Weihrauch; 5-Lipoxygenase- und NF-κB-Hemmung
CaMKKβ
Calmodulin-abhängige Proteinkinase Kinase β – aktiviert AMPK upstream
Carvacrol
Monoterpen aus Oregano/Thymian; PPARγ, Alpha-Glucosidase-Hemmung
CAT
Katalase – antioxidatives Enzym; baut H₂O₂ ab
CB2
Cannabinoid-Rezeptor Typ 2 – G-Protein-gekoppelter Rezeptor; anti-neuroinflammatorisch
Cinnamaldehyd
Hauptwirkstoff des Zimtöls (60–80 %); AMPK-Aktivator, GLUT4-Induktor
姜黄素
Hauptwirkstoff der Kurkuma (3–5 %); PPARγ, NF-κB, AMPK
CYP2C9
Cytochrom P450 2C9 – metabolisiert Sulfonylharnstoffe und einige Terpene
细胞色素P450 3A4
Cytochrom P450 3A4 – wichtigstes Metabolisierungsenzym für Terpene und viele Medikamente
DPP-4
Dipeptidylpeptidase-4 – Enzym, das GLP-1 abbaut; Angriffspunkt der Gliptine
丁香酚
Phenylpropanoid aus Nelke (70–90 %); Alpha-Glucosidase-Hemmung, Insulinsekretion
G6Pase
Glukose-6-Phosphatase – finales Enzym der hepatischen Glukoseproduktion
Gingerol
Hauptwirkstoff des Ingweröls; GLP-1-Potenzierung und GLUT4-Induktion via Rab8/Rab10
GLP-1
Glucagon-like Peptide-1 – Inkretin-Hormon; stimuliert glucoseabhängig Insulinsekretion
GLUT4
Glukosetransporter Typ 4 – insulinabhängiger Glukose-Transporter in Muskel und Fettgewebe
GPx
Glutathionperoxidase – antioxidatives Enzym; reduziert Lipidperoxide
GSH
Glutathion – wichtigstes intrazelluläres Antioxidans
HbA1c
Glykiertes Hämoglobin – Langzeit-Blutzuckermarker (3-Monats-Durchschnitt)
HOMA-IR
Homeostatic Model Assessment of Insulin Resistance — Maß für Insulinresistenz
IR
Insulinrezeptor – Tyrosinkinase-Rezeptor; aktiviert IRS-1/2 → PI3K → Akt → GLUT4
IRS-1/2
Insulinrezeptor-Substrat 1/2 – Adapterprotein im Insulinsignalweg
KATP
ATP-sensitiver Kaliumkanal – in Beta-Zellen; Angriffspunkt der Sulfonylharnstoffe
柠檬烯
Monoterpen aus Zitrusfrüchten/Bergamotte; antioxidativ, insulinsensitisierend
芳樟醇
Monoterpen aus Koriander/Lavendel; GABA-A, anxiolytisch (Stress-Hyperglykämie)
LKB1
Liver Kinase B1 – upstream-Kinase von AMPK
mTORC1
Mechanistic Target of Rapamycin Complex 1 – Wachstums-/Metabolismus-Regulator; durch AMPK gehemmt
NF-κB
Nuclear Factor kappa B – Transkriptionsfaktor; Master-Regulator der Neuroinflammation
Nrf2
Nuclear factor erythroid 2-related factor 2 – Transkriptionsfaktor; Master-Regulator der antioxidativen Antwort
PEPCK
Phosphoenolpyruvat-Carboxykinase – Schlüsselenzym der Glukoneogenese in der Leber
PI3K
Phosphoinositid-3-Kinase – Schlüsselenzym im Insulinsignalweg
PPARγ
Peroxisom-Proliferator-aktivierter Rezeptor gamma – Transkriptionsfaktor; Angriffspunkt der Glitazone
PTP1B
Protein-Tyrosin-Phosphatase 1B – dephosphoryliert Insulinrezeptor; hemmt Insulinsignalweg
Rab8/Rab10
Rab-GTPasen – regulieren GLUT4-Vesikel-Exozytose in Skelettmuskel
ROS
Reaktive Sauerstoffspezies – oxidative Stressmoleküle
SERT
Serotonin-Transporter (Referenz aus Depression-Bericht)
SGLT2
Natrium-Glukose-Cotransporter 2 – renaler Glukose-Transporter; Angriffspunkt der Gliflozine
SOD
Superoxiddismutase – antioxidatives Enzym; schützt vor Superoxid-Radikalen
T2DM
Diabetes mellitus Typ 2 – häufigste Form des Diabetes (>90 % aller Fälle)
Thymoquinon
Hauptwirkstoff des Schwarzkümmelöls (20–48 %); AMPK, Nrf2, Beta-Zell-Schutz
trans-Anethol
Hauptwirkstoff des Fenchelöls (50–80 %); Alpha-Glucosidase-Hemmung
TRPM8
Transient Receptor Potential Melastatin 8 – Kälterezeptor; aktiviert durch Menthol
β-石竹烯
Sesquiterpen; CB2-Agonist; GLUT4, NF-κB-Hemmung